Настоящее изобретение относится к способу достижения сосудоразрушающего эффекта у теплокровных животных, таких как человек, в особенности к способу лечения раковых заболеваний, включая солидную опухоль, который включает введение сосудоразрушающего агента разделенными дозами. В особенности настоящее изобретение относится к такому способу, где сосудоразрушающим агентом является ZD6126.
Нормальный ангиогенез играет важную роль в различных процессах, включая эмбриональное развитие, заживление ран и некоторые составляющие репродуктивной функции женщин. Нежелательный или патологический ангиогенез связан с болезненными состояниями, включающими диабетическую ретинопатию, псориаз, рак, ревматоидный артрит, атерому, саркому Капоши и гемангиому (Fan et al., 1995, Trends Pharmacol. Sci. 16: 57-66; Folkman, 1995, Nature Medicine 1: 27-31). Образование новой сосудистой сети посредством ангиогенеза лежит в основе развития патологической картины различных заболеваний (J. Folkman, New England Journal of Medicine 333, 1757-1763 (1995)). Например, для роста солидной опухоли должна развиться своя собственная система кровоснабжения, от которой критически зависит ее снабжение кислородом и питательными веществами; если эту систему кровоснабжения механически разрушить, опухоль подвергнется некротической гибели. Неоваскуляризация также является клинической чертой повреждения кожи при псориазе, инвазивном паннусе в суставах больных ревматоидным артритом и в атеросклеротических бляшках. Патологической является ретинальная неоваскуляризация при макулярной дегенерации и при диабетической ретинопатии.
Можно ожидать, что обратное развитие при разрушении эндотелия новообразованных сосудов будет иметь полезный терапевтический эффект. Определен ряд сосудоразрушающих агентов (также известных, как нацеленные на сосуды агенты), например комбретастатин А4фосфат и соединение Ажимоното АС-7700 (Nihei Y. Et al., Japanese Journal of Cancer Research, 1999, 90, 1016-1025).
Обнаружено, что соединения:
международной патентной заявки № PCT/GB98/01977 (публикация № WO 99/02166) и международной патентной заявки №PCT/GB99/04436 (публикация № WO 00/40529), в которых описаны трициклические соединения; и
международной патентной заявки № PCT/GB/00099 (публикация № WO 00/41669), которая описывает гетероароматические соединения;
обладают избирательным разрушающим эффектом на новообразованную сосудистую сеть в отличие от различных видов нормального, существующего сосудистого эндотелия хозяина. Это свойство имеет существенное значение при лечении заболеваний, связанных с ангиогенезом, таких как рак, диабет, псориаз, ревматоидный артрит, саркома Капоши, гемангиома, острые и хронические нефропатии, атерома, рестеноз артерий, аутоиммунные заболевания, острые воспаления, избыточное образование рубца и образование спаек, эндометриоз, дисфункциональное кровотечение из мочевого пузыря и глазные болезни с пролиферацией сосудов сетчатки.
Одно соединение, описанное в PCT/GB98/01977 (публикация № WO 99/02166)представляет N-ацетилколхинол-О-фосфат (также известное, как (5S)-5-(ацетиламино)-9,10,11-триметокси-6,7-дигидро-5Н-дибензо[а,с]циклогептен-3-ил-дигидрофосфат; пример 1 в WO 99/02166), которое определяется как ZD6126.
Полагают, не ограничивая этим изобретение, что ZD6126 разрушает новообразованную сосудистую сеть, например сосудистую сеть опухолей, таким образом эффективно реверсируя процесс ангиогенеза. Это можно сравнить с другими известными антиангиогенными агентами, которые склонны быть менее эффективными, когда сосудистая сеть уже образована.
К удивлению авторы заявки неожиданно обнаружили, что сосудоразрушающие агенты, такие как ZD6126, при дозировании в виде разделенных доз (также известных как дробные дозы) производят больший антиопухолевый эффект, чем при введении в виде однократной дозы агента.
Антиопухолевые эффекты способа лечения настоящего изобретения включают, не ограничиваясь ими, подавление опухолевого роста, замедление роста опухоли, регрессию опухоли, сокращение размера опухоли, увеличение времени повторного роста опухоли при прекращении лечения, замедление прогрессирования заболевания. Ожидается, что когда способ лечения по настоящему изобретению назначается теплокровному животному, такому как человек, нуждающемуся в лечении рака, включая солидную опухоль, указанный способ лечения будет производить эффект, определяемый, например, по одному или нескольким из следующих показателей: степень антиопухолевого эффекта, скорость ответа, время прогрессирования заболевания и коэффициент выживания.
В соответствии с настоящим изобретением предлагается способ получения сосудоразрушающего эффекта у теплокровных животных, таких как человек, который включает введение указанному животному в виде разделенных доз эффективного количества сосудоразрушающего агента или его фармацевтически приемлемой соли.
В соответствии с еще одним аспектом настоящего изобретения предлагается способ лечения рака, включая солидную опухоль, у теплокровных животных, таких как человек, который включает введение указанному животному в виде разделенных доз эффективного количества сосудоразрушающего агента или его фармацевтически приемлемой соли.
В соответствии с другим аспектом изобретения также предлагается способ получения сосудоразрушающего эффекта у теплокровных животных, таких как человек, который включает введение указанному животному в виде разделенных доз эффективного количества ZD6126:
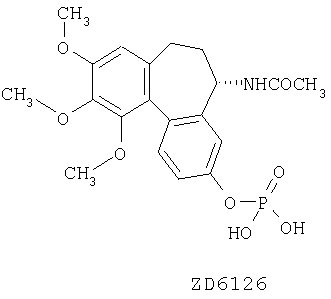
или его фармацевтически приемлемой соли.
В соответствии с еще одним аспектом изобретения предлагается способ лечения рака, включая солидную опухоль, у теплокровных животных, таких как человек, который включает введение указанному животному в виде разделенных доз эффективного количества ZD6216 или его фармацевтически приемлемой соли.
В соответствии с настоящим изобретением предлагается способ получения сосудоразрущающего эффекта у теплокровных животных, таких как человек, который включает введение указанному животному в виде разделенных доз эффективного количества сосудоразрушающего агента или его фармацевтически приемлемой соли, где сосудоразрушающий агент или его фармацевтически приемлемая соль могут необязательно вводиться вместе с фармацевтически приемлемым эксципиентом или носителем.
В соответствии с еще одним аспектом настоящего изобретения предлагается способ лечения рака, включая солидную опухоль, у теплокровных животных, таких как человек, который включает введение указанному животному в виде разделенных доз эффективного количества сосудоразрушающего агента или его фармацевтически приемлемой соли, где сосудоразрушающий агент или его фармацевтически приемлемая соль могут необязательно вводиться вместе с фармацевтически приемлемым эксципиентом или носителем.
В соответствии с еще одним аспектом настоящего изобретения предлагается способ получения сосудоразрушающего эффекта у теплокровных животных, таких как человек, который включает введение указанному животному в виде разделенных доз эффективного количества ZD6126 или его фармацетически приемлемой соли, где ZD6126 или его фармацевтически приемлемая соль могут необязательно вводиться вместе с фармацевтически приемлемым эксципиентом или носителем.
В соответствии с еще одним аспектом настоящего изобретения предлагается способ лечения рака, включая солидную опухоль, у теплокровных животных, таких как человек, который включает введение указанному животному в виде разделенных доз эффективного количества ZD6126 или его фармацевтически приемлемой соли, где ZD6126 или его фармацевтически приемлемая соль могут необязательно вводиться вместе с фармацевтически приемлемым эксципиентом или носителем.
В соответствии с еще одним аспектом настоящего изобретения ожидается, что эффект способа лечения по настоящему изобретению, используя разделенные дозы сосудоразрушающего агента, такого как ZD6126, будет значительно больше, чем эффект способа лечения с использованием однократной дозы сосудоразрушающего агента, такого как ZD6126.
В соответствии с еще одним аспектом настоящего изобретения предлагается лекарственный препарат, включающий две или большее количество частей доз сосудоразрушающего агента или его фармацевтически приемлемой соли, которые вместе составляют общую дневную дозу, для введения в виде разделенных доз для использования в способе лечения человека или животного терапевтическим путем.
В соответствии с еще одним аспектом настоящего изобретения предлагается набор, включающий две или более частей доз сосудоразрушающего агента или его фармацевтически приемлемой соли, которые вместе составляют общую дневную дозу для введения в виде разделенных доз.
В соответствии с еще одним аспектом изобретения предлагается набор, включающий:
a) две или большее количество частей доз сосудоразрушающего агента или его фармацевтически приемлемой соли, которые вместе составляют общую дневную дозу для введения в виде разделенных доз;
b) контейнер для помещения указанных дозированных форм.
В соответствии с еще одним аспектом настоящего изобретения предлагается набор, включающий:
а) две или более частей доз сосудоразрушающего агента или его фармацевтически приемлемой соли, которые вместе составляют общую дневную дозу вместе с фармацевтически приемлемым эксципиентом или носителем, в виде единичных дозированных форм; и
b) контейнер для помещения указанных дозированных форм.
В соответствии с еще одним аспектом настоящего изобретения предлагается использование сосудоразрушающего агента или его фармацевтически приемлемой соли в производстве лекарственного средства для введения в виде разделенных доз, предназначенного для использования в получении сосудоразрушающего эффекта у теплокровных животных, таких как человек.
В соответствии с еще одним аспектом настоящего изобретения предлагается использование сосудоразрушающего агента или его фармацевтически приемлемой соли в производстве лекарственного препарата для введения в виде разделенных доз, предназначенного для использования в получении противоракового эффекта у теплокровных животных, таких как человек.
В соответствии с еще одним аспектом настоящего изобретения предлагается использование сосудоразрушающего агента или его фармацевтически приемлемой соли в производстве лекарственного препарата для введения в виде разделенных доз, предназначенного для использования в получении противоопухолевого эффекта у теплокровных животных, таких как человек.
В соответствии с еще одним аспектом настоящего изобретения предлагается лекарственное средство, включающее две или более частей доз ZD6126 или его фармацевтически приемлемой соли, которые вместе составляют общую дневную дозу для введения в виде разделенных доз, предназначенный для использования в способе лечения человека или животного терапевтическим путем.
В соответствии с еще одним аспектом настоящего изобретения предлагается набор, включающий две или большее количество частей доз ZD6126 или его фармацевтически приемлемой соли, которые вместе составляют общую дневную дозу для введения в виде разделенных доз.
В соответствии с еще одним аспектом настоящего изобретения предлагается набор, включающий:
a) две или большее количество частей ZD6126 или его фармацевтической соли, которые вместе составляют общую дневную дозу, в единичных дозированных формах для введения в виде разделенных доз;
b) контейнер для помещения указанных дозированных форм.
В соответствии с еще одним аспектом настоящего изобретения предлагается набор, включающий:
a) две или большее количество частей доз SD6126 или его фармацевтической соли, которые вместе составляют общую дневную дозу вместе с фармацевтически приемлемым эксципиентом или носителем в единичных дозированных формах;
b) контейнер для помещения указанных дозированных форм.
В соответствии с еще одним аспектом настоящего изобретения предлагается использование ZD6126 или его фармацевтически приемлемой соли в производстве лекарственного средства для введения в виде разделенных доз для использования в получении сосудоразрушающего эффекта у теплокровных животных, таких как человек.
В соответствии с еще одним аспектом настоящего изобретения предлагается использование ZD6126 или его фармацевтически приемлемой соли, в производстве лекарственного средства для введения в виде разделенных доз, предназначенного для использования в получении противоракового эффекта у теплокровного животного, такого как человек.
В соответствии с еще одним аспектом настоящего изобретения предлагается использование ZD6126 или его фармацевтически приемлемой соли в производстве лекарственного препарата для введения в виде разделенных доз, предназначенного для использования в получении антиопухолевого эффекта у теплокровного животного, такого как человек.
Сосудоразрушающие агенты (VDAs) представляют собой агенты, которые разрушают сосудистую сеть, в особенности новообразованную сосудистую сеть, такую как сосудистая сеть опухоли.
Предпочтительными (VDAs) являются такие, которые описаны в международной патентной заявке № PCT/GB98/01977 (публикация WO 99/02166), полное раскрытие которой включено в описании в качестве ссылки.
Другие предпочтительные (VDAs) представляют собой описанные в международной патентной заявке № PCT/GB99/04436 (публикация № WO 00/40529), полное раскрытие которой включено в описание в качестве ссылки.
Другие предпочтительные (VDAs) представляют собой такие, которые описаны в международной патентной заявке № PCT/GB99/00099 (публикация № WO 00/41669), полное раскрытие которой включено в качестве ссылки.
Другой VDA представляет собой комбретастатин А4 фосфат.
Другой VDA представляет собой соединение Ajinomoto AC-7700 (Nihei Y et al., Japanese Journal of Cancer Research, 1999, 90, 1016-1025).
Наиболее предпочтительным VDA является ZD6126.
Сосудоразрушающий агент может быть представлен в форме, подходящей для перорального введения, например, как таблетка или капсула, для назального введения или введения путем ингаляции, например, как порошок или раствор, для парентеральной инъекции (включая внутривенную, подкожную, внутримышечную, внутрисосудистую или инфузионную), например, как стерильный раствор, суспензия или эмульсия, для местного введения, например, как мазь или крем, для ректального введения, например, как суппозиторий, или путь введения может быть представлен в виде непосредственной инъекции в опухоль, или региональной доставкой, или местной доставкой. В других воплощениях настоящего изобретения VDA способа лечения может доставляться эндоскопически, интратрахеально, внутриочагово, чрескожно, внутривенно, подкожно, интраперитонеально или интратуморально. VDA может быть в форме фармацевтической композиции, где VDA или его фармацевтически приемлемая соль находится вместе с фармацевтически приемлемым эксципиентом или носителем. В целом, описанные здесь композиции могут быть получены общепринятым способом с использованием общепринятых эксципиентов. Композиции по настоящему изобретению удобно производить в виде единичных дозированных форм.
Разделенные дозы, также называемые дробными дозами, означают, что общую дозу, подлежащую введению теплокровному животному, такому как человек, в любой суточный период (например, в течение 24 часа от полночи до полночи) делят на две или большее количество частей общей дозы, и эти части вводят через временной период между каждой частью, составляющий от около более 0 часов до около 10 часов, предпочтительно от около 1 часа до около 6 часов, более предпочтительно от около 2 часов до около 4 часов. Части общей дозы могут быть равными или неравными. Предпочтительно общую дозу делят на две части, которые могут быть примерно равными или неравными. Интервалы времени между дозами могут быть, например, выбраны из следующих:
около 1 часа, около 1,5 часов, около 2 часов, около 2,5 часов, около 3 часов, около 3,5 часов, около 4 часов, около 4,5 часов, около 5 часов, около 5,5 часов и около 6 часов.
Интервалы времени между дозами могут иметь любое число (включая нецелое число) минут, от более 0 минут до 600 минут, предпочтительно от 45 до 375 минут включительно. Если вводится более 2 доз, интервалы времени между каждой дозой могут быть равными или неравными.
Предпочтительно две дозы вводятся с интервалом времени между ними более или равным 1 часу и менее 6 часов.
Более предпочтительно две дозы дают с интервалом времени между ними от более или равным двум часам до менее 5 часов.
Еще более предпочтительно две дозы дают с интервалом времени между ними от более или равным двум часам до менее или равным 4 часам.
Конкретно, общая доза делится на две части, которые могут быть равными или неравными с интервалом времени между дозами от более или равным двум часам до менее или равным около 4 часам.
Более конкретно общую дозу делят на две части, которые могут быть примерно равны с интервалом времени от более или равным двум часам до менее или равным примерно 4 часам.
Чтобы избежать сомнения относительно термина "примерно", в описании периодов времени он означает данное время плюс или минус 15 минут, так, например, около одного часа означает от 45 до 75 минут, около 1,5 часов означает от 75 до 105 минут. В других местах описания термин "примерно" имеет свое обычное словарное значение.
ZD6126 обычно вводится теплокровным животным в единичной дозе в интервале 10-500 мг на квадратный метр площади тела животного, например, приблизительно 0,3-15 мг/кг у человека. Рассматривается дозированная единица в интервале, например, 0,3-15 мг/кг, предпочтительно 0,5-5 мг/кг, являющаяся нормальной эффективной терапевтической дозой. Дозированная единица, такая как таблетка или капсула, обычно содержит, например, 25-250 мг активного ингредиента. Предпочтительно используется дневная доза в интервале от 0,5 до 5 мг/кг.
Что касается размера общей дневной дозы, которая требуется для терапевтического или профилактического лечения конкретного болезненного состояния, она варьируется в зависимости от хозяина, подвергающегося лечению, пути введения и серьезности заболевания, подлежащего лечению. Соответственно оптимальная дозировка будет определяться лечащим врачом, который лечит любого конкретного больного. Например, может быть необходимо или желательно снизить вышеприведенные дозы лечения с целью снижения токсичности.
Способы лечения по настоящему изобретению, как определено в описании, могут применяться в качестве единственного лечения, или могут включать дополнительно к сосудоразрушающему агенту, введенному в виде разделенных доз, один или большее количество других веществ и/или видов лечения. Такое сочетанное лечение может достигаться путем одновременного, последовательного или раздельного введения отдельных компонентов лечения. В области медицинской онкологии нормальной практикой является использование сочетания различных форм лечения для лечения каждого больного раком. В медицинской онкологии другой компонент(ы) такого сочетанного лечения в дополнение к VDA, введенному в виде разделенных доз, может быть: хирургия, радиотерапия или химиотерапия. Так химиотерапия может включать следующие категории терапевтических агентов:
(i) антиангиогенные агенты (например, линомид, ингибиторы интегрин αvβ3 функции, ангиостатин, эндостатин, разоксин, талидомид) и включая фактор роста сосудистого эндотелия (VEGF) ингибиторы рецептора тирозинкиназы (RTKIs) (например, описанные в международных патентных публикациях № WO 97/22596, WO 97/30035, WO 97/32856 и WO 98/13354, полное раскрытие которых включено в качестве ссылки, также, например, описанные в публикации международной патентной заявки № WO 00/47212, полное описание которой включено в качестве ссылки);
(ii) цитостатические агенты, такие как антиэстрогены (например, тамоксифен, торемифен, ралоксифен, дролоксифен, иодоксифен), гестагены (например, мегестрол ацетат), ингибиторы ароматазы (например, анастрозол, летразол, воразол, экземестан), антигестагены, антиандрогены (например, флютамид, нилютамид, бикалютамид, ципротерон ацетат), LHRH агонисты и антагонисты (например, гозерелин ацетат, люпролид), ингибиторы тестостерон 5α-дигидроредуктазы (например, финастерид), антиинвазивные агенты (например, ингибиторы металлопротеиназы, такие как маримастат и ингибиторы активатора функции рецептора урокиназы плазминогена) и ингибиторы функции фактора роста (причем фактор роста включает, например, эпидермальный фактор роста (EGF), фактор роста тромбоцитов и фактор роста гепатоцитов, причем такие ингибиторы включают антитела к фактору роста, антитела к рецептору фактора роста, ингибитора тирозинкиназы и ингибиторы серин/треонинкиназы);
(iii) модификаторы биологического ответа (например, интерферон);
(iv) антитела (например, эдреколомаб);
(v) антипролиферативные/антинеопластические лекарственные средства и их сочетания, используемые в медицинской онкологии, такие как антиметаболиты (например, антифолаты, подобные метотрексату, фторпиримидины, подобные 5-фторурацилу, аналоги пурина и аденозина, цитозинарабинозид); противоопухолевые антибиотики (например, антрациклины, подобные доксорубицину, дауномицину, эпирубицину и идарубицину, митомицин-С, дактиномицин, митрамицин), производные платины (например, цисплатин, карбоплатин); алкилирующие агенты (например, азотистый иприт, мелфалан, хлорамбицил, бусульфан, циклофосфамид, ифосфамид, нитрозомочевины, тиотепа); антимитотические агенты (например, алкалоиды винка, такие как винкристин, и таксоиды, такие как таксол, таксотер); ферменты (например, аспарагиназа); ингибиторы тимидилатсинтазы (например, ралтитрексед); ингибиторы топоизомеразы (например, эпиподофилотоксины, подобные этопозиду и тенипозиду, амзакрин, топотекан, иринотекан).
Если VDA представляет собой ZD6126, соли для использования в фармацевтической композиции будут представлять фармацевтически приемлемые соли, но в производстве ZD6126 и его фармацевтически приемлемых солей могут быть пригодны и другие соли. Такие соли могут быть образованы с неорганическим или органическим основанием, которое предоставляет фармацевтически приемлемый катион. Подобные соли с неорганическими или органическими основаниями включают, например, соль щелочного металла, такую как натриевая или калиевая соль, соль щелочноземельного металла, такую как кальциевую или магниевую соль, соль аммония или, например, соль с метиламином, диметиламином, триметиламином, пиперидином, морфолином или трис-(2-гидроксиэтиламином).
ZD6126 можно получить в соответствии со следующим процессом.
N-ацетилколхинол (30,0 г, 83,9 ммоль) растворяют в ацетонитриле в инертной атмосфере, и через шприц добавляют 1,2,3-триазол (14,67 г, 212,4 ммоль). Добавляют ди-трет-бутил-диэтилфосфорамидит (37,7 г, 151,4 ммоль) и реакционную смесь перемешивают при примерно 20°С, чтобы завершить образование промежуточного фосфитного эфира. Добавляют гидропероксид (24,4 г, 159,2 ммоль) при 10°С и реакционную смесь перемешивают, пока не завершится окисление. Добавляют бутилацетат (50 мл) и раствор гидроксида натрия (250 мл 1 М), реакционную смесь перемешивают и водную фазу отбрасывают. Органический раствор промывают раствором гидроксида натрия (2×250 мл 1М) и насыщенным раствором хлорида натрия. Добавляют трифторуксусную кислоту (95,3 г, 836 ммоль) при 15°С. Реакционную смесь дистиллируют при атмосферном давлении, ZD6126 кристаллизуют и выделяют при комнатной температуре.
Анализ выживания клеток
Активность ZD6126, вводимого в виде дробных доз, может быть продемонстрирована с помощью следующего анализа выживания клеток.
In vivo выживание клеток измеряется с использованием анализа иссечения (D.J.Chaplin et al., Anticancer Reseach 19: 1890196 (1999)).
Для каждого нижеприведенного анализа а) и b) выжившая фракция опухолевых клеток определяется следующим образом:
Опухоль иссекают примерно через 18 часов после обработки, взвешивают и дезагрегируют в течение 1 часа при 37 градусах по Цельсию в ферментном коктейле, содержащем 1 мг/мл проназы, 0,5 мг/мл ДНКазы и 0,5 мг/мл коллагеназы. Проводят гемоцитометрические измерения клеток, не окрашенных трипаном голубым, и видимые клетки высевают в соответствующих концентрациях, получая 50 колоний на чашку после инкубации in vitro. Облученные большими дозами питающие клетки (V79 клетки) используются при концентрации 25000/мл для поддерживания роста выживших CaNT клеток. Данные подсчитывают в виде выживших фракций на грамм опухоли.
А) CaNT опухолевая модель: Эффект интервала доз
В модель опухоли аденокарциномы мыши CaNT, выращенной на самках СВА мышей (Hill, S.A. et al.,Int. J.Cancer 63, 119-123, 1995) вводили ZD6126 в виде разделенных доз, получая в результате улучшенный противоопухолевый эффект по сравнению с ZD6126, введенный в однократной дозе при измерении выжившей фракции опухолевых клеток. Смотри Фиг.1.
Методология
Однократная доза
ZD6126 вводят в однократной дозе 200 мг интраперитонеально (i.p.) в физиологическом растворе с небольшим количеством 1% карбоната натрия, добавленного для облегчения растворения ZD6126.
Разделенные дозы
ZD6126 дозируют, используя дробную схему введения как 100 мг/кг ZD6126 с последующим введением еще 100 мг/кг ZD6126; дозы вводят интраперитонеально (i.p.) в физиологическом растворе с небольшим количеством 1% карбоната натрия, добавленного для облегчения растворения ZD6126. Используемые интервалы времени составляли 1,2,3,4 и 6 часов.
Выжившие фракции на грамм опухоли определяли, как описано выше, и наносили на график, как показано на фигуре 1.
Две дозы по 100 мг/кг, разделенные 2, 3 или 4 часами, значительно более эффективны на этой модели, чем однократная доза в 200 мг/кг.
b) Модем CaNT опухоли: Эффект интервала между дозами и пропорций дробных доз
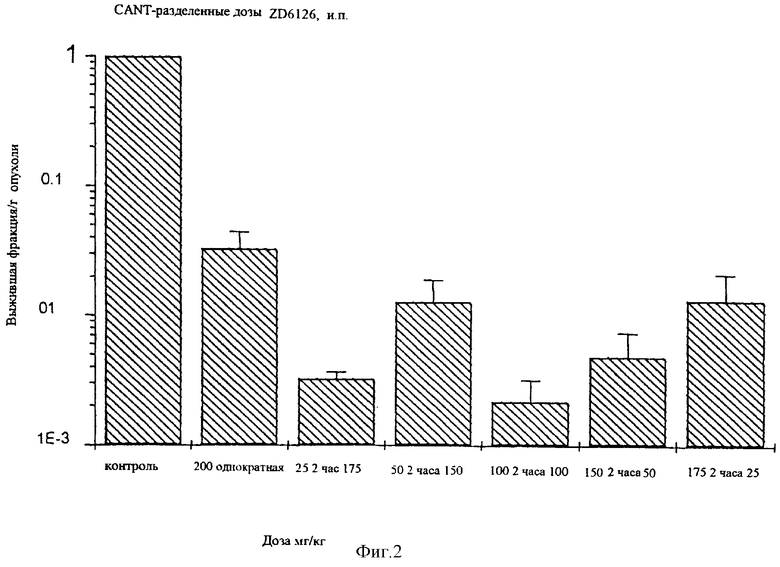
В модель опухоли аденокарциномы мыши CaNT, выращенной на самках СВА мышей (Hill, S.A. et al.,Int. J.Cancer 63, 119-123, 1995) вводили ZD6126 в виде разделенных доз, получая в результате улучшенный противоопухолевый эффект, что измерено по фракции выживших опухолевых клеток, по сравнению с ZD6126, введенном в однократной дозе. Данный улучшенный эффект варьировался пропорционально общей дозе, введенной в первой и второй дозах. Смотри фиг.2.
Методология
Однократная доза
ZD6126 вводят в виде однократной дозы в 200 мг интраперитонеально (i.p.) в физиологическом растворе с небольшим количеством 1% карбоната натрия, добавленного для облегчения растворения ZD6126.
Разделенные дозы
ZD6126 дозируют, используя дробные дозы:
i) 25 мг/кг ZD6126, затем интервал в 2 часа с последующим введением еще 175 мг/кг ZD6126;
ii) 50 мг/кг ZD6126, затем интервал в 2 часа с последующим введением еще 150 мг/кг ZD6126;
iii) 100 мг/кг ZD6126, затем интервал в 2 часа с последующим введением еще 100 мг/кг ZD6126;
iv) 150 мг/кг ZD6126, затем интервал в 2 часа с последующим введением еще 50 мг/кг ZD6126;
v) 175 мг/кг ZD6126, затем интервал в 2 часа с последующим введением еще 25 мг/кг ZD6126;
Все дозы дают интраперитонеально (i.p.) в физиологическом растворе с небольшим количеством 1% карбоната натрия, добавленного для облегчения растворения ZD6126.
Противоопухолевый эффект, измеренный по выжившей фракции опухолевых клеток, был больше при разделенных дозах ZD6126, чем при однократной дозе ZD6126. Подобный усиленный эффект был важен, когда разделенные дозы ZD6126 вводили в соответствии с i), iii), или iv, описанными выше. Наилучший эффект наблюдался с равными дробными дозами, то есть в соответствии с вышеприведенным iii).
| название | год | авторы | номер документа |
|---|---|---|---|
| КОМБИНИРОВАННЫЕ ТЕРАПИИ С ИСПОЛЬЗОВАНИЕМ АКТИВНОСТИ, ПОВРЕЖДАЮЩЕЙ СОСУДЫ | 2001 |
|
RU2268729C2 |
| СПОСОБ ЛЕЧЕНИЯ РАКА | 2002 |
|
RU2284184C2 |
| КОМБИНИРОВАННОЕ ЛЕЧЕНИЕ | 2014 |
|
RU2666999C2 |
| КОМБИНИРОВАННАЯ ХИМИОТЕРАПИЯ | 2001 |
|
RU2284818C2 |
| КОМБИНАЦИИ (СОСТАВЫ), ВКЛЮЧАЮЩИЕ DMXAA ДЛЯ ЛЕЧЕНИЯ РАКА | 2006 |
|
RU2404765C2 |
| ПРИМЕНЕНИЕ ЭРИБУЛИНА В ЛЕЧЕНИИ РАКА | 2015 |
|
RU2699545C2 |
| КОМБИНИРОВАННАЯ ХИМИОТЕРАПИЯ | 2006 |
|
RU2429838C2 |
| КОМБИНИРОВАННАЯ ХИМИОТЕРАПИЯ | 2010 |
|
RU2587013C2 |
| ЛЕЧЕНИЕ РАКА КОМБИНАЦИЕЙ ПЛИНАБУЛИНА И ТАКСАНА | 2013 |
|
RU2662298C2 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМБИНАЦИЯ, ВКЛЮЧАЮЩАЯ ИНГИБИТОР ФОСФАТИДИЛИНОЗИТОЛ 3-КИНАЗЫ И ИНГИБИТОР АРОМАТАЗЫ | 2013 |
|
RU2651023C2 |
Изобретение относится к медицине и касается использования сосудоразрушающего агента или его фармацевтически приемлемой соли для введения теплокровному животному в виде разделенных доз для получения противоопухолевого эффекта. В частности, сосудоразрушающий агент представляет собой ZD6126, АС-7700, комбретастатина А4 фосфат или их фармацевтически приемлемые соли. При этом общая дневная доза сосудоразрушающего агента разделена на две или более равных или неравных частей, и интервал времени между введением каждой части составляет от более 0 часов до около 6 часов. Изобретение позволяет получить больший противоопухолевый эффект по сравнению с эффектом, получаемым при введении такой же общей дозы сосудоразрушающего агента в виде единичной дозы. 5 н. и 13 з.п. ф-лы, 2 ил.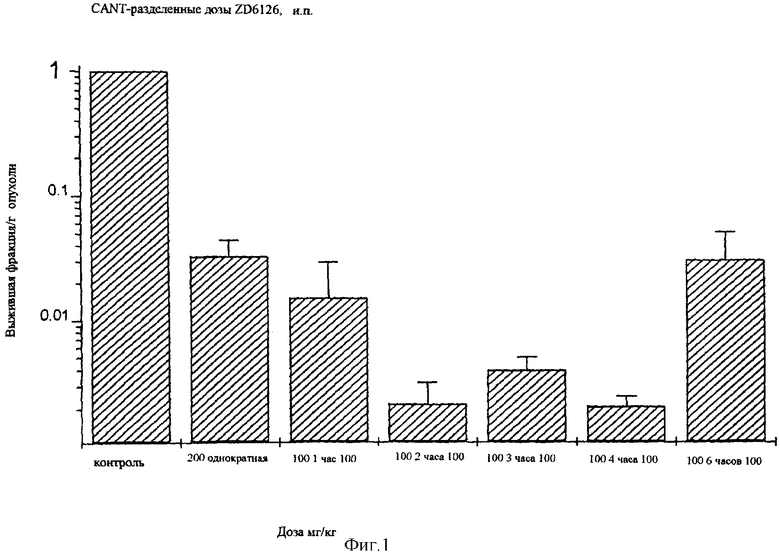
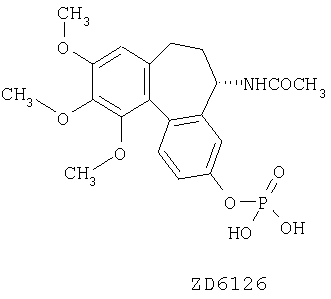
или его фармацевтически приемлемая соль.

или его фармацевтически приемлемой соли, при этом общая доза ZD6126, вводимая в течение одного дня, разделена на две или более частей, которые являются равными или неравными, и интервал времени между введением каждой части более или равен примерно 2 ч или менее или равен примерно 4 ч, причем противоопухолевый эффект, получаемый при введении общей дневной дозы ZD 6126 указанными разделенными частями, больше, чем эффект, получаемый при введении такой же общей дозы ZD 6126 в виде единичной дозы.
| Автоматический огнетушитель | 0 |
|
SU92A1 |
| RU 98100678 A, 20.02.2000, реферат | |||
| Прибор, замыкающий сигнальную цепь при повышении температуры | 1918 |
|
SU99A1 |
| Огнетушитель | 0 |
|
SU91A1 |
| Огнетушитель | 0 |
|
SU91A1 |
| Brewer G.J | |||
| et al | |||
| Treatment of metastatic cancer with tetrathiomolybdate, an anticooper, antiangiogenic agent: Phase I study // Clin | |||
| Cancer Res | |||
| ЩИТОВОЙ ДЛЯ ВОДОЕМОВ ЗАТВОР | 1922 |
|
SU2000A1 |
Авторы
Даты
2006-07-10—Публикация
2001-03-27—Подача