Область изобретения
Настоящее изобретение относится к способам лечения болезней, являющихся результатом когнитивных расстройств, таких как болезнь Альцгеймера, и повышения дееспособности; указанные способы замедляют прогрессирование этих болезней.
Предпосылки создания изобретения
Раньше соединения, пригодные для лечения когнитивных расстройств, таких как болезнь Альцгеймера, включали донепезил, ривастигмин и галантамин, основываясь на их активности, как следует дальше в U.S. Patent №5409948, April 25, 1995, в качестве ингибиторов ацетилхолинэстеразы. В дополнение, другой ингибитор ацетилхолинэстеразы - фенсерин, который имеет структуру отрицательного оптического энантиомера (-) N-(-)-N-фенилкарбамоилэсеролина и его соли, клинически используется для лечения когнитивных расстройств.
Вследствие того что все эти соединения являются антихолинэстеразными ингибиторами, они имеют ряд недостатков, вызывая нежелательные побочные эффекты, обусловленные их активностью как ингибиторов ацетилхолинэстеразы. Эти нежелательные побочные эффекты связаны с их токсичностью из-за подавления ацетилхолинэстеразы. Благодаря тому факту, что эти соединения, которые принимаются постоянно, имеют низкий терапевтический индекс (соотношение между токсичностью и терапевтическим эффектом), они вызывают ряд патологических состояний, связанных с холинэргической активностью. Следовательно, благодаря длительности лечения когнитивных расстройств желательно предоставить агент, который эффективен и не вызывает побочных токсических эффектов, присущих ингибиторам ацетилхолинэстеразы.
Краткое изложение сущности изобретения
В соответствии с данным изобретением было установлено, что соединение формулы (II)

или его фармацевтически приемлемые соли могут быть использованы для лечения больных, имеющих когнитивные расстройства, такие как болезнь Альцгеймера и возрастные когнитивные ухудшения, без побочных эффектов, обусловленных токсическим профилем ингибиторов антихолинэстеразы.
Это изобретение направлено на лечение пациентов с когнитивными расстройствами при пероральном назначении соединения формулы II или его фармацевтически приемлемых солей и составов для назначения соединения больным.
Подробное описание
В соответствии с данным изобретением было установлено, что соединение формулы (II) и его фармацевтически приемлемые соли эффективны для лечения больных, страдающих от когнитивных расстройств, и могут назначаться больным перорально, без токсических побочных эффектов, обусловленных антихолинэстеразной активностью, совместно с таким соединением, как фенсерин, ривастигмин, донепезил и галантамин. Это особенно неожиданно, учитывая тот факт, что соединение формулы II, т.е. (+) 9-N-фенилкарбинолэсеролин, не является природным (+) изомером фенсерина (соединение формулы I) и обладает минимальной антихолинэстеразной активностью. Действительно, в отличие от фенсерина соединение формулы I и его соли имеют очень низкую антихолинэстеразную ингибиторную активность или даже совсем не имеют никакой. Следовательно, побочные эффекты, такие как тошнота, рвота, головокружение, брадикардия и т.д., обусловлены введением антихолинэстеразных агентов и не касаются способа этого изобретения.
В соответствии с данным изобретением было обнаружено, что (+) энантиомер фенсерина является сильнодействующим ингибитором развития когнитивных ухудшений, связанных с возрастом или болезнью Альцгеймера. Соединение формулы (II) было раскрыто Pei, Greig и др. ("Inhibition of Human Acetylcholinesterase" Med Cem Research Acad. (1995) 5: 265-270). В этой статье было показано, что в отличие от отрицательного энантиомера фенсерина соединение формулы II было менее активно в качестве ингибитора человеческой ацетилхолинэстеразы. Однако, несмотря на это, было показано в соответствии с изобретением, что соединение формулы II является сильнодействующим агентом в понижении уровня потенциально опасного амилоидного β-пептида (Аβ) и что этот Аβ белок ослабляет развитие неврастенического состояния, ведущего к снижению памяти, характеризующегося появлением возрастных бляшек, основу которых составляют Аβ и клубки нервных волокон. Аβ представляет собой пептид, состоящий из 40-42 остатков, получаемый из более высокомолекулярного белка βАРР, состоящего из 695-770 остатков. βАРР превращается в белок Аβ, который может вызывать патологические отличительные признаки когнитивных ухудшений.
Как часть этого изобретения, было показано, что соединение формулы II и его фармацевтически приемлемые соли, подобные фенсерину, могут управлять белком βАРР с получением неамилоидогенных побочных продуктов и, таким образом, уменьшать продуцирование Аβ белка. Принимая во внимание, что соединение формулы II в отличие от его отрицательного изомера фенсерина не является сильным антихолинэстеразным ингибитором, оно не вызывает побочных эффектов, обусловленных антихолинэстеразной активностью. То, что (+) форма энантиомера не является сильнодействующим ингибитором ацетилхолинэстеразы, видно из результатов, сообщенных Shaw и др. в Proc. Natl. Academy Science USA (2001) 98(13) 7605-7610, где было указано, что "концентрация соединения, требуемая для снижения ацетилхолинэстеразной активности на 50%, составляет 22 нМ для (-)-фенсерина, тогда как (+)-фенсерин неактивен при концентрации более 25000 нМ". Благодаря результатам, опубликованным Shaw, в отличие от отрицательного энантиомера фенсерина соединение формулы II и его соли не являются эффективными ингибиторами ацетилхолинэстеразы.
В соответствии с данным изобретением, (+) энантиомер формулы II эффективен для лечения болезни Альцгеймера, небольших когнитивных ухудшений, связанных с возрастным ухудшением памяти, включая любое другое слабоумие, связанное с когнитивными ухудшениями. Кроме того, в отличие от применения других терапевтических средств для лечения когнитивных ухудшений соединение формулы II и его соли из-за недостаточной антихолинэстеразной активности не имеют токсических побочных эффектов, связанных с антихолинэстеразными ингибиторами, таких как тошнота, диарея, рвота, головокружение и брадикардия. Так как соединение формулы II и/или его соли не воздействуют на холинэстеразу, соединение этого изобретения может быть назначено больным в высоких дозах для достижения хороших результатов лечения без риска токсических побочных эффектов.
Способ лечения ориентирован на пациентов, имеющих болезненное состояние, которое проявляется когнитивными ухудшениями и симптомами, связанными с возрастом или болезнью Альцгеймера. Для многих больных, страдающих таким когнитивным ухудшением, очень трудно окончательно диагностировать, относятся ли эти симптомы непосредственно к болезни Альцгеймера или к возрастным изменениям. Следовательно, способ этого изобретения целесообразно применять к больным старше 50 лет, страдающим от симптомов когнитивных ухудшений, связанных с возрастом или болезнью Альцгеймера.
Обычно лечебная доза зависит от пути введения, возраста, веса и состояния когнитивных ухудшений больных. В основном дозы от 0,5 до 10 мг/кг в день соединения формулы II и/или его солей назначают больным перорально для достижения положительного лечебного эффекта. В соответствии с данным изобретением предпочтительно использовать перорально от 1,0 до 5,0 мг на кг массы тела ежедневно, особенно предпочтительно от 1 до 2 мг на кг массы тела ежедневно. Соединение формулы II и/или его соли могут быть назначены перорально от 1 до 4 раз в день при указанной выше дозировке. Важно отметить, что любое лечение когнитивных расстройств, таких как болезнь Альцгеймера и другие когнитивные ухудшения, связанные с возрастом, требует длительного лечения (т.е. непрерывного лечения) в течение всей жизни. В этом способе ухудшение, обусловленное когнитивными нарушениями вследствие указанных когнитивных расстройств и симптомов таких расстройств, стабилизируется или замедляется и в некоторых случаях наступает улучшение. Когнитивные расстройства, являющиеся результатом таких болезней, прогрессируют всю жизнь. Лечение по этому изобретению предотвращает развитие этих когнитивных расстройств. Следовательно, способ этого изобретения обеспечивает средства для уменьшения развития этих болезненных состояний.
Способность соединения формулы II и/или его солей улучшать когнитивные действия может быть определена с использованием различных известных средств. Среди этих средств есть стандартные методы, определяющие развитие этого болезненного состояния, такие как Mini-Mental State Examination, Clinical Dementia Rating, также как Alzheimer's Disease Assessment Scale (ADAS- cog). ADAS-cog представляет собой комплексный подход для оценки когнитивных действий, который включает элементы памяти, ориентацию, способность к запоминанию, рассудок, речь и практические навыки. ADAS-cog имеет оценочный диапазон от 0 до 70, при более высоком значении констатируются когнитивные ухудшения. Средний пожилой человек может набрать от 0 до 1, но для пожилых людей, не страдающих слабоумием, более высокий балл не является необычным. Производя оценку с использованием теста ADAS-cog, оценивают изменения в течение длительного периода времени перед и во время лечения, определяя прогрессирование болезни, также сравнивают этот балл с контрольной группой больных. Для больных, подвергнутых лечению в соответствии со способом данного изобретения, было установлено, что в ходе лечения больные имели такие же или лучшие показатели в данном тесте по сравнению с контрольной группой. Также способность способа данного изобретения клинически давать результаты у большинства больных можно оценить, используя тест "Clinical Interview Board Impression of Change" (CIBIC-тест). Результаты по этому исследованию получают от лиц, оказывающих помощь, а также врачей, беседовавших с больными, и от исследований таких функций, как общая когнитивная функция, функции поведения и повседневная жизнедеятельность. Шкала CIBIC разделена на 7 категорий от 1, что означает заметное улучшение, до 4, что означает отсутствие изменений, и до 7, что указывает на заметное ухудшение. В течение лечения в соответствии с данным изобретением большинство больных набирают 4 балла, а некоторые набирают лучшее значение баллов (т.е. меньшее). С другой стороны, что касается больных, не подвергнутых лечению, имеющих такую же общую оценку в тот же момент времени, то большинство больных набирают более высокий балл (>4), который определяет ухудшение их состояния.
Соединение формулы II синтезируются по следующей схеме реакций:
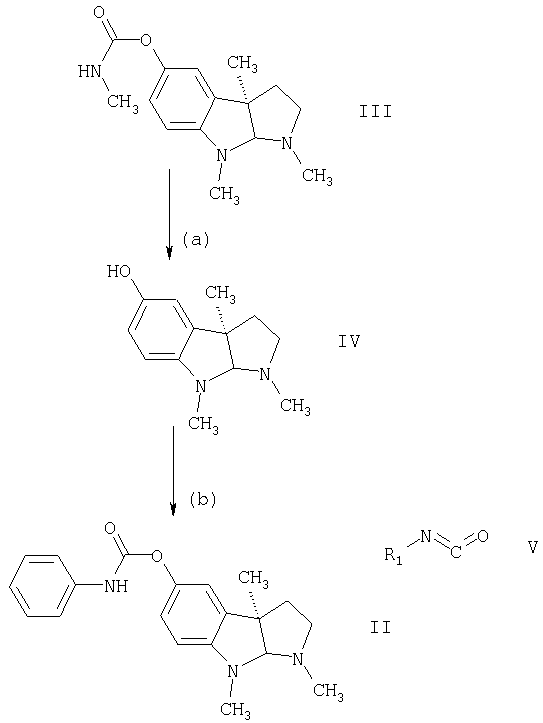
где R1 означает фенил.
В соответствии со способом данного изобретения физостигминовое соединение формулы III или его соль реагируют с образованием (+) эсеролинового соединения формулы IV при гидролизе физостигминового соединения формулы III гидроксидом щелочного металла в водной среде. Эсеролиновое соединение формулы IV затем выделяют в чистом виде из водной реакционной среды.
Очищенный эсеролин затем обрабатывают сильным органическим основанием в безводной среде, содержащей смешивающийся с водой органический растворитель. Обработанное эсеролиновое соединение затем взаимодействует, без выделения из предыдущей реакционной смеси, с изоцианатом формулы V. Эту реакцию проводят, смешивая вышеупомянутый изоцианат формулы V с эсеролиновым соединением в вышеупомянутой реакционной среде с образованием энантиомера формулы II. После этого реакцию останавливают прибавлением воды, что дает возможность легко выделить в чистом виде (+) фенсериновое соединение формулы III. В данном случае, вода может быть прибавлена к реакционной смеси, или реакционная смесь может быть прибавлена к воде. Обычно предпочтительно прибавлять реакционную смесь к воде.
В соответствии с данным изобретением любая фармацевтически приемлемая аддитивная соль кислоты с соединением формулы II может быть использована в способе лечения и композициях по данному изобретению. Понятие "фармацевтически приемлемые соли" относится к аддитивным солям кислот. Выражение "фармацевтически приемлемые аддитивные соли кислот" применимо к любым нетоксичным органическим и неорганическим солям соединения формулы II, причем предпочтительной является тартратная соль. Примерами неорганических кислот, которые образуют соответствующие соли, являются хлороводородная, бромоводородная, серная, фосфорная и такие кислые соли металлов, как моногидроортофосфат натрия и гидросульфат калия. Примерами органических кислот, образующих приемлемые соли, являются моно-, ди- и трикарбоновые кислоты. Примерами таких кислот могут быть, например, уксусная, гликолевая, молочная, пировиноградная, малоновая, янтарная, глутаровая, фумаровая, яблочная, винная, лимонная, аскорбиновая, малеиновая, гидроксималеиновая, бензойная, гидроксибензойная, фенилуксусная, коричная, салициловая, 2-феноксибензойная и такие сульфокислоты, как п-толуолсульфокислота, метансульфоновая кислота и 2-гидроксиэтансульфоновая кислота.
В соответствии с данным изобретением вышеупомянутое соединение или формула I или их фармацевтически приемлемые соли вводят перорально или через кожу, причем пероральное введение предпочтительно. Данные фармацевтические композиции настоящего изобретения для перорального введения и введения через кожу содержат соединение формулы I или его фармацевтически приемлемые соли в комбинации с совместимыми фармацевтически приемлемыми носителями. Может быть использован любой общепринятый носитель. Носитель может быть органическим или неорганическим инертным носителем, подходящим для такого введения. Подходящие носители включают воду, желатин, гуммиарабик, лактозу, крахмал, стеарат магния, тальк, растительные масла, полиалкиленгликоли, вазелин и им подобные носители. В дальнейшем, фармацевтические препараты могут содержать другие фармацевтически активные агенты. Дополнительные добавки, такие как органолептические добавки, консерванты, стабилизаторы, эмульгаторы, буферы, могут быть добавлены в соответствии с фармацевтической практикой.
Соединение формулы II и/или его фармацевтически приемлемые соли могут быть в соответствии с предпочтительным вариантом реализации данного изобретения назначены в виде разовой пероральной дозированной формы. Могут быть использованы любые общепринятые разовые дозированные пероральные формы, предпочтительной разовой дозированной формой являются таблетки или капсулы. Ежедневно для достижения желаемого результата можно использовать пероральные формы, содержащие приблизительно от 20 до 300 мг активного ингредиента, особо предпочтительны разовые дозированные пероральные формы, содержащие приблизительно от 50 до 150 мг. Кроме носителей эти пероральные дозированные формы обычно содержат общепринятые реципиенты, такие как связующие, дезинтегранты, смазки и вещества, улучшающие скольжение. Кроме того, любые общепринятые способы могут быть использованы для получения лекарственных форм для перорального применения в соответствии с данным изобретением.
Фармацевтические препараты можно получать в виде общепринятой разовой дозированной формы для перорального применения, включая твердые формы, такие как таблетки, капсулы, пилюли, порошки, гранулы и подобные им формы. Фармацевтические препараты могут быть стерилизованы и/или содержать такие вспомогательные вещества, как консерванты, стабилизаторы, смачивающие агенты, эмульгаторы, соли для создания осмотического давления и/или буферы.
Изобретение далее проиллюстрировано следующими примерами, которые предназначены только для иллюстративных целей и не ограничивают его.
Примеры
Пример 1
В атмосфере аргона, 50%(вес.) раствор гидроксида натрия (67,7 г, 0,8462 моль) прибавляли по каплям к взвеси (+) энантиомера салицилата физостигмина (100 г, 0,2418 моль) в дегазированной, деионизированной воде (300 мл) при 45°С. Во время прибавления температуру поддерживали в диапазоне 45-55°С. Затем выдерживали в течение 3 часов при 45°С, раствор желтого цвета охлаждали до 25-30°С и прибавляли трет-бутилметиловый эфир (300 мл). рН водной фазы доводили до 9,1 прибавлением водного раствора метабисульфита натрия (54 г Na2S2O5, 250 мл воды). Смесь перемешивали в течение 30 минут, фазам давали отстояться и затем разделяли. Водную фазу экстрагировали дважды по 30 минут, двумя порциями трет-бутилметилового эфира по 300 мл. Органические фазы объединяли, и промывали три раза 20%(вес.) раствором хлорида натрия по 200 мл, и высушивали над сульфатом магния (150 г) в течение ночи. Взвесь отфильтровывали через целит и осадок с фильтра промывали трет-бутилметиловым эфиром. Фильтрат концентрировали до 300 мл при 25-29 дюйм. вакуума и осадок дважды совместно перегоняли с диэтоксиметаном (300 мл каждый раз). Осадок разбавляли диэтоксиметаном (300 мл) и нагревали до 50°С. Полученную легкую взвесь охлаждали до 5°С и перемешивали в течение 45 минут, затем концентрировали до 300 л. Холодный гептан (300 мл) прибавляли по каплям, взвесь перемешивали в течение 45 минут и увеличивали объем прибавлением холодного гептана (125 мл). После перемешивания в течение приблизительно 2 часов взвесь отфильтровывали на воронке Бюхнера. Собранное твердое вещество промывали холодным гептаном (200 мл), затем сушили в вакууме в течение ночи. (+) Эсеролиновое основание (35,6 г) получено в виде белого твердого вещества с выходом 67,4% и степенью чистоты 98,3%.
Пример 2
В атмосфере аргона (+) эсеролиновый энантиомер (50 г) растворяли в 400 мл безводного диметоксиэтана. Каталитическое количество 2,5 М н-бутиллития в гексане (6,4 мл, 16 ммоль) прибавляли в течение 1 минуты и перемешивали раствор в течение 10 минут. Фенилизоцианат (27,269 г, 0,2286 ммоль) прибавляли в течение 32 минут, поддерживая температуру в диапазоне 20-23°С. Реакционный раствор перемешивали при комнатной температуре в течение 2 часов 20 минут, затем переносили в капельную воронку. Реакционный раствор прибавляли в течение 49 минут к смеси деионизированной воды (630 мл) и диметоксиэтана при интенсивном перемешивании. Полученную взвесь перемешивали в течение 30 минут, затем отфильтровывали на воронке Бюхнера (фильтровальная бумага Whatman#3). Твердый осадок промывали четыре раза деионизированной водой по 100 мл и один раз 100 мл гептана, затем осадок сушили при 45°С и >29 дюймов вакуума в течение 9 часов. (+) Энантиомер N-фенилкарбамоилэсеролина (74,4 г) был получен в виде красноватого твердого вещества с выходом 96,2% и степенью чистоты 95,1%.
Пример 3
В атмосфере аргона раствор винной кислоты (17,12 г, 0,114 моль) в смеси абсолютного этанола (131 мл) и деионизированной воды прибавляли в течение 32 минут к взвеси (+) энантиомера N-фенилкарбамоилэсеролина (35 г, 0,1037 моль), полученного выше, в смеси абсолютного этанола (126 мл) и деионизированной воды. После того как добавили от 60 до 75% раствора винной кислоты, в реакционный раствор вносили кристалл тартрата фенсерина (72 мг). Реакционную смесь перемешивали в течение 19 часов 15 минут при комнатной температуре и затем добавляли смесь изопропанола (490 мл) и воды (912 мл) в течение 30 минут. Взвесь перемешивали в течение 3,5 часов и отфильтровали на воронке Бюхнера (фильтровальная бумага Whatman#3). Осадок белого цвета дважды промывали изопропиловым спиртом (100 мл), затем высушивали при 45°С и вакууме 29 дюймов в течение 19 часов с получением тартрата (+) энантиомера N-фенилкарбамоилэсеролина с выходом 76% и степенью чистоты 99,4% в виде белого твердого вещества.
Пример 4
(+) Энантиомер формулы I, получение которого описано в примере 2, был исследован в сравнении с фенсерином в отношении контролирования уровней β-АРР и образования токсичных амилоидных протеинов (Аβ протеинов), которые получаются из β-АРР протеина по методике, раскрытой Shaw и др. в Proc. Nat. Acad. Sci. USA (2001) 98(13), 7605-7610, страницы 7606 и 7607, за исключением того, что сравнивали фенсерин и его (+) энантиомер друг с другом в снижении β-АРР и Аβ протеинов. Методика Shaw, по которой были проведены исследования, приводится ниже.
Обработка лекарством. SK-N-SH клетки нейробластомы выращивали на 60 мм чашках при концентрации 3×106 клеток и SH-SY-5Y клетки нейробластомы выращивали на 100 мм чашках при концентрации 3×105 клеток. Клетки выращивали на полной питательной среде (10% FBS, 2мМ глутамина в DMEM) в течение от 3 до 4 дней до достижения ими 70% слияния. Перед началом эксперимента обедненную среду заменяли на свежую (DMEM + 0,5% FBS), содержащую 0,5 или 50 мкМ (-)- или (+)-фенсерина, и клетки инкубировали при 37°С и 5% СО2 в течение специально указанного времени.
Приготовление лизата: Через определенные промежутки времени истощенную среду собирали и консервировали при -70°С для последующих анализов секреторных уровней β-АРР. Лизированные клетки получали, как описано раньше (Lahiri et al., 1997 and 1998). Уровни протеина в маточном растворе анализировали протеиновой пробой Бредфорда (BioRad, Melvill, NY).
Вестерн-блот: 50 мг протеина из каждого образца загружали в 10% NuPAGE Bis-Tris гель 1X NuPAGE MOPS SDS, элюирующий буфер (NOVEX, San Diego, CA) и протеины разделяли при 200 V в течение 45 минут. Затем гель переносили на нитроцеллюлозу при 25 V за 1,5 часа. Неспецифическое связывание блокировали и каждое пятно исследовали в течение 2 часов с помощью 22С11 N-концевого антитела анти-βАРР (2,5 мкг/мл, Boehringer Mannheim, Indianapolis, IN) или антиактивированного антитела ERK (25 нг/мл Promega, Madison, WI). Анти-мышиный Igg или анти-кроличий IgG, конъюгированные с пероксидазой хрена, использовали в качестве вторичных антител. Эквивалентную нагрузку образца определяли по окрашиванию Понсо С (Sigma, St. Louis, MO). Определение размера хемилюминисцирующего пятна проводили с использованием CD-камеры и NIH-IMAGE (вариант 4.1).
Проба лактата дегидрогеназы: Измерение свободного лактата дегидрогеназы (LDH) в определенной среде было использовано как маркер на выживаемость и целостность клеток, как описано раньше (Lahiri et al., 1997 и 1998).
Общая Аβ проба: Общие пептидные уровни Аβ в SH-SY-5Y и SK-N-SH образцах были определены чувствительным ELISA (Suzuki et al., 1994). Для измерения общего Аβ сэндвичевую иммунологическую пробу с поликлональным антителом кролика к остаткам 1-40 Аβ в качестве поглощающих антител для всех видов Аβ пептида Аβ1-40 и Аβ1-42 и моноклональным антителом к остаткам 17-25 Аβ использовали для определения уровней Аβ пептида и величины выражали как среднее из шести независимых экспериментов.
Результаты
Результаты данного исследования демонстрируют, что уменьшение уровней βАРР может быть использовано в качестве контроля в разные интервалы времени, используя фенсерин в различных дозах от 0,5 мкМ до 50 мкМ. 1) Сравнение с контролем показало, что использование высоких доз фенсерина снижает уровни βАРР в SK-N-SH клетках. Во всех случаях, даже после 16 часов, количество βАРР протеина уменьшалось при использовании фенсерина; 2) уровни Аβ протеина были существенно снижены по сравнению с контролем, особенно через 10 часов, благодаря использованию фенсерина; 3) как положительные, так и отрицательные антиподы фенсерина эффективны в снижении уровней βАРР, так же как и уровней Аβ протеинов по сравнению с контролем. Поэтому (+)-фенсериновый антипод, который не обладает антихолинэстеразной активностью, имеет схожее с фенсерином, который является (-) антиподом, действие на β-АРР и Аβ протеины в SK-N-SH клетках.
Пример 5
Способ исследования in vivo
При внутрибрюшинном введении (-) фенсерина грызунам (1 мл на кг веса в изотоническом растворе) в итоге тремор наблюдали при дозе 5 мг на кг массы тела. Это классическое центральное (мозговое) холинергическое возбуждение (сверхстимуляция). Такой тремор продолжается около одного часа. Тремор с симптомами периферической сверхстимуляции (слезо- и слюнотечение) был отмечен при дозировках (-) фенсерина 7,5 мг на кг массы тела. При дозировках (-) фенсерина 20 мг на кг массы тела жизнеспособность грызунов снижалась за счет тяжелого тремора и побочных периферических эффектов (в основном слюнотечение и затрудненное дыхание), и из 5 подопытных животных 2 погибали. Однако введение того же количества 20 мг на кг массы тела (+) фенсерина не вызвало у животных никаких симптомов (даже незначительного тремора), и животные выглядели подобно животным, получавшим чистый носитель, и контрольным животным.
Результаты исследования in vivo
(-) Фензерин улучшает обучаемость и навыки грызунов (так же как и человека) через его антихолинэстеразное воздействие, повышает уровень холинергических нейротрансмиттеров, ацетилхолина, который понижен в мозгу больного болезнью Альцгеймера. Нейротрансмиттер ацетилхолин отвечает за многие функции вне мозга, регулируя частоту сердечных сокращений, моторику желудочно-кишечного тракта, потоотделение, слюноотделение, слезотечение и т.д. Благодаря этим воздействиям, так же как сверхстимуляции холинэргической системы мозга, степень токсичности классических антихолинэстеразных препаратов (ривастигмин и галантамин) такая же, как при использовании фенсерина в высоких дозировках. С другой стороны, (+) фенсерин, однако, не имеет антихолинэстеразной активности и отсюда не обладает холинэргической активностью. Он может поэтому вводиться в более высоких дозировках, чем (-) фенсерин.
Пример 6
Капсулу готовили, используя в качестве активного компонента виннокислую соль соединения формулы I ("Активный компонент"):
Пример 7
Твердая желатиновая капсула, содержащая 100 мг активного компонента:
Состав: одна капсула содержит:
Методика:
Активный компонент во влажном виде размалывали в растворе желатина, мальтодекстрина, dl-α-токоферола и аскорбата натрия.
Полученную суспензию подвергали распылительной сушке.
Порошок после распылительной сушки смешивали с микрокристаллической целлюлозой и стеаратом магния.
260 мг этой смеси заполняли твердую желатиновую капсулу подходящего цвета и размера.
Пример 8
Таблетка, содержащая 150 мг активного компонента:
Состав:
Ядро таблетки:
Оболочка:
Методика:
Активный компонент смешивали с безводной лактозой и микрокристаллической целлюлозой.
Смесь гранулировали в воде с раствором/дисперсией поливинилпирролидона, dl-α-токоферола и аскорбата натрия.
Гранулированный материал смешивали со стеаратом магния и затем формовали в виде ядер весом 250 мг каждое.
Ядра покрывали оболочкой из раствора/суспензии указанного выше состава.
Пример 9
Этот пример иллюстрирует средства, с помощью которых эффективность (+) энантиомера формулы I в виде виннокислой соли может быть измерена.
Проводили случайный, двойной «слепой» опыт с контрольным плацебо для измерения эффективности (+) виннокислой соли фенсерина или лекарственной формы, описанной в Примере 6, ежедневно более 12 недель у 60 больных, имеющих симптомы, схожие с теми, что имеют место при болезни Альцгеймера (PAD). В этом исследовании участвовало 60 больных с PAD, говорящих по-английски, больные были мужчины и женщины от 50 до 85 лет.
План исследований
Полный план изучения
Общие замечания
Сорок больных получали в течение двух недель РТ и 50 мг BID, при этом их дозы увеличивали до 100 мг BID, которую оставляли без изменений в течение последних десяти недель. Параллельно двадцати больным назначили плацебо, и они получали похожие капсулы плацебо, не содержащие активного вещества, в течение всего исследования, длившегося 12 недель. Достаточное число потенциальных пациентов были осмотрены, чтобы гарантировать отбор 60 требуемых случаев. Все участники исследования были оценены до начала исследования (Первый уровень) и далее периодически тестировались, используя следующие стандартные тесты оценки эффективности;
- NPI (Neuropsychiatric Inventory,
- CGIC (Clinician's Global Impression of Change)
- ADAS-cog (Alzheimer's Disease Assessment Scale - cognitive subscale)
- MMSE (Mini-Mental State Exam)
- CANTAB (Cambridge Neuropsychological Test Automated Battery)
- ADCS-ADL (Activities of Daily Living)
К концу 12 недели исследований больные из подвергнутой лечению группы сохранили уровень не ниже Первого уровня перед лечением во всех упомянутых тестах. К концу 12 недели состояние около 30% больных улучшилось. С другой стороны, у пациентов, не подвергшихся лечению не было отмечено улучшений относительно Первого уровня по оценкам вышеупомянутых тестов, и состояние большинства пациентов в этой группе ухудшилось по сравнению с Первым уровнем.
Изобретение относится к медицине и касается способа лечения болезней, являющихся результатом когнитивных расстройств, в частности болезни Альцгеймера. Изобретение включает использование (+) энантиомера фенсерина - (+) 9-N-фенилкарбинолэсеролина, обладающего минимальной антихолинэстеразной активностью, или его фармацевтически приемлемой соли, например кислотно-аддитивной соли, в частности, в качестве активного компонента в составе фармацевтической композиции. Дозированная форма такой композиции содержит 20-500 мг активного компонента. При этом активный компонент вводят больному в количестве 0,5-10 мг/кг массы тела в день. Изобретение позволяет получить клинический эффект при указанных расстройствах в отсутствие побочных токсических эффектов, обусловленных антихолинэстеразной активностью, присущей агентам, обычно используемым при этих расстройствах. 6 н. и 8 з.п. ф-лы.
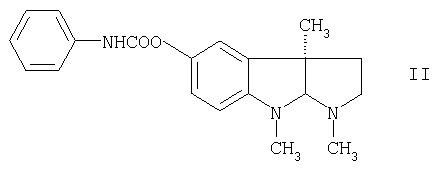
и его фармацевтически приемлемой соли,
указанный активный компонент и его соль назначают в количестве, эффективном для замедления развития упомянутых болезненных состояний.

и его соли,
указанную композицию назначают перорально, обеспечивая больному дозировку активного компонента от 0,5 до 10 мг на кг массы тела в день.

и его фармацевтически приемлемых солей, и
фармацевтически приемлемый носитель, подходящий для назначения внутрь, указанный активный компонент присутствует в количестве, подходящем для замедления развития расстройства.

или его фармацевтически приемлемые соли, и фармацевтически приемлемый носитель, подходящий для перорального введения, где указанный активный компонент присутствует в количестве от 20 до 300 мг.


и, по меньшей мере, один фармацевтически приемлемый эксципиент.
| Patel N | |||
| et al | |||
| Phenserine, a novel acetylcholinesterase inhibitor, attenuates impaired learning of rats in a 14-unit T-maze induced by blockade of the N-methyl-D-aspartate receptor | |||
| Neuroreport | |||
| Способ и аппарат для получения гидразобензола или его гомологов | 1922 |
|
SU1998A1 |
| Экономайзер | 0 |
|
SU94A1 |
| СПОСОБ ЛЕЧЕНИЯ АФАЗИИ | 1994 |
|
RU2123858C1 |
| СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ БОЛЕЗНИ АЛЬЦГЕЙМЕРА | 1995 |
|
RU2106864C1 |
Авторы
Даты
2006-07-27—Публикация
2003-03-18—Подача