Настоящее изобретение касается штаммов нового цирковируса свиней (сокращенно называемого PCV), ответственных за синдром PMWS (многосистемный вастинг-синдром свиней, называемый также много системным вастинг-синдромом после прекращения грудного вскармливания), реагентов и способов, позволяющих их обнаруживать, способов вакцинации и вакцин, а также способов получения этих реагентов и вакцин.
PCV первоначально обнаружили в виде нецитопатогенного загрязнителя в клеточных линиях РК/15 почек свиней. Этот вирус классифицировали как относящийся к Circoviridae, к которым также относятся вирус анемии кур (сокращенно называемый CAV) и вирус PBFDV (вирус болезни клюва и перьев попугаев). Это мелкие (от 15 до 24 нм), не имеющие оболочки вирусы, общей характеристикой которых является то, что они содержат геном в форме кольцевой одноцепочечной ДНК размером от 1,76 до 2,31 т.п.н. Первоначально предполагали, что этот геном кодирует полипептид массой около 30 кДа (Todd et al., Arch. Virol. 1991, 117; 129-135). Однако недавно проведенные исследования показали более сложную транскрипцию (Meehan B.M. et al., 1997, 78; 221-227). Более того, не найдено существенной гомологии в нуклеотидных последовательностях или в обычных антигенных детерминантах между этими тремя известными типами цирковирусов.
PCV, происходящий из клеток РК/15, считается непатогенным. Его последовательность известна из работы В.М.Meehan et al., J. Gen. Virol., 1997 (78) 221-227). Еще совсем недавно некоторые авторы считали, что штаммы PCV могут быть патогенными и связанными с синдромом PMWS (Gupi P.S. Nayar et al., Can. Vet. J., vol.38, 1997: 385-387, и Clark E.G., Proc Am. Assoc. Swine Prac. 1997; 499-501). Nayar et al. с помощью метода ПЦР обнаружили ДНК PCV у свиней, имеющих синдром PMWS. Однако ни один штамм PCV дикого типа до сих пор не выделен.
Синдром PMWS, обнаруженный в Канаде, в Соединенных Штатах Америки и во Франции, клинически характеризуется постепенной потерей веса и такими проявлениями, как тахипноэ (учащенное дыхание без его углубления), одышка и желтуха. С точки зрения патологии он проявляется лимфоцитной или грануломатозной инфильтрацией, лимфаденопатиями и, реже, гепатитом или лимфоцитическим или грануломатозным нефритом (Clark E.G., Proc Am. Assoc. Swine Prac. 1997; 499-501; La Semaine Vétérinaire №26, supplement to La Semaine Vétérinaire 1996 (834); La Semaine Vétérinaire 1997 (857): 54; (Gupi P.S. Nayar et al., Can. Vet. J., vol.38, 1997: 385-387).
Заявителю удалось выделить пять новых штаммов PCV из легочных и ганглиозных образцов, полученных с ферм, расположенных в Канаде, в США (Калифорния) и во Франции (Бретань), далее называемых цирковирусами в соответствии с настоящим изобретением. Эти вирусы обнаружили в местах с патологическими изменениями у свиней с синдромом PMWS, а у здоровых свиней таких вирусов не обнаружено.
Кроме того, заявитель расшифровал геномы четырех из этих штаммов, а именно штаммов, полученных из Канады, США, а также двух штаммов из Франции. Эти штаммы проявляют очень сильную гомологию относительно друг друга на нуклеотидном уровне, превышающую 96%, и гораздо более слабую относительно штамма РК/15 - около 76%. Таким образом, новые штаммы можно считать представителями нового типа цирковирусов свиней, которые здесь называют типом II, а тип I представлен РК/15.
Поэтому предметом настоящего изобретения являются цирковирусы свиней типа II, определенные выше, изолированные или в форме очищенного препарата.
Изобретение касается любых цирковирусов свиней, которые можно выделить из физиологического образца или из тканевого образца, особенно из пораженных болезнью участков, из больных свиней, имеющих синдром PMWS, особенно с помощью способа, описанного в примерах, в частности, цирковируса типа II.
Более конкретно, предметом настоящего изобретения являются очищенные препараты пяти штаммов, депонированных в ЕСАСС (Европейской коллекции клеточных культур Центра прикладной микробиологии и научных исследований, Porton Down, Salisbury, Wiltshire S54 OJG, United Kingdom), в четверг 2 октября 1997:
- коллекционный № V97100219 (называемый здесь Imp.1008PCV);
- коллекционный № V97100218 (называемый здесь Imp.1010PCV);
- коллекционный № V97100217 (называемый здесь Imp.999PCV);
и полученных в пятницу 16 января 1998:
- коллекционный № V98011608 (называемый здесь Imp.1011-48285);
- коллекционный № V98011609 (называемый здесь Imp.1011-48121).
Изобретение ставит своей целью рассмотрение цирковирусов свиней, изолированных из больной свиньи, и/или цирковирусов, имеющих значительное серологическое подобие со штаммами по настоящему изобретению, и/или цирковирусов, перекрестно гибридизующихся со штаммами по настоящему изобретению, в условиях такой степени строгости, чтобы они не позволяли осуществление гибридизации со штаммом PCV РК/15.
Вирусные штаммы, выделенные из физиологического образца или из тканевого образца, особенно из пораженного болезнью участка, из свиньи, имеющей синдром PMWS, можно успешно размножать на клеточных линиях, особенно таких, как клеточные линии почек свиней, в частности клетки РК/15, свободные от контаминации (в частности, для PCV, а также для пестивирусов, аденовирусов свиней и парвовирусов свиней), с целью их размножения и особенно с целью продуцирования ими антигена, целого (например, вируса) и/или его субъединиц (например, полипептидов).
Очень примечательно и неожиданно, что эти изоляты оказались весьма продуктивными в культуре клеткок РК/15, что имеет несомненное преимущество для продуцирования вируса или антигена, в частности для выработки инактивированной вакцины.
Предметом настоящего изобретения являются также препараты цирковирусов, изолированных после пассирования на клетках, особенно на клеточных линиях, например на клетках РК/15, культивируемых in vitro при инфецировании по меньшей мере одним из цирковирусов по настоящему изобретению или любым цирковирусом свиней, который можно изолировать из физиологического образца или тканевого образца, особенно из пораженных болезнью участков, из свиней, имеющих синдром PMWS. Целью изобретения также является культуральный экстракт или надосадочная жидкость, которые могут быть очищены с помощью стандартных методов, и в общем любые антигенные препараты, полученные из культур in vitro.
Предметом изобретения также являются иммуногенно-активные ингредиенты и вакцины, содержащие по меньшей мере один антиген, как определено выше.
Они могут представлять собой иммуногенно-активные ингредиенты, основанные на аттенюированных (ослабленных) живых целых вирусах, или вакцины, полученные с помощью этих активных ингредиентов, причем аттенюирование (ослабление) проводят обычными способами, например путем пассирования на клетках, предпочтительно путем пассирования на клетках свиньи, особенно на линиях, таких как клеточная линия РК/15 (используя, например, от 50 до 150, особенно порядка 100 пассажей). Эти вакцины, как правило, включают носитель или разбавитель, пригодный с ветеринарной точки зрения, необязательно адъювант, пригодный с ветеринарной точки зрения, а также необязательно стабилизатор для лиофилизации.
Эти вакцины предпочтительно содержат от 103 до 106 TCID50.
Они могут представлять собой иммуногенно-активные ингредиенты или вакцины, основанные на антигене цирковируса в соответствии с настоящим изобретением, в инактивированном состоянии. Кроме того, вакцина включает носитель или разбавитель, пригодные с ветеринарной точки зрения, с необязательной добавкой адъюванта, пригодного с ветеринарной точки зрения.
Цирковирусы по настоящему изобретению с фракциями, которые могут присутствовать, инактивируют в соответствии со способами, известными специалистам в данной области техники. Инактивацию предпочтительно осуществляют химически путем, например путем обработки антигена химическим агентом, таким как формальдегид (формалин), параформальдегид, β-пропиолактон или этиленимин или его производные. Предпочтительным способом инактивации для данного изобретения является обработка химическим агентом, в частности этиленимином или β-пропиолактоном.
Предпочтительно, к инактивированной вакцине по настоящему изобретению добавляют адъювант, который лучше использовать в форме эмульсий, например эмульсии воды в масле или масла в воде, в соответствии со способами, хорошо известными специалистам в данной области техники. Возможно также, чтобы адъювант поступал из обычного адъювантного соединения, включенного в активный ингредиент.
Из адъювантов, которые можно использовать, в качестве примеров можно упомянуть гидроксид алюминия, сапонины (например, сапонин Quillaja или Quil А; см. Vaccine Design, The Subunit and Adjuvant Approach, 1995, edited by Michael F. Powel and Mark J. Newman, Plennum Press, New-York and London, p.210), Avridine® (Vaccine Design, p.148), DDA (бромид диметилдиоктадецил-аммония, Vaccine Design, p.157), полифосфазен (Vaccine Design, p.204) или в качестве альтернативы - эмульсии масла в воде, основанные на минеральном масле, сквалене (например, эмульсия SPT, Vaccine Design, p.147), сквален (например, MF59, Vaccine Design, p.183), или эмульсии воды в масле, основанные на метаболизируемом масле (предпочтительно в соответствии с публикацией WO-A-94 20071), а также эмульсии, описанные в US-A-5422109. Можно также выбрать комбинации адъювантов, например Avridine® или DDA, с эмульсией.
Эти вакцины предпочтительно содержат от 106 до 108 TCID50.
Адъюванты для живых вакцин можно выбрать из адъювантов, приведенных для инактивированных вакцин. Предпочтительны эмульсии. К адъювантам, указанным для инактивированных вакцин, можно добавить адъюванты, описанные в публикации WO-A-9416681.
В качестве стабилизатора для лиофилизации, можно упомянуть, к примеру, SPGA (Bovarnik et al., J. Bacteriology 59, 509, 950), углеводы, такие как сорбит, маннит, крахмал, сахароза, декстран или глюкоза, белки, такие как альбумин или казеин, производные этих соединений, или буферы, такие как фосфаты щелочных металлов.
Кроме того, заявитель получил геномы четырех изолятов, обозначенные как последовательности (ПОСЛЕДОВ.) №№ от 1 до 4 и необязательно №6.
Поэтому предметом настоящего изобретения является фрагмент ДНК, содержащий все эти последовательности или их часть. Не стоит и говорить, что изобретение автоматически охватывает все эквивалентные последовательности, например последовательности, которые не изменяют функциональные свойства или штамм-специфичность описанной последовательности или кодируемых этой последовательностью полипептидов. Безусловно, изобретение также включает последовательности, отличающиеся вследствие вырожденности кода.
Изобретение также охватывает последовательности, эквивалентные в том смысле, что они способны гибридизоваться с вышеописанной последовательностью в условиях высокой степени строгости и/или имеют высокую гомологию со штаммами по настоящему изобретению и принадлежат к группе II, определенной выше.
Эти последовательности и их фрагменты можно удобно использовать для экспрессии полипептидов in vitro или in vivo с помощью соответствующих векторов.
В частности, открытые рамки считывания, образующие фрагменты ДНК в соответствии с настоящим изобретением, которые можно использовать для получения этого эффекта, идентифицировали на геномной последовательности цирковирусов типа II. Изобретение касается любого полипептида, содержащего по меньшей мере одну из этих открытых рамок считывания (соответствующую аминокислотную последовательность). Предпочтительно, изобретение касается белка, по существу состоящего из ORF4, ORF7, ORF10 или ORF13 (ORF - открытая рамка считывания).
Для экспрессии субъединиц in vitro в качестве средства экспрессии предпочтительно используют Е. coli или бакуловирус (US-A-4745051). Кодирующую последовательность (или последовательности) или их фрагменты встраивают в геном бакуловируса (нитевидного вируса) (например, baculovirus Autographa californica Nuclear Polyhedrosis Virus AcNPV), а затем последний размножают в клетках насекомого, например Spodoptera frugiperda Sf9 (Образец из Американской коллекции клеточных культур АТСС CRL 1711). Субъединицы можно также продуцировать в клетках эукариот, таких как дрожжи (например, Saccharomyces cerevisiae) или в клетках млекопитающих (например, в клетках СНО- яичников китайского хомяка, в клетках ВНК).
Предметом настоящего изобретения также являются полипептиды, продуцируемые in vitro с помощью этих средств экспрессии, а затем необязательно очищаемые в соответствии с обычными методами. Предметом изобретения также является субъединичная (основанная на субъединицах) вакцина, включающая по меньшей мере один полученный таким образом полипептид или фрагмент, в носителе или разбавителе, пригодных с ветеринарной точки зрения, и необязательно адъювант, пригодный с ветеринарной точки зрения.
Для экспрессии in vivo, в целях продуцирования рекомбинантных живых вакцин, кодирующая последовательность или последовательности или их фрагменты встраивают в подходящий вектор экспрессии в условиях, обеспечивающих экспрессию данного полипептида или полипептидов. В качестве подходящих векторов можно использовать живые вирусы, предпочтительно способные к размножению в свиньях, непатогенные для свиней (обладающие естественной или искусственно приданной непатогенностью), в соответствии с методами, хорошо известными специалистам в данной области техники. В частности, можно использовать вирусы герпеса свиней, такие как вирус болезни Ауески (ложного бешенства), аденовирус свиней, вирусы оспы, особенно вирус коровьей оспы, вирус птичьей оспы, вирус оспы канареек, вирус оспы свиней. В качестве векторов можно также использовать плазмидные ДНК (WO-A-9011092, WO-A-9319813, WO-A-9421797, WO-A-9520660).
Предметом настоящего изобретения поэтому также являются векторы и рекомбинантные живые вакцины или плазмидные вакцины (полинуклеотидные или ДНК-вакцины), полученные таким образом, причем эти вакцины включают, кроме того, носитель или разбавитель, пригодный с ветеринарной точки зрения.
Вакцины в соответствии с настоящим изобретением (живые ослабленные, инактивированные, субъединичные, рекомбинантные и плазмидные вакцины) могут включать один или более активных ингредиентов (антигенов) одного или более (2 или 3) цирковирусов в соответствии с настоящим изобретением.
Для каждого вышеописанного типа вакцины настоящее изобретение также предлагает комбинированную вакцинацию против цирковирусов свиней с вакцинацией против других патогенов свиней, в частности против тех, которые могут быть связаны с синдромом PMSW. Поэтому вакцины в соответствии с настоящим изобретением, в частности инактивированные, могут включать другую валентность, соответствующую другому патогену свиней. Среди этих других патогенов свиней, предпочтительно можно назвать PRRS (репродуктивно-респираторный синдром свиней) (специалисты в данной области техники могут обратиться к следующим публикациям: WO-A-93/07898, WO-A-94/18311, FR-A-2709966; С.Chareyre et al., Proceedings of the 15th IPVS Congress, Birmingham, England. 5-9 July 1998, p.139, которые включены в настоящее описание в качестве ссылок) и/или Mycoplasma hyopneumonia (специалисты в данной области техники могут обратиться к следующим публикациям: ЕР-А-597852, ЕР-А-550477, ЕР-А-571-648; О.Martinon et al., р.157, 284, 285 and G.Reynaud et al., p.150, все в вышецитированном издании Proceedings of the 15th IPVS Congress, которые включены в настоящее описание в качестве ссылок). Среди других интересных валентностей можно упомянуть также Actinobacillus pleuropneumoniae, E. coli, атрофический ринит свиней, а также ложное бешенство (болезнь Ауески), холеру свиней, свиной грипп.
Предметом настоящего изобретения также является способ, позволяющий индуцировать у свиней иммунную реакцию на цирковирусы в соответствии с настоящим изобретением. Предметом изобретения, в частности, является способ вакцинации, который эффективен для свиней.
Способ предлагает введение свиньям одной или более порций вышеописанной вакцины. Можно также объединять несколько вышеописанных вакцин в одной и той же схеме вакцинации.
Этот способ применим не только для взрослых свиней, но также и для поросят или для беременных самок. Вакцинация последних делает возможным создание пассивного иммунитета у новорожденных (антитела материнского происхождения).
Изобретение также предлагает возможность диагностики присутствия цирковирусов по настоящему изобретению у свиней. Предметом изобретения поэтому также являются диагностические тесты и способы диагностики, связанные с использованием реагентов, которые будут описаны ниже.
Знание последовательностей различных цирковирусов позволяет определить общие последовательности, что в свою очередь делает возможным получение реагентов, способных распознавать все известные цирковирусы свиней.
Специалисты в данной области техники могут также выбрать фрагменты последовательностей, соответствующие областям, лишь в малой степени проявляющим гомологию или совсем не проявляющим гомологии с соответствующей последовательностью цирковируса РК/15, для того, чтобы поставить конкретный диагноз.
Сопоставление последовательностей позволяет специалистам в данной области техники выбрать реагент в соответствии с их пожеланиями.
Первый реагент состоит из описываемых здесь последовательностей ДНК и их фрагментов, которые, в частности, можно использовать в качестве зондов или праймеров в хорошо известных методах гибридизации или ПЦР (полимеразной цепной реакции).
Второй реагент состоит из полипептидов, кодируемых этими последовательностями вируса, или экспрессируемых с помощью вектора (см. выше), или синтезированных химическим путем в соответствии с обычными способами синтеза пептидов.
Третий и четвертый реагенты соответственно состоят из поликлональных и моноклональных антител, которые можно получить в соответствии с обычными способами вирусов, полипептидов или фрагментов, экстрагированных или кодируемых последовательностями ДНК.
Эти второй, третий и четвертый реагенты можно использовать в способе диагностики, являющемся одним из предметов данного изобретения, в котором тестируют на образец физиологической жидкости (кровь, плазма, сыворотка и т.п.) или образец ткани (ганглий, печень, легкие, почки и т.п.), полученный от подлежащей тестированию свиньи, на присутствие антигена, специфичного для цирковируса в соответствии с настоящим изобретением, путем поиска и обнаружения либо самого антигена, либо антител, направленных против этого антигена.
Антигены и антитела по настоящему изобретению можно использовать в любом известном лабораторном методе диагностики.
Однако предпочтительно использовать их в методах, которые могут использовать непосредственно в полевых условиях ветеринарный врач, селекционер или владелец животного. Специалисты в данной области техники имеют в своем распоряжении различные лабораторные и полевые методы, и поэтому вполне могут адаптировать к своим условиям применение этого антигена и/или антител в качестве реагента или реагентов для диагностики.
Методами диагностики, которые предпочтительно использовать в рамках настоящего изобретения, являются вестерн-блотинг, иммунофлуоресцентный анализ, ИФА (иммуноферментный анализ) и иммунохроматография.
Что касается использования методов иммунохроматографии, то специалисты могут обратиться, в частности, к публикации Robert F.Zurk et al., Clin. Chem. 31/7, 1144-1150 (1985), а также к патентам и заявкам на патенты WO-A-88/08 534, WO-A-91/12528, ЕР-А-291176, ЕР-А-299428, ЕР-А-291194, ЕР-А-284232, US-A-5120643, US-A-5030558, US-A-5266497, US-A-4740468, US-A-5266497, US-A-4855240, US-A-5451-504, US-A-5141850, US-A-5232835 и US-A-5238652.
Соответственно, предпочтительно осуществлять поиск и обнаружение специфичных антител в образце с помощью непрямого теста, используя конкуренцию или замещение. Чтобы сделать это, в качестве реагента для диагностики используют сам антиген или фрагмент этого антигена, все еще способный распознаваться антителами. Мечение можно успешно осуществлять путем мечения пероксидазой или с помощью особых способов мечения, предпочтительно коллоидным золотом.
Может также быть желательным обнаружение самого антигена в образце с помощью меченого антитела, специфичного для данного антигена. Мечение лучше всего проводить так, как описано выше.
Под антителом, специфичным для антигена, которое можно использовать, в частности, при конкуренции или замещении или для обнаружения самого антигена, подразумеваются моноклональные или поликлональные антитела, специфичные для антигена, фрагменты этих антител, предпочтительно фрагменты Fab или F(ab)'2.
Другим признаком данного изобретения является получение поликлональных или моноклональных антител, специфичных для антигена в соответствии с настоящим изобретением, причем эти антитела затем можно использовать, в частности, в качестве реагентов для диагностики, для обнаружения антигена в образце физиологической жидкости или в образце ткани или даже для обнаружения антител, присутствующих в таких образцах. Изобретение также включает иммунологически функциональные фрагменты этих антител, в частности фрагменты F(ab) или F(ab)'2.
Антитела можно получить обычными способами. Можно, в частности, сослаться на следующие публикации: Antibodies, A Laboratory Manual, 1988, Cold Spring Harbor Laboratory, USA или J.M.Goding, Monoclonal Antibodies: Principles and Practice, Academic Press Inc., содержание которых включено в настоящее описание в качестве ссылки.
В частности, можно, как это известно per se (само по себе), осуществить слияние клеток селезенки мышей, иммунизированных антигеном или по меньшей мере одним из его фрагментов, соответствующими миеломатозными клетками.
Предметом настоящего изобретения является также получение предпочтительно очищенных или частично очищенных, или даже неочищенных моноклональных или поликлональных антител, специфичных для антигена, особенно мышиных или кроличьих антител.
Настоящее изобретение также позволяет определить представляющие интерес эпитопы, особенно на основе описанных здесь последовательностей ДНК, независимо от того, представляют ли данные эпитопы интерес для вакцины или для диагностики. На основе последовательности ДНК генома цирковируса в соответствии с настоящим изобретением специалисты в данной области техники в состоянии определить эпитопы в соответствии с известными методами, например с помощью соответствующей компьютерной программы или метода PEPSCAN. Эпитопы представляют собой иммунодоминантные области белков, расположенные на поверхности белков. Поэтому их могут распознавать антитела и поэтому они особенно применимы в области диагностики либо для получения антител в целях диагностики, либо для продуцирования соответствующих пептидов, которые можно использовать в качестве реагентов для диагностики.
По меньшей мере, эпитоп представляет собой пептид, имеющий от 8 до 9 аминокислот. Обычно предпочтительным является, чтобы эпитоп имел минимум от 13 до 25 аминокислот.
Поэтому специалисты в данной области техники в состоянии, используя один или более этих методов, а также и другие подходящие методы, найти эпитопы для использования пептидов или антител в диагностических целях.
Предметом настоящего изобретения является также набор для диагностики, включающий этот антиген и/или поликлональные или моноклональные антитела, специфичные для этого антигена. В частности, это наборы для диагностики, соответствующие вышеописанным методам диагностики.
Далее изобретение описывается более подробно, с помощью неограничительных, приведенных в качестве примеров вариантов его осуществления со ссылками на чертежи, в которых:
Фиг.1: Последовательность ДНК генома штамма Imp.1011-48121.
Фиг.2: Последовательность ДНК генома штамма Imp.1011-48285.
Фиг.3: Последовательность ДНК генома штамма Imp. 999.
Фиг.4: Последовательность ДНК генома штамма Imp. 1010.
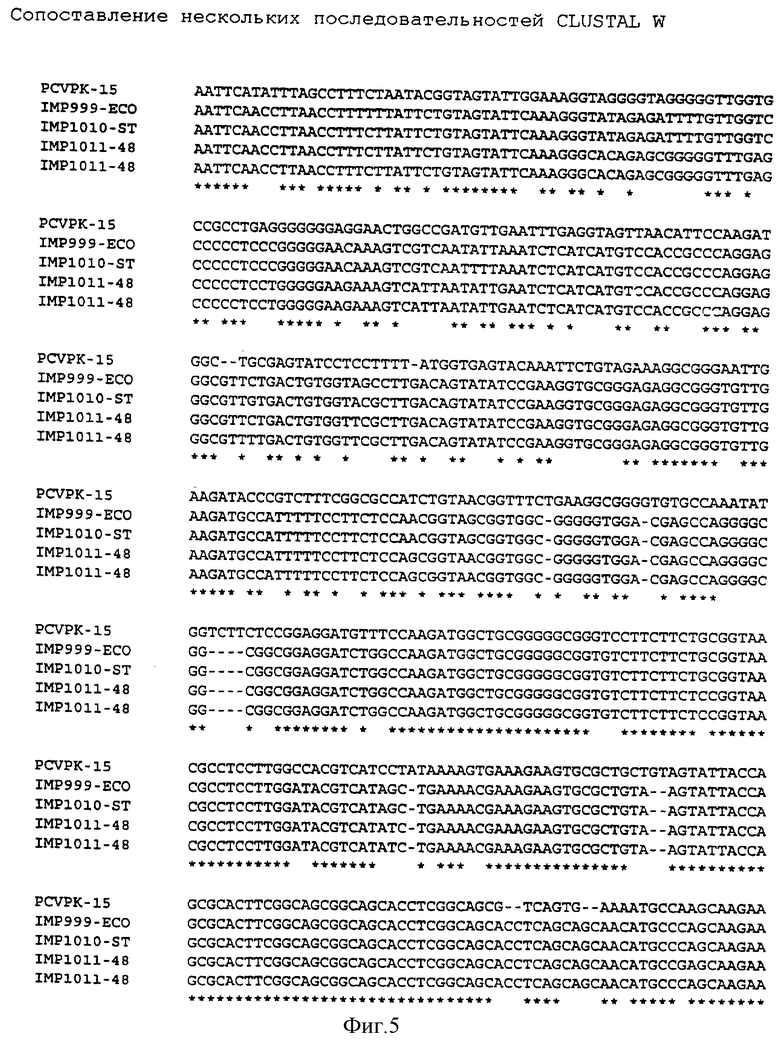
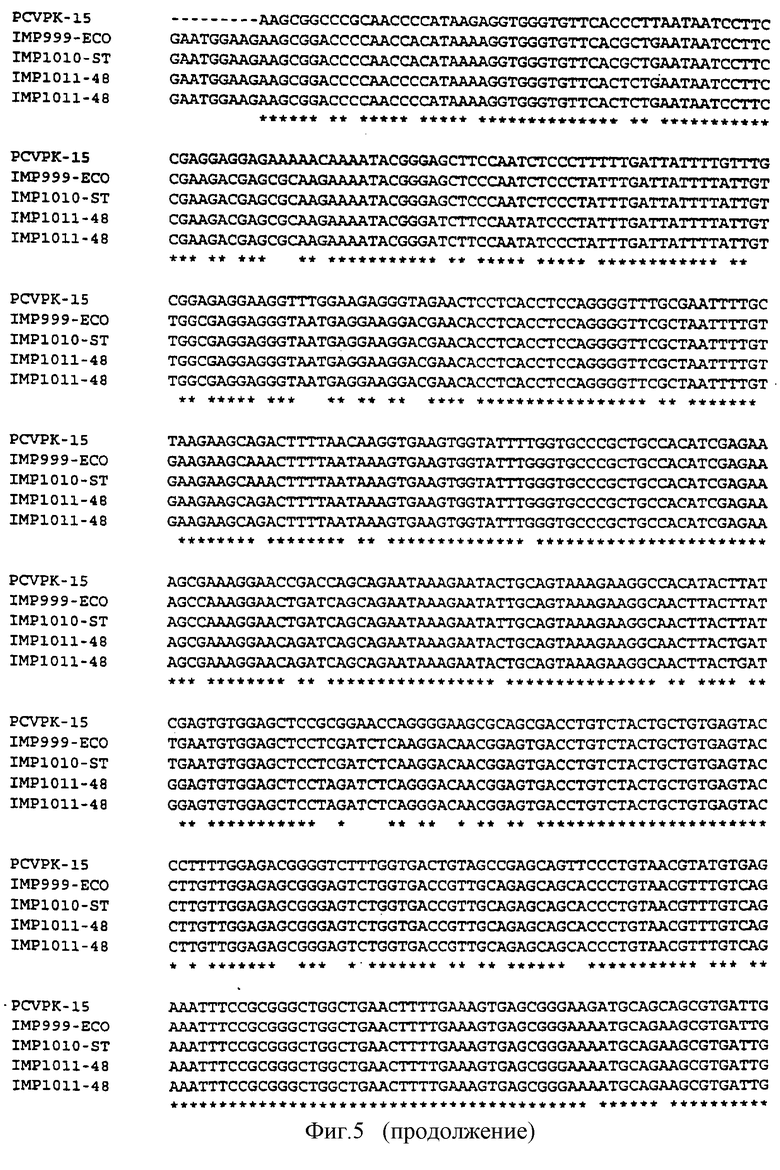
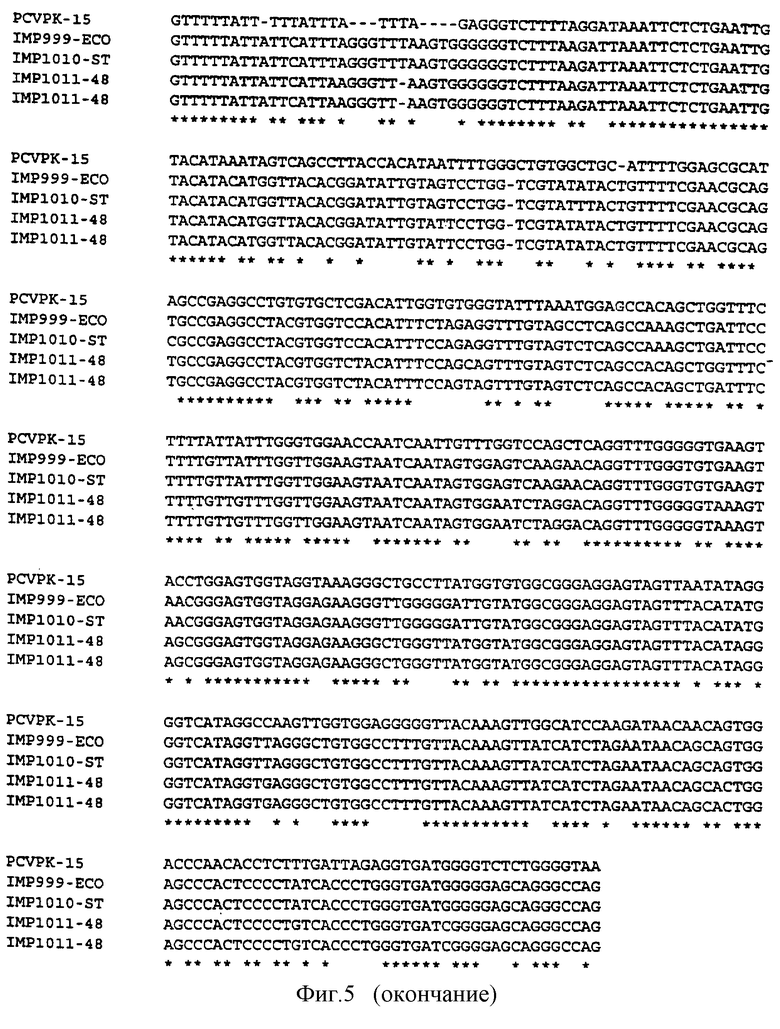
Фиг.5: Сопоставление 4 последовательностей в соответствии с фиг.1-4 с последовательностью штамма PCV РК/15.
Фиг.6: Последовательность ДНК генома штамма Imp.999, определенная при его первой регистрации во Франции 3 октября 1997.
Фиг.7: Сопоставления последовательности фиг.6 с последовательностью штамма РК/15.
Перечень последовательностей, №№ последовательностей.
ПОСЛЕДОВ. №1: Последовательность ДНК генома штамма Imp. 1011-48121.
ПОСЛЕДОВ. №2: Последовательность ДНК генома штамма Imp. 1011-48285.
ПОСЛЕДОВ. №3: Последовательность ДНК генома штамма Imp. 999.
ПОСЛЕДОВ. №4: Последовательность ДНК генома штамма Imp. 1010.
ПОСЛЕДОВ. №5: Последовательность ДНК генома штамма РК/15.
ПОСЛЕДОВ. №6: Последовательность ДНК генома штамма Imp. 999, определенная при его первой регистрации во Франции 3 октября 1997.
ПРИМЕРЫ
ПРИМЕР 1. Культивирование и выделение штаммов цирковирусов свиней.
Образцы тканей отбирали во Франции, в Канаде и в США из легких и лимфатических узлов поросят. Эти поросята проявляли клинические признаки типичного многосистемного вастинг-синдрома после прекращения грудного вскармливания. Чтобы облегчить выделение вирусов, образцы тканей сразу же после аутопсии (вскрытия трупов) замораживали при -70°.
Для выделения вирусов готовили суспензии, содержащие около 15% образца ткани, в содержащей соли минимальной среде по Earl (ЕМЕМ, BioWhittaker UK Ltd., Wokingham, UK), пенициллин (100 мкг/мл) и стрептомицин (100 мкг/мл) (среда MEM-SA), путем растирания тканей со стерильным песком с помощью ступки и пестика. Измельченный препарат переносили в среду MEM-SA, a затем центрифугировали при 3000 g в течение 30 минут при +4°С, чтобы получить и собрать надосадочную жидкость.
Перед инокуляцией клеточных культур к 2 мл каждой надосадочной жидкости добавляли по 100 мкл хлороформа и непрерывно перемешивали в течение 10 минут при комнатной температуре. Эту смесь затем переносили в микроцентрифужную пробирку, центрифугировали при 3000 g в течение 30 минут, после чего собирали надосадочную жидкость. Надосадочную жидкость использовали в качестве инокулята для экспериментов по выделению вирусов.
Все исследования по выделению вирусов выполняли на клеточных культурах РК/15, для которых было известно, что они не заражены цирковирусом свиней (PCV), пестивирусами, аденовирусами свиней и парвовирусами свиней (Allan G. et al., Pathogenesis of porcine circovirus experimental infections of colostrum-deprived piglets and examination of pig foetal material. Vet. Microbiol. 1995, 44, 49-64).
Выделение цирковирусов свиней осуществляли в соответствии со следующим методом:
Монослои клеток РК/15 диссоциировали посредством трипсинизации (смесью трипсина и версена) из конфлюэнтных (сливающихся) культур, а затем переносили в среду MEM-SA, содержащую 15% фетальной телячьей сыворотки, не загрязненную пестивирусом (среда MEM-G), с конечной концентрацией около 400000 клеток на 1 мл. Фракции этой суспензии аликвотами по 10 мл смешивали с 2-миллилитровыми аликвотами фракций вышеописанных инокулятов и окончательную смесь переносили аликвотами по 6 мл в 2 фальконовских флакона на 25 см2. Затем эти культуры инкубировали при температуре +37°С в течение 18 часов в атмосфере CO2.
После инкубации культуральную среду полуконфлюэнтных монослоев обрабатывали 300 мМ D-глюкозамина (Cat. № G48175, Sigma-Aldrich Company Limited, Poole, UK) (Tischr I. et al., Arch. Virol., 1987, 96, 39-57), затем продолжали инкубацию еще в течение 48-72 часов при +37°С. После этой последней инкубации один из двух фальконовских флаконов для каждого инокулята подвергали трем последовательным циклам замораживания/оттаивания. Клетки РК/15 из оставшихся флаконов обрабатывали раствором смеси трипсина и версена, вновь суспендировали в 20 мл среды MEM-G, а затем инокулировали в фальконовские флаконы на 75 см2 при концентрации 400000 клеток/мл. Затем свежеинокулированные флаконы суперинфецировали путем добавления 5 мл соответствующего лизата, полученного после циклов замораживания/оттаивания.
ПРИМЕР 2. Получение образцов клеточных культур для обнаружения цирковирусов свиней с помощью иммунофлуоресценции или путем гибридизации in situ.
Отбирали 5 мл суперинфецированной суспензии и инокулировали в чашки Петри диаметром 55 мм, в которых находились стерильные обезжиренные покровные стекла. Культуры в флаконах и на покровных стеклах инкубировали при +37°С и обрабатывали глюкозамином, как описано в примере 1. Через 24 до 48 часов после обработки глюкозамином культуры на покровных стеклах фиксировали либо ацетоном в течение 10 минут при комнатной температуре, либо 10%-ным забуференным формальдегидом в течение 4 часов. После этой фиксации все до использования фиксированных стекол для исследований по гибридизации in situ и иммуноцитохимическими методами покровные стекла хранили при -70°С на силикагеле.
ПРИМЕР 3. Методы обнаружения последовательностей PCV посредством гибридизации in situ.
Гибридизацию in situ осуществляли на тканях, взятых у больных свиней и фиксированных формальдегидом, а также на препаратах клеточных культур, инокулированных для выделения вирусов (см. пример 2) и фиксированных на покровных стеклах.
Использовали полные геномные зонды, соответствующие цирковирусам свиней (PCV) PK/15 и инфекционному вирусу анемии кур (CAV). Плазмиду pPCV1, содержащую репликативную форму генома PCV, клонированую в форме одинарной вставки величиной в 1,7 тысяч пар оснований (т.п.о.) (Meehan В. et al. Sequence of porcine circovirus DNA: affinities with plant circoviruses, J. Gen. Virol. 1997, 78, 221-227), использовали в качестве источника вирус-специфической PCV ДНК. Аналогичную плазмиду, рСАА1, содержащую репликативную форму цирковируса птиц CAV размером в 2,3 т.п.о., использовали в качестве отрицательного контроля. Соответствующие глицерольные штоки этих двух плазмид использовали для продуцирования и очистки плазмид методом щелочного лизиса (Sambrook J. et al. Molecular cloning: A laboratory Manual, 2nd Edition, Cold Spring Harbor laboratory, Cold Spring Harbor, New York, 1989) с тем, чтобы далее использовать их в качестве матриц для получения зондов. Цирковирусные зонды, репрезентативные для полного генома PCV и CAV, получали из очищенных плазмид, описанных выше (по 1 мкг для каждого зонда), и из гексануклеотидных праймеров, для которых рандомизированно использовали коммерческий набор нерадиоактивных меток ("DIG DNA labelling kit", Boehringer Mannheim, Lewes, UK), в соответствии с рекомендациями изготовителя.
Меченые дигоксигенином зонды растворяли в 50-100 мкл стерильной воды прежде, чем использовать их для гибридизации in situ.
Образцы тканей больных свиней, заключенные в парафин и фиксированные формальдегидом, а также препараты инфецированных клеточных культур, фиксированные формальдегидом, получали для обнаружения нуклеиновых кислот PCV в соответствии со следующим методом:
Из тканевых блоков, заключенных в парафин, делали срезы толщиной 5 мкм, освобождали их от парафина, а затем дегидрировали в растворах с последовательно уменьшающимися концентрациями спирта. Срезы тканей и клеточные культуры, фиксированные формальдегидом, инкубировали соответственно в течение 15 и 5 минут при +37°С в растворе 0,5% протеиназы К в 0,05 М Трис-HCl-буфере, содержащем 5 мМ EDTA (рН 7,6). Затем предметные стекла с препаратами помещали в 1% раствор глицина в автоклавированной дистиллированной воде на 30 секунд, дважды промывали 0,01 М PBS (физраствором с фосфатным буфером) (рН 7,2) и, наконец, промывали в течение 5 минут в стерильной дистиллированной воде. Затем их окончательно высушивали на открытом воздухе и приводили в контакт с зондами.
Каждый препарат ткани/зонда покрывали чистым обезжиренным покровным стеклом, а затем помещали в печь с температурой +90°С на 10 минут, прикладывали кусок льда на 1 минуту и, наконец, инкубировали в течение 18 часов при +37°С. Затем препараты ненадолго погружали в 2XSSC (рН 7,0), чтобы удалить защитные покровные стекла, после чего дважды по 5 минут промывали 2Х SSC- и, наконец, дважды по 5 минут промывали PBS.
После этих промывок препараты погружали в раствор 0,1 М малеиновой кислоты, 0,15 М NaCl (рН 7,5) (малеиновый буфер) на 10 минут, а затем инкубировали в 1% растворе блокирующего реагента (Cat. №1096176, Boehringer Mannheim, Lewes, East Sussex, UK) в малеиновом буфере в течение 20 минут при +37°С.
Затем препараты инкубировали с 1/250 раствором антидигоксигениновых моноклональных антител (Boehringer Mannheim) в блокирующем буфере в течение 1 часа при +37°С, промывали PBS и, наконец, инкубировали с биотинилированными антимышиными антителами в течение 30 минут при +37°С. Препараты промывали PBS, активность эндогенной пероксидазы блокировали посредством обработки 0,5% раствором перекиси водорода в PBS в течение 20 минут при комнатной температуре. Затем препараты снова промывали PBS и инкубировали с субстратом 3-амино-9-диэтилкарбазоловым (AEC) (Cambridge Bioscience, Cambridge, UK), приготовленным непосредственно перед использованием.
После окончательной промывки водопроводной водой препараты подвергали контрастному окрашиванию гематоксилином, «подсинивали» под водопроводной водой, а затем заливали на покровном стекле для микроскопирования заливочной жидкостью (GVA Mount, Cambridge Bioscience, Cambridge, UK). Контрольные варианты включали использование неподходящего отрицательного зонда (CAV) и положительного зонда (PCV) на образцах, полученных от больных свиней и от здоровых свиней.
ПРИМЕР 4. Метод обнаружения PCV с помощью иммунофлуоресценции
Первоначальный скрининг всех препаратов клеточных культур, фиксированных ацетоном, осуществляли методом непрямой иммунофлуоресценции (IIF) с использованием пула сывороток взрослых свиней в разведении 1/100. Этот пул сывороток включал сыворотки от 25 взрослых свиноматок из Северной Ирландии, а также содержал антитела против широкого спектра вирусов свиней, включая PCV, парвовирус свиней, аденовирус свиней и вирус PRRS (репродуктивно-респираторного синдрома свиней). Анализ методом IIF выполняли путем инкубации сыворотки (разведенной PBS) с клеточными культурами в течение 1 часа при +37°С с последующей двукратной промывкой PBS. Затем клеточные культуры инкубировали с разведенными 1/80 PBS антителами кролика к свиному иммуноглобулину, конъюгированными с изотиоцианатом флуоресцеина (FITC) в течение 1 часа, после чего промывали PBS и заливали в глицериновом буфере перед микроскопическим исследованием под ультрафиолетовым светом.
ПРИМЕР 5. Результаты гибридизации in situ на тканях больных свиней.
Гибридизация in situ, проводившаяся с помощью зонда на основе генома PCV, выделенного из тканей, взятых у французских, канадских и калифорнийских поросят, имеющих патологические изменения, вызванные многосистемным вастинг-синдромом, и зафиксированных формальдегидом, продемонстрировала присутствие нуклеиновых кислот PCV, связанных с пораженными болезнью участками, в нескольких из изученных пораженных болезнью участков. Никаких сигналов не наблюдалось, когда зонды на основе генома PCV использовали на тканях, взятых у здоровых свиней, или когда на тканях больных свиней использовали зонд CAV. Присутствие нуклеиновой кислоты PCV идентифицировали в цитоплазме и ядре многочисленных одноядерных клеток, инфильтрующих пораженные болезнью участки в легких калифорнийских поросят. Было также продемонстрировано присутствие нуклеиновой кислоты PCV в пневмоцитах, бронхиальных и бронхиолярных эпителиальных клетках, а также в эндотелиальных клетках артериол, венулах и лимфатических сосудах.
У больных поросят из Франции присутствие нуклеиновой кислоты PCV обнаружили в цитоплазме многочисленных фолликулярных лимфоцитов и в интрасинусоидальных одноядерных клетках лимфатических узлов. Нуклеиновую кислоту PCV обнаружили также в некоторых синцитиях. В зависимости от результатов обнаружения нуклеиновой кислоты PCV, образцы легких калифорнийских свиней, лимфатических узлов брыжейки французских свиней и органов канадских свиней использовали для выделения новых штаммов цирковирусов свиней.
ПРИМЕР 6. Результаты культивирования клеток с новыми штаммами цирковируса свиней и обнаружение с помощью иммунофлуоресценции
Никакого цитопатического эффекта не наблюдалось в клеточных культурах, инокулированных образцами, взятыми у французских поросят (штамм Imp.1008), у калифорнийских поросят (штамм Imp.999) и у канадских поросят (штамм Imp.1010), проявляющих клинические признаки многосистемного вастинг-синдрома. Однако иммунное мечение препаратов, полученных из инокулированных клеточных культур, фиксированных ацетоном, и с пулом свиных поликлональных сывороток, выявило ядерную флуоресценцию в многочисленных клетках в культурах, инокулированных с использованием легких калифорнийских поросят (штамм Imp.999), с использованием лимфатических узлов брыжейки французских поросят (штамм Imp.1008) и с использованием органов канадских поросят (штамм Imp.1010).
ПРИМЕР 7. Экстрагирование геномной ДНК цирковирусов свиней.
Репликативные формы новых штаммов цирковируса свиней (PCV) получали путем инфецирования клеточных культур РК/15 (см. пример 1) (10 флаконов по 75 см3), собранных после 72-76 часов инкубации и обработанных глюкозамином, как описано для клонирования репликативной формы CAV (Todd D. et al. Dot blot hybridization assay for chicken anemia agent using a cloned DNA probe. J. Clin. Microbiol. 1991, 29, 933-939). Двухцепочечную ДНК репликативных форм экстрагировали в соответствии с модификацией метода Хирта (Hirt В. Selective extraction of polyoma virus DNA from infected cell cultures, J. Mol. Biol., 1967, 36, 365-369), описанной Молитором (Molitor T.W. et al. Porcine parvovirus DNA: characterization of the genomic and replicative form DNA of two virus isolates, Virology, 1984, 137, 241-254).
ПРИМЕР 8. Рестрикционная карта репликативной формы генома штамма Imp.999 цирковируса свиней.
ДНК (1-5 мкг), экстрагированную с помощью метода Хирта, обрабатывали S1-нуклеазой (Amersham) в соответствии с рекомендациями поставщика, а затем эту ДНК расщепляли различными рестрикционными ферментами (Boehringer Mannheim, Lewes, East Sussex, UK) и продукты расщепления разделяли с помощью электрофореза в 1,5%-ном агарозном геле в присутствии бромида этидия, как описано Тоддом и др. (Purification and biochemical characterization of chicken anemia agent. J. Gen. Virol. 1990, 71, 819-823). ДНК, экстрагированная из культур штамма Imp.999, обладает уникальным сайтом EcoRI, двумя сайтами SacI и не имеет ни одного сайта PstI. Поэтому этот профиль рестрикции отличается от профиля рестрикции штамма PCV PK/15 (Meehan В. et al. Sequence of porcine circovirus DNA; affinities with plant circoviruses, 1997, 78; 221-227), который, наоборот, имеет сайт PstI и не имеет ни одного сайта EcoRI.
ПРИМЕР 9. Клонирование генома штамма Imp.999 цирковируса свиней.
Рестрикционный фрагмент величиной около 1,8 т.п.о., полученный при расщеплении двухцепочечной репликативной формы штамма PCV Imp.999 EcoRI, выделяли после разделения электрофорезом в 1,5%-ном агарозном геле (см. пример 3) с помощью коммерческого набора Qiagen (QIAEXII Gel Extraction Kit, Cat # 20021, QIAGEN Ltd., Crawley, West Sussex, UK). Фрагмент EcoRI-EcoRI затем лигировали с вектором pGEM-7 (Promega, Medical Supply Company, Dublin, Ireland), предварительно расщепленным тем же рестрикционным ферментом и дефосфорилированным в соответствии со стандартными методами клонирования (Sambrook J. et al., Molecular cloning: A laboratory Manual, 2nd Edition, Cold Spring Harbor laboratory, Cold Spring Harbor, New York, 1989). Полученными плазмидами трансформировали штамм Escherichia coli JM109 (Stratagene, La Jolla, USA) в соответствии со стандартными методами. Рестрикционный фрагмент EcoRI-EcoRI штамма PCV Imp.999 также клонировали в сайт EcoRI вектора pBlueScript SK+ (Stratagene Inc., La Jolla, USA). Среди клонов, полученных от каждого штамма, отобрали по меньшей мере 2 клона, содержащих фрагменты ожидаемого размера. Полученные клоны затем культивировали в малом объеме (2 мл) или в большом объеме (250 мл) и выделяли плазмиды, содержащие полный геном штамма Imp.999, в соответствии со стандартными методами получения и очистки плазмид.
ПРИМЕР 10. Секвенирование геномной ДНК (двухцепочечной репликативной формы) штамма PCV Imp.999.
Нуклеотидную последовательность двух клонов EcoRI (клоны pGEM-7/2 и pGEM-7/8) определяли дидеоксинуклеотидным методом Сангера (Sanger) с помощью набора для секвенирования "AmpliTaq DNA polymerase FS" (Cat # 402079 РЕ Applied Biosystems, Warrington, UK) и аппарата для автоматического секвенирования Applied Biosystems AB1373A в соответствии с рекомендациями поставщика. Первоначальные реакции секвенирования проводили с помощью «прямого» и «обратного» универсального праймеров М13. Последующие реакции секвенирования проводили в соответствии с методом «DNA-Walking». Олигонуклеотиды, необходимые для последующих секвенирований, были синтезированы компанией Life Technologies (Inchinnan Business Park, Paisley, UK).
Jghtltktyyst последовательности собирали и анализировали с помощью версии 3.2 компьютерной программы MacDNASIS (Cat. # 22020101, Appligene, Durham, UK). Различные открытые рамки считывания анализировали с помощью алгоритма BLAST, имеющегося на сервере Национального центра биотехнологической информации (NCBI, Bethesda, MD, USA).
Полная последовательность (фрагмент EcoRI-EcoRI), первоначально полученная из клона pGEM-7/8 (ПОСЛЕДОВ. №6), представлена на фиг.6. Она произвольно начинается после G сайта EcoRI и проявляет несколько неопределенностей с точки зрения нуклеотидов.
Затем секвенирование оптимизировали, и ПОСЛЕДОВ. № 3 (фиг.3) дает общую последовательность этого штамма, которая была получена таким образом, чтобы она произвольно начиналась от сайта EcoRI, т.е. G используется в качестве первого нуклеотида.
Подобным же образом получали последовательности других трех изолятов в соответствии с настоящим изобретением (см. ПОСЛЕДОВ. №№1, 2 и 4 и фиг.1, 2 и 4).
Величина генома этих четырех штаммов следующая:
ПРИМЕР 11. Анализ последовательности штамма PCV Imp.999.
Анализ гомологии последовательности, полученной из штамма Imp.999, по отношению к последовательностям, содержащимся в банке данных GenBank, показал, что единственной обнаруженной значимой гомологией оказалась примерно 76%-ная гомология (на уровне нуклеиновой кислоты) с последовательностью штамма РК/15 (коллекционные номера Y09921 и U49186) (см. фиг.5).
На аминокислотном уровне тест на гомологию при трансляции последовательностей в 6 фазах с банками данных (алгоритм BLAST X на сервере NCBI) позволил продемонстрировать 94%-ную гомологию с открытой рамкой считывания, соответствующей теоретической репликазе вируса BBTV, подобного цирковирусам растений (идентификационный номер банка данных GenBank - 1841515), кодируемым последовательностью U49186 из банка данных GenBank.
Никакие другие последовательности, имеющиеся в банках данных, не продемонстрировали значительной гомологии с последовательностью, полученной из штамма PCV Imp.999.
Анализ последовательностей, полученных из штамма Imp.999, культивированного из участков больных органов и тканей, взятых у калифорнийских поросят, имеющих клинические признаки многосистемного вастинг-синдрома, ясно показывает, что этот вирусный изолят представляет собой новый штамм цирковируса свиней.
ПРИМЕР 12. Сравнительный анализ последовательностей
Провели сопоставление нуклеотидных последовательностей четырех новых штаммов PCV с последовательностью штамма PCV PK/15 (фигура 5). Разработали матрицу гомологии, которая учитывает четыре новых штамма и предшествующий им штамм PK/15. Получили следующие результаты:
1: Imp.1011-48121
2: Imp.1011-48285
3: Imp.999
4: Imp.1010
5: РК/15
Гомология между двумя французскими штаммами Imp.1011-48121 и Imp.1011-48285 составляет более 99% (0,9977).
Гомология между двумя североамериканскими штаммами Imp.999 и Imp.1010 также выше 99% (0,9949). Гомология между французскими штаммами и североамериканскими штаммами немного выше 96%.
Гомология между всеми этими штаммами и РК/15 находится в интервале между 75 и 76%.
Из этого следует, что штаммы по настоящему изобретению являются представителями нового типа цирковируса свиней, отличного от типа, представленного штаммом РК/15. Этот новый тип, выделенный из свиней, проявляющий синдром PMWS, назвали цирковирусом свиней типа II, а РК/15 представляет собой тип I. Штаммы, принадлежащие к типу II, проявляют значительную гомогенность нуклеотидных последовательностей, хотя фактически их выделили из образцов, поступивших из очень отдаленных друг от друга географических регионов.
ПРИМЕР 13. Анализ белков, кодируемых геномом новых штаммов PCV.
Нуклеотидная последовательность изолята Imp.1010 признана представителем других штаммов цирковируса, связанных с многосистемным вастинг-синдромом. Эту последовательность проанализировали более подробно с помощью алгоритма BLASTX (Altschul et al., J. Mol. Biol., 1990, 215, 403-410) и с помощью комбинации программ из комплекта программного обеспечения MacVector 6,0 (Oxford Molecular Group, Oxford OХ4 4GA, UK). Ha этой последовательности (кольцевом геноме) удалось обнаружить 13 открытых рамок считывания (ORF) размером свыше 20 аминокислот. Это следующие 13 открытых рамок считывания:
Позиции начала и конца каждой ORF (открытой рамки считывания) относятся к последовательности, представленной на фиг.4 (ПОСЛЕДОВ. №4), генома штамма 1010. Границы ORF1 до ORF13 идентичны для штамма 999. Они идентичны также для штаммов 1011-48121 и 1011-48285 за исключением ORF3 и ORF13:
ORF3 1432-1539, смысловая, 108 nt, 35 аа
ORF13 314-1377, антисмысловая, 705 nt, 234 аа.
Из этих тринадцати ORF четыре имеют значительную гомологию с аналогичными ORF, расположенными на геноме клонированного вируса PCV РК-15. Проанализировали каждую из открытых рамок считывания, присутствующих на геноме всех изолятов цирковируса, связанного с многосистемным вастинг-синдромом. Эти четыре ORF следующие:
Позиции начала и конца каждой ORF относятся к последовательности, представленной на фиг.4 (ПОСЛЕДОВ. №4). Размер ORF (в нуклеотидах - нт) включает терминирующий кодон.
Сравнение организации геномов изолятов PCV Imp.1010 и PCV РК-15 позволило идентифицировать 4 рамки считывания, сохранившиеся в геномах двух вирусов. Следующая таблица показывает степень наблюдавшейся гомологии:
Самую большую идентичность последовательностей наблюдали между ORF4 Imp.1010 и ORF1 РК-15 (гомология 86%). Это было ожидаемым, поскольку этот белок, по-видимому, участвует в репликации вирусной ДНК и является существенным для репликации вирусов (Meehan et al., J. Gen. Virol., 1997, 78, 221-227); Mankertz et al., J. Gen. Virol., 1998, 79, 381-384).
Идентичность последовательностей между ORF13 Imp.1010 и ORF2 РК-15 меньше (гомология 66,4%), но каждая из этих двух ORF действительно демонстрирует хорошо сохранившуюся N-концевой базовую область, идентичную N-концевей области основного структурного белка цирковируса птиц CAV (Meehan et al., Arch. Virol., 1992, 124, 301-319). Кроме того, наблюдались большие различия между ORF7 Imp.1010 и ORF3 РК-15 и между ORF10 Imp.1010 и ORF4 РК-15. В каждом случае имеется делеция в С-концевой области ORF7 и ORF10 изолята Imp.1010, если их сравнивать с ORF3 и ORF4 штамма PCV РК-15. Наибольшую гомологию последовательностей наблюдали на уровне N-концевых областей ORF7/ORF3 (гомология 61,5% на уровне перекрывания) и ORF10/ORF4 (гомология 83% на уровне перекрывания).
Выяснилось, что геномная организация цирковируса свиней довольно сложная, как следствие чрезвычайной плотности его генома. Основной структурный белок, по-видимому, происходит в результате сплайсинга между несколькими рамками считывания, расположенными на одной и той же цепи генома цирковируса свиней. Поэтому можно считать, что любая открытая рамка считывания (от ORF1 до ORF13), описанная в вышеприведенной таблице, может представлять собой весь антигенный белок или часть этого белка, кодируемого цирковирусом свиней типа II, и поэтому потенциально является антигеном, который можно использовать для установления конкретного диагноза и/или для вакцинации. Поэтому изобретение касается любого белка, включающего по меньшей мере одну из этих открытых рамок считывания. Предпочтительно, изобретение касается белка, по существу состоящего из ORF4, ORF7, ORF10 или ORF13.
ПРИМЕР 14. Инфекционный характер генома PCV, клонированного из новых штаммов.
Плазмидой pGEM-7/8, содержащей полный геном (репликативную форму) изолята Imp.999, трансфецировали клетки РК/15 в соответствии с методом, описанным Meehan В. et al. (Characterization of viral DNAs from cells infected with chicken anemia agent: sequence analysis of the cloned replicative form and transfection capabilities of cloned genome fragments. Arch. Virol. 1992, 124, 301-319). Иммунофлуоресцентный анализ (см. пример 4), выполненный при первом пассаже после трансфецирования на неконтаминированных клетках РК/15, показал, что плазмида клона pGEM7/8 способна индуцировать продуцирование инфекционного вируса PCV. Наличие клона, содержащего инфекционный генетический материал PCV, позволяет осуществлять любые полезные манипуляции на вирусном геноме для того, чтобы продуцировать модифицированные вирусы PCV (либо ослабленные в свиньях, либо дефектные), которые можно использовать для выработки ослабленных или рекомбинантных вакцин или для продуцирования антигенов для диагностических наборов.
ПРИМЕР 15. Продуцирование антигенов PCV путем культивирования in vitro.
Культивирование неконтаминированных клеток РК/15 и размножение вирусов осуществляли теми же методами, которые описаны в примере 1. Инфецированные клетки собирали после трипсинизации, после 4 суток инкубации при 37°С и подсчитывали. Следующий пассаж инокулировали инфецированными клетками с концентрацией в 400000 инфецированных клеток на 1 мл.
ПРИМЕР 16 Инактивация вирусных антигенов
В конце культивирования с вирусами инфецированные клетки собирали и лизировали с помощью ультразвука (Branson Sonifer) или с помощью коллоидной мельницы роторно-статорного типа (UltraTurrax, IKA). Затем суспензию центрифугировали при 3700 g в течение 30 минут. Суспензию вирусов инактивировали 0,1%-ным этиленимином в течение 18 часов при +37°С или 0,5%-ным бета-пропиолактоном в течение 24 часов при +28°С. Если титр вирусов перед инактивацией был недостаточным, суспензию вирусов концентрировали путем ультрацентрифугирования, используя мембрану пропускающую соединения до 300 кДа (Millipore РТМК300). Инактивированную суспензию вирусов хранили при +5°С.
ПРИМЕР 17 Получение вакцины в форме эмульсии на основе минерального масла
Вакцину получали в соответствии со следующей формулой:
Водную фазу и масляную фазу стерилизовали по отдельности с помощью фильтрации. Эмульсию готовили путем смешивания и гомогенизации ингредиентов с помощью турбинного эмульгатора модели Silverson.
Одна доза вакцины содержит около 107,5 TCID50. Объем одной дозы вакцины составляет 0,5 мл для внутрикожного введения и 2 мл для внутримышечного введения.
ПРИМЕР 18 Получение вакцины в форме метаболизируемой эмульсии на основе масла
Вакцину получали в соответствии со следующей формулой:
Водную фазу и масляную фазу стерилизовали по отдельности с помощью фильтрации. Эмульсию готовили путем смешивания и гомогенизации ингредиентов с помощью турбинного эмульгатора модели Silverson.
Одна доза вакцины содержит около 107,5 TCID50. Объем одной дозы вакцины составляет 2 мл для внутримышечного введения.
ПРИМЕР 19 Результаты непрямого флуоресцентного анализа штаммов вируса PCV из США и Франции и РК/15 с гипериммунной сывороткой (PCV-T), с применением набора моноклональных антител F99, полученных из РК/15, и гипериммунной сывороткой, полученной из канадского штамма (PCV-C)















Изобретение относится к области ветеринарной вирусологии. Предложены 5 штаммов цирковируса свиней типа II (РСЧ II). Штаммы являются возбудителями послеотъемного мультисистемного синдрома истощения (PMWS) у свиней. Кроме того, предложены различные иммуногенные композиции и вакцины, основанные на этих штаммах, предназначенные для борьбы с PMWS. Также предложены векторы, вирусные препараты, клеточные экстракты, супернатанты клеточных культур, содержащие вирус PCV II или его нуклеотидные или белковые компоненты. Предложен также способ диагностики заражения РСЧ II, а также диагностическая композиция и диагностический набор для его осуществления. Изобретение может быть использовано в ветеринарии для борьбы с PMWS свиней. 37 н. и 141 з.п. ф-лы, 7 ил., 5 табл.
(a) последовательность, приведенную в SEQ ID No 1, 2, 3, 4 или 6, либо
(b) фрагмент, который кодирует полипептид или пептид, содержащий вирусспецифический эпитоп, причем указанный фрагмент (b) гибридизируется с последовательностью (а) в строгих условиях, при которых отсутствует гибридизация с геномной нуклеотидной последовательностью PCVI.
Приоритет по пунктам;
| ALLAN G.M | |||
| et all, «Production, premiminary characterisation and application of monoclonal antibodies to porcine circovirus», Vet Immunol Immunopathol, 1994 Nov; 43(4): 357-71 | |||
| US 6211431, 03.04.2001. |
Авторы
Даты
2006-09-20—Публикация
1998-10-01—Подача