Изобретение относится к области пищевой технологии, а именно к способам защиты липидов, масел, жиров от окисления и окислительной деструкции, и может быть использовано в пищевой, косметической и химико-фармацевтической промышленности для получения стабильных липидосодержащих пищевых добавок (нутрицевтиков), лечебно-косметических средств и лекарственных препаратов.
Для торможения процессов окисления применяют антиоксиданты (ингибиторы окисления), которые находят все более широкое применение для предотвращения окислительных превращений липидов и содержащих их препаратов in vitro, а также in vivo в комплексной терапии широкого круга заболеваний [Герчук М.П. Антиокислители в пищевой промышленности // Журн. Всесоюз. хим. общества им. Д.И. Менделеева. - 1960. - N 4. - С. 395-402; Авакумов В.М., Ковлер М.А., Кругликова-Львова Р.П. Лекарственные средства метаболической терапии на основе витаминов и ферментов (Обзор) // Вопросы мед. химии. - 1992. - Т. 38. - N 4. - С. 14-21; Дурнев А.Д., Середенин С.В. Антиоксиданты как средства защиты генетического аппарата //Хим.-фарм. журн. - 1990. - N 2. - С. 92-100.]. Таким образом, антиоксиданты, присутствующие в лекарственном или косметическом препарате, являются не только действующим началом этих средств, но могут значительно тормозить их окисление в процессе длительного хранения, способствуя сохранению в нативном состоянии легкоокисляемых биологически активных компонентов.
Рекомендуемые курсы назначения нутрицевтиков, пероральных лекарственных средств, липидных препаратов с антиоксидантами достаточно продолжительны (до 30 дней), что определяет особую тщательность в подборе ингибиторов окисления [Дегтярев И.А., Заиков Г.Е. Ионол. Распределение в организме и биологическое действие // Хим.-фарм. журн. - 1985. - N 10. - С. 1160-1168. Ленинжер А. Основы биохимии. - М. - Мир. - 1985. - Т.1. - 385 С.]. Во всем мире ведется целенаправленный скрининг (отбор) полифункциональных стабилизаторов, лекарств антиоксидантного действия.
Известен состав для стабилизации липидов, включающий природный фенольный антиоксидант (α-токоферол или α-токоферол ацетат) и L-карнитин, действующий как синергист по отношению к ингибитору окисления, при следующих соотношениях компонентов: α-токоферол или α-токоферол ацетат 75,0- 94,5 %; L-карнитин 5,5 - 25,0 %, добавляемых в концентрации 0,28 - 0,50% от массы липидов [Патент 2157829 RU, МПК7 С 11 В 5/00, опубликованный 20. 10. 2000 г.].
α-Токоферол (6-гидрокси-2,5,7,8-тетраметил-2-фитил-хроман) является наиболее изученным природным антиоксидантом. Свойства α-токоферола как антиоксиданта проявляются в целом ряде сложных эффектов на всех уровнях организации от мембранных образований до организма в целом. [Ленинжер А. Основы биохимии. - М. - Мир. - 1985. - T.1. - 385 С.].
Задачей предлагаемого изобретения является экономия использования дорогостоящих соединений, достижение ингибирующего эффекта меньшим количеством антиоксиданта.
Техническим результатом изобретения является упрощение состава и повышение его ингибирующего эффекта при наименьших концентрациях антиоксидантов.
Указанный технический результат достигается тем, что в составе для стабилизации липидов, включающем фенольный антиоксидант, особенностью является то, что в качестве фенольного антиоксиданта используют амид 1-(N-4'-гидроксифенилпропил-3',5'-дитри-трет-бутил)-5-этил салициловой кислоты, или амид 1-(N-4'-гидроксифенилпропил-3,3',5'-три-трет-бутил)-5-этил салициловой кислоты, или сульфид 1-(N-4'-гидроксифенилпропил-3,3',5'-три-трет-бутил)-5-этил салициловой кислоты в следующих концентрациях: от 0,10 до 5,00 мМ, добавляемых в количестве 0,01-0,68% от массы липидов.
Предлагаемые соединения обладают сравнимой антиоксидантной активностью, имеют близкое химическое строение и могут быть взаимозаменяемыми.
Предлагаемые в качестве фенольного антиоксиданта соединения были синтезированы в Новосибирском Институте органической химии им. Н.Н.Ворожцова СО РАН с целью расширения ассортимента нетоксичных биологически активных ингибиторов окисления. Производные салициловой кислоты представляют собой стерически затрудненные фенолы: амид 1-N-4'-гидроксифенилпропил-3',5'-дитри-трет-бутил)-5-этил салициловой кислоты, или амид 1-(N-4'-гидроксифенилпропил-3,3',5'-три-трет-бутил)-5-этил салициловой кислоты, или сульфид 1-(N-4'-гидроксифенилпропил-3,3',5'-три-трет-бутил)-5-этил салициловой кислоты. Установлено, что соединения не обладают местным и общетоксическим действием [Перевозкина М.Г. Кинетика и механизм ингибирующего действия производных фенозана, салициловой кислоты и их синергических смесей с α-токоферолом и фосфолипидами. Автореф. дис... канд. хим. наук. Тюмень.: Тюменский государственный нефтегазовый университет, 2003. С.28]. Эффективность стабилизаторов оценивалась несколькими независимыми методами [Сторожок Н.М. Межмолекулярные взаимодействия компонентов природных липидов в процессе окисления. Дис.... д-ра хим. наук. М.: Институт биохимической физики им. Н.М. Эмануэля РАН, 1996. С. 360; Цепалов В.Ф., Харитонова А.А., Гладышев Г.П. и др. Определение констант скорости и коэффициентов ингибирования фенолов-антиоксидантов с помощью модельной цепной реакции // Кинетика и катализ. - 1977. - Т.18.- вып.5. - С.1261-1267]:
- изучалась кинетика поглощения кислорода при инициированном окислении липидных субстратов различного происхождения в присутствии предлагаемого состава и прототипа;
- тестировалась кинетика накопления первичных продуктов окисления - гидропероксидов методом йодометрического титрования (ПЧ) при аутоокислении липидов при повышенных температурах (60±0,2°С)
Изучение кинетики поглощения кислорода проводилось манометрическим методом в установках типа Варбурга при инициированном окислении липидов в присутствии инициатора азобисизобутиронитрила (АИБН) в концентрации 3 мМ при температуре 60±0,5° С. Контролем служили образцы липидов без добавок антиоксидантов.
В качестве субстратов окисления использовали как природные липиды (сиговых рыб) и метиловые эфиры олеиновой кислоты (метилолеат). Опытная серия рыбных липидов была наработана на Салехардском рыбоконсервном заводе по методу [Сторожок Н.М., Кутузова И.В. Состав для стабилизации липидов. Патент 2077552, Россия, опубл. в БИ № 11.- 1997 г.]. Изучение жирнокислотного состава липидов позволило установить присутствие значительного количества полиненасыщенных жирных кислот (до 37%), в том числе пента- и гексаенов до 12 и 2% соответственно [Ушкалова В.Н., Артамонова Н.А., Сторожок Н.М., Горяев М.И. Жирнокислотный состав общих и нейтральных липидов сиговых Обского бассейна// Химия природ. соединен. - 1981. - № 5. - С. 555-558].
Эффективность индивидуальных компонентов и их комбинаций исследовалась в широком диапазоне концентраций и соотношений компонентов:
В присутствии определенной добавки индивидуальных ингибиторов окисления α-токоферола, амида 1-(N-4′-гидроксифенилпропил-3',5'-дитри-трет-бутил)-5-этил салициловой кислоты, или амида 1-(N-4′-гидроксифенилпропил-3,3',5'-три-трет-бутил)-5-этил салициловой кислоты, или сульфида 1-(N-4′-гидроксифенилпропил-3,3',5'-три-трет-бутил)-5-этил салициловой кислоты, а также прототипа записывалась кинетика окисления с использованием вышеописанных методов. На основании полученных данных строились кинетические кривые поглощения кислорода (мм3 О2) либо накопления пероксидов (г I2 /100 г липида).
Из кинетических кривых определялись периоды индукции (τ ), за которые принимали:
время (мин), за которое процесс инициированного окисления липидов достигал максимальной скорости (τинд );
время (час) накопления пероксидов, количественно соответствующих значению ПЧ 0,1 % I2.
Ингибирующее действие индивидуальных компонентов и их смесей оценивали по абсолютному значению разницы между периодами индукции окисления субстратов с индивидуальным антиоксидантом (τАО), смесью стабилизирующих добавок (τинг.) и без них (τо) по формуле:
ε = Δτ =τинг.- τАО,
либо выражали ее в относительных единицах Δτ / τАО, %.
Критерием антиоксидантного действия служили начальная (W o2 нач ×10-7, M×c-1) и максимальная (W o2 max ×10-7, M×c-1) скорости процесса окисления в присутствии и в отсутствие антиоксиданта. Эффективность стабилизации окисления определяли также по величине W о2max (МО) / W о2max (МО+АО), количественно характеризующей степень уменьшения скорости поглощения кислорода в присутствии метилолеата (МО) и метилолеата с добавками индивидуальных антиоксидантов (АО).
Было установлено, что зависимость изменения периодов индукции для индивидуального α-токоферола носит экстремальный характер. Диапазон эффективных концентраций расположен в области (0,25 - 8,0) мМ, что соответствует (0,03 - 1,08) % от массы липидов, максимум указанной зависимости определялся при концентрации 2,5мМ (0,34% от массы липидов). Зависимости изменения величины периодов индукции от концентрации амида 1-(N-4'-гидроксифенилпропил-3',5'-дитри-трет-бутил)-5-этил салициловой кислоты, или амида 1-(N-4'-гидроксифенилпропил-3,3',5'-три-трет-бутил)-5-этил салициловой кислоты, или сульфида 1-(N-4'-гидроксифенилпропил-3,3',5'-три-трет-бутил)-5-этил салициловой кислоты в системе окисления носили линейный характер, указанные соединения превосходили по своему ингибирующему действию смесь α-токоферола с L-карнитином.
Сущность изобретения иллюстрируется следующими примерами:
ПРИМЕР 1
Берут 10 г (точная навеска) эфиров ненасыщенных высших жирных кислот, например метилолеата или метиллинолеата, и добавляют 0,0078 г (0,6 мМ) амида 1-(N-4'-гидроксифенилпропил-3',5'-дитри-трет-бутил)-5-этил салициловой кислоты, или амида 1-(N-4'-гидроксифенилпропил-3,3',5'-три-трет-бутил)-5-этил салициловой кислоты, или сульфида 1-(N-4'-гидроксифенилпропил-3,3',5'-три-трет-бутил)-5-этил салициловой кислоты, что составляет соответственно 0,08% от массы липидов.
ПРИМЕР 2
Берут 10 г (точная навеска) эфиров ненасыщенных высших жирных кислот, например метилолеата или метиллинолеата. Добавляют 0,0049 г (0,4 мМ) амида 1-(N-4'-гидроксифенилпропил-3',5'-дитри-трет-бутил)-5-этил салициловой кислоты, или амида 1-(N-4'-гидроксифенилпропил-3,3',5'-три-трет-бутил)-5-этил салициловой кислоты, или сульфида 1-(N-4'-гидроксифенилпропил-3,3',5'-три-трет-бутил)-5-этил салициловой кислоты, что составляет соответственно 0,05% от массы липидов.
ПРИМЕР 3
Берут 10 г (точная навеска) рыбных липидов, например липидов сиговых рыб. Добавляют 0,0108 г (0,8 мМ) амида 1-(N-4'-гидроксифенилпропил-3',5'-дитри-трет-бутил)-5-этил салициловой кислоты, или амида 1-(N-4'-гидроксифенилпропил-3,3',5'-три-трет-бутил)-5-этил салициловой кислоты, или сульфида 1-(N-4'-гидроксифенилпропил-3,3',5'-три-трет-бутил)-5-этил салициловой кислоты, что составляет 0,11% от массы липидов.
ПРИМЕР 4
Берут 10 г (точная навеска) эфиров ненасыщенных высших жирных кислот, например метилолеата или метиллинолеата, и добавляют 0,0027 г (0,2 мМ) амида 1-(N-4'-гидроксифенилпропил-3',5'-дитри-трет-бутил)-5-этил салициловой кислоты, или амида 1-(N-4'-гидроксифенилпропил-3,3',5'-три-трет-бутил)-5-этил салициловой кислоты, или сульфида 1-(N-4'-гидроксифенилпропил-3,3',5'-три-трет-бутил)-5-этил салициловой кислоты, что составляет соответственно 0,03% от массы липидов.
ПРИМЕР 5
Берут 10 г (точная навеска) эфиров ненасыщенных высших жирных кислот, например метилолеата или метиллинолеата, и добавляют 0,0338 г (2,5 мМ) амида 1-(N-4'-гидроксифенилпропил-3',5'-дитри-трет-бутил)-5-этил салициловой кислоты, или амида 1-(N-4'-гидроксифенилпропил-3,3',5'-три-трет-бутил)-5-этил салициловой кислоты, или сульфида 1-(N-4'-гидроксифенилпропил-3,3',5'-три-трет-бутил)-5-этил салициловой кислоты, что составляет соответственно 0,34% от массы липидов.
ПРИМЕР 6
Берут 10 г (точная навеска) эфиров ненасыщенных высших жирных кислот, например метилолеата или метиллинолеата, и добавляют 0,0676 г (5 мМ) амида 1-(N-4'-гидроксифенилпропил-3',5'-дитри-трет-бутил)-5-этил салициловой кислоты, или амида 1-(N-4'-гидроксифенилпропил-3,3',5'-три-трет-бутил)-5-этил салициловой кислоты, или сульфида 1-(N-4'-гидроксифенилпропил-3,3',5'-три-трет-бутил)-5-этил салициловой кислоты, что составляет соответственно 0,68% от массы липидов.
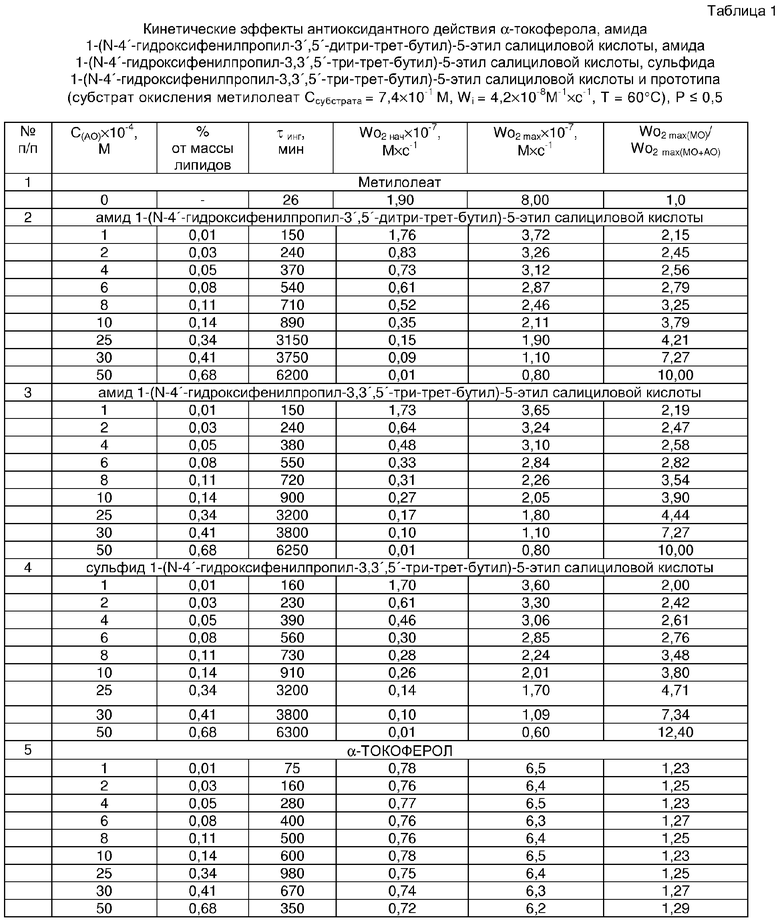
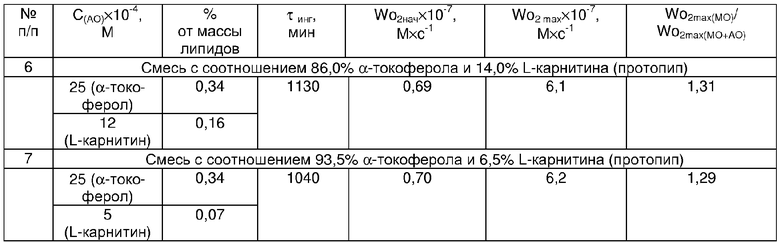
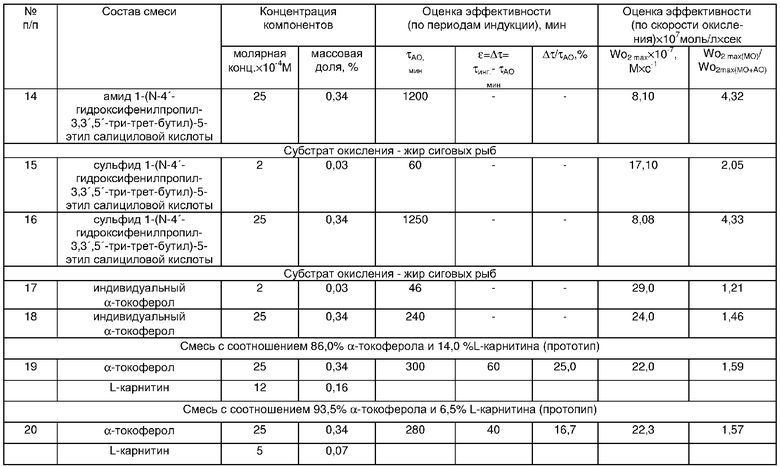
Эффективность ингибирующего действия указанных выше соединений оценивали на основании данных кинетики поглощения кислорода, получаемых с использованием манометрического метода, подробно изложенного в описании изобретения. Полученные результаты приведены в табл.1. Из данных табл.1 видно, что все рекомендуемые концентрации ингибиторов окисления превосходят по величине эффективности прототип. Наибольшую эффективность по сравнению с прототипом проявляет амид 1-(N-4'-гидроксифенилпропил-3',5'-дитри-трет-бутил)-5-этил салициловой кислоты, или амид 1-(N-4'-гидроксифенилпропил-3,3',5'-три-трет-бутил)-5-этил салициловой кислоты, или сульфид 1-(N-4'-гидроксифенилпропил-3,3',5'-три-трет-бутил)-5-этил салициловой кислоты, в концентрации 5 мМ, что составляет 0,68% от массы липидов. Так, при окислении метилолеата в присутствии амида 1-(N-4′-гидроксифенилпропил-3',5'-дитри-трет-бутил)-5-этил салициловой кислоты, или амида 1-(N-4′-гидроксифенилпропил-3,3',5'-три-трет-бутил)-5-этил салициловой кислоты, или сульфида 1-(N-4′-гидроксифенилпропил-3,3',5'-три-трет-бутил)-5-этил салициловой кислоты, максимально достигаемый ингибирующий эффект составляет 6200, 6250 и 6300 мин соответственно, тогда как смесь α-токоферола с L-карнитином (включающая 86,0% α-токоферола и 14,0% L-карнитина) обеспечивает максимальный индукционный период в 1130 мин, при этом эффективность предлагаемой смеси выше эффективности прототипа на 449-458%.
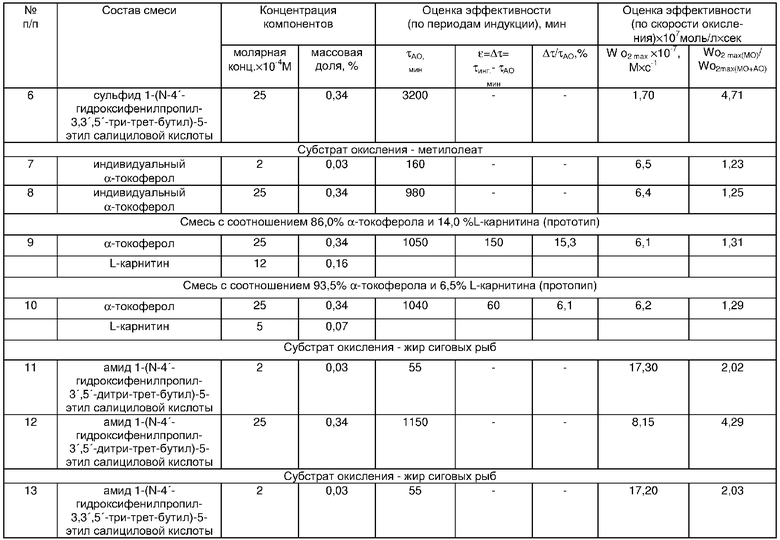
Высокоэффективной является концентрация, приведенная в примере 5, соизмеримая с концентрацией α-токоферола в прототипе. При ингибировании окисления с добавками 2,5 мМ амида 1-(N-4′-гидроксифенилпропил-3',5'-дитри-трет-бутил)-5-этил салициловой кислоты, или амида 1-(N-4′-гидроксифенилпропил-3,3',5'-три-трет-бутил)-5-этил салициловой кислоты, или сульфида 1-(N-4′-гидроксифенилпропил-3,3',5'-три-трет-бутил)-5-этил салициловой кислоты рыбных липидов индукционные периоды составили 1150, 1200 и 1250 мин соответственно. Следовательно, эффективной для метилолеата, а также рыбных липидов оказалась концентрация антиоксидантов 2,5 мМ, что составляет 0,34% от массы липидов
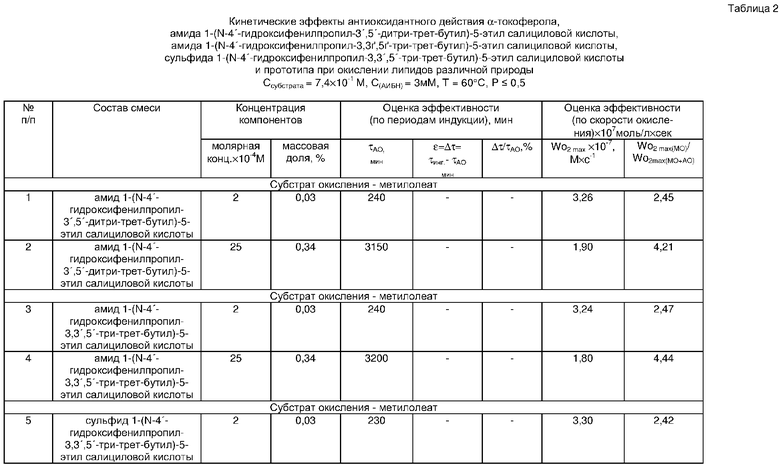
Эффективность указанной выше концентрации в идентичных условиях окисления была сопоставлена с периодами индукции опыта-контроля (неингибированных липидов) и антиоксидантным действием прототипа (табл. 1, 2).
Было установлено, что эффективность использования новых антиоксидантов в разных субстратах составляет от (174-185)% по сравнению со смесью α-токоферола с L-карнитином (прототип) (табл. 1).
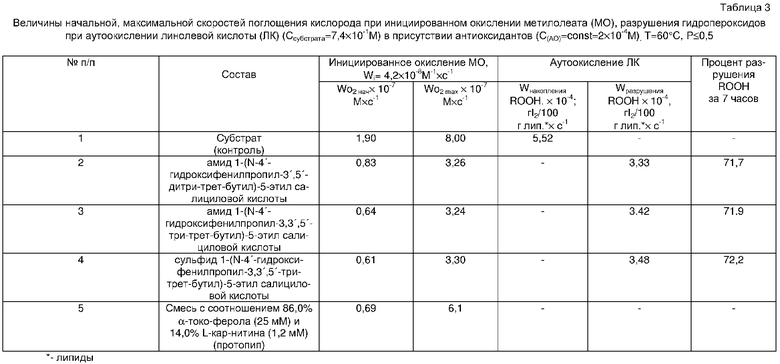
При изучении кинетики накопления гидропероксидов было показано, что в опытах с концентрацией амида 1-(N-4′-гидроксифенилпропил-3',5'-дитри-трет-бутил)-5-этил салициловой кислоты, или амида 1-(N-4′-гидроксифенилпропил-3,3',5'-три-трет-бутил)-5-этил салициловой кислоты, или сульфида 1-(N-4′-гидроксифенилпропил-3,3',5'-три-трет-бутил)-5-этил салициловой кислоты 0,2 мМ, добавляемой в количестве 0,03% от массы липидов, процент разрушения гидропероксидов составляет 70-73%, что не наблюдается в присутствии прототипа (табл. 3).
Из сравнения ингибирующего действия исследуемых концентраций видно, что абсолютная величина периодов индукции наиболее эффективной концентрации амида 1-(N-4′-гидроксифенилпропил-3',5'-дитри-трет-бутил)-5-этил салициловой кислоты, или амида 1-(N-4′-гидроксифенилпропил-3,3',5'-три-трет-бутил)-5-этил салициловой кислоты, или сульфида 1-(N-4′-гидроксифенилпропил-3,3',5'-три-трет-бутил)-5-этил салициловой кислоты, добавляемых в количестве 0,34% от массы липидов, выше при окислении метилолеата (3100, 3150 и 3200 мин соответственно), чем при окислении рыбных липидов (1150, 1200 и 1250 мин соответственно). Эти данные объясняются более высокой степенью ненасыщенности входящих в состав рыбных липидов высших жирных кислот [Ушкалова В.Н., Артамонова Н.А., Сторожок Н.М., Горяев М.И. Жирнокислотный состав общих и нейтральных липидов сиговых Обского бассейна// Химия природ. соединен. - 1981. - № 5. - С. 555-558.], следовательно, и более высокой их окисляемостью. Введение рекомендуемой концентрации исследуемых соединений воссоздает антиоксидантную систему и обеспечивает эффективную защиту липидов от окисления. Более высокая ингибирующая способность указанной выше смеси по сравнению с прототипом была доказана несколькими независимыми методами (обсуждаемыми выше) (табл. 1,2,3). Установлен наиболее эффективный диапазон концентраций антиоксидантов от 0,10 до 5,00 мМ, ниже концентрации 0,10 мМ антиоксидант малоэффективен (период индукции составляет 30-40 мин), свыше концентрации 5 мМ эффективность снижается из-за предела растворимости соединений в субстрате окисления.
Причинно-следственная связь между существенными признаками изобретения и достижением технического результата следующая. Эффекты ингибирования амида 1-(N-4′-гидроксифенилпропил-3',5'-дитри-трет-бутил)-5-этил салициловой кислоты, или амида 1-(N-4′-гидроксифенилпропил-3,3',5'-три-трет-бутил)-5-этил салициловой кислоты, или сульфида 1-(N-4′-гидроксифенилпропил-3,3',5'-три-трет-бутил)-5-этил салициловой кислоты могут быть объяснены исходя из представлений о механизме антиоксидантного действия используемых соединений. Установлено, что антиоксиданты воздействуют на сложный многостадийный процесс окисления по различным механизмам.
Так, в соответствии с литературными данными α-токоферол проявляет чрезвычайно высокую активность в реакции с пероксидными радикалами (RO2 •), ведущими окисление. Константа скорости реакции α-токоферола с RO2 • (реакции 7 согласно классической схемы) составляет 3,60×106 М-1×с-1, что превышает значение К7 для всех изученных природных и синтетических антиоксидантов [Сторожок Н.М., Храпова Н.Г., Бурлакова Е.Б. Исследование межмолекулярных взаимодействий компонентов природных липидов в процессе окисления // Химическая кинетика. - 1995. - т. 14. - № 11. - с.29-46; Бурлакова Е.Б., Крашаков С.А., Храпова Н.Г. Роль токоферола в пероксидном окислении липидов биомембран // Биологические мембраны. - 1998. - т.15. - № 2. - с.137-168.].
Таким образом, амид 1-(N-4′-гидроксифенилпропил-3',5'-дитри-трет-бутил)-5-этил салициловой кислоты, или амид 1-(N-4′-гидроксифенилпропил-3,3',5'-три-трет-бутил)-5-этил салициловой кислоты, или сульфид 1-(N-4′-гидроксифенилпропил-3,3',5'-три-трет-бутил)-5-этил салициловой кислоты проявляют активность в реакции с пероксидными радикалами с константой скорости реакции К7 =0,52×104 М-1×с-1, К7 =0,85×104 М-1×с-1 и К7 =0,74×104 М-1×с-1 соответственно, снижают скорость процесса окисления липидов в 2-10 раз, а также дополнительно снижают уровень гидропероксидов, образующихся в процессе окисления липидов, на 70-73 % (табл.3). Разрушение гидропероксидов под влиянием изучаемых соединений, в свою очередь, является причиной выигрыша в периодах индукции и обеспечения высокой эффективности.
Предлагаемый состав, включающий амид 1-(N-4′-гидроксифенилпропил-3',5'-дитри-трет-бутил)-5-этил салициловой кислоты, или амид 1-(N-4′-гидроксифенилпропил-3,3',5'-три-трет-бутил)-5-этил салициловой кислоты, или сульфид 1-(N-4′-гидроксифенилпропил-3,3',5'-три-трет-бутил)-5-этил салициловой кислоты значительно достигает эффекта ингибирования по сравнению с прототипом. Сочетание в одной композиции антиоксиданта, действующего на разные элементарные реакции сложного окислительного процесса, позволяет увеличить ингибирующую способность антиоксиданта и эффективно тормозить окисление полиненасыщенных субстратов.
| название | год | авторы | номер документа |
|---|---|---|---|
| СОСТАВ ДЛЯ СТАБИЛИЗАЦИИ ЛИПИДОВ | 2006 |
|
RU2308477C1 |
| СОСТАВ ДЛЯ СТАБИЛИЗАЦИИ ЛИПИДОВ | 2006 |
|
RU2308479C1 |
| СОСТАВ ДЛЯ СТАБИЛИЗАЦИИ ЛИПИДОВ | 2006 |
|
RU2315088C1 |
| СОСТАВ ДЛЯ СТАБИЛИЗАЦИИ ЛИПИДОВ | 2006 |
|
RU2308478C1 |
| СОСТАВ ДЛЯ СТАБИЛИЗАЦИИ ЛИПИДОВ | 2005 |
|
RU2284348C1 |
| СОСТАВ ДЛЯ СТАБИЛИЗАЦИИ ЛИПИДОВ К ОКИСЛЕНИЮ | 2013 |
|
RU2545651C1 |
| СОСТАВ ДЛЯ СТАБИЛИЗАЦИИ ЛИПИДОВ | 2005 |
|
RU2284349C1 |
| СОСТАВ ДЛЯ СТАБИЛИЗАЦИИ ЛИПИДОВ | 2005 |
|
RU2294958C1 |
| СОСТАВ ДЛЯ СТАБИЛИЗАЦИИ ЛИПИДОВ | 2005 |
|
RU2288258C1 |
| СОСТАВ ДЛЯ СТАБИЛИЗАЦИИ ЛИПИДОВ К ОКИСЛЕНИЮ | 2013 |
|
RU2546225C1 |
Изобретение относится к масложировой промышленности, а именно к способам защиты липидов, масел и жиров от окисления. Состав включает в себя фенольный антиоксидант. При этом в качестве фенольного антиоксиданта используют амид 1-(N-4'-гидроксифенилпропил-3',5'-дитри-трет-бутил)-5-этил салициловой кислоты, или амид 1-(N-4'-гидроксифенилпропил-3,3',5'-три-трет-бутил)-5-этил салициловой кислоты, или сульфид 1-(N-4'-гидроксифенилпропил-3,3',5'-три-трет-бутил)-5-этил салициловой кислоты, в концентрациях от 0,10 до 5,00 мМ. Заявленный состав добавляют в количестве 0,01-0,68% от массы липидов. Изобретение позволяет снизить скорость процесса окисления липидов в 2-10 раз, а также снизить уровень гидропероксидов, образующихся в процессе окисления липидов, на 70-73%. 3 табл.
Состав для стабилизации липидов, включающий фенольный антиоксидант, отличающийся тем, что в качестве фенольного антиоксиданта используют амид 1-(N-4'-гидроксифенилпропил-3',5' -дитри-трет-бутил)-5-этил салициловой кислоты, или амид 1-(N-4'-гидроксифенилпропил-3,3',5'-три-трет-бутил)-5-этил салициловой кислоты, или сульфид 1-(N-4'-гидроксифенилпропил-3,3',5'-три-трет-бутил)-5-этил салициловой кислоты в концентрациях от 0,10 до 5,00 мМ, добавляемый в количестве 0,01-0,68% от массы липидов.
| СОСТАВ ДЛЯ СТАБИЛИЗАЦИИ ЛИПИДОВ | 1999 |
|
RU2157829C1 |
| СОСТАВ ДЛЯ СТАБИЛИЗАЦИИ ЛИПИДОВ | 2000 |
|
RU2181757C2 |
| ЭМАНУЭЛЬ Н.М., ЛЯСКОВСКАЯ Ю.Н | |||
| «Торможение процессов окисления жиров», М., Пищепромиздат, 1961, стр.236-282. | |||
Авторы
Даты
2006-11-27—Публикация
2005-03-28—Подача