Предлагаемое изобретение относится к офтальмологии и предназначено для лечения и профилактики сосудистых и дистрофических заболеваний глазного дна (диабетическая ретинопатия, высокая осложненная миопия, центральная хориоретинальная дистрофия, посттромботическая ретинопатия, порафофеолярные субретинальные неоваскулярные мембраны) без экссудативно-геморрагического процесса.
Хорошо известны терапевтические, хирургические и энергетические методы лечения вышеперечисленных видов офтальмопатологии, направленные на улучшение микроциркуляции и транскапиллярного обмена. Однако достичь стойкого и высокого терапевтического эффекта зачастую не удается (Лысенко B.C. Геморрагический синдром при сосудистых заболеваниях сетчатки. - Дис......д.м.н. М., 2003).
Наше внимание в проблеме сосудистых и дистрофических заболеваний внутренних оболочек глаза привлек обмен нуклеозидов, мононуклеотид-монофосфатов, ди- и трифосфатов, динуклеотидов. Указанные вещества являются мощными источниками энергии, служат строительными блоками для РНК (рибонуклеиновых кислот) и необходимы для нормального течения репаративных процессов и предупреждения развития дистрофических процессов (Л.Страйер. Биохимия, М., 1985, т.2, с.255-278, Кольман Я., Рем К.Г. Наглядная биохимия, М., 2004, с.86-87).
Очевидно, что процесс дистрофии как таковой связан с нарушением энергетического баланса клеток, вовлеченных в этот процесс. Касаясь энергетического баланса клетки, известно, что регуляция метаболизма направлена, в частности, на поддержание энергетического заряда в сравнительно узких пределах. Энергетический заряд клетки, так же, как рН клетки, забуферен. Его значение в большинстве клеток находится в диапазоне 0,80-0,95 (Л.Страйер. Биохимия, М., 1985, т.2, с.19). Доказано, что при нормальном зрительном восприятии фоторецепторные клетки преобразуют энергию света в нервный импульс. Электрические сигналы, генерированные фоторецепторными клетками, преобразуются, проходя по сложной сети нервных клеток в сетчатке, и затем передаются в мозг по волокнам зрительного нерва. Однако следует иметь в виду, что нормальное состояние зрительных функций обеспечивается, прежде всего, тем, что в фоторецепторных клетках сетчатки с очень высокой скоростью вырабатывается АТФ, и идет активный синтез белков (Л.Стайер. Биохимия, М., 1985, т.3, с.340). Очевидно, что при развитии сосудистых и дистрофических процессов во внутренних оболочках глаза энергетический баланс и синтез белков в фоторецепторных клетках снижен, что приводит к снижению зрительных функций. В связи с этим возникает вопрос о том, имеется ли существенная разница в крови у здоровых и больных с сосудистыми и дистрофическими заболеваниями глазного дна концентрации тех веществ, например нуклеозидов, мононуклеотид-монофосфатов, ди- и трифосфатов, динуклеотидов, от которых в определяющей степени зависят энергетические и синтетические процессы в клетке.
Предпринятые нами исследования показали, что масс-спектральный анализ плазмы крови у здоровых лиц и больных с вышеуказанной офтальмопатологией не выявил сколь-нибудь значимых изменений в уровне нуклеозидов, мононуклеотид-монофосфатов, ди- и трифосфатов, динуклеотидов. Эти результаты позволяют предположить, что для ликвидации существующего дистрофического очага(ов) и предупреждения прогрессирования дистрофического процесса необходимо восстановление энергетического заряда каждой клетки, входящей в дистрофический очаг. Для этого, как нам представляется, необходим более высокий уровень в плазме крови больных определенного комплекса веществ, обеспечивающих как многочисленные энергетические, так и синтетические процессы в клетке. Очевидно, что нормальный уровень вышеуказанных веществ (как показали наши исследования) обеспечивает у здоровых людей поддержание нормального энергетического заряда и трофики здоровых клеток и недостаточен для восстановления клеток со сниженной трофикой и сниженным энергетическим зарядом. Понятно, что при офтальмопатологии, связанной с нарушением сосудистого - дистрофического процесса имеют место процессы нарушения трофики. В связи с этим была поставлена задача разработать способ лечения, позволяющий существенно повысить зрительные функции у больных с нарушенной трофикой внутренних оболочек глаза. Для реализации поставленной задачи было необходимо убедиться в правильности выдвинутой нами гипотезы о том, что при кратковременном лишении зрительной информации (помещение испытуемого в темноту) организм впадает в своего рода стресс, проявляющийся в готовности к выполнению любой физической деятельности и компенсации, в какой-то степени, зрительной информации слуховой и тактильной чувствительностью с пониженным порогом восприятия. Такое состояние организма может быть обеспечено, по нашему мнению, наличием в крови повышенной концентрации легкоподвижных, равномерно распределенных по всему организму, низкомолекулярных веществ, обладающих высоким энергетическим, пластическим и синтетическим потенциалом, имеющихся в организме всегда в достаточном запасе, т.е. не нуждающихся в синтезе de novo (с начала) и, в зависимости от ситуации, легко трансформирующихся друг в друга. Известно, что перечисленными свойствами обладают нуклеозиды и нуклеотиды (Jan Koolman, Klaus-Heinrich Rohm. Taschenatlas der Biocheme. Stuttgart - New York, 1998; Кольман Я., Рем К.Г. Наглядная биохимия, М., 2004, с.44-45, с.86-87, с.188-191; Л.Страйер. Биохимия, М., 1985, т.2, с.255-279). Однако до настоящего времени отсутствуют лечебные препараты, представляющие собой сложный нуклеозидный комплекс, обеспечивающий повышение энергетических, пластических и синтетических процессов в клетке, в частности, сетчатке. В связи с этим мы пошли по пути активизации процессов в организме, обеспечивающих повышение концентрации названной группы веществ. Согласно современным представлениям о механизме зрительного восприятия в темноте лежат особенности работы сигнального каскада - в темноте накапливается циклический гуанозинмонофосфат (цГМФ) с высокой концентрацией, которая способствует тому, что цГМФ зависимые каналы плазматической мембраны остаются открытыми и катионы Na и Са беспрепятственно поступают в клетку. При этом зрительная клетка постоянно выбрасывает нейромедиатор глутамат в синаптическую щель. Для работы катионного насоса требуется большая концентрация АТФ. За счет указанного механизма обеспечивается минимальное зрение при неблагоприятной освещенности. На свету уровень цГМФ резко падает за счет активации фосфодиэстеразы, что приводит к закрытию ионных каналов, и зрительная система пациента возвращается в состояние, которое он имел до наступления темноты. Причем этот переход осуществляется в течение нескольких миллисекунд.
Известно, что нуклеотиды принадлежат к наиболее сложным метаболитам. Их биосинтез требует много времени и высоких затрат энергии. Поэтому понятно, что нуклеотиды не полностью разрушаются, а по большей части снова участвуют в синтезе. Прежде всего это относится к пуриновым основаниям и гуанину. В организме высших животных 90% пуриновых оснований снова превращаются в нуклеозидмонофосфаты.
В настоящее время науке не известно, что происходит в крови бодрствующего организма, когда он внезапно лишается информации зрительного анализатора в условиях темноты. Естественно предположить, что центральная нервная система, лишившись информационного влияния зрительного анализатора, например, при передвижении в темноте, впадает в ожидание изменения скорости биохимических реакций. Известно, что скорость реакций зависит от энергии активации и изменения концентрации реагентов. Можно предположить, что в этой ситуации «фактор темноты» может реализоваться по принципу сигнального каскада и одновременного и равномерного распределения во всех частях кровеносного русла мобильных (низкомолекулярных) веществ, обеспечивающих высокий энергетический и пластический потенциал, необходимый в экстремальных условиях темноты. В клиническом эксперименте на здоровых волонтерах было показано, что при нахождении их в темноте в течение 45 минут с открытыми глазами в плазме крови в 2-5 раз повышался исходный уровень нуклеозидов (гуанозина, цитидина, тимидина), мононуклеотид-монофосфатов, ди- и трифосфатов. У больных с сосудистыми и дистрофическими заболеваниями глазного дна, помещенных в аналогичные условия, в плазме крови также повышались вышеуказанные вещества в 2-5 раза, сравнительно с исходным уровнем, если исходная острота зрения была не ниже 0,2. При остроте зрения ниже 0,2 повышение концентрации нуклеозидов и других вышеуказанных веществ не происходило. Характерно также, что повышение биологически активных веществ было напрямую связано и с условиями забора крови - так, после нахождения испытуемых в условиях темновой адаптации (темноты) и взятии крови в условиях обычной освещенности процедурного кабинета и со светонепроницаемой повязкой на обоих глазах обеспечивало повышение вышеуказанных уровней нуклеозидов и других вышеуказанных биологически активных веществ. Кровь, взятая при произвольно открытых глазах пациента и при обычной освещенности, по указанным параметрам не отличалась от исходного уровня.
Техническим результатом предлагаемого изобретения является эффективное повышение зрительных функций у больных с сосудистыми и дистрофическими заболеваниями глазного дна.
Технический результат достигается за счет внутривенного введения аутокрови с повышенным содержанием нуклеозидов, мононуклеотид-монофосфатов, ди- и трифосфатов, динуклеотидов.
Нами была разработана технология получения аутокрови с повышенным содержанием нуклеозидов, мононуклеотид-монофосфатов, ди- и трифосфатов, динуклеотидов. Она состоит в следующем.
Субъекта помещают на 45 минут в темное помещение со светонепроницаемыми жалюзи и дверями. В течение указанного времени испытуемый находится с открытыми глазами. Затем кровь в количестве 60,0 мл забирают гепаринизированным шприцем в условиях темноты, после чего через 20 минут пациенту в условиях обычной освещенности вводят внутривенно эту аутокровь. Ранее, в предварительных исследованиях, выполненных нами, с помощью высокочувствительного инструментального метода масс-спектры образцов плазмы крови (для определения содержания в них нуклеозидов и других биологически активных веществ) снимали на приборе VISION 2000 THERMO BIOANALYSIS CORP (Англия) с времяпролетным детектором по методике матрично-активированной лазерной десорбции/ионизации. (МАЛДИ). Прибор имеет азотистый лазер с длинной волны луча 337 нм с частотой импульса 3 нс и максимальной энергией импульса 250 кДж. Пробу плазмы крови объемом 50 мкл помещали в пластиковую пробирку, приливали 50 мкл смеси растворителей вода/метанол (1:1) и тщательно перемешивали, осадок отделяли центрифугированием и 0,2 мкл надосадочной жидкости наносили на предварительно нанесенные на мишень 0,2 мкл матрицы - 2,5-дигидроксибензойной кислоты. Пятна высушивали при комнатной температуре и мишень после высушивания пятен помещали в источник ионизации. Высокочувствительный метод масс-спектра МАЛДИ позволяет определить молекулярные веса компонентов плазмы крови и оценить их относительное содержание по интенсивности ионов в масс-спектре. Результаты исследований показали, что масс-спектры образцов плазмы до помещения в темноту и сразу после пребывания в темноте (кровь бралась с открытыми глазами у исследуемого и при нормальной освещенности) были идентичны. В образцах плазмы крови, взятой при нормальной освещенности и светонепроницаемой повязкой на обоих глазах после 45-минутного пребывания больного в условиях темноты с открытыми глазами были выявлены в больших концентрациях (в 2-5 раза, превышающих исходные уровни в образцах плазмы взятых при других условиях) рибозиды оснований нуклеиновых кислот: тимина, цитозина и гуанина. Остальные пики во всех образцах плазмы имели низкую интенсивность. Различие в компонентном составе образцов плазмы установлены в диапазоне масс ионов от массы (m/z) 300 до 1000 единиц атомных масс (а.е.м) при усилении этого участка спектра в 8-10 раз. В этом интервале масс-спектров выявлено 4 взаимосвязанных участка, характеризующих области мононуклеотид-монофосфатов - масса (т/г) 300-390 единиц атомных масс (а.е.м.), дифосфатов (m/z 400-550 а.е.м.), трифосфатов (m/z 340-600 а.е.м.) и их солей и область динуклеотидов или ассоциатов мононуклеотидов (m/z 600 а.е.м. и выше).
Таким образом, выполненные исследования показали, что аутокровь, взятая в вышеуказанных специфических условиях, в 2-5 раза превышает исходный уровень нуклеозидов, мононуклеотид-монофосфатов, ди- и трифосфатов, динуклеотидов и таким образом может быть использована в лечебных целях.
Способ осуществляется следующим образом: аутокровь для лечения забирали в количестве 60,0 мл гепаринизированными шприцами в условиях темноты после пребывания больного в темноте в течение 45 минут с открытыми глазами. Через 20 минут взятую аутокровь вводили внутривенно один раз в сутки. Курс лечения составил 6-12 введений в течение 2-3 недель.
Пример 1. Больная А.Г., 78 лет. Диагноз: Сахарный диабет 1 типа. Диабетическая ретинопатия (васкулярная стадия). Объективно: острота зрения правого глаза =0,5 не корригирует, острота зрения левого глаза =0,5 не корригирует. Глазное дно: диск зрительного нерва с четкими контурами, сосудистый пучок в ходе не изменен, вены расширены, извиты, множество микроаневризм и отложения мелкого твердого экссудата. В центральном поле зрения (ЦПЗ) 21 абсолютная и 11 относительных скотом.
Больной 1 раз в сутки внутривенно вводили 60,0 мл аутокрови, полученной при соблюдении вышеописанных условий. Всего выполнено 11 инъекций. После четвертой инъекции ежедневный прирост остроты зрения составлял 0,1-0,15. К 10-й инъекции острота зрения на обоих глазах достигла максимальной величины и составила 1,0 без коррекции. На глазном дне обоих глаз офтальмоскопически динамики не выявлено. По результатам исследования ЦПЗ существенно уменьшилось количество абсолютных и относительных скотом - 5 и 3 соответственно. Достигнутый терапевтический результат сохранялся на протяжении наблюдаемых 14 месяцев.
Пример 2. Больная И.Б., 65 лет. Диагноз обоих глаз: Неэкссудативная центральная хориоретинальная дистрофия. Объективно: острота зрения правого глаза =0,4 не корригирует, острота зрения левого глаза =0,3 не корригирует. Глазное дно: диски зрительных нервов бледно-розовые, с четкими контурами, сосудистый пучок в ходе не изменен, артерии неравномерного калибра, склерозированы, вены незначительно расширены, в центральной области глазного дна дистрофические очаги, перераспределение пигмента. ЦПЗ - 14 абсолютных и 34 относительных скотом. Больной 1 раз в сутки внутривенно вводили аутокровь в количестве 60,0 мл, полученной по вышеописанной методике. В течение курса лечения (три недели) выполнили 12 внутривенных инъекций. Результаты лечения: острота зрения правого глаза повысилась с 0,4 до 1,0 без коррекции, острота зрения левого глаза повысилась с 0,3 до 0,7 без коррекции, ЦПЗ - уменьшилось количество скотом - 5 абсолютных и 9 относительных. На глазном дне динамики не отмечено. Терапевтический эффект сохранялся в течение наблюдаемых 8 месяцев.
Всего предложенным способом было пролечено 25 пациентов с сосудистой и дистрофической патологией глазного дна без экссудативно-геморрагического процесса (центральная хориретинальная дистрофия - 8, диабетическая ретинопатия - 9, парафовеолярные субретинальные мембраны - 3, высокая осложненная миопия - 3, посттромботическая ретинопатия - 2) в возрасте от 30 до 85 лет. В результате внутривенного применения аутокрови с повышенным содержанием нуклеозидов, мононуклеотид-монофосфатов, ди- и трифосфатов, динуклеотидов отмечено существенное повышение остроты зрения (на 0,3-0,7) и достоверное улучшение ЦПЗ у больных с исходной остротой зрения не ниже 0,2. Длительность наблюдения составила 14 месяцев. Терапевтическая эффективность сохранялась в течение 6,5-14 месяцев.
Таким образом, впервые показано, что в результате влияния «фактора темноты» в крови больных с сосудистой патологией глазного дна повышается содержание нуклеозидов, мононуклеотид-монофосфатов, ди- и трифосфатов, динуклеотидов, которые при вышеуказанных условиях могут сохраняться во взятой аутокрови и использоваться как лечебное средство при сосудистых и дистрофических заболеваниях глазного дна для существенного повышения зрительных функций.
ПРИЛОЖЕНИЕ
К описанию изобретения «Способ повышения зрительных функций у больных с сосудистыми и дистрофическими заболеваниями».
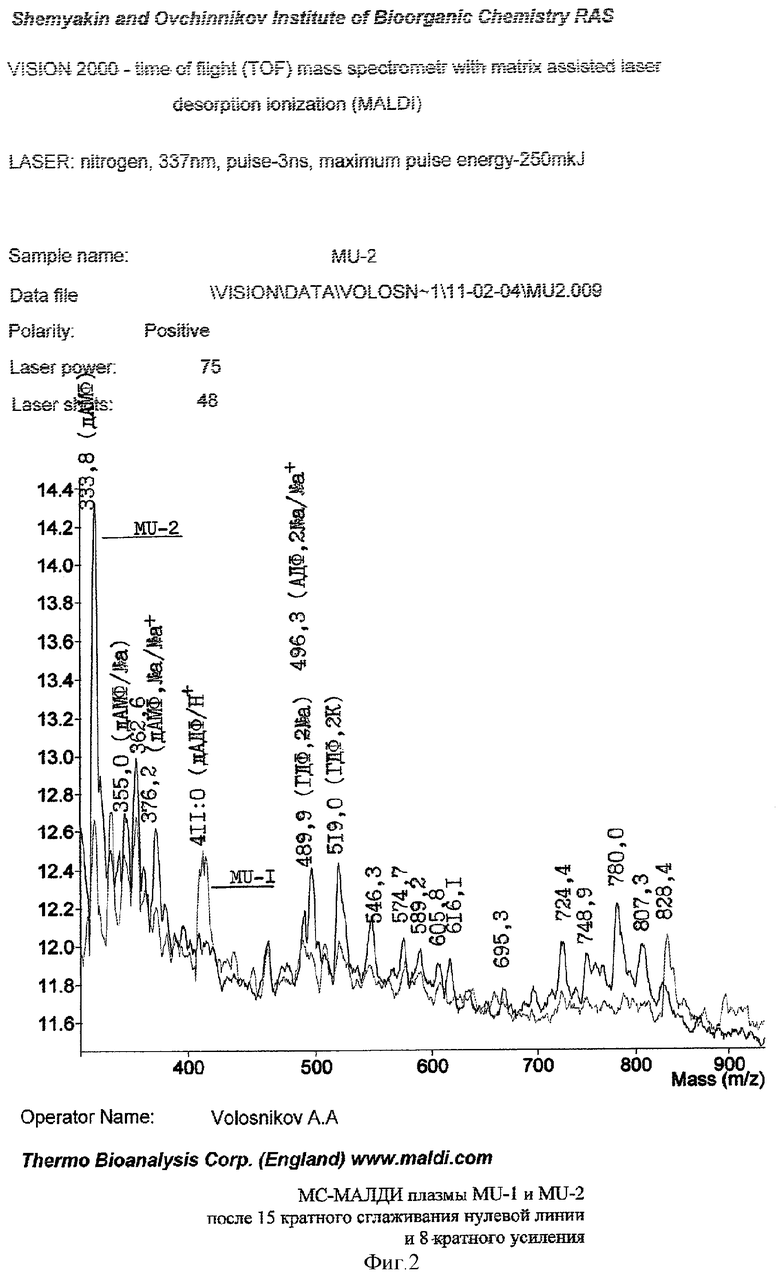
Фиг.1. Представлены масс-спектры пациента MU. Для большей наглядности и легкости отнесения пиков масс-спектры MU-1 (до помещения пациента в условия темновой адаптации) и MU-2 (после 45-минутного пребывания пациента в темноте) расположены в одних и тех же координатах масс ионов. По вертикали расположена шкала интенсивности ионов в масс-спектре. По горизонтали - масса определяемых веществ.
Как видно, в плазме крови MU-2, сравнительно с MU-1, в 2-5 раз выше уровень нуклеозидов (гуанозина - РибГ, цитидина - РибС, тимидина - РибТ ) с массой до 305 а.е.м.(единиц атомных масс).
Фиг.2. Представлены различия в компонентном составе плазмы крови MU-2 в диапазоне масс ионов от т/г(массы) 300 до 900 а.е.м. при усилении этого участка в 8 раз.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ КРОВИ С ПОВЫШЕННЫМ СОДЕРЖАНИЕМ НУКЛЕОЗИДОВ И НУКЛЕОТИДОВ | 2004 |
|
RU2290938C2 |
| СПОСОБ ПОВЫШЕНИЯ ОСТРОТЫ ЗРЕНИЯ У БОЛЬНЫХ С СОСУДИСТЫМИ И ДИСТРОФИЧЕСКИМИ ЗАБОЛЕВАНИЯМИ СЕТЧАТКИ | 2003 |
|
RU2258490C1 |
| СПОСОБ ЦИТОФЛАВИН-ЭЛЕКТРОКУМУЛЯЦИИ ПРИ ЛЕЧЕНИИ СОСУДИСТЫХ И ДИСТРОФИЧЕСКИХ ЗАБОЛЕВАНИЙ СЕТЧАТКИ И ЗРИТЕЛЬНОГО НЕРВА | 2011 |
|
RU2462280C1 |
| СПОСОБ ПРОФИЛАКТИКИ И ЛЕЧЕНИЯ РЕТИНОПАТИИ НЕДОНОШЕННЫХ ДЕТЕЙ | 2008 |
|
RU2387416C1 |
| СПОСОБ ТЕРАПЕВТИЧЕСКОГО ЛЕЧЕНИЯ ПЕРВИЧНОЙ ОТКРЫТОУГОЛЬНОЙ ГЛАУКОМЫ | 2003 |
|
RU2244528C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ ОСТРОТЫ ЗРЕНИЯ | 2007 |
|
RU2353298C1 |
| Способ лечения эндотелиально-эпителиальной дистрофии роговицы | 2020 |
|
RU2730975C1 |
| СПОСОБ УЛУЧШЕНИЯ ЗРИТЕЛЬНЫХ ФУНКЦИЙ ПРИ ПЕРВИЧНОЙ ОТКРЫТОУГОЛЬНОЙ ГЛАУКОМЕ С НОРМАЛИЗОВАННЫМ ОФТАЛЬМОТОНУСОМ | 2007 |
|
RU2351299C1 |
| СПОСОБ ЛЕЧЕНИЯ ГЕМОФТАЛЬМА | 1997 |
|
RU2148972C1 |
| СПОСОБ ЛЕЧЕНИЯ ЗАБОЛЕВАНИЙ ЗРИТЕЛЬНОГО НЕРВА И СЕТЧАТКИ | 2008 |
|
RU2373904C1 |
Изобретение относится к области медицины, а именно к офтальмологии, и предназначено для лечения сосудистых и дистрофических заболеваний глазного дна. Для этого больным с исходной остротой зрения не менее 0,2 внутривенно вводят аутокровь, причем забор крови осуществляют после 45-минутного пребывания больного в темноте с открытыми глазами, а взятие крови осуществляют при нормальной освещенности и наличии светонепроницаемой повязки на глазах пациентов. Способ обеспечивает эффективное лечение за счет повышения содержания нуклеозидов, мононуклеотид-монофосфатов, ди- и трифосфатов и динуклеотидов в аутокрови при заявленных условиях ее получения. 1 з.п. ф-лы, 2 ил.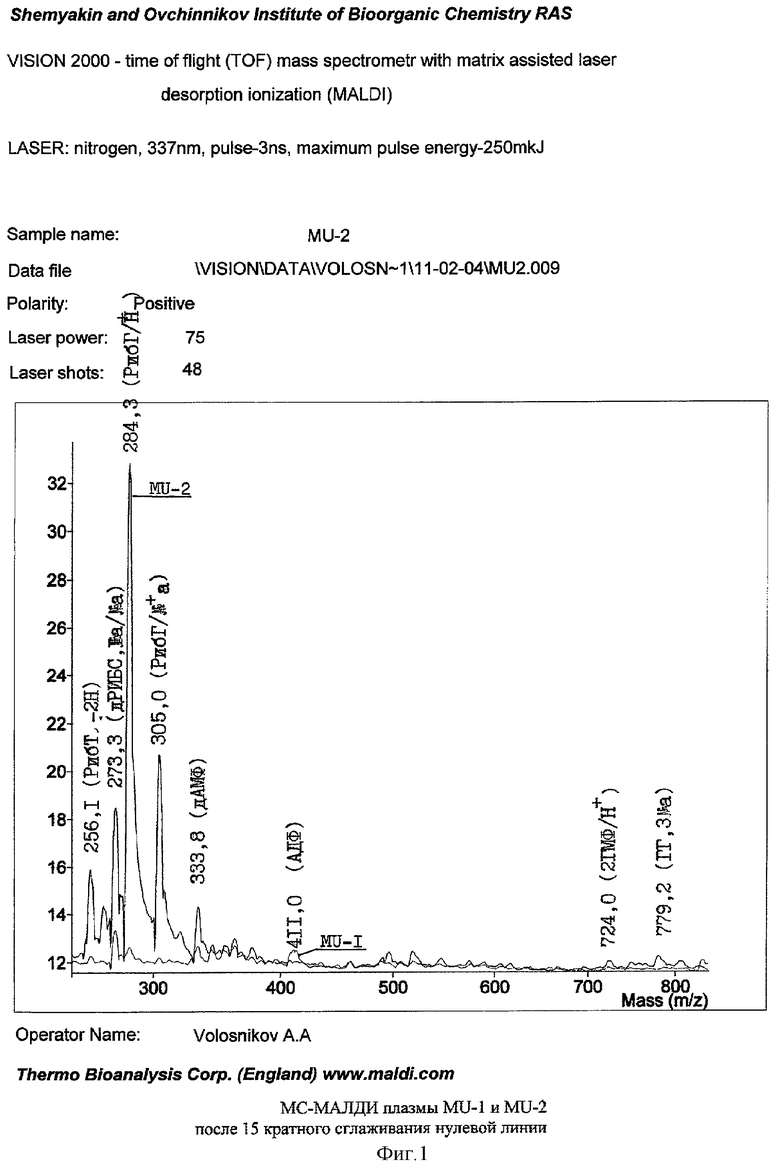
| СПОСОБ ЛЕЧЕНИЯ НАЧАЛЬНОЙ СТАДИИ ЦЕНТРАЛЬНОЙ ИНВОЛЮЦИОННОЙ ХОРИОРЕТИНАЛЬНОЙ ДИСТРОФИИ | 1992 |
|
RU2022542C1 |
| СПОСОБ СТИМУЛЯЦИИ РЕПАРАТИВНЫХ И ТРОФИЧЕСКИХ ПРОЦЕССОВ В ТКАНЯХ ОРГАНИЗМА | 1994 |
|
RU2095067C1 |
| СПОСОБ СОЗДАНИЯ МЕТАЛЛИЗАЦИИ ИНТЕГРАЛЬНЫХ СХЕМ | 1987 |
|
SU1477175A1 |
| US 2004204350, 14.10.2004 | |||
| СТАЙЕР Л | |||
| "Биохимия" Москва, 1985, т.2, с.255-278 | |||
| ФИЛИНА А.А | |||
| и др | |||
| "Влияние гемокомпетентной терапии (активированной аутоплазмы) на уровень глутатиона в крови больных с сосудистой патологией глазного дна" | |||
| Вести офтальмологии, 2000, 116, №5, | |||
Авторы
Даты
2007-01-20—Публикация
2004-12-15—Подача