Изобретение относится к новым ПЭГ-производным белков, в частности к ПЭГ-производным интерферона, которые могут быть использованы в медицине, например при лечении вирусных заболеваний.
Лечение нативными препаратами пептидной структуры имеет ряд существенных недостатков: белки быстро гидролизуются в гастроинтестинальном отделе пищеварительного тракта и поэтому используются, как правило, парентерально. Относительно короткий период полураспада таких препаратов в организме пациента препятствует достижению их максимального терапевтического воздействия и предусматривает их многократное использование. Еще одним важным негативным фактором, ограничивающим применение нативных или рекомбинантных белковых препаратов, является их высокая иммуногенность и связанные с ней сенситивные реакции. Принципиальное изменение структуры их молекулы либо нивелирует их биологические свойства, либо влечет за собой увеличение побочных эффектов, связанных с их применением. Одним из путей повышения эффективности лекарственных препаратов белковой структуры является химическая модификация их молекулы, состоящая не в собственно изменении их структуры, а в физико-химической трансформации, достигаемой соединением нативной молекулы с полиэтиленгликолем (ПЭГ). Данный процесс получил название «пегилирование». Подобная химическая модификация фармакологических препаратов пептидной структуры направлена на улучшение их переносимости, снижение иммуногенности, повышение периода их полужизни, и как следствие всего перечисленного, на значительное увеличение эффективности лечения и повышение качества жизни в процессе его проведения.
ПЭГ в качестве потенциального объекта - модификатора веществ пептидной структуры привлек внимание исследователей еще в начале 1970х годов. Молекулы ПЭГ - это водорастворимые полимеры окиси этилена с двумя терминальными гидроксильными группами. Молекулярный вес молекул ПЭГ может колебаться в пределах 300-4000 Дальтон, а выстроенные в цепи макромолекулы ПЭГ могут формировать как разветвленную, так и линейную стереохимию. Именно масса ПЭГ и его стереохимическая структура, как правило, определяют свойства модифицированного пептидного субстрата.
Гидрофильность модифицированных ПЭГ-молекул формирует принципиально новые физико-химические свойства измененного пептида. Высокое содержание атомов водорода даже в одной молекуле ПЭГ позволяет ей связываться с 2-3 молекулами воды. Подобный эффект влечет за собой формирование «водного облака» вокруг модифицированной молекулы «ПЭГ-белок». Этот своеобразный «щит» воды вокруг модифицированной молекулы с одной стороны значительно повышает растворимость и биодоступность препарата, с другой - защищает молекулу от других белков (нейтрализующие антитела, комплемент). Таким образом ПЭГ-модифицированные пептиды значительно более защищены от опсонизации и активного фаго- и эндоцитоза клеточных структур макроорганизма.
Изменения фармакокинетических и фармакодинамических свойств ПЭГ-модифицированных пептидов зависят от массы молекулы ПЭГ, специфических мест связи с белком, строения молекулы модифицирующего агента.
Интерфероны - это группа биологически активных белков или гликопротеидов, синтезируемых клеткой в процессе защитной реакции на чужеродные агенты - вирусную инфекцию, антигенное или митогенное воздействие. ИФН не обладают специфичностью в отношении вирусов и действуют угнетающе на репродукцию различных вирусов. Важны также другие эффекты ИФН, интерес к ним обусловлен высокой эффективностью применения препаратов интерферона при таких патологических состояниях, как и онкологические заболевания, болезни крови, а также неуклонным ростом числа больных, страдающих вышеперечисленными заболеваниями.
Пегилированный интерферон представляет собой конъюгат молекулы интерферона и ковалентно прикрепленного к ней участка молекулы полиэтиленгликоля, который защищает молекулу интерферона от ферментного разрушения и обеспечивает препарату ряд других преимуществ.
Известны, в частности, пэгилированные производные интерферона, полученные присоединением молекулы разветвленного полиэтиленгликоля к интерферону α-2а (Патент РФ №2180595, 20.03.2002). Эти пэгилированные производные характеризуются более продолжительным временем полужизни в сыворотке крови по сравнению с немодифицированным интерфероном. Из источника Kozlowski A., et al. "Development of Pegylated interferons for the treatment of Chronic Hepatitis C", BioDrugs, 2001, 15(7), известны конъюгаты интерферонов альфа и производного полиэтиленгликоля, в которых молекулярная масса звеньев полиэтиленгликоля составляет 30 кДа и меньше.
Задачей, на решение которой направлено изобретение, является создание новых конъюгированных производных интерферона, обладающих повышенной стабильностью по сравнению с известными аналогами.
Для решения поставленной задачи в рамках настоящего изобретения были синтезированы новые ПЭГ-производные интерферона. В ходе проведенных экспериментов было неожиданно обнаружено, что эти пэгилированные производные обладают значительно более длительным сроком персистирования в организме, чем известные. Данное свойство этих соединений позволит поддерживать постоянную эффективную концентрацию препаратов на их основе в крови при меньшей кратности введения, что позволит повысить эффективность проводимой терапии и снизит затраты на лечение.
ПЭГ-производные белков согласно настоящему изобретению представляют собой конъюгат белка и производного полиэтиленгликоля формулы
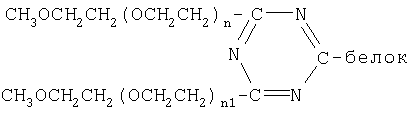
где белок представляет собой интерферон α-2b, a n и n1 имеют такие значения, что средняя молекулярная масса звеньев полиэтиленгликоля составляет от приблизитеольно 7500 Да до приблизительно 35000 Да. Предпочтительным вариантом является конъюгат, в котором n=n1=120, a молекулярная масса звеньев полиэтиленгликоля составляет приблизительно 10000 Да. Изобретение также относится к фармацевтической композиции, обладающей противовирусной активностью, содержащей указанный коньюгат, и терапевтически инертный носитель; и к способу борьбы с вирусной инфекцией, включающий введение в организм указанного ПЭГ-конъюгата.
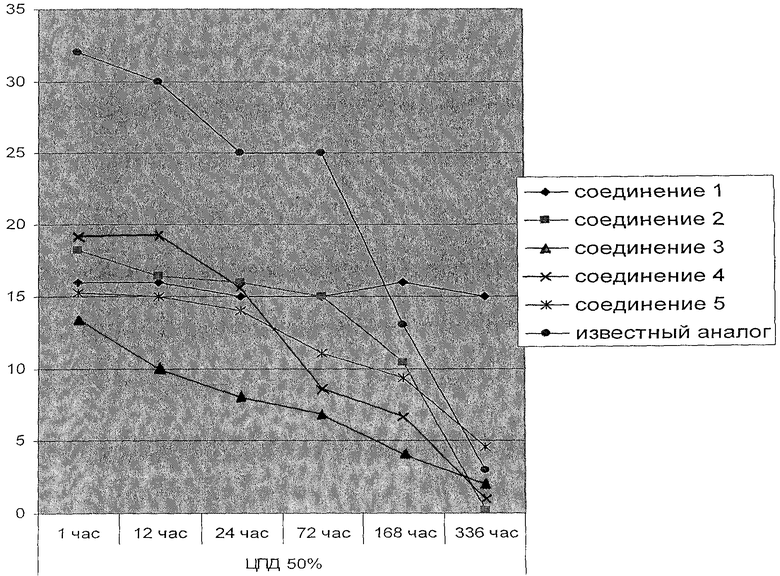
График (см. чертеж) отражает уровень биологически активного интерферона в сыворотке крови в условных единицах активности. Из графика видно, что заявленные соединения обладают значительно более высокой стабильностью по сравнению с другими производными - в течение 14 дней наблюдения его выведение из организма не отмечалось. На графике использованы следующие обозначения:
Соединение 1 - конъюгат по изобретению,
Соединение 2 - конъюгат 2,4-бис-(метоксиполиэтилен)триазина и интерферона α-2а,
Соединение 3 - конъюгат 2,4-бис-(метоксиполиэтилен)триазина и интерферона α-1,
Соединение 4 - конъюгат 2,4-бис-(метоксиполиэтилен)триазина и интерферона β-1,
Соединение 5 - конъюгат 2,4-бис-(метоксиполиэтилен)триазина и интерферона α-4.
Известный аналог - конъюгат полиэтиленгликоля и интерферона α-2а.
Пример 1. Получение ПЭГ-производных
Вначале получают полиэтиленоксид многостадийным или одностадийным синтезом. В качестве стартового вещества использовали олигоэтиленоксид с молекулярной массой 250 (средняя степень полимеризации 4,5), полученный при взаимодействии окиси этилена с метилатом натрия. При одностадийном синтезе к 100 г стартового вещества постепенно в течение 12 дней при повышении температуры от 120 до 170°С под давлением 4-5 атм добавляли 2500 г окиси этилена. Многостадийный синтез проводят следующим образом:
1 стадия. К 100 г стартового вещества добавляют 700 г окиси этилена. Реакцию проводят в стальном реакторе с мешалкой в атмосфере азота под давлением 4 атм при температуре 120°С в течение 8 часов.
2 стадия. К 100 г продукта, полученного на стадии 1, добавляют 700 г окиси этилена. Реакцию проводят в тех же условиях в течение 9 часов.
3 стадия. К 170 г продукта, полученного на стадии 2, добавляют 330 г окиси этилена. Реакцию проводят при температуре 140°С в течение 9 часов.
4 стадия. К 200 г продукта, полученного на стадии 3, добавляют 330 г окиси этилена. Реакцию проводят при температуре 140°С в течение 9 часов.
5 стадия. К 400 г продукта, полученного на стадии 4, добавляют 120 г окиси этилена. Реакцию проводят при температуре 160°С в течение 9 часов.
6 стадия. К 210 г продукта, полученного на стадии 5, добавляют 340 г окиси этилена. Реакцию проводят при температуре 170°С в течение 9 часов.
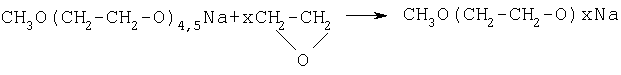
Синтез полиэтиленоксидов, разветвленных с помощью цианурхлорида осуществляют в одну стадию в растворе 1,2-дихлорэтана путем взаимодействия очищенного методом возгонки цианурхлорида с NaO-полиэтиленоксидом с различной длиной цепи. При этом проводят взаимодействие между 15% раствором полиэтиленоксида с цианурхлоридом в присутствии триэтиламина (25% моль от общего количества концевых групп)
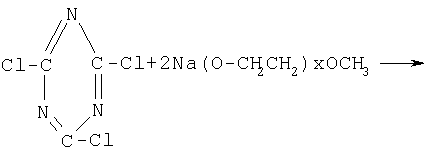
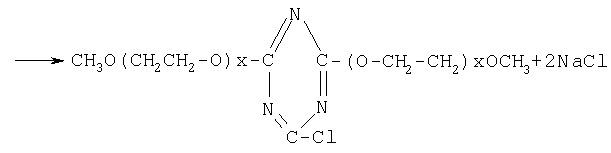
Реакцию проводят при 80°С в течение часа. Полученный полимер высаживают в 4-х кратный избыток серного эфира, а затем трехкратно промывают им же.
Таким образом получают триазиновые производные полиэтиленоксида формулы:
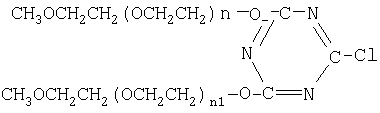
Пример 2. ПЭГилирование интерферона-α-2b
Возможность использования этих соединений для модификации белков продемонстрирована на примере интерферона. Интерферон-α-2в фирмы Hydrola Ltd. 20 мг препарата растворяют в 4 мл воды. Аликвоты по 1 мл (5 мг) переносят в реакционные флаконы. Для модификации рН раствора доводят до 9.5 50 мМ фосфатно-карбонатным буфером. Реагенты добавляют 5 раз в 10-кратном молярном избытке с интервалами в 6-12 часов. За ходом реакции следят с помощью проведения гель-фильтрационной ВЭЖХ. Спустя 60 часов реакцию останавливают добавлением 50 мМ метилового эфира глицина. Физико-химические характеристики полученного конъюгата: молекулярная масса 10000 Да, рН - 6,0, прозрачность 2,3 FTU, осмоляльность 375 мОсм/кг (осмометр Vogel ОМ 802), бактериальные эндотоксины - 0,15 EU/мкг, чистота (обращено-фазовая ВЭЖХ) - 98% площади.
Пример 3. Антивирусная активность конъюгатов интерферона-α-2b
Отбирают пробы по 2 мл следующей расчетной активности:
1) стандарт (исходный интерферон) - 25 мкг/мл (3.5×106)
2) конъюгат по изобретению - 24 мкг/мл (3.36×106)
Противовирусную активность проверяют стандартным методом в культуре клеток легких человека Л-68 против вирусного везикулярного стоматита.
Биологическое тестирование дало следующие результаты:
Биоактивность приведенная - биоактивность определенная, умноженная на коэффициент, получаемый от деления расчетной активности стандарта на определенную активности стандарта. Приведенную биоактивность рассчитывают для определения уменьшения удельной активности интерферона в процессе модификации.
Таким образом, модифицированный интерферон-α-2b согласно данному изобретению сохраняет значительную антивирусную активность, подобную известному препарату, для которого таковая составляет 7% при удельной биоактивности 1.4×107.
Пример 4. Исследование фармакокинетики препаратов
Беспородным крысам внутривенно вводили следующие препараты:
Конъюгат по изобретению по 0,56 мл=13,5 мкг/крыса.
Известный аналог - пэгилированное производное интерферона (согласно RU 2180595) - по 0,1 мл=13,5 мкг/крыса
У каждой крысы через 1 час после введения из хвостовой вены брали по 0,5 мл крови. Для этого скальпелем отсекали 1,5-2 мм плоти хвоста. Кровь собирали в пробирки типа Eppendorf. Пробирки помещали в термостат и инкубировали 30 минут при 37°С. Стеклянным капилляром отделяли образовавшийся тромб от стенок пробирки. Пробирки помещали в холодильную камеру и инкубировали 4-6 часов при +4°С. Автоматической пипеткой отсасывали сыворотку и для удаления клеток крови центрифугировали при 5000 об/мин в течение 5 минут. Для стерилизации образцов сыворотки крови супернатанты переносили в системы фильтрации Ultrafree-MC (Amicon) и центифугировали при 2000 об/мин в течение 10 минут. Образцы для тестирования хранили при +4°С.
Результаты измерения уровня биологически активного интерферона за период 14 дней показаны на графике.
Пример 5. Токсичность полученных ПЭГ-производных
Эксперименты по изучению острой токсичности выполнялись на белых нелинейных мышах и крысах. Для исследования каждой дозы препарата использовались группы по 6 животных. При использовании интервала доз от 1 до 15 МЕ/кг летальных эффектов не наблюдалось. Учитывая то, что максимальная терапевтическая доза для человека составит около 0,03 МЕ/кг, препараты являются малотоксичными.
Пример 6. Противовирусная активность in vivo
Для определения противовирусной активности 20 мышам весом 10-12 г вводят 0,2 мл препарата 24 мкг/мл внутрибрюшинно за 24 и 2 ч до заражения смертельным вирусом. Животных наблюдают в течение 14 дней. Если процент выживаемости составляет более 60%, то тестируемый препарат считается активным. Для конъюгата по изобретению этот показатель составил 90%, что позволяет отнести его к высокоактивным.
| название | год | авторы | номер документа |
|---|---|---|---|
| ПЭГИЛИРОВАННЫЙ ИНТЕРФЕРОН ДЛЯ БОРЬБЫ С ВИРУСНОЙ ИНФЕКЦИЕЙ | 2004 |
|
RU2311930C2 |
| ЛЕКАРСТВЕННОЕ СРЕДСТВО НА ОСНОВЕ МОДИФИЦИРОВАННОГО ИНТЕРФЕРОНА АЛЬФА С ПРОЛОНГИРОВАННЫМ ТЕРАПЕВТИЧЕСКИМ ДЕЙСТВИЕМ | 2008 |
|
RU2382048C1 |
| КОНЪЮГАТЫ ИНТЕРФЕРОНОВ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2011 |
|
RU2466138C1 |
| НОВЫЙ ФУНКЦИОНАЛЬНО АКТИВНЫЙ ВЫСОКООЧИЩЕННЫЙ СТАБИЛЬНЫЙ КОНЪЮГАТ ИНТЕРФЕРОНА α С ПОЛИЭТИЛЕНГЛИКОЛЕМ, ПРЕДСТАВЛЕННЫЙ ОДНИМ ПОЗИЦИОННЫМ ИЗОМЕРОМ ПЭГ-NH-ИФН, С УМЕНЬШЕННОЙ ИММУНОГЕННОСТЬЮ, С ПРОЛОНГИРОВАННЫМ БИОЛОГИЧЕСКИМ ДЕЙСТВИЕМ, ПРИГОДНЫЙ ДЛЯ МЕДИЦИНСКОГО ПРИМЕНЕНИЯ, И ИММУНОБИОЛОГИЧЕСКОЕ СРЕДСТВО НА ЕГО ОСНОВЕ | 2010 |
|
RU2447083C1 |
| МОЛЕКУЛА ИНТЕРФЕРОНА-β-1а ЧЕЛОВЕКА, МОДИФИЦИРОВАННАЯ ПОЛИЭТИЛЕНГЛИКОЛЕМ, ОБЛАДАЮЩАЯ ПРОТИВОВИРУСНОЙ, ИММУНОМОДУЛИРУЮЩЕЙ И АНТИПРОЛИФЕРАТИВНОЙ АКТИВНОСТЯМИ, С ПОВЫШЕННОЙ СТАБИЛЬНОСТЬЮ, УМЕНЬШЕННОЙ ИММУНОГЕННОСТЬЮ, УЛУЧШЕННЫМИ ФАРМАКОКИНЕТИЧЕСКИМИ И ФАРМАКОДИНАМИЧЕСКИМИ ПАРАМЕТРАМИ, ПРИГОДНАЯ ДЛЯ МЕДИЦИНСКОГО ПРИМЕНЕНИЯ И ИММУНОБИОЛОГИЧЕСКОЕ СРЕДСТВО НА ЕЕ ОСНОВЕ | 2013 |
|
RU2576372C2 |
| ИНТЕРФЕРОН, КОНЪЮГИРОВАННЫЙ С ПОЛИЭТИЛЕНГЛИКОЛЕМ | 2010 |
|
RU2433135C1 |
| ПЕГИЛИРОВАННЫЙ КОНЪЮГАТ ВАРИАНТА РЕКОМБИНАНТНОГО КОНСЕНСУСНОГО ИНТЕРФЕРОНА И СПОСОБ ЕГО ПОЛУЧЕНИЯ, И ПРИМЕНЕНИЕ | 2011 |
|
RU2575796C9 |
| НОВЫЙ СОСТАВ, СОДЕРЖАЩИЙ КОНЪЮГАТ ПЭГ И ИНТЕРФЕРОН-АЛЬФА-2БЕТА, ОБЛАДАЮЩИЙ СНИЖЕННОЙ БОЛЕЗНЕННОСТЬЮ ПРИ ВВЕДЕНИИ | 2014 |
|
RU2572800C1 |
| ДЕНДРИМЕР-ПЭГ С ЧЕТЫРЬМЯ ВЕТКАМИ ДЛЯ КОНЪЮГИРОВАНИЯ С БЕЛКАМИ И ПЕПТИДАМИ | 2006 |
|
RU2409389C2 |
| Пролонгированный фактор эритропоэза человека и лекарственное средство на его основе | 2015 |
|
RU2664588C2 |
Изобретение относится к новым физиологически активным конъюгатам белка, которые могут быть использованы в медицине. Предложенный конъюгат образован молекулой белка и полиэтиленгликоля и имеет следующую формулу:
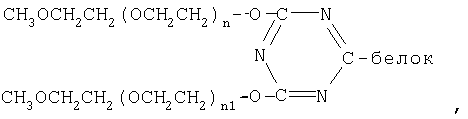 где белок представляет собой интерферон α-2b, a n и n1 имеют такие значения, что средняя молекулярная масса звеньев полиэтиленгликоля составляет от приблизительно 7500 Да до приблизительно 35000 Да. Конъюгат обладает повышенной стабильностью по сравнению с известными аналогами. Изобретение также относится к фармацевтической композиции с противовирусной активностью, содержащей указанный коньюгат, и к способу борьбы с вирусной инфекцией. 3 н. и 1 з.п. ф-лы, 1 ил.
где белок представляет собой интерферон α-2b, a n и n1 имеют такие значения, что средняя молекулярная масса звеньев полиэтиленгликоля составляет от приблизительно 7500 Да до приблизительно 35000 Да. Конъюгат обладает повышенной стабильностью по сравнению с известными аналогами. Изобретение также относится к фармацевтической композиции с противовирусной активностью, содержащей указанный коньюгат, и к способу борьбы с вирусной инфекцией. 3 н. и 1 з.п. ф-лы, 1 ил.
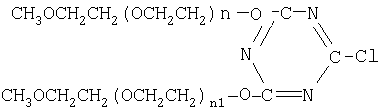
где белок представляет собой интерферон α-2b, a n и n1 имеют такие значения, что средняя молекулярная масса звеньев полиэтиленгликоля составляет от приблизительно 7500 Да до приблизительно 35000 Да.
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ ЦИТОКИНОВОГО И ИММУНОМОДУЛИРУЮЩЕГО ДЕЙСТВИЯ | 2002 |
|
RU2222345C2 |
| Способ крашения тканей | 1922 |
|
SU62A1 |
| Приспособление для точного наложения листов бумаги при снятии оттисков | 1922 |
|
SU6A1 |
| Кипятильник для воды | 1921 |
|
SU5A1 |
| Кипятильник для воды | 1921 |
|
SU5A1 |
| УСТРОЙСТВО ДЛЯ КОРРЕКЦИИ ГИРОСКОПИЧЕСКОГО | 0 |
|
SU332323A1 |
| Kozlowski A | |||
| et al | |||
| Development of pegylated interferons for the treatment of chronic hepatitis C | |||
| BioDrugs | |||
| Перекатываемый затвор для водоемов | 1922 |
|
SU2001A1 |
Авторы
Даты
2007-05-10—Публикация
2004-04-30—Подача