Изобретение относится к медицине, а именно к разделу сердечно-сосудистой хирургии.
Пороки аортального клапана в 40-70% случаев осложняются инфекционным эндокардитом и кальцинозом, что приводит к разрушению створки фиброзного кольца, аортальных синусов и зоны митрально-аортального контакта. После иссечения пораженных тканей формируются обширные дефекты, требующие пластического восстановления корня аорты аутотканями или другими (синтетическими, биологическими) материалами для последующей имплантации аортального протеза. В таких условиях расширяется объем хирургического вмешательства и возрастает вероятность развития кровотечения из несостоятельных тканей корня аорты, нарушений атрио-вентрикулярной проводимости, нарушения коронарного кровообращения, развития дисфункции протеза аортального клапана.
Известен аутопластический способ коррекции, при котором образовавшиеся дефекты тканей корня аорты ушивают, сопоставляя ткани корня аорты и формируя шов параллельно фиброзному кольцу аорты [1]. Однако при этом способе происходит деформация устья аорты с уменьшением его диаметра и сохраняется высокий риск развития жизненно опасных осложнений.
Известен метод аортального протезирования легочным аутографтом (ствол легочной артерии с клапаном), включающий реимплантацию устий коронарных артерий и имплантацию биологического кондуита в позицию легочного ствола - операция Росса [2]. Однако этот способ показан только при анатомически сохранном фиброзном кольце аорты и не предусматривает закрытие воспалительно-деструктивных дефектов аортального корня.
С целью устранения указанных выше негативных последствий предложен способ коррекции пороков, осложненных разрушением корня аорты, в котором применяют собственный клапан легочной артерии с мышечным лоскутом из миокарда выходного отдела правого желудочка для замещения аортального клапана и одновременной пластики дефектов аортального корня, а в позиции легочного ствола используют биологический кондуит.
Способ выполняется следующим образом.
После кардиоплегической остановки сердечной деятельности и достижения «сухого сердца доступом через поперечную аортотомию ревизуют аортальный клапан и подклапанное пространство. Оценивают степень разрушения аорты и распространения кальциноза, выраженность воспалительно-деструктивных изменений.
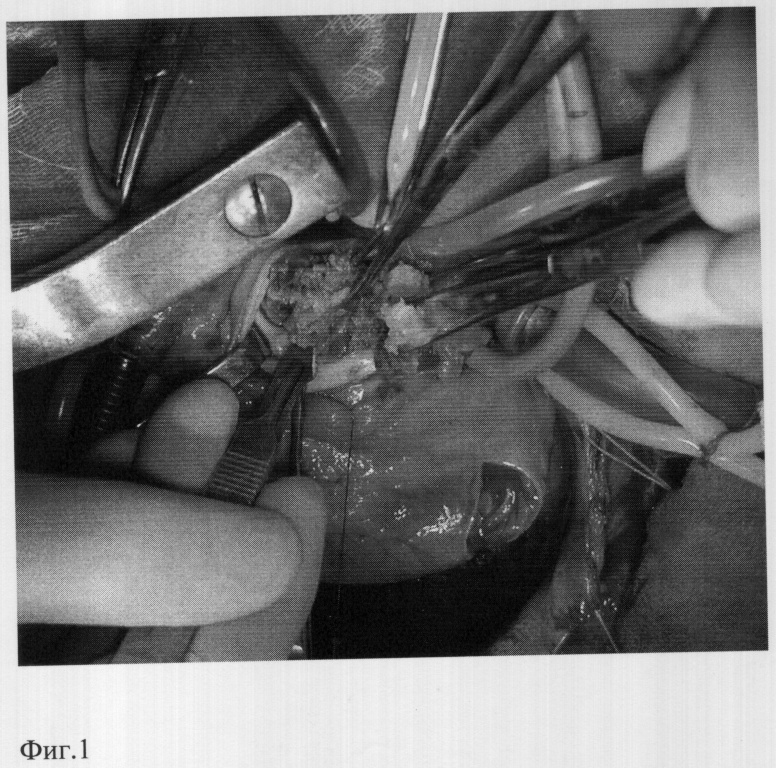
При выраженных изменениях аортального клапана и обширном распространении деструктивных изменений иссекают пораженные ткани: клапан аорты, участки аортальных синусов, фиброзного кольца, зоны митрально-аортального контакта (фиг.1).
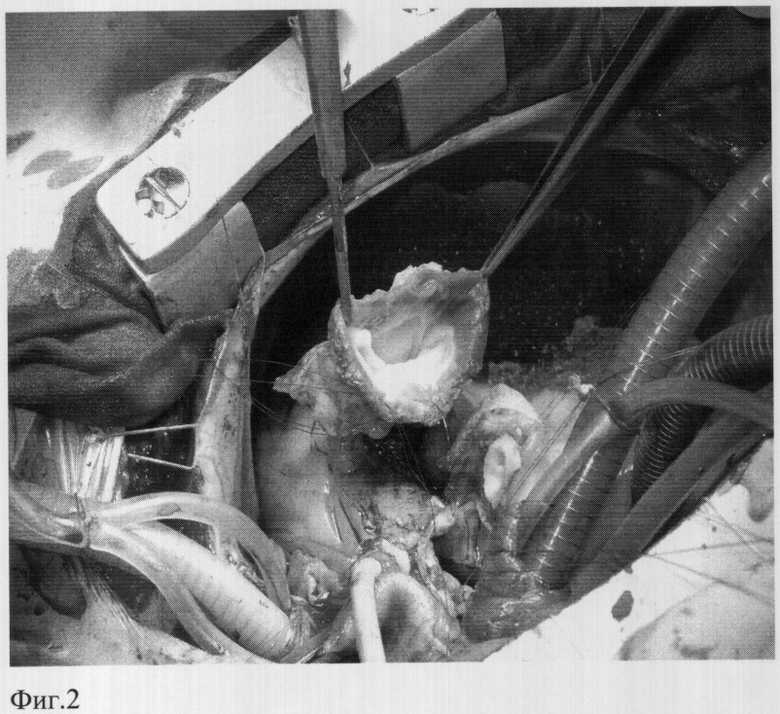
Затем выделяют и иссекают легочный ствол, содержащий клапан, с захватом мышечного лоскута выходного отдела правого желудочка шириной 15-20 мм (фиг.2). Причем проксимальный фрагмент легочного аутографта, а именно мышечный компонент, выкраивают по размерам, соответствующим дефекту тканей корня аорты, формируют мышечный лоскут.
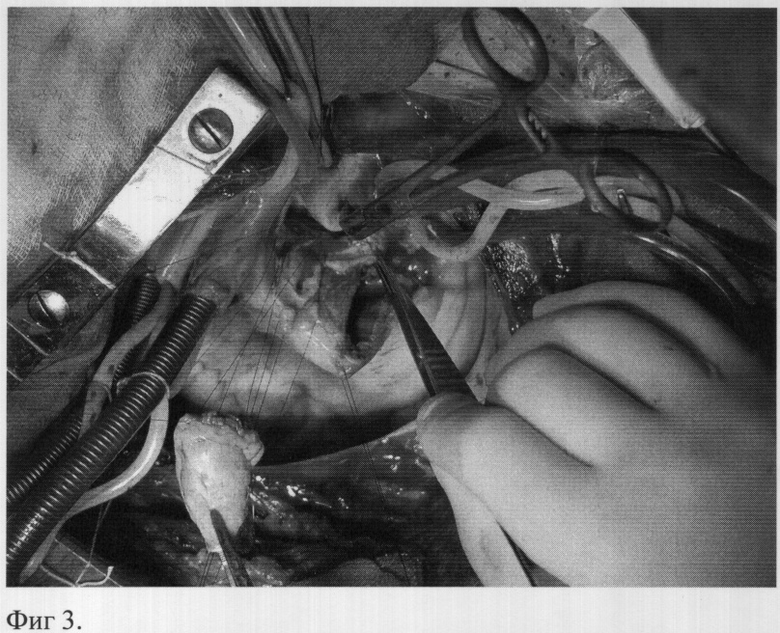
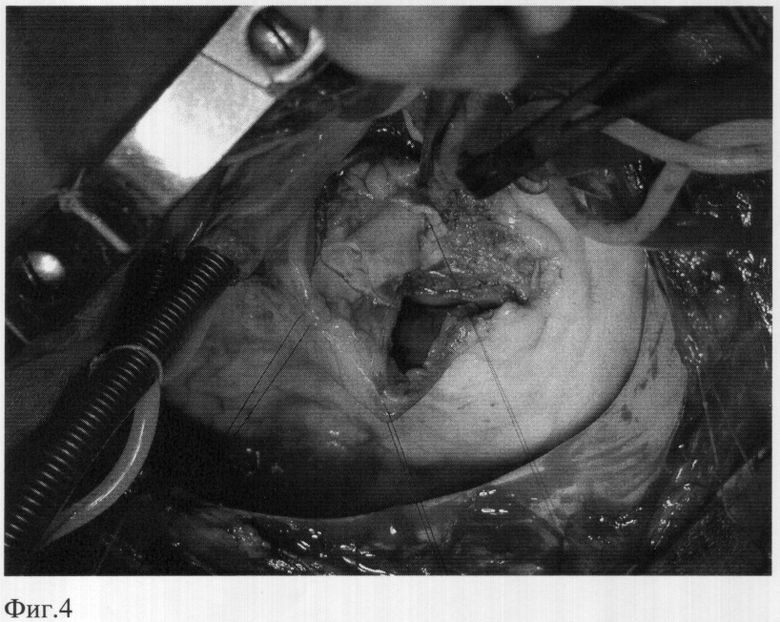
Имплантируют в аортальную позицию легочный аутографт, ориентируя его таким образом, чтобы существовало анатомическое соответствие устьев коронарных артерий синусам Морганьи, а также и соответствие мышечного продолжения аутографта дефекту основания аорты. Сначала проводят три П-образных шва (пролен 4/0) через комиссуры аутографта и через окружающие ткани в области локализовавшихся ранее комиссур корня аорты (фиг.3), аутографт выворачивают в левый желудочек и прошивают по основанию к тканям корня аорты обвивным швом от комиссуры до комиссуры, закрывая при этом дефекты корня аорты (фиг.4). Затем поочередно реимплантрируют устья коронарных артерий, левое, затем правое (пролен 5/0), формируют дистальный анастомоз между легочным аутографтом и восходящим отделом аорты. В позицию легочного ствола имплантируют биологический кондуит обвивными швами (дистальный анастомоз пролен 4/0, проксимальный пролен 3/0).
Пример выполнения способа
Больной В-ев В.Н., 51 года, история болезни № 1195, поступил в ГУ ННИПК им. Акад. Е.Н.Мешалкина 07.03.03 г, с диагнозом: Ревматический порок сердца, сочетанный аортальный порок с преобладанием стеноза, относительная митральная недостаточность. Кальциноз аортального клапана. ИБС.Стенокардия напряжения и покоя III ФК. Недостаточность крвообращения IIA-Б, III-IV ФК (NYHA). ХПН I.
Порок диагностирован в 1999 г. При поступлении жалобы на одышку при незначительной физической нагрузке (медленная ходьба), ночное удушье, боли в области сердца давящего характера как при нагрузке, так и в покое, отеки на ногах.
Состояние тяжелое. Дыхание везикулярное, ЧДД-20 в мин. Ритм сердца правильный, ЧСС 92 уд. в мин, грубый распространенный ситолический шум с эпицентром на аорте. АД-110/70 торр. Увеличена печень на 10 см, голени пастозны.
Результаты обследования. ЭКГ: синусовый ритм, блокада передней ветви левой ножки п. Гисса, гипертрофия левого предсердия.
Рентгенологически: Сосудистый легочный рисунок изменен по типу легочной гипертензии, интерстициального и артерио-венозного застоя. СЛК-56%. Расширен левый желудочек.
ЭХО-КГ: кдрЛЖ - 57 мм, ксрЛЖ - 47 мм, кдо158 мл, ксо - 81 мл, ЛП - 68 мм, ПП - 53 мм, ПЖ - 21 мм, толщина задней стенки ЛЖ - 17 мм, толщина межжелудочковой перегородки - 18 мм. Склероз корня аорты, створки аортального клапана изменены кальцинозом, систолический градиент - 91 мм рт.ст. Аортальная регургитация умеренная по объему. Створки митрального клапана неоднородны, площадь - 3,5 см2, регургитация умеренная. Фракция выброса ЛЖ - 41%.
Коронарография: тип кровообращения правый, стеноз передней нисходящей артерии до 60%.
Операция (21.03.03 г). Протезирование аортального клапана легочным аутографтом, протезирование легочного ствола биологическим кондуитом «Кемерово А-В композит 25», маммарокоронарное шунтирование передней нисходящей артерии.
Срединная стернотомия, выделение внутренней грудной артерии слева, выделение магистральных сосудов, подключение аппарата искусственного кровообращения по схеме полые вены - аорта. После окклюзии аорты и полых вен вскрыта поперечным доступом аорта. Кровяная антеградная кардиоплегия в устья коронарных артерий, затем ретроградно в коронарный синус. Аортальный клапан изменен грубым кальцинозом, переходящим на фиброзное кольцо и межжелудочковую перегородку. С большими техническими трудностями клапан иссечен, при этом образовались дефекты фиброзного кольца и правого коронарного синуса. Принято решение имплантировать легочный аутографт с миокардиальным лоскутом для пластики дефектов корня аорты. Выполнено вылущивание легочного ствола с мышечным лоскутом выходного отдела правого желудочка.
Легочный аутографт имплантирован комбинированным методом, на трех П-образных швах (пролен 4/0) через вершины комиссур и обвивным швом по остальной полуокружности, закрывая дефекты корня аорты, затем в аутографт поочередно реимплантированы устья коронарных артерий. В позицию легочного ствола имплантирован биологический кондуит «Кемерово А-В композит - 25», (пролен 4/0), вначале дистальный, затем проксимальный конец кондуита. Следующим этапом наложен анастомоз между аутографтом и восходящим отделом аорты (пролен 4/0). Последним этапом выполнено маммарокоронарное шунтирование передней нисходящей артерии.
Окклюзия аорты составила 185 мин. В ближайшем п/о периоде отмечались нарушения ритма сердца, явления сердечной, легочной недостаточности. Больной выписан на 24 сутки.
Предложенный метод реконструкции корня аорты у больных с воспалительно-деструктивными разрушениями позволяет выполнить адекватную замену аортального клапана полноценным собственным клапаном легочной артерии, закрыть дефекты стенок аорты, зоны митрально-аортального контакта, фиброзного кольца аорты мышечным лоскутом. Метод позволяет восстановить анатомию и функцию аортального корня, а также уменьшить число жизненно опасных осложнений (кровотечений, нарушений ритма сердца, дисфункций аортального клапана) у этой категории больных. Кроме того, у этих пациентов исключен прием антикоагулянтов в отдаленном периоде.
Источники информации
1. Способ расширения фиброзного кольца аортального клапана. RU 2196515 С2, 20.01. 2003.
2. Ross D., Jacson M., Davies I / The pulmonary autograft a permanent aortic valve // Eur. J. Cardiothorac Surg. - 1992. - Vol.6. - P.113-6.
| название | год | авторы | номер документа |
|---|---|---|---|
| АЛЛОГРАФТ (ВАРИАНТЫ), СПОСОБ ЕГО ПОЛУЧЕНИЯ (ВАРИАНТЫ) И СПОСОБ ПРОВЕДЕНИЯ АОРТАЛЬНОГО ПРОТЕЗИРОВАНИЯ | 2017 |
|
RU2712000C2 |
| Способ замещения корня аорты композитным биологическим кондуитом, состоящим из бесшовного клапанного протеза и линейного сосудистого протеза | 2022 |
|
RU2802744C1 |
| СПОСОБ БИЛАТЕРАЛЬНОЙ АОРТОАННУЛОПЛАСТИКИ ПРИ УЗКОМ ФИБРОЗНОМ КОЛЬЦЕ АОРТЫ | 2004 |
|
RU2300321C2 |
| СПОСОБ ПРОВЕДЕНИЯ ОПЕРАЦИИ НОРВУДА, СОСУДИСТЫЙ ГОМОГРАФТ И СПОСОБ ПОЛУЧЕНИЯ СОСУДИСТОГО ГОМОГРАФТА | 2017 |
|
RU2696057C2 |
| СПОСОБ ПРОТЕЗИРОВАНИЯ АТРИОВЕНТРИКУЛЯРНОГО КЛАПАНА СЕРДЦА ЛЕГОЧНЫМ АУТОГРАФТОМ | 2009 |
|
RU2392872C1 |
| Способ задней пластики корня аорты и выводного тракта левого желудочка для имплантации в аортальную позицию большего размера протеза | 2021 |
|
RU2774779C1 |
| Способ хирургического лечения гипертрофической обструктивной кардиомиопатии | 2015 |
|
RU2608705C1 |
| СПОСОБ ХИРУРГИЧЕСКОГО ЛЕЧЕНИЯ ВРОЖДЕННОГО ПЕРЕРЫВА ДУГИ АОРТЫ У ДЕТЕЙ ГРУДНОГО ВОЗРАСТА И НОВОРОЖДЕННЫХ | 2022 |
|
RU2784772C1 |
| СПОСОБ ПРОТЕЗИРОВАНИЯ ВСЕХ СТРУКТУР ВЫХОДНОГО ОТДЕЛА ПРАВОГО ЖЕЛУДОЧКА, ПУЛЬМОНАЛЬНОГО КЛАПАНА, ЛЕГОЧНОГО СТВОЛА | 2019 |
|
RU2747362C2 |
| СПОСОБ ПРОТЕЗИРОВАНИЯ ВСЕХ СТРУКТУР КОРНЯ АОРТЫ | 2018 |
|
RU2734748C2 |
Изобретение относится к медицине, а именно к сердечно-сосудистой хирургии и может быть использовано в ходе реконструкции пути оттока левого желудочка при экстравальвулярном разрушении устья аорты, для этого ствол легочной артерии с клапаном выделяют и иссекают вместе с мышечным лоскутом, формируя его, захватывая мышечную часть выходного отдела правого желудочка. При этом выкраивают мышечную часть проксимального фрагмента легочного аутографта по размерам, соответствующим дефекту аортального корня. Затем имплантируют легочный аоутографт в аортальную позицию. Мышечным лоскутом закрывают дефект корня аорты, проводя швы через окружающие ткани в области локализовавшихся ранее комиссур, прошивая обвивным швом основание аутографта и ткани основания аорты от комиссуры до комиссуры. После чего поочередно реимплантируют устья коронарных артерий, формируют дистальный анастомоз между аутографтом и восходящим отделом аорты, а в позицию легочного ствола имплантируют биологический кондуит. Способ позволяет выполнить адекватную замену аортального клапана полноценным собственным клапаном легочной артерии, закрыть дефекты стенок аорты, зоны митрально-аортального контакта, фиброзного кольца аорты мышечным лоскутом, восстановить анатомию и функцию аортального корня, а также уменьшить число жизненно опасных осложнений, в то же время у таких пациентов исключен прием антикоагулянтов в отдаленном периоде. 4 ил.
Способ реконструкции пути оттока левого желудочка при экстравальвулярном разрушении устья аорты, включающий имплантацию легочного аутографта в аортальную позицию и биокондуита в легочную, отличающийся тем, что ствол легочной артерии с клапаном выделяют и иссекают вместе с мышечным лоскутом, формируя его, захватывая мышечную часть выходного отдела правого желудочка, выкраивая мышечную часть проксимального фрагмента легочного аутографта по размерам, соответствующим дефекту аортального корня, затем соответственно анатомии основания аорты имплантируют легочный аутографт в аортальную позицию, мышечным лоскутом закрывают дефект корня аорты, проводя швы через окружающие ткани в области локализовавшихся ранее комиссур, прошивая обвивным швом основание аутографта и ткани основания аорты от комиссуры до комиссуры, после чего поочередно реимплантируют устья коронарных артерий, формируют дистальный анастомоз между аутографтом и восходящим отделом аорты, а в позицию легочного ствола имплантируют биологический кондуит.
| СИНЕЛЬНИКОВ Ю.С | |||
| и др., Первый опыт выполнения процедуры Росса у детей | |||
| Патология кровообращения и кардиохирургия | |||
| Топчак-трактор для канатной вспашки | 1923 |
|
SU2002A1 |
| БУРАКОВСКИЙ В.И., БОКЕРИЯ Л.А., Сердечно-сосудистая хирургия, М.: Медицина, 1996, с.431-432 | |||
| СПОСОБ РАСШИРЕНИЯ ФИБРОЗНОГО КОЛЬЦА АОРТАЛЬНОГО КЛАПАНА | 2000 |
|
RU2196515C2 |
| ROSS D | |||
| et al | |||
| The pulmonary autograft a permanent aortic valve, Eur | |||
| J | |||
| Cardiothorac Surg, 1992, Vol.6, p.113-6. | |||
Авторы
Даты
2007-06-10—Публикация
2004-07-15—Подача