Изобретение относится к биохимии, конкретно к биологически активным пептидам, обладающим антимикробным действием, которые могут найти применение в биотехнологии и медицине.
Стремительный рост числа структурно новых антибиотиков, вводимых в клиническую практику, наблюдавшийся в 40-50-х годах прошлого столетия, сменился длительным инновационным кризисом, который продолжается и сегодня [Walsh С. Where will new antibiotics come from? // Nat. Rev. Microbiol. - 2003. - Vol.1. - P.65-70]. Широкое применение антибиотиков в качестве лечебных препаратов вызывает быстрое накопление устойчивых форм микроорганизмов, у которых клинически существенная резистентность возникает за период от нескольких месяцев до нескольких лет. Распространены случаи устойчивости целого ряда патогенов человека (Enlerococcus faecalis, Mycobacterium tuberculosis, Pseudomonas aeruginosa, Salmonella typhi, Staphylococcus aureus, Streptococcus pneumoniae, Vibrio cholerae и многих других) практически к любому из применяемых препаратов [Walsh С. Molecular mechanisms that confer antibacterial drug resistance // Nature. - 2000. - Vol.406. - P.775-781].
По-видимому, принципиально новым классом природных антибиотиков, которые будут введены в клиническую практику, являются так называемые антимикробные пептиды [Finlay В.В., Hancock R.E.W. Can innate immunity be enhanced to treat microbial infections? // Nat. Rev. Microbiol. - 2004. - Vol.2. - P.497-504]. Несмотря на существование более сильных антибиотиков, действующих при меньших концентрациях, антимикробные пептиды обладают рядом преимуществ. Способность быстро убивать клетки-мишени, широкий спектр действия, активность в отношении штаммов, резистентных к другим антибиотикам, а также относительная трудность в селекции устойчивых мутантов in vitro, позволяют рассматривать эти вещества в качестве основы для создания эффективных лекарств, особенно на фоне снижения потенциала обычных антибиотиков [Hancock R.E.W., Lehrer R. Cationic peptides: a new source of antibiotics // Trends Biotechnol. - 1998. - Vol.16. - P.82-88].
Известно несколько сотен антимикробных пептидов [Brahmachary M. et al. ANTIMIC: a database of antimicrobial sequences // Nucleic Acids Res. - 2004. - Vol.32. - P.D586-D589]. Для большинства антимикробных пептидов мишенью действия, по-видимому, являются мембраны клеток патогенных организмов, а механизмом действия - нарушение нормальной проницаемости этих мембран. Для подавляющего большинства антимикробных пептидов характерны следующие структурные и функциональные особенности: общий положительный заряд молекулы и склонность к формированию амфипатических структур, что, как полагают, является основой их взаимодействия с мембранами, а также способность к ингибированию роста целого ряда микроорганизмов в концентрациях порядка 1-10 мкМ [Brogden K.A. Antimicrobial peptides: роге formers or metabolic inhibitors in bacteria? // Nat. Rev. Microbiol. - 2005. - Vol.3. - P.238-250].
Особое место занимают антимикробные пептиды, не содержащие в своем составе остатков цистеина, поскольку такая структурная особенность значительно облегчает их производство химическим или биотехнологическим путем и снижает себестоимость. Много внимания уделяется линейным пептидам, склонных к организации в амфипатическую α-спираль при контакте с мембранами, обсуждаются подходы к оптимизации их свойств с целью повышения терапевтического потенциала [Tossi A., Sandri L., Giangaspero A. Amphipathic, α-helical antimicrobial peptides // Biopolymers. - 2000. - Vol.55. - P.4-30].
В числе свойств, которые необходимо контролировать у потенциальных антибиотиков, - цитотоксическое действие на клетки макроорганизма, чаще оцениваемое в стандартных тестах на гемолитическую активность. Наличие подобной активности у целого ряда антимикробных пептидов является серьезным недостатком и ограничивает возможность их применения в качестве лекарственных средств.
Наиболее близким к заявляемым пептидам по структуре и антимикробным свойствам является пептид аденорегулин из кожи лягушки Phyllomedusa bicolor [Daly J.W. el al. Frog secretions and hunting magic in the upper Amazon: Identification of a peptide that interacts with an adenosine receptor // Proc. Natl. Acad. Sci. U.S.A. - 1992. - Vol.89. - P.10960-10963]. Этот пептид относится к группе дермасептинов, состоит из 33 аминокислотных остатков, полностью ингибирует рост некоторых бактерий в концентрациях 3-40 мкМ и не проявляет гемолитической активности при 80 мкМ [Mor A., Nicolas P. Isolation and structure of novel defensive peptides from frog skin // Eur. J. Biochem. - 1994. - Vol.219. - P.145-154].
Изобретение решает задачу расширения ассортимента антимикробных пептидов.
Поставленная задача решается за счет структуры пептида латарцина, имеющего следующую аминокислотную последовательность:
X1-Lys-Leu-X2-X3-X4-X5-X6-Arg-Lys-Ala-Ile-Ser-Tyr-Ala-Val-Lys-Lys-Ala-X7,
где X1 отсутствует, или является остатком глицина (Gly), или дипептида Phe-Gly, или трипептида Leu-Phe-Gly, или тетрапептида Gly-Leu-Phe-Gly; X2 - остаток глутамина (Gin) или изолейцина (Ile); Х3 - остаток аргинина (Arg) или лизина (Lys); X4 - остаток аргинина (Arg) или лизина (Lys); X5 - остаток лизина (Lys) или фенилаланина (Phe); Х6 - остаток глицина (Gly) или лейцина (Leu); X7 отсутствует, или является остатком аргинина (Arg), или дипептида Arg-Gly, или трипептида Arg-Gly-Lys, или тетрапептида Arg-Gly-Lys-His, или тетрапептида Arg-Gly-Lys-Asn.
Заявляемые пептиды проявляют антимикробную активность в отношении ряда грамположительных (Arthrobacter globiformis, Bacillus subtilis, Micrococcus luteus, Staphylococcus aureus) и грамотрицательных (Escherichia coli, Pseudomonas aeruginosa) бактерий, а также дрожжевых грибов (Pichia pastoris). Для полного ингибирования роста перечисленных организмов in vitro необходимы микромолярные концентрации пептидов. При этом некоторые латарцины характеризуются низкой гемолитической активностью и низкой цитотоксичностью в отношении нормальных лейкоцитов (эффекты отсутствуют при концентрации пептидов 45 мкМ). Кроме того, в микромолярных концентрациях латарцины проявляют выраженный токсический эффект по отношению к клеткам эритролейкемии человека. Техническим результатом предлагаемого изобретения является высокая антимикробная активность заявляемых пептидов.
Заявляемые латарцины состоят из 22-26 аминокислотных остатков, т.е. являются сравнительно небольшими молекулами, что упрощает их получение химическим синтезом. Кроме того, пептиды являются линейными и не содержат остатков цистеина, что также упрощает их получение химическим синтезом или биотехнологически, поскольку исключает риск образования неактивных форм за счет некорректного замыкания дисульфидов.
Пептид латарцин-2а (LtAMP-2a) получают из природного источника - яда среднеазиатского паука Lachesana tarabaevi Zonstein et Ovtchinnikov, 1999, который относится к семейству Zodariidae, отряду Araneae, классу Arachnida, типу Arthropoda.
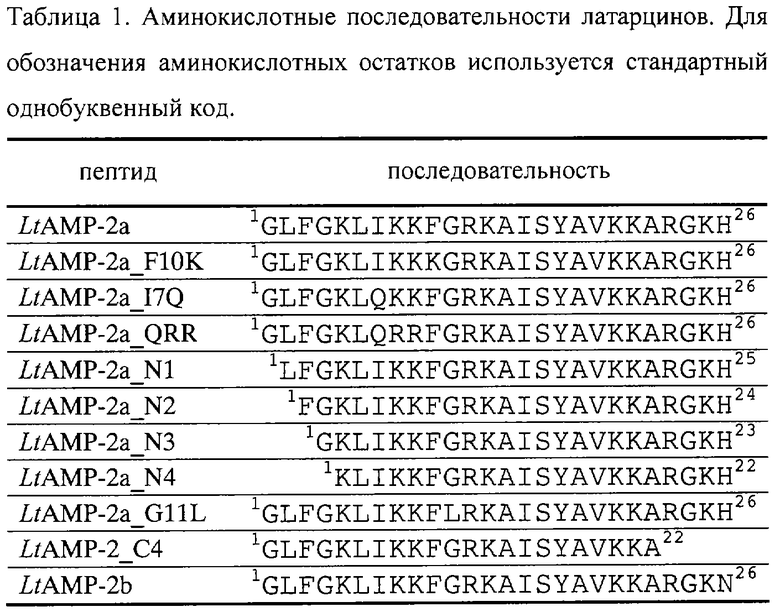
Пептиды латарцины LtAMP-2a, LtAMP-2a_F10K, LtAMP-2a_I7Q, LtAMP-2a_QRR, LtAMP-2a_N1, LtAMP-2a_N2, LtAMP-2a_N3, LtAMP-2a_N4, LtAMP-2a_G11L, LtAMP-2_C4, LtAMP-2b (см. табл.1) получают химическим синтезом, они являются гомологами и демонстрирует сходные биологические свойства.
Заявляемые пептиды представляют собой новые соединения и не являются близкими гомологами других белков или пептидов.
Изобретение иллюстрируют примеры.
Пример 1.
Выделение антимикробного пептида латарцина-2а (LtAMP-2a) из яда паука Lachesana tarabaevi.
Цельный яд паука Lachesana tarabaevi подвергают разделению по методу ВЭЖХ на колонке с обращенной фазой Jupiter С5 (2×150 мм, размер пор 300 Å, диаметр частиц 5 мкм, Phenomenex, США). Фракционирование проводят в линейном градиенте концентрации ацетонитрила от 0 до 60% (v/v) в 0,1%-ной (v/v) трифторуксусной кислоте в течение 60 минут со скоростью элюции 0,3 мл/мин. Детекцию осуществляют по оптическому поглощению при 210 нм. Полученные фракции тестируют на способность ингибировать рост Escherichia coli. Пептид LtAMP-2a элюируется с колонки в составе фракции со временем удерживания 37 минут (фиг. 1).
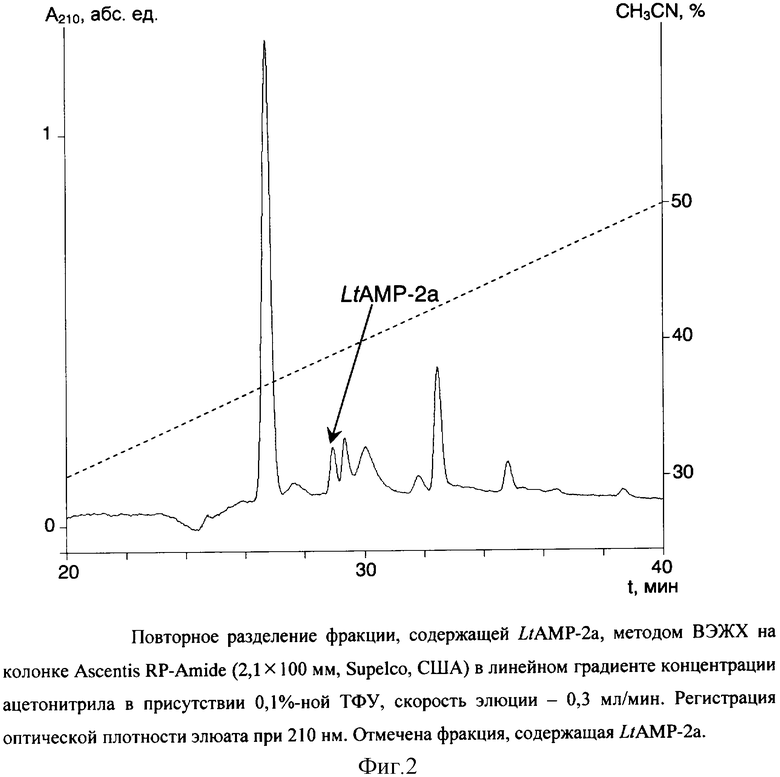
Выделенную фракцию далее разделяют по методу ВЭЖХ на колонке Ascends RP-Amide (2,1×100 мм, диаметр частиц 3 мкм, Supeico, США). Фракционирование проводят в линейном градиенте концентрации ацетонитрила от 10 до 60% (v/v) в 0,1%-ной (v/v) трифторуксусной кислоте в течение 50 минут со скоростью элюции 0,3 мл/мин. Детекцию осуществляют по оптическому поглощению при 210 нм. Полученные фракции тестируют на способность ингибировать рост Escherichia coli. Пептид LtAMP-2a элюируется с колонки со временем удерживания 29 минут (фиг. 2).
Содержание примесей в очищенной фракции, соответствующей LtAMP-2a, составляет 3%, что подтверждается разделением по методу ВЭЖХ на аналитической колонке Luna C18 (1×150 мм, размер пор 100 Å, диаметр частиц 3 мкм, Phenomenex, США) в линейном градиенте концентрации ацетонитрила от 20 до 50% (v/v) в 0,1%-ной (v/v) трифторуксусной кислоте в течение 40 минут со скоростью элюции 50 мкл/мин, детекцию осуществляют по оптическому поглощению при 210 нм.
Пример 2.
Установление аминокислотной последовательности латарцина-2а.
Определение N-концевой аминокислотной последовательности очищенного пептида LtAMP-2a проводят методом ступенчатой деградации по Эдману на автоматическом секвенаторе Precise 492 (Applied Biosystems, США). В результате устанавливают полную аминокислотную последовательность латарцина-2а, состоящую из 26 аминокислотных остатков:
H2N-Gly-Leu-Phe-Gly-Lys-Leu-Ile-Lys-Lys-Phe-Gly-Arg-Lys-Ala-Ile-Ser-Tyr-Ala-Val-Lys-Lys-Ala-Arg-Gly-Lys-His
Пример 3.
Определение относительной молекулярной массы латарцинов.
Индивидуальность очищенных веществ подтверждают масс-спектрометрическим анализом. Масс-спектры получают на MALDI-времяпролетном масс-спектрометре ultraflex II TOF/TOF (Bruker Daltonik, Германия), с идентификацией положительных ионов в рефлекторном режиме. В качестве матрицы используют α-циано-4-гидроксикоричную кислоту (10 мг/мл) в 50%-ном (v/v) ацетонитриле, содержащем 0,1%-ную (v/v) трифторуксусную кислоту. Для калибровки прибора используют стандартную смесь пептидов с диапазоном молекулярных масс 700-3500 Да (Sigma, США).
Измеренная моноизотопная молекулярная масса природного пептида LtAMP-2a составляет 2901,0 Да. Расчетная моноизотопная молекулярная масса пептида составляет 2900,8 Да, т.е. отличается от измеренной на 0,2 Да. Таким образом, латарцин-2а (LtAMP-2a) является линейным пептидом и не содержит каких-либо химических модификаций. Анализ аминокислотной последовательности латарцина-2а (распределение гидрофобных и гидрофильных остатков, общий заряд молекулы) позволяет предположить склонность этого пептида к образованию амфипатической α-спирали при взаимодействии с мембранами.
Пример 4.
Химический синтез латарцинов.
Пептид LtAMP-2a синтезируют твердофазным методом путем наращивания цепи с С-концевого остатка на 2-хлор-тритил-хлоридной (с нагрузкой 0,8-1,44 ммоль/г) смоле (PepChem, Германия), для временной защиты α-NH2-групп используют флуоренилметоксикарбонильную группу (Fmoc) [Chan W.C., White P.D. Fmoc Solid Phase Peptide Synthesis. - 2000. - University Press, Oxford]. Защиту боковых групп аминокислотных остатков выбирают с расчетом на конечное деблокирование трифторуксусной кислотой: для защиты боковых групп остатков Ser и Туг используют третбутильную группу, для Lys - третбутилоксикарбонильную группу, для His - тритильную группу, для Arg - 2,2,4,6,7-пентаметилдегидробензофуран-5-сульфонильную группу.
Для присоединения первой (С-концевой) аминокислоты к смоле 1,5 экв (по отношению к количеству активных групп на смоле) Fmoc-защищенной аминокислоты растворяют в дихлорметане (из расчета 10 мл дихлорметана на 1 г смолы) с 1,5 экв диизопропилэтиламина. К полученному раствору добавляют еще 1,5 экв диизопропилэтиламина и приливают к сухой смоле, мягко перемешивают в течение 45 мин. Непрореагировавшие активные группы на смоле блокируют метанолом (из расчета 1 мл метанола на 1 г смолы) в течение 20 мин, после чего смолу промывают тремя объемами дихлорметана, тремя объемами N,N-диметилформамида и тремя объемами этанола, высушивают под вакуумом. Аминокислотные остатки присоединяют к пептидил-полимеру с образованием гидроксибензотриазолового эфира в присутствии 1,3-диизопропилкарбодиимида, для активации 1 экв аминокислоты используют 1,2 экв N-гидроксибензотриазола и 1 экв 1,3-диизопропилкарбодиимида. Для наращивания полипептидной цепи в ходе каждого синтетического цикла проводят конденсацию пептидил-полимера с 5 экв активированной Fmoc-аминокислоты (1-12 часов при 37°С), содержание непрореагировавших аминогрупп контролируют визуально по окрашиванию рН-зависимого индикатора бромфенолового синего.
Отщепление продукта от 2-хлор-тритил-хлоридного полимера с одновременным деблокированием боковых групп проводят смесью трифторуксусной кислоты, воды и этандитиола (95:2,5:2,5, v/v/v) из расчета 1 мл смеси на 50 мг смолы. Суспензию перемешивают в течение 2 часов, затем раствор пептида в трифторуксусной кислоте отфильтровывают от полимера. Продукт высаживают 10-кратным избытком (по объему) охлажденного диэтилового эфира, отфильтровывают, дважды промывают эфиром, после чего высушивают лиофильно.
Синтезированный пептид подвергают очистке по методу ВЭЖХ на колонке с обращенной фазой Luna C18 (10×250 мм, размер пор 100 Å, диаметр частиц 10 мкм, Phenomenex, США). Фракционирование проводят в линейном градиенте концентрации ацетонитрила от 0 до 50% (v/v) в 0,1%-ной (v/v) трифторуксусной кислоте в течение 60 минут со скоростью элюции 2 мл/мин. Детекцию осуществляют по оптическому поглощению при 210 нм.
Содержание примесей в синтетическом препарате LtAMP-2a составляет 1%, что подтверждается разделением по методу ВЭЖХ на аналитической колонке Luna C18 (1×150 мм, размер пор 100 Å, диаметр частиц 3 мкм, Phenomenex, США) в линейном градиенте концентрации ацетонитрила от 20 до 50% (v/v) в 0,1%-ной (v/v) трифторуксусной кислоте в течение 40 минут со скоростью элюции 50 мкл/мин, детекцию осуществляют по оптическому поглощению при 210 нм.
Идентичность синтезированного LtAMP-2a природному доказывают при помощи масс-спектрометрического анализа, сравнением хроматографических подвижностей при разделении на аналитической колонке Luna C18 (1×150 мм, Phenomenex, США), а также сравнением биологических свойств.
Пептиды LtAMP-2a_F10K, LtAMP-2a_I7Q, LtAMP-2a_QRR, LtAMP-2a_N1, LtAMP-2a_N2, LtAMP-2a_N3, LtAMP-2a_N4, LtAMP-2a_G11L, LtAMP-2_C4, LtAMP-2b синтезируют аналогичным способом, внося необходимые аминокислоты. Для защиты боковых цепей Asn, Gin используют тритильную группу.
Пример 5.
Антимикробные свойства латарцинов.
Для определения антимикробной активности фракций, полученных в ходе хроматографического разделения компонентов яда паука Lachesana tarabaevi, очищенного латарцина-2а, а также синтетических латарцинов. используют следующие штаммы микроорганизмов: Arthrobacler globiformis BKM Ac-1112, Bacillus subtilis BKM В-501, Escherichia coli C600, Escherichia coli DH5α, Escherichia coli MH1, Pichia pastoris GS115, Pseudomonas aeruginosa PAO1, Staphylococcus aureus 209-P. Антимикробная активность оценивается по методу ингибирования роста культуры в жидкой среде. Определение минимальных концентраций пептидов, необходимых для полного ингибирования роста микроорганизмов (минимальных ингибирующих концентраций), проводят методом серийных разведений, используют модифицированную методику [Amsterdam D. Susceptibility testing of antimicrobials in liquid media // Loman V., ed. Antibiotics in laboratory medicine, 4th ed. - Williams and Wilkins, Baltimore. - 1996. - P.52-111].
Бактерии культивируют в жидкой низкосолевой среде LB (1% бакто-триптон, 0,5% бакто-дрожжевой экстракт, 0,5% NaCl, pH 7) при 37°С и перемешивании со скоростью 220 об/мин, дрожжи - в жидкой среде YPD (1% бакто-дрожжевой экстракт, 2% бакто-пептон, 2% глюкоза, pH 5,3) при 30°С и перемешивании со скоростью 150 об/мин в течение 18 ч. Полученные культуры разбавляют в 200 раз, используя те же среды, и выращивают в тех же условиях в течение 3-5 ч до достижения экспоненциальной фазы роста (оптическая плотность культуры при 620 нм OD620˜0,3-0,5), после чего снова разбавляют, используя исходные среды, до концентрации клеток 105 колоний образующих единиц в 1 мл. Культуры помещают в стерильные 96-луночные планшеты, по 90 мкл в лунку, куда затем добавляют по 10 мкл растворов тестируемых веществ различных концентраций, получаемых серийными разведениями. Отрицательным контролем служит культура клеток с добавлением 10 мкл чистой воды, положительным - чистая среда для культивирования. Планшеты инкубируют в условиях, описанных выше, в течение 24 ч для бактериальных культур и 48 ч для дрожжевых, после чего измеряют OD620, минимальные ингибирующие концентрации определяют как наименьшие концентрации веществ, полностью подавляющие рост микроорганизмов. Опыт проводят в трех независимых повторах.
Результаты определения минимальных ингибирующих концентраций для латарцина-2а представлены в таблице 2. Биологическая активность синтетического латарцина-2а идентична активности природного. Результаты для пептидов LtAMP-2a, LtAMP-2a_F10K, LtAMP-2a_I7Q, LtAMP-2a_QRR, LtAMP-2a_N1, LtAMP-2a_N2, LtAMP-2a_N3, LtAMP-2a_N4, LtAMP-2a_G11L, LtAMP-2_C4 представлены в таблице 3.
Антимикробные свойства латарцина LtAMP-2a.
Антимикробные свойства латарцинов.
В-501
Пример 6.
Тестирование латарцинов на гемолитическую активность.
Гемолитическую активность пептидов определяют с использованием крови здорового донора (группа В, Rh+). К 100 мкл свежей крови добавляют 900 мкл среды RPM1-1640, содержащей 2 мМ L-глутамин, 8% эмбриональной бычьей сыворотки (ЭБС) и гепарин (10 ед/мл). Определяют плотность клеток, после чего суспензию разводят средой RPM1-1640 до плотности 107 клеток/мл. К полученной суспензии добавляют тестируемый пептид нужной концентрации, в качестве отрицательного контроля используют клетки без добавления пептида. Инкубируют при 37°С и перемешивании со скоростью 120 об/мин в течение 3 ч, после чего клетки осаждают центрифугированием в течение 5 мин при 4000 g. 100 мкл супернатанта отбирают в стерильные 96-луночные планшеты, выход гемоглобина из эритроцитов оценивают по оптической плотности при 414 нм. Гемолитическая активность пептидов (см. табл. 4) выражается в % от максимально возможного гемолиза, максимально возможный лизис эритроцитов (положительный контроль) получают за счет ресуспендирования осажденных клеток в чистой воде до плотности 107 клеток/мл.
Цитотоксические свойства латарцинов.
** - активность отсутствует при концентрациях до 45 мкМ
# - эффективная концентрация, вызывающая 20% лизис
Пример 7.
Тестирование латарцинов на цитотоксичность по отношению к лейкоцитам и клеткам эритролейкемии человека.
Оценку цитотоксических свойств латарцинов для лейкоцитов человека проводят на фракции крови здорового донора (группа В, Rh+), обогащенной лейкоцитами, которую получают отстаиванием гепаринизированной (10 ед/мл) крови в течение 2 ч при 15°С в темноте. Отбирают фракцию выше эритроцитарного столба, соотношение лейкоцитов и эритроцитов в которой 1:10, добавляют 1,5 объема среды RPMI-1640, содержащей 2 мМ L-глутамин и 8% ЭБС. Клетки осаждают центрифугированием в течение 5 мин при 200 g, супернатант удаляют, клетки ресуспендируют в равном объеме среды RPMI-1640. Операцию повторяют дважды, после чего клетки рассаживают в 96-луночные плоскодонные культуральные планшеты (106 клеток/мл, 150 мкл среды RPMI-1640, содержащей 2 мМ L-Gln и 8% ЭБС, на лунку).
Клетки эритролейкемии человека К562 культивируют в среде RPMI-1640 с добавлением 2 мМ L-глутамина и 8% ЭБС при 37°С, в атмосфере 100%-ной влажности с 5%-ным содержанием CO2. За день до эксперимента клетки рассаживают в 96-луночные планшеты (106 клеток/мл).
В лунки вносят исследуемые пептиды в нужной концентрации, в качестве отрицательного контроля в лунки добавляют чистую воду. Клетки (К562 и лейкоциты) инкубируют с различными концентрациями пептидов в течение 3 ч при 37°С, затем в лунки вносят флуоресцентные красители Hoechst33342 (20 мкМ, окрашивает ядра всех клеток) и пропидиум иодид (20 мкМ, окрашивает ядра мертвых клеток) и через 15 мин регистрируют флуоресцентные изображения клеток с помощью инвертированного флуоресцентного микроскопа Axiovert 200M (Zeiss, Германия) с цифровой камерой AxioCam MRc (Zeiss, Германия) в области флуоресценции Hoechst33342 (фильтры на возбуждение - ВР 365/12, на эмиссию - LP 397) и в области флуоресценции пропидиум иодида (фильтры на возбуждение - ВР 510-560, на эмиссию - LP 590). По этим изображениям для каждой концентрации пептида подсчитывают общее число клеток (1000 клеток на одно измерение) и число мертвых клеток среди них, а затем рассчитывают концентрацию пептида, вызывающую гибель 50% клеток, ИК50. Результаты (см. табл.4, фиг.3) усредняют по трем независимым экспериментам.
| название | год | авторы | номер документа |
|---|---|---|---|
| ПЕПТИДЫ ЛАТАРЦИНЫ, ПРОЯВЛЯЮЩИЕ АНТИМИКРОБНУЮ АКТИВНОСТЬ | 2006 |
|
RU2319745C1 |
| ПЕПТИДЫ ЛАТАРЦИНЫ, ПРОЯВЛЯЮЩИЕ АНТИМИКРОБНУЮ АКТИВНОСТЬ | 2005 |
|
RU2302466C1 |
| ПЕПТИДЫ, ПРОЯВЛЯЮЩИЕ АНТИМИКРОБНУЮ АКТИВНОСТЬ | 2005 |
|
RU2302425C2 |
| ПЕПТИДЫ ЛАТАРЦИНЫ, ПРОЯВЛЯЮЩИЕ АНТИМИКРОБНУЮ АКТИВНОСТЬ | 2005 |
|
RU2302467C1 |
| СПОСОБ ПОЛУЧЕНИЯ АНТИМИКРОБНЫХ ПЕПТИДОВ С ПОНИЖЕННОЙ ГЕМОЛИТИЧЕСКОЙ АКТИВНОСТЬЮ | 2006 |
|
RU2316336C1 |
| УСОВЕРШЕНСТВОВАННЫЙ СПОСОБ ПОЛУЧЕНИЯ ПРЕДШЕСТВЕННИКА ИНСУЛИНА С ПРАВИЛЬНО СОЕДИНЕННЫМИ ЦИСТИНОВЫМИ МОСТИКАМИ | 1998 |
|
RU2205836C2 |
| СПОСОБ ПОЛУЧЕНИЯ ИНСУЛИНА ИЛИ ПРОИЗВОДНЫХ ИНСУЛИНА С ПРАВИЛЬНО СОЕДИНЕННЫМИ ЦИСТИНОВЫМИ МОСТИКАМИ | 2002 |
|
RU2302882C2 |
| ПЛАЗМИДНЫЙ ВЕКТОР pET-His8-TrxL-Acip1, ШТАММ БАКТЕРИИ Escherichia coli BL21(DE3)/pET-His8-TrxL-Acip1 ДЛЯ ЭКСПРЕССИИ АНТИМИКРОБНОГО ПЕПТИДА АЦИПЕНСИНА-1 И СПОСОБ ПОЛУЧЕНИЯ УКАЗАННОГО ПЕПТИДА | 2015 |
|
RU2580031C2 |
| ПОЛИПЕПТИДЫ ЛИЗИНА, АКТИВНЫЕ ПРОТИВ ГРАМОТРИЦАТЕЛЬНЫХ БАКТЕРИЙ | 2016 |
|
RU2724545C2 |
| ПРОИЗВОДНЫЕ ПЕПТИДОВ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 1992 |
|
RU2087480C1 |


Изобретение относится к химико-фармацевтической промышленности, и касается биологически активных пептидов, обладающих антимикробным действием, которые могут найти применение в биотехнологии и медицине. Изобретение решает задачу расширения ассортимента антимикробных пептидов с общей формулой (1) X1-Lys-Leu-X2-X3-X4-X5-X6-Arg-Lys-Ala-Ile-Ser-Tyr-Ala-Val-Lys-Lys-Ala-Х7 (1), за счет модификации исходной структуры пептида латарцина, при этом в (1) X1 отсутствует, или является остатком глицина (Gly), или дипептидом Phe-Gly, или трипептидом Leu-Phe-Gly, или тетрапептидом Gly-Leu-Phe-Gly; X2 - остаток глутамина (Gln) или изолейцина (Ile); Х3 - остаток аргинина (Arg) или лизина (Lys); X4 - остаток аргинина (Arg) или лизина (Lys); X5 - остаток лизина (Lys) или фенилаланина (Phe); Х6 - остаток глицина (Gly) или лейцина (Leu); X7 отсутствует, или является остатком аргинина (Arg), или дипептидом Arg-Gly, или трипептидом Arg-Gly-Lys, или тетрапептидом Arg-Gly-Lys-His, или тетрапептидом Arg-Gly-Lys-Asn. 4 табл., 3 ил.
Пептид латарцин, проявляющий антимикробную активность, имеющий следующую аминокислотную последовательность:
X1-Lys-Leu-X2-X3-X4-X5-X6-Arg-Lys-Ala-Ile-Ser-Tyr-Ala-Val-Lys-Lys-Ala-X7,
где X1 отсутствует или является остатком глицина (Gly), или дипептидом Phe-Gly, или трипептидом Leu-Phe-Gly, или тетрапептидом Gly-Leu-Phe-Gly; Х2 - остаток глутамина (Gln) или изолейцина (Ile); Х3 - остаток аргинина (Arg) или лизина (Lys); X4 - остаток аргинина (Arg) или лизина (Lys); Х5 - остаток лизина (Lys) или фенилаланина (Phe); Х6 - остаток глицина (Gly) или лейцина (Leu); X7 отсутствует или является остатком аргинина (Arg), или дипептидом Arg-Gly, или трипептидом Arg-Gly-Lys, или тетрапептидом Arg-Gly-Lys-His, или тетрапептидом Arg-Gly-Lys-Asn.
| Daly J.W | |||
| el al | |||
| Frog secretions and hunting magic in the upper Amazon: Identification of a peptide that interacts with an adenosine receptor | |||
| // Proc | |||
| Natl | |||
| Acad | |||
| Sci | |||
| U.S.A | |||
| Пуговица для прикрепления ее к материи без пришивки | 1921 |
|
SU1992A1 |
| Способ размножения копий рисунков, текста и т.п. | 1921 |
|
SU89A1 |
| Приспособление к молотилкам для очистки зерна и удаления пыли | 1925 |
|
SU10960A1 |
| ПЕПТИД, ОБЛАДАЮЩИЙ БИОЦИДНОЙ АКТИВНОСТЬЮ | 2000 |
|
RU2183643C1 |
| ПОЛИПЕПТИДЫ ИЛИ ИХ СОЛИ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 1992 |
|
RU2083589C1 |
| АЛЛОФЕРОНЫ-ИММУНОМОДУЛИРУЮЩИЕ ПЕПТИДЫ | 1999 |
|
RU2172322C1 |
| RU 2002112327/13 A1, 20.11.2003. | |||
Авторы
Даты
2007-09-20—Публикация
2006-05-15—Подача