Изобретение относится к области медицины, в частности к медицинским моделям, используемым для исследования костной ткани в ортопедии и травматологии для восстановления поврежденных сегментов конечностей, кроме того, может использоваться в ветеринарии для лечения травм костей у животных.
Известен способ стимуляции репаративной регенерации костной ткани путем многократного воздействия на больной участок конечности в послеоперационный период электромагнитными колебаниями, при этом воздействие осуществляется бесконтактным способом путем помещения больного участка конечности в электромагнитное поле элемента воздействия (Заявка №2002129633, РФ. Опубл. 27.04.2004).
Известен способ стимуляции регенерации костной ткани, включающий остеоперфорацию шейки бедра, при котором производят остеоперфорацию метафиза и шейки бедренной кости до снижения внутрикостного давления на 15% от исходного (Заявка №2002125305, РФ. Опубл. 27.03.2004).
Известен состав для стимуляции регенерации костных тканей, содержащий, мас.%: биосовместимый рассасывающийся сополимер винилпирролидона с акрилатом 65,0-85,0, порошкообразные лиофилизированные фетаткани 5,0-15,0, лекарственное вещество, способствующее регенерации тканей, 5,0-15,0, вещество, содержащее связанный кальций, 5,0-15,0, которые обеспечивают ускорение регенерации костной ткани при заполнении костных полостей и при осуществлении операций по удлинению конечностей (Пат. №2146928, РФ. Опубл. 27.03.2000).
Известен препарат для стимулирования физиологической и репаративной регенерации "Стимбон-1", стимулирующий физиологическую и репаративную регенерацию, который получают из зрелой костной ткани животных путем декальцинации очищенной от мягких тканей измельченной кости соляной кислотой, экстрагирования неколлагеновых белков раствором мочевины, освобождения от водонерастворимых белков путем диализа против воды, фракционирования по высаливаемости сульфатом аммония, молекулярной массе и сродству к ионообменникам (Пат. №2050158, РФ. Опубл. 20.12.1995).
Известен способ стимуляции посттравматической частичной регенерации конечностей, хвоста и кожи у млекопитающих, при котором травмированный орган помещают в 0,9%-ный раствор поваренной соли и проводят замену раствора 2 раза в сутки до полной эпителизации раны, при этом физиологический раствор поваренной соли оказывает выраженное стимулирующее влияние на процесс регенерации кожи и костно-хрящевых образований у экспериментальных животных (Пат. №2053775, РФ. Опубл. 10.02.1996).
Известна мембрана для использования при направленной регенерации тканей для стимуляции костеобразования в стоматологии, содержащая матриксный и барьерный слои, применяемая для лечения дефектов костей и хрящей в теле человека и животных, которую накладывают на дефект и ориентируют так, что барьерный слой или слои предотвращают врастание нежелательных тканей в зону регенерации кости или хряща (Заявка №2000109319, РФ (аналог GB 98/02976, заявлено: 05.10.1998). Опубл. 20.02.2003).
Известно экспериментальное применение трубки из политетрафторэтилена, надеваемой на отломки кости, при этом интерпозиция мягких тканей в область дефекта не допускается (Nyman R. et al. // Acta Orthop. Scand. - 1995. - №2. - P.169-173).
Однако в известном способе из-за отсутствия остеоиндуктивных свойств у политетрафторэтилена и методики имплантации происходит образование замыкательных пластинок на концах костных отломков и замещения дефекта не происходит.
Задачей настоящего изобретения является разработка способа моделирования стимуляции регенерации костной ткани, в котором создают условия для восстановления анатомической целостности кости при ее значительном повреждении.
Поставленная задача решается тем, что в способе моделирования стимуляции регенерации костной ткани, включающем отграничение области повреждения длинной трубчатой кости пленкой, зачищают концы костных фрагментов от надкостницы на 5-7 мм выше опилов, используют пленку, изготовленную из динитроцеллюлозы, которую накладывают циркулярно с перекрытием зачищенных концов костных фрагментов, после чего пленку плотно сшивают нитями вдоль линии стыка, концы костных фрагментов фиксируют устройством для чрескостного остеосинтеза и оставляют в условиях нейтрального чрескостного остеосинтеза.
Настоящее изобретение поясняют подробным описанием, экспериментальным примером выполнения способа и иллюстративным материалом в виде рентгенограмм, на которых:
Фиг.1 - Рентгенограмма в день операции, на которой просматривается область дефекта, при этом мембрана из динитроцеллюлозы, отграничивающая дефект от окружающих тканей, не видна, так как она не рентгеноконтрастна.
Фиг.2 - Рентгенограмма через 14 суток эксперимента. Отграниченный мембраной из динитроцеллюлозы дефект, в котором видны оссифицированные гомогенные тени проксимального и дистального костных отделов регенерата в форме полусферических колпачков, растущие из костно-мозговой полости фрагментов кости, занимающие большую часть диастаза. Высота дистального отдела превышает высоту проксимального примерно в три раза, его поперечник незначительно больше поперечника проксимального костного фрагмента.
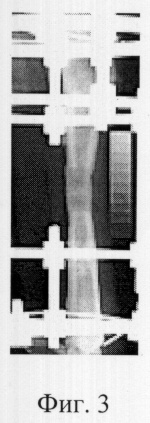
Фиг.3 - Рентгенограмма через 60 суток эксперимента. Отграниченный мембраной из динитроцеллюлозы дефект, полностью заполненный новообразованной костной тканью. Проксимальный и дистальный костные отделы регенерата срослись между собой, хорошо видна линия стыка, регенерат стал единым, линии опилов костных фрагментов нечеткие, размытые. В основаниях регенерата видны участки просветления, характеризующие формирование костно-мозговой полости регенерата, периферические отделы регенерата уплотнены, что связано с формированием корковой пластинки регенерата.
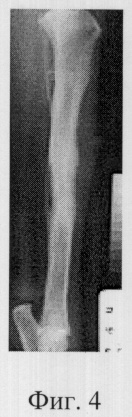
Фиг.4 - Рентгенограмма через 180 суток эксперимента. В области дефекта виден новообразованный участок кости. Поперечник материнской кости восстановлен, сформирована единая костно-мозговая полость, суженная в центре, корковая пластинка регенерата утолщена.
Способ осуществляют следующим образом.
В условиях операционной экспериментальному животному под внутривенным барбитуровым наркозом через боковые разрезы производят резекцию участков берцовых костей относительной длинной 1,5-2,0 поперечника большеберцовой кости в центральной части диафиза. С концов костных фрагментов на 5-7 мм выше опилов удаляют надкостницу. Область дефекта закрывают циркулярно пленкой из динитроцеллюлозы. Концы костных фрагментов оборачивают пленкой на высоту 5-7 мм от торцовых поверхностей и по линии стыка плотно закрепляют нитями. Фиксируют проксимальный и дистальный костные фрагменты в аппарате для чрескостного остеосинтеза. Рану послойно ушивают.
На этапах эксперимента (день операции, 14-е, 60-е, 180-е сутки) выполняют рентгенологические исследования.
Пример выполнения способа.
История болезни №182, животное №5413, возраст 2 года, вес 18 кг, длина голени 15 см.
В условиях операционной у наркотизированного животного провели обработку операционного поля 5% спиртовым раствором йода. От пленки из динитроцеллюлозы вырезали лоскут необходимой величины. Перед операцией его поместили в раствор муравьиной кислоты с массовой долей 2,4%. Из разрезов с латеральной и медиальной поверхностей в центральной части голени резецировали поперечно участки диафизов берцовых костей протяженностью 20 мм. С концов костных фрагментов скальпелем соскоблили надкостницу на протяжении 5 мм от опилов костей. Область дефекта закрыли циркулярно пленкой из динитроцеллюлозы. Концы костных фрагментов обернули пленкой на высоту 5 мм от торцовых поверхностей и на стыке продольно закрепили нитями. Фиксировали проксимальный и дистальный костные фрагменты в метафизарных областях с помощью спиц, концы которых закрепили в опорах аппарата для чрескостного остеосинтеза. Рану послойно ушили (Фиг.1).
На рентгенограмме к 14-м суткам после операции в дефекте появлялись гомогенные тени проксимального и дистального костных отделов регенерата в виде полусферических колпачков, которые выступали из костно-мозговой полости фрагментов. Высота проксимального костного отдела регенерата достигала 9,0 мм, при этом она в 3 раза превышала высоту дистального. Поперечник проксимального отделов регенерата был шире диаметра костных фрагментов (Фиг.2). К 21-м суткам отмечали увеличение высоты преимущественно дистального оссифицированного отдела регенерата. К 28-м суткам после операции большая часть диастаза между фрагментами была заполнена новообразованной костной тканью гомогенной структуры, костные отделы разделяла узкая (высотой 2,0-3,0 мм) неоссифицированная зона. При этом дистальный отдел регенерата приближался по высоте к проксимальному. Между оссифицированными отделами регенерата появлялись соединяющие их костные "мостики". Через 60 суток после операции оссифицированные отделы регенерата полностью соединялись между собой. Линии опилов фрагментов нечеткие, размытые. В основаниях костных отделов регенерата появлялись участки просветления, периферические отделы регенерата уплотнялись. В области стыка проксимального и дистального отделов наступало костное сращение, позволявшее снять аппарат. После снятия аппарата происходила органотипическая перестройка костной ткани в новообразованном участке диафиза (Фиг.3). К 180 суткам после операции поперечник кости восстанавливался, сформировалась единая костно-мозговая полость, суженная в центре, корковая пластинка регенерата была утолщена (Фиг.4).
Предлагаемый способ позволяет эффективно предотвратить врастание окружающих мягких тканей в область повреждения кости. Используемая мембрана из динитроцеллюлозы создает отграничивающий эффект на время, достаточное для роста и созревания новообразованной костной ткани.
Кроме того, восстановленная анатомическая целостность кости обладает достаточной механической жесткостью и прочностью, зона дефекта изолирована от параоссальных тканей нерассасывающейся пленкой.
Предлагаемый способ создает условия для активизации репаративных процессов в месте повреждения длинной кости (значительных костных дефектов диафиза) путем стабильной фиксаций костных фрагментов.
Положительный результат, полученный в эксперименте на собаках, позволяет говорить о возможности клинических испытаний нашего способа при лечении больных с сегментарными дефектами длинных трубчатых костей.
Предложенный способ может иметь возможности дальнейшего клинического применения в сочетании с другими способами управления репаративным остеогенезом.
Кроме того, предлагаемый способ доступен (можно применять любую компьютерную программу, работающую с геометрическими характеристиками объекта) и прост для выполнения, не требует использования дорогостоящей аппаратуры, основан на анализе рентгенологического материала, который можно получить практически в любом лечебном учреждении. Точность диагностики делает возможным использование способа не только в эксперименте, но и при выборе корректной тактики для проведения хирургических.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ МОДЕЛИРОВАНИЯ ЗАМЕЩЕНИЯ ДЕФЕКТА ДЛИННОЙ ТРУБЧАТОЙ КОСТИ | 2003 |
|
RU2281050C2 |
| СПОСОБ МЕХАНИЧЕСКОЙ СТИМУЛЯЦИИ ЗАМЕДЛЕННОГО ОСТЕОГЕНЕЗА ПРИ ПЕРЕЛОМАХ КОСТЕЙ | 2007 |
|
RU2354322C1 |
| СПОСОБ МОДЕЛИРОВАНИЯ СТИМУЛЯЦИИ РЕПАРАТИВНОГО ОСТЕОГЕНЕЗА ЭКСТРАКТОМ КЛЕТОК ФЕТАЛЬНОЙ КОСТНОЙ ТКАНИ | 2010 |
|
RU2433794C2 |
| СПОСОБ СТИМУЛЯЦИИ РЕПАРАТИВНОГО ОСТЕОГЕНЕЗА | 1998 |
|
RU2193868C2 |
| СПОСОБ СТИМУЛЯЦИИ ПЕРИФЕРИЧЕСКОГО КРОВООБРАЩЕНИЯ И УСТРОЙСТВО ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ | 1995 |
|
RU2102025C1 |
| СПОСОБ ЗАМЕЩЕНИЯ ДЕФЕКТОВ ДЛИННЫХ КОСТЕЙ | 1998 |
|
RU2157129C2 |
| СПОСОБ ЭКСПЕРИМЕНТАЛЬНОГО МОДЕЛИРОВАНИЯ ЗАМЕДЛЕННОГО ДИСТРАКЦИОННОГО ОСТЕОГЕНЕЗА ПРИ УКОРОЧЕНИИ КОСТЕЙ КОНЕЧНОСТЕЙ | 2011 |
|
RU2463668C1 |
| СПОСОБ МОДЕЛИРОВАНИЯ ЗАМЕДЛЕННОГО ОСТЕОГЕНЕЗА | 2005 |
|
RU2301457C2 |
| СПОСОБ УДЛИНЕНИЯ КОНЕЧНОСТИ | 2002 |
|
RU2235519C2 |
| СПОСОБ ОЦЕНКИ СТЕПЕНИ РОСТА КОСТНОГО РЕГЕНЕРАТА | 2003 |
|
RU2270606C2 |


Изобретение может быть применимо для моделирования стимуляции регенерации костной ткани. Зачищают концы костных фрагментов от надкостницы. Накладывают пленку, изготовленную из динитроцеллюлозы, циркулярно с перекрытием зачищенных концов костных фрагментов. Сшивают пленку продольно по линии ее стыка нитями. Фиксируют костные фрагменты в условиях чрескостного остеосинтеза. Способ позволяет стимулировать репаративные процессы в условиях значительных дефектов кости. 4 ил.
Способ моделирования стимуляции регенерации костной ткани, включающий отграничение области повреждения длинной трубчатой кости пленкой, отличающийся тем, что зачищают концы костных фрагментов от надкостницы, применяют пленку, изготовленную из динитроцеллюлозы, которую накладывают циркулярно с перекрытием зачищенных концов костных фрагментов, после чего пленку продольно сшивают по линии ее стыка нитями, фиксацию костных фрагментов производят в условиях чрескостного остеосинтеза.
| NYMAN R | |||
| Membrane-guided bone regeneration | |||
| Segmental radius defects studied in the rabbit | |||
| Топка с качающимися колосниковыми элементами | 1921 |
|
SU1995A1 |
| Пленкообразующая композиция | 1985 |
|
SU1540830A1 |
| СПОСОБ ЛЕЧЕНИЯ ПОВРЕЖДЕНИЙ СУХОЖИЛИЙ СГИБАТЕЛЕЙ ПАЛЬЦЕВ КИСТИ | 1998 |
|
RU2155007C2 |
| RU 2053725 C1, 10.02.1996 | |||
| ЛОПУХИН Ю.М | |||
| Экспериментальная хирургия | |||
| М., «Медицина», 1971, с.278, 211 | |||
| JP 2002325830, 12.11.2002 | |||
| АРТЮШКЕВИЧ А.С | |||
| и др. | |||
Авторы
Даты
2007-10-27—Публикация
2005-01-11—Подача