Изобретение относится к области медицины, в частности к способам лечения опорно-двигательного аппарата и научным медицинским моделям, а именно предназначено для стимуляции остеогенеза трубчатых костей в области их повреждения.
Известен способ заживления костных дефектов, в котором создают круглые сквозные костные дефекты по обеим сторонам челюсти, один из них закрывают мембраной из пористого политетрафлюороэтилена, на 2-3 мм превышающей размер отверстия, затем фиксируют ее по краю отверстия шелком (Christer Dahlin, Anders Linde, Jan Gottlow, Sture Nyman;. Healing of bone defects by guided tissue regeneration; Plast. Reconstr. Surg. - 1988.- Vol.81, № 5. -p.672-676).
Известен способ замещения дефектов с использованием коллагеновой мембраны, которую устанавливают для отграничения зоны остеотомии от параоссальных тканей (Mundell RD, Mooney MP, Siegel MI, Losken A; Osseous guided tissue regeneration using a collagen barrier membrane; J Oral Maxillofac Surg. 1993 Sep; 51(9): 1004-12).
Известен способ замещения дефектов длинных трубчатых костей, в котором для предотвращения врастания мягких тканей в 10-миллиметровый дефект лучевой кости применялся кусочек силиконовой мембраны, сшитой в виде трубки (Lu S, Zhang Z, Wang J; Guided bone regeneration in long bone. An experimental study; Chin Med J (Engl.) 1996 Jul; 109(7): 551-4).
Известно экспериментальное применение рассасывающихся мембран для остеорегенерации при закрытии сквозного дефекта альвеолярного отростка верхней челюсти, при котором костный дефект закрывали мембраной различной толщины (Юлова Н.А., Воложин А. И., Рогинский В.В.; Экспериментальное обоснование применения рассасывающихся мембран для остеорегенерации при закрытии сквозного дефекта альвеолярного отростка верхней челюсти; Биомедицинские технологии. - Вып.9, Труды научно-исследовательского и учебно-методического центра биомедицинских технологий ВИЛАР, 1998).
Известен способ замещения дефектов лучевой кости с использованием мембраны, в котором дефект закрывался мембранным барьером из расширяющегося тефлона в форме трубки (O'Brien WD, Mishkin DJ, Engler WO, Miller MC, Neville BW; Guided tissue regeneration using a biodegradable barrier membrane for new attachment: a clinical, histologic, and histometric study in dogs; Int. J Periodontics Restorative Dent 1995 Oct; 15(5): 446-61).
Однако в известном способе после заполнения дефекта костной тканью необходимо повторное оперативное вмешательство для удаления мембраны, изготовленной из нерассасывающегося материала.
В известном из уровня техники решении костные дефекты заполняют деминерализованным брефотрансплантатом и перорально вводят препарат «Дона». При его выполнении костные дефекты заполняют деминерализованным ортотопическим брефотрансплантатом, длина и толщина которого соответствовуют размерам удаленного костного фрагмента, а фиксация его с концами опилов материнской кости осуществлялась с помощью металлических штифтов, также фиксация фрагментов трубчатой кости осуществляется гипсовой повязкой или в опорах аппарата для наружной фиксации, с первого дня после операции перорально вводят препарат «Дона» (Пат. РФ 2180534. Опубл.20.03.2002 г.).
Однако известное решение создает эффект стимуляции репаративной регенерации за счет заполнения дефекта кости костным деминерализованным брефотрансплантатом и позволяет ускорить процесс созревания костной ткани за счет применения препарата «Дона». Оно не предназначено для создания оптимальных условий для репаративной регенерации костной ткани, для стимулирования процесса остеогенеза посредством отграничения области дефекта длинной трубчатой кости от параоссальных тканей рассасывающимся материалом. При этом возможности получения брефотрансплантатов ограничены, процесс их заготовки и обработки дорогостоящий.
Известен способ моделирования замещения дефекта длинной трубчатой кости в котором для изготовления имплантанта в виде цилиндрической трубки использовали деминерализованный костный матрикс (Пат. РФ 21218115. Опубл.20.11.1998 г.).
Однако известный способ, при выполнении которого трубку размещают в костномозговом канале на длину одного диаметра трубки, является достаточно травматичным, так как в момент введения имплантанта происходит нарушение васкуляризации и разрушение структур костномозговой полости. Деминерализованный трубчатый имплантант не обладает достаточной прочностью и жесткостью для использования при замещении дефектов у более крупных биологических объектов в связи с высокой механической нагрузкой, обусловленной весом тела. Кроме того, изготовление деминерализованного имплантанта в форме трубки трудоемко и требует наличие специального инструментария.
Он обеспечивает органотипическую регенерацию трубчатой кости при ее дефекте, что достигается подготовкой и помещением перфорированного деминерализованного имплантанта в виде полого цилиндра (трубки) в костный дефект.
Известен способ замещения дефекта длинной трубчатой кости, включающий изоляцию области костного дефекта от окружающих параоссальных тканей путем размещения между костными фрагментами мембраны в виде трубки (муфты), выполненной из консервированной аллокости, и фиксацию костных фрагментов (Белоусов В.Д. и др. Консервативное лечение ложных суставов длинных трубчатых костей.-Кишинев. -ШТИИНЦА. -1990. -c.58).
Однако известный способ замещения дефекта длинной трубчатой кости предназначен не для моделирования, а для лечения дефекта кости, кроме того отсутствие фиксации чрескостным аппаратом не позволяет создать условия для изучения процесса репаративной регенерации костной ткани и его стимуляции, в условиях отграничения области дефекта от окружающих тканей.
Задачей настоящего изобретения является разработка способа моделирования условий для стимуляции роста новообразованной костной ткани посредством отграничения области дефекта длинной трубчатой кости рассасывающимся материалом.
Поставленная задача решается тем, что в способе моделирования замещения дефекта длинной трубчатой кости, включающем отграничение области костного дефекта от окружающих параоссальных тканей мембраной в виде трубки, мембрану изготавливают из формалинизированной трубчатой аллокости, длина и наружный диаметр которой равны длине дефекта и диаметру костных фрагментов, затем мембрану устанавливают между фрагментами трубчатой кости, которые фиксируют в опорах аппарата наружной чрескостной фиксации.
Целесообразно для центрации и предотвращения смещения мембраны относительно оси фрагментов кости концы костных фрагментов ввести в мембрану, при этом ее длина должна быть более длины дефекта, а внутренний диаметр должен соответствовать диаметру костных фрагментов.
Настоящее изобретение поясняют подробным описанием, экспериментальным примером выполнения способа и иллюстративным материалом, на котором:
Фиг.1 - схема модели оперативного вмешательства, в котором использована мембрана из трубчатой аллокости, длина которой соответствует длине дефекта трубчатой кости, а ее диаметр - диаметру костных фрагментов;
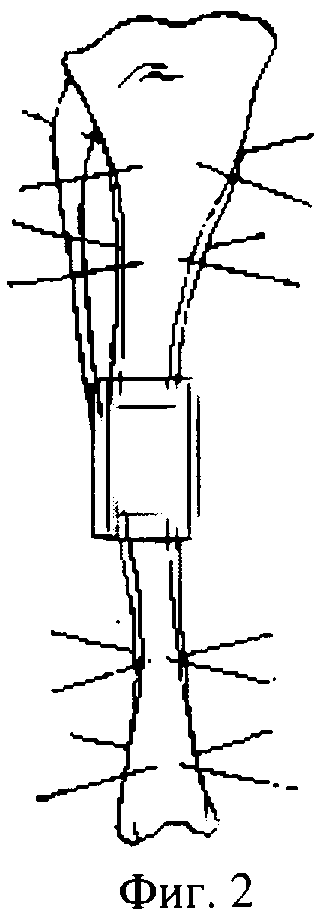
Фиг.2 - схема модели оперативного вмешательства, в котором использована мембрана из трубчатой аллокости, длина которой превышает на 2-6 мм длину дефекта трубчатой кости, а внутренний диаметр мембраны соответствует диаметру костных фрагментов;
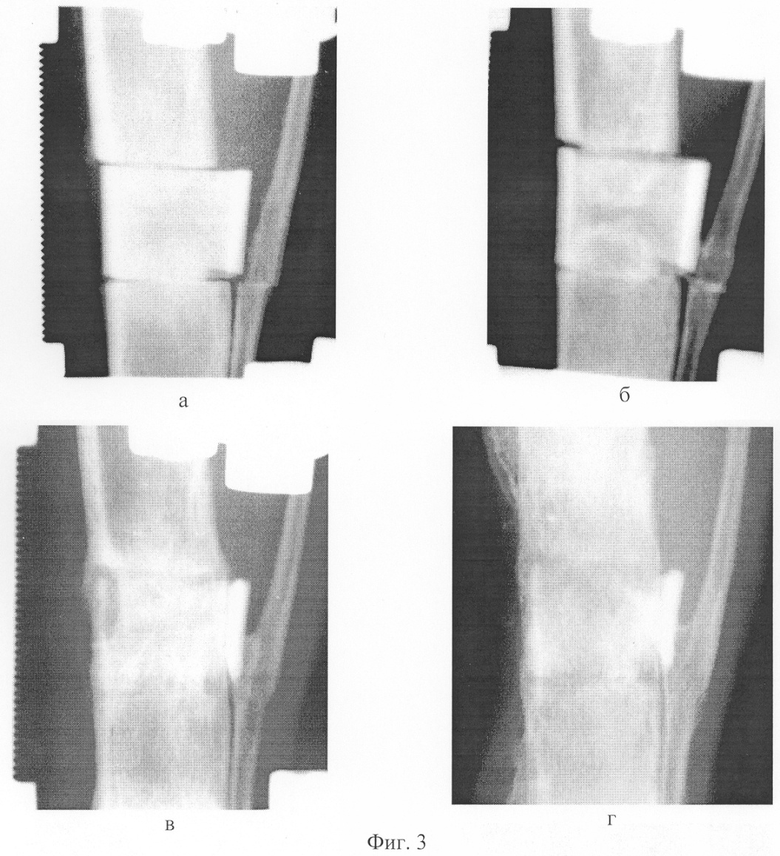
Фиг.3 - рентгенограммы на этапах моделирования замещения дефекта длинной трубчатой кости с использованием мембраны из трубчатой аллокости, длина которой соответствует длине дефекта трубчатой кости, а ее диаметр - диаметру костных фрагментов;
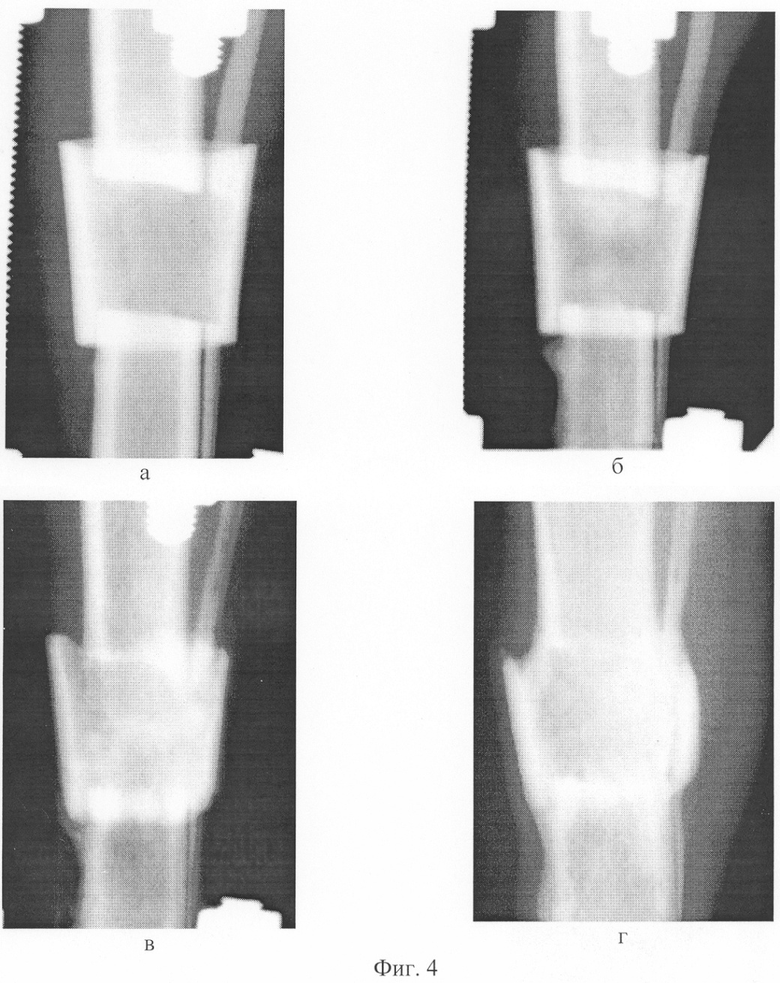
Фиг.4 - рентгенограммы на этапах моделирования замещения дефекта длинной трубчатой кости с использованием мембраны из трубчатой аллокости, длина которой превышает на 6 мм длину дефекта трубчатой кости, а внутренний диаметр мембраны соответствует диаметру костных фрагментов.
Способ осуществляют следующим образом.
Мембраны заготавливают из рассасывающегося материала, например из диафизов трубчатых костей, в нестерильных условиях. Заготовленные таким способом мембраны помещают в раствор формалина (консервант), который готовят следующим образом: к 10 мл 10% раствора формалина добавляют 90 мл дистиллированной воды.
Мембраны помещают в сосуд с консервантом с таким расчетом, чтобы объем консерванта превышал их объем. Флаконы с мембранами из трубчатой аллокости хранят при комнатной температуре. Через 30 дней трубчатая аллокость, консервированная в растворе формалина (формалинизированная) готова к применению. Трубчатые аллокости различной длины и диаметра, обработанные аналогичным образом, используют для создания банка мембран.
В условиях операционной животному под общим барбитуровым наркозом после обработки операционного поля 5% спиртовым раствором йода на голень накладывают аппарат для чрескостного остеосинтеза (далее аппарат) с фиксацией проксимального и дистального концов кости. Из двух боковых разрезов с латеральной и медиальной сторон в средней трети голени чрезнадкостнично пилой Джигли резецируют поперечно участки диафизов берцовых костей. Между проксимальным и дистальным фрагментами большеберцовой кости устанавливают мембрану из рассасывающегося материала, например из трубчатой аллокости, в форме трубки. Трубчатую аллокость необходимой длины и диаметра, которые соответствуют длине дефекта и диаметрам проксимального и дистального костных фрагментов на уровне опилов, выбирают из банка мембран.
Для центрации и предотвращения смещения мембраны целесообразно выполнять ее из рассасывающегося материала, например из трубчатой аллокости кости, внутренний диаметр которой соответствует диаметру костных фрагментов и длина которой превышает длину дефекта на 2-6 мм.
Из банка мембран выбирают мембрану, превышающую на 2 - 6 мм длину дефекта с внутренним диаметром, соответствующим диаметру костных фрагментов. На голень накладывают аппарат и осуществляют резекцию участков диафизов берцовых костей. Удаляют резьбовые стержни между проксимальной и дистальной опорами аппарата. На концы костных фрагментов надевают мембрану из рассасывающегося материала, например из трубчатой аллокости. Резьбовые стержни устанавливают в исходное положение. На мягкие ткани послойно накладывают швы.
Аппарат снимают при рентгенологически определяемом сращении проксимального и дистального костных отделов регенерата. Основными показателями для снятия аппарата являются результаты клинической пробы, которую осуществляют следующим образом: удаляют резьбовые стержни, соединяющие между собой подсистемы аппарата. На кость прикладывают осторожные флексионные и ротационные нагрузки. Критерием для снятия аппарата при этом является отсутствие патологической подвижности и болезненности в области новообразованного участка диафиза.
Пример выполнения способа.
История болезни №20, животное №2504, возраст 2 года, вес 17 кг, длина голени 14,5 см.
В условиях операционной у наркотизированного животного провели обработку операционного поля 5% спиртовым раствором йода. Через проксимальный и дистальный концы большеберцовой кости провели по две пары взаимоперекрещивающихся спиц, которые закрепили в опорах аппарата. Из двух боковых разрезов с латеральной и медиальной сторон в средней трети голени чрезнадкостнично пилой Джигли резецировали поперечно участок диафизов берцовых костей протяженностью 17 мм. Для отграничения области дефекта от параоссальных тканей между проксимальным и дистальным фрагментами большеберцовой кости устанавливали мембрану из трубчатой аллокости, длина которой соответствовала длине дефекта, а диаметр соответствовал диаметру костных фрагментов. Накладывали швы послойно на мягкие ткани. По окончании оперативного вмешательства операционное поле обработали 5% спиртовым раствором йода.
На рентгенограммах через 14 суток после операции в проекции дефекта наблюдали слабые гомогенные тени проксимального и дистального костных отделов регенерата полу сферической формы, растущих аппозиционно навстречу друг другу. Тени аллотранспланта, отграничивающего дефект, имели ровные контуры. На 28 сутки опыта отмечался дальнейший прирост проксимального и дистального костных отделов регенерата, которые теряли гомогенный характер, становились более плотными по периферии, структура трансплантата оставалась без изменений, между костными фрагментами и аллокостью прослеживались четкие щели. К 120 суткам эксперимента значительно большая часть дефекта была заполнена новообразованной костной тканью, в области стыка оссифицированных проксимального и дистального отделов регенерата произошло сращение. Трансплантат имел нечеткие контуры, его кортикальная пластинка была истончена. Щели между костями донора и реципиента прослеживались с трудом, при этом наблюдали частичное рассасывание кортикальной пластинки большеберцовой кости. Периостальные костные разрастания были слабо выражены. Через 270 дней перестройка костной ткани в новообразованном участке диафиза и трансплантате продолжалась.
История болезни №9, животное №2493, возраст 1,5 года, вес 14 кг, длина голени 15 см.
В данном примере используется мембрана, которая выполняется из трубчатой аллокости с внутренним диаметром, соответствующим диаметру фрагментов трубчатой кости, длиной, превышающей длину дефекта на 6 мм. Предварительная подготовка аллокости, наложение аппарата, резекция участка диафиза протяженностью 16 мм осуществлялись аналогично описанному выше. Отграничение области дефекта от параоссальных тканей осуществляли путем введения проксимального и дистального фрагментов большеберцовой кости в мембрану. Накладывали швы послойно на мягкие ткани. По окончании оперативного вмешательства операционное поле обработали 5% спиртовым раствором йода.
На рентгенограммах через 14 суток после операции признаков костной регенерации в проекции дефекта не наблюдали. Тени аллотранспланта, изолирующего дефект, имели ровные контуры. На 28 сутки опыта в дефекте отмечали тени оссифицированных проксимального и дистального отделов регенерата, которые росли навстречу друг другу и имели гомогенный характер, линии опилов костных фрагментов были ровными, структура трансплантата оставалась без изменений. К 120 суткам эксперимента дефект был заполнен новообразованной костной тканью, линия стыка костных отделов регенерата, между которыми произошло сращение, прослеживалась с трудом, в основаниях костного регенерата наблюдали участки просветления, по периферии - уплотнение костной ткани. Трансплантат имел нечеткие контуры, его кортикальная пластинка была истончена, линии опилов фрагментов большеберцовой кости размыты. Периостальные костные разрастания были слабо выражены. Через 270 дней продолжалась перестройка костной ткани в области бывшего дефекта и трансплантате, которая заключалась в формировании костномозговой полости и корковой пластинки в новообразованном участке диафиза, в рассасывании и замещении новообразованной костной тканью трубчатой аллокости.
После снятия аппарата общее состояние экспериментальных животных (собаки) было удовлетворительным. Они полностью опирались на оперированную конечность, функция смежных суставов сохранялась в полном объеме. Атрофия мягких тканей оперированной конечности не определялась.
Использование мембраны из рассасывающегося материала, например из трубчатой аллокости, предотвращает врастание мягких тканей в область дефекта, не требует повторной операции для ее удаления.
Предлагаемый способ позволяет создать оптимальные условия для репаративной регенерации костной ткани посредством отграничения области дефекта длинной трубчатой кости рассасывающимся материалом, стимулирует процесс остеогенеза, способствует полноценной регенерации трубчатой кости.
Предлагаемый способ может быть использован при замещении дефектов, образовавшихся после удаления костных опухолей.
Кроме того, он менее трудоемок, малозатратен по сравнению с известными.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ МОДЕЛИРОВАНИЯ СТИМУЛЯЦИИ РЕГЕНЕРАЦИИ КОСТНОЙ ТКАНИ | 2005 |
|
RU2309463C2 |
| СПОСОБ ОЦЕНКИ СТЕПЕНИ РОСТА КОСТНОГО РЕГЕНЕРАТА | 2003 |
|
RU2270606C2 |
| Устройство, комплект и способ для введения трансплантата в костный регенерат | 2020 |
|
RU2741206C1 |
| СПОСОБ ГИСТОМОРФОМЕТРИЧЕСКОГО ИССЛЕДОВАНИЯ ДИСТРАКЦИОННОГО ОСТЕОГЕНЕЗА | 2001 |
|
RU2213963C2 |
| СПОСОБ ЛЕЧЕНИЯ ПАЦИЕНТА С НЕСОСТОЯТЕЛЬНЫМ ДИСТРАКЦИОННЫМ КОСТНЫМ РЕГЕНЕРАТОМ В СТАДИИ ОССИФИКАЦИИ | 2024 |
|
RU2837475C1 |
| СПОСОБ УДЛИНЕНИЯ БЕДРА | 1999 |
|
RU2180811C2 |
| Способ трансплантации биокомпозитных сфероидов для обеспечения возможности восстановления целостности кости при дефектах, размеры которых превышают критические | 2020 |
|
RU2744756C1 |
| СПОСОБ ЭКСПЕРИМЕНТАЛЬНОГО МОДЕЛИРОВАНИЯ ЗАМЕДЛЕННОГО ДИСТРАКЦИОННОГО ОСТЕОГЕНЕЗА ПРИ УКОРОЧЕНИИ КОСТЕЙ КОНЕЧНОСТЕЙ | 2011 |
|
RU2463668C1 |
| СПОСОБ ХИРУРГИЧЕСКОГО ЛЕЧЕНИЯ ТРАВМАТИЧЕСКИХ ПОВРЕЖДЕНИЙ КОСТЕЙ | 2000 |
|
RU2180534C2 |
| СПОСОБ МОДЕЛИРОВАНИЯ ЗАМЕДЛЕННОГО ОСТЕОГЕНЕЗА | 2005 |
|
RU2301457C2 |
Изобретение относится к области медицины. При моделировании замещения дефекта длинной трубчатой кости изолируют область дефекта от окружающих параоссальных тканей мембраной в виде трубки. Мембрану изготавливают из формалинизированной трубчатой аллокости. Костные фрагменты фиксируют в опорах аппарата наружной чрескостной фиксации. Изготавливают мембрану, длина и наружный диаметр которой равны длине дефекта и диаметру костных фрагментов, и устанавливают ее между костными фрагментами, или мембрану, длина которой более длины дефекта, а внутренний диаметр соответствует диаметру костных фрагментов, и вводят в нее концы костных фрагментов. Изобретение позволяет создать оптимальные условия для репаративной регенерации костной ткани. 4 ил.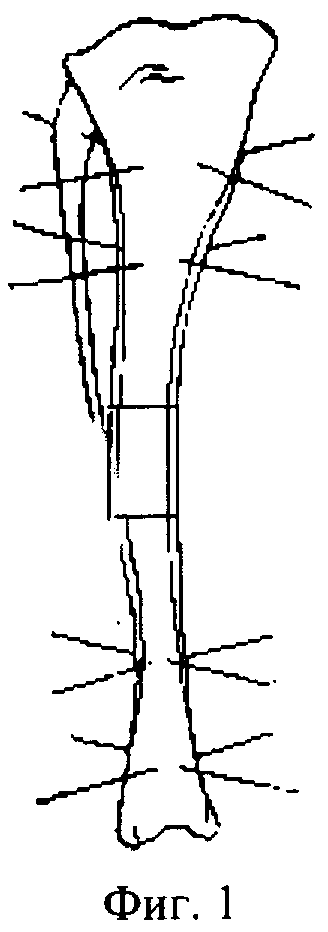
Способ моделирования замещения дефекта длинной трубчатой кости, включающий изоляцию области дефекта от окружающих параоссальных тканей мембраной в виде трубки, отличающийся тем, что мембрану изготавливают из формалинизированной трубчатой аллокости, а костные фрагменты фиксируют в опорах аппарата наружной чрескостной фиксации, при этом изготавливают мембрану, длина и наружный диаметр которой равны длине дефекта и диаметру костных фрагментов, и устанавливают ее между костными фрагментами, или мембрану, длина которой более длины дефекта, а внутренний диаметр соответствует диаметру костных фрагментов, и вводят в нее концы костных фрагментов.
| O'BRIEN WD, MISHKIN DJ, ENGLER WO, MILLER MC, NEVILLE BW | |||
| Guided tissue regeneration using a biodegradable barrier membrane for new attachment: a clinical, histologic, and histometric study in dogs, International Journal of Periodontics and Restorative, 1995, Volume 15, Issue 5, с.447-462. |
Авторы
Даты
2006-08-10—Публикация
2003-05-28—Подача