Изобретение относится к способам измерения уровня метастабильности водных растворов, подвергнутых униполярной электрохимической активации /ЭХА/ на стандартных диафрагменных электрохимических реакторах с проточными модульными элементами, и может найти применение в различных сферах медико-биологической деятельности людей, а также во многих отраслях народного хозяйства.
Технология ЭХА основана на униполярном разделении процессов катодной и анодной обработки водных растворов, минерализованных в диапазоне от 0,05 до 5 г/л (даже дистиллированная вода относится к водным растворам, поскольку содержит до 5 мг/л растворенных солей) [1]. B результате униполярного воздействия водные растворы приобретают метастабильное состояние, обусловленное повышением активности ионов водорода и электронов, приводящей к образованию нестабильных химических соединений с аномальными физико-химическими параметрами, релаксирующимися во времени после ЭХА до нового устойчивого термодинамического состояния. Оба потока водного раствора, выходящие параллельно из диафрагменного проточного электрохимического реактора и названные католитом /электрод катод/ и анолитом /электрод анод/, приобретают соответствующую щелочную реакцию и соответствующую кислотную. Значения кислотности и щелочности, приобретенные водным раствором после ЭХА, определяются по водородному показателю рН и окислительно-восстановительному потенциалу ОВП (или ϕ) [2].
Измерение значений рН осуществляется с помощью рН-метра, представляющего собой высокоомный милливольтметр, подключенный к двум электродам, погруженным в исследуемый водный раствор. Разность потенциалов между этими электродами - измерительным стеклянным и хлорсеребряным сравнения - пропорциональна приобретаемой ионами водорода активности. Измерение ϕ производится также высокоомным милливольтметром, подсоединенным также к двум электродам, один из которых хлорсеребряный электрод сравнения, а другой из платины - измерительный. Разность потенциалов, образуемая между данными электродами, пропорциональна приобретаемой электронами активности. Количественной мерой активности служит уровень метастабильности водного раствора, приобретаемый после ЭХА. Оценивается уровень метастабильности градиентом изменения кислотности и щелочности. Способ измерения уровня метастабильности водных растворов, обработанных по технологии ЭХА, многостадийное. Первоначально измеряются рН и ϕ исходного водного раствора, затем измеряются аналогичные показатели у католита и анолита сразу после выхода их из электрохимического реактора. Конечная стадия - вычитание из значений рН и ϕ католита и анолита значения рН и ϕ исходного водного раствора. Полученные после вычитания значения ΔрН и Δϕ являются градиентами изменения кислотности и щелочности водного раствора после ЭХА. По ним оценивают уровень метастабильности, приобретенный как католитом, так и анолитом. Значения градиентов изменения располагаются в области физического саморегулирования релаксирующихся параметров. Область регулирования ограничивается максимальными и минимальными значениями рН и ϕ. Для водных растворов с минерализованностью 0,05÷5,0 г/л границы максимальных и минимальных значений следующие. Верхняя граница рНmax равняется 12,5, а нижняя граница рНmin равняется 1,8. По окислительно-восстановительному потенциалу верхняя граница ϕmax равняется +1250 мВ, а нижняя граница ϕmin равняется -850 мВ. Максимальные и минимальные значения градиентов метастабильности у католита и анолита указывают на максимальные и минимальные уровни метастабильного состояния, приобретаемые после ЭХА, и равняются следующим значениям: ΔрНmax=12,5-7=5,5; ΔрНmin=1,2-7=|-5,8|; Δϕmax=1250-250=1000 мВ; Δϕmin=-850-250=-1100 мВ.
Данный способ измерения уровня метастабильности водных растворов с минерализованностью 0,05÷5,0 г/л имеет недостатки, делающие его неэффективным. Недостатки следующие. Во-первых, для измерения уровня метастабильности водного раствора используются сложные в эксплуатации, трудоемкие в работе, дорогостоящие по цене приборы. Во-вторых, от персонала аналитической лаборатории требуются глубокие профессиональные знания и практические навыки. В-третьих, приборы предназначены для работы в лабораторных условиях.
Предлагаемое изобретение решает задачу повышения эффективности способа намерения уровня метастабильности водных растворов после электрохимической активации.
Поставленная задача решается тем, что измерение уровня метастабильности водных растворов, подвергнутых униполярной электрохимической активации, характеризуемой аномальностью значений физико-химических параметров по водородному показателю и окислительно-восстановительному потенциалу, проводят методом капиллярного подъема жидкости в стеклянном калиброванном капилляре, причем значение изменения высоты подъема жидкости является количественным показателем метастабильного состояния водного раствора, при этом диаметр капилляра берется равным одному из значений, лежащих в диапазоне от 0,1 до 0,5 мм.
Повышение эффективности достигается следующим образом. Определение уровня метастабильиости осуществляется путем измерения смачивающей способности водного раствора до и после ЭХА [3], состоящего в замере высоты подъема жидкости вверх по капилляру в соответствии с законом Жюрена [4]. Измерение же уровня метастабильности, получаемого водным раствором, связано с операциями замера высоты подъема водного раствора до ЭХА и после ЭХА и определения градиента изменения высоты подъема путем вычитания полученных значений как у католита, так и у анолита из значений уровня метастабильности исходного раствора. Полученное значение градиента является количественным показателем приобретенного метастабильного состояния водного раствора. Чем больше градиент (разница вычитания) изменения высоты подъема, тем выше уровень приобретенной метастабильности водным раствором. Метод капиллярного подъема жидкости в капилляре является наиболее точным и проверенным на практике способом определения смачивающей способности жидкости [5]. Простота конструктивного исполнения, несложность изготовления, надежность в работе позволяют оперативно измерять уровень метастабильности. Отличительный признак - диапазон значений диаметра капилляра, равный 0,5-0,1 мм, - был установлен опытным путем. Так, при значении диаметра более 0,5 мм высота подъема воды в капилляре после ЭХА не выше 10 мм. Для такой высоты очень затруднительно осуществить градуировку шкалы измерения. При значении диаметра капилляра менее 0,1 мм возникают трудности в визуальном контроле за движением жидкости в капилляре и наблюдением за уровнем мениска. Положительным моментом применения метода капиллярного подъема жидкости в капилляре служит факт появления возможности оценки уровня метастабильности воды параллельно по двум основным параметрам: рН и ϕ - путем выведения их на шкалу измерения в виде делений, отградуированных соответствующим образом относительно делений, указывающих высоту подъема.
Способ измерения уровня метастабильности водных растворов реализуется на установке, представленной на чертеже. Установка состоит из: 1 - мерного стакана; 2 - штатива; 3 - стеклянного капилляра с калиброванным диаметром; 4 - винтового микрометрического механизма для опускания в водный раствор и поднятия из него стеклянного капилляра; 5 - увеличительной линзы для точного замера уровня жидкости в капилляре; 6 - шкалы измерения, отградуированной в значениях рН, ϕ, h.
Измерение уровня метастабильности водных растворов предлагаемым способом многостадийное и осуществляется следующим образом.
ПРИМЕР 1: Исходная жидкость - питьевая вода с минерализацией 1,7 г/л. Параметры, характеризующие ее кислотность и щелочность: рН 7,0 и ϕ=280 мВ /среда нейтральная/. Установка для электрохимической активации воды - СТЕЛ. Режим ЭХА: производительность - 10 л/час, напряжение - 40 В, сила тока 3 А, температура воды - 15°С. Измерение уровня метастабильности осуществляется на установке с диаметром капилляра 0,45 мм /см. чертеж/. На первой стадии в мерный стакан 1 наливается исходная питьевая вода. Поворотом головки винта микрометрического механизма 4, закрепленного жестко на штативе 2, опускается стеклянный капилляр 3 нижним торцом в воду на глубину 0,5-1,0 мм от поверхности воды. С момента касания капилляром 3 поверхности воды она начинает подниматься в капилляре 3. Прекращается подъем воды после достижения в капилляре 3 равновесия между силой гидростатического давления воды с силой капиллярного подъема [5]. Для стабилизации данного равновесия между возникшими силами производится легкое 2-3-кратное постукивание деревянной палочкой /или пальцем руки/ самого капилляра 3. Затем производится визуальное, через увеличительное стекло 5, фиксирование уровня мениска воды в капилляре 3. По высоте подъема определяется на шкале измерений 6 соответствующие значению высоты h значения рН и ϕ. Для данных условий анализа и режима ЭХА высота подъема соответствует 12 мм, рН равняется 7,0, ϕ равняется +280 мВ. На второй стадии аналогичным образом определяется высота подъема католита в капилляре 3. В мерный стакан 1 заливается уже не исходная вода, а католит. Для установленных условий анализа и режима ЭХА высота подъема католита составляет 16,5 мм. Соответствующие ей значения рН и ϕ равняются 10,5 и -900 мВ. На третей стадии проводится анализ анолита. По выше изложенной методике в мерный стакан 1 наливается анолит и определяется для данных условий анализа и режима ЭХА высота подъема его в капилляре 3. Она составляет 14,3 мм. Соответствующие значения рН и ϕ имеют следующие значения: 4,7 и +800 мВ. Последняя стадия измерения уровня метастабильности католита и анолита - определение градиента изменения кислотности и щелочности после ЭХА. Для этого производится вычитание из определенных значений высот католита и анолита hк, hа значения высоты подъема исходной воды hв. Полученные значения следующие Δhк=4,5; Δhа=2,3. Аналогичным образом определяются градиенты изменения кислотности и щелочности у католита и анолита по параметрам рН и ϕ. Вычитание дало следующие результаты: ΔpH 3,5: Δϕ=-650 мВ; ΔрН 2,3; Δϕ=+550 мВ. По данным значениям градиентов изменения высоты подъема католита и анолита можно сделать следующее заключение: питьевая вода с минерализацией 1,7 г/л, обработанная по технологии ЭХА в режиме, приведенном выше, приобрела метастабильное состояние, уровнем, соответствующим 3/5 его максимального значения.
ПРИМЕР 2: Методика измерения уровня метастабильности та же. Водный раствор тот же. Режим ЭХА тот же. Диаметр капилляра 0,30 мм. Результаты измерения уровня метастабильности следующие: hв=15 мм, hк=19,5 мм, hа=17,5 мм; pH 7,0, рНк 10,8, рНа 4,7; ϕв=+280 мВ, ϕк=-900 мВ, ϕа=+800 мВ. Расчеты, сделанные по данным значениям, установили, что уровень метастабильности соответствует также 3/5 его максимального значения.
ПРИМЕР 3: Методика измерения уровня метастабильности та же. Водный раствор тот же. Режим ЭХА тот же. Диаметр капилляра 0,15 мм. Результаты измерения уровня метастабильности следующие: hв=17 мм, hk=21,5 мм, ha=19,2 мм; pHв 7, pHк 10,8, pHа 4,7; ϕв=+280 мВ, ϕк=-900 мВ, ϕа=+800 мВ. Результаты расчетов уровня метастабильности соответствуют 3/5 его максимального значения.
Как видно из примеров 1-3, предлагаемый способ измерения уровня метастабильности водного раствора, обработанного по технологии ЭХА, является более эффективным. Повышение эффективности связано с появлением возможности замены в аналитической работе трудоемких и энергоемких в эксплуатации, сложных в конструкции и дорогих в цене приборов, измеряющих рН и ϕ на простую по техническому исполнению, надежную в работе, недорогую по цене установку. Одним из качественных показателей преимущества предлагаемого способа может сложить универсальность его аналитической возможности, заключающейся в одновременном измерении кислотности и щелочности водных растворов как до обработки ЭХА, так и после. Простота метода измерения высоты подъема жидкости в капилляре, высокая точность замера параметров, возможность измерения без источников электроснабжения, небольшие габаритные размеры способствуют решению задачи по широкому практическому применению предлагаемого способа во многих отраслях народного хозяйства, а также в различных сферах медико-биологической деятельности людей.
ИСТОЧНИКИ ИНФОРМАЦИИ
1. В.М.Бахир. Современные технические электрохимические системы для обеззараживания, очистки и активирования воды. М., 1999, с 26-39.
2. В.М.Бахир, Ю.Г.Задорожнкй и др. Электрохимическая активация: очистка воды и получение полезных растворов. ВНИИИМТ, Изд. "Маркетинг Саппорт Сервисиз", 2001, с.7-23.
3. В.И.Прилуцкий, В.М.Бахир. Электрохимическая активированная вода: аномальные свойства, механизм биологического действия. М., ВНИИИМТ АО НПО "Экран", 1997, с.9-12.
4. Р.В.Телеснин. Молекулярная физика. М.: Высшая школа, 1973, с.244-246.
5. А.Адамсон. Физическая химия поверхностей. Пер. с анг. М.: Мир, 1979, с.14-20.
| название | год | авторы | номер документа |
|---|---|---|---|
| УСТРОЙСТВО ДЛЯ ЭЛЕКТРОХИМИЧЕСКОЙ ОБРАБОТКИ ЖИДКИХ СРЕД И СПОСОБ ЕГО ИСПОЛЬЗОВАНИЯ | 2007 |
|
RU2333157C1 |
| ЭЛЕКТРОХИМИЧЕСКАЯ МОДУЛЬНАЯ ЯЧЕЙКА ДЛЯ ОБРАБОТКИ РАСТВОРОВ ЭЛЕКТРОЛИТОВ | 2007 |
|
RU2350692C1 |
| СПОСОБ ПОСОЛА РЫБЫ | 2005 |
|
RU2302739C1 |
| СПОСОБ ПРОИЗВОДСТВА СОЛОДА | 2003 |
|
RU2247143C1 |
| СПОСОБ ПРОФИЛАКТИКИ И ЛЕЧЕНИЯ НАЧАЛЬНОГО КАРИЕСА ЗУБОВ | 2000 |
|
RU2163114C1 |
| Способ получения католитов-антиоксидантов электроактивированных водных растворов солей и их хранение | 2019 |
|
RU2712614C1 |
| СПОСОБ ХРАНЕНИЯ МЯСА ЖИВОТНЫХ В ОХЛАЖДЕННОМ СОСТОЯНИИ | 2011 |
|
RU2487546C2 |
| СПОСОБ АЭРОЗОЛЬНОЙ ДЕЗИНФЕКЦИИ ЗАМКНУТЫХ ПРОСТРАНСТВ, ВКЛЮЧАЯ ВОЗДУШНУЮ СРЕДУ И ПРЕДМЕТЫ, А ТАКЖЕ ЖИВОТНЫХ, ПТИЦ, РАСТЕНИЙ И ЧЕЛОВЕКА, НАХОДЯЩИХСЯ В ЭТИХ ПРОСТРАНСТВАХ, С ИСПОЛЬЗОВАНИЕМ ЭЛЕКРОХИМИЧЕСКИХ АКТИВИРОВАННЫХ РАСТВОРОВ (САД) | 2001 |
|
RU2218183C2 |
| СПОСОБ ВОЗДЕЛЫВАНИЯ ОВОЩНЫХ КУЛЬТУР ПРИ КАПЕЛЬНОМ ОРОШЕНИИ | 2011 |
|
RU2485757C2 |
| СПОСОБ ПОЛУЧЕНИЯ КАТОЛИТА-АНТИОКСИДАНТА И УСТРОЙСТВО ДЛЯ ЕГО РЕАЛИЗАЦИИ | 2010 |
|
RU2456246C2 |
Изобретение применяется в различных сферах медико-биологической деятельности людей, а также во многих отраслях народного хозяйства для измерения уровня метастабильности водных растворов, подвергнутых униполярной электрохимической активации на стандартных диафрагменных электрохимических реакторах с проточными модульными элементами. Техническим результатом изобретения является повышение эффективности способа. Измерение уровня метастабильности водных растворов основано на определении кислотности и щелочности по водородному показателю и окислительно-восстановительному потенциалу на рН метре. Измерение проводят способом капиллярного подъема жидкости в стеклянном калиброванном капилляре, значение изменения высоты подъема жидкости является количественным показателем метастабильного состояния водного раствора. Диаметр капилляра берется равным одному из значений, лежащему в диапазоне от 0,1 до 0,5 мм. 1 ил.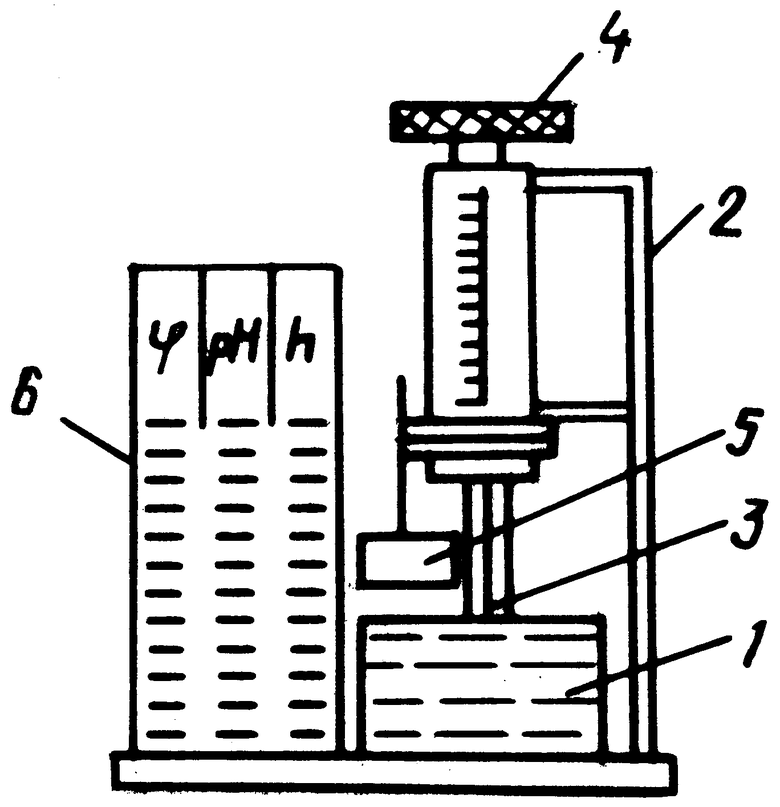
Способ измерения уровня метастабильности водных растворов, подвергнутых униполярной электрохимической активации, характеризуемой аномальностью значений физико-химических параметров по водородному показателю и окислительно-восстановительному потенциалу, отличающийся тем, что измерение уровня метастабильности водных растворов проводится методом капиллярного подъема жидкости в стеклянном калиброванном капилляре, причем значение изменения высоты подъема жидкости является количественным показателем метастабильного состояния водного раствора, при этом диаметр капилляра берется равным одному из значений, лежащих в диапазоне от 0,1 до 0,5 мм.
| БАХИР В.М., ЗАДОРОЖНЫЙ Ю.Г | |||
| и др | |||
| Электрохимическая активация: очистка воды и получение полезных растворов, ВНИИИМТ, Изд | |||
| "Маркетинг Саппорт Сервисиз", 2001, с.7-23 | |||
| УСТРОЙСТВО ДЛЯ ЭЛЕКТРОХИМИЧЕСКОЙ ОБРАБОТКИ ВОДЫ | 1992 |
|
RU2038322C1 |
| УСТРОЙСТВО ДЛЯ АКТИВАЦИИ ВОДЫ | 1997 |
|
RU2144506C1 |
| Датчик диагностики износа узлов трения | 1983 |
|
SU1104387A1 |
Авторы
Даты
2008-01-27—Публикация
2005-12-30—Подача