Изобретение относится к способам определения отдельных видов электрохимических и биохимических коррозионных процессов, а именно к бытовым стиральных машинам, центрифугам с вертикальной осью вращения, содержащим АУ с перемещением корректирующей массы.
Известен способ определения скорости коррозии углеродистой стали, находящейся в коррозионной среде, включающий измерение потенциала коррозии, изменение содержания деполяризатора в среде, наложение на образец постоянного потенциала, равного потенциалу коррозии, выдержку образца до установившегося значения тока и определение его величины, по которой судят о степени коррозии (RU 2094773 С1, 27.10.1997).
Прототипом заявляемого изобретения является способ для определения скорости коррозии углеродистой стали 10 (RU 2224238 С1, 20.02.2004) в стиральной машине, содержащей бак и установленный с возможностью вращения относительно вертикальной оси отжимной резервуар-барабан, входящие в состав внутренней подвижной части стиральной машины, балансировочное кольцо, установленное в верхней части отжимного резервуара, четыре опоры, которые ориентированы в пространстве вертикально и шарнирно соединены с корпусом и внутренней подвижной частью стиральной машины, а нижний конец опор соединен с внутренней подвижной частью стиральной машины выше центра тяжести внутренней подвижной части так, что все точки внутренней подвижной части при отклонении от положения равновесия в вертикальной плоскости, проходящей через опоры и центр тяжести внутренней подвижной части, движутся поступательно. Внутри барабана на высоте 40 см от его дна на проволоке, протянутой через два отверстия, выполненных в стенке барабана, подвешен груз, внутри балансировочного кольца дополнительно установлен кольцевой желоб для свободного перемещения испытуемых образцов в виде металлических шариков, изготовленных из углеродистой стали 10 и занимающих 1/6 часть внутренней полости балансировочного кольца, причем часть полости кольца заполнена 10% водным раствором хлорида аммония.
Устройства [1, 2] не используются для определения отдельных видов электрохимических и биохимических коррозионных процессов.
Заявляемое изобретение решает новую задачу определения отдельных видов электрохимических и биохимических коррозионных процессов, которые обнаруживают себя в механических системах с дисбалансом вращающейся системы и автоматической балансировкой ротора с использованием свободного перемещения корректирующих масс.
Технический результат при использовании изобретения заключается в распознавании широкого спектра отдельных видов электрохимических и биохимических коррозионных процессов при отсутствии информации о них. Это обусловливает возможность проектирования экспертных технических систем и алгоритмов. Динамические или статические способы изучения отдельных видов электрохимических и биохимических коррозионных процессов не используют быстровращающиеся конструкции.
Способ определения коррозионных характеристик проводится в конструкциях бытовых стиральных машин, содержащих бак и установленный, с возможностью вращения относительно вертикальной оси отжимной резервуар-барабан, входящие в состав внутренней подвижной части стиральной машины, балансировочное кольцо с крышкой и желобом, четыре опоры в виде штоков, которые ориентированы в пространстве вертикально и шарнирно соединены с корпусом и внутренней подвижной частью стиральной машины. Нижний конец опор соединен с внутренней подвижной частью выше ее центра тяжести так, что все точки внутренней подвижной части в случае вращения неуравновешенного барабана при отклонении от положения равновесия в вертикальной плоскости, проходящей через опоры и центр ее тяжести, движутся поступательно. Причем снята верхняя панель стиральной машины, измерены и выравнены расстояния между краем бака и стенкой корпуса по всем четырем направлениям путем установки под опоры компенсирующих шайб. Внутренняя подвижная часть имеет такую геометрию, что центр ее тяжести находится выше дна барабана. В стенке барабана выполнены два отверстия, через которые протянута проволока для грузов различной массы, и внутри балансировочного кольца размещают испытуемые образцы в виде шариков одинакового размера из углеродистой стали. При этом они размещаются в ограниченном секторе, образованном связанными подвижными радиальными перегородками, и находятся в соприкосновении друг с другом. Способ отличается тем, что для определения отдельных видов электрохимических и биохимических процессов грузы различной массы и балансировочное кольцо располагают на высоте центра тяжести внутренней подвижной части. Внутреннюю полость балансировочного кольца заполняют коррозионной средой. На внутренней боковой поверхности большего радиуса балансировочного кольца выполняют дополнительные радиальные перегородки с зазубринами, в желобе делают отверстия для удаления продуктов коррозии. В крышке балансировочного кольца выполняют отверстия для выхода газов и летучих продуктов коррозии. На электроприводе, закрепленном неподвижно в нижней части внутренней подвижной части, устанавливают электронный измеритель потребляемой мощности. Закрывают на время движения отверстия в крышке балансировочного кольца пробками из пластичного материала, осуществляют разгон барабана без грузов (неуравновешенной массы). Измеряют ряд значений мощности Рпуск, P1,..., Pi,..., Pk и вычисляют их среднее значение Рcp(j), где k - число измерений во время разгона, на основе схем умножения двух сигналов, пропорциональных значениям напряжения и тока, последовательно в течение разгона барабана и совершении им трех оборотов вокруг своей вертикальной оси. Подвешивая к стенке барабана дополнительные грузы, определяют критическую неуравновешенную массу mj, при наличии которой барабан при разгоне задевает стенку корпуса в заданных габаритах рабочей зоны внутренней подвижной части, после совершения трех оборотов вокруг своей вертикальной оси, в момент времени tj, где j - номер измерения. Далее через промежуток времени Δt=tj+1-tj, в момент времени tj+1, совершая такие же измерения, получают следующие значения средней мощности
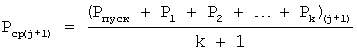
неуравновешенной присоединяемой массы mj+1. Измерение мощности и присоединяемой неуравновешенной массы делают периодически. Если относительная разница 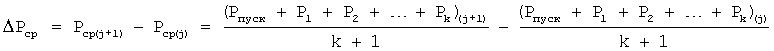 больше нуля и Δm=m(j+1)-m(j)≤0, то сравнивают эти значения с предварительно полученными данными для течения биохимической коррозии в присутствии аэробных и анаэробных микроорганизмов. В случае их совпадения делают заключение о наличии в исследуемой коррозионной среде данного вида биохимической коррозии. Если разница Δm=m(j+1)-m(j)>0 и Pcp(j+1)≥Pcp(j), то сравнивают эти значения с предварительно полученными данными для течения электрохимической коррозии с кислородной деполяризацией. В случае их совпадения делают заключение о наличии в исследуемой коррозионной среде данного вида электрохимической коррозии. Если разница Δm=m(j+1)-m(j)>0 и Pcp(j+1)<Pcp(j), то сравнивают эти значения с предварительно полученными данными для течения электрохимической коррозии с водородной деполяризацией. В случае их совпадения делают заключение о наличии в исследуемой коррозионной среде данного вида электрохимической коррозии.
больше нуля и Δm=m(j+1)-m(j)≤0, то сравнивают эти значения с предварительно полученными данными для течения биохимической коррозии в присутствии аэробных и анаэробных микроорганизмов. В случае их совпадения делают заключение о наличии в исследуемой коррозионной среде данного вида биохимической коррозии. Если разница Δm=m(j+1)-m(j)>0 и Pcp(j+1)≥Pcp(j), то сравнивают эти значения с предварительно полученными данными для течения электрохимической коррозии с кислородной деполяризацией. В случае их совпадения делают заключение о наличии в исследуемой коррозионной среде данного вида электрохимической коррозии. Если разница Δm=m(j+1)-m(j)>0 и Pcp(j+1)<Pcp(j), то сравнивают эти значения с предварительно полученными данными для течения электрохимической коррозии с водородной деполяризацией. В случае их совпадения делают заключение о наличии в исследуемой коррозионной среде данного вида электрохимической коррозии.
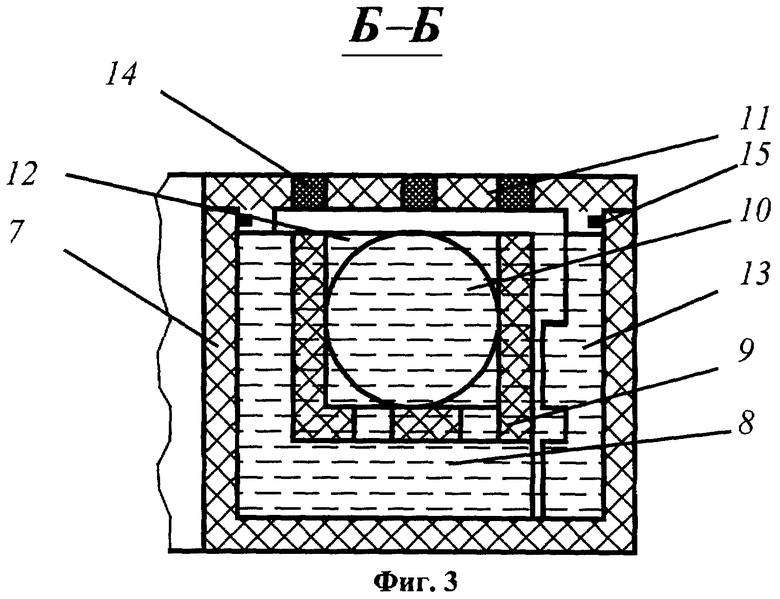
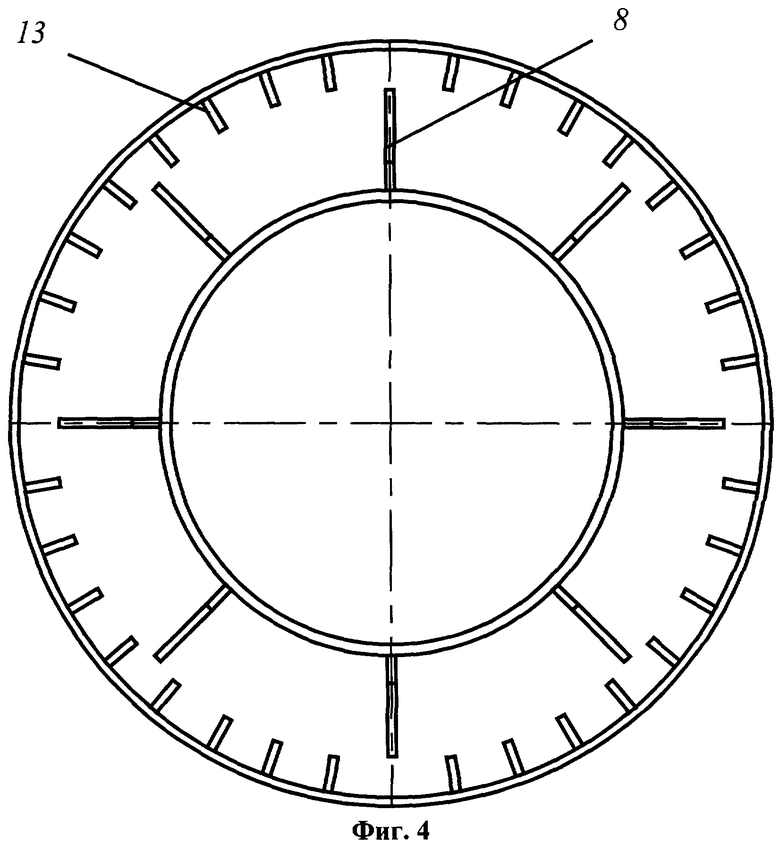
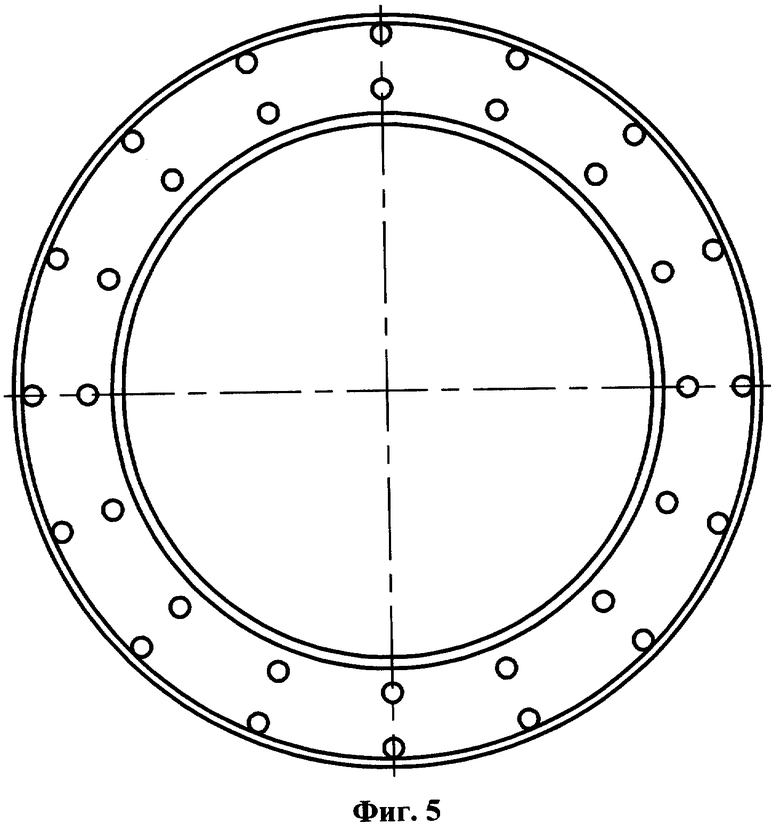
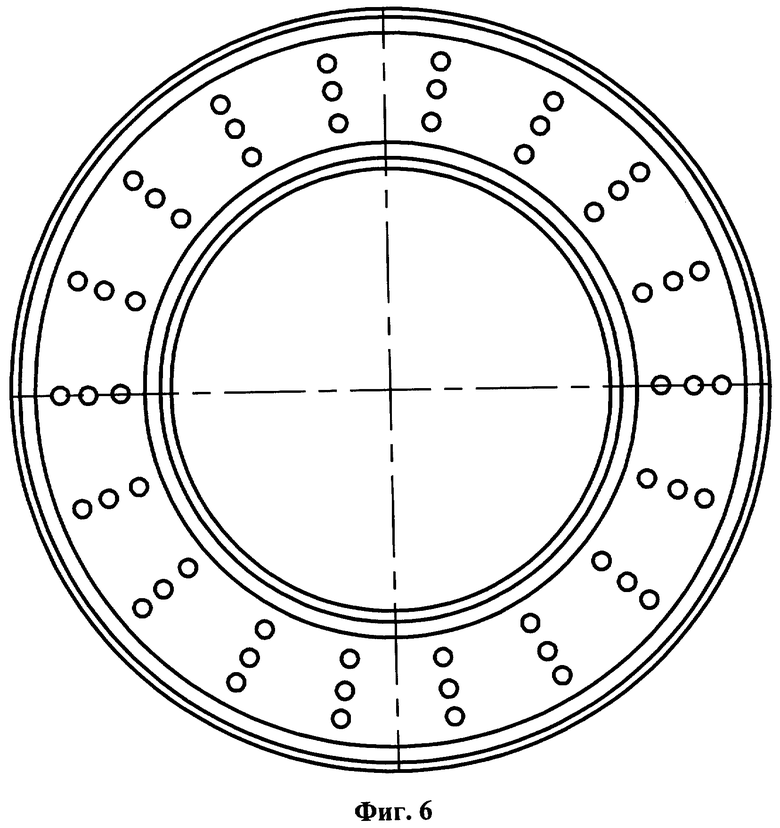
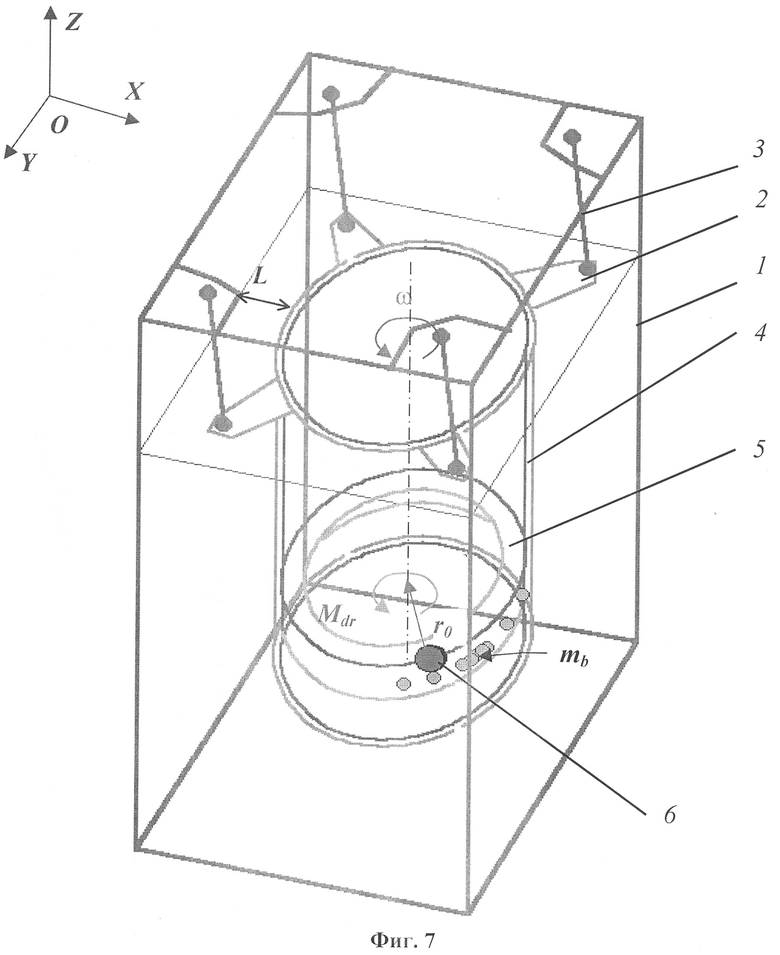
На фиг.1 приведено устройство для проведения способа определения отдельных видов электрохимических и биохимических коррозионных процессов на базе стиральной машины с установкой автобалансирующего устройства, вид сверху; на фиг.2 показан поперечный разрез А-А устройства на фиг.1; на фиг.3 представлен разрез Б-Б на фиг.1; на фиг.4 представлено балансировочное кольцо; на фиг.5 изображен перфорированный желоб, вдоль которого перемещаются шарики; на фиг.6 показана крышка автобалансирующего устройства, вид снизу; на фиг.7 приведена структурная пространственная схема устройства для проведения способа определения отдельных видов электрохимических и биохимических коррозионных процессов на базе стиральной машины с установкой автобалансирующего устройства.
Использованы следующие обозначения: 1 - корпус; 2 - бак, входящий в состав внутренней подвижной части; 3 - опоры со сферическими шарнирами; 4 - барабан; 5 - балансировочное кольцо в составе автобалансирующего устройства (АУ); 6 - неуравновешенная масса; 7 - корпус АУ; 8 - радиальные перегородки; 9 - кольцевой желоб; 10 - шарики; 11 - перфорированная крышка АУ; 12 - исследуемая жидкость; 13 - дополнительные радиальные перегородки с зазубринами; 14 - герметичные пробки из пластичного материала; 15 - резиновые уплотнения; L - расстояние между кромкой бака и стенкой корпуса; XOYZ - система отсчета; ω - угловая скорость движения ротора-барабана; Мdr - приводной крутящий момент; mb - корректирующая масса, представляющая группу испытуемых шариков; r0 - радиус вращения неуравновешенной массы; ЦТ - центр тяжести внутренней подвижной части.
Устройство, используемое в способе определения отдельных видов электрохимических и биохимических коррозионных процессов, содержит расположенные в корпусе 1 бак 2, установленный с возможностью вращения относительно вертикальной оси барабан 4, балансировочное кольцо 5, входящее в состав АУ со съемной зафиксированной перфорированной крышкой 11, герметично закрывающей рабочую полость балансировочного кольца, на время движения барабана отверстия заполняются герметичными пробками 14 из пластичного материала, и четыре опоры 3 со сферическими шарнирами. Балансировочное кольцо установлено в барабане на высоте центра тяжести всей внутренней подвижной части. На проволоке, протянутой через два отверстия, выполненных в стенке барабана 4, на высоте, соответствующей положению центра тяжести внутренней подвижной части, подвешена неуравновешенная масса 6 в виде грузов. В кольцевом желобе 9, устанавливаемом в балансировочном кольце на неподвижных радиальных перегородках 8, свободно размещаются шарики 10 из углеродистой стали одинаковых размеров. На внутренней боковой поверхности большего радиуса балансировочного кольца выполняют дополнительные радиальные перегородки с зазубринами 13. Заливка исследуемой жидкости 12 производится во внутреннюю полость балансировочного кольца.
Способ проводится следующим образом. Снимается крышка АУ и внутреннюю полость балансировочного кольца заполняют жидкостью. Крышку закрывают пробками из пластичного материала. Электропривод барабана включают кратковременно в работу для разгона барабана и, когда барабан совершает три полных оборота, отключают. Дополнительные радиальные перегородки с зазубринами улучшают перемешивание ингибитора коррозии и усиливают турбулентность потока жидкости. Во время вращения барабана без неуравновешенной массы (грузов) измеряют ряд значений мощности Рпуск, P1,..., Pi,..., Pk, где k - число измерений во время разгона, с помощью электронного измерителя потребляемой мощности, установленного на электроприводе, закрепленном неподвижно в нижней части внутренней подвижной части, на основе схем умножения двух сигналов, пропорциональных значениям напряжения и тока. Вычисляют среднюю мощность
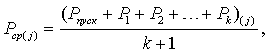
где j - номер текущего измерения. Затем подвешивают дополнительные грузы и приводят барабан во вращение снова. Если на стадии разгона не произошло касания бака о стенку корпуса с характерным шумом, подвешивают дополнительные грузы и производят повторные кратковременные пуски барабана. Увеличение массы дополнительных грузов производят до тех пор, пока при разгоне барабана не произойдет касание края бака о стенку корпуса с характерным шумом. Полученное таким путем критическое для вращающейся системы значение неуравновешенной, дисбалансной массы (массы грузов) mj, где j - индекс текущего измерения, считают количественной мерой способности внутренней подвижной части сопротивляться воздействию центробежной силы инерции, приложенной к дисбалансной массе. Таким образом, при разгоне барабана определяют предельный дисбаланс (критическую неуравновешенную массу) системы в заданных габаритах рабочей зоны внутренней подвижной части.
Далее через промежуток времени Δt=tj+1-tj, в момент времени tj+1, совершая такие же измерения, получают следующие значения неуравновешенной присоединяемой массы mj+1 и средней мощности

Измерение мощности и присоединяемой неуравновешенной массы делают периодически в течение процесса исследования природы жидкости. Далее полученные результаты анализируются.
Изменения состояний стального шарика в разных коррозионных средах влияют на кинематику и динамику его кругового движения по кольцевому желобу балансировочного кольца. Если скорость качения велика, то центробежная сила инерции, приложенная к шарику, создает значительное усилие, передающееся на корпус конструкции, в которой устанавливается устройство. Выполнив конструкцию подвижной, в виде маятниковой подвески, имеем колебательное движение последней, параметры которого зависят от размеров, формы перемещающегося шарика, физических характеристик исследуемой коррозионной среды в полости балансировочного кольца, химического состава жидких фаз, количества вещества в каждой из фаз.
С течением времени, по мере уменьшения металлической корректирующей массы, ухудшаются или улучшаются вибрационные свойства механической системы с неуравновешенным ротором в зависимости от вида электрохимических и биохимических коррозионных процессов. Шарики и жидкости при изменении их природы и размеров получают различный импульс движения под действием трения.
Для заданной геометрии рабочей зоны механизма, в котором перемещаются корректирующие массы в виде шариков, находится величина, характеризующая предельный дисбаланс ротора. Это предельное значение неуравновешенной (дисбалансной) массы m0.
Связь величины неуравновешенной массы вращающейся системы с процессом коррозии выражается дифференциальным уравнением

где ρ(t) - скорость коррозии;
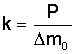 - коэффициент пропорциональности; dt - дифференциал времени; Р - общий вес металлических шариков; S - общая площадь поверхности шариков; dm0 - дифференциал неуравновешенной критической массы ротора при разгоне, которая является инерционной составляющей в дифференциальных уравнениях его движения; Δm0 - диапазон изменения m0 за промежуток времени Δt, соответствующий полному коррозионному разрушению шариков.
- коэффициент пропорциональности; dt - дифференциал времени; Р - общий вес металлических шариков; S - общая площадь поверхности шариков; dm0 - дифференциал неуравновешенной критической массы ротора при разгоне, которая является инерционной составляющей в дифференциальных уравнениях его движения; Δm0 - диапазон изменения m0 за промежуток времени Δt, соответствующий полному коррозионному разрушению шариков.
В основе заявляемых измерений лежит утверждение, что при движении в условиях ограниченного пространства, в поле сил тяжести данной механической системы, включающей статически неуравновешенный ротор, внутри которого происходят изменения в природе корректирующих масс, его предельный дисбаланс определяет размер замкнутой области, в которой периодическое движение вблизи положения равновесия системы устойчиво.
Анализ полученных результатов эксперимента строится на теоретических исследованиях в области коррозии и защиты металлов и основан на предварительно подготовленных измеренных искомых значений для многих видов электрохимических и биохимических коррозионных процессов. Изучается коррозионно-электрохимическое поведение углеродистой стали различных марок.
1. Обычно в коррозионном процессе участвуют бактерии многих видов, ассоциативно связанные между собой и совместно обусловливающие явление коррозии. При этом анаэробные условия часто могут быть созданы деятельностью аэробных бактерий, что экспериментально удалось показать Рейнитцу. На практике аэробные и анаэробные бактерии существуют совместно. С возможностью биохимического разъедания приходится считаться в морских, речных, прудовых, канальных и сточных водах, во влажной почве, в болотах и на суше, в зонах с высоким уровнем грунтовых вод. На нефте- и газопромыслах может происходить биохимическая коррозия, вызываемая бактериями, продуцирующими сероводород, а тионовые бактерии образуют значительное количество серной кислоты. В морях и реках многие водные организмы прикрепляются к различным металлическим телам, попадающим в зону их обитания, и развиваются на них. Это приводит к осложнениям в эксплуатации подводных сооружений. Обрастатели (совокупность этих существ) способны забить ограждающие решетки на всасывающих устройствах гидроэлектростанций. Обрастание подводной части кораблей вызывает ухудшение эксплуатационных качеств судна: снижение скорости, увеличение осадки, повышение расхода топлива. Имеет место разрушение обрастателями лакокрасочных противокоррозионных покрытий и металлического корпуса.
Поэтому обрастание поверхности металлических шариков в зоне обитания бактериями и микроорганизмами способствует повышению моментов трения между шариками и стенками, дном желоба балансировочного кольца и шариков друг с другом. Нагрузочный момент возрастает и мощность, отбираемая приводом от источника электрической энергии, увеличивается, что фиксируется во время эксперимента. В то же время, в отсутствие снижения корректирующей массы, не наблюдается изменение предельной неуравновешенной массы. Таким образом, если относительная разница измеренных за некоторый промежуток времени Δt значений потребляемой мощности ΔРcp=Pcp(j+1)-Pcp(j)>0, а критической неуравновешенной массы Δm=m(j+1)-m(j)≤0, то правомерно сравнить эти значения с предварительно полученными данными для течения биохимической коррозии в присутствии аэробных и анаэробных микроорганизмов. В случае их совпадения можно сделать заключение о наличии в исследуемой коррозионной среде данного вида биохимической коррозии.
Рассмотрим электрохимический механизм протекания процессов окисления металла и восстановления окислителя в присутствии микроорганизмов и бактерий.
В обычных природных условиях (аэробных) окислителем является кислород, растворенный в воде:
O2+2H2O+4e-→4OH-.
Если же воздух поступает с трудом, то кислород, ранее находившийся в воде, быстро используется и электрохимическая коррозия прекращается.
Помимо растворенного в воде кислорода в качестве окислителя могут выступать и ионы водорода:
2H++2e-→Н2.
Однако ионов водорода в водном растворе мало (если это только не раствор кислоты), кроме того, выделяющийся водород покрывает поверхность металла газовой пленкой, оттесняющей воду, так что коррозия в условиях слабого доступа воздуха (анаэробные условия) почти не идет, если нет в воде бактерий, способных использовать водород, выделяющийся при водородной деполяризации катода. К таковым относятся водородные и сульфатредуцирующие бактерии.
В присутствии анаэробных микроорганизмов происходит анодное окисление железа. Сульфатредуцирующие бактерии пользуются связанным кислородом из сульфатов. Мерой интенсивности биохимической коррозии является величина рН, так как она максимальна в случаях обилия бактерий.
4Fe→4Fe2++8е-.
При этом освободившиеся электроны восстанавливают ионы водорода, образовавшиеся из воды при диссоциации Н2О↔Н++ОН-, в элементарный водород:
8H++8е-→8Н (катодная реакция).
Анаэробные бактерии могут побудить этот элементарный водород каталитически реагировать с сульфатами:
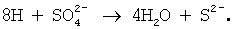
В качестве продуктов коррозии при этом могут образоваться:
Fe2++S2-→FeS (черный сульфид железа)
и
3Fe2++6OH-→3Fe(OH)2 (белый гидроксид железа (II)).
Не все штаммы сульфатвосстанавливающих бактерий катализируют восстановление сульфатов водородом. Так, в присутствии сульфата кальция и угольной кислоты происходят следующие превращения:
4Fe+CaSO4+2Н2СО3+2H2О→3Fe(ОН)2+FeS+Са(НСО3)2.
В отсутствие угольной кислоты реакция протекает по следующей схеме:
4Fe+CaSO4+4RH2O→3Fe(ОН)2+FeS+Са(ОН)2.
Из приведенных выше уравнений реакций следует, что железо непосредственно не взаимодействует с кислородом воздуха.
Коррозионный процесс, вызываемый сульфатвосстанавливающими бактериями, нельзя рассматривать изолированно от других химических реакций, которые также оказывают влияние. Так, H2S и СО2, образующиеся как продукты обмена веществ бактерий, могут растворяться во влажной среде и создавать агрессивную среду.
Нитратвосстанавливающие бактерии могут ускорять коррозию стали в морской воде в 1,5-1,7 раза. Восстановление азотной кислоты или ее солей можно выразить следующим уравнением:
4Fe+HNO3+5Н2О→4Fe(ОН)2+NH3.
Бактерии понижают значение рН вблизи стальной поверхности до 0,14. При благоприятных условиях для действия бактерий средняя скорость коррозии достигает 0,1338 г/(м2·ч) против 0,0176 г/(м2·ч) без участия бактерий. Благодаря деятельности восстановителей нитрата может происходить косвенная коррозия металла, так как денитрификация осуществляется за счет битумов и других соединений углерода, значит органические соединения окисляются бактериями, и процесс окисления служит источником энергии. При этом образуются коррозионно-активные соединения (например, СО2 и NH3), которые могут привести к электрохимической коррозии металла с образованием различных концентрационных элементов, а также к коррозии за счет углекислого газа.
Бактерии, образующие метан, обусловливают процесс коррозии, характеризуемый следующими реакциями:
4Fe=4Fe2++8е- (анодная реакция),
8Н2O+8е-=8OН-+8Н (катодная реакция).
Оба эти основных уравнения тождественны всем биохимическим реакциям, при которых выделяется водород. Разные бактерии отличаются лишь своим каталитическим действием. Энергия, необходимая бактериям, получается при восстановлении диоксида углерода
CO2+8Н=СН4+2Н2O.
Полная реакция протекает следующим образом:
4Fe+6Н2О+CO2=4Fe(ОН)2+СН4.
В качестве продукта коррозии образуется гидроксид железа (II). Наиболее благоприятными значениями рН являются 6,0-8,0. Бактерии, образующие метан, сосуществуют с сульфатвосстанавливающими бактериями и усиливают их способность к растворению железа.
При наличии аэробных микроорганизмов происходит анодное окисление железа в присутствии атмосферного кислорода. Окисление серы или неорганических сернистых соединений в аэробных условиях вызывается бактериями вида Tiobacillus thiooxydans. Энергия, необходимая для развития и роста серобактерий, возникает в результате окисления серы. Конечный продукт этого окисления - серная кислота.
Эти бактерии лучше всего развиваются в кислой среде (рН от 0 до 6) и производят много серной кислоты так, что концентрация ее достигает 10% (≈2 н. H2SO4), и разрушают до 66% используемого материала.
Серобактерии получают энергию, необходимую для их жизненных процессов, главным образом за счет окисления сероводорода. Реакция протекает следующим образом:
2H2S+O2=2H2O+2S.
Экспериментально установлено, что в присутствии серобактерий в грунтовой воде скорость коррозии может быть усилена в 11-13 раз. Стойкость углеродистой стали в этих условиях ниже, чем хромистой стали. Потеря железа из-за аэробной коррозии может достигать 30-100 мг/(дм2·сутки).
Железобактерии поглощают железо в ионном состоянии. Бактерии окисляют железо внутри своих клеток. Являясь аэробными, они потребляют кислород из воды.
Реакция окисления железа может протекать следующим образом:
2FeCO3+3Н2О+1/2O2=2Fe(ОН)3+2СО2.
Железобактерии получают энергию для своего развития за счет следующей реакции:
2Fe2++2Н2O+1/2O2→Fe2О3+4H+.
Как правило, продукты коррозии желто-красного, кровяного или коричнево-красного цвета.
Величина рН, при которой существуют железобактерии, лежит в пределах 4-10, а температура воды в интервале 5-40°С. В качестве источника углерода служит растворенный в воде диоксид углерода, а источником азота - аммиак.
2. В растворах, близких к нейтральным, коррозия железа протекает с кислородной деполяризацией.
Железо, корродируя внутри АУ в процессе эксплуатации технического устройства, переходит в раствор в виде гидратированных ионов (анодный процесс):
Fe+mH2O↔Fe2+·mH2О+2е-.
Катодный процесс выражается следующим уравнением реакции:
Н2О+1/2O2+2е-↔2OН-.
Гидратированные ионы железа и гидроксид-ионы образуют первичный продукт коррозии - гидроксид железа (II):
Fe2+·mH2О+2OН-→Fe(OH)2↓+mH2O,
который, взаимодействуя с растворенным в электролите кислородом, образует более труднорастворимый гидроксид железа (III) бурого цвета (вторичный продукт коррозии):
4Fe(OH)2+O2+2Н2O→4Fe(ОН)3↓
Эти продукты коррозии могут претерпевать дальнейшее превращение с образованием сложных гидратированных оксидов железа xFeO·yFe2O3·zH2O. Отличительной особенностью таких коррозионных процессов является их сложность и многостадийность в условиях кинематики и динамики механических движений.
Таким образом, при эксплуатации шариков имеет место появление в растворе бурого осадка и его постепенное осаждение на дне балансировочного кольца через отверстия в желобе. С течением времени размер шариков незначительно уменьшается. Этот процесс усиливается возникающим при движении корректирующей массы трением между шариками. Скорость коррозии шарика определяет глубину разрушения металла за единицу времени, например, мм/год.
Металл, вступивший в реакцию окисления, вытесняется с поверхности его за счет трения с соседними шариками. Поэтому коррозия поверхности металлических шариков способствует изменению моментов трения между шариками и стенками, дном желоба балансировочного кольца и шариков друг с другом. Нагрузочный момент немного возрастает и мощность, отбираемая приводом от источника электрической энергии, соответственно, возрастает незначительно, что фиксируется во время эксперимента. В то же время происходит снижение корректирующей массы и наблюдается увеличение предельной неуравновешенной массы. Таким образом, если относительная разница измеренных за некоторый промежуток времени Δt значений потребляемой мощности ΔPcp=Pcp(j+1)-Pcp(j)≥0, а критической неуравновешенной массы Δm=m(j+1)-m(j)>0, то правомерно сравнить эти значения с предварительно полученными данными для течения электрохимической коррозии углеродистой стали в нейтральной среде с кислородной деполяризацией. В случае их совпадения можно сделать заключение о наличии в исследуемой среде данного вида электрохимической коррозии.
Катодное восстановление кислорода в нейтральных растворах протекает по следующей кинетической схеме [3]:
1) 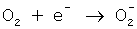 (образование молекулярного иона кислорода);
(образование молекулярного иона кислорода);
2) 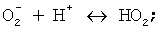
3) 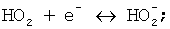
4) 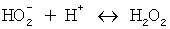 (образование пероксида водорода);
(образование пероксида водорода);
5) 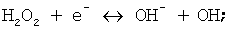
6)  (возникновение гидроксид-иона).
(возникновение гидроксид-иона).
Суммируя реакции, получим
O2+2H2O+4e-→4OH-.
В щелочных растворах металлы, образующие амфотерные оксиды, окисляются молекулами воды, восстанавливая их до Н2. Катодное восстановление кислорода в щелочных растворах протекает по следующей кинетической схеме:
1) 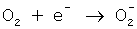 (образование молекулярного иона кислорода);
(образование молекулярного иона кислорода);
2) 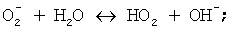
3) 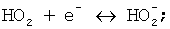
4) 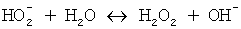 (образование пероксида водорода);
(образование пероксида водорода);
5) 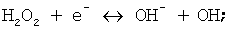
6) 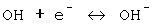 (возникновение гидроксид-иона).
(возникновение гидроксид-иона).
Скорость коррозии углеродистой стали с кислородной деполяризацией определяется диффузией кислорода.
3. Механизм анодного растворения железа в кислых средах предложен К.Хойслером [4] с учетом образования на поверхности железного электрода промежуточных адсорбционных комплексов:
1) Fe+ОН-↔[FeOH]адс+е-;
2) [FeOH]адс+Fe↔Fe[FeOH]адс;
3) Fe[FeOH]адс+ОН-→[FeOH]адс+[FeOH]++2е-;
4) Fe[OH]++H+↔Fe2++H2O.
Для кислых сульфатных растворов Дж.Бокрисом с соавторами [5] был предложен другой механизм:
1) Fe+ОН-↔[FeOH]адс+е-;
2) [FeOH]адс→[FeOH]++е-;
3) Fe[ОН]+↔Fe2++ОН-.
Механизм катодного выделения водорода в кислых средах подробно исследован в работах А.Н.Фрумкина с соавторами [6], в соответствии с которыми в отсутствие кислорода протекают следующие процессы:
1 процесс:
а) H3O++e-→Hадс+H2O (разряд водородных ионов);
б) Hадс+H2O→H3O++e- (ионизация адсорбированного водорода).
2 процесс:
а) Надс+Н3О++е-↔Н2О+Н2 (электрохимическая десорбция);
б) 2Hадс↔Н2 (рекомбинационный механизм).
В кислых растворах металл окисляется преимущественно Н3О+-ионами, активность которых достаточно велика. Катодный процесс, протекающий на поверхности железа, представляется схемой:
Fe+H3O++е-↔Fe|Надс+H2О;
Fe|Надс+Fe|Надс→2Fe+H2;
Fe|Надс+H3O++е-→Fe+H2+H2O.
Молекулы водорода могут раствориться в электролите или образуются пузырьки газа, которые покидают поверхность металла, достигнув размеров, необходимых для отрыва от поверхности шариков. Возможно удаление водорода в окружающую атмосферу через отверстия в крышке за счет диффузии от пересыщенного раствора. Кроме этого, происходит водородное охрупчивание стали ввиду растворения водорода в железе и стали (наводораживание).
Металл, вступивший в реакцию окисления, интенсивно вытесняется с поверхности его за счет трения с соседними шариками в связи с наводораживанием стали. Поэтому интенсивная коррозия поверхности металлических шариков способствует быстрому изменению моментов трения между шариками и стенками, дном желоба балансировочного кольца и шариков друг с другом. Кроме того, происходит удаление водорода в окружающую атмосферу через отверстия в крышке. Все это обусловливает снижение нагрузочного момента, и мощность, отбираемая приводом от источника электрической энергии, соответственно, уменьшается, что фиксируется во время эксперимента. В то же время происходит снижение корректирующей массы и наблюдается увеличение предельной неуравновешенной массы на стадии разгона неуравновешенного ротора. Таким образом, если относительная разница измеренных за некоторый промежуток времени Δt значений потребляемой мощности ΔPcp=Pcp(j+1)-Pcp(j)<0, а критической неуравновешенной массы Δm=m(j+1)-m(j)>0, то правомерно сравнить эти значения с предварительно полученными данными для течения электрохимической коррозии углеродистой стали в нейтральной среде с водородной деполяризацией. В случае их совпадения можно сделать заключение о наличии в исследуемой среде данного вида электрохимической коррозии.
Источники информации
1. Патент РФ №2094773, 1997.
2. Патент РФ №2224238, кл. G01N 17/00, 2004.
3. Скорчеллетти В.В. Теоретические основы коррозии металлов. Л.: Химия, 1973. 264 с.
4. Heusler K.E. // Z. Elektrochem. 1958. Bd.62. № 5. S.582
5. Bockris J.O′M, Drazic D., Despic A.R. // Electrochim. acta. 1961. V.4. № 4. P.325.
6. Фрумкин А.Н. и др. Кинетика электродных процессов. М., МГУ, 1952.

Способ определения коррозионных характеристик в конструкциях бытовых стиральных машин, содержащих бак и установленный с возможностью вращения относительно вертикальной оси отжимной резервуар-барабан, входящие в состав внутренней подвижной части стиральной машины балансировочное кольцо с крышкой и желобом, четыре опоры в виде штоков, которые ориентированы в пространстве вертикально и шарнирно соединены с корпусом и внутренней подвижной частью стиральной машины. Нижний конец опор соединен с внутренней подвижной частью выше ее центра тяжести так, что все точки внутренней подвижной части в случае вращения неуравновешенного барабана при отклонении от положения равновесия в вертикальной плоскости, проходящей через опоры и центр ее тяжести, движутся поступательно. Внутренняя подвижная часть имеет такую геометрию, что центр ее тяжести находится выше дна барабана. На проволоке, протянутой через два отверстия, выполненных в стенке барабана, на высоте, соответствующей положению центра тяжести внутренней подвижной части, подвешены грузы различной массы. Внутри балансировочного кольца, установленного в барабане на высоте центра тяжести внутренней подвижной части, размещены испытуемые образцы в виде шариков одинакового размера из углеродистой стали, которые размещаются в ограниченном секторе, образованном связанными подвижными радиальными перегородками. Шарики находятся в соприкосновении друг с другом. При этом внутреннюю полость балансировочного кольца заполняют жидкостями, состав и природа которых до начала испытаний не известны. На электроприводе, закрепленном неподвижно в нижней части внутренней подвижной части, устанавливают электронный измеритель потребляемой мощности. Сначала закрывают на время движения отверстия в крышке балансировочного кольца пробками из пластичного материала, осуществляют разгон барабана без грузов (неуравновешенной массы) и измеряют ряд значений мощности и вычисляют их среднее значение. Подвешивают к стенке барабана дополнительные грузы, определяют критическую неуравновешенную массу, при наличии которой барабан при разгоне задевает стенку корпуса. После совершения трех оборотов вокруг своей вертикальной оси в определенный момент времени и далее через некоторый промежуток времени совершают такие же измерения и получают значения неуравновешенной присоединяемой массы и средней мощности. Рассчитывают некоторые значения изменения средней мощности и, исходя из определенных математических предпосылок, определяют вид коррозионного процесса. Изобретение обеспечивает расширение спектра видов электрохимических и биохимических коррозионных процессов. 7 ил.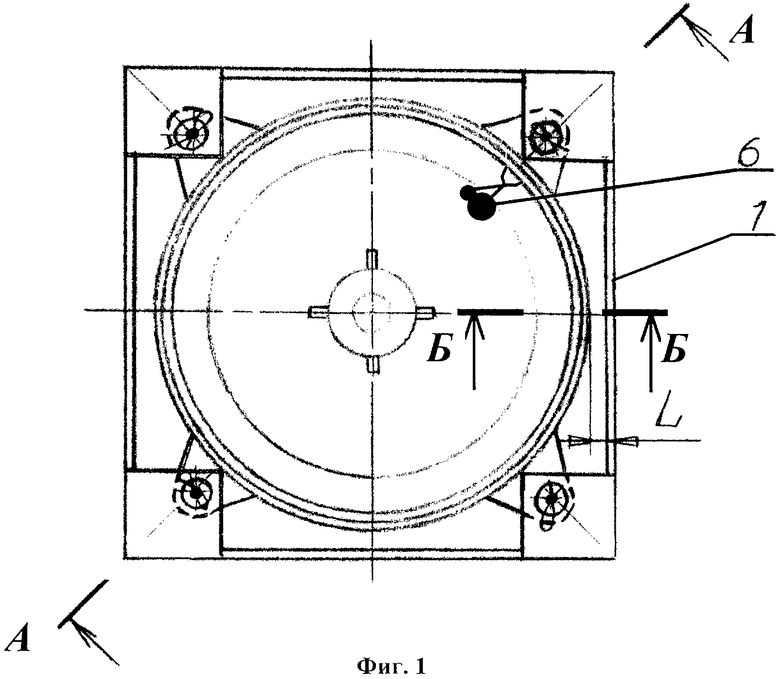
Способ определения коррозионных характеристик в конструкциях бытовых стиральных машин, содержащих бак и установленный с возможностью вращения относительно вертикальной оси отжимной резервуар-барабан, входящие в состав внутренней подвижной части стиральной машины, балансировочное кольцо с крышкой и желобом, четыре опоры в виде штоков, которые ориентированы в пространстве вертикально и шарнирно соединены с корпусом и внутренней подвижной частью стиральной машины, нижний конец опор соединен с внутренней подвижной частью выше ее центра тяжести так, что все точки внутренней подвижной части в случае вращения неуравновешенного барабана, при отклонении от положения равновесия в вертикальной плоскости, проходящей через опоры и центр ее тяжести, движутся поступательно, причем снята верхняя панель стиральной машины, измерены и выравнены расстояния между краем бака и стенкой корпуса по всем четырем направлениям путем установки под опоры компенсирующих шайб, и внутренняя подвижная часть имеет такую геометрию, что центр ее тяжести находится выше дна барабана, в стенке барабана выполнены два отверстия, через которые протянута проволока для грузов различной массы, и внутри балансировочного кольца размещают испытуемые образцы в виде шариков одинакового размера из углеродистой стали, при этом они размещаются в ограниченном секторе, образованном связанными подвижными радиальными перегородками, и находятся в соприкосновении друг с другом, отличающийся тем, что для определения отдельных видов электрохимических и биохимических коррозионных процессов грузы различной массы и балансировочное кольцо располагают на высоте центра тяжести внутренней подвижной части, внутреннюю полость балансировочного кольца заполняют коррозионной средой, на внутренней боковой поверхности большего радиуса балансировочного кольца выполняют дополнительные радиальные перегородки с зазубринами, в желобе делают отверстия для удаления продуктов коррозии, в крышке балансировочного кольца выполняют отверстия для выхода газов и летучих продуктов коррозии, а на электроприводе, закрепленном неподвижно в нижней части внутренней подвижной части, устанавливают электронный измеритель потребляемой мощности и закрывают на время движения отверстия в крышке балансировочного кольца пробками из пластичного материала, осуществляют разгон барабана без грузов (неуравновешенной массы) и измеряют ряд значений мощности Рпуск, P1,..., Pi,..., Pk и вычисляют их среднее значение Pcp(j), где k - число измерений во время разгона, на основе схем умножения двух сигналов, пропорциональных значениям напряжения и тока, последовательно в течение разгона барабана и совершения им трех оборотов вокруг своей вертикальной оси и затем, подвешивая к стенке барабана дополнительные грузы, определяют критическую неуравновешенную массу mj, при наличии которой барабан при разгоне задевает стенку корпуса в заданных габаритах рабочей зоны внутренней подвижной части, после совершения трех оборотов вокруг своей вертикальной оси в момент времени tj, где j - номер измерения, и далее через промежуток времени Δt=tj+1-tj в момент времени tj+1, совершая такие же измерения, получают следующие значения средней мощности 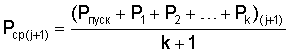
и неуравновешенной присоединяемой массы mj+1, причем измерение мощности и присоединяемой неуравновешенной массы делают периодически в течение процесса исследования природы жидкости, и если относительная разница 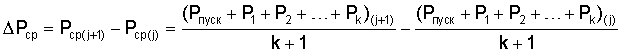 больше нуля и Δm=m(j+1)-m(j)≤0, то сравнивают эти значения с предварительно полученными данными для течения биохимической коррозии в присутствии аэробных и анаэробных микроорганизмов и в случае их совпадения делают заключение о наличии в исследуемой коррозионной среде данного вида биохимической коррозии, если разница Δm=m(j+1)-m(j)>0 и Pcp(j+1)≥Pcp(j), то сравнивают эти значения с предварительно полученными данными для течения электрохимической коррозии с кислородной деполяризацией и в случае их совпадения делают заключение о наличии в исследуемой коррозионной среде данного вида электрохимической коррозии, если разница Δm=m(j+1)-m(j)>0 и Pcp(j+1)<Pcp(j), то сравнивают эти значения с предварительно полученными данными для течения электрохимической коррозии с водородной деполяризацией и в случае их совпадения делают заключение о наличии в исследуемой коррозионной среде данного вида электрохимической коррозии.
больше нуля и Δm=m(j+1)-m(j)≤0, то сравнивают эти значения с предварительно полученными данными для течения биохимической коррозии в присутствии аэробных и анаэробных микроорганизмов и в случае их совпадения делают заключение о наличии в исследуемой коррозионной среде данного вида биохимической коррозии, если разница Δm=m(j+1)-m(j)>0 и Pcp(j+1)≥Pcp(j), то сравнивают эти значения с предварительно полученными данными для течения электрохимической коррозии с кислородной деполяризацией и в случае их совпадения делают заключение о наличии в исследуемой коррозионной среде данного вида электрохимической коррозии, если разница Δm=m(j+1)-m(j)>0 и Pcp(j+1)<Pcp(j), то сравнивают эти значения с предварительно полученными данными для течения электрохимической коррозии с водородной деполяризацией и в случае их совпадения делают заключение о наличии в исследуемой коррозионной среде данного вида электрохимической коррозии.
| УСТРОЙСТВО ДЛЯ ОПРЕДЕЛЕНИЯ СКОРОСТИ КОРРОЗИИ УГЛЕРОДИСТОЙ СТАЛИ 10 | 2002 |
|
RU2224238C1 |
| Способ определения вида коррозии алюминия и его сплавов | 1990 |
|
SU1823924A3 |
| Способ определения вида коррозии металлов и сплавов на основе железа, алюминия и магния | 1988 |
|
SU1635078A1 |
| Плавающая оптическая головка | 1984 |
|
SU1167650A1 |
| JP 62162949 A, 18.07.1987 | |||
| JP 59013937 A, 24.01.1984. | |||
Авторы
Даты
2008-03-20—Публикация
2005-11-24—Подача