Предлагаемое изобретение относится к медицине, а именно к хирургии, и может быть использовано для хирургического лечения сахарного диабета в центрах трансплантологии и в специализированных лечебных учреждениях.
Проблема лечения сахарного диабета является чрезвычайно актуальной. Главные причины этого заключаются в распространенности, тяжести и осложнениях этого заболевания. Диабет ведет к повышению смертности и инвалидности в 2-3 раза. Главная причина инвалидности - тяжелые осложнения сахарного диабета (ретино- и нейропатия, поражение периферических сосудов, нефропатия).
Классическая инсулинотерапия связана с трудностями индивидуального подбора дозы и вида препарата, развитием инсулинорезистентности, появлением аллергических реакций и липодистрофий. Кроме того, экзогенное введение инсулина не в состоянии предотвратить прогрессирование вторичных осложнений диабета.
Аллотрансплантация поджелудочной железы - единственный в настоящее время метод, позволяющий стойко стабилизировать уровень гликемии у больных инсулинрезистентным инсулинзависимым сахарным диабетом и таким образом предотвратить прогрессирование осложнений.
Спорным остается вопрос о хирургической организации венозного оттока от трансплантата - в портальную систему или в системный кровоток. Имеются данные, что венозное дренирование трансплантата в большой круг кровообращения приводит к гиперинсулинемии в послеоперационном периоде. Вместе с тем портальное дренирование трансплантата не является необходимым условием для обеспечения нормальной печеночной регуляции углеводного обмена. Тем не менее, предложенные с этой целью методики (Dubernard J.M., Sutherland D., 1989; Sutherland D., Gores P.F., Farneu A.C., 1993) отличаются высокой травматичностью, так как предполагают полное прекращение кровотока по системе нижней брыжеечной артерии и вены, что при условии недостаточного развития толстокишечных аркад и путей коллатерального кровотока может привести к тяжелым осложнениям, вплоть до некроза части толстой кишки.
Все вышесказанное обусловливает актуальность исследований по разработке высокоэффективных хирургических технологий сегментарной трансплантации поджелудочной железы при инсулинрезистентном сахарном диабете.
Известен способ сегментарной трансплантации поджелудочной железы на подвздошные сосуды реципиента [Молитвословов А.Б., Тимошин А.Д. Пересадка поджелудочной железы. - в кн.: Введение в клиническую трансплантологию, под ред. Константинова А.Б., Дземешкевича С.Л. - М. - 1993. - С.162-166]. Способ заключается в заборе дистального сегмента (хвоста и тела) поджелудочной железы у донора, его консервацию и трансплантацию реципиенту. Реваскуляризацию трансплантата осуществляют последовательным формированием артериального и венозного анастомозов между проксимальными культями селезеночной артерии и вены трансплантата и общими подвздошными артерией и веной реципиента по типу «конец в бок».
Недостатки:
а) Способ не предполагает естественного портального оттока венозной крови от трансплантированной поджелудочной железы, что нарушает физиологический метаболизм инсулина и углеводов в печени, может привести к выраженной гиперинсулинемии. В результате ухудшаются показатели компенсации углеводного обмена в посттрансплантационном периоде и уменьшаются сроки функционирования трансплантата.
б) Вследствие трансплантации поджелудочной железы на подвздошные сосуды невозможно впоследствии осуществить формирование панкреатоэнтероанастомоза с проксимальными отделами тонкой кишки, что существенно нарушает механизмы регуляции внешнесекреторной функции пересаженной поджелудочной железы, способствуя быстрой функциональной деградации экзокринной, а затем и эндокринной паренхимы трансплантата.
За ближайший аналог нами принят способ сегментарной трансплантации поджелудочной железы на нижние брыжеечные сосуды [Федоров В.Д., Буриев И.М., Икрамов Р.З. Хирургическая панкреатология. - М.: Медицина. - 1999. - С.196-197]. Способ заключается в заборе дистального сегмента (хвоста и тела) поджелудочной железы у донора, его консервацию и трансплантацию реципиенту. Реваскуляризацию трансплантата осуществляют последовательным формированием артериального и венозного анастомозов между проксимальными культями селезеночной артерии и вены трансплантата и проксимальной и дистальной культями нижних брыжеечных артерии и вены реципиента по типу «конец в конец».
Недостатки:
а) Способ предполагает полное прекращение кровотока по системе нижней брыжеечной артерии, что при недостаточном развитии ободочных межсосудистых аркад и коллатералей может привести к острым нарушениям кровоснабжения части толстой кишки и ее некрозу.
б) Ретроперитонеальное расположение трансплантированного сегмента поджелудочной железы при данном способе реваскуляризации также оказывается достаточно низким для адекватного формирования панкреатоэнтероанастомоза с проксимальными отделами тонкой кишки, а тем более двенадцатиперстной кишкой. Это существенно нарушает механизмы регуляции внешнесекреторной функции пересаженной поджелудочной железы, способствуя быстрой функциональной деградации экзокринной, а затем и эндокринной паренхимы трансплантата.
Задачи:
1. Разработать способ, обеспечивающий сохранение кровотока по системе нижней брыжеечной артерии.
2. Обеспечить оптимальное расположение трансплантированного сегмента поджелудочной железы для адекватного формирования панкреатоэнтероанастомоза с проксимальными отделами тонкой кишки.
Для решения поставленных задач формируют венозный анастомоз с нижней брыжеечной веной на уровне нижней горизонтальной ветви двенадцатиперстной кишки, а артериальную реваскуляризацию трансплантата осуществляют путем анастомозирования дистального конца селезеночной артерии с левой общей подвздошной артерией реципиента по типу «конец в бок», при этом проксимальный конец селезеночной артерии трансплантата лигируют.
По отношению к ближайшему аналогу заявляемый способ имеет следующий технический результат.
Формирование венозного анастомоза с нижней брыжеечной веной как можно более краниально, то есть на уровне нижней горизонтальной ветви двенадцатиперстной кишки позволяет добиться максимально высокого расположения трансплантата, что делает технологически выполнимым формирование панкреатоэнтероанастомоза с первой петлей тощей кишки или двенадцатиперстной кишкой. Формирование артериального анастомоза осуществляется с дистальным концом селезеночной артерии трансплантата и левой подвздошной артерией реципиента по типу «конец в бок», что позволяет избежать прекращения кровотока по системе нижней брыжеечной артерии. При недостаточном развитии ободочных межсосудистых аркад и коллатералей способ позволяет избежать острого нарушения кровоснабжения части толстой кишки и ее некроза, позволяет адекватно укрыть его брыжейкой сигмовидной кишки и изолировать от окружающих тканей, что уменьшает риск послеоперационных осложнений и способствует ускорению реиннервации поджелудочной железы.
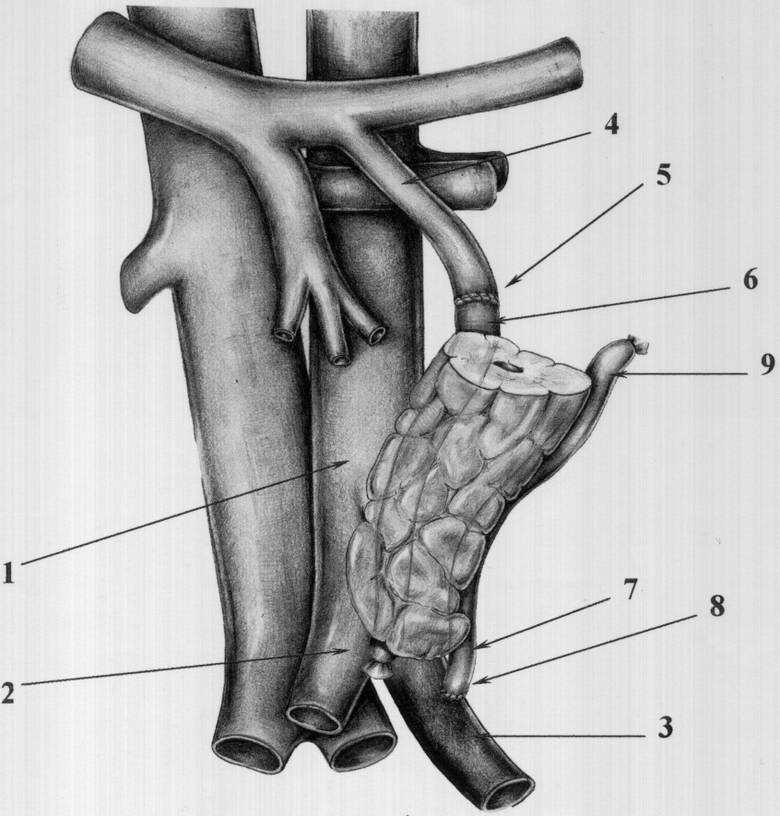
Способ поясняется чертежом, где
1 - брюшной отдел аорты; 2 - зона бифуркации аорты; 3 - левая подвздошная артерия; 4 - нижняя брыжеечная вена; 5 - анастомоз между селезеночной веной трансплантата и культей нижней брыжеечной вены; 6 - селезеночная вена панкреатического трансплантата; 7 - дистальный конец селезеночной артерии трансплантата; 8 - анастомоз между дистальным концом селезеночной артерии панкреатического трансплантата и левой подвздошной артерией; 9 - проксимальный конец селезеночной артерии.
После традиционных этапов забора дистального сегмента (хвоста и тела) поджелудочной железы у трупа или живого родственного донора и его консервации, осуществления доступа в брюшную полость реципиента вскрывают париетальную брюшину от дуодено-еюнального угла до бифуркации аорты. Визуализируют брюшной отдел аорты (1), зону ее бифуркации (2), левую подвздошную артерию (3). Мобилизуют верхнюю часть брыжейки сигмовидной кишки от предпочечной фасции. Выделяют дистальную (краниальную) часть нижней брыжеечной вены (4), пересекают ее на уровне нижней горизонтальной ветви двенадцатиперстной кишки, проксимальный (каудальный) конец вены лигируют. Трансплантат укладывают забрюшинно в сформированное ложе между предпочечной фасцией и брыжейкой сигмовидной кишки. Формируют концевой сосудистый анастомоз (5) между селезеночной веной трансплантата (6) и культей нижней брыжеечной вены, после чего формируют анастомоз (8) между дистальным концом селезеночной артерии (7) панкреатического трансплантата и левой общей подвздошной артерией по типу «конец в бок» после полного предварительного отжатия последней. Снимают зажим с нижней брыжеечной вены, затем включают артериальный кровоток, восстанавливают кровоснабжение панкреатического трансплантата. При этом по интенсивности кровотечения из проксимального конца селезеночной артерии (9) трансплантата проверяют адекватность артериального кровоснабжения сегмента поджелудочной железы, после чего проксимальную культю селезеночной артерии лигируют. Формируют панкреатоэнтероанастомоз с первой петлей тощей кишки традиционной техникой. Панкреатический трансплантат укрывают сверху брыжейкой сигмовидной кишки, которую фиксируют отдельными швами по верхнему и нижнему краю поджелудочной железы к предпочечной фасции.
Заявляемый способ сегментарной трансплантации поджелудочной железы апробирован у 6 больных инсулинрезистентным сахарным диабетом. Во всех случаях выполнена близкородственная трансплантация дистального сегмента (тело и хвост) поджелудочной железы. Группу сравнения составили 10 больных, у которых осуществлялась традиционная реваскуляризация панкреатического трансплантата на общие или наружные подвздошные сосуды.
В группе пациентов, на которых был апробирован заявляемый способ сегментарной трансплантации поджелудочной железы, летальных исходов не отмечено, частота послеоперационных осложнений составила 16,7%, функция трансплантата - первичная, полная коррекция углеводного обмена с отказом от приема экзогенного инсулина отмечена у всех больных, 3-летняя выживаемость трансплантата и реципиентов - 100%, гиперинсулинемии в послеоперационном периоде не отмечено. У всех пациентов основной группы был сформирован панкреатоэнтероанастомоз с У-образно отключенной первой петлей тощей кишки.
В группе сравнения летальных исходов не было, общая послеоперационных осложнений составила 40,0%, причем у одного больного в посттрансплантационном периоде развилась острая недостаточность кровоснажения нисходящей ободочной кишки с ее некрозом, что потребовало выполнения релапаротомии и левосторонней гемиколэктомии. Полная компенсация углеводного обмена с отказом от экзогенного инсулина достигнута у 60,0%. 3-летняя выживаемость трансплантата составила 70,0%, 3-летняя выживаемость реципиентов - 80,0%. При применении традиционной технологии сегментарной трансплантации поджелудочной железы возможность формирования панкреатоэнтероанастомоза имелась только 4 (40,0%) больных, в остальных случаях был сформирован панкреатоцистоанастомоз. Гиперинсулинемия в посттрансплантационном периоде отмечена у 3 (30,0%) больных.
Возможность практического использования заявляемого способа иллюстрируется примером его выполнения в клинической практике.
Пример. Больной Г., 25 лет поступил в клинику 11.02.2002 г. с диагнозом инсулинрезистентный сахарный диабет, осложненное течение, диабетическая нефропатия средней степени тяжести. Анамнез заболевания 14 лет. Инсулинзависимость с 15 лет. Инсулинрезистентность с 24 лет. Уровень глюкозы натощак при поступлении 20,6 ммоль/л. В анамнезе две кетоацидотические комы. После обследования и подготовки больному 19.02.02 г. выполнена близкородственная сегментарная трансплантация поджелудочной железы заявляемым способом (донор - мать больного). Послеоперационный период протекал без осложнений. Полная компенсация углеводного обмена с отказом от использования экзогенного инсулина достигнута на 1-е сутки послеоперационного периода. Уровень глюкозы крови натощак при выписке - 5,7 ммоль/л. Больной выписан из клиники в относительно удовлетворительном состоянии на 12-е сутки после операции (03.03.2002 г.). После трансплантации больной неоднократно обследован. Выявлено: компенсация углеводного обмена адекватная, стойкая, необходимости в приеме экзогенного инсулина нет, достигнута ремиссия диабетической нефропатии, больной придерживается рекомендованной диеты. Через 3 года после операции - функция трансплантата удовлетворительная.
Таким образом, применение заявляемого способа позволяет осуществить адекватную реваскуляризацию панкреатического трансплантата, обеспечить физиологический отток венозной крови от него в портальную систему, избежать нарушения кровоснабжения толстой кишки, обеспечить оптимальные условия для формирования панкреатоэнтероанастомоза с проксимальными отделами тонкой кишки. Изобретение практически осуществимо, является доступным и высокоэффективным способом радикального лечения инсулинрезистентного сахарного диабета.
Социально-экономическое значение. Разработанный способ позволяет уменьшить частоту ранних послеоперационных осложнений, увеличить сроки функционирования панкреатического трансплантата, повысить отдаленную выживаемость больных после сегментарной трансплантации поджелудочной железы.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ СЕГМЕНТАРНОЙ ТРАНСПЛАНТАЦИИ ПОДЖЕЛУДОЧНОЙ ЖЕЛЕЗЫ | 2006 |
|
RU2316265C1 |
| СПОСОБ СЕГМЕНТАРНОЙ ТРАНСПЛАНТАЦИИ ПОДЖЕЛУДОЧНОЙ ЖЕЛЕЗЫ | 2006 |
|
RU2316266C1 |
| СПОСОБ СЕГМЕНТАРНОЙ ТРАНСПЛАНТАЦИИ ПОДЖЕЛУДОЧНОЙ ЖЕЛЕЗЫ | 2006 |
|
RU2311135C1 |
| СПОСОБ СЕГМЕНТАРНОЙ ТРАНСПЛАНТАЦИИ ПОДЖЕЛУДОЧНОЙ ЖЕЛЕЗЫ | 2006 |
|
RU2316264C1 |
| СПОСОБ СЕГМЕНТАРНОЙ ТРАНСПЛАНТАЦИИ ПОДЖЕЛУДОЧНОЙ ЖЕЛЕЗЫ | 2006 |
|
RU2311880C1 |
| Способ трансплантации поджелудочной железы | 2021 |
|
RU2757632C1 |
| СПОСОБ ПАНКРЕАТОДУОДЕНАЛЬНОЙ РЕЗЕКЦИИ ПРИ МЕСТНОРАСПРОСТРАНЕННОМ РАКЕ ПЕРИАМПУЛЯРНОЙ ОБЛАСТИ С ОПУХОЛЕВОЙ ИНВАЗИЕЙ УСТЬЯ ВОРОТНОЙ ВЕНЫ | 2006 |
|
RU2311875C1 |
| СПОСОБ ПАНКРЕАТОДУОДЕНАЛЬНОЙ РЕЗЕКЦИИ ПРИ МЕСТНОРАСПРОСТРАНЕННОМ РАКЕ ПЕРИАМПУЛЯРНОЙ ОБЛАСТИ С ОПУХОЛЕВОЙ ИНВАЗИЕЙ ВЕРХНЕЙ БРЫЖЕЕЧНОЙ ВЕНЫ | 2006 |
|
RU2316270C1 |
| СПОСОБ ПАНКРЕАТОДУОДЕНАЛЬНОЙ РЕЗЕКЦИИ ПРИ МЕСТНОРАСПРОСТРАНЕННОМ РАКЕ ПЕРИАМПУЛЯРНОЙ ОБЛАСТИ С ОБШИРНОЙ ОПУХОЛЕВОЙ ИНВАЗИЕЙ МАГИСТРАЛЬНЫХ ВЕН МЕЗЕНТЕРИКО-ПОРТАЛЬНОЙ СИСТЕМЫ | 2006 |
|
RU2312608C1 |
| СПОСОБ ТРАНСПЛАНТАЦИИ ПОДЖЕЛУДОЧНОЙ ЖЕЛЕЗЫ | 2021 |
|
RU2760537C1 |
Изобретение относится к медицине, а именно к хирургии и трансплантологии. Выполняют забор дистального сегмента поджелудочной железы у донора, его консервацию и трансплантацию реципиенту с обеспечением венозного оттока от трансплантата в систему воротной вены. При этом формируют венозный анастомоз между селезеночной веной трансплантата и нижней брыжеечной веной на уровне нижней горизонтальной ветви двенадцатиперстной кишки. Артериальную реваскуляризацию трансплантата осуществляют путем анастомозирования дистального конца селезеночной артерии с левой общей подвздошной артерией реципиента по типу "конец в бок", при этом проксимальный конец селезеночной артерии трансплантата лигируют. Способ позволяет избежать прекращения кровотока по системе нижней брыжеечной артерии, острого нарушения кровоснабжения части толстой кишки и ее некроза, позволяет уменьшить риск послеоперационных осложнений, способствует ускорению реиннервации поджелудочной железы. 1 ил.
Способ сегментарной трансплантации поджелудочной железы, включающий забор дистального сегмента поджелудочной железы у донора, его консервацию и трансплантацию реципиенту с обеспечением венозного оттока от трансплантата в систему воротной вены, отличающийся тем, что формируют венозный анастомоз между селезеночной веной трансплантата и нижней брыжеечной веной на уровне нижней горизонтальной ветви двенадцатиперстной кишки, а артериальную реваскуляризацию трансплантата осуществляют путем анастомозирования дистального конца селезеночной артерии с левой общей подвздошной артерией реципиента по типу "конец в бок", при этом проксимальный конец селезеночной артерии трансплантата лигируют.
| ФЕДОРОВ В.Д | |||
| и др | |||
| Хирургическая панкреатология | |||
| - М.: Медицина, 1999, с.193-203 | |||
| ПОТАШЕВ Л.В | |||
| и др | |||
| Трансплантация поджелудочной железы | |||
| Вестник хирургии им | |||
| И.И.Грекова, 2000, №2, с.123-126 | |||
| Рекламный прибор | 1925 |
|
SU3001A1 |
| SHAPIRA Z | |||
| et al | |||
| Pancreas transplantation, J | |||
| Pediatr Endocrinol Metab, 1999 Jan-Feb; 12(1):3-15. | |||
Авторы
Даты
2008-05-27—Публикация
2006-04-07—Подача