Настоящее изобретение относится к новым производным бензотиазол-4,7-диона и бензоксазол-4,7-диона, которые ингибируют cdc25-фосфатазы, в частности cdc25-C-фосфатазу, и/или CD45-фосфатазу.
Регуляция перехода из одной фазы в другую клеточного цикла во время митоза или мейоза обеспечивается группой белков с ферментативной активностью, которые связаны с различными состояниями фосфорилирования. Данные состояния регулируются двумя большими классами ферментов: киназами и фосфатазами.
Синхронизация различных фаз клеточного цикла позволяет, таким образом, реорганизовать клеточную структуру в каждом цикле во всем живом мире (у микроорганизмов, дрожжей, позвоночных, растений). Среди киназ циклин-зависимые киназы (СДК) играют основную роль в данной регуляции клеточного цикла. Ферментативная активность данных различных КДК регулируется двумя другими семействами ферментов, которые «работают» противоположно (Jessus and Ozon, Prog. Cell Cycle Res. (1995), 1, 215-228). Первые включают киназы такие, как Wee1 и Mik1, которые дезактивируют СДК фосфорилированием некоторых аминокислот (Den Haese et al., Mol. Biol. Cell (1995), 6, 371-385). Вторые включают фосфатазы такие, как Сdc25, которые активируют СДК дефосфорилированием остатков тирозина и треонина СДК (Gould et al., Science (1990), 250, 1573-1576).
Фосфатазы подразделяются на 3 группы: серин/треонин-фосфатазы (РРазы), тирозинфосфатазы (РТР) и фосфатазы с двойной специфичностью (DSPазы). Данные фосфатазы играют важную роль в регуляции многочисленных клеточных функций.
В отношении cdc25-фосфатаз человека, то 3 гена (cdc25-A, cdc25-B и cdc25-C) кодируют cdc25-белки. Кроме того, идентифицированы различные варианты в результате альтернативного сплайсинга cdc25B-гена: ими являются cdc25B1, cdc25B2 и cdc25B3 (Baldin et al., Oncogene (1997), 14, 2485-2495).
В настоящее время хорошо известна роль Сdc25-фосфатаз в онкогенезе, и механизм действия данных фосфатаз описывается, в частности, в следующих источниках: Galaktionov et al., Science (1995), 269, 1575-1577; Galaktionov et al., Nature (1996), 382, 511-517, и Mailand et al., Science (2000), 288, 1425-1429.
В частности, в настоящее время сообщается о гиперэкспрессии различных форм cdc25 в многочисленных видах опухолей человека:
рак молочной железы: смотри Cangi et al., Resume 2984, AACR meeting San Francisco, 2000);
лимфомы: смотри Hernandez et al., Int. J. Cancer (2000), 89, 148-152, и Hernandez et al., Cancer Res. (1998), 58, 1762-1767;
опухоли шеи и головы: смотри Gasparotto et al., Cancer Res. (1997), 57, 2366-2368.
Кроме того, группа E.Sausville сообщает о наличии обратной корреляции между уровнем экспрессии cdc25-B в 60 линиях и их чувствительностью к ингибиторам CDK, на основании чего можно предположить, что присутствие cdc25 может быть причиной возникновения резистентности к некоторым противоопухолевым средствам и конкретнее к ингибиторам CDK (Hose et al., Proceedings of AACR, Abstract 3571, San Francisco, 2000).
Следовательно, в настоящее время в фармацевтической промышленности среди других мишеней проводится поиск соединений, способных ингибировать Сdc25-фосфатазы для использования их в качестве противоопухолевых средств.
Также Сdc25-фосфатазы играют роль в развитии нейродегенеративных заболеваний таких, как болезнь Альцгеймера (смотри Zhou et al., Cell Mol. Life Sci. (1999), 56 (9-10), 788-806; Ding et al., Am. J. Pathol. (2000), 157(6), 1983-90; Vincent et al., Neuroscience (2001), 105 (3), 639-50) так, что в результате также возможно обеспечение соединений, обладающих ингибирующей активностью в отношении данных фосфатаз для лечения подобных заболеваний.
Другой проблемой, на которую направлено изобретение, является поиск лекарственных препаратов, предназначенных для профилактики или лечения отторжения трансплантатов органов или для лечения аутоиммунных заболеваний. При данных нарушениях/заболеваниях происходит неадекватная активация лимфоцитов и моноцитов/макрофагов. Иммуносупрессоры, известные в настоящее время, обладают побочными эффектами, которые трудно снизить или модифицировать продуктами, специфически направленными на сигнальные пути в гемопоэтических клетках, которые инициируют и поддерживают воспаление.
CD45-фосфатаза играет решающую роль в передаче сигналов от рецепторов на Т-лимфоцитах регуляцией фосфорилирования и активности тирозинкиназ семейства src, отрицательной регуляцией сайтов р56lck и p59fyn, способных к дефосфорилированию.
Следовательно, CD45-фосфатаза является потенциальной мишенью при лечении иммунных заболеваний. Фактически, блокирование CD45-фосфатазы анти-CD45-антителами подавляет активацию Т-лимфоцитов in vitro (Prickett and Hart, Immunology (1990), 69, 250-256). Аналогичным образом, Т-лимфоциты трансгенных мышей, не экспрессирующих CD45 (мыши полученные методом «нокаута» CD45) не отвечают на стимуляцию антигеном (Trowbridge and Thomas, Annu. Rev. Immunol. (1994), 12, 85-116).
Кроме того, CD45 может дефосфорилировать субъединицу, связанную с Lyn, которая будет «запускать» поток кальция и активацию тучных клеток. Hamaguchi et al. (Bioorg. Med. Chem. Lett. (2000), 10, 2657-2660) показали, что специфический ингибитор CD45 (со значением IC50, равным 280 нМ) будет подавлять высвобождение гистамина из крысиных перитонеальных тучных клеток и защищать мышей от анафилактического шока.
Следовательно, преимущество поиска ингибиторов CD45-фосфатаз являются очевидными, в частности, когда имеется интерес в
- получении иммуносупрессорного действия в целом и, в частности
для лечения аутоиммунных заболеваний (Zong et al., J. Mol. Med. (1998), 76 (8), 572-580), например, таких, как рассеянный склероз или аутоиммунный энцефалит (Yacyshyn et al., Dig. Dis. Sci. (1996), 41 (12), 2493-8) и диабет (Shimada et al., J. Autoimmun. (1996), 9 (2), 263-269);
для лечения отторжения трансплантатов;
- лечении воспаления в целом и, в частности
для лечения артрита (Pelegri et al., Clin. Exp. Immunol. (2001), 125 (3), 470-477), ревматоидного артрита, ревматических заболеваний, конъюнктивита (Iwamoto et al., Graefes Arch. Clin. Opthalmol. (1999), 237 (5), 407-414) и зуда;
для лечения воспалительных заболеваний органов пищеварительного тракта, например болезни Крона (Yacyshyn et al., Dig. Dis. Sci. (1996), 41 (12), 2493-2498), геморрагического ректоколита и гепатита (Volpes et al., Hepatology (1991), 13 (5), 826-829);
- лечении аллергии (Pawlik et al., Tohoku J. Exp. Med. (1997), 182 (1), 1-8).
Изобретение предлагает новые ингибиторы cdc25-фосфатазы (в частности, ингибиторы cdc25-С-фосфатазы и/или ингибиторы CD45-фосфатазы, которые являются производными бензотиазол-4,7-диона и бензоксазол-4,7-диона, соответствующие общей формуле (I), определенной ниже. С учетом вышеуказанного данные соединения можно применять в качестве лекарственных препаратов, в частности, при лечении следующих заболеваний/нарушений:
подавления пролиферации опухолей одни или в комбинации с другими видами лечения;
подавления нормальной пролиферации клеток одни или в комбинации с другими видами лечения;
нейродегенеративных заболеваний таких, как болезнь Альцгеймера;
профилактики спонтанной алопеции;
профилактики алопеции, вызванной экзогенными продуктами;
профилактики алопеции, вызванной облучением;
профилактики спонтанного или индуцированного апоптоза нормальных клеток;
подавления мейоза или оплодотворения;
подавления созревания ооцитов;
при всех заболеваниях/всех нарушениях, соответствующих применениям ингибиторов CDK и, в частности, неопухолевых пролиферативных заболеваниях (например, ангиогенезе, псориазе или рестенозе), опухолевых пролиферативных заболеваниях, паразитологии (пролиферация простейших), вирусных инфекциях, нитродегегеративных заболеваниях, миопатиях;
при всех заболеваниях/всех нарушениях, соответствующих клиническим применениям витамина К и его производных;
при аутоиммунных заболеваниях, например, таких, как рассеянный склероз и ревматоидный артрит, и
при диабете.
Кроме того, также соединения по настоящему изобретению за счет их способности ингибировать cdc25-фосфатазы можно использовать для подавления пролиферации микроорганизмов, в частности дрожжей. Одним из преимуществ данных соединений является их низкая токсичность для здоровых клеток.
Уже известен определенный ряд производных бензотиазол-4,7-диона и бензоксазол-4,7-диона.
В частности, патент GB 1534275 относится к гербицидам, активный ингредиент которых представляет соединение, соответствующее одной из общих формул (А1) или (А2)
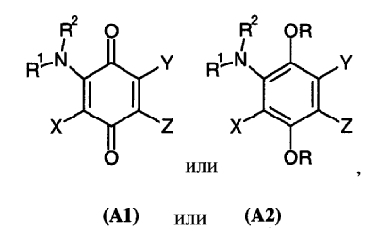
в которой R1 представляет, в частности, атом водорода или алкил, или циклоалкил;
R2 представляет, в частности, атом водорода или алкил, или циклоалкил;
Х представляет, в частности, атом галогена или алкокси;
Y и Z могут, в частности, вместе с атомом углерода, к которому они присоединены, образовать тиазоловое кольцо, необязательно замещенное алкилом, и
R представляет, в частности, алкил.
Кроме того, в заявке на патент РСТ WO 99/32115 описываются соединения общей формулы (А3)
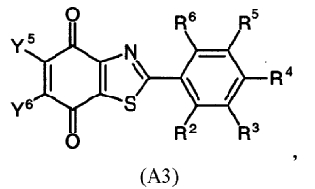
в которой заместители R2-R6 выбраны из группы, состоящей из атома водорода, электронодонорных заместителей, электроноакцепторных заместителей и электрономодулирующих заместителей, и
Y5 и Y6, в частности, выбраны из группы, состоящей из атома водорода, электронодонорных заместителей, электроноакцепторных заместителей и электрономодулирующих заместителей.
В заявке на патент РСТ WO 99/32115 термин «электронодонорный заместитель» относится к функциональной группе, обладающей способностью отдавать электронную плотность; упоминаются заместители алкил, алкенил и алкинил. В данной заявке на патент «электроноакцепторные заместители» всегда относятся к функциональной группе, обладающей способностью к захвату электронной плотности; упоминаются циано, ацил, карбонил, фтор, нитро, сульфонил и тригалогенметил. Наконец, «электрономодулирующий заместитель» определяется в данной заявке как функциональная группа, обладающая способностью изменять электронную плотность, которая может как присоединять, так и отдавать электроны и, следовательно, может стабилизировать катионное промежуточное соединение в реакции ароматического электрофильного замещения; упомянутые функциональные группы включают, например, заместители амино (например, -NH2, алкиламино или диалкиламино), гидрокси, алкокси или арил, гетероциклические заместители, атомы галогена и т.п.
Соединения общей формулы (А3) представлены в качестве модуляторов рецепторов рианодина, которые можно использовать в качестве пестицидов или терапевтических средств, например, при лечении застойной сердечной недостаточности, мигреней, гипертензии, болезни Паркинсона или болезни Альцгеймера или для профилактики выкидыша.
Наконец, производные бензоксазол-4,7-диона общей формулы (А4)
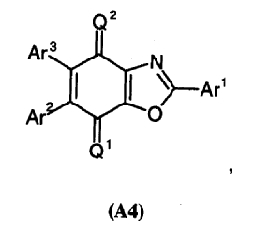
в которой Ar1 представляет необязательно замещенный арил,
каждый из Ar2 и Ar3 представляет атом водорода или необязательно замещенный арил и
каждый Q1 и Q2 представляет, в частности, О,
описаны в качестве активных веществ фоточувствительных слоев фоторецепторов.
В настоящее время заявители установили, что соединения, соответствующие общей формуле (I)
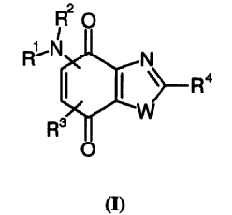
в которой R1 представляет атом водорода или алкил, алкоксиалкил, алкилтиоалкил, циклоалкил, -(CH2)-X-Y, -(CH2)-Z-NR5R6 или
-CHR35R36, в котором R35 и R36 образуют вместе с атомом углерода, к которому они присоединены, инданил или тетралинил, или также R35 и R36 образуют вместе с атомом углерода, к которому они присоединены, насыщенный гетероцикл, содержащий 5-7 членов и 1-2 гетероатома, выбранных из О, N и S, где атомы азота указанного гетероцикла необязательно замещены радикалами, выбранными из алкила и бензила,
R1 также может, когда W является О, представлять собой карбоциклический арил, необязательно замещенный 1-3 заместителями, независимо выбранными из атома галогена и алкила, галогеналкила или алкокси,
Х представляет связь или нормальный, или разветвленный алкилен, содержащий 1-5 атомов углерода,
Y представляет насыщенную углеродсодержащую циклическую систему, содержащую 1-3 конденсированных кольца, независимо выбранных из колец с 3-7 членами, или Y представляет насыщенный гетероцикл, содержащий 1-2 гетероатома, независимо выбранных из O, N или S, и соединенный с радикалом Х посредством N- или СН-члена, где указанный насыщенный гетероцикл, кроме того, содержит 2-6 дополнительных членов, независимо выбранных из -CHR7-, -CO-, -NR8-, -O- и -S-, где R7 представляет атом водорода или алкил и R8 представляет атом водорода или алкил, или аралкил, или также Y представляет карбоциклический или гетероциклический арил, необязательно замещенный 1-3 заместителями, независимо выбранными из группы, состоящей из атома галогена, алкила, галогеналкила, алкокси, галогеналкокси, гидрокси, нитро, циано, фенила, SO2NHR9 и NR10R11, где R9 представляет атом водорода или алкил, или фенил и R10 и R11 независимо представляют алкил,
Z представляет связь или нормальный, или разветвленный алкилен, содержащий 1-5 атомов углерода,
R5 и R6 независимо выбраны из атома водорода, алкила, аралкила или -(СН2)n-OH, в котором n представляет целое число от 1 до 6,
или R5 представляет алкоксикарбонил, галогеналкоксикарбонил или аралкоксикарбонил и R6 представляет атом водорода или метил,
или также R5 и R6 образуют вместе с атомом азота гетероцикл с 4-7 членами, содержащий 1-2 гетероатома, где члены, необходимые для замыкания гетероцикла, независимо выбраны из
-CR12R13-, -O-, -S- и -NR14, где R12 и R13 независимо представляют, когда они имеются, атом водорода или алкил и R14 представляет атом водорода или алкил, или аралкил, или также R14 представляет фенил, необязательно замещенный 1-3 заместителями, независимо выбранными из атома галогена и алкила, или алкокси,
R2 представляет атом водорода или алкил, или аралкил;
или также R1 и R2 образуют вместе с атомом азота гетероцикл с 4-8 членами, содержащий 1-2 гетероатома, где члены, необходимые для замыкания гетероцикла, независимо выбраны из
-CR15R16-, -O-, -S- или -NR17, где R15 и R16 независимо представляют, когда они имеются, атом водорода или алкил, и R17 представляет атом водорода или алкил, или аралкил;
R3 представляет атом водорода, атом галогена или алкил, галогеналкил, алкокси или алкилтио;
R4 представляет алкил, циклоалкил, циклоалкилалкил, циано, амино, -CH2-COOR18, -CH2-CO-NR19R20 или -CH2-NR21R22, или R4 представляет карбоциклический или гетероциклический арил, необязательно замещенный 1-4 заместителями, независимо выбранными из атома галогена и алкила, галогеналкила, алкокси, галогеналкокси или NR37R38, или также R4 представляет фенил, имеющий два заместителя, которые вместе образуют метилендиокси или этилендиокси,
R18 представляет атом водорода или алкил,
R19 представляет атом водорода, алкил или аралкил, арильная группа которого необязательно замещена 1-3 заместителями, независимо выбранными из группы, состоящей из атома галогена, алкила, галогеналкила, алкокси, галогеналкокси, гидрокси, нитро, циано, фенила, SO2NHR23 и NR24R25, где R23 представляет атом водорода или алкил, или фенил и R24 и R25 независимо представляют алкил,
R20 представляет атом водорода или алкил,
или также R19 и R20 образуют вместе с атомом азота гетероцикл с 4-7 членами, содержащий 1-2 гетероатома, где члены, необходимые для замыкания гетероцикла, независимо выбраны из
-CR26R27-, -O-, -S- или -NR28, где R26 и R27 независимо представляют, когда они имеются, атом водорода или алкил и R28 представляет атом водорода или алкил, или аралкил, или также R28 представляет фенил, необязательно замещенный 1-3 заместителями, независимо выбранными из атома галогена и алкила, или алкокси,
R21 представляет атом водорода, алкил или аралкил, арильная группа которого необязательно замещена 1-3 заместителями, независимо выбранными из группы, состоящей из атома галогена, алкила, галогеналкила, алкокси, галогеналкокси, гидрокси, нитро, циано, фенила, SO2NHR29 и NR30R31, где R29 представляет атом водорода или алкил, или фенил и R30 и R31 независимо представляют алкил
R22 представляет атом водорода или алкил,
или также R21 и R22 образуют вместе с атомом азота гетероцикл с 4-7 членами, содержащий 1-2 гетероатома, где члены, необходимые для замыкания гетероцикла, независимо выбраны из
-CR32R33-, -O-, -S- или -NR34, где R32 и R33 независимо представляют, когда они имеются, атом водорода или алкил и R34 представляет атом водорода, алкил или аралкил, или также R34 представляет фенил, необязательно замещенный 1-3 заместителями, независимо выбранными из атома галогена и алкила или алкокси,
R37 и R38 независимо выбраны из атома водорода и алкила или R37 и R38 образуют вместе с атомом азота гетероцикл с 4-7 членами, содержащий 1-2 гетероатома, где члены, необходимые для замыкания гетероцикла, независимо выбраны из -CR39R40-, -O-, -S- или -NR41, где R39 и R40 независимо представляют, когда они имеются, атом водорода или алкил и R41 представляет атом водорода или алкил;
W представляет О или S;
или фармацевтически приемлемые соли соединений общей формулы (I), определенной выше, являются ингибиторами cdc25-фосфатаз, в частности ингибиторами cdc25-С-фосфатазы, и/или ингибиторами CD45-фосфатазы, и, следовательно, могут использоваться для получения лекарственного препарата, предназначенного для ингибирования cdc25-фосфатаз, в частности cdc25-С-фосфатазы, и/или CD45-фосфатазы.
Под алкилом подразумевается, если не указано иначе, нормальный или разветвленный алкил, содержащий 1-12 атомов углерода, предпочтительно 1-10 атомов углерода и более предпочтительно 1-8 атомов углерода (и, в частности, 1-6 атомов углерода). Под циклоалкилом подразумевается, если не указано иначе, циклоалкил, содержащий 3-7 атомов углерода. Под карбоциклическим или гетероциклическим арилом подразумевается карбоциклическая или гетероциклическая система из 1-3 конденсированных колец, содержащая по меньшей мере одно ароматическое кольцо, где система называется гетероциклической, когда, по меньшей мере, одно из колец, входящих в ее состав, содержит гетероатом (O, N или S); когда карбоциклический или гетероциклический арил называют замещенным без дополнительного пояснения, то это означает, что указанный карбоциклический или гетероциклический арил замещен 1-3 раза, предпочтительно один-два раза, различными радикалами атома водорода, которые, если не указано иначе, выбраны из атома галогена и алкила или алкокси; кроме того, если не указано иначе, под арилом подразумевается исключительно карбоциклический арил. Под галогеналкилом подразумевается алкил, в котором по меньшей мере один из атомов водорода (и необязательно все) замещен атомом галогена.
Под циклоалкилалкилом, алкокси, галогеналкилом, галогеналкокси и аралкилом подразумевается соответственно циклоалкилалкил, алкокси, галогеналкил, галогеналкокси и аралкил, в которых алкил, циклоалкил и арил имеют значения, определенные выше.
В случае, когда указывается, что радикал необязательно замещен 1-3 раза, предпочтительно необязательно он замещен один-два раза и предпочтительно необязательно замещен один раз.
Под нормальным или разветвленным алкилом, имеющим 1-6 атомов углерода, подразумевается, в частности, метил, этил, пропил, изопропил, бутил, изобутил, вторичный бутил и трет-бутил, пентил, неопентил, изопентил, гексил, изогексил. Под галогеналкилом подразумевается, в частности, трифторметил. Под галогеналкокси подразумевается, в частности, трифторметокси. Под карбоциклическим арилом подразумевается, в частности, фенил и нафтил. Под аралкилом подразумевается, в частности, фенилалкил, в частности бензил. Под насыщенной углеродсодержащей циклической системой, содержащей 1-3 конденсированных кольца, независимо выбранных из колец с 3-7 членами, подразумевается, в частности, циклопропил, циклобутил, циклогексил и адамантил. Под гетероциклическим или гетероарильным арилом подразумевается, в частности, тиенил, фуранил, пирролил, имидазолил, тиазолил, оксазолил и пиридил. Наконец, под галогеном подразумеваются атомы фтора, хлора, брома или йода.
Под фармацевтически приемлемой солью подразумеваются, в частности, аддитивные соли неорганических кислот такие, как гидрохлорид, гидробромид, гидройодид, сульфат, фосфат, дифосфат и нитрат, или органических кислот такие, как ацетат, малеат, фумарат, тартрат, сукцинат, цитрат, лактат, метансульфонат, п-толуолсульфонат, памоат и стеарат. Также в объеме настоящего изобретения, когда их можно использовать, находятся соли, полученные из оснований таких, как гидроокись натрия или калия. Другие примеры фармацевтически приемлемых солей можно найти в «Salt selection for basic drugs», Int. J. Pharm. (1986), 33, 201-217.
В некоторых случаях соединения по настоящему изобретению могут содержать асимметрические атомы углерода. В результате соединения по настоящему изобретению имеют две возможные энантиомерные формы, т.е. «R» и «S» конфигурации. Настоящее изобретение включает две энантиомерные формы и все комбинации данных форм, включая «RS» рацемические смеси. В целях упрощения, когда в структурных формулах не указывается конкретная конфигурация, следует понимать, что представлены две энантиомерные формы и их смеси.
В соответствии с конкретным вариантом изобретения соединения общей формулы (I) представляют соединения общей формулы (I)'
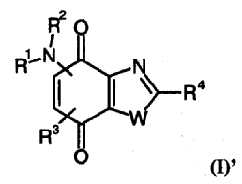
в которой R1 представляет атом водорода или алкил, алкоксиалкил, алкилтиоалкил, циклоалкил, -(CH2)-X-Y, -(CH2)-Z-NR5R6 или
-CHR35R36, в котором R35 и R36 образуют вместе с атомом углерода, к которому они присоединены, инданил или тетралинил, или также R35 и R36 образуют вместе с атомом углерода, к которому они присоединены, насыщенный гетероцикл, содержащий 5-7 членов и 1-2 гетероатома, выбранных из О, N и S, где атомы азота указанного гетероцикла необязательно замещены радикалами, выбранными из алкила и бензила,
R1 также может, когда W является О, представлять собой карбоциклический арил, необязательно замещенный 1-3 заместителями, независимо выбранными из атома галогена и алкила, галогеналкила или алкокси,
Х представляет связь или нормальный, или разветвленный алкилен, содержащий 1-5 атомов углерода,
Y представляет насыщенную углеродсодержащую циклическую систему, содержащую 1-3 конденсированных кольца, независимо выбранных из колец с 3-7 членами, или Y представляет насыщенный гетероцикл, содержащий 1-2 гетероатома, независимо выбранных из O, N или S, и соединенный с радикалом Х посредством N- или СН-члена, где указанный насыщенный гетероцикл, кроме того, содержит 2-6 дополнительных членов, выбранных из -CHR7-, -CO-, -NR8-, -O- и -S-, где R7 представляет атом водорода или алкил и R8 представляет атом водорода или алкил, или аралкил, или также Y представляет карбоциклический или гетероциклический арил, необязательно замещенный 1-3 заместителями, независимо выбранными из группы, состоящей из атома галогена, алкила, галогеналкила, алкокси, галогеналкокси, гидрокси, нитро, циано, фенила, SO2NHR9 и NR10R11, где R9 представляет атом водорода или алкил, или фенил и R10 и R11 независимо представляют алкил,
Z представляет связь или нормальный, или разветвленный алкилен, содержащий 1-5 атомов углерода,
R5 и R6 независимо выбраны из атома водорода, алкила, аралкила или -(СН2)n-OH, в котором n представляет целое число от 1 до 6,
или R5 представляет алкоксикарбонил, галогеналкоксикарбонил или аралкоксикарбонил и R6 представляет атом водорода или метил,
или также R5 и R6 образуют вместе с атомом азота гетероцикл с 4-7 членами, содержащий 1-2 гетероатома, где члены, необходимые для замыкания гетероцикла, независимо выбраны из
-CR12R13-, -O-, -S- и -NR14, где R12 и R13 независимо представляют, когда они имеются, атом водорода или алкил, и R14 представляет атом водорода или алкил или аралкил, или также R14 представляет фенил, необязательно замещенный 1-3 заместителями, независимо выбранными из атома галогена и алкила, или алкокси,
R2 представляет атом водорода или алкил, или аралкил,
или также R1 и R2 образуют вместе с атомом азота гетероцикл с 4-8 членами, содержащий 1-2 гетероатома, где члены, необходимые для замыкания гетероцикла, независимо выбраны из
-CR15R16-, -O-, -S- или -NR17, где R15 и R16 независимо представляют, когда они имеются, атом водорода или алкил и R17 представляет атом водорода или алкил, или аралкил,
R3 представляет атом водорода, атом галогена или алкил, галогеналкил, алкокси или алкилтио,
R4 представляет алкил, циклоалкил, циклоалкилалкил, циано, амино, -CH2-COOR18, -CH2-CO-NR19R20 или -CH2-NR21R22, или также R4 представляет карбоциклический или гетероциклический арил, необязательно замещенный 1-3 заместителями, независимо выбранными из атома галогена и алкила, галогеналкила, алкокси или NR37R38,
R18 представляет атом водорода или алкил,
R19 представляет атом водорода, алкил или аралкил, арильная группа которого необязательно замещена 1-3 заместителями, независимо выбранными из группы, состоящей из атома галогена, алкила, галогеналкила, алкокси, галогеналкокси, гидрокси, нитро, циано, фенила, SO2NHR23 и NR24R25, где R23 представляет атом водорода или алкил, или фенил и R24 и R25 независимо представляют алкил,
R20 представляет атом водорода или алкил,
или также R19 и R20 образуют вместе с атомом азота гетероцикл с 4-7 членами, содержащий 1-2 гетероатома, где члены, необходимые для замыкания гетероцикла, независимо выбраны из
-CR26R27-, -O-, -S- или -NR28, где R26 и R27 независимо представляют, когда они имеются, атом водорода или алкил и R28 представляет атом водорода или алкил, или аралкил, или также R28 представляет фенил, необязательно замещенный 1-3 заместителями, независимо выбранными из атома галогена и алкила, или алкокси,
R21 представляет атом водорода, алкил или аралкил, арильная группа которого необязательно замещена 1-3 заместителями, независимо выбранными из группы, состоящей из атома галогена, алкила, галогеналкила, алкокси, галогеналкокси, гидрокси, нитро, циано, фенила, SO2NHR29 и NR30R31, где R29 представляет атом водорода или алкил, или фенил и R30 и R31 независимо представляют алкил,
R22 представляет атом водорода или алкил,
или также R21 и R22 образуют вместе с атомом азота гетероцикл с 4-7 членами, содержащий 1-2 гетероатома, где члены, необходимые для замыкания гетероцикла, независимо выбраны из
-CR32R33-, -O-, -S- или -NR34, где R32 и R33 независимо представляют, когда они имеются, атом водорода или алкил и R34 представляет атом водорода, алкил или аралкил, или также R34 представляет фенил, необязательно замещенный 1-3 заместителями, независимо выбранными из атома галогена и алкила, или алкокси,
R37 и R38 независимо выбраны из атома водорода и алкила или R37 и R38 образуют вместе с атомом азота гетероцикл с 4-7 членами, содержащий 1-2 гетероатома, где члены, необходимые для замыкания гетероцикла, независимо выбраны из -CR39R40-, -O-, -S- или -NR41, где R39 и R40 независимо представляют, когда они имеются, атом водорода или алкил и R41 представляет атом водорода или алкил и
W представляет О или S,
или фармацевтически приемлемые соли соединений общей формулы (I)', определенной выше.
По более конкретному варианту изобретения соединения, используемые по изобретению, представляют соединения общей формулы (I)"
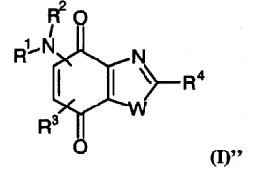
в которой R1 представляет атом водорода или алкил, циклоалкил, -(CH2)-X-Y или -(CH2)-Z-NR5R6,
R1 также может, когда W является О, также представлять собой карбоциклический арил, необязательно замещенный 1-3 заместителями, независимо выбранными из атома галогена и алкила, галогеналкила или алкокси,
Х представляет связь или нормальный, или разветвленный алкилен, содержащий 1-5 атомов углерода,
Y представляет насыщенную углеродсодержащую циклическую систему, содержащую 1-3 конденсированных кольца, независимо выбранных из колец с 3-7 членами, или Y представляет насыщенный гетероцикл, содержащий 1-2 гетероатома, независимо выбранных из O, N или S, и соединенный с радикалом Х посредством N- или СН-члена, где указанный насыщенный гетероцикл, кроме того, содержит 2-6 дополнительных членов, независимо выбранных из -CHR7-, -CO-, -NR8-, -O- и -S-, где R7 представляет атом водорода или алкил и R8 представляет атом водорода или алкил, или аралкил, или также Y представляет карбоциклический или гетероциклический арил, необязательно замещенный 1-3 заместителями, независимо выбранными из группы, состоящей из атома галогена, алкила, галогеналкила, алкокси, галогеналкокси, гидрокси, нитро, циано, фенила, SO2NHR9 и NR10R11, где R9 представляет атом водорода или алкил, или фенил и R10 и R11 независимо представляют алкил,
Z представляет связь или нормальный, или разветвленный алкилен, содержащий 1-5 атомов углерода,
R5 и R6 независимо выбраны из атома водорода, алкила, аралкила или -(СН2)n-OH, в котором n представляет целое число от 1 до 6, или R5 и R6 образуют вместе с атомом азота гетероцикл с 4-7 членами, содержащий 1-2 гетероатома, где члены, необходимые для замыкания гетероцикла, независимо выбраны из -CR12R13-, -O-, -S- и -NR14, где R12 и R13 независимо представляют, когда они имеются, атом водорода или алкил и R14 представляет атом водорода или алкил, или аралкил, или также R14 представляет фенил, необязательно замещенный 1-3 заместителями, независимо выбранными из атома галогена и алкила, или алкокси,
R2 представляет атом водорода или алкил,
или также R1 и R2 образуют вместе с атомом азота гетероцикл с 4-7 членами, содержащий 1-2 гетероатома, где члены, необходимые для замыкания гетероцикла, независимо выбраны из
-CR15R16-, -O-, -S- или -NR17, где R15 и R16 независимо представляют, когда они имеются, атом водорода или алкил и R17 представляет атом водорода или алкил, или аралкил,
R3 представляет атом водорода, атом галогена или алкил, галогеналкил, или алкокси,
R4 представляет алкил, циклоалкил, циклоалкилалкил, циано, амино, -CH2-COOR18, -CH2-CO-NR19R20 или -CH2-NR21R22, или также R4 представляет гетероциклический арил, необязательно замещенный 1-3 заместителями, независимо выбранными из атома галогена и алкила, галогеналкила или алкокси,
R18 представляет атом водорода или алкил,
R19 представляет атом водорода, алкил или аралкил, арильная группа которого необязательно замещена 1-3 заместителями, независимо выбранными из группы, состоящей из атома галогена, алкила, галогеналкила, алкокси, галогеналкокси, гидрокси, нитро, циано, фенила, SO2NHR23 и NR24R25, где R23 представляет атом водорода или алкил, или фенил и R24 и R25 независимо представляют алкил,
R20 представляет атом водорода или алкил,
или также R19 и R20 образуют вместе с атомом азота гетероцикл с 4-7 членами, содержащий 1-2 гетероатома, где члены, необходимые для замыкания гетероцикла, независимо выбраны из
-CR26R27-, -O-, -S- или -NR28, где R26 и R27 независимо представляют, когда они имеются, атом водорода или алкил и R28 представляет атом водорода или алкил, или аралкил, или также R28 представляет фенил, необязательно замещенный 1-3 заместителями, независимо выбранными из атома галогена и алкила, или алкокси,
R21 представляет атом водорода, алкил или аралкил, арильная группа которого необязательно замещена 1-3 заместителями, независимо выбранными из группы, состоящей из атома галогена, алкила, галогеналкила, алкокси, галогеналкокси, гидрокси, нитро, циано, фенила, SO2NHR29 и NR30R31, где R29 представляет атом водорода или алкил, или фенил и R30 и R31 независимо представляют алкил,
R22 представляет атом водорода или алкил,
или также R21 и R22 образуют вместе с атомом азота гетероцикл с 4-7 членами, содержащий 1-2 гетероатома, где члены, необходимые для замыкания гетероцикла, независимо выбраны из
-CR32R33-, -O-, -S- или -NR34, где R32 и R33 независимо представляют, когда они имеются, атом водорода или алкил, R34 представляет атом водорода, алкил или аралкил, или также R34 представляет фенил, необязательно замещенный 1-3 заместителями, независимо выбранными из атома галогена и алкила, или алкокси,
W представляет О или S,
или фармацевтически приемлемые соли соединений общей формулы (I)", определенной выше.
Применение соединений по настоящему изобретению также обычно имеют четыре варианта.
В соответствии с первым вариантом используются соединения общей формулы (I), которые также соответствуют общей субформуле (I)1
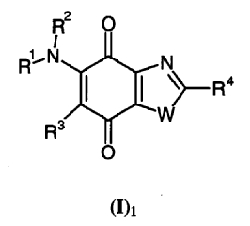
в которой W представляет S и R1, R2, R3 и R4 имеют те же значения, что в общей формуле (I), или их фармацевтически приемлемые соли;
в соответствии со вторым вариантом используются соединения общей формулы (I), которые также соответствуют общей субформуле (I)2
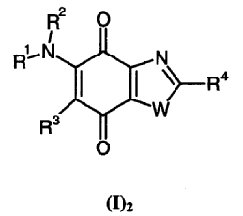
в которой W представляет О и R1, R2, R3 и R4 имеют те же значения, что в общей формуле (I), или их фармацевтически приемлемые соли;
в соответствии с третьим вариантом используются соединения общей формулы (I), которые также соответствуют общей субформуле (I)3
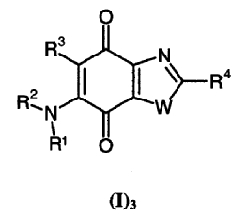
в которой W представляет S и R1, R2, R3 и R4 имеют те же значения, что в общей формуле (I), или их фармацевтически приемлемые соли;
в четвертом варианте используются соединения общей формулы (I), которые также соответствуют общей субформуле (I)4
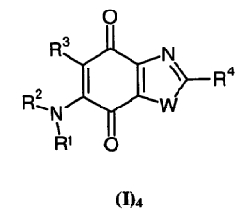
в которой W представляет О и R1, R2, R3 и R4 имеют те же значения, что в общей формуле (I), или их фармацевтически приемлемые соли.
Следовательно, изобретение относится, в частности, к применению соединений общей формулы (I)1 или (I)2, или их фармацевтически приемлемых солей для получения лекарственного препарата, предназначенного для ингибирования cdc25-фосфатаз, в частности cdc25-С-фосфатазы, и/или CD45-фосфатазы. Аналогично изобретение относится к применению соединений общей формулы (I)3 или (I)4, или их фармацевтически приемлемых солей для получения лекарственного препарата, предназначенного для ингибирования cdc25-фосфатаз, в частности, cdc25-С-фосфатазы, и/или CD45-фосфатазы.
Предпочтительно соединения общей формулы (I), (I)', (I)", (I)1, (I)2, (I)3 или (I)4, используемые по изобретению, будут включать по меньшей мере одну из следующих характеристик:
R1 представляет алкил, циклоалкил, алкоксиалкил, -(CH2)-X-Y, -(CH2)-Z-NR5R6 или -CHR35R36;
R2 представляет атом водорода или метил, этил или бензил;
R1 или R2 образуют вместе с атомом азота гетероцикл с 4-8 членами (предпочтительно 5-7 членами, в частности 6 членами), содержащий 1-2 гетероатома (и предпочтительно 2 гетероатома), где члены, необходимые для замыкания гетероцикла, независимо выбраны из -СН2-, -О- и -NR17 (и предпочтительно из -СН2- и -NR17), где R17 представляет метил или бензил;
R3 представляет атом водорода, атом галогена или алкил, алкокси или алкилтио;
R4 представляет алкил, -CH2-COOR18 или -CH2-CO-NR19R20, или
-CH2-NR21R22, или также карбоциклический или гетероциклический арил, необязательно замещенный 1-4 (и, в частности, 1-3) заместителями, независимо выбранными из атома галогена и алкила, галогеналкила, алкокси или NR37R38.
Как правило, для применения по изобретению будут предпочтительными соединения общей формулы (I), (I)' или (II)", в которых W представляет атом серы. Тем не менее другой интересной альтернативой для применения по изобретению является применение соединений общей формулы (I), (I)' или (I)", в которых W представляет атом кислорода.
Кроме того, радикал Х будет предпочтительно представлять связь или нормальный алкилен, содержащий 1-5 атомов углерода. Также предпочтительно, если радикал Y будет представлять насыщенную углеродсодержащую циклическую систему, содержащую 1-3 конденсированных кольца, независимо выбранных из колец с 3-7 членами, и Y будет представлять карбоциклический арил, необязательно замещенный (предпочтительно необязательно замещенный 1-3 радикалами, выбранными из атома галогена и алкила, галогеналкила, алкокси, галогеналкокси, SO2NHR9 или NR10R11, и более предпочтительно необязательно замещенный 1-3 радикалами, выбранными из атома галогена и алкила, алкокси, SO2NHR9 или NR10R11), или также Y будет представлять необязательно замещенный гетероциклический арил, где указанный гетероциклический арил предпочтительно выбран из арильных радикалов с 5 членами (и, в частности, из имидазолила, тиенила или пиридинила), и предпочтительно необязательно замещенный 1-3 радикалами, выбранными из атома галогена и алкила, галогеналкила, алкокси, галогеналкокси, SO2NHR9 или NR10R11, и более предпочтительно необязательно замещенный 1-3 радикалами, выбранными из атома галогена и алкила, алкокси, SO2NHR9 или NR10R11; R9 будет предпочтительно представлять атом водорода, R10 и R11 будут предпочтительно представлять радикалы, независимо выбранные из алкила. Радикал Z будет предпочтительно представлять алкилен, содержащий 1-5 атомов углерода, в частности радикал -(СН2)р-, в котором р представляет целое число от 1 до 3 (р предпочтительно равно 1 или 2 и более предпочтительно равно 1). Также предпочтительно, чтобы R5 и R6 были независимо выбраны из атома водорода и алкила, или также R5 и R6 образовывали вместе с атомом азота, к которому они присоединены, гетероцикл с 4-7 членами, содержащий 1-2 гетероатома, где указанный гетероцикл предпочтительно представляет один из азетидинила, пирролидинила, пиперидинила, пиперазинила, гомопиперазинила, морфолинила и тиоморфолинила, необязательно замещенных 1-3 алкилами (и предпочтительно 1-3 метилами); еще более предпочтительно, когда R5 и R6 независимо выбраны из алкила или алкоксикарбонила (и, в частности, R5 и R6 каждый представляет метил или трет-бутоксикарбонил), или R5 и R6 будут образовывать вместе с атомом азота, к которому они присоединены, гетероцикл с 4-7 членами, содержащий 1-2 гетероатома, где указанный гетероцикл предпочтительно представляет один из азетидинила, пирролидинила, пиперидинила, пиперазинила, гомопиперазинила, морфолинила и тиоморфолинила, необязательно замещенных 1-3 алкилами (и предпочтительно 1-3 метилами). R18 будет предпочтительно представлять атом водорода или метил, или этил.
Кроме того, радикалы R7, R12, R13, R15, R16, R26, R27, R39 и R40 предпочтительно независимо выбраны из атома водорода и метила и радикалы R8, R14, R17, R28 и R41 предпочтительно независимо выбраны из атома водорода и метила, или бензила.
Кроме того, в отношении R19 и R20 будут предпочтительными случаи, когда R19 представляет атом водорода, алкил или бензил и R20 представляет атом водорода или метил, а также таковые, когда R19 и R20 образуют вместе с атомом азота, к которому они присоединены, гетероцикл с 4-7 членами, содержащий 1-2 гетероатома, где указанный гетероцикл предпочтительно представляет один из азетидинила, пирролидинила, пиперидинила, пиперазинила, гомопиперазинила, морфолинила и тиоморфолинила, необязательно замещенных 1-3 алкилами (и предпочтительно необязательно замещенных 1-3 метилами).
Кроме того, в отношении R21 и R22 будут предпочтительными случаи, когда R21 представляет атом водорода, алкил или бензил и R22 представляет атом водорода или метил, а также таковые, когда R21 и R22 образуют вместе с атомом азота, к которому они присоединены, гетероцикл с 4-7 членами, содержащий 1-2 гетероатома, где указанный гетероцикл предпочтительно представляет один из азетидинила, пирролидинила, пиперидинила, пиперазинила, гомопиперазинила, морфолинила и тиоморфолинила. В отношении соответствующих радикалов R32, R33 и R34 предпочтительным является, когда R32 и R33 независимо выбраны из атома водорода и алкила, предпочтительно из атома водорода и метила (еще более предпочтительно, когда R32 и R33 оба представляют атомы водорода), и R34 представляет атом водорода, алкил и фенил, необязательно замещенный 1-3 заместителями, независимо выбранными из атома галогена и алкила, или алкокси (еще более предпочтительно, когда R34 представляет атом водорода или метил, или фенил).
Кроме того, в отношении R35 и R36 будут предпочтительными случаи, когда R35 и R36 образуют вместе с атомом углерода, к которому они присоединены, инданил или R35 и R36 образуют вместе с атомом углерода, к которому они присоединены, насыщенный гетероцикл, содержащий 5-7 членов и 1-2 гетероатома, выбранных из O, N и S, где атомы азота указанного гетероцикла необязательно замещены радикалами, выбранными из алкила и бензила.
Кроме того, в отношении R37 и R38 будут предпочтительными случаи, когда R37 и R38 независимо представляют радикалы, выбранные из алкила.
Наконец, когда R4 представляет карбоциклический или гетероциклический арил, необязательно замещенный 1-4 заместителями, то предпочтительно он выбран из группы, состоящей из карбоциклического и гетероциклического арила, необязательно замещенного 1-3 заместителями, независимо выбранными из атома галогена и алкила, галогеналкила, алкокси, галогеналкокси или NR37R38 (и, в частности, 1-3 заместителями, независимо выбранными из атома галогена и алкила, галогеналкила, алкокси или галогеналкокси) и 2,3,4,5-тетрафторфенила. Более предпочтительно, когда R4 представляет карбоциклический или гетероциклический арил, необязательно замещенный 1-4 заместителями, R4 выбран из группы, состоящей из карбоциклического и гетероциклического арила, необязательно замещенного одним-двумя заместителями, независимо выбранными из атома галогена, алкила, галогеналкила, алкокси, галогеналкокси или NR37R38 (и, в частности, одним-двумя заместителями, независимо выбранными из атома галогена и алкила, галогеналкила, алкокси или галогеналкокси), 3,4,5-тригалогенфенила и 2,3,4,5-тетрафторфенила.
Более предпочтительно, когда соединения общей формулы (I), (I)', (I)", (I)1, (I)2, (I)3 или (I)4, используемые по изобретению, будут включать по меньшей мере одну из следующих характеристик:
R1 представляет алкил, циклоалкил или -(CH2)-Z-NR5R6;
R2 представляет атом водорода или метил;
R3 представляет атом водорода, атом галогена или метокси;
R4 представляет алкил, -CH2-NR21R22 или также карбоциклический или гетероциклический арил, необязательно замещенный 1-4 заместителями (и, в частности, 1-3 заместителями), независимо выбранными из атома галогена и алкила, или NR37R38.
Еще более предпочтительно, когда соединения общей формулы (I), (I)', (I)", (I)1, (I)2, (I)3 или (I)4, используемые по изобретению, будут включать по меньшей мере одну из следующих характеристик:
R1 представляет -(CH2)-Z-NR5R6;
R2 представляет атом водорода;
R3 представляет атом водорода или атом галогена (где указанный атом галогена предпочтительно представляет атом хлора или брома);
R4 представляет алкил или также фенил, пиридил, тиенил или фуранил, необязательно замещенные 1-4 (предпочтительно 1-3) атомами галогена, или NR37R38.
В еще более предпочтительном воплощении соединения общей формулы (I), (I)', (I)", (I)1, (I)2, (I)3 или (I)4, используемые по изобретению, будут включать по меньшей мере одну из следующих характеристик:
R3 представляет атом водорода или атом хлора (и более предпочтительно атом водорода);
R4 представляет алкил или также фенил, пиридил, тиенил, фуранил, необязательно замещенные 1-4 (предпочтительно 1-3) атомами галогена (и, в частности, R4 представляет алкил и предпочтительно алкил, содержащий 1-4 атома углерода, и еще более предпочтительно метил или этил).
По конкретному варианту изобретения W представляет О. В данном конкретном случае предпочтительно, когда R1 представляет арил, в частности фенил, необязательно замещенный 1-3 заместителями, независимо выбранными из атома галогена и алкила, галогеналкила или алкокси. Еще более предпочтительно, когда W представляет О, и предпочтительно, когда R1 представляет фенил, необязательно замещенный атомом галогена (где указанный атом галогена представляет атом фтора).
По конкретному аспекту изобретения R4 будет представлять фенил или гетероциклический арил с 5-6 членами, необязательно замещенный 1-4 (и предпочтительно 1-3) заместителями, выбранными из группы, состоящей из атомов галогена, трифторметила и трифторметокси (и предпочтительно выбранными из группы, состоящей из атомов галогена и трифторметила). В частности, указанный необязательно замещенный гетероциклический арил с 5-6 членами представляет необязательно замещенный пиридин, тиофен, фуран или пиррол.
Другой конкретный аспект данного изобретения относится к применению соединений общей формулы (I), в которой W представляет S, R3 представляет атом водорода, заместитель NR1R2 (остаются применимыми предпочтения, указанные выше для R1 и R2) находится в 5-ом положении кольца бензотиазоледиона и R4 выбран из алкила, циклоалкилалкила, -CH2-COOR18, -CH2-CO-NR19R20 и -CH2-NR21R22 (где R4 предпочтительно представляет алкил или циклоалкилалкил и более предпочтительно алкил по данному конкретному аспекту изобретения).
Для применения по изобретению соединения общей формулы (I), описанные (если является подходящим в виде солей или смесей) в примерах 1-131, или фармацевтически приемлемые соли данных соединений являются особенно предпочтительными (в частности, описанные в примерах 1-65, или их фармацевтически приемлемые соли и, в частности, описанные в примерах 1-17, или их фармацевтически приемлемые соли). Из соединений примеров 1-131 и их фармацевтически приемлемых солей (и, в частности, соединения примеров 1-14, 18-39, 48-52, 55, 57, 58 и 60-131 (и, в частности, соединения примеров 1-14, 18-39 и 55 и их фармацевтически приемлемые соли) в основном будут представлять больший интерес для данного изобретения.
Кроме того, соединения общей формулы (I), описанные (если является подходящим в виде солей или смесей) в примерах 2-5, 16, 19-26, 32, 34, 38-40, 43-47, 55-58, 60-77, 79-98 и 101-115, или фармацевтически приемлемые соли данных соединений также являются особенно предпочтительными для применения по изобретению.
Кроме того, соединения общей формулы (I), описанные (если является подходящим в виде солей или смесей) в примерах 2, 19, 20, 23, 24, 34, 57, 60, 62, 63, 67-77, 80-92, 94, 96-98, 103, 104, 106 и 110-113, или фармацевтически приемлемые соли данных соединений являются наиболее предпочтительными для применения по изобретению.
Другой предмет изобретения относится, в качестве лекарственных препаратов, к соединениям общей формулы (I)М
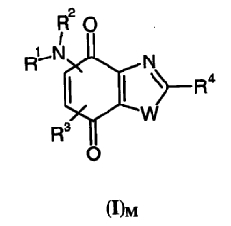
в которой R1 представляет атом водорода или алкил, алкоксиалкил, алкилтиоалкил, циклоалкил, -(CH2)-X-Y, -(CH2)-Z-NR5R6 или
-CHR35R36, в котором R35 и R36 образуют вместе с атомом углерода, к которому они присоединены, инданил или тетралинил, или также R35 и R36 образуют вместе с атомом углерода, к которому они присоединены, насыщенный гетероцикл, содержащий 5-7 членов и 1-2 гетероатома, выбранных из О, N и S, где атомы азота указанного гетероцикла необязательно замещены радикалами, выбранными из алкила и бензила,
R1 также может, когда W является О, представлять собой карбоциклический арил, необязательно замещенный 1-3 заместителями, независимо выбранными из атома галогена и алкила, галогеналкила или алкокси,
Х представляет связь или нормальный, или разветвленный алкилен, содержащий 1-5 атомов углерода,
Y представляет насыщенную углеродсодержащую циклическую систему, содержащую 1-3 конденсированных кольца, независимо выбранных из колец с 3-7 членами, или Y представляет насыщенный гетероцикл, содержащий 1-2 гетероатома, независимо выбранных из O, N или S, и соединенный с радикалом Х посредством N- или СН-члена, где указанный насыщенный гетероцикл, кроме того, содержит 2-6 дополнительных членов, независимо выбранных из -CHR7-, -CO-, -NR8-, -O- и -S-, где R7 представляет атом водорода или алкил и R8 представляет атом водорода или алкил, или аралкил, или также Y представляет карбоциклический или гетероциклический арил, необязательно замещенный 1-3 заместителями, независимо выбранными из группы, состоящей из атома галогена, алкила, галогеналкила, алкокси, галогеналкокси, гидрокси, нитро, циано, фенила, SO2NHR9 и NR10R11, где R9 представляет атом водорода или алкил, или фенил и R10 и R11 независимо представляют алкил,
Z представляет связь или нормальный, или разветвленный алкилен, содержащий 1-5 атомов углерода,
R5 и R6 независимо выбраны из атома водорода, алкила, аралкила или -(СН2)n-OH, в котором n представляет целое число от 1 до 6,
или R5 представляет алкоксикарбонил, галогеналкоксикарбонил или аралкоксикарбонил и R6 представляет атом водорода или метил,
или также R5 и R6 образуют вместе с атомом азота гетероцикл с 4-7 членами, содержащий 1-2 гетероатома, где члены, необходимые для замыкания гетероцикла, независимо выбраны из
-CR12R13-, -O-, -S- и -NR14, где R12 и R13 независимо представляют, когда они имеются, атом водорода или алкил и R14 представляет атом водорода или алкил, или аралкил, или также R14 представляет фенил, необязательно замещенный 1-3 заместителями, независимо выбранными из атома галогена и алкила, или алкокси,
R2 представляет атом водорода или алкил, или аралкил,
или также R1 и R2 образуют вместе с атомом азота гетероцикл с 4-8 членами, содержащий 1-2 гетероатома, где члены, необходимые для замыкания гетероцикла, независимо выбраны из
-CR15R16-, -O-, -S- или -NR17, где R15 и R16 независимо представляют, когда они имеются, атом водорода или алкил и R17 представляет атом водорода или алкил, или аралкил,
R3 представляет атом водорода, атом галогена или алкил, галогеналкил, алкокси или алкилтио,
R4 представляет алкил, циклоалкил, циклоалкилалкил, циано, амино, -CH2-COOR18, -CH2-CO-NR19R20 или -CH2-NR21R22, или R4 представляет карбоциклический или гетероциклический арил, необязательно замещенный 1-4 заместителями, независимо выбранными из атома галогена и алкила, галогеналкила, алкокси, галогеналкокси или NR37R38, или также R4 представляет фенил, имеющий два заместителя, которые вместе образуют метилендиокси или этилендиокси,
R18 представляет атом водорода или алкил,
R19 представляет атом водорода, алкил или аралкил, арильная группа которого необязательно замещена 1-3 заместителями, независимо выбранными из группы, состоящей из атома галогена, алкила, галогеналкила, алкокси, галогеналкокси, гидрокси, нитро, циано, фенила, SO2NHR23 и NR24R25, где R23 представляет атом водорода или алкил, или фенил и R24 и R25 независимо представляют алкил,
R20 представляет атом водорода или алкил,
или также R19 и R20 образуют вместе с атомом азота гетероцикл с 4-7 членами, содержащий 1-2 гетероатома, где члены, необходимые для замыкания гетероцикла, независимо выбраны из
-CR26R27-, -O-, -S- или -NR28, где R26 и R27 независимо представляют, когда они имеются, атом водорода или алкил, и R28 представляет атом водорода или алкил, или аралкил, или также R28 представляет фенил, необязательно замещенный 1-3 заместителями, независимо выбранными из атома галогена и алкила, или алкокси,
R21 представляет атом водорода, алкил или аралкил, арильная группа которого необязательно замещена 1-3 заместителями, независимо выбранными из группы, состоящей из атома галогена, алкила, галогеналкила, алкокси, галогеналкокси, гидрокси, нитро, циано, фенила, SO2NHR29 и NR30R31, где R29 представляет атом водорода или алкил, или фенил и R30 и R31 независимо представляют алкил,
R22 представляет атом водорода или алкил,
или также R21 и R22 образуют вместе с атомом азота гетероцикл с 4-7 членами, содержащий 1-2 гетероатома, где члены, необходимые для замыкания гетероцикла, независимо выбраны из
-CR32R33-, -O-, -S- или -NR34, где R32 и R33 независимо представляют, когда они имеются, атом водорода или алкил, R34 представляет атом водорода, алкил или аралкил, или также R34 представляет фенил, необязательно замещенный 1-3 заместителями, независимо выбранными из атома галогена и алкила, или алкокси,
R37 и R38 независимо выбраны из атома водорода и алкила или R37 и R38 образуют вместе с атомом азота гетероцикл с 4-7 членами, содержащий 1-2 гетероатома, где члены, необходимые для замыкания гетероцикла, независимо выбраны из -CR39R40-, -O-, -S- или -NR41, где R39 и R40 независимо представляют, когда они имеются, атом водорода или алкил и R41 представляет атом водорода или алкил и
W представляет О или S,
необходимо понимать, что если W является S и R4 представляет необязательно замещенный арил, то тогда R1 выбран из заместителей алкоксиалкила, алкилтиоалкила, циклоалкила -(CH2)-X-Y и -(CH2)-Z-NR5R6,
и к фармацевтически приемлемым солям соединений общей формулы (I)М.
По конкретному варианту изобретения лекарственные препараты представляют соединения общей формулы (I)'M
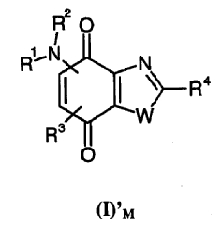
в которой R1 представляет атом водорода или алкил, алкоксиалкил, алкилтиоалкил, циклоалкил, -(CH2)-X-Y, -(CH2)-Z-NR5R6 или
-CHR35R36, в котором R35 и R36 образуют вместе с атомом углерода, к которому они присоединены, инданил или тетралинил, или также R35 и R36 образуют вместе с атомом углерода, к которому они присоединены, насыщенный гетероцикл, содержащий 5-7 членов и 1-2 гетероатома, выбранных из О, N и S, где атомы азота указанного гетероцикла необязательно замещены радикалами, выбранными из алкила и бензила,
R1 также может, когда W является О, представлять собой карбоциклический арил, необязательно замещенный 1-3 заместителями, независимо выбранными из атома галогена и алкила, галогеналкила или алкокси,
Х представляет связь или нормальный, или разветвленный алкилен, содержащий 1-5 атомов углерода,
Y представляет насыщенную углеродсодержащую циклическую систему, содержащую 1-3 конденсированных кольца, независимо выбранных из колец с 3-7 членами, или Y представляет насыщенный гетероцикл, содержащий 1-2 гетероатома, независимо выбранных из O, N или S, и соединенный с радикалом Х посредством N- или СН-члена, где указанный насыщенный гетероцикл, кроме того, содержит 2-6 дополнительных членов, независимо выбранных из -CHR7-, -CO-, -NR8-, -O- и -S-, где R7 представляет атом водорода или алкил и R8 представляет атом водорода или алкил, или аралкил, или также Y представляет карбоциклический или гетероциклический арил, необязательно замещенный 1-3 заместителями, независимо выбранными из группы, состоящей из атома галогена, алкила, галогеналкила, алкокси, галогеналкокси, гидрокси, нитро, циано, фенила, SO2NHR9 и NR10R11, где R9 представляет атом водорода или алкил, или фенил и R10 и R11 независимо представляют алкил,
Z представляет связь или нормальный, или разветвленный алкилен, содержащий 1-5 атомов углерода,
R5 и R6 независимо выбраны из атома водорода, алкила, аралкила или -(СН2)n-OH, в котором n представляет целое число от 1 до 6,
или R5 представляет алкоксикарбонил, галогеналкоксикарбонил или аралкоксикарбонил и R6 представляет атом водорода или метил,
или также R5 и R6 образуют вместе с атомом азота гетероцикл с 4-7 членами, содержащий 1-2 гетероатома, где члены, необходимые для замыкания гетероцикла, независимо выбраны из
-CR12R13-, -O-, -S- и -NR14, где R12 и R13 независимо представляют, когда они имеются, атом водорода или алкил и R14 представляет атом водорода или алкил, или аралкил, или также R14 представляет фенил, необязательно замещенный 1-3 заместителями, независимо выбранными из атома галогена и алкила, или алкокси,
R2 представляет атом водорода или алкил, или аралкил,
или также R1 и R2 образуют вместе с атомом азота гетероцикл с 4-8 членами, содержащий 1-2 гетероатома, где члены, необходимые для замыкания гетероцикла, независимо выбраны из
-CR15R16-, -O-, -S- или -NR17, где R15 и R16 независимо представляют, когда они имеются, атом водорода или алкил и R17 представляет атом водорода или алкил, или аралкил,
R3 представляет атом водорода, атом галогена или алкил, галогеналкил, алкокси или алкилтио,
R4 представляет алкил, циклоалкил, циклоалкилалкил, циано, амино, -CH2-COOR18, -CH2-CO-NR19R20 или -CH2-NR21R22, или также R4 представляет карбоциклический или гетероциклический арил, необязательно замещенный 1-3 заместителями, независимо выбранными из атома галогена и алкила, галогеналкила, алкокси или NR37R38,
R18 представляет атом водорода или алкил,
R19 представляет атом водорода, алкил или аралкил, арильная группа которого необязательно замещена 1-3 заместителями, независимо выбранными из группы, состоящей из атома галогена, алкила, галогеналкила, алкокси, галогеналкокси, гидрокси, нитро, циано, фенила, SO2NHR23 и NR24R25, где R23 представляет атом водорода или алкил, или фенил и R24 и R25 независимо представляют алкил,
R20 представляет атом водорода или алкил,
или также R19 и R20 образуют вместе с атомом азота гетероцикл с 4-7 членами, содержащий 1-2 гетероатома, где члены, необходимые для замыкания гетероцикла, независимо выбраны из
-CR26R27-, -O-, -S- или -NR28, где R26 и R27 независимо представляют, когда они имеются, атом водорода или алкил и R28 представляет атом водорода или алкил, или аралкил, или также R28 представляет фенил, необязательно замещенный 1-3 заместителями, независимо выбранными из атома галогена и алкила, или алкокси,
R21 представляет атом водорода, алкил или аралкил, арильная группа которого необязательно замещена 1-3 заместителями, независимо выбранными из группы, состоящей из атома галогена, алкила, галогеналкила, алкокси, галогеналкокси, гидрокси, нитро, циано, фенила, SO2NHR29 и NR30R31, где R29 представляет атом водорода или алкил, или фенил и R30 и R31 независимо представляют алкил,
R22 представляет атом водорода или алкил,
или также R21 и R22 образуют вместе с атомом азота гетероцикл с 4-7 членами, содержащий 1-2 гетероатома, где члены, необходимые для замыкания гетероцикла, независимо выбраны из
-CR32R33-, -O-, -S- или -NR34, где R32 и R33 независимо представляют, когда они имеются, атом водорода или алкил и R34 представляет атом водорода, алкил или аралкил, или также R34 представляет фенил, необязательно замещенный 1-3 заместителями, независимо выбранными из атома галогена и алкила, или алкокси,
R37 и R38 независимо выбраны из атома водорода и алкила или R37 и R38 образуют вместе с атомом азота гетероцикл с 4-7 членами, содержащий 1-2 гетероатома, где члены, необходимые для замыкания гетероцикла, независимо выбраны из -CR39R40-, -O-, -S- или -NR41, где R39 и R40 независимо представляют, когда они имеются, атом водорода или алкил и R41 представляет атом водорода или алкил,
W представляет О или S,
необходимо понимать, что если W является S и R4 представляет необязательно замещенный арил, то тогда R1 выбран из заместителей алкоксиалкила, алкилтиоалкила, циклоалкила, -(CH2)-X-Y и -(CH2)-Z-NR5R6,
и фармацевтически приемлемые соли соединений общей формулы (I)'М.
В случае, когда W является S и R4 представляет необязательно замещенный арил, то соединения общей формулы (I)М или (I)'М, в которых R1 выбран из заместителей -(CH2)-Z-NR5R6, являются особенно предпочтительными.
Предметом изобретения в качестве лекарственных препаратов также являются соединения общей формулы (I)" или их фармацевтически приемлемые соли. Аналогично оно относится к композициям, содержащим в качестве активного ингредиента по меньшей мере одно из соединений общей формулы (I)", (I)M или (I)'M, определенных выше, или фармацевтически приемлемую соль данного соединения.
Изобретение также относится к соединениям общей формулы (II)
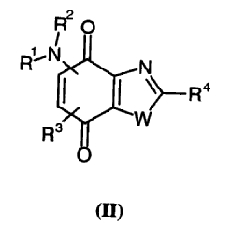
в которой R1 представляет атом водорода или алкил, алкоксиалкил, алкилтиоалкил, циклоалкил, -(CH2)-X-Y, -(CH2)-Z-NR5R6 или
-CHR35R36, в котором R35 и R36 образуют вместе с атомом углерода, к которому они присоединены, инданил или тетралинил, или также R35 и R36 образуют вместе с атомом углерода, к которому они присоединены, насыщенный гетероцикл, содержащий 5-7 членов и 1-2 гетероатома, выбранных из О, N и S, где атомы азота указанного гетероцикла необязательно замещены радикалами, выбранными из алкила и бензила,
R1 также может, когда W является О, представлять собой карбоциклический арил, необязательно замещенный 1-3 заместителями, независимо выбранными из атома галогена и алкила, галогеналкила или алкокси,
Х представляет связь или нормальный, или разветвленный алкилен, содержащий 1-5 атомов углерода,
Y представляет насыщенную углеродсодержащую циклическую систему, содержащую 1-3 конденсированных кольца, независимо выбранных из колец с 3-7 членами, или Y представляет насыщенный гетероцикл, содержащий 1-2 гетероатома, независимо выбранных из O, N или S, и соединенный с радикалом Х посредством N- или СН-члена, где указанный насыщенный гетероцикл, кроме того, содержит 2-6 дополнительных членов, выбранных из -CHR7-, -CO-, -NR8-, -O- и -S-, где R7 представляет атом водорода или алкил и R8 представляет атом водорода или алкил, или аралкил, или также Y представляет карбоциклический или гетероциклический арил, необязательно замещенный 1-3 заместителями, независимо выбранными из группы, состоящей из атома галогена, алкила, галогеналкила, алкокси, галогеналкокси, гидрокси, нитро, циано, фенила, SO2NHR9 и NR10R11, где R9 представляет атом водорода или алкил, или фенил и R10 и R11 независимо представляют алкил,
Z представляет связь или нормальный, или разветвленный алкилен, содержащий 1-5 атомов углерода,
R5 и R6 независимо выбраны из атома водорода, алкила, аралкила или -(СН2)n-OH, в котором n представляет целое число от 1 до 6,
или R5 представляет алкоксикарбонил, галогеналкоксикарбонил или аралкоксикарбонил и R6 представляет атом водорода или метил,
или также R5 и R6 образуют вместе с атомом азота гетероцикл с 4-7 членами, содержащий 1-2 гетероатома, где члены, необходимые для замыкания гетероцикла, независимо выбраны из
-CR12R13-, -O-, -S- и -NR14, где R12 и R13 независимо представляют, когда они имеются, атом водорода или алкил и R14 представляет атом водорода или алкил, или аралкил, или также R14 представляет фенил, необязательно замещенный 1-3 заместителями, независимо выбранными из атома галогена и алкила, или алкокси,
R2 представляет атом водорода или алкил, или аралкил,
или также R1 и R2 образуют вместе с атомом азота гетероцикл с 4-8 членами, содержащий 1-2 гетероатома, где члены, необходимые для замыкания гетероцикла, независимо выбраны из
-CR15R16-, -O-, -S- или -NR17, где R15 и R16 независимо представляют, когда они имеются, атом водорода или алкил и R17 представляет атом водорода или алкил, или аралкил,
R3 представляет атом водорода, атом галогена или алкил, галогеналкил, алкокси или алкилтио,
R4 представляет алкил, циклоалкил, циклоалкилалкил, циано, амино, -CH2-COOR18, -CH2-CO-NR19R20 или -CH2-NR21R22, или R4 представляет карбоциклический или гетероциклический арил, необязательно замещенный 1-4 заместителями, независимо выбранными из атома галогена и алкила, галогеналкила, алкокси, галогеналкокси или NR37R38, или также R4 представляет фенил, имеющий два заместителя, которые вместе образуют метилендиокси или этилендиокси,
R18 представляет атом водорода или алкил,
R19 представляет атом водорода, алкил или аралкил, арильная группа которого необязательно замещена 1-3 заместителями, независимо выбранными из группы, состоящей из атома галогена, алкила, галогеналкила, алкокси, галогеналкокси, гидрокси, нитро, циано, фенила, SO2NR23 и NHR24R25, где R23 представляет атом водорода или алкил, или фенил и R24 и R25 независимо представляют алкил,
R20 представляет атом водорода или алкил,
или также R19 и R20 образуют вместе с атомом азота гетероцикл с 4-7 членами, содержащий 1-2 гетероатома, где члены, необходимые для замыкания гетероцикла, независимо выбраны из
-CR26R27-, -O-, -S- или -NR28, где R26 и R27 независимо представляют, когда они имеются, атом водорода или алкил и R28 представляет атом водорода или алкил, или аралкил, или также R28 представляет фенил, необязательно замещенный 1-3 заместителями, независимо выбранными из атома галогена и алкила, или алкокси,
R21 представляет атом водорода, алкил или аралкил, арильная группа которого необязательно замещена 1-3 заместителями, независимо выбранными из группы, состоящей из атома галогена, алкила, галогеналкила, алкокси, галогеналкокси, гидрокси, нитро, циано, фенила, SO2NHR29 и NR30R31, где R29 представляет атом водорода или алкил, или фенил и R30 и R31 независимо представляют алкил,
R22 представляет атом водорода или алкил,
или также R21 и R22 образуют вместе с атомом азота гетероцикл с 4-7 членами, содержащий 1-2 гетероатома, где члены, необходимые для замыкания гетероцикла, независимо выбраны из
-CR32R33-, -O-, -S- или -NR34, где R32 и R33 независимо представляют, когда они имеются, атом водорода или алкил и R34 представляет атом водорода, алкил или аралкил, или также R34 представляет фенил, необязательно замещенный 1-3 заместителями, независимо выбранными из атома галогена и алкила, или алкокси,
R37 и R38 независимо выбраны из атома водорода и алкила или R37 и R38 образуют вместе с атомом азота гетероцикл с 4-7 членами, содержащий 1-2 гетероатома, где члены, необходимые для замыкания гетероцикла, независимо выбраны из -CR39R40-, -O-, -S- или -NR41, где R39 и R40 независимо представляют, когда они имеются, атом водорода или алкил и R41 представляет атом водорода или алкил,
W представляет О или S,
необходимо понимать, что
если W является S и R4 представляет алкил, то тогда R1 не является атомом водорода или алкилом, или циклоалкилом, и/или R3 представляет атом водорода или алкил,
если W является S и R4 представляет необязательно замещенный арил, то тогда R1 выбран из заместителей алкоксиалкила, алкилтиоалкила, циклоалкила, -(CH2)-X-Y и -(CH2)-Z-NR5R6,
а также е солям соединений общей формулы (II).
По конкретному варианту изобретения соединения общей формулы (II) представляют соединения общей формулы (II)'
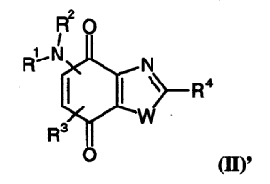
в которой R1 представляет атом водорода или алкил, алкоксиалкил, алкилтиоалкил, циклоалкил, -(CH2)-X-Y, -(CH2)-Z-NR5R6 или
-CHR35R36, в котором R35 и R36 образуют вместе с атомом углерода, к которому они присоединены, инданил или тетралинил, или также R35 и R36 образуют вместе с атомом углерода, к которому они присоединены, насыщенный гетероцикл, содержащий 5-7 членов и 1-2 гетероатома, выбранных из О, N и S, где атомы азота указанного гетероцикла необязательно замещены радикалами, выбранными из алкила и бензила,
R1 также может, когда W является О, представлять собой карбоциклический арил, необязательно замещенный 1-3 заместителями, независимо выбранными из атома галогена и алкила, галогеналкила или алкокси,
Х представляет связь или нормальный, или разветвленный алкилен, содержащий 1-5 атомов углерода,
Y представляет насыщенную углеродсодержащую циклическую систему, содержащую 1-3 конденсированных кольца, независимо выбранных из колец с 3-7 членами, или Y представляет насыщенный гетероцикл, содержащий 1-2 гетероатома, независимо выбранных из O, N или S, и соединенный с радикалом Х посредством N- или СН-члена, где указанный насыщенный гетероцикл, кроме того, содержит 2-6 дополнительных членов, независимо выбранных из -CHR7-, -CO-, -NR8-, -O- и -S-, где R7 представляет атом водорода или алкил и R8 представляет атом водорода или алкил, или аралкил, или также Y представляет карбоциклический или гетероциклический арил, необязательно замещенный 1-3 заместителями, независимо выбранными из группы, состоящей из атома галогена, алкила, галогеналкила, алкокси, галогеналкокси, гидрокси, нитро, циано, фенила, SO2NHR9 и NR10R11, где R9 представляет атом водорода или алкил, или фенил и R10 и R11 независимо представляют алкил,
Z представляет связь или нормальный, или разветвленный алкилен, содержащий 1-5 атомов углерода,
R5 и R6 независимо выбраны из атома водорода, алкила, аралкила или -(СН2)n-OH, в котором n представляет целое число от 1 до 6,
или R5 представляет алкоксикарбонил, галогеналкоксикарбонил или аралкоксикарбонил и R6 представляет атом водорода или метил,
или также R5 и R6 образуют вместе с атомом азота гетероцикл с 4-7 членами, содержащий 1-2 гетероатома, где члены, необходимые для замыкания гетероцикла, независимо выбраны из
-CR12R13-, -O-, -S- и -NR14, где R12 и R13 независимо представляют, когда они имеются, атом водорода или алкил и R14 представляет атом водорода или алкил, или аралкил, или также R14 представляет фенил, необязательно замещенный 1-3 заместителями, независимо выбранными из атома галогена и алкила, или алкокси,
R2 представляет атом водорода или алкил, или аралкил,
или также R1 и R2 образуют вместе с атомом азота гетероцикл с 4-8 членами, содержащий 1-2 гетероатома, где члены, необходимые для замыкания гетероцикла, независимо выбраны из
-CR15R16-, -O-, -S- или -NR17, где R15 и R16 независимо представляют, когда они имеются, атом водорода или алкил и R17 представляет атом водорода или алкил, или аралкил,
R3 представляет атом водорода, атом галогена или алкил, галогеналкил, алкокси или алкилтио,
R4 представляет алкил, циклоалкил, циклоалкилалкил, циано, амино, -CH2-COOR18, -CH2-CO-NR19R20 или -CH2-NR21R22, или R4 представляет карбоциклический или гетероциклический арил, необязательно замещенный 1-3 заместителями, независимо выбранными из атома галогена и алкила, галогеналкила, алкокси или NR37R38,
R18 представляет атом водорода или алкил,
R19 представляет атом водорода, алкил или аралкил, арильная группа которого необязательно замещена 1-3 заместителями, независимо выбранными из группы, состоящей из атома галогена, алкила, галогеналкила, алкокси, галогеналкокси, гидрокси, нитро, циано, фенила, SO2NHR23 и NR24R25, где R23 представляет атом водорода или алкил, или фенил и R24 и R25 независимо представляют алкил,
R20 представляет атом водорода или алкил,
или также R19 и R20 образуют вместе с атомом азота гетероцикл с 4-7 членами, содержащий 1-2 гетероатома, где члены, необходимые для замыкания гетероцикла, независимо выбраны из
-CR26R27-, -O-, -S- или -NR28, где R26 и R27 независимо представляют, когда они имеются, атом водорода или алкил и R28 представляет атом водорода или алкил, или аралкил, или также R28 представляет фенил, необязательно замещенный 1-3 заместителями, независимо выбранными из атома галогена и алкила, или алкокси,
R21 представляет атом водорода, алкил или аралкил, арильная группа которого необязательно замещена 1-3 заместителями, независимо выбранными из группы, состоящей из атома галогена, алкила, галогеналкила, алкокси, галогеналкокси, гидрокси, нитро, циано, фенила, SO2NHR29 и NR30R31, где R29 представляет атом водорода или алкил, или фенил и R30 и R31 независимо представляют алкил,
R22 представляет атом водорода или алкил,
или также R21 и R22 образуют вместе с атомом азота гетероцикл с 4-7 членами, содержащий 1-2 гетероатома, где члены, необходимые для замыкания гетероцикла, независимо выбраны из
-CR32R33-, -O-, -S- или -NR34, где R32 и R33 независимо представляют, когда они имеются, атом водорода или алкил и R34 представляет атом водорода, алкил или аралкил, или также R34 представляет фенил, необязательно замещенный 1-3 заместителями, независимо выбранными из атома галогена и алкила, или алкокси,
R37 и R38 независимо выбраны из атома водорода и алкила или R37 и R38 образуют вместе с атомом азота гетероцикл с 4-7 членами, содержащий 1-2 гетероатома, где члены, необходимые для замыкания гетероцикла, независимо выбраны из -CR39R40-, -O-, -S- или -NR41, где R39 и R40 независимо представляют, когда они имеются, атом водорода или алкил и R41 представляет атом водорода или алкил,
W представляет О или S,
необходимо понимать, что
если W является S и R4 представляет алкил, то тогда R1 не является атомом водорода или алкилом, или циклоалкилом, и/или R3 представляет атом водорода или алкил,
если W является S и R4 представляет необязательно замещенный алкил, то тогда R1 выбран из заместителей алкоксиалкила, алкилтиоалкила, циклоалкила, -(CH2)-X-Y и -(CH2)-Z-NR5R6,
или соли соединений общей формулы (II)'.
По более конкретному варианту изобретения соединения общей формулы (II)' представляют соединения общей формулы (II)"
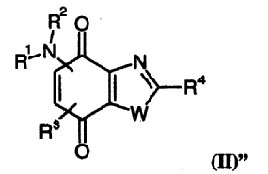
в которой R1 представляет атом водорода или алкил, циклоалкил, -(CH2)-X-Y или -(CH2)-Z-NR5R6,
R1 также может, когда W является О, представлять собой карбоциклический арил, необязательно замещенный 1-3 заместителями, независимо выбранными из атома галогена и алкила, галогеналкила или алкокси,
Х представляет связь или нормальный, или разветвленный алкилен, содержащий 1-5 атомов углерода,
Y представляет насыщенную углеродсодержащую циклическую систему, содержащую 1-3 конденсированных кольца, независимо выбранных из колец с 3-7 членами, или Y представляет насыщенный гетероцикл, содержащий 1-2 гетероатома, независимо выбранных из O, N или S, и соединенный с радикалом Х посредством N- или СН-члена, где указанный насыщенный гетероцикл, кроме того, содержит 2-6 дополнительных членов, выбранных из -CHR7-, -CO-, -NR8-, -O- и -S-, где R7 представляет атом водорода или алкил и R8 представляет атом водорода или алкил, или аралкил, или также Y представляет карбоциклический или гетероциклический арил, необязательно замещенный 1-3 заместителями, независимо выбранными из группы, состоящей из атома галогена, алкила, галогеналкила, алкокси, галогеналкокси, гидрокси, нитро, циано, фенила, SO2NHR9 и NR10R11, где R9 представляет атом водорода или алкил, или фенил и R10 и R11 независимо представляют алкил,
Z представляет связь или нормальный, или разветвленный алкилен, содержащий 1-5 атомов углерода,
R5 и R6 независимо выбраны из атома водорода, алкила, аралкила или -(СН2)n-OH, в котором n представляет целое число от 1 до 6,
или R5 и R6 образуют вместе с атомом азота гетероцикл с 4-7 членами, содержащий 1-2 гетероатома, где члены, необходимые для замыкания гетероцикла, независимо выбраны из -CR12R13-, -O-, -S- и -NR14, где R12 и R13 независимо представляют, когда они имеются, атом водорода или алкил и R14 представляет атом водорода или алкил, или аралкил, или также R14 представляет фенил, необязательно замещенный 1-3 заместителями, независимо выбранными из атома галогена и алкила или алкокси,
R2 представляет атом водорода или алкил
или также R1 и R2 образуют вместе с атомом азота гетероцикл с 4-7 членами, содержащий 1-2 гетероатома, где члены, необходимые для замыкания гетероцикла, независимо выбраны из
-CR15R16-, -O-, -S- или -NR17, где R15 и R16 независимо представляют, когда они имеются, атом водорода или алкил и R17 представляет атом водорода или алкил или аралкил;
R3 представляет атом водорода, атом галогена или алкил, галогеналкил или алкокси;
R4 представляет алкил, циклоалкил, циклоалкилалкил, циано, амино, -CH2-COOR18, -CH2-CO-NR19R20 или -CH2-NR21R22, или R4 представляет гетероциклический арил, необязательно замещенный 1-3 заместителями, независимо выбранными из атома галогена, алкила, галогеналкила или алкокси,
R18 представляет атом водорода или алкил,
R19 представляет атом водорода, алкил или аралкил, арильная группа которого необязательно замещена 1-3 заместителями, независимо выбранными из группы, состоящей из атома галогена, алкила, галогеналкила, алкокси, галогеналкокси, гидрокси, нитро, циано, фенила, SO2NHR23 и NR24R25, где R23 представляет атом водорода или алкил, или фенил и R24 и R25 независимо представляют алкил,
R20 представляет атом водорода или алкил,
или также R19 и R20 образуют вместе с атомом азота гетероцикл с 4-7 членами, содержащий 1-2 гетероатома, где члены, необходимые для замыкания гетероцикла, независимо выбраны из
-CR26R27-, -O-, -S- и -NR28, где R26 и R27 независимо представляют, когда они имеются, атом водорода или алкил и R28 представляет атом водорода или алкил, или аралкил, или также R28 представляет фенил, необязательно замещенный атомом галогена, алкилом или алкокси,
R21 представляет атом водорода, алкил или аралкил, арильная группа которого необязательно замещена 1-3 заместителями, независимо выбранными из группы, состоящей из атома галогена, алкила, галогеналкила, алкокси, галогеналкокси, гидрокси, нитро, циано, фенила, SO2NHR29 и NR30R31, где R29 представляет атом водорода или алкил, или фенил и R30 и R31 независимо представляют алкил,
R22 представляет атом водорода или алкил,
или также R21 и R22 образуют вместе с атомом азота гетероцикл с 4-7 членами, содержащий 1-2 гетероатома, где члены, необходимые для замыкания гетероцикла, независимо выбраны из
-CR32R33-, -O-, -S- и -NR34, где R32 и R33 независимо представляют, когда они имеются, атом водорода или алкил и R34 представляет атом водорода, алкил, или аралкил, или также R34 представляет фенил, необязательно замещенный атомом галогена, алкилом или алкокси, и
W представляет О или S,
необходимо понимать, что если W является S и R4 представляет алкил, то тогда R1 представляет -(CH2)-X-Y или
-(CH2)-Z-NR5R6, и/или R3 представляет атом водорода или алкил,
а также соли соединений общей формулы (II)".
Как правило, соединения общей формулы (II), (II)' или в которых R1 представляет -(CH2)-X-Y или -(CH2)-Z-NR5R6, будут предпочтительными, поскольку W является S и R4 представляет алкил.
Предпочтительно соединения общей формулы (I), (I)', (I)", (I)1, (I)2, (I)3, (I)4, (I)М, (I)М', (II), (II)' или (II)" или их фармацевтически приемлемые соли используются для получения лекарственного препарата, предназначенного для лечения заболевания, выбранного из следующих заболеваний/следующих нарушений: опухолевых пролиферативных заболеваний, в частности рака, неопухолевых пролиферативных заболеваний, нейродегенеративных заболеваний, паразитарных заболеваний, вирусных инфекций, спонтанной алопеции, алопеции, вызванной экзогенными продуктами, алопеции, вызванной облучением, аутоиммунных заболеваний, отторжения трансплантатов, воспалительных заболеваний и аллергии.
В частности, соединения общей формулы (I), (I)', (I)", (I)1, (I)2, (I)3, (I)4, (I)М, (I)М', (II), (II)' или (II)" или их фармацевтически приемлемые соли можно использовать для получения лекарственного препарата, предназначенного для лечения рака, в частности рака молочной железы, лимфом, опухолей шеи и головы, рака легких, рака ободочной кишки, рака простаты и рака поджелудочной железы.
Согласно конкретному варианту изобретения соединения общей формулы (I), (I)', (I)", (I)1, (I)2, (I)3, (I)4, (I)М, (I)М', (II), (II)' или (II)" или их фармацевтически приемлемые соли можно использовать для получения лекарственного препарата, предназначенного для лечения спонтанной алопеции, алопеции, вызванной экзогенными продуктами, или алопеции, вызванной облучением.
Предметом изобретения также является способ лечения опухолевых пролиферативных заболеваний, в частности рака, неопухолевых пролиферативных заболеваний, нейродегенеративных заболеваний, паразитарных заболеваний, вирусных инфекций, спонтанной алопеции, алопеции, вызванной экзогенными продуктами, или алопеции, вызванной облучением, аутоиммунных заболеваний, отторжения трансплантатов, воспалительных заболеваний и аллергии, где указанный способ включает введение терапевтически эффективной дозы соединения общей формулы (I), (I)', (I)", (I)1, (I)2, (I)3, (I)4, (I)М, (I)М' (или соединения общей формулы (II), (II)' или (II)") пациенту при необходимости подобного лечения.
Как правило, применимы по аналогии те же предпочтения, что указывались для применений соединений общей формулы (I), (I)', (I)", (I)1, (I)2, (I)3 или (I)4 для лекарственных препаратов, фармацевтических композиций и соединений по изобретению независимо от того, относятся ли последние к соединениям общей формулы (I), (I)', (I)", (I)1, (I)2, (I)3, (I)4, (I)М, (I)М' или к таковым общей формулы (II), (II)' или (II)".
Фармацевтические композиции, содержащие соединение по изобретению, могут находиться в виде твердых веществ, например порошков, гранул, таблеток, желатиновых капсул, липосом или суппозиториев. Соответствующими твердыми носителями могут быть фосфат кальция, стеарат магния, тальк, сахара, лактоза, декстрин, крахмал, желатин, целлюлоза, метилцеллюлоза, натриевая соль карбоксиметилцеллюлозы, поливинилпирролидон и воск.
Фармацевтические композиции, содержащие соединение по изобретению, могут находиться в жидкой форме, например в виде растворов, эмульсий, суспензий или сиропов. Соответствующими жидкими носителями могут быть, например, вода, органические растворители такие, как глицин или гликоли, а также их смеси в различных пропорциях в воде.
Введение лекарственного препарата по изобретению можно проводить местным, пероральным, парентеральным путем, внутримышечной инъекцией и т.д.
Доза для введения, предусмотренная для лекарственного препарата по изобретению, составляет от 0,1 мг до 10 г в зависимости от типа используемого активного соединения.
Согласно изобретению соединения общей формулы (I) (или таковые общей формулы (II), которые все также являются соединениями общей формулы (I)) можно получить, например, способами, описанными ниже.
Получение соединений общей формулы (I)
Способы получения, представленные ниже, даны в качестве иллюстрации, и специалисты в данной области могут подвергнуть их пригодным на их взгляд изменениям как в отношении реагентов, так и условий и схем реакций.
Общий способ
В общем, соединения формулы (I) можно получить по схеме, представленной на схеме 1 ниже.
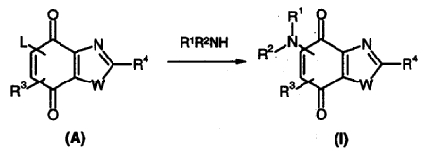
Схема 1
Согласно данному способу соединения общей формулы (I), в которых R1, R2,R3, R4 или W имеют значения, определенные выше, получают обработкой соединений общей формулы (А), в которых L представляет метокси, атом галогена или атом водорода и R3, R4 и W имеют те же значения, что в общей формуле (I), аминами общей формулы NR1R2H в протонном растворителе таком, как метанол или этанол, при температуре в пределах от 0 до 50°С и необязательно в присутствии основания, например, такого, как диизопропилэтиламин (Yasuyuki Kita et al., J. Org. Chem. (1996), 61, 223-227).
В конкретном случае, когда соединения общей формулы (А) представляют таковые, в которых L и R3 каждый представляет атом галогена, соединения общей формулы (I) можно получить в виде смеси изомеров по 2-му положению, но затем возможно разделить их хроматографией на колонке с силикагелем с использованием соответствующего элюента.
Альтернативно соединения общей формулы (I), в которой R3 представляет атом галогена (Hal), можно получить, схема 1а, из соединений общей формулы (I), в которых R3 представляет атом водорода, например, воздействием N-хлорсукцинимида или N-бромсукцинимида в апротонном растворителе таком, как дихлорметан или тетрагидрофуран (Paquette et Farley, J. Org. Chem. (1967), 32, 2725-2731), воздействием водного раствора гипохлорита натрия (обесцвечивание) в растворителе таком, как уксусная кислота (Jagadeesh et al., Synth. Commun. (1998), 28, 3827-3833), воздействием Cu(II) (в смеси CuCl2/HgCl2) в присутствии каталитического количества йода в растворителе таком, как теплая уксусная кислота (Thapliyal, Synth. Commun. (1998), 28, 1123-1126), воздействием агента такого, как бензилтриметиламмонийдихлорйодат в присутствии NaHCO3 в растворителе таком, как смесь дихлорметан/метанол (Kordik and Reitz, J. Org. Chem. (1996), 61, 5644-5645) или также при использовании хлора, брома или йода в растворителе таком, как дихлорметан (J.Renault, S.Giorgi-Renault et al., J. Med. Chem. (1983), 26, 1715-1719).
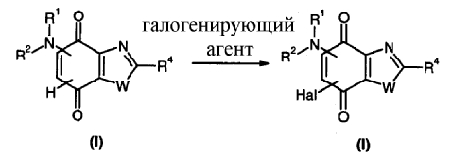
Схема 1а
Альтернативно также можно получить соединения общей формулы (I), в которых R3 представляет алкокси или алкитио, схема 1b, из соединений общей формулы (I), в которых R3 представляет атом галогена, например, воздействием спирта общей формулы R3'-ОН или тиола общей формулы R3'-SH (где R3' является таковым, что R3=R3'О или R3'-S) в растворителе таком, как безводный этанол в присутствии основания, например, такого, как диизопропилэтиламин.
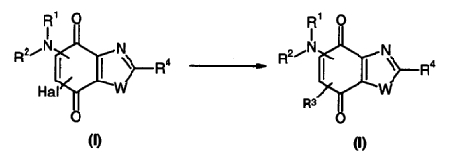
Схема 1b
Получение промежуточных соединений общей формулы (А)
Можно получить соединения общей формулы (А), в которых L, R3, R4 и W имеют значения, определенные выше, схема 2, начиная с соединений общей формулы (В), в которых L, R3, R4 и W имеют значения, определенные выше, и
один из Q и Q' представляет амино или гидроксил, а другой представляет атом водорода или
Q и Q' каждый представляет амино, или
Q и Q' каждый представляет гидрокси, или, наконец,
Q и Q' каждый представляет метокси.
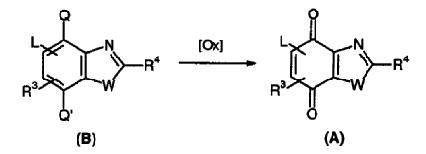
Схема 2
В случае, когда соединения общей формулы (В) являются таковыми, что Q и Q' представляют метокси, соединения общей формулы (А) получают обработкой церием (IV) и нитратом аммония (Beneteau et al., Eur. J. Med. Chem. (1999), 34 (12), 1053-1060). В других случаях соединения общей формулы (А) получают окислением соединений общей формулы (В), например, при использовании FeCl3 в кислой среде (Antonini et al., Heterocycles (1982), 19 (12), 2313-2317) или соли Фреми (нитрозодисульфоната калия) (Ryu et al., Bioorg. Med. Chem. Lett. (2000), 10, 461-464) или при использовании реагента, содержащего йод с наивысшей валентностью такой, как [бис(ацетокси)йод]бензол или [бис(трифторацетокси)йод]бензол в водном ацетонитриле при температуре предпочтительно в пределах от -20°С до комнатной температуры (т.е. примерно 25°С) и предпочтительно примерно при -5°С (Kinugawa et al., Synthesis (1996), 5, 633-636).
В конкретном случае, когда L и R3 представляют атомы галогена, соединения общей формулы (А) можно получить, схема 3, окислением галогена соединений общей формулы (В), в которых L и R3 представляют атомы водорода и Q и/или Q' выбран (выбраны) из амино и гидрокси, воздействием, например, перхлората калия или натрия в кислой среде (Ryu et al., Bioorg. Med. Chem. Lett. (1999), 9, 1075-1080).
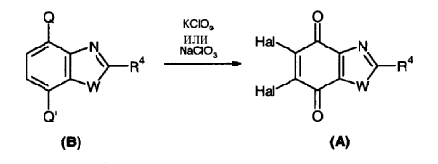
Схема 3
Получение промежуточных соединений общей формулы (В)
Некоторые соединения общей формулы (В), в которых L, R3, R4, Q, Q' и W имеют значения, определенные выше, являются известными промышленными продуктами, доступными от обычных поставщиков.
Если они не являются промышленно доступными и в конкретном случае, когда Q и Q' представляют амино, то соединения общей формулы (В) можно, в частности, получить из нитропроизводных формулы (В.ii), в которой Q и Q' представляют нитро, способами восстановления, которые хорошо известны специалистам в данной области такими, как, например, гидрирование в присутствии катализатора палладия или обработкой хлоридом олова в соляной кислоте. Если они не являются промышленно доступными, то, в свою очередь, соединения общей формулы (В.ii) можно получить из соединений общей формулы (В.i), в которой положения, соответствующие Q и Q' замещены атомами водорода, способами нитрования, которые хорошо известны специалистам в данной области такими, как, например, обработка смесью азотной кислоты и серной кислоты (смотри схему 4, где представлен случай, когда соединения общей формулы (В) являются такими, что Q=NH2 и Q'=H).
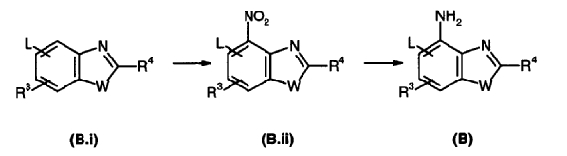
Схема 4
Альтернативно соединения общей формулы (В), которые не являются промышленно доступными, в которых Q представляет амино, Q' является атомом водорода и W представляет атом кислорода, можно получить обработкой тетрагидробензоксазолов общей формулы (В.vi) гидроксиламином гидрохлоридом с получением оксимов общей формулы (B.v), которые, в свою очередь, обрабатывают теплой полифосфорной кислотой (смотри Young Kook Koh et al., J. Heterocyclic Chem. (2001), 38, 89-92) с получением соединений общей формулы (B). Соединения общей формулы (B.vi), в свою очередь, можно получить из циклических 1,3-дикетонов общей формулы (B.viii) вначале превращением в диазодикетоны общей формулы (B.vii) в реакции диазоперегруппировки, например, при воздействии тозилазида или 4-ацетамидобензолсульфонилазида в присутствии триэтиламина в растворителе таком, как безводный дихлорметан или хлороформ (V.V.Popic et al., Synthesis (1991), 3, 195-198) с последующим циклоприсоединением данных диазодикетонов общей формулы (B.vii) с нитрилами общей формулы R4-CN в присутствии катализатора типа родия (II) (Y.R.Lee, Heterocycles (1998), 48, 875-883) (смотри схему 4а).
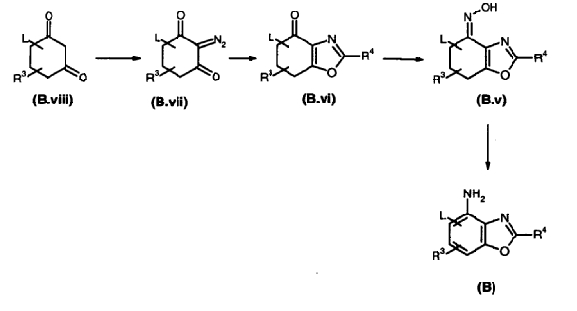
Схема 4а
Если они не являются промышленно доступными и в конкретном случае, когда Q представляет гидроксил, Q' является атомом водорода и W представляет атом кислорода, соединения общей формулы (B) можно получить ароматизацией оксазолоциклогексанонов общей формулы (B.vi). Подобную ароматизацию можно проводить в две стадии, как показано на схеме 4b, вначале галогенированием по положению α карбонила (что приводит к образованию промежуточных продуктов общей формулы (B.ix), в которой Hal представляет атом галогена), затем β-элиминированием галогена обработкой основанием. Галогенирование можно проводить, например, с использованием брома в уксусной кислоте при комнатной температуре, пиридиния трибромида в уксусной кислоте при 50°С, бромида меди (II) в этилацетате или ацетонитриле при кипячении с обратным холодильником или также фенилселенилхлорида в этилацетате при комнатной температуре. Элиминацию полученного галогенида можно проводить с помощью диазабицикло[5.4.0]ундек-7-ена (DBU) в тетрагидрофуране при комнатной температуре или карбоната лития в диметилформамиде. Примеры данных реакций имеются у M.Tany et al., Chem. Pharm. Bull. (1996), 44, 55-61; M.A.Ciufolini et al., J. Am. Chem. Soc. (1995), 117, 12460-12469, и M.E.Jung и L.S.Starkey, Tetrahedron (1997), 53, 8815-8824.
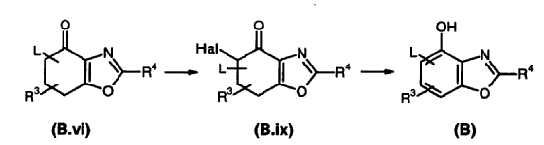
Схема 4b
Если они являются промышленно доступными, и в конкретном случае, когда R4 представляет -CH2-NR21R22, соединения общей формулы (B) можно получить, схема 5, из соединений общей формулы (B.iii), в которой R4 представляет метил, который вначале подвергается реакции бромирования с использованием N-бромсукцинимида в присутствии инициатора такого, как 2',2-азобис(2-метилпропионитрил) или дибензоилпероксид, в апротонном растворителе таком, как четыреххлористый углерод (CCl4) при температуре предпочтительно в пределах от комнатной температуры (т.е. примерно 25°С) до 80°С и под облучением с помощью УФ-лампы (Mylari et al., J. Med. Chem. (1991), 34, 108-122) с последующим замещением промежуточного соединения общей формулы (B.iv) аминами формулы NHR21R22, где R21 и R22 имеют значения, определенные выше.
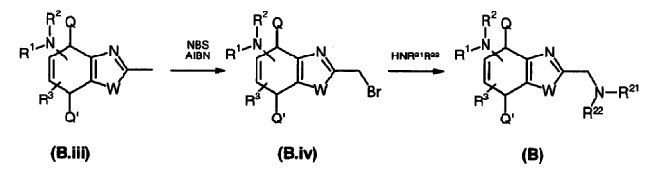
Схема 5
Альтернативно соединения общей формулы (В), которые не являются промышленно доступными, в которых R4 представляет -CH2-NR21R22, можно получить способом, представленным на схеме 4 выше, начиная с соединений общей формулы (B.i), в которой R4 представляет -CH2-NR21R22, которые, в свою очередь, получают из соединений общей формулы (B.i), в которой R4 представляет CH2-Br, замещением аминами формулы NHR21R22, где R21 и R22 имеют значения, определенные выше. Соединения общей формулы (B.i), в которой R4 представляет CH2-Br, можно получить, как описано выше, из соединений общей формулы (B.i), в которых R4 представляет метил, который подвергают реакции бромирования.
Если они не являются промышленно доступными, и в конкретном случае, когда R4 представляет -CH2-CO-NR19R20, соединения общей формулы (B) можно получить из соединений общей формулы (B), в которой R4 представляет -CH2-COOH, обычными способами синтеза пептидов (M.Bodansky, The Practice of Peptide Synthesis, 145 (Springer-Verlag, 1984)), например, в тетрагидрофуране, дихлорметане или диметилформамиде в присутствии реагента для сочетания такого, как циклогексилкарбодиимид (DCC), 1,1'-карбонилдиимидазол (CDI) (J. Med. Chem. (1992), 35, (23), 4464-4472) или бензотриазол-1-илокси-трис-пирролидинофосфонийгексафторфосфат (PyBOP) (Coste et al., Tetrahedron Lett. (1990), 31, 205).
Соединения общей формулы (B), в которых R4 представляет -CH2-COOH, можно получить из соединений общей формулы (B), в которой R4 представляет -CH2-COOR18, где R18 является алкилом, гидролизом эфирной группы в условиях, известных специалистам в данной области.
Соединения общей формулы (B), в которой W представляет S, Q и Q' каждый представляет метокси и L представляет атом галогена или атом водорода, можно получить, схема 6, обработкой N-(2,5-диметоксифенил)тиоамидов общей формулы (B.x) водным раствором феррицианида калия в щелочной среде при комнатной температуре (Lyon et al., J. Chem. Soc. Perkin Trans. 1 (1999), 437-442). Соединения общей формулы (B.x), в свою очередь, можно получить, начиная с соответствующих ацилированных 2,5-диметоксианилинов общей формулы (B.xii), например, воздействием хлорангидрида общей формулы R4COCl или карбоновой кислоты общей формулы R4COOH, активированными способами, известными в данной области, с получением N-(2,5-диметоксифенил)амидов общей формулы (B.xi) с их превращением в тиоамиды общей формулы (B.x) действием реагента Лавессона в толуоле при кипячении с обратным холодильником.
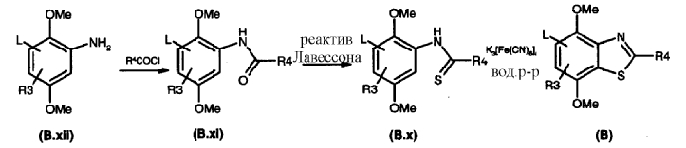
Схема 6
В других случаях соединения общей формулы (B) можно получить, схема 6, из соединений общей формулы (С), в которой L, R3 и W имеют значения, определенные выше, и Q и Q' представляют NO2, конденсацией с ортоэфиром общей формулы R4C(OR)3, в которой R представляет алкил, например, в присутствии каталитического количества кислоты такой, как, например, пара-толуолсульфоновая кислота, при температуре в пределах от комнатной температуры до 200°С и предпочтительно при 110°С (Jenkins et al., J. Org. Chem. (1961), 26, 274) или также в протонном растворителе таком, как этанол, при температуре в пределах от комнатной температуры (т.е. примерно 25°С) до 80°С и предпочтительно примерно при 60°С (Scott et al., Synth. Commun. (1989), 19, 2921). Определенные ортоэфиры являются известными промышленными продуктами, доступными от обычных поставщиков. Получение ортоэфиров обработкой различных нитрилов газообразным хлористым водородом в спирте является известным специалистам в данной области.
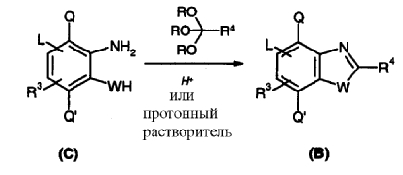
Схема 6а
Соединения общей формулы (B), в которой L, R3 и W имеют значения, определенные выше, и Q или Q' представляет NO2, можно также получить из соединений общей формулы (С), в которой L, R3, R4 и W имеют значения, определенные выше, и один из Q и Q' представляет NO2, в то время как другой представляет атом водорода, конденсацией последнего с хлорангидридом формулы R4-COCl в инертной атмосфере и в полярном и слегка щелочном растворителе таком, как N-метил-2-пирролидинон (Brembilla et al., Synth. Commun. (1990), 20, 3379-3384) или конденсацией последнего с карбоновой кислотой общей формулы R4-COOH в присутствии полифосфорной кислоты при высокой температуре (Ying-Hung So et al., Synth. Commun. (1998), 28, 4123-4135) или в присутствии борной кислоты в растворителе таком, как ксилол, при кипячении с обратным холодильником (M.Terashima, Synthesis (1982), 6, 484-485).
Соединения общей формулы (B), в которой L, R3, R4 и W имеют значения, определенные выше, и Q или Q' представляет NO2, можно также получить из соединений общей формулы (С), в которой L, R3, R4 и W имеют значения, определенные выше, и один из Q и Q' представляет NO2, в то время как другой является атомом водорода, конденсацией с альдегидом общей формулы R4-CHO с последующей обработкой основанием Шиффа, полученного с окисляющим агентом таким, как [бис(ацетокси)йод]бензол, хлорид железа (III) или диметилсульфоксид (Racane et al., Monatsh. Chem. (1995), 126 (12), 1375-1381) или дегидратацией ледяной уксусной кислотой при температуре в пределах от комнатной температуры (т.е. примерно 25°С) до 100°С (Katrizky and Fan, J. Heterocyclic Chem. (1988), 25, 901-906).
Соединения общей формулы (В), в которой L, R3, R4 и W имеют значения, определенные выше, и один из Q и Q' представляет NO2, в то время как другой является атомом водорода, можно также получить из соединений общей формулы (С) конденсацией с нитрилом общей формулы R4-CN в смеси растворителей типа метанол/ледяная уксусная кислота при температуре в интервале от комнатной температуры (т.е. примерно 25°С) до 100°С (Nawwar and Shafik, Collect. Czech. Chem. Commun. (1995), 60 (12), 2200-2208).
Получение промежуточных соединений общей формулы (С)
Некоторые соединения общей формулы (С), в которых L, R3, R4, Q, Q' и W имеют значения, определенные выше, являются промышленно доступными продуктами от обычных поставщиков.
Некоторые соединения общей формулы (С), в которых один из Q и Q' представляет NO2, в то время как другой представляет атом водорода, можно получить из соединений общей формулы (D)
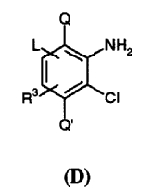
в которой L, R3, Q и Q' имеют значения, определенные выше, взаимодействием, в случае, когда W представляет S, с гидратированным сульфидом натрия при температуре в интервале от комнатной температуры (т.е. примерно 25°С) до 100°С (Katrizky and Fan, J. Heterocyclic Chem. (1988), 25, 901-906).
Наконец, в конкретном случае, когда W представляет О, соединения общей формулы (С) являются известными промышленно доступными продуктами от обычных поставщиков или их можно синтезировать из подобных продуктов с использованием обычных способов, известных специалистам в данной области.
Разделение смесей региоизомеров
В некоторых случаях может так случиться, что соединения общей формулы (I), полученные вышеуказанными способами, получают в виде смесей региоизомеров.
В подобных ситуациях смеси можно разделить с использованием стандартных методов жидкостной хроматографии на колонке или препаративной тонкослойной хроматографии (с использованием носителя такого, как силикагель или также гель такой, как поперечно-сшитый полидекстран, образующий трехмерную сеть такую, как гель типа Сефадекс® LH-20). Специалисты в данной области выберут наиболее подходящий элюент для разделения смеси; подобным элюентом может быть, например, смесь из трех компонентов изопропанол/этилацетат/вода 1/1/1.
Что касается температуры в данном тексте, то термин «примерно ХХ°С» указывает, что данная температура соответствует пределу более или менее 10°С с одной стороны температуры ХХ°С и предпочтительно пределу более или менее 5°С с другой стороны температуры ХХ°С.
Если не указывается иначе, то все технические и научные термины, использованные здесь, имеют те же значения, что обычно понимаются специалистами в данной области, к которой относится настоящее изобретение. Аналогично все публикации, заявки на патент, все патенты и все другие источники, упомянутые здесь, включены для сведения.
Последующие примеры представлены для иллюстрации вышеуказанных способов, и их ни в коем случае не следует рассматривать в качестве ограничивающих объем изобретения.
Примеры
Способ, использованный для определения времени удерживания (r.t.) и молекулярного пика (МН+)
Соединения характеризуются временем удерживания (r.t.), выраженным в минутах, определяемым жидкостной хроматографией (ЖХ), и их молекулярным пиком (МН+), определяемым масс-спектрометрией (МС), для чего использовали четырехполюсный масс-спектрометр (Micromass, Platform model), снабженный источником электрораспыления с разрешением 0,8 Da при 50% долине.
Для примеров 1-122 ниже условия элюирования, соответствующие указанным результатам, являются следующими: переход от смеси ацетонитрил-вода-трифторуксусная кислота 50-950-0,2 (А) к смеси ацетонитрил-вода 950-50 (В) в линейном градиенте в течение 8,5 мин с последующим элюированием чистой смесью В в течение 10,5 мин.
Пример 1: 2-метил-5-{[2-(4-морфолинил)этил]амино}-1,3-бензотиазол-4,7-дион
51,2 мкл (0,39 ммоль; 3 экв) 4-(2-аминоэтил)морфолина добавляют к раствору 27 мг (0,129 ммоль) 5-метокси-2-метил-4,7-диоксобензотиазола в 2 мл безводного этанола. Реакционную смесь перемешивают при кипячении с обратным холодильником в течение 18 ч, затем растворитель выпаривают при пониженном давлении. Остаток очищают на колонке с силикагелем (элюент: 5% метанола в дихлорметане). Предполагаемое соединение получают в виде красного порошка.
ЯМР 1Н (ДМСО d6, 400 мГц, δ): 7,45 (т, 1Н, NH), 5,49 (с, 1Н, СН), 3,58-3,55 (м, 4Н, 2 СН2), 3,26 (т, 2Н, СН2), 2,75 (с, 3Н, СН3), 2,54 (т, 2Н, СН2), 2,42-2,40 (м, 4Н, 2 СН2).
МС-ЖХ: МН+ = 308,25; время удерживания = 6,89 мин.
Пример 2: 5-{[2-(диметиламино)этил]амино}-2-метил-1,3-бензотиазол-4,7-дион гидрохлорид
2.1) 5-{[2-(Диметиламино)этил]амино}-2-метил-1,3-бензотиазол-4,7-дион
Данное соединение получают способом, аналогичным использованному для соединения примера 1.
ЯМР 1Н (ДМСО d6, 400 мГц, δ): 7,34 (т, 1Н, NH), 5,48 (с, 1Н, СН), 3,24-3,20 (м, Н, СН2), 2,77 (с, 3Н, СН3), 2,47 (м, 2Н, СН2), 2,18 (с, 6Н, 2 СН3).
МС-ЖХ: МН+ = 266,27; время удерживания = 6,83 мин.
2.2) 5-{[2-(Диметиламино)этил]амино}-2-метил-1,3-бензотиазол-4,7-диона гидрохлорид
0,166 г промежуточного продукта 2.1 растворяют в 1,88 мл (1,88 ммоль; 3 экв) 1М раствора соляной кислоты в диэтиловом эфире и реакционную смесь перемешивают в течение 3 ч при комнатной температуре. Полученный осадок собирают фильтрованием с последующим промыванием этиловым эфиром и высушиванием при пониженном давлении с получением темно-красного твердого вещества. Точка плавления 138-140°С.
ЯМР 1Н (ДМСО d6, 400 мГц, δ): 10,00 (т, 1Н, NH+), 7,78 (т, 1Н, NH), 5,68 (с, 1Н, СН), 3,59-3,55 (м, 2Н, СН2), 3,32-3,27 (м, 2Н, СН2), 2,85-2,80 (с, 6Н, 2 СН3), 2,76 (с, 3Н, СН3).
МС-ЖХ: МН+ = 266,12; время удерживания = 6,92 мин.
Соединения примеров 3-14 получают способом, аналогичным использованному для примера 1.
Пример 3: 5-{[6-(диметиламино)гексил]амино}-2-метил-1,3-бензотиазол-4,7-дион
МС-ЖХ: МН+ = 322,33; время удерживания = 7,36 мин.
Пример 4: 5-{[3-(диметиламино)-2,2-диметилпропил]амино}-2-метил-1,3-бензотиазол-4,7-дион
ЯМР 1Н (ДМСО d6, 400 мГц, δ): 8,62 (т, 1Н, NH), 5,45 (с, 1Н, СН), 3,07-3,06 (м, 2Н, СН2), 2,74 (с, 3Н, СН3), 2,29-2,30 (м, 2Н, СН2), 2,27 (с, 6Н, 2 СН3), 0,93 (с, 6Н, 2 СН3).
МС-ЖХ: МН+ = 308,32; время удерживания = 7,16 мин.
Пример 5: 2-метил-5-{[3-(4-метил-1-пиперазинил)пропил]амино}-1,3-бензотиазол-4,7-дион
ЯМР 1Н (ДМСО d6, 400 мГц, δ): 8,14 (т, 1Н, NH), 5,46 (с, 1Н, СН), 3,25-3,26 (м, 2Н, СН2), 3,21-3,19 (м, 2Н, СН2), 2,74 (с, 3Н, СН3), 2,49-2,48 (м, 2Н, СН2), 2,37-2,32 (м, 6Н, 3СН2), 2,16 (с, 3Н, СН3), 1,72 (т, 2Н, СН2).
МС-ЖХ: МН+ = 335,34; время удерживания = 6,87 мин.
Пример 6: 5-[(1-этилгексил)амино]-2-метил-1,3-бензотиазол-4,7-дион
МС-ЖХ: МН+ = 307,32; время удерживания = 11,45 мин.
Пример 7: 5-[(1-адамантилметил)амино]-2-метил-1,3-бензотиазол-4,7-дион
МС-ЖХ: МН+ = 343,31; время удерживания = 11,73 мин.
Пример 8: 2-метил-5-[(2-тиенилметил)амино]-1,3-бензотиазол-4,7-дион
МС-ЖХ: МН+ = 291,16; время удерживания = 9,24 мин.
Пример 9: 5-[(3-хлорбензил)амино]-2-метил-1,3-бензотиазол-4,7-дион
МС-ЖХ: МН+ = 319,24; время удерживания = 9,95 мин.
Пример 10: 2-метил-5-[(4-пиридинилметил)амино]-1,3-бензотиазол-4,7-дион
МС-ЖХ: МН+ = 286,13; время удерживания = 6,97 мин.
Пример 11: 2-метил-5-(пропиламино)-1,3-бензотиазол-4,7-дион
МС-ЖХ: МН+ = 237,16; время удерживания = 8,74 мин.
Пример 12: 5-{[3-(1Н-имидазол-1-ил)пропил]амино}-2-метил-1,3-бензотиазол-4,7-дион
МС-ЖХ: МН+ = 303,17; время удерживания = 7,07 мин.
Пример 13: 4-{2-[(2-метил-4,7-диоксо-4,7-дигидро-1,3-бензотиазол-5-ил)амино]этил}бензолсульфонамид
МС-ЖХ: МН+ = 378,10; время удерживания = 8,31 мин.
Пример 14: 5-(4-бензил-1-пиперазинил)-2-метил-1,3-бензотиазол-4,7-дион
МС-ЖХ: МН+ = 354,19; время удерживания = 7,53 мин.
Пример 15: 5-анилино-2-этил-4,7-дигидробензо[d][1,3]оксазол-4,7-дион
15.1) 2-Этил-4-нитро-1,3-бензоксазол
Смесь 2-амино-3-нитрофенола (1 экв), триэтилортопропионата (2 экв) и п-толуолсульфоновой кислоты (в каталитическом количестве) перемешивают при 100°С до исчезновения аминофенола, что подтверждают тонкослойной хроматографией (2 ч). После охлаждения реакционную смесь переводят в толуол с последующим упариванием в вакууме, затем обрабатывают изопропанолом. Полученный осадок собирают фильтрованием с последующим промыванием изопропанолом и изопентаном, затем высушивают при пониженном давлении с получением фиолетово-коричневого твердого вещества.
ЯМР 1Н (ДМСО d6, 400 мГц, δ): 8,15 (дд, 2Н), 7,58 (т, 1Н), 3,06 (кв, 2Н), 1,38 (т, 3Н).
МС-ЖХ: МН+ = 193,02; время удерживания = 9,23 мин.
15.2) 2-Этил-1,3-бензоксазол-4-амин
2-Этил-4-нитро-1,3-бензоксазол гидрируют под давлением 8 бар в присутствии 10% палладия на угле (0,01 экв) с использованием метанола в качестве растворителя. Катализатор отделяют фильтрованием и метанол удаляют при пониженном давлении. Остаток переводят в этиловый эфир с получением бледно-фиолетового твердого вещества, которое собирают фильтрованием и высушивают. Точка плавления 46°С.
ЯМР 1Н (ДМСО d6, 400 мГц, δ): 6,97 (т, 1Н), 6,72 (д, 1Н), 6,47 (д, 1Н), 5,45 (с, 2Н), 2,87 (кв, 2Н), 1,32 (т, 3Н).
МС-ЖХ: МН+ = 162,99; время удерживания = 8,72 мин.
15.3) 2-Этил-1,3-бензоксазол-4,7-дион
Раствор [бис-(трифторацетокси)йод]бензола (2,2 экв) в смеси ацетонитрил/вода (80/20) добавляют по каплям к раствору 2-этил-1,3-бензоксазол-4-амина (1 экв) в той же смеси ацетонитрил/вода при -5°С. Затем реакционную смесь разбавляют водой с последующей экстракцией дихлорметаном. Полученную органическую фазу промывают водой с последующим высушиванием над сульфатом натрия и концентрируют с получением коричневой пасты. Очистка хроматографией среднего давления на силикагеле дает, после перевода в диизопропиловый эфир, желтое кристаллическое твердое вещество. Точка плавления 99°С.
ЯМР 1Н (CDCl3, 400 мГц, δ): 6,75 (дд, 2Н), 2,99 (кв, 2Н), 1,45 (т, 3Н).
МС-ЖХ: МН+ = 177,83; время удерживания = 8,29 мин.
15.4) 5-Анилино-2-этил-1,3-бензоксазол-4,7-дион
Смесь 2-этил-1,3-бензоксазол-4,7-диона (1 экв) и анилина (1,1 экв) в этаноле перемешивают в течение 1 ч. Цвет реакционной смеси становится темно-фиолетовым. После концентрирования остаток очищают хроматографией среднего давления на силикагеле с получением фиолетового порошка. Точка плавления 200°С.
ЯМР 1Н (ДМСО d6, 400 мГц, δ): 9,38 (с, 1Н), 7,44 (т, 2Н), 7,36 (д, 2Н), 7,22 (т, 1Н), 5,69 (с, 1Н), 2,94 (кв, 2Н), 1,29 (т, 3Н).
МС-ЖХ: МН+ = 269,11; время удерживания = 9,76 мин.
Пример 16: 5-анилино-6-хлор-2-этил-1,3-бензоксазол-4,7-дион
Раствор 5-анилино-2-этил-1,3-бензоксазол-4,7-диона (1 экв) в уксусной кислоте обрабатывают N-хлорсукцинимидом (1,1 экв) при комнатной температуре. Реакционную смесь перемешивают в течение 2 ч перед концентрированием с последующим переводом в этанол и вновь концентрируют. Остаток очищают хроматографией среднего давления на силикагеле с получением фиолетового порошка. Точка плавления 159°С.
ЯМР 1Н (CDCl3, 400 мГц, δ): 9,39 (с, 1Н), 7,30 (т, 2Н), 7,11 (м, 3Н), 2,96 (кв, 2Н), 1,30 (т, 3Н).
МС-ЖХ: МН+ = 303,01; время удерживания = 10,28 мин.
Пример 17: 2-этил-5-[(4-фторфенил)амино]-1,3-бензоксазол-4,7-дион
Применяемая методика аналогична описанной в примере 15 с использованием 4-фторанилина вместо анилина на четвертой и последней стадии. Точка плавления 232°С.
ЯМР 1Н (CDCl3, 400 мГц, δ): 9,38 (с, 1Н), 7,37 (т, 2Н), 7,26 (т, 2Н), 5,57 (с, 1Н), 2,93 (кв, 2Н), 1,30 (т, 3Н).
МС-ЖХ: МН+ = 287,09; время удерживания = 9,88 мин.
Соединения примеров 18-31 получают способом, аналогичным описанному в примере 1.
Пример 18: 5-[(2-метоксиэтил)амино]-2-метил-1,3-бензотиазол-4,7-дион
МС-ЖХ: МН+ = 253,20; время удерживания = 8,00 мин.
Пример 19: 2-метил-5-[(2-пирролидин-1-илэтил)амино]-1,3-бензотиазол-4,7-дион
ЯМР 1Н (ДМСО d6, 400 мГц, δ): 7,45 (т, 1Н, NH), 5,47 (с, 1Н, СН), 3,28-3,23 (м, 2Н, СН2), 2,75 (с, 3Н, СН3), 2,66-2,63 (м, 2Н, СН2), 2,48-2,49 (м, 4Н, 2СН2), 1,68-1,67 (м, 4Н, 2СН2).
МС-ЖХ: МН+ = 292,13; время удерживания = 7,11 мин.
Пример 20: 2-метил-5-[(2-пиперидин-1-илэтил)амино]-1,3-бензотиазол-4,7-дион
МС-ЖХ: МН+ = 306,24; время удерживания = 7,22 мин.
Пример 21: 5-{[2-(диизопропиламино)этил]амино}-2-метил-1,3-бензотиазол-4,7-дион
МС-ЖХ: МН+ = 322,33; время удерживания = 7,37 мин.
Пример 22: 5-[(1-бензилпирролидин-3-ил)амино]-2-метил-1,3-бензотиазол-4,7-дион
МС-ЖХ: МН+ = 354,28; время удерживания = 7,70 мин.
Пример 23: 5-{[3-(диметиламино)пропил]амино}-2-метил-1,3-бензотиазол-4,7-дион
МС-ЖХ: МН+ = 280,15; время удерживания = 7,01 мин.
Пример 24: 2-метил-5-{[1-метилпирролидин-2-ил)этил]амино}-1,3-бензотиазол-4,7-дион
МС-ЖХ: МН+ = 306,30; время удерживания = 7,23 мин.
Пример 25: 2-метил-5-{[3-(2-метилпиперидин-1-ил)пропил]амино}-1,3-бензотиазол-4,7-дион
МС-ЖХ: МН+ = 334,29; время удерживания = 7,38 мин.
Пример 26: 5-{[4-(диметиламино)бутил]амино}-2-метил-1,3-бензотиазол-4,7-дион
МС-ЖХ: МН+ = 294,16; время удерживания = 7,11 мин.
Пример 27: 5-{[5-(диметиламино)пентил]амино}-2-метил-1,3-бензотиазол-4,7-дион
МС-ЖХ: МН+ = 308,16; время удерживания = 7,22 мин.
Пример 28: 5-(2,3-дигидро-1Н-инден-1-иламино)-2-метил-1,3-бензотиазол-4,7-дион
МС-ЖХ: МН+ = 311,26; время удерживания = 10,16 мин.
Пример 29: 5-{бензил[2-(диметиламино)этил]амино}-2-метил-1,3-бензотиазол-4,7-дион
ЯМР 1Н (ДМСО d6, 400 мГц, δ): 7,73-7,28 (м, 5Н, H аром.), 5,61 (с, 1Н, СН), 4,57 (с, 2Н, СН2), 3,71-3,68 (м, 2Н, СН2), 2,75 (с, 3Н, СН3), 2,39-2,37 (м, 2Н, СН2), 1,95 (с, 6Н, 2 СН3).
МС-ЖХ: МН+ = 365,10; время удерживания = 7,70 мин.
Пример 30: трет-бутилметил{3-[(2-метил-4,7-диоксо-4,7-дигидро-1,3-бензотиазол-5-ил)амино]пропил}карбамат
ЯМР 1Н (ДМСО d6, 400 мГц, δ): 7,75 (м, 1Н, NH), 5,45 (с, 1Н, СН), 3,22-3,18 (м, 2Н, СН2), 3,15-3,12 (м, 2Н, СН2), 2,76 (м, 3Н, СН3), 2,75 (с, 3Н, СН3), 1,78-1,75 (м, 2Н, СН2), 1,35 (м, 9Н, 3 СН3).
МС-ЖХ: МН+ = 366,15; время удерживания = 9,61 мин.
Пример 31: трет-бутил-3-[(2-метил-4,7-диоксо-4,7-дигидро-1,3-бензотиазол-5-ил)амино]пропилкарбамат
МС-ЖХ: МН+ = 352,22; время удерживания = 9,09 мин.
Пример 32: 2-метил-5-{[3-(метиламино)пропил]амино}-1,3-бензотиазол-4,7-дион
25 мг (68,5 мкмоль) соединения примера 30 суспендируют в 10 мл диэтилового эфира. Добавляют 4 мл 1М раствора соляной кислоты в диэтиловом эфире, затем реакционную смесь перемешивают при комнатной температуре в течение 2 ч. Полученный осадок собирают фильтрованием и последующим промыванием диэтиловым эфиром с последующим высушиванием при пониженном давлении с получением коричневато-красного твердого вещества.
ЯМР 1Н (ДМСО d6, 400 мГц, δ): 8,61 (м, 2Н, NH2), 7,87-7,81 (м, 1Н, NH), 5,55 (с, 1Н, СН), 3,29-3,24 (м, 2Н, СН2), 2,91-2,88 (м, 2Н, СН2), 2,75 (с, 3Н, СН3), 2,53-2,52 (м, 3Н, СН3), 1,89-1,86 (м, 2Н, СН2).
МС-ЖХ: МН+ = 266,06; время удерживания = 7,04 мин.
Пример 33: 5-[(3-аминопропил)амино]-2-метил-1,3-бензотиазол-4,7-дион
20 мг (57 мкмоль) соединения примера 30 суспендируют в 10 мл диэтилового эфира. Добавляют 840 мкл 1М раствора соляной кислоты в диэтиловом эфире, затем реакционную смесь перемешивают при комнатной температуре в течение 2 ч. Полученный осадок собирают фильтрованием с последующим промыванием диэтиловым эфиром, затем высушивают при пониженном давлении с получением коричневато-красного твердого вещества.
ЯМР 1Н (ДМСО d6, 400 мГц, δ): 7,84-7,78 (м, 3Н, NH, NH2), 5,56 (с, 1Н, СН), 3,28-3,23 (м, 2Н, СН2), 2,86-2,81 (м, 2Н, СН2), 2,75 (с, 3Н, СН3), 1,85-1,82 (м, 2Н, СН3).
МС-ЖХ: МН+ = 280,15; время удерживания = 7,01 мин.
Пример 34: 6-хлор-5-{[2-(диметиламино)этил]амино}-2-метил- 1,3-бензотиазол-4,7-дион
58,6 мг (0,22 ммоль) промежуточного соединения 2.1 растворяют в 5 мл уксусной кислоты. Добавляют 32,5 мг (0,24 ммоль; 1,1 экв) N-хлорсукцинимида и реакционную смесь перемешивают в течение 3 ч при комнатной температуре. После концентрирования остаток очищают хроматографией на колонке с силикагелем (элюент: дихлорметан/метанол, 90/10) и получают предполагаемый продукт после перевода в этиловый эфир в виде фиолетового порошка.
ЯМР 1Н (ДМСО d6, 400 мГц, δ): 7,31 (м, 1Н, NH), 3,79-3,74 (м, 2Н, СН), 2,75 (с, 3Н, СН3), 2,47-2,44 (м, 2Н, СН2), 2,13 (с, 6Н, 2 СН3).
МС-ЖХ: МН+ = 300,09; время удерживания = 7,17 мин.
Пример 35: 6-бром-5-{[2-(диметиламино)этил]амино}-2-метил-1,3-бензотиазол-4,7-дион
102 мг (0,38 ммоль) промежуточного соединения 2.1 растворяют в 10 мл уксусной кислоты. Добавляют 77,3 мг (0,43 ммоль; 1,1 экв) N-бромсукцинимида и реакционную смесь перемешивают в течение 3 ч при комнатной температуре. После концентрирования при пониженном давлении остаток очищают хроматографией на силикагеле (элюент: дихлорметан/метанол, 90/10) и получают предполагаемый продукт после перевода в этиловый эфир в виде фиолетового порошка.
ЯМР 1Н (ДМСО d6, 400 мГц, δ): 7,24 (м, 1Н, NH), 3,78-3,74 (м, 2Н, СН2), 2,75 (с, 3Н, СН3), 2,45-2,42 (м, 2Н, СН2), 2,11 (с, 6Н, 2 СН3).
МС-ЖХ: МН+ = 343,97; время удерживания = 7,22 мин.
Пример 36: 6-(бутилтио)-5-{[2-(диметиламино)этил]амино}-2-метил-1,3-бензотиазол-4,7-дион
20 мкл (0,115 ммоль; 1,2 экв) диизопропилэтиламина и 16 мкл (0,154 ммоль; 1,6 экв) бутантиола добавляют к раствору 33 мг (96 мкмоль) соединения примера 35 в 4 мл безводного этанола. Реакционную смесь перемешивают в течение 24 ч при 60°С, затем после концентрации при пониженном давлении остаток очищают хроматографией на колонке с силикагелем (элюент: дихлорметан/метанол, 95/5) и получают предполагаемый продукт после перевода в этиловый эфир в виде фиолетового порошка.
ЯМР 1Н (ДМСО d6, 400 мГц, δ): 7,56 (м, 1Н, NH), 3,84-3,83 (м, 2Н, СН2), 2,75 (с, 3Н, СН3), 2,64-2,60 (т, 2Н, СН2), 2,45-2,42 (м, 2Н, СН2), 2,20 (с, 6Н, 2 СН3), 1,44-1,46 (м, 2Н, СН2), 1,37-1,33 (м, 2Н, СН2), 0,85-0,82 (т, 3Н, СН3).
Пример 37: 5-{[2-(диметиламино)этил]амино}-2-(морфолин-4-илметил)-1,3-бензотиазол-4,7-дион
37.1) 2-(Бромметил)-5-метокси-1,3-бензотиазол
2,58 г (14,5 ммоль; 1,3 экв) N-бромсукцинимида и аза-бис-изобутиронитрил на кончике шпателя добавляют к раствору 2 г (11,16 ммоль) 2-метил-5-метокси-1,3-бензотиазола в 25 мл безводного четыреххлористого углерода. Реакционную смесь нагревают при кипячении с обратным холодильником и при облучении в течение 6 ч добавляют аза-бис-изобутиронитрила на кончике шпателя каждые 2 ч. После охлаждения до комнатной температуры отфильтровывают нерастворимую фракцию, растворитель выпаривают при пониженном давлении и остаток очищают хроматографией на колонке с силикагелем (элюент: этилацетат/гептан, 1/4). Предполагаемый продукт получают в виде белого твердого вещества.
ЯМР 1Н (ДМСО d6, 400 мГц, δ): 7,98-7,96 (м, 1Н, H аром.), 5,54-7,53 (м, 1Н, Н аром.), 7,13-7,10 (м, 1Н, Н аром.), 5,09 (с, 2Н, СН2), 3,84 (с, 3Н, СН3).
МС-ЖХ: МН+ = 258,38; время удерживания = 10,36 мин.
37.2) 5-Метокси-2-(морфолин-4-илметил)-1,3-бензотиазол
678 мкл диизопропилэтиламина (3,9 ммоль; 2 экв) добавляют к раствору 0,5 г промежуточного соединения 37.1 в 20 мл безводного толуола. 187 мкл (2,14 ммоль; 1,1 экв) морфолина и йодид натрия на кончике шпателя добавляют к предыдущему раствору, затем реакционную смесь перемешивают при 80°С в течение 3 ч. После охлаждения реакционную смесь промывают водой (3 раза по 20 мл), затем органическую фазу высушивают над сульфатом магния и концентрируют. Очистка хроматографией на колонке с силикагелем (элюент: этилацетат/гептан, 1/1) дает предполагаемый продукт в виде бежевого твердого вещества.
ЯМР 1Н (ДМСО d6, 400 мГц, δ): 7,91-7,89 (м, 1Н, H аром.), 5,47-7,46 (с, 1Н, Н аром.), 7,05-7,02 (м, 1Н, Н аром.), 3,92 (с, 2Н, СН2), 3,82 (с, 3Н, СН3), 3,63-3,61 (м, 4Н, 2СН2), 2,56-2,53 (м, 4Н, 2СН2).
МС-ЖХ: МН+ = 265,10; время удерживания = 7,55 мин.
37.3) 5-Метокси-2-(морфолин-4-илметил)-4-нитро-1,3-бензотиазол
84 мг (0,83 ммоль; 1,2 экв) нитрата калия добавляют порциями к раствору 0,2 г (0,76 ммоль) промежуточного соединения 37.2 в 0,7 мл концентрированной серной кислоты при 0°С. После охлаждения до комнатной температуры реакционную смесь перемешивают в течение 18 ч, нейтрализуют добавлением 10М водного раствора соды с последующей экстракцией 3 раза по 50 мл дихлорметана. Полученную органическую фазу высушивают над сульфатом магния с последующим концентрированием, затем очищают хроматографией на колонке с силикагелем (элюент: этилацетат/гептан, 1/1). Предполагаемый продукт получают в виде желтого масла.
ЯМР 1Н (ДМСО d6, 400 мГц, δ): 8,26-8,24 (м, 1Н, H аром.), 7,48-7,46 (с, 1Н, Н аром.), 3,98-3,96 (2с, 5Н, СН3, СН2), 3,63-3,61 (м, 4Н, 2СН2), 2,59-2,56 (м, 4Н, 2СН2).
МС-ЖХ: МН+ = 310,11; время удерживания = 8,03 мин.
37.4) 5-Метокси-2-(морфолин-4-илметил)-1,3-бензотиазол-4-амин
0,93 г (4,11 ммоль; 5 экв) хлорида олова добавляют к раствору 0,254 г (0,822 ммоль) промежуточного соединения 37.3 в 7 мл концентрированной соляной кислоты. Реакционную смесь перемешивают в течение 3 ч при 70°С. После охлаждения до комнатной температуры реакционную смесь разбавляют добавлением 20 мл этилацетата с последующей нейтрализацией насыщенным раствором NaHCO3 и конечным промыванием водой 3 раза по 20 мл. Органические фазы объединяют с последующим высушиванием над сульфатом магния и концентрированием с получением предполагаемого продукта в виде бежевого порошка.
ЯМР 1Н (ДМСО d6, 400 мГц, δ): 7,12-7,10 (м, 1Н, H аром.), 7,02-7,00 (м, 1Н, Н аром.), 5,04 (с, 2Н, NH2), 3,88 (с, 2Н, СН2), 3,81 (с, 3Н, СН3), 3,63-3,60 (м, 4Н, 2 СН2), 2,55-2,52 (м, 4Н, 2СН2).
МС-ЖХ: МН+ = 280,11; время удерживания = 7,29 мин.
37.5) 5-Метокси-2-(морфолин-4-илметил)-1,3-бензотиазол-4,7-дион
Раствор 84 мг (0,31 ммоль; 1,8 экв) соли Фреми, растворенной в 14 мл буферного раствора (0,3М) вторичного кислого фосфата натрия, добавляют к раствору 0,0483 мг (0,17 ммоль) промежуточного соединения 37.4 в 10 мл ацетона. Реакционную смесь перемешивают в течение 18 ч при комнатной температуре с последующей экстракцией дихлорметаном 3 раза по 30 мл, затем органические фазы промывают водой дважды по 20 мл. Затем органические фазы объединяют с последующим высушиванием над сульфатом магния и концентрированием при пониженном давлении. Остаток очищают хроматографией на колонке с силикагелем (элюент: этилацетат/гептан, 1/1) и предполагаемый продукт получают в виде желтого масла.
МС-ЖХ: МН+ = 295,06; время удерживания = 7,11 мин.
37.6) 5-{[2-(Диметиламино)этил]амино}-2-(морфолин-4-илметил)-1,3-бензотиазол-4,7-дион
Применяемая методика аналогична описанной в примере 1 с использованием промежуточного соединения 37.5 вместо 5-метокси-2-метил-4,7-диоксобензотиазола.
МС-ЖХ: МН+ = 351,38; время удерживания = 3,07 мин.
Пример 38: 5-{[2-(Диметиламино)этил]амино}-2-[(4-фенилпиперазин-1-ил)метил]-1,3-бензотиазол-4,7-дион
Применяемая методика аналогична описанной в примере 37 с использованием N-фенилпиперазина вместо морфолина на второй стадии.
МС-ЖХ: МН+ = 426,18; время удерживания = 7,39 мин.
Пример 39: 5-{[2-(диметиламино)этил]амино}-2-(пиперидин-1-илметил)-1,3-бензотиазол-4,7-дион
Применяемая методика аналогична описанной в примере 37 с использованием пиперидина вместо морфолина на второй стадии.
МС-ЖХ: МН+ = 349,13; время удерживания = 2,82 мин.
Соединения примеров 40-52 получают способом, аналогичным описанному в примере 15, с использованием первичных или вторичных аминов вместо анилина на четвертой и последней стадии.
Пример 40: 5-{[2-(диметиламино)этил]амино}-2-этил-1,3-бензоксазол-4,7-дион или 6-{[2-(диметиламино)этил]амино}-2-этил-1,3-бензоксазол-4,7-дион
Точка плавления 123°С.
ЯМР 1Н (ДМСО d6, 400 мГц, δ): 7,39 (т, 1Н, NH), 5,30 (с, 1Н, СН), 3,30-3,31 (м, 2Н, СН2), 3,24-3,20 (м, 2Н, СН2), 2,95-2,88 (кв, 2Н, СН2), 2,17 (с, 6Н, 2 СН3), 1,30 (т, 3Н, СН3).
МС-ЖХ: МН+ = 264,13; время удерживания = 7,02 мин.
Пример 41: трет-бутил-2-{[2-этил-4,7-диоксо-4,7-дигидро-1,3-бензоксазол-5-ил)(метил)амино]этилкарбамат или трет-бутил-2-{[2-этил-4,7-диоксо-4,7-дигидро-1,3-бензоксазол-6-ил)(метил)амино]этилкарбамат
Точка плавления 135°С.
ЯМР 1Н (ДМСО d6, 400 мГц, δ): 7,82 (т, 1Н, NH), 5,36 (с, 1Н, СН), 3,38-3,36 (м, 2Н, СН2), 3,30-3,27 (м, 2Н, СН2), 2,93-2,88 (кв, 2Н, СН2), 2,79 (с, 3Н, СН3), 1,37-1,26 (м, 12Н, 4 СН3).
МС-ЖХ: МН+ = 350,14; время удерживания = 9,72 мин.
Пример 42: трет-бутил 2-{[2-этил-4,7-диоксо-4,7-дигидро-1,3-бензоксазол-5-ил)амино]этилкарбамат или трет-бутил 2-{[2-этил-4,7-диоксо-4,7-дигидро-1,3-бензоксазол-6-ил)амино]этилкарбамат
Точка плавления 173°С.
ЯМР 1Н (ДМСО d6, 400 мГц, δ): 7,73 (т, 1Н, NH), 6,97 (т, 1Н, NH), 5,36 (с, 1Н, СН), 3,20-3,17 (м, 2Н, СН2), 3,15-3,12 (м, 2Н, СН2), 2,93-2,88 (кв, 2Н, СН2), 1,36 (с, 9Н, 3СН3), 1,28 (т, 3Н, СН3).
МС-ЖХ: МН+ = 336,23; время удерживания = 9,24 мин.
Пример 43: 5-{[3-(диметиламино)пропил]амино}-2-этил-1,3-бензоксазол-4,7-дион или 6-{[3-(диметиламино)пропил]амино}-2-этил-1,3-бензоксазол-4,7-дион
Точка плавления 101°С.
ЯМР 1Н (ДМСО d6, 400 мГц, δ): 8,09 (м, 1Н, NH), 5,28 (с, 1Н, СН), 3,21-3,16 (м, 2Н, СН2), 2,93-2,88 (кв, 2Н, СН2), 2,28-2,25 (м, 2Н, СН2), 2,13 (с, 6Н, 2 СН3), 1,71-1,67 (м, 2Н, СН2), 1,28 (т, 3Н, СН3).
МС-ЖХ: МН+ = 278,19; время удерживания = 7,09 мин.
Пример 44: 2-этил-5-{[2-(1-метилпирролидин-2-ил)этил]амино}-1,3-бензоксазол-4,7-дион или 2-этил-6-{[2-(1-метилпирролидин-2-ил)этил]амино}-1,3-бензоксазол-4,7-дион
Точка плавления 121°С.
ЯМР 1Н (ДМСО d6, 400 мГц, δ): 8,11 (т, 1Н, NH), 5,24 (с, 1Н, СН), 3,19-3,17 (м, 2Н, СН2), 2,95-2,93 (м, 1Н, СН), 2,92-2,87 (кв, 2Н, СН2), 2,21 (с, 3Н, СН3), 2,16-2,05 (м, 2Н, СН2), 1,88-1,84 (м, 2Н, СН2), 1,63-1,57 (м, 4Н, 2 СН2), 1,28 (т, 3Н, СН3).
МС-ЖХ: МН+ = 304,20; время удерживания = 7,20 мин.
Пример 45: 5-{[4-(диметиламино)бутил]амино}-2-этил-1,3-бензоксазол-4,7-дион или 6-{[4-(диметиламино)бутил]амино}-2-этил-1,3-бензоксазол-4,7-дион
ЯМР 1Н (ДМСО d6, 400 мГц, δ): 8,06 (т, 1Н, NH), 5,28 (с, 1Н, СН), 3,17-3,12 (м, 2Н, СН2), 2,93-2,88 (кв, 2Н, СН2), 2,22-2,19 (м, 2Н, СН2), 2,11 (с, 6Н, 2СН3), 1,61-1,56 (м, 2Н, СН2), 1,46-1,42 (м, 2Н, СН2), 1,28 (т, 3Н, СН3).
МС-ЖХ: МН+ = 292,20; время удерживания = 7,10 мин.
Пример 46: 2-этил-5-[(4-пирролидин-1-илбутил)амино]-1,3-бензоксазол-4,7-дион или 2-этил-6-[(4-пирролидин-1-илбутил)амино]-1,3-бензоксазол-4,7-дион
Точка плавления 102°С.
ЯМР 1Н (ДМСО d6, 400 мГц, δ): 7,95 (т, 1Н, NH), 5,28 (с, 1Н, СН), 3,17-3,13 (м, 2Н, СН2), 2,93-2,87 (кв, 2Н, СН2), 2,41-2,37 (м, 6Н, 3СН2), 1,63-1,58 (м, 2Н, СН2), 1,49-1,45 (м, 2Н, СН2), 1,28 (т, 3Н, СН3).
МС-ЖХ: МН+ = 318,20; время удерживания = 7,30 мин.
Пример 47: 5-{[5-(диметиламино)пентил]амино}-2-этил-1,3-бензоксазол-4,7-дион или 6-{[5-(диметиламино)пентил]амино}-2-этил-1,3-бензоксазол-4,7-дион
ЯМР 1Н (ДМСО d6, 400 мГц, δ): 7,83 (т, 1Н, NH), 5,27 (с, 1Н, СН), 3,17-3,13 (м, 2Н, СН2), 2,93-2,87 (кв, 2Н, СН2), 2,18-2,14 (м, 2Н, СН2), 2,09 (с, 6Н, 2СН3), 1,58-1,54 (м, 2Н, СН2), 1,41-1,38 (м, 2Н, СН2), 1,28 (т, 3Н, СН3).
МС-ЖХ: МН+ = 306,20; время удерживания = 7,30 мин.
Пример 48: смесь 5-{[6-(диметиламино)гексил]амино}-2-этил-1,3-бензоксазол-4,7-диона и 6-{[6-(диметиламино)гексил]амино}-2-этил-1,3-бензоксазол-4,7-диона
МС-ЖХ: МН+ = 320,20; время удерживания = 7,50 мин.
Пример 49: смесь 2-этил-5-(4-метилпиперазин-1-ил)-1,3-бензоксазол-4,7-диона и 2-этил-6-(4-метилпиперазин-1-ил)-1,3-бензоксазол-4,7-диона
МС-ЖХ: МН+ = 276,10; время удерживания = 7,10 мин.
Пример 50: смесь 2-этил-5-[(1-этилгексил)амино]-1,3-бензоксазол-4,7-диона и 2-этил-6-[(1-этилгексил)амино]-1,3-бензоксазол-4,7-диона
МС-ЖХ: МН+ = 305,20; время удерживания = 11,50 мин.
Пример 51: смесь 5-азокан-1-ил-2-этил-1,3-бензоксазол-4,7-диона и 6-азокан-1-ил-2-этил-1,3-бензоксазол-4,7-диона
МС-ЖХ: МН+ = 289,20; время удерживания = 10,40 мин.
Пример 52: смесь 2-этил-5-морфолин-4-ил-1,3-бензоксазол-4,7-диона и 2-этил-6-морфолин-4-ил-1,3-бензоксазол-4,7-диона
МС-ЖХ: МН+ = 263,10; время удерживания = 8,60 мин.
Пример 53: 6-хлор-5-{[2-(диметиламино)этил]амино}-2-этил-1,3-бензоксазол-4,7-дион или 5-хлор-6-{[2-(диметиламино)этил]амино}-2-этил-1,3-бензоксазол-4,7-диона
Применяемая методика аналогична описанной в примере 34 с использованием соединения примера 40 вместо промежуточного соединения 2.1. Точка плавления 110°С.
ЯМР 1Н (ДМСО d6, 400 мГц, δ): 7,35 (т, 1Н, NH), 3,78-3,74 (м, 2Н, СН2), 2,94-2,89 (кв, 2Н, СН2), 2,48-2,45 (м, 2Н, СН2), 2,15 (с, 6Н, 2СН3), 1,28 (т, 3Н, СН3).
МС-ЖХ: МН+ = 298,10; время удерживания = 7,20 мин.
Пример 54: 6-бром-5-{[2-(диметиламино)этил]амино}-2-этил-1,3-бензоксазол-4,7-дион или 5-бром-6-{[2-(диметиламино)этил]амино}-2-этил-1,3-бензоксазол-4,7-дион
Применяемая методика аналогична описанной в примере 35 с использованием соединения 40 вместо промежуточного соединения 2.1.
ЯМР 1Н (ДМСО d6, 400 мГц, δ): 7,27 (т, 1Н, NH), 3,78-3,74 (м, 2Н, СН2), 2,94-2,89 (кв, 2Н, СН2), 2,46-2,43 (м, 2Н, СН2), 2,13 (с, 6Н, 2СН3), 1,26 (т, 3Н, СН3).
МС-ЖХ: МН+ = 342,00; время удерживания = 7,30 мин.
Пример 55: 5-{[2-(диметиламино)этил]амино}-2-этил-6-метил-1,3-бензоксазол-4,7-дион
55.1) 2-Диазо-5-метилциклогексан-1,3-дион
12,25 мл (87,2 ммоль; 2,2 экв) триэтиламина и 8,57 г (35,67 ммоль; 0,9 экв) 4-ацетамидобензолсульфонилазида добавляют к раствору 5 г (39,6 ммоль) 5-метилциклогексан-1,3-диона в 100 мл дихлорметана. Реакционную смесь перемешивают в течение 75 мин при комнатной температуре, затем охлаждают до 0°С и фильтруют через слой силикагеля. После концентрирования при пониженном давлении раствор промывают водой 3 раза по 50 мл. Органические фазы объединяют, высушивают над сульфатом натрия и концентрируют. Полученное твердое вещество переводят в этиловый эфир с последующим фильтрованием и высушиванием при пониженном давлении. Его используют на последующей стадии без дополнительной очистки.
МС-ЖХ: МН+ = 153,49; время удерживания = 7,21 мин.
55.2) 2-Этил-6-метил-6,7-дигидро-1,3-бензоксазол-4(5Н)-он
285 мг (0,644 ммоль; 0,02 экв) ацетата родия добавляют к раствору 4,9 г (32,2 ммоль) промежуточного соединения 55.1 в 50 мл пропионитрила. Реакционную смесь перемешивают в инертной атмосфере аргона при 60°С в течение 2 ч. Затем растворитель выпаривают и остаток очищают хроматографией на колонке с силикагелем (элюент: этилацетат/гептан, 1/1). Предполагаемый продукт получают в виде желтого масла.
ЯМР 1Н (ДМСО d6, 400 мГц, δ): 3,02-2,97 (м, 1Н, CH), 2,80-2,74 (кв, 2Н, СН2), 2,68-2,61 (м, 1Н, СН2), 2,44-2,39 (м, 2Н, СН2), 2,34-2,30 (м, 1Н, СН2), 1,23 (т, 3Н, СН3), 1,08 (с, 3Н, СН3).
МС-ЖХ: МН+ = 180,25; время удерживания = 8,55 мин.
55.3) (4Е)-2-Этил-6-метил-6,7-дигидро-1,3-бензоксазол-4(5Н)-он оксим
647 мг (9,31 ммоль; 1,2 экв) гидроксиламина гидрохлорида и 764 мг (9,31 ммоль; 1,2 экв) ацетата аммония добавляют к раствору 1,39 (7,76 ммоль) промежуточного соединения 55.2 в 200 мл метанола. Реакционную смесь перемешивают в течение 90 мин при кипячении метанола с обратным холодильником, затем растворитель выпаривают, остаток переводят в 50 мл воды, затем нейтрализуют с использованием насыщенного раствора NaHCO3. Предполагаемый продукт получают экстракцией этилацетатом дважды по 50 мл, затем дважды промывают 30 мл воды. Органические фазы объединяют, высушивают над сульфатом натрия и концентрируют при пониженном давлении. Желаемый продукт получают в виде темно-желтого твердого вещества, которое используют на последующей стадии без дополнительной очистки.
МС-ЖХ: МН+ = 195,09; время удерживания = 8,73 мин.
55.4) 2-Этил-6-метил-1,3-бензоксазол-4-амин
1,45 г (7,46 ммоль) промежуточного соединения 55.3 растворяют в 25 г полифосфорной кислоты. После перемешивания в течение 1 ч при 140°С раствор гидролизуют добавлением воды со льдом, затем нейтрализуют 50% водным раствором соды. Полученный продукт экстрагируют дихлорметаном и органическую фазу промывают водой 3 раза по 25 мл, высушивают над сульфатом натрия и концентрируют при пониженном давлении. Желаемый продукт получают после очистки хроматографией на колонке с силикагелем (элюент: дихлорметан/этанол, 98/2).
МС-ЖХ: МН+ = 177,21; время удерживания = 9,12 мин.
55.5) 2-Этил-6-метил-1,3-бензоксазол-4,7-дион
Применяемая методика аналогична описанной для стадии 15.3 примера 15 с использованием промежуточного соединения 55.4 вместо промежуточного соединения 15.2.
ЯМР 1Н (ДМСО d6, 400 мГц, δ): 6,72 (с, 1Н, CH), 2,98-2,93 (кв, 2Н, СН2), 2,04 (с, 3Н, СН3), 1,30 (т, 3Н, СН3).
МС-ЖХ: МН+ = 192,06; время удерживания = 8,93 мин.
55.6) 5-{[2-(Диметиламино)этил]амино}-2-этил-6-метил-1,3-бензоксазол-4,7-дион
Применяемая методика аналогична описанной для стадии 15.4 примера 15 с использованием промежуточного соединения 55.5 вместо промежуточного соединения 15.3 и N-диметилэтилендиамина вместо анилина. Точка плавления 135°С.
ЯМР 1Н (ДМСО d6, 400 мГц, δ): 6,63 (т, 1Н, NH), 3,62-3,58 (м, 2Н, СН2), 2,92-2,86 (кв, 2Н, СН2), 2,44-2,41 (м, 2Н, СН2), 2,14 (с, 6Н, 2СН3), 1,97 (с, 3Н, СН3), 1,27 (т, 3Н, СН3).
МС-ЖХ: МН+ = 278,12; время удерживания = 7,27 мин.
Пример 56: 2-циклопропил-5-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-дион или 2-циклопропил-6-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-дион
Применяемая методика аналогична описанной в примере 55 с использованием циклогексан-1,3-диона вместо 5-метилциклогексан-1,3-диона на первой стадии и циклопропанкарбонитрила вместо пропионитрила на второй стадии. Точка плавления 155°С.
ЯМР 1Н (ДМСО d6, 400 мГц, δ): 7,35 (т, 1Н, NH), 5,27 (с, 1Н, СН), 3,30-3,18 (м, 2Н, СН2), 2,49-2,46 (м, 2Н, СН2), 2,28-2,25 (м, 1Н, СН), 2,17 (с, 6Н, 2СН3), 1,18-1,07 (м, 4Н, 2 СН2).
МС-ЖХ: МН+ = 276,10; время удерживания = 7,10 мин.
Пример 57: смесь 5-{[2-(диметиламино)этил]амино}-2-фенил -1,3-бензоксазол-4,7-диона и 6-{[2-(диметиламино)этил]амино}-2-фенил-1,3-бензоксазол-4,7-диона
Применяемая методика аналогична описанной в примере 15 с использованием триметилортобензоата вместо триэтилортопропионата на первой стадии и N,N-диметилэтилендиамина вместо аналина на четвертой и последней стадии. Точка плавления 147°С.
ЯМР 1Н (ДМСО d6, 400 мГц, δ): 8,15-8,08 (м, 2Н, H аром.), 7,70-7,61 (м, 3Н, Н аром.), 7,33 (т, 1Н, NH), 5,38 (с, 1Н, СН), 3,26-3,21 (м, 4Н, 2 СН2), 2,19 (с, 6Н, 2СН3).
Два компонента смеси можно охарактеризовать сдвигами в спектре ЯМР (400 мГц) единичного протона кольца бензоксазоледиона, которые составляют 5,38 и 5,39 м.д.
МС-ЖХ: МН+ = 312,20; время удерживания = 7,70 мин.
Пример 58: смесь 5-{[6-(диметиламино)гексил]амино}-2-фенил-1,3-бензоксазол-4,7-диона и 6-{[6-(диметиламино)гексил]амино}-2-фенил-1,3-бензоксазол-4,7-диона
Применяемая методика аналогична описанной в примере 15 с использованием триметилортобензоата вместо триэтилортопропионата на первой стадии и 6-(диметиламино)гексиламина вместо анилина на четвертой и последней стадии.
Два компонента смеси можно охарактеризовать сдвигами в спектре ЯМР (400 мГц) единичного протона кольца бензоксазоледиона, которые составляют 5,34 и 5,35 м.д.
МС-ЖХ: МН+ = 368,20; время удерживания = 8,10 мин.
Пример 59: 5-[(1-этилгексил)амино]-2-фенил-1,3-бензоксазол-4,7-дион или 6-[(1-этилгексил)амино]-2-фенил-1,3-бензоксазол-4,7-дион
Применяемая методика аналогична описанной в примере 15 с использованием триметилортобензоата вместо триэтилортопропионата на первой стадии и 2-этилгексиламина вместо анилина на четвертой и последней стадии.
МС-ЖХ: МН+ = 353,20; время удерживания = 12,50 мин.
Пример 60: смесь 2-(2,6-дифторфенил)-5-[(2-пирролидин-1-илэтил)амино]-1,3-бензоксазол-4,7-диона и 2-(2,6-дифторфенил)-6-[(2-пирролидин-1-илэтил)амино]-1,3-бензоксазол-4,7-диона
60.1) 2-(2,6-Дифторфенил)-4-нитро-1,3-бензоксазол
2 г (32,4 ммоль; 1 экв) борной кислоты добавляют к раствору 5 г (32,4 ммоль) 2-амино-3-нитрофенола и 5,12 г (32,4 ммоль; 1 экв) 2,6-дифторбензойной кислоты в 50 мл ксилола. Смесь кипятят с обратным холодильником в ксилоле в течение 8 ч с удалением образовавшейся воды аппаратом Дин-Старка. После охлаждения до комнатной температуры реакционную среду разбавляют 100 мл этилацетата и нейтрализуют 10% водным раствором соды. Органическую фазу промывают водой 3 раза по 50 мл, затем насыщенным раствором NaCl перед высушиванием над сульфатом натрия, фильтруют и концентрируют при пониженном давлении. 2-(2,6-Дифторфенил)-4-нитро-1,3-бензоксазол используют на последующей стадии без дополнительной очистки.
МС-ЖХ: МН+ = 277,00; время удерживания = 10,45 мин.
60.2) 2-(2,6-Дифторфенил)-1,3-бензоксазол-4-амин
14,3 г (63,5 ммоль; 5 экв) хлорида олова добавляют к раствору 3,5 г (12,7 ммоль) 2-(2,6-дифторфенил)-4-нитро-1,3-бензоксазола в 60 мл концентрированной соляной кислоты. Смесь перемешивают в течение 2 ч при 60°С, затем после охлаждения до комнатной температуры и добавления 100 мл воды ее нейтрализуют 50% водным раствором соды. Образовавшийся осадок отфильтровывают через слой целита и промывают этанолом. Полученный раствор концентрируют при пониженном давлении, затем желаемый продукт экстрагируют этилацетатом 3 раза по 50 мл. Органические фазы объединяют, дважды промывают насыщенным раствором хлорида натрия по 30 мл, высушивают над сульфатом натрия и концентрируют при пониженном давлении. 2-(2,6-Дифторфенил)-1,3-бензоксазол-4-амин используют на последующей стадии без дополнительной очистки.
МС-ЖХ: МН+ = 247,08; время удерживания = 10,02 мин.
60.3) 2-(2,6-Дифторфенил)-1,3-бензоксазол-4,7-дион
Применяемая методика аналогична описанной для стадии 15.3 примера 15 с использованием промежуточного соединения 60.2 вместо промежуточного соединения 15.2. Предполагаемый продукт получают в виде желтых кристаллов.
МС-ЖХ: МН+ = 261,93; время удерживания = 9,62 мин.
60.4) Смесь 2-(2,6-дифторфенил)-5-[(2-пирролидин-1-илэтил)амино]-1,3-бензоксазол-4,7-диона и 2-(2,6-дифторфенил)-6-[(2-пирролидин-1-илэтил)амино]-1,3-бензоксазол-4,7-диона
Применяемая методика аналогична описанной для стадии 15.4 примера 15 с использованием промежуточного соединения 60.3 вместо промежуточного соединения 15.3 и (2-аминоэтил)пирролидина вместо анилина. Точка плавления 150°С.
ЯМР 1Н (ДМСО d6, 400 мГц, δ): 7,78-7,76 (м, 1Н, H аром.), 7,43-7,37 (м, 2Н, Н аром.), 5,41 (с, 1Н, СН), 3,38-3,36 (м, 2Н, СН2), 3,28-3,26 (м, 4Н, 2 СН2), 2,68-2,64 (м, 2Н, СН2), 1,70-1,67 (м, 4Н, 2 СН2).
Два компонента смеси можно охарактеризовать сдвигами в спектре ЯМР (400 мГц) единичного протона кольца бензоксазоледиона, которые составляют 5,40 и 5,42 м.д.
МС-ЖХ: МН+ = 373,99; время удерживания = 7,76 мин.
Соединения примеров 61-65 получают способом, аналогичным описанному в примере 60.
Пример 61: смесь 2-[4-(диэтиламино)фенил]-5-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-диона и 2-[4-(диэтиламино)фенил]-6-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-диона
ЯМР 1Н (ДМСО d6, 400 мГц, δ): 7,91-7,89 (д, 2Н, H аром.), 6,83-6,81 (д, 2Н, Н аром.), 5,29 (с, 1Н, СН), 3,47-3,42 (м, 4Н, 2 СН2), 3,41-3,38 (м, 2Н, СН2), 3,25-3,21 (м, 2Н, СН2), 2,19 (с, 6Н, 2 СН3), 1,12 (т, 6Н, 2 СН3).
Два компонента смеси можно охарактеризовать сдвигами в спектре ЯМР (400 мГц) единичного протона кольца бензоксазоледиона, которые составляют 5,29 и 5,30 м.д.
МС-ЖХ: МН+ = 383,20; время удерживания = 8,30 мин.
Пример 62: смесь 2-[4-(диэтиламино)фенил]-5-[(2-пирролидин-1-илэтил)амино]-1,3-бензоксазол-4,7-диона и 2-[4-(диэтиламино)фенил]-6-[(2-пирролидин-1-илэтил)амино]-1,3-бензоксазол-4,7-диона
ЯМР 1Н (ДМСО d6, 400 мГц, δ): 7,91-7,88 (д, 2Н, H аром.), 6,83-6,81 (д, 2Н, Н аром.), 5,29 (с, 1Н, СН), 3,47-3,42 (м, 4Н, 2 СН2), 3,37-3,35 (м, 2Н, СН2), 3,26-3,23 (м, 4Н, 2СН2), 2,66 (т, 2Н, СН2), 1,70-1,68 (м, 4Н, 2СН2), 1,14 (т, 6Н, 2СН3).
Два компонента смеси можно охарактеризовать сдвигами в спектре ЯМР (400 мГц) единичного протона кольца бензоксазоледиона, которые составляют 5,28 и 5,29 м.д.
МС-ЖХ: МН+ = 409,10; время удерживания = 8,40 мин.
Пример 63: смесь 2-(4-хлорфенил)-5-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-диона и 2-(4-хлорфенил)-6-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-диона
Точка плавления 169°С.
Два компонента смеси можно охарактеризовать сдвигами в спектре ЯМР (400 мГц) единичного протона кольца бензоксазоледиона, которые составляют 5,39 и 5,41 м.д.
МС-ЖХ: МН+ = 346,20; время удерживания = 8,10 мин.
Пример 64: смесь 2-(4-хлорфенил)-5-{[3-(диметиламино)пропил]амино}-1,3-бензоксазол-4,7-диона и 2-(4-хлорфенил]-6-{[3-(диметиламино)пропил]амино}-1,3-бензоксазол-4,7-диона
МС-ЖХ: МН+ = 360,10; время удерживания = 8,10 мин.
Пример 65: смесь 2-(4-хлорфенил)-5-{[4-(диметиламино)бутил]амино}-1,3-бензоксазол-4,7-диона и 2-(4-хлорфенил)-6-{[4-(диметиламино)бутил]амино}-1,3-бензоксазол-4,7-диона
ЯМР 1Н (ДМСО d6, 400 мГц, δ): 8,13-8,09 (м, 2Н, H аром.), 7,70-7,67 (м, 2Н, Н аром.), 5,36 (с, 1Н, СН), 3,18-3,15 (м, 2Н, СН2), 2,25-2,21 (м, 2Н, СН2), 2,13 (с, 6Н, 2СН3), 1,62-1,58 (м, 2Н, СН2), 1,48-1,44 (м, 2Н, СН2).
Два компонента смеси можно охарактеризовать сдвигами в спектре ЯМР (400 мГц) единичного протона кольца бензоксазоледиона, которые составляют 5,35 и 5,37 м.д.
МС-ЖХ: МН+ = 374,10; время удерживания = 8,20 мин.
Пример 66: смесь 2-(2-фторфенил)-5-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-диона и 2-(2-фторфенил)-6-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-диона
66.1) 2-Диазоциклогексан-1,3-дион
Смесь 4-ацетамидобензолсульфонилазида (25 г; 104 ммоль) и триэтиламина (36 мл; 250 ммоль) в дихлорметане при температуре ниже 30°С с помощью внешнего охлаждения обрабатывают по каплям раствором циклогексан-1,3-диона (13 г; 115 ммоль) в 200 мл дихлорметана. Реакционную смесь перемешивают в течение 75 мин при комнатной температуре, затем фильтруют через целит. После концентрирования до объема примерно 300 мл фильтрат промывают водой, затем высушивают над сульфатом натрия. Коричнево-желтое твердое вещество (14 г; 88%), полученное при выпаривании растворителя при пониженном давлении, является аналогичным полученному в примере 55.1 и используется на последующей стадии.
ЯМР 1Н (ДМСО d6, δ): 1,93 (м, 2Н), 2,50 (т, 4Н).
ЯМР 13С (ДМСО d6, δ): 18,20, 36,68, 190,96.
66.2) 2-(2-Фторфенил)-6,7-дигидро-1,3-бензоксазол-4(5Н)-он
Смесь ацетата родия (32 мг; 72 мкмоль) и 2-фторбензонитрила (2,31 мл; 22 ммоль) в перфторбензоле (5 мл) обрабатывают при 60°С по каплям раствором диазоциклогександиона (полученного на стадии 66.1; 1 г; 7,24 ммоль) в 5 мл перфторбензола. Реакционную смесь выдерживают при 60°С до окончания выделения азота (1 ч; ТСХ на SiO2: 2% MeOH/CH2Cl2). После охлаждения до комнатной температуры и фильтрования растворитель фильтрата выпаривают. Остаток очищают хроматографией (SiO2: AcOEt/гептан, 1/1) с получением светло-желтого порошка.
ЯМР 1Н (CDCl3, δ): 2,31 (м, 2Н), 2,66 (м, 2Н), 3,09 (т, 2Н), 7,19-7,28 (м, 2Н), 7,48-7,50 (м, 1Н), 8,15-8,19 (м, 1Н).
МС-ЖХ: МН+ = 232,08; время удерживания = 9,28 мин.
66.3) 5-Бром-2-(2-фторфенил)-6,7-дигидро-1,3-бензоксазол-4(5Н)-он
Раствор промежуточного соединения 66.2 (470 мг; 2 ммоль) в уксусной кислоте (5 мл) обрабатывают бромом в уксусной кислоте (0,2М; 10 мл; 2 ммоль) в течение 4 суток при комнатной температуре (ТСХ на SiO2: ACOEt/гептан, 1/1). Затем реакционную смесь разбавляют водой и экстрагируют с использованием дихлорметана. Органические фазы объединяют, промывают насыщенным раствором бикарбоната натрия, затем 5% раствором дисульфита натрия. После высушивания над сульфатом натрия и удаления летучих компонентов при пониженном давлении получают желтое масло, которое очищают хроматографией (SiO2: AcOEt/гептан, 1/1) с получением белого порошка.
ЯМР 1Н (ДМСО d6, δ): 2,49 (м, 2Н), 2,73 (м, 1Н), 3,15 (м, 2Н), 4,95 (т, 1Н), 7,39-7,48 (м, 2Н), 7,63-7,67 (м, 1Н), 8,03-8,08 (т, 1Н).
МС-ЖХ: МН+ = 309,93; время удерживания = 10,08 мин.
66.4) 2-(2-Фторфенил)-4-гидрокси-1,3-бензоксазол
Раствор промежуточного соединения 66,3 (6,52 г; 21 ммоль) в тетрагидрофуране (100 мл) обрабатывают по каплям диазабицикло[5.4.0]ундек-7-еном (4,7 мл; 31 ммоль). Когда реакция заканчивается (1,5 ч; ТСХ на SiO2: AcOEt/гептан, 1/1), реакционную смесь разбавляют этилацетатом, затем последовательно промывают 1 н. соляной кислотой и насыщенным раствором хлорида натрия. Объединенные органические фазы высушивают и концентрируют с получением коричневого остатка, который очищают хроматографией (SiO2: AcOEt/гептан, 1/1) с получением бежевого порошка.
ЯМР 1Н (ДМСО-d6, δ): 6,80 (д, 1Н), 7,19-7,26 (м, 2Н), 7,41-7,49 (м, 2Н), 7,65 (м, 1Н), 8,18 (т, 1Н), 10,43 (с, 1Н).
МС-ЖХ: МН+ = 230,07; время удерживания = 10,03 мин.
66.5) 2-(2-Фторфенил)-1,3-бензоксазол-4,7-дион
Применяемая методика аналогична описанной для стадии 15.3 примера 15 с использованием промежуточного соединения 66.4 вместо промежуточного соединения 15.2. Получают желтый порошок.
ЯМР 1Н (ДМСО-d6, δ): 6,94 (шир., 2Н), 7,45-7,54 (м, 2Н), 7,74 (м, 2Н), 8,18 (т, 1Н).
МС-ЖХ: МН+ = 244,04; время удерживания = 9,73 мин (61%) и MH3 + = 246,06; время удерживания = 8,70 мин.
66.6) Смесь 2-(2-фторфенил)-5-[{2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-диона и 2-(2-фторфенил)-6-[{2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-диона
Применяемая методика аналогична описанной для стадии 15.4 примера 15 с использованием промежуточного соединения 66.5 вместо промежуточного соединения 15.3 и N,N-диметилэтилендиамина вместо анилина. Получают рубиновый порошок. Точка плавления 191°С.
ЯМР 1Н (ДМСО-d6, δ): 2,19 (с, 6Н), 2,5 (м, 2Н), 3,27 (м, 2Н), 5,41 (с, 1Н), 7,42-7,52 (м, 3Н), 7,70 (м, 2Н), 8,13 (м, 1Н).
Два компонента смеси можно охарактеризовать сдвигами в спектре ЯМР (400 мГц) единичного протона кольца бензоксазоледиона, которые составляют 5,40 и 5,41 м.д.
МС-ЖХ: МН+ = 330,14; время удерживания = 7,69 мин.
Пример 67: смесь 2-(2-фторфенил)-5-[(2-пирролидин-1-илэтил)амино]-1,3-бензоксазол-4,7-диона и 2-(2-фторфенил)-6-[2-пирролидин-1-илэтил)амино]-1,3-бензоксазол-4,7-диона
Применяемая методика аналогична описанной в примере 66 с использованием N-(2-аминоэтил)пирролидина вместо N,N-диметилэтилендиамина. Точка плавления 152°С.
Два компонента смеси можно охарактеризовать сдвигами в спектре ЯМР (400 мГц) единичного протона кольца бензоксазоледиона, которые составляют 5,39 и 5,41 м.д.
МС-ЖХ: МН+ = 356,1; время удерживания = 7,8 мин.
Пример 68: смесь 2-(2-бромфенил)-5-{[(2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-диона и 2-(2-бромфенил)-6-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-диона
68.1) 2-(2-Бромфенил)-6,7-дигидро-1,3-бензоксазол-4(5Н)-он
Применяемая методика аналогична описанной для стадии 66.2 с использованием 2-бромбензонитрила вместо 2-фторбензонитрила. Получают желтое твердое вещество.
МС-ЖХ: МН+ = 292,0; время удерживания = 9,8 мин.
68.2) 5-Бром-2-(2-бромфенил)-6,7-дигидро-1,3-бензоксазол-4(5Н)-он
Смесь промежуточного соединения 68.1 (6,6 г; 22 ммоль) и CuBr2 (10 г; 45 ммоль) в этилацетате (250 мл) примерно с 1 мл уксусной кислоты, добавленной к ней, кипятят с обратным холодильником в течение 3 ч (ТСХ на SiO2: AcOEt/гептан, 1/1). Затем реакционную смесь фильтруют через целит, фильтрат упаривают при пониженном давлении и остаток очищают на колонке (SiO2: AcOEt/гептан, 1/1) с получением светло-желтого порошка.
МС-ЖХ: МН+ = 371,8; время удерживания = 10,5 мин.
68.3) 2-(2-Бромфенил)-5-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-дион
Данное соединение получают из промежуточного соединения 68.2, следуя способам, описанным для стадий 66.4, 66.5 и 66.6. Точка плавления 138°С.
Два компонента смеси можно охарактеризовать сдвигами в спектре ЯМР (400 мГц) единичного протона кольца бензоксазоледиона, которые составляют 5,41 и 5,43 м.д.
МС-ЖХ: МН+ = 390,0; время удерживания = 7,9 мин.
Пример 69: смесь 2-(2-бромфенил)-5-[(2-пирролидин-1-илэтил)амино]-1,3-бензоксазол-4,7-диона и 2-(2-бромфенил)-6-[(2-пирролидин-1-илэтил)амино]-1,3-бензоксазол-4,7-диона
Применяемая методика аналогична описанной в примере 68 с использованием N-(2-аминоэтил)пирролидина вместо N,N-диметилэтилендиамина. Точка плавления 122°С.
Два компонента смеси можно охарактеризовать сдвигами в спектре ЯМР (400 мГц) единичного протона кольца бензоксазоледиона, которые составляют 5,40 и 5,42 м.д.
МС-ЖХ: МН+ = 416,0; время удерживания = 8,0 мин.
Пример 70: смесь 2-(2-бромфенил)-5-{[3-(диметиламино)пропил]амино}-1,3-бензоксазол-4,7-диона и 2-(2-бромфенил)-6-{[3-(диметиламино)пропил]амино}-1,3-бензоксазол-4,7-диона
Применяемая методика аналогична описанной в примере 68 с использованием N,N-диметилпропилендиамина вместо N,N-диметилэтилендиамина. Точка плавления 119°С.
Два компонента смеси можно охарактеризовать сдвигами в спектре ЯМР (400 мГц) единичного протона кольца бензоксазоледиона, которые составляют 5,38 и 5,40 м.д.
МС-ЖХ: МН+ = 404,0; время удерживания = 8,0 мин.
Пример 71: смесь 2-(2-хлорфенил)-5-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-диона и 2-(2-хлорфенил)-6-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-диона
Применяемая методика аналогична описанной в примере 66 с использованием 2-хлорбензонитрила вместо 2-фторбензонитрила. Точка плавления 137°С.
Два компонента смеси можно охарактеризовать сдвигами в спектре ЯМР (400 мГц) единичного протона кольца бензоксазоледиона, которые составляют 5,39 и 5,41 м.д.
МС-ЖХ: МН+ = 346,1; время удерживания = 7,8 мин.
Пример 72: смесь 2-(2-хлорфенил)-5-[(2-пирролидин-1-илэтил)амино]-1,3-бензоксазол-4,7-диона и 2-(2-хлорфенил)-6-[(2-пирролидин-1-илэтил)амино]-1,3-бензоксазол-4,7-диона
Применяемая методика аналогична описанной в примере 71 с использованием N-(2-аминоэтил)пирролидина вместо N,N-диметилэтилендиамина. Точка плавления 85°С.
Два компонента смеси можно охарактеризовать сдвигами в спектре ЯМР (400 мГц) единичного протона кольца бензоксазоледиона, которые составляют 5,40 и 5,41 м.д.
МС-ЖХ: МН+ = 372,1; время удерживания = 8,0 мин.
Пример 73: смесь 2-(3-бромфенил)-5-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-диона или 2-(3-бромфенил)-6-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-диона
Применяемая методика аналогична описанной в примере 68 с использованием 3-бромбензонитрила вместо 2-бромбензонитрила. Точка плавления 133°С.
Два компонента смеси можно охарактеризовать сдвигами в спектре ЯМР (400 мГц) единичного протона кольца бензоксазоледиона, которые составляют 5,39 и 5,41 м.д.
МС-ЖХ: МН+ = 390,0; время удерживания = 8,1 мин.
Пример 74: смесь 2-(4-бромфенил)-5-[(2-пирролидин-1-илэтил)амино]-1,3-бензоксазол-4,7-диона и 2-(4-бромфенил)-6-[(2-пирролидин-1-илэтил]амино}-1,3-бензоксазол-4,7-диона
Применяемая методика аналогична описанной в примере 68 с использованием 4-бромбензонитрила вместо 2-бромбензонитрила и N-(2-аминоэтил)пирролидина вместо N,N-диметилэтилендиамина. Точка плавления 181°С.
Два компонента смеси можно охарактеризовать сдвигами в спектре ЯМР (400 мГц) единичного протона кольца бензоксазоледиона, которые составляют 5,37 и 5,39 м.д.
МС-ЖХ: МН+ = 415,0; время удерживания = 8,3 мин.
Пример 75: смесь 2-(4-бромфенил)-5-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-диона и 2-(4-бромфенил)-6-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-диона
Применяемая методика аналогична описанной в примере 74 с использованием N,N-диметилэтилендиамина вместо N-(2-аминоэтил)пирролидина. Точка плавления 184°С.
Два компонента смеси можно охарактеризовать сдвигами в спектре ЯМР (400 мГц) единичного протона кольца бензоксазоледиона, которые составляют 5,38 и 5,40 м.д.
МС-ЖХ: МН+ = 390,1; время удерживания = 8,2 мин.
Пример 76: смесь 2-(4-фторфенил)-5-[(2-пирролидин-1-илэтил)амино]-1,3-бензоксазол-4,7-диона и 2-(4-фторфенил)-6-[(2-пирролидин-1-илэтил)амино]-1,3-бензоксазол-4,7-диона
76.1) 2-(4-Фторфенил)-6,7-дигидро-1,3-бензоксазол-4(5Н)-он
Применяемая методика аналогична описанной для стадии 66.2 с использованием 4-фторбензонитрила вместо 2-фторбензонитрила. Получают желтое твердое вещество.
МС-ЖХ: МН+ = 232,1; время удерживания = 9,4 мин.
76.2) 5-Бром-2-(4-фторфенил)-6,7-дигидро-1,3-бензоксазол-4(5Н)-он
Пиридинийтрибромид (996 мг; 3,11 ммоль) добавляют тремя порциями с интервалом 2-3 мин к раствору промежуточного соединения 76.1 (600 мг; 2,59 ммоль) в ледяной уксусной кислоте (25 мл), нагретой до 50°С. Реакционную смесь выдерживают при 50°С в течение 4 ч (ТСХ на SiO2: AcOEt/гептан, 1/1). Летучие компоненты выпаривают при пониженном давлении, затем остаток переводят в воду и экстрагируют дихлорметаном. Затем реакционную смесь фильтруют через целит, фильтрат упаривают при пониженном давлении и остаток очищают на колонке (SiO2: AcOEt/гептан, 1/1) с получением светло-желтого порошка. Органические фазы объединяют и промывают 10% раствором бикарбоната натрия, затем насыщенным раствором хлорида натрия. После высушивания над сульфатом натрия и удалением летучих компонентов при пониженном давлении остаток очищают хроматографией на колонке (SiO2: AcOEt/гептан, 1/1) с получением бежевого порошка.
МС-ЖХ: МН+ = 312,0; время удерживания = 10,3 мин.
76.3) Смесь 2-(4-фторфенил)-5-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-диона и 2-(4-фторфенил)-6-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-диона
Данное соединение получают из промежуточного соединения 76.2, следуя способам, описанным для стадий 66.4, 66.5 и 66.6. Точка плавления 162°С.
Два компонента смеси можно охарактеризовать сдвигами в спектре ЯМР (400 мГц) единичного протона кольца бензоксазоледиона, которые составляют 5,37 и 5,39 м.д.
МС-ЖХ: МН+ = 356,1; время удерживания = 8,0 мин.
Пример 77: смесь 5-{[2-(диметиламино)этил]амино}-2-(4-фторфенил)-1,3-бензоксазол-4,7-диона и 6-{[2-(диметиламино)этил]амино}-2-(4-фторфенил)-1,3-бензоксазол-4,7-диона
Применяемая методика аналогична описанной в примере 76 с использованием N-(2-аминоэтил)пирролидина вместо N,N-диметилэтилендиамина. Точка плавления 170°С.
Два компонента смеси можно охарактеризовать сдвигами в спектре ЯМР (400 мГц) единичного протона кольца бензоксазоледиона, которые составляют 5,38 и 5,39 м.д.
МС-ЖХ: МН+ = 330,1; время удерживания = 7,8 мин.
Пример 78: смесь 5-[(1-бензилпирролидин-3-ил)амино]-2-(4-фторфенил)-1,3-бензоксазол-4,7-диона и 6-[(1-бензилпирролидин-3-ил)амино]-2-(4-фторфенил)-1,3-бензоксазол-4,7-диона
Применяемая методика аналогична описанной в примере 76 с использованием (1-бензилпирролидин-3-ил)амина вместо N,N-диметилэтилендиамина. Точка плавления 180°С.
Два компонента смеси можно охарактеризовать сдвигами в спектре ЯМР (400 мГц) единичного протона кольца бензоксазоледиона, которые составляют 5,37 и 5,39 м.д.
МС-ЖХ: МН+ = 418,0; время удерживания = 8,5 мин.
Пример 79: смесь 5-{[3-(диметиламино)пропил]амино}-2-(4-фторфенил)-1,3-бензоксазол-4,7-диона и 6-{[3-(диметиламино)пропил]амино}-2-(4-фторфенил)-1,3-бензоксазол-4,7-диона
Применяемая методика аналогична описанной в примере 76 с использованием N,N-диметилпропилендиамина вместо N,N-диметилэтилендиамина. Точка плавления 149°С.
Два компонента смеси можно охарактеризовать сдвигами в спектре ЯМР (400 мГц) единичного протона кольца бензоксазоледиона, которые составляют 5,35 и 5,37 м.д.
МС-ЖХ: МН+ = 344,2; время удерживания = 7,9 мин.
Пример 80: смесь 2-(3,5-дифторфенил)-5-[(2-пирролидин-1-илэтил)амино]-1,3-бензоксазол-4,7-диона и 2-(3,5-дифторфенил)-6-[(2-пирролидин-1-илэтил)амино]-1,3-бензоксазол-4,7-диона
Применяемая методика аналогична описанной в примере 68 с использованием 3,5-дифторбензонитрила вместо 2-бромбензонитрила и N-(2-аминоэтил)пирролидина вместо N,N-диметилэтилендиамина. Точка плавления 158°С.
Два компонента смеси можно охарактеризовать сдвигами в спектре ЯМР (400 мГц) единичного протона кольца бензоксазоледиона, которые составляют 5,41 и 5,43 м.д.
МС-ЖХ: МН+ = 374,0; время удерживания = 8,0 мин.
Пример 81: смесь 2-(3,5-дифторфенил)-5-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-диона и 2-(3,5-дифторфенил)-6-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-диона
Применяемая методика аналогична описанной в примере 68 с использованием 3,5-дифторбензонитрила вместо 2-бромбензонитрила. Точка плавления 175°С.
Два компонента смеси можно охарактеризовать сдвигами в спектре ЯМР (400 мГц) единичного протона кольца бензоксазоледиона, которые составляют 5,33 и 5,41 м.д.
МС-ЖХ: МН+ = 348,0; время удерживания = 7,9 мин.
Пример 82: смесь 2-(2,5-дифторфенил)-5-[(2-пирролидин-1-илэтил)амино]-1,3-бензоксазол-4,7-диона и 2-(2,5-дифторфенил)-6-[(2-пирролидин-1-илэтил)амино]-1,3-бензоксазол-4,7-диона
Применяемая методика аналогична описанной в примере 68 с использованием 2,5-дифторбензонитрила вместо 2-бромбензонитрила и N-(2-аминоэтил)пирролидина вместо N,N-диметилэтилендиамина. Точка плавления 163°С.
Два компонента смеси можно охарактеризовать сдвигами в спектре ЯМР (400 мГц) единичного протона кольца бензоксазоледиона, которые составляют 5,40 и 5,42 м.д.
МС-ЖХ: МН+ = 374,0; время удерживания = 7,9 мин.
Пример 83: смесь 2-(2,5-дифторфенил)-5-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-диона и 2-(2,5-дифторфенил)-6-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-диона
Применяемая методика аналогична описанной в примере 68 с использованием 2,5-дифторбензонитрила вместо 2-бромбензонитрила.
Два компонента смеси можно охарактеризовать сдвигами в спектре ЯМР (400 мГц) единичного протона кольца бензоксазоледиона, которые составляют 5,41 и 5,43 м.д.
МС-ЖХ: МН+ = 348,0; время удерживания = 7,7 мин.
Пример 84: смесь 2-(2,3-дифторфенил)-5-{[3-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-диона и 2-(2,3-дифторфенил)-6-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-диона
Применяемая методика аналогична описанной в примере 68 с использованием 2,5-дифторбензонитрила вместо 2-бромбензонитрила. Точка плавления 167°С.
Два компонента смеси можно охарактеризовать сдвигами в спектре ЯМР (400 мГц) единичного протона кольца бензоксазоледиона, которые составляют 5,41 и 5,43 м.д.
МС-ЖХ: МН+ = 348,1; время удерживания = 7,8 мин.
Пример 85: смесь 2-(2,3-дифторфенил)-5-[(2-пирролидин-1-илэтил)амино]-1,3-бензоксазол-4,7-диона и 2-(2,3-дифторфенил)-6-[(2-пирролидин-1-илэтил)амино]-1,3-бензоксазол-4,7-диона
Применяемая методика аналогична описанной в примере 68 с использованием 2,3-дифторбензонитрила вместо 2-бромбензонитрила и N-(2-аминоэтил)пирролидина вместо N,N-диметилэтилендиамина. Точка плавления 150°С.
Два компонента смеси можно охарактеризовать сдвигами в спектре ЯМР (400 мГц) единичного протона кольца бензоксазоледиона, которые составляют 5,40 и 5,42 м.д.
МС-ЖХ: МН+ = 374,1; время удерживания = 7,9 мин.
Пример 86: смесь 2-(2,3-дифторфенил)-5-{[3-(диметиламино)пропил]амино}-1,3-бензоксазол-4,7-диона и 2-(2,3-дифторфенил)-6-{[3-(диметиламино)пропил]амино}-1,3-бензоксазол-4,7-диона
Применяемая методика аналогична описанной в примере 68 с использованием 2,3-дифторбензонитрила вместо 2-бромбензонитрила и N,N-диметилпропилендиамина вместо N,N-диметилэтилендиамина. Точка плавления 169°С.
Два компонента смеси можно охарактеризовать сдвигами в спектре ЯМР (400 мГц) единичного протона кольца бензоксазоледиона, которые составляют 5,38 и 5,41 м.д.
МС-ЖХ: МН+ = 362,1; время удерживания = 7,8 мин.
Пример 87: смесь 5-[(2-пирролидин-1-илэтил)амино]-2-(3,4,5-трифторфенил)-1,3-бензоксазол-4,7-диона и 6-[(2-пирролидин-1-илэтил)амино]-2-(3,4,5-трифторфенил)-1,3-бензоксазол-4,7-диона
Применяемая методика аналогична описанной в примере 68 с использованием 3,4,5-трифторбензонитрила вместо 2-бромбензонитрила и N-(2-аминоэтил)пирролидина вместо N,N-диметилэтилендиамина.
Два компонента смеси можно охарактеризовать сдвигами в спектре ЯМР (400 мГц) единичного протона кольца бензоксазоледиона, которые составляют 5,39 и 5,41 м.д.
МС-ЖХ: МН+ = 392,0; время удерживания = 8,2 мин.
Пример 88: смесь 5-{[2-(диметиламино)этил]амино}-2-(3,4,5-трифторфенил)-1,3-бензоксазол-4,7-диона и 6-{[2-(диметиламино)этил]амино}-2-(3,4,5-трифторфенил)-1,3-бензоксазол-4,7-диона
Применяемая методика аналогична описанной в примере 68 с использованием 3,4,5-трифторфенила вместо 2-бромбензонитрила.
Два компонента смеси можно охарактеризовать сдвигами в спектре ЯМР (400 мГц) единичного протона кольца бензоксазоледиона, которые составляют 5,40 и 5,42 м.д.
МС-ЖХ: МН+ = 366,1; время удерживания = 8,1 мин.
Пример 89: смесь 5-[(2-пирролидин-1-илэтил)амино]-2-(2,3,4,5-тетрафторфенил)-1,3-бензоксазол-4,7-диона и 6-[(2-пирролидин-1-илэтил)амино]-2-(2,3,4,5-тетрафторфенил)-1,3-бензоксазол-4,7-диона
Применяемая методика аналогична описанной в примере 68 с использованием 2,3,4,5-тетрафторбензонитрила вместо 2-бромбензонитрила и N-(2-аминоэтил)пирролидина вместо N,N-диметилэтилендиамина.
Два компонента смеси можно охарактеризовать сдвигами в спектре ЯМР (400 мГц) единичного протона кольца бензоксазоледиона, которые составляют 5,42 и 5,44 м.д.
МС-ЖХ: МН+ = 410,0; время удерживания = 8,2 мин.
Пример 90: смесь 5-{[2-(диметиламино)этил]амино}-2-(2,3,4,5-тетрафторфенил)-1,3-бензоксазол-4,7-диона и 6-{[2-(диметиламино)этил]амино}-2-(2,3,4,5-тетрафторфенил)-1,3-бензоксазол-4,7-диона
Применяемая методика аналогична описанной в примере 68 с использованием 2,3,4,5-тетрафторбензонитрила вместо 2-бромбензонитрила. Точка плавления 160°С.
Два компонента смеси можно охарактеризовать сдвигами в спектре ЯМР (400 мГц) единичного протона кольца бензоксазоледиона, которые составляют 5,42 и 5,45 м.д.
МС-ЖХ: МН+ = 384,0; время удерживания = 8,1 мин.
Пример 91: смесь 5-{[2-(диметиламино)этил]амино}-2-[2-фтор-6-(трифторметил)фенил]-1,3-бензоксазол-4,7-диона и 6-{[2-(диметиламино)этил]амино}-2-[2-фтор-6-(трифторметил)фенил]-1,3-бензоксазол-4,7-диона
Применяемая методика аналогична описанной в примере 68 с использованием 2-фтор-6-(трифторметил)бензонитрила вместо 2-бромбензонитрила.
Два компонента смеси можно охарактеризовать сдвигами в спектре ЯМР (400 мГц) единичного протона кольца бензоксазоледиона, которые составляют 5,44 и 5,46 м.д.
МС-ЖХ: МН+ = 398,0; время удерживания = 8,0 мин.
Пример 92: смесь 2-[2-фтор-6-(трифторметил)фенил]-5-[(2-пирролидин-1-илэтил]амино}-1,3-бензоксазол-4,7-диона и 2-[2-фтор-6-(трифторметил)фенил]-6-{[2-пирролидин-1-илэтил]амино}-1,3-бензоксазол-4,7-диона
Применяемая методика аналогична описанной в примере 68 с использованием 2-фтор-6-(трифторметил)бензонитрила вместо 2-бромбензонитрила и N-(2-аминоэтил)пирролидина вместо N,N-диметилэтилендиамина. Точка плавления 166°С.
Два компонента смеси можно охарактеризовать сдвигами в спектре ЯМР (400 мГц) единичного протона кольца бензоксазоледиона, которые составляют 5,43 и 5,45 м.д.
МС-ЖХ: МН+ = 424,1; время удерживания = 8,1 мин.
Пример 93: смесь 5-{[3-(диметиламино)пропил]амино}-2-[2-фтор-6-(трифторметил)фенил]-1,3-бензоксазол-4,7-диона и 6-{[3-(диметиламино)пропил]амино}-2-[2-фтор-6-(трифторметил)фенил]-1,3-бензоксазол-4,7-диона
Применяемая методика аналогична описанной в примере 68 с использованием 2-фтор-6-(трифторметил)бензонитрила вместо 2-бромбензонитрила и N,N-диметилпропилендиамина вместо N,N-диметилэтилендиамина. Точка плавления 128°С.
Два компонента смеси можно охарактеризовать сдвигами в спектре ЯМР (400 мГц) единичного протона кольца бензоксазоледиона, которые составляют 5,42 и 5,43 м.д.
МС-ЖХ: МН+ = 412,0; время удерживания = 8,0 мин.
Пример 94: смесь 2-[2-хлор-5-(трифторметил)фенил]-5-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-диона и 2-[2-хлор-5-(трифторметил)фенил]-6-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-диона
Применяемая методика аналогична описанной в примере 68 с использованием 2-хлор-5-(трифторметил)бензонитрила вместо 2-бромбензонитрила. Точка плавления 182°С.
Два компонента смеси можно охарактеризовать сдвигами в спектре ЯМР (400 мГц) единичного протона кольца бензоксазоледиона, которые составляют 5,43 и 5,46 м.д.
МС-ЖХ: МН+ = 414,0; время удерживания = 8,3 мин.
Пример 95: смесь 2-[2-хлор-5-(трифторметил)фенил]-5-[(2-пирролидин-1-илэтил)амино]-1,3-бензоксазол-4,7-диона и 2-[2-хлор-5-(трифторметил)фенил]-6-[(2-пирролидин-1-илэтил)амино]-1,3-бензоксазол-4,7-диона
Применяемая методика аналогична описанной в примере 68 с использованием 2-хлор-5-(трифторметил)бензонитрила вместо 2-бромбензонитрила и N-(2-аминоэтил)пирролидина вместо N,N-диметилэтилендиамина. Точка плавления 152°С.
Два компонента смеси можно охарактеризовать сдвигами в спектре ЯМР (400 мГц) единичного протона кольца бензоксазоледиона, которые составляют 5,43 и 5,45 м.д.
МС-ЖХ: МН+ = 440,0; время удерживания = 8,5 мин.
Пример 96: смесь 2-[2-хлор-5-(трифторметил)фенил]-5-{[3-(диметиламино)пропил]амино}-1,3-бензоксазол-4,7-диона и 2-[2-хлор-5-(трифторметил)фенил]-6-{[3-(диметиламино)пропил]амино}-1,3-бензоксазол-4,7-диона
Применяемая методика аналогична описанной в примере 68 с использованием 2-хлор-5-(трифторметил)бензонитрила вместо 2-бромбензонитрила и N,N-диметилпропилендиамина вместо N,N-диметилэтилендиамина. Точка плавления 121°С.
Два компонента смеси можно охарактеризовать сдвигами в спектре ЯМР (400 мГц) единичного протона кольца бензоксазоледиона, которые составляют 5,41 и 5,43 м.д.
МС-ЖХ: МН+ = 428,0; время удерживания = 8,4 мин.
Пример 97: смесь 2-[2-хлор-6-фторфенил]-5-{[3-(диметиламино)пропил]амино}-1,3-бензоксазол-4,7-диона и 2-[2-хлор-6-(фторфенил]-6-{[3-(диметиламино)пропил]амино}-1,3-бензоксазол-4,7-диона
Применяемая методика аналогична описанной в примере 68 с использованием 2-хлор-6-фторбензонитрила вместо 2-бромбензонитрила.
Два компонента смеси можно охарактеризовать сдвигами в спектре ЯМР (400 мГц) единичного протона кольца бензоксазоледиона, которые составляют 5,43 и 5,45 м.д.
МС-ЖХ: МН+ = 364,1; время удерживания = 7,8 мин.
Пример 98: смесь 2-[2-хлор-6-фторфенил]-5-[(2-пирролидин-1-илэтил)амино]-1,3-бензоксазол-4,7-диона и 2-[2-хлор-6-фторфенил]-6-[(2-пирролидин-1-илэтил)амино]-1,3-бензоксазол-4,7-диона
Применяемая методика аналогична описанной в примере 68 с использованием 2-хлор-6-фторбензонитрила вместо 2-бромбензонитрила и N-(2-аминоэтил)пирролидина вместо N,N-диметилэтилендиамина. Точка плавления 124°С.
Два компонента смеси можно охарактеризовать сдвигами в спектре ЯМР (400 мГц) единичного протона кольца бензоксазоледиона, которые составляют 5,42 и 5,44 м.д.
МС-ЖХ: МН+ = 390,1; время удерживания = 7,9 мин.
Пример 99: смесь 2-[3,4-диметоксифенил]-5-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-диона и 2-[3,4-диметоксифенил]-6-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-диона
99.1) 2-(3,4-Диметоксифенил)-6,7-дигидро-1,3-бензоксазол-4(5Н)-он
Применяемая методика аналогична описанной для стадии 66.2 с использованием 3,4-диметоксибензонитрила вместо 2-фторбензонитрила. Получают желтое твердое вещество.
МС-ЖХ: МН+ = 274,0; время удерживания = 8,9 мин.
99.2) 5-Йод-2-(3,4-диметоксифенил)-6,7-дигидро-1,3-бензоксазол-4(5Н)-он
Раствор промежуточного соединения 99,1 (500 мг; 1,83 ммоль) в уксусной кислоте (30 мл) обрабатывают в течение 96 ч при комнатной температуре поли[стирол-со-(4-винилпиридиния дихлорйодатом(1-))](2,6 г; 8,25 мэкв, приготовлен по способу B  et al., Bull. Chem. Soc. Jpn (1989), 62, 3406-3408) (подтверждение ТСХ на SiO2: 2% MeOH/CH2Cl2). Полимер удаляют фильтрованием и летучие компоненты выпаривают при пониженном давлении. Остаток очищают на колонке (SiO2: 1% MeOH/CH2Cl2) с получением желтого масла.
et al., Bull. Chem. Soc. Jpn (1989), 62, 3406-3408) (подтверждение ТСХ на SiO2: 2% MeOH/CH2Cl2). Полимер удаляют фильтрованием и летучие компоненты выпаривают при пониженном давлении. Остаток очищают на колонке (SiO2: 1% MeOH/CH2Cl2) с получением желтого масла.
МС-ЖХ: МН+ = 399,9; время удерживания = 9,8 мин.
99.3) Смесь 2-(3,4-диметоксифенил)-5-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-диона и 2-(3,4-диметоксифенил)-6-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-диона
Данное соединение получают из промежуточного соединения 99.2, следуя способам, описанным для стадий 66.4, 66.5 и 66.6. Точка плавления 181°С.
Два компонента смеси можно охарактеризовать сдвигами в спектре ЯМР (400 мГц) единичного протона кольца бензоксазоледиона, которые составляют 5,35 и 5,36 м.д.
МС-ЖХ: МН+ = 372,1; время удерживания = 7,6 мин.
Пример 100: смесь 2-[2-бром-3-пиридил]-5-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-диона и 2-[2-бром-3-пиридил]-6-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-диона
Применяемая методика аналогична описанной в примере 68 с использованием 2-бромникотинонитрила вместо 2-бромбензонитрила. Точка плавления 133°С.
Два компонента смеси можно охарактеризовать сдвигами в спектре ЯМР (400 мГц) единичного протона кольца бензоксазоледиона, которые составляют 5,43 и 5,45 м.д.
МС-ЖХ: МН+ = 391,0; время удерживания = 7,4 мин.
Пример 101: смесь 2-циклогексил-5-[(2-пирролидин-1-илэтил)амино]-1,3-бензотиазол-4,7-диона и 2-циклогексил-6-[(2-пирролидин-1-илэтил)амино]-1,3-бензотиазол-4,7-диона
101.1) N-(2,5-Диметоксифенил)циклогексанкарбоксамид
1 мл (7,62 ммоль; 1,1 экв) хлорангидрида циклогексановой кислоты добавляют к раствору 1,05 г (6,89 ммоль) 2,5-диметоксианилина в 10 мл смеси толуол/метанол (1/1). Реакционную смесь перемешивают при 70°С в течение 1,5 ч после охлаждения до комнатной температуры, ее выливают в 50 мл воды. Предполагаемый продукт экстрагируют толуолом дважды по 50 мл, затем промывают водой дважды по 50 мл. Органические фазы объединяют, высушивают над сульфатом магния и растворитель выпаривают при пониженном давлении. Получают 1,46 г (выход 67%) N-(2,5-диметоксифенил)циклогексанкарбоксамида и используют на последующей стадии без дополнительной очистки.
ЯМР 1Н (ДМСО d6, 400 МГц, δ): 8,84 (с, 1Н, NH), 7,72-7,71 (м, 1Н, Н аром.), 6,93-6,91 (д, 1Н, Н аром.), 6,60-6,57 (м, 1Н, Н аром.), 3,76 (с, 3Н, СН3), 3,66 (с, 3Н, СН3), 1,78-1,70 (м, 6Н, СН2, СН), 1,38-1,24 (м, 5Н, СН2).
МС-ЖХ: МН+ = 264,14; время удерживания = 10,76 мин.
101.2) N-(2,5-Диметоксифенил)циклогексанкарботиоамид
1,46 г (5,54 ммоль) N-(2,5-диметоксифенил)циклогексанкарбоксамида растворяют в 40 мл безводного толуола. Раствор нагревают до 100°С и к реакционной смеси добавляют 3,34 г (8,26 ммоль; 1,5 экв) реагента Лавессона при перемешивании при 100°С в течение 4 ч. После охлаждения до комнатной температуры раствор выливают в 50 мл воды со льдом и экстрагируют толуолом. Органические фазы высушивают над сульфатом магния и растворитель выпаривают. Затем N-(2,5-диметоксифенил)циклогексанкарботиоамид очищают хроматографией на колонке с силикагелем (элюент: дихлорметан/гептан, 1/1 затем 3/2). Получают 1,26 г (выход 81%) продукта в виде желтого масла.
ЯМР 1Н (ДМСО d6, 400 МГц, δ): 10,76 (с, 1Н, NH), 7,28-7,27 (м, 1Н, Н аром.), 7,02-6,99 (д, 1Н, Н аром.), 6,82-6,80 (м, 1Н, Н аром.), 3,73 (с, 3Н, СН3), 3,68 (с, 3Н, СН3), 1,77-1,75 (м, 4Н, СН2), 1,67-1,58 (м, 3Н, СН2, СН), 1,31-1,15 (м, 4Н, 2СН2).
МС-ЖХ: МН+ = 280,12; время удерживания = 11,38 мин.
101.3) 2-Циклогексил-4,7-диметокси-1,3-бензотиазол
1,26 г (4,50 ммоль) N-(2,5-диметоксифенил)циклогексанкарботиоамида растворяют в 100 мл 1,5М раствора гидроокиси натрия (100 мл) и реакционную смесь охлаждают до 0°С перед добавлением 25 мл свежеприготовленного 20% водного раствора феррицианида калия (5,05 г К3[Fe(CN)6]; 3,4 экв). Реакционную смесь перемешивают при комнатной температуре в течение 24 ч, затем получают 1,1 г (выход 88%) предполагаемого производного бензотиазола фильтрованием, промыванием холодной водой и высушиванием при пониженном давлении в присутствии Р2О5.
ЯМР 1Н (ДМСО d6, 400 МГц, δ): 6,95-6,85 (дд, 2Н, Н аром.), 3,88 (с, 6Н, 2СН3), 3,10-3,04 (м, 1Н, СН), 2,10-2,07 (м, 2Н, СН2), 1,81-1,77 (м, 2Н, СН2), 1,70-1,67 (м, 1Н, СН), 1,57-1,51 (м, 2Н, СН2), 1,42-1,39 (м, 2Н, СН2), 1,26-1,28 (м, 1Н, СН).
МС-ЖХ: МН+ = 278,09; время удерживания = 11,91 мин.
101.4) 2-Циклогексил-1,3-бензотиазол-4,7-дион
Готовят суспензию 1 г (3,61 ммоль) 2-циклогексил-4,7-диметокси-1,3-бензотиазола в смеси ацетонитрил/вода (3/1) при 0°С, затем к суспензии добавляют 4,36 г (7,96 ммоль; 2,2 экв) церия (IV) и нитрата аммония. Реакционную смесь перемешивают в течение 1,5 ч при комнатной температуре, затем после фильтрования, промывания холодной водой и высушивания при пониженном давлении получают 0,78 г (выход 88%) 2-циклогексил-1,3-бензотиазол-4,7-диона.
ЯМР 1Н (ДМСО d6, 400 МГц, δ): 6,90 (с, 2Н), 3,15-3,10 (м, 1Н, СН), 2,10-2,07 (м, 2Н, СН2), 1,81-1,77 (м, 2Н, СН2), 1,65-1,70 (м, 1Н, СН), 1,55-1,39 (м, 5Н, СН, СН2).
МС-ЖХ: МН+ = 248,12; время удерживания = 10,82 мин.
101.5) N-(2,5-Диметоксифенил)циклогексанкарбоксамид
Применяемая методика аналогична описанной для стадии 15.4 примера 15 с использованием промежуточного соединения 101.4 вместо промежуточного соединения 15.3 и N,N-диметилэтилендиамина вместо анилина. Получают смесь 2-циклогексил-5-{[2-(диметиламино)этил]амино}-1,3-бензотиазол-4,7-диона и 2-циклогексил-6-{[2-(диметиламино)этил]амино}-1,3-бензотиазол-4,7-диона (80% и 9%).
ЯМР 1Н (ДМСО d6, 400 МГц, δ): 7,20 (т, 1Н, NH), 5,49 и 5,43 (2с, Н), 3,24-3,21 (м, 2Н, СН2), 3,09-3,12 (м, 3Н, СН, СН2), 2,19 (с, 6Н, 2СН3), 2,09-2,06 (м, 2Н, СН2), 1,80-1,77 (м, 3Н, СН, СН2), 1,53-1,49 (м, 4Н, 2СН2), 1,41-1,38 (м, 1Н, СН).
МС-ЖХ: МН+ = 334,17; время удерживания = 7,99 и 8,06 мин.
Соединения примеров 102-113 получают способом, аналогичным описанному для примера 101.
Пример 102: смесь 2-циклогексил-5-[(2-пирролидин-1-илэтил)амино]-1,3-бензотиазол-4,7-диона и 2-циклогексил-6-[(2-пирролидин-1-илэтил)амино]-1,3-бензотиазол-4,7-диона
МС-ЖХ: МН+ = 360,16; время удерживания = 8,19 мин.
Пример 103: смесь 5-[(2-пирролидин-1-илэтил)амино]-2-тиен-2-ил-1,3-бензотиазол-4,7-диона и 6-[(2-пирролидин-1-илэтил)амино]-2-тиен-2-ил-1,3-бензотиазол-4,7-диона
МС-ЖХ: МН+ = 360,01; время удерживания = 7,78 и 7,86 мин.
Пример 104: смесь 2-(2,5-дихлортиен-3-ил)-5-{[2-(диметиламино)этил]амино}-1,3-бензотиазол-4,7-диона и 2-(2,5-дихлортиен-3-ил)-6-{[2-(диметиламино)этил]амино}-1,3-бензотиазол-4,7-диона
МС-ЖХ: МН+ = 427,87; время удерживания = 8,63 и 8,80 мин.
Пример 105: смесь 2-(2,5-дихлортиен-3-ил)-5-[(2-пирролидин-1-илэтил)амино]-1,3-бензотиазол-4,7-диона и 2-(2,5-дихлортиен-3-ил)-6-[(2-пирролидин-1-илэтил)амино]-1,3-бензотиазол-4,7-диона
МС-ЖХ: МН+ = 427,87; время удерживания = 8,63 и 8,80 мин.
Пример 106: смесь 2-(2-фурил)-5-[(2-пирролидин-1-илэтил)амино]-1,3-бензотиазол-4,7-диона и 2-(2-фурил)-5-[(2-пирролидин-1-илэтил)амино]-1,3-бензотиазол-4,7-диона
МС-ЖХ: МН+ = 344,04; время удерживания = 7,57 и 7,64 мин.
Пример 107: смесь 5-{[2-(диметиламино)этил]амино}-2-(2-метоксифенил)-1,3-бензотиазол-4,7-диона и 6-{[2-(диметиламино)этил]амино}-2-(2-метоксифенил)-1,3-бензотиазол-4,7-диона
МС-ЖХ: МН+ = 358,18; время удерживания = 7,88 и 7,97 мин.
Пример 108: смесь 5-{[2-(диметиламино)этил]амино}-2-(2-фторфенил)-1,3-бензотиазол-4,7-диона и 6-{[2-(диметиламино)этил]амино}-2-(2-фторфенил)-1,3-бензотиазол-4,7-диона
МС-ЖХ: МН+ = 346,14; время удерживания = 7,85 и 7,94 мин.
Пример 109: смесь 2-(2-фторфенил)-5-[(2-пирролидин-1-илэтил)амино]-1,3-бензотиазол-4,7-диона и 2-(2-фторфенил)-6-[(2-пирролидин-1-илэтил)амино]-1,3-бензотиазол-4,7-диона
МС-ЖХ: МН+ = 372,14; время удерживания = 7,97 и 8,06 мин.
Пример 110: смесь 2-(4-фторфенил)-5-[(2-пирролидин-1-илэтил)амино]-1,3-бензотиазол-4,7-диона и 2-(4-фторфенил)-6-[(2-пирролидин-1-илэтил)амино]-1,3-бензотиазол-4,7-диона
МС-ЖХ: МН+ = 372,05; время удерживания = 7,98 и 8,07 мин.
Пример 111: смесь 5-{[2-(диметиламино)этил]амино}-2-(4-фторфенил)-1,3-бензотиазол-4,7-диона и 6-{[2-(диметиламино)этил]амино}-2-(4-фторфенил)-1,3-бензотиазол-4,7-диона
МС-ЖХ: МН+ = 346,05; время удерживания = 7,87 и 7,95 мин.
Пример 112: смесь 2-(2,6-дифторфенил)-5-[(2-пирролидин-1-илэтил)амино]-1,3-бензотиазол-4,7-диона и 2-(2,6-дифторфенил)-6-[(2-пирролидин-1-илэтил)амино]-1,3-бензотиазол-4,7-диона
МС-ЖХ: МН+ = 390,04; время удерживания = 7,89 и 7,95 мин.
Пример 113: смесь 2-(2,6-дифторфенил)-5-{[2-(диметиламино)этил]амино}-1,3-бензотиазол-4,7-диона и 2-(2,6-дифторфенил)-6-{[2-(диметиламино)этил]амино}-1,3-бензотиазол-4,7-диона
МС-ЖХ: МН+ = 364,05; время удерживания = 7,78 и 7,83 мин.
Пример 114: 5-[[2-(диметиламино)этил](этил)амино]-2-метил-1,3-бензотиазол-4,7-дион
Данное соединение получают способом, аналогичным описанному в примере 1 с использованием N,N,N'-триметилэтилендиамина вместо 4-(2-аминоэтил)морфолина.
ЯМР 1Н (ДМСО d6, 400 МГц, δ): 5,53 (с, 1Н, СН), 3,73-3,70 (т, 2Н, СН2), 2,93 (с, 3Н, СН3), 2,74 (с, 3Н, СН3), 2,32-2,30 (т, 2Н, СН2), 1,92 (с, 6Н, 2СН3).
МС-ЖХ: МН+ = 280,11; время удерживания = 7,03 мин.
Пример 115: 5-[[2-(диметиламино)этил](метил)амино]-2-метил-1,3-бензотиазол-4,7-дион
Применяемая методика аналогична описанной в примере 1 с использованием N,N-диметил-N'-этилендиамина вместо 4-(2-аминоэтил)морфолина.
МС-ЖХ: МН+ = 294,07; время удерживания = 7,20 мин.
Пример 116: смесь 2-[2,6-дихлор-5-фтор-3-пиридил]-5-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-диона и 2-[2,6-дихлор-5-фтор-3-пиридил]-6-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-диона
Применяемая методика аналогична описанной в примере 68 с использованием 2,6-дихлор-5-фторникотинонитрила вместо 2-бромбензонитрила.
МС-ЖХ: МН+ = 399,1; время удерживания = 8,1 мин.
Пример 117: смесь 2-[2,6-дихлор-5-фтор-3-пиридил]-5-[(2-пирролидин-1-илэтил)амино]-1,3-бензоксазол-4,7-диона и 2-[2,6-дихлор-5-фтор-3-пиридил]-6-[(2-пирролидин-1-илэтил)амино]-1,3-бензоксазол-4,7-диона
Применяемая методика аналогична описанной в примере 68 с использованием 2,6-дихлор-5-фторникотинонитрила вместо 2-бромбензонитрила и N-(2-аминоэтил)пирролидина вместо N,N-диметилэтилендиамина.
МС-ЖХ: МН+ = 399,1; время удерживания = 8,1 мин.
Пример 118: смесь 2-(2,4-дифторфенил)-5-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-диона и 2-(2,4-дифторфенил)-6-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-диона
Применяемая методика аналогична описанной в примере 68 с использованием 2,4-дифторбензонитрила вместо 2-бромбензонитрила.
МС-ЖХ: МН+ = 348,1; время удерживания = 7,8 мин.
Пример 119: смесь 5-{[2-(диметиламино)этил]амино}-2-(2,3,4-трифторфенил)-1,3-бензоксазол-4,7-диона и 6-{[2-(диметиламино)этил]амино}-2-(2,3,4-трифторфенил)-1,3-бензоксазол-4,7-диона
Применяемая методика аналогична описанной в примере 68 с использованием 2,3,4-трифторбензонитрила вместо 2-бромбензонитрила. Точка плавления 156°С.
МС-ЖХ: МН+ = 366,1; время удерживания = 8,0 мин.
Пример 120: смесь 5-[(2-пирролидин-1-илэтил)амино]-2-(2,3,4-трифторфенил)-1,3-бензоксазол-4,7-диона и 6-[(2-пирролидин-1-илэтил)амино]-2-(2,3,4-трифторфенил)-1,3-бензоксазол-4,7-диона
Применяемая методика аналогична описанной в примере 68 с использованием 2,3,4-трифторбензонитрила вместо 2-бромбензонитрила и N-(2-аминоэтил)пирролидина вместо N,N-диметилэтилендиамина.
МС-ЖХ: МН+ = 392,1; время удерживания = 8,1 мин.
Пример 121: смесь 2-(3-фтор-4-метилфенил)-5-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-диона и 2-(3-фтор-4-метилфенил)-6-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-диона
Применяемая методика аналогична описанной в примере 68 с использованием 3-фтор-4-метилбензонитрила вместо 2-бромбензонитрила. Точка плавления 179°С.
МС-ЖХ: МН+ = 344,1; время удерживания = 8,1 мин.
Пример 122: смесь 2-(3-фтор-4-метилфенил)-5-[(2-пирролидин-1-илэтил)амино]-1,3-бензоксазол-4,7-диона и 2-(3-фтор-4-метилфенил)-6-[(2-пирролидин-1-илэтил)амино]-1,3-бензоксазол-4,7-диона
Применяемая методика аналогична описанной в примере 68 с использованием 3-фтор-4-метилбензонитрила вместо 2-бромбензонитрила и N-(2-аминоэтил)пирролидина вместо N,N-диметилэтилендиамина.
МС-ЖХ: МН+ = 370,1; время удерживания = 8,2 мин.
Соединения примеров 123-127 получают способом, аналогичным описанному для примера 101.
Пример 123: смесь 2-(4-хлорфенил)-5-{[2-(диметиламино)этил]амино}-1,3-бензотиазол-4,7-диона и 2-(4-хлорфенил)-6-{[2-(диметиламино)этил]амино}-1,3-бензотиазол-4,7-диона
МС-ЖХ: МН+ = 362,07; время удерживания = 8,11 и 8,20 мин.
Пример 124: смесь 2-(4-хлорфенил)-5-[(2-пирролидин-1-илэтил)амино]-1,3-бензотиазол-4,7-диона и 2-(4-хлорфенил)-6-[(2-пирролидин-1-илэтил)амино]-1,3-бензотиазол-4,7-диона
МС-ЖХ: МН+ = 388,04; время удерживания = 8,23 и 8,34 мин.
Пример 125: смесь 5-{[2-(диметиламино)этил]амино}-2-(2,3,4,5-тетрафторфенил)-1,3-бензотиазол-4,7-диона и 6-{[2-(диметиламино)этил]амино}-2-(2,3,4,5-тетрафторфенил)-1,3-бензотиазол-4,7-диона
МС-ЖХ: МН+ = 400,01; время удерживания = 8,23 и 8,32 мин.
Пример 126: смесь 5-{[2-(диметиламино)этил]амино}-2-(3,4,5-трифторфенил)-1,3-бензотиазол-4,7-диона и 6-{[2-(диметиламино)этил]амино}-2-(3,4,5-трифторфенил)-1,3-бензотиазол-4,7-диона
МС-ЖХ: МН+ = 382,03; время удерживания = 8,10 и 8,19 мин.
Пример 127: смесь 5-[(2-пирролидин-1-илэтил)амино]-2-(2,4,6-трифторфенил)-1,3-бензотиазол-4,7-диона и 6-[(2-пирролидин-1-илэтил)амино]-2-(2,4,6-трифторфенил)-1,3-бензотиазол-4,7-диона
МС-ЖХ: МН+ = 408,02; время удерживания = 7,97 и 8,05 мин.
Соединения примеров 128-131 получают способом, аналогичным описанному для примера 66.
Пример 128: смесь 2-(1,3-бензодиоксол-5-ил)-5-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-диона и 2-(1,3-бензодиоксол-5-ил)-6-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-диона
Два компонента смеси можно охарактеризовать сдвигами в спектре ЯМР (400 мГц) единичного протона кольца бензоксазоледиона, которые составляют 5,35 и 5,37 м.д.
МС-ЖХ: МН+ = 356,07; время удерживания = 7,72 мин.
Пример 129: смесь 5-{[2-(диметиламино)этил]амино}-2-(4-этилфенил)-1,3-бензоксазол-4,7-диона и 6-{[2-(диметиламино)этил]амино}-2-(4-этилфенил)-1,3-бензоксазол-4,7-диона
Два компонента смеси можно охарактеризовать сдвигами в спектре ЯМР (400 мГц) единичного протона кольца бензоксазоледиона, которые составляют 5,36 и 5,38 м.д.
МС-ЖХ: МН+ = 340,18; время удерживания = 8,24 мин.
Пример 130: смесь 2-(4-этилфенил)-5-[(2-пирролидин-1-илэтил)амино]-1,3-бензоксазол-4,7-диона и 2-(4-этилфенил)-6-[(2-пирролидин-1-илэтил)амино]-1,3-бензоксазол-4,7-диона
Два компонента смеси можно охарактеризовать сдвигами в спектре ЯМР (400 мГц) единичного протона кольца бензоксазоледиона, которые составляют 5,35 и 5,36 м.д.
МС-ЖХ: МН+ = 366,15; время удерживания = 8,34 мин.
Пример 131: смесь 5-{[2-(диметиламино)этил]амино}-2-(2-фтор-6-метоксифенил)-1,3-бензоксазол-4,7-диона и 6-{[2-(диметиламино)этил]амино}-2-(2-фтор-6-метоксифенил)-1,3-бензоксазол-4,7-диона
Два компонента смеси можно охарактеризовать сдвигами в спектре ЯМР (400 мГц) единичного протона кольца бензоксазоледиона, которые составляют 5,39 и 5,40 м.д.
МС-ЖХ: МН+ = 360,09; время удерживания = 7,67 мин.
Фармакологическое изучение соединений по изобретению
Протоколы тестов
i) Определение фосфатазной активности очищенного рекомбинантного фермента Cdc25C
Фосфатазную активность белка МВР-Сdc25C определяли дефосфорилированием 3-О-метилфлуоресцеинфосфата (OMFP) с превращением в 3-О-метилфлуоресцеин (OMF) при определении по флуоресценции продукта реакции при 475 нм. С помощью данного теста можно идентифицировать ингибиторы рекомбинантного фермента cdc25. Получение гибридного белка МВР-Сdc25C описано в заявке на патент РСТ WO 01/44467.
Реакцию проводят в 384-луночном планшете в конечном объеме 50 мкл. Белок МВР-Сdc25C (полученный, как описано выше) хранили в следующем элюирующем буфере: 20 мМ Трис-HCl, рН 7,4; 250 мМ NaCl; 1 мМ ЭДТА; 1 мМ дитиотреитола (DTT); 10 мМ мальтозы. Его разбавляли до концентрации 60 мкМ в следующем буфере для реакции: 50 мМ Трис-HCl, рН 8,2; 50 мМ NaCl; 1 мМ DTT; 20% глицерина. Определение фона проводили с буфером без добавления фермента. Продукты тестировали в уменьшающихся концентрациях, начиная с 40 мкМ. Реакцию инициировали путем добавления раствора OMFP при конечной концентрации 500 мкМ (полученного экстемпоро из 12,5 мМ исходного раствора в 100% ДМСО (Sigma #M2629)). Через 4 ч при 30°С в одноразовых 384-луночных планшетах определяли флуоресценцию при 475 нм с использованием ридера для планшетов Victor2 (EGG-Wallac). Определяли 50% ингибирующую концентрацию ферментативной реакции по результатам трех независимых опытов. Для анализа линейной регрессии брали значения, находящиеся в линейной части сигмоидальной кривой.
ii) Определение тирозинфосфатазной активности фермента CD45
Определение тирозинфосфатазной активности CD45 основано на дефосфорилировании пептида рр60c-src под действием CD45. Для определения использовали только цитоплазматический домен очищенного человеческого фермента CD45 (аминокислоты 584-1281, молекулярная масса 95 kDa), экспрессированный в дрожжевой экспрессирующей системе. Субстратом является синтетический пептид на основе последовательности отрицательного регуляторного домена рр60c-src. Высвобождаемый фосфат определяют с помощью малахитового зеленого реагента.
Реакцию проводят в 384-луночных планшетах при конечном объеме 20 мкл. Субстрат рр60c-src (P-301, BIOMOL, Plymouth Meeting, PA, USA) разбавляли до концентрации 925 мкМ следующим буфером для реакции: 50 мМ Hepes, рН 7,2; 1 мМ ЭДТА; 1 мМ дитиотреитола (DTT); 0,05% поверхностно-активного вещества NP-40. Конечная концентрация субстрата равнялась 185 мкМ. Испытываемые соединения тестировали в пределах уменьшающихся концентраций, начиная со 160 мкМ. Реакцию начинали добавлением CD45 (SE-135, BIOMOL, Plymouth Meeting, PA, USA) при 15 U/мкл (1 U = 1 пмоль/мин), разбавленного в буфере для реакции. Конечная концентрация фермента равняется 1,75 U/мкл. После инкубации в течение 1 ч при 30°С добавляют зеленый реагент Biomol (AK-111, BIOMOL, Plymouth Meeting, PA, USA) в объеме 50 мкл/лунку. Через 20-30 мин, в течение периода, когда развивается окраска, определяли поглощение при 620 нм с использованием ридера для планшетов Victor2 (EGG-Wallac). Определяли 50% ингибирующую концентрацию ферментативной реакции по результатам трех независимых опытов.
iii) Характеристика антипролиферативной активности
В качестве примера оценивали влияние обработки соединениями из примеров, описанных выше, на двух человеческих клеточных линиях Mia-Paca2 и DU145. Клеточную линию DU145 (клетки злокачественной опухоли простаты человека) и Mia-Paca2 (клетки злокачественной опухоли поджелудочной железы человека) получали из Американской коллекции тканевых культур (Rockville, Maryland, USA). Клетки, находящиеся в 80 мкл среды Игла, модифицированной по способу Дульбекко (Gibco-Brl, Cergy-Pontoise, Франция) с добавлением 10% фетальной телячьей сыворотки, инактивированной нагреванием (Gibco-Brl, Cergy-Pontoise, Франция), 50000 единиц/л пенициллина и 50 мг/л стрептомицина (Gibco-Brl, 10378-057, Cergy-Pontoise, Франция) и 2 мМ глутамина ((Gibco-Brl, Cergy-Pontoise, Франция), высевали в 96-луночные планшеты на 0 день. На 1 день клетки обрабатывали в течение 96 ч каждым из тестируемых соединений в возрастающих концентрациях до 10 мкМ. В конце данного периода количественно оценивали пролиферацию клеток с помощью колориметрического теста, основанного на расщеплении соли тетразолия WST1 под действием митохондриальных дегидрогеназ в живых клетках, что приводит к образованию формазана (Boehringer Mannheim, Meylan, Франция). Данные тесты проводят в двух параллельных исследованиях с 8 определениями на каждую тестируемую концентрацию. Для каждого тестируемого соединения для анализа линейной регрессии отбирали значения, находящиеся в линейной части сигмоидальной кривой и использовали для установления ингибирующей концентрации IC50. Продукты солюбилизировали в диметилсульфоксиде (ДМСО) при 10-2 М и использовали в культуре с конечной концентрацией ДМСО, равной 0,1%.
Результаты тестов
а) Соединения примеров 1-98, 101-104 и 107-115 имели значения CI50 ниже или равные 10 мкМ в отношении фосфатазной активности очищенного рекомбинантного фермента Сdc25C.
b) Соединения примеров 1-5 имели значения CI50 ниже или равные 10 мкМ в отношении тирозинфосфатазной активности фермента СD45.
с) Соединения примеров 1-9, 11, 14-34, 36-53, 55-58, 60-98 и 101-115 имели значения CI50 ниже или равные 10 мкМ в отношении пролиферации клеток линии Mia-Paca2.
d) Соединения примеров 1-9, 11, 14-34, 36-53, 55-58, 60-98 и 101-115 имели значения CI50 ниже или равные 10 мкМ в отношении пролиферации клеток линии DU-145.
Результаты испытаний соединения, полученного в примере 2 (кодовое название BN 82685)
Регуляторы клеточного цикла, такие как CDC25 фосфатазы, являются потенциальными мишенями для разработки новых противоопухолевых лекарственных средств. Заявитель представляет данные по идентификации и характеристике BN82685, ингибитора CDC25 на основе хинона, который является активным in vitro и in vivo. BN82685 ингибирует рекомбинантные CDC25A, В. и С фосфатазы in vitro. Он ингибирует рост клеточных линий опухолей человека с IC50 в субмикромолярном диапазоне, независимо от их устойчивости к действию химиотерапевтических средств. Этот ингибирующий эффект является необратимым в отношении как очищенного фермента CDC25 in vitro, так и в отношении пролиферации опухолевых клеток. Специфичность BN82685 в отношении CDC25 фосфатаз показана увеличением циклин-зависимых киназ 1 тирозин 15 фосфорилирования, путем реверсии индуцирующего митоз эффекта гиперэкспрессии CDC25B в клетках HeLa, и за счет недостаточного ингибирующего рост эффекта в исследовании, основанном на использовании СDС25-независимой модели делящихся дрожжей. Наконец, при пероральном BN82685 показано ингибирование роста опухоли поджелудочной железы человека Mia РаСа-2, ксенотрансплантированной бестимусным мышам «nude». Следовательно, BN82685 является перспективным новым соединением, нацеленным на CDC25, которое поддерживает интерес к ингибированию этих ферментов как стратегии противоопухолевой терапии [Mol Cancer Ther 2005: 4(9): 1378-87).
Было исследовано действие BN82685 в отношении ингибирования роста клеточных линий человека. Ингибирование роста указанных клеточных линий для гидрохлоридных и бензоатных солей изучали с помощью анализа клеточной пролиферации WST1. Полученные значения IC50 (в наномолях) рассчитывали по меньшей мере по двум независимым экспериментам с восьмью определениями на тестируемую концентрацию. Все данные сведены в таблицу 2. В таблице - ND не определено.
Также была показана активность BN82685 в отношении ингибирования клеточной пролиферации in vitro.
Действие BN82685 либо в форме его гидрохлоридной соли, либо бензоатной соли на клеточную пролиферацию оценивали in vitro на нескольких нормальных и опухолевых клеточных линиях человека (таблица 2). Всякий раз, когда обе соли тестировали параллельно, гидрохлоридная и бензоатная соль демонстрировали эквивалентную активность в отношении клеточной пролиферации. Все изучаемые клеточные линии были чувствительны к BN82685 в интервале от 250 нмоль/л до 1 мкмоль1/л. Наиболее чувствительными клеточными линиями были DU-145, Mia РаСа-2 и высокоагрессивная метастазирующая меланомная клеточная линия А2058 с IC50 90, 118 и 134 нмоль/л, соответственно, и наименее чувствительными клетками были нормальные фибробласты IMR-90 с IC50 1 мкмоль/л. BN82685 был активным как в отношении первичной опухоли толстой кишки - линия SW480, так и в отношении его метастазирующей клеточной линии SW620. Не было подтверждения явной корреляции между in vitro IC50 и гормонально-зависимого статуса любой из тестируемых клеточных линий, в том числе MCF-7, MDA-MB231, ВТ20 и T47D. Все эти линии демонстрировали сходную чувствительность к BN82685 (таблица 2).
Также заявитель обнаружил, что BN82685 был одинаково активным в отношении клеточной линии острого промиелоцитарного лейкоза HL60 и полученных от нее клеточных линий, устойчивых к цитотоксическим лекарственным средствам, экспрессирующих белок множественной лекарственной устойчивости или Р-гликопротеин, который делает их устойчивыми к даунорубицину и адриамицину, соответственно. Подобным образом, BN82685 был активным в отношении клеток HL60 клеток, устойчивых к митоксантрону и в отношении клеток лимфобластного лейкоза CCRF, независимо от их статуса устойчивости к этопозиду (таблица 3).
Исследовано также транзиторное ингибирование роста опухолевых клеток человека in vivo, ксенотрансплантированных мышам «nude».
Клеточную линию опухоли поджелудочной железы человека Mia РаСа-2 имплантировали подкожно мышам «nude». По достижении объема полученных в результате опухолей около 75 мм3 начинали лечение BN82685 путем перорального введения в дозе либо 10, либо 15 мг/кг, дважды в день в течение 2 дней, с последующими 5 днями без лечения, с тремя циклами лечения. Во время лечения наблюдалась очень ограниченная потеря массы тела с полным и быстрым восстановлением при прекращении. Это лечение приводило к стабилизации роста опухолей Mia РаСа-2 в течение первых 10 дней лечения, после чего опухоли снова начинали расти (см. чертеж).
Что касается примера получения фармацевтической композиции, заявитель просит принять следующее.
Фармацевтические композиции по настоящему изобретению получены традиционным способом, а именно путем смешения активного ингредиента (например, соединения по примеру 2, причем можно указать любое из полученных соединений) и инертного носителя, которым является фосфат кальция, стеарат магния, тальк, сахар, лактоза, желатин метилцеллюлоза, поливинилпирролидон. Кроме того, могут быть добавлены улучшители вкуса, сиропы малины, клубники и т.д. Причем количество активного ингредиента составляет от 0,1 мг до 10 г на стандартную дозу (например, таблетку). Это зависит от состояния пациента, возраста и назначения врача. Если готовят таблетку, смесь компонентов таблетируют в специальной таблетирующей машине.
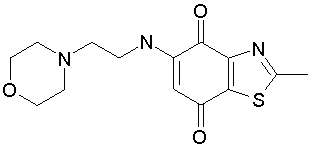
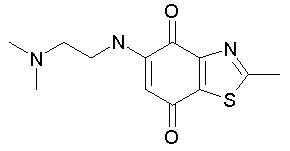
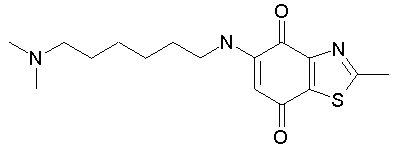
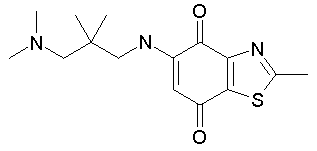
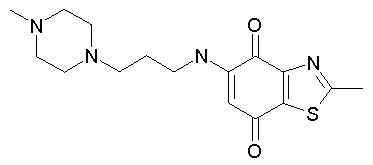
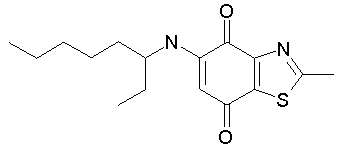
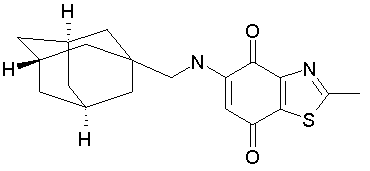
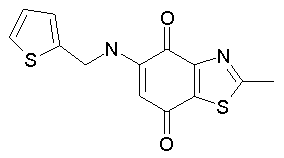
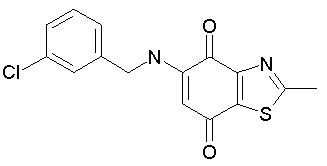
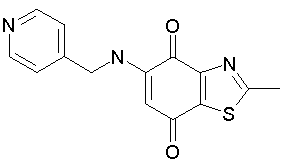
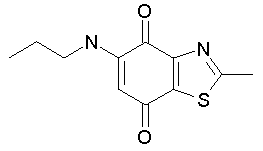
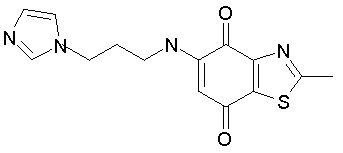
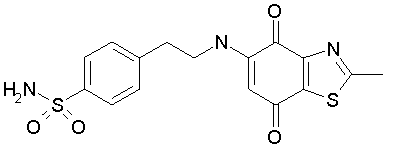
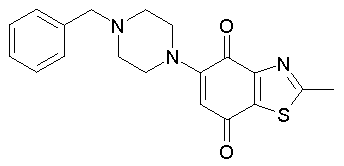
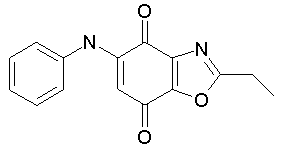
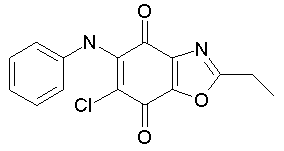
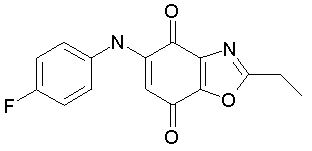
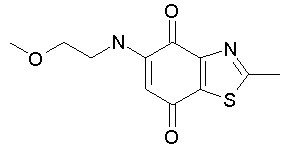
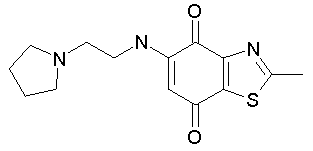
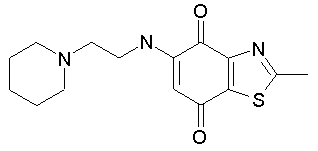
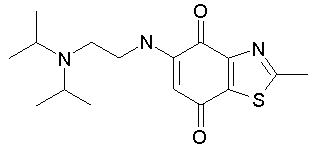
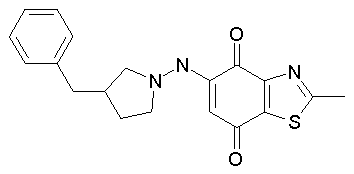
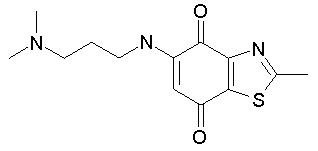
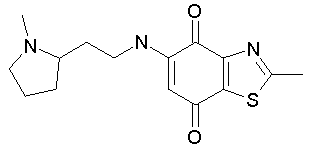
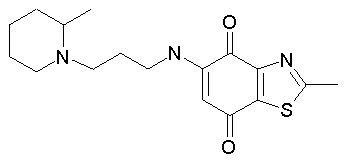
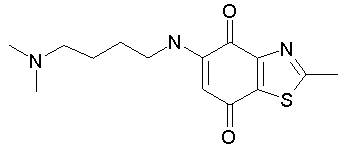
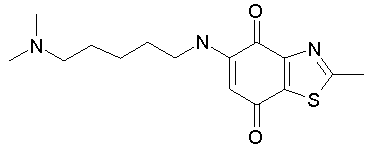
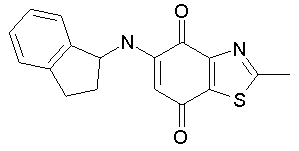
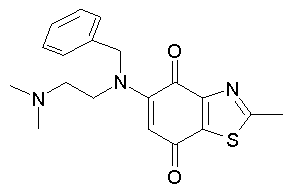
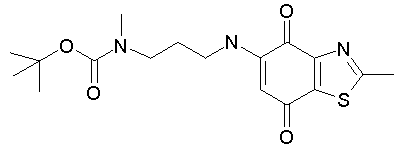
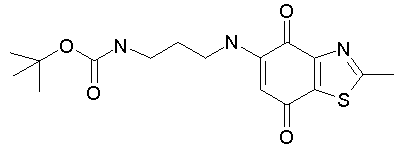
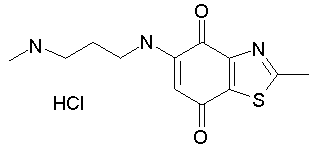
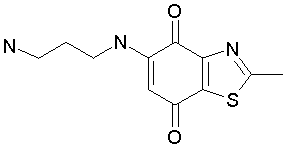
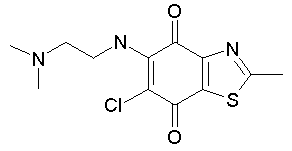
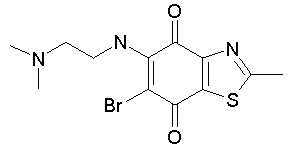
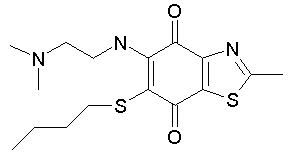
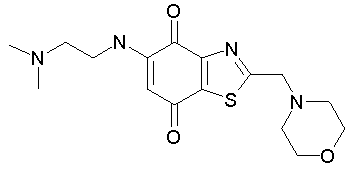
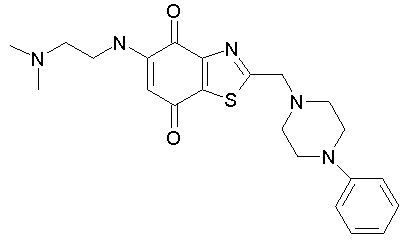
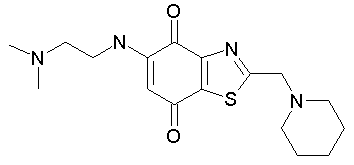
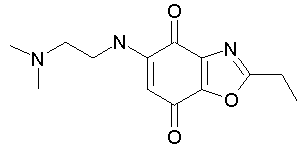
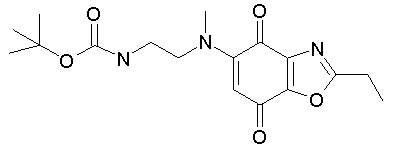
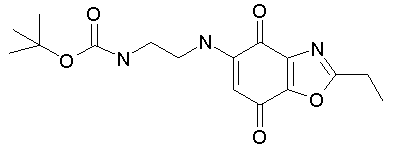
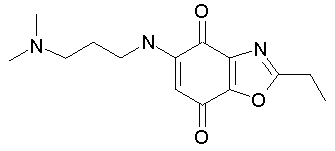
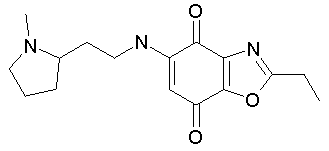
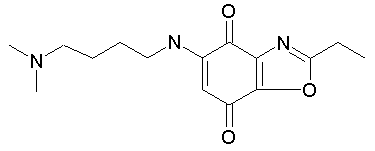
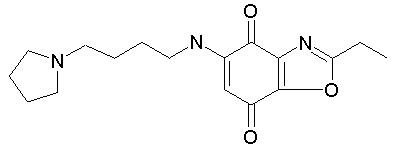
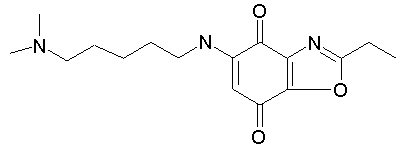
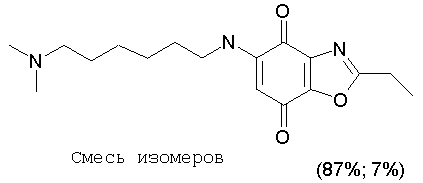
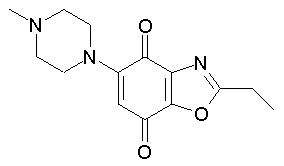
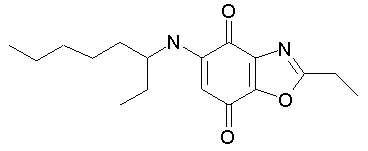
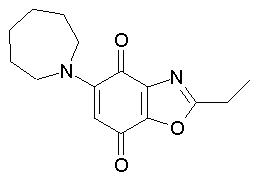
Смесь изомеров (69%; 22%)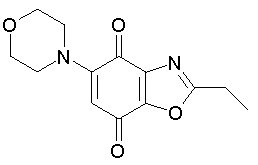
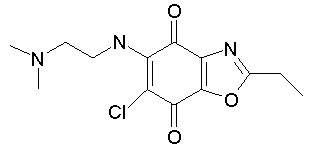
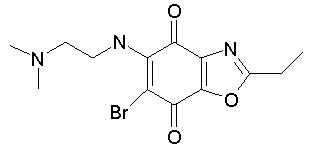
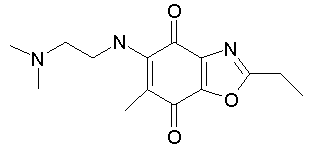
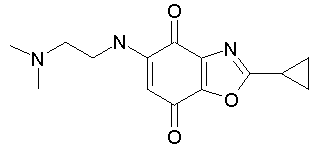
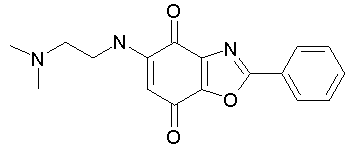
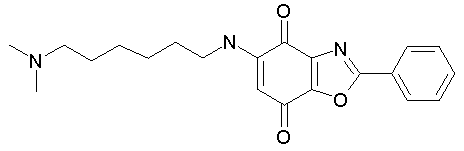
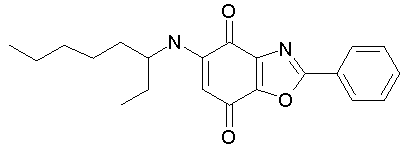
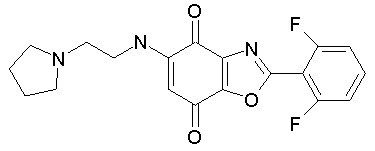
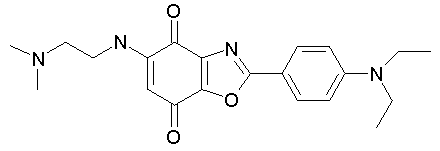
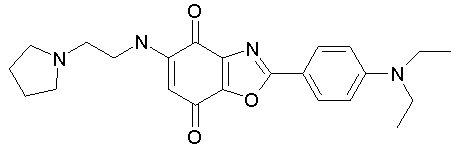
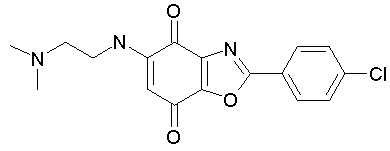
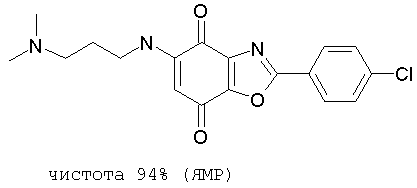
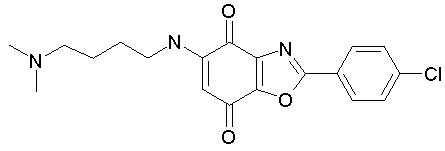
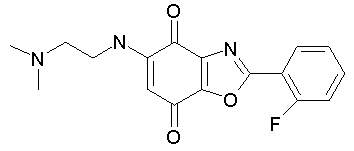
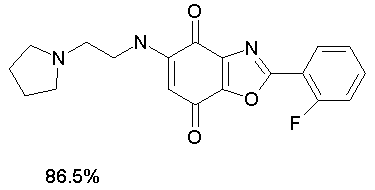
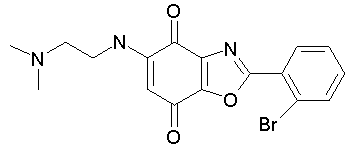
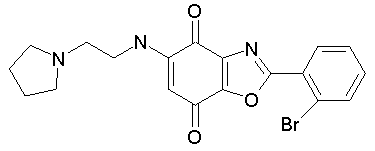
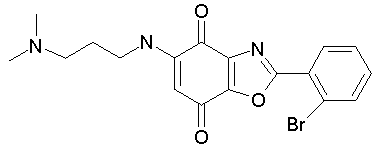
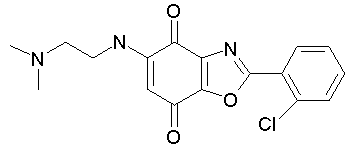
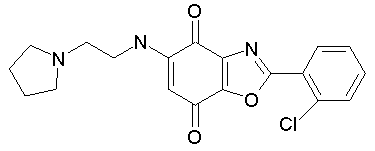
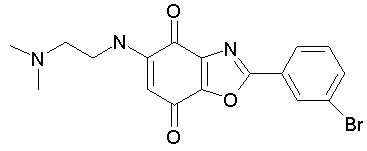
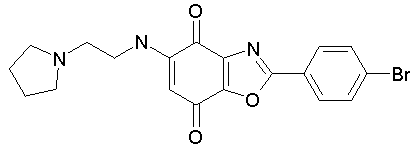
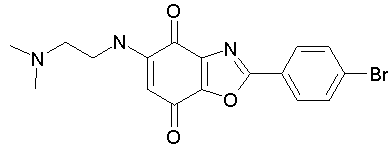
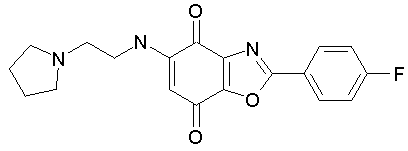
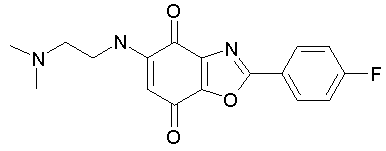
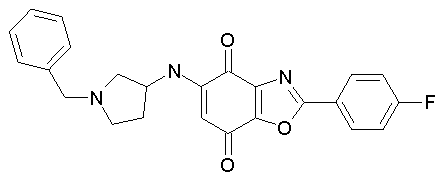
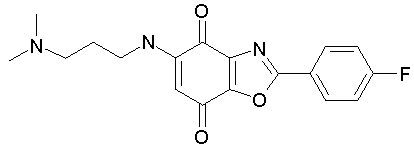
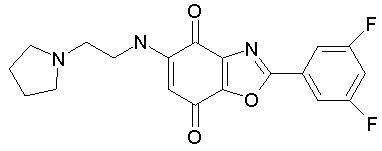
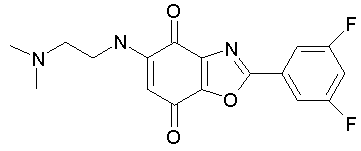
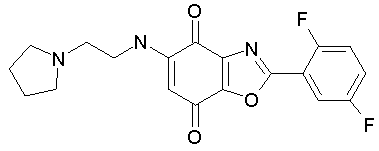
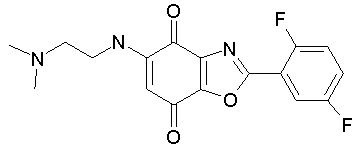
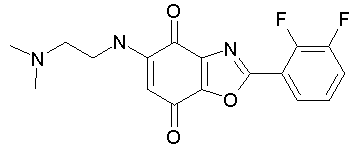
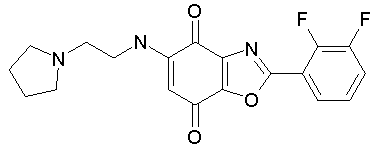
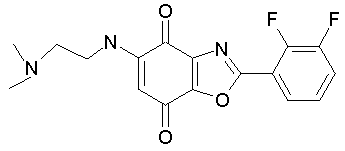
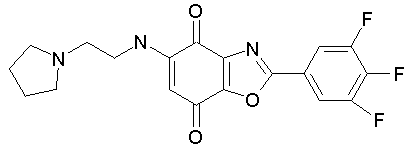
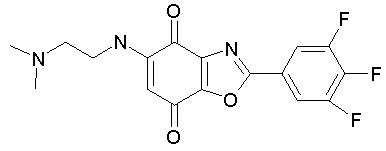
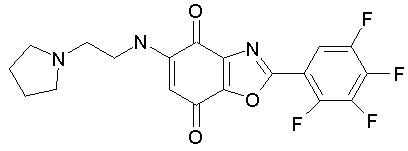
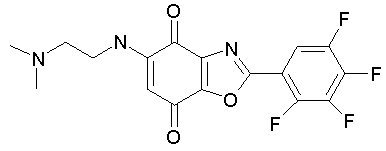
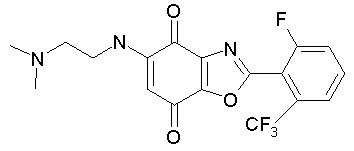
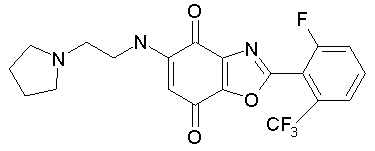
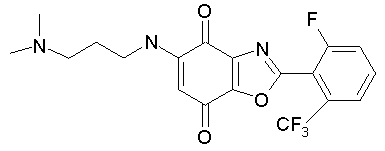
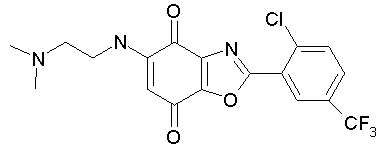
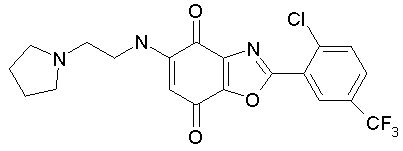
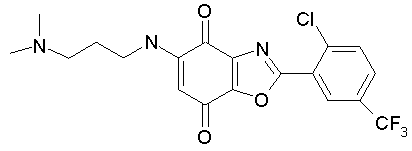
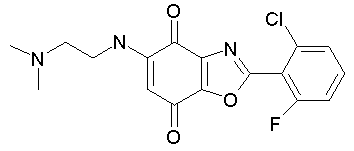
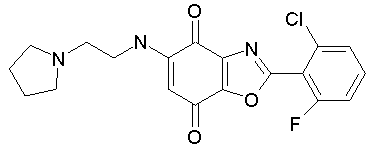
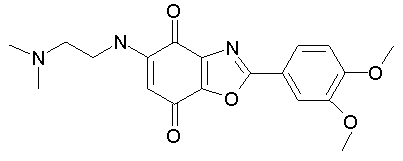
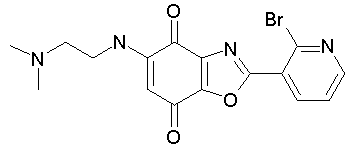
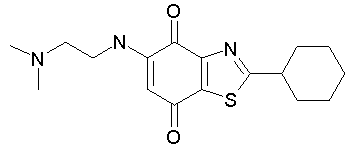
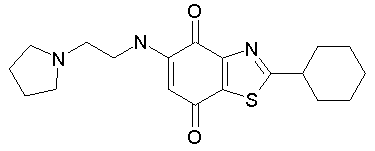
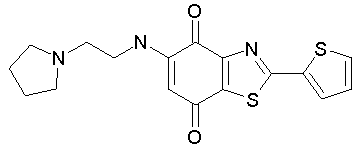
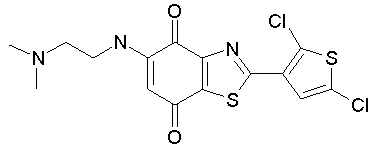
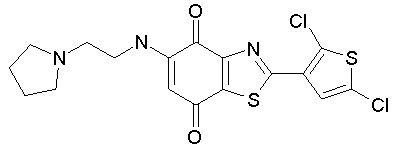
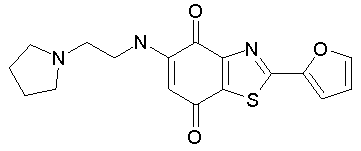
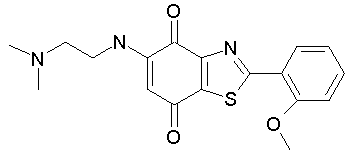
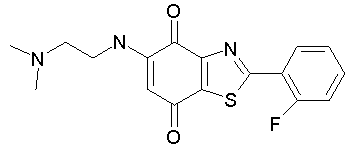
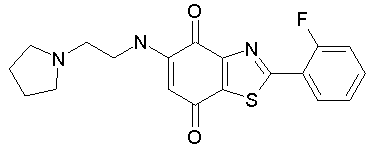
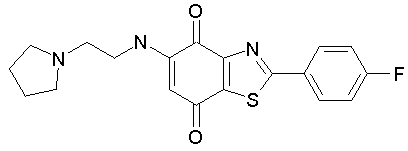
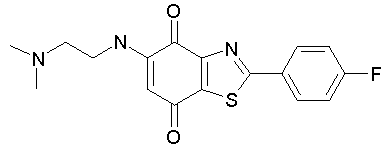
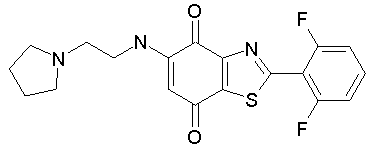
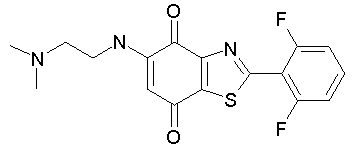
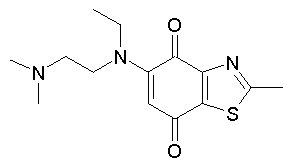
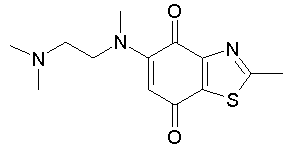
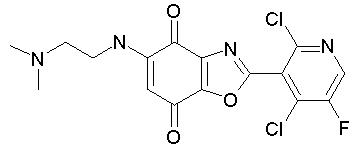
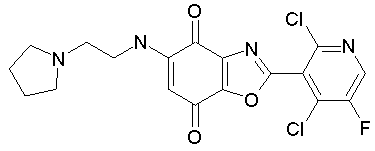
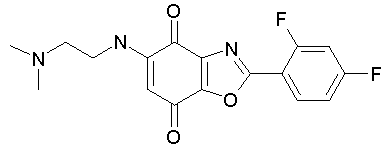
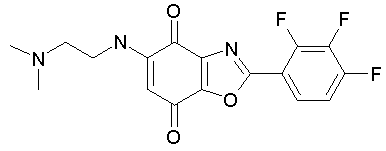
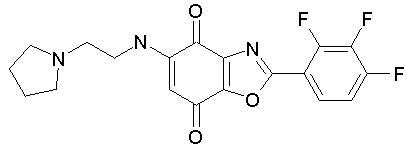
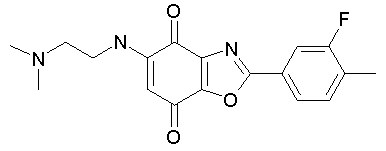
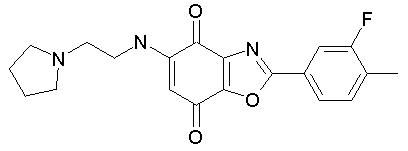
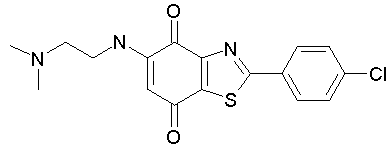
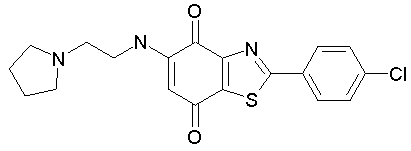
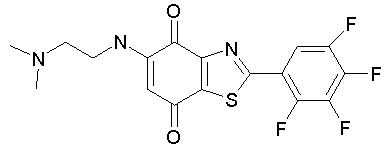
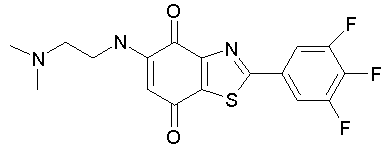
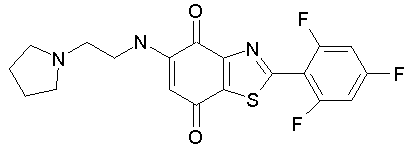
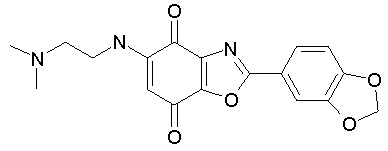
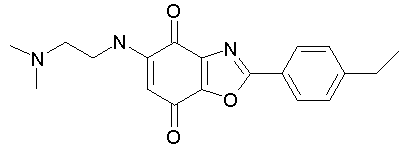
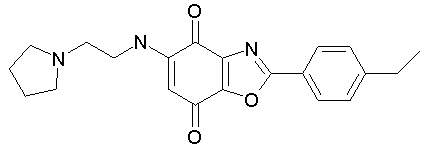
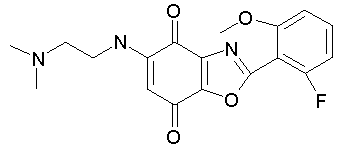
BN82685 ингибирует рост клеточных линий человека
BN82 685 ингибирует рост клеточных линий человека, устойчивых к цитотоксическим лекарственным средствам
Пример получения композиции, мг:
Активный компонент композиции (соединение примера 2) тщательно смешивают с аддитивами, указанными выше, и смесь либо расфасовывают в виде порошка, либо готовят таблетки, используя машину для прессования таблеток. Стандартная доза лекарственного средства содержит от 0,1 мг до 10 г активного компонента.
| название | год | авторы | номер документа |
|---|---|---|---|
| ИНГИБИТОРЫ ФОСФАТАЗ Сdc25 | 2005 |
|
RU2395510C2 |
| ПРОИЗВОДНЫЕ ПЯТИЧЛЕННЫХ ГЕТЕРОЦИКЛОВ, СПОСОБ ИХ ПОЛУЧЕНИЯ И ИХ ПРИМЕНЕНИЕ В КАЧЕСТВЕ ЛЕКАРСТВЕННЫХ СРЕДСТВ | 2000 |
|
RU2380362C2 |
| ПРОИЗВОДНЫЕ ПЯТИЧЛЕННЫХ ГЕТЕРОЦИКЛОВ, СПОСОБ ИХ ПОЛУЧЕНИЯ И ИХ ПРИМЕНЕНИЕ В КАЧЕСТВЕ ЛЕКАРСТВЕННЫХ СРЕДСТВ | 2009 |
|
RU2530882C2 |
| ПРОИЗВОДНЫЕ ПЯТИЧЛЕННЫХ ГЕТЕРОЦИКЛОВ, СПОСОБ ИХ ПОЛУЧЕНИЯ И ИХ ПРИМЕНЕНИЕ В КАЧЕСТВЕ ЛЕКАРСТВЕННЫХ СРЕДСТВ | 2000 |
|
RU2271355C2 |
| ИНГИБИТОРЫ ФОСФАТАЗ cdc25 | 2001 |
|
RU2285521C2 |
| СПОСОБЫ И КОМПОЗИЦИИ ДЛЯ УЛУЧШЕНИЯ КОГНИТИВНЫХ ФУНКЦИЙ | 2012 |
|
RU2665021C2 |
| НОВЫЕ ПРОИЗВОДНЫЕ АРИЛИМИДАЗОЛА, ИХ ПРЕПАРАТЫ И ИХ ТЕРАПЕВТИЧЕСКИЕ ПРИМЕНЕНИЯ | 2003 |
|
RU2323216C2 |
| ЗАМЕЩЕННЫЕ ДИКЕТОПИПЕРАЗИНЫ КАК АНТАГОНИСТЫ ОКСИТОЦИНА | 2002 |
|
RU2303032C2 |
| ЗАМЕЩЕННЫЕ МЕТИЛФЕНИЛКЕТОНЫ, ПРИГОДНЫЕ ДЛЯ ИСПОЛЬЗОВАНИЯ В КАЧЕСТВЕ ИНГИБИТОРОВ PDE4 | 2007 |
|
RU2493149C2 |
| ПРОИЗВОДНЫЕ 5-ЧЛЕННЫХ ГЕТЕРОЦИКЛОВ, ИХ ПОЛУЧЕНИЕ И ПРИМЕНЕНИЕ В КАЧЕСТВЕ ЛЕКАРСТВЕННЫХ СРЕДСТВ | 2002 |
|
RU2288224C2 |
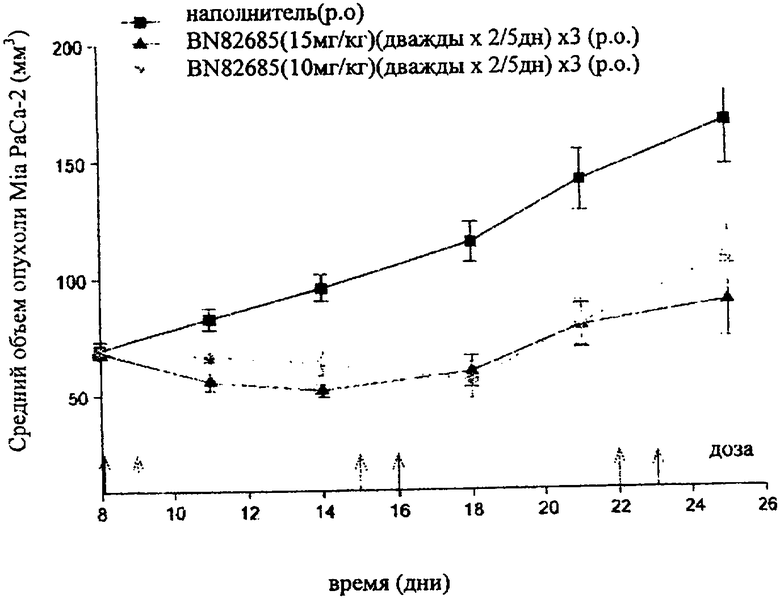
Изобретение относится к области фармакологии и медицины и касается применения соединений общей формулы I для получения лекарственного средства для ингибирования сdc25-фосфатаз и/или CD45-фосфатазы, лекарственного средства для ингибирования cdc25-фосфатаз или СD45-фосфатазы, фармацевтических композиций для ингибирования cdc25-фосфатаз или СD45-фосфатазы; изобретение касается также соединений формулы 1 и обеспечивает высокую степень ингибирования cdc25-фосфатаз и/или СD45-фосфатазы. 6 н. и 16 з.п. ф-лы, 1 ил., 3 табл.
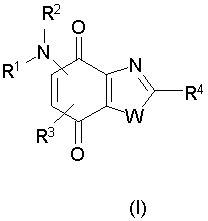
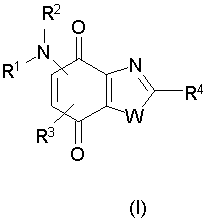
в которой
R1 представляет атом водорода или алкил, алкоксиалкил, алкилтиоалкил, циклоалкил, -(СН2)-X-Y, -(СН2)-Z-NR5R6 или
-CHR35R36, в котором R35 и R36 образуют вместе с атомом углерода, к которому они присоединены, инданил или тетралинил, или также R35 и R36 образуют вместе с атомом углерода, к которому они присоединены, насыщенный гетероцикл, содержащий 5-7 членов и 1-2 гетероатома, выбранных из О, N и S, где атомы азота указанного гетероцикла необязательно замещены радикалами, выбранными из алкила и бензила,
R1 также может, когда W является О, представлять собой карбоциклический арил, необязательно замещенный 1-3 заместителями, независимо выбранными из атома галогена и алкила, галогеналкила или алкокси,
X представляет связь или нормальный, или разветвленный алкилен, содержащий 1-5 атомов углерода,
Y представляет насыщенную углеродсодержащую циклическую систему, содержащую 1-3 конденсированных кольца, независимо выбранных из колец с 3-7 членами, или Y представляет насыщенный гетероцикл, содержащий 1-2 гетероатома, независимо выбранных из О, N или S, и соединенный с радикалом X посредством N- или СН-члена, где указанный насыщенный гетероцикл, кроме того, содержит 2-6 дополнительных членов, независимо выбранных из -CHR7-, -СО-, -NR8-, -О- и -S-, где R7 представляет атом водорода или алкил, и R8 представляет атом водорода или алкил, или аралкил, или также Y представляет карбоциклический или гетероциклический арил, необязательно замещенный 1-3 заместителями, независимо выбранными из группы, состоящей из атома галогена, алкила, галогеналкила, алкокси, галогеналкокси, гидрокси, нитро, циано, фенила, SO2NHR9 и NR10R11, где R9 представляет атом водорода или алкил, или фенил, и R10 и R11 независимо представляют алкил,
Z представляет связь или нормальный, или разветвленный алкилен, содержащий 1-5 атомов углерода,
R5 и R6 независимо выбраны из атома водорода, алкила, аралкила или -(СН2)n-ОН, в котором n представляет целое число от 1 до 6,
или R5 представляет алкоксикарбонил, галогеналкоксикарбонил или аралкоксикарбонил, и R6 представляет атом водорода или метил,
или также R5 и R6 образуют вместе с атомом азота гетероцикл с 4-7 членами, содержащий 1-2 гетероатома, где члены, необходимые для замыкания гетероцикла, независимо выбраны из -CR12R13-, -O-, -S- и -NR14, где R12 и R13 независимо представляют, когда они имеются, атом водорода или алкил, и R14 представляет атом водорода или алкил, или аралкил, или также R14 представляет фенил, необязательно замещенный 1-3 заместителями, независимо выбранными из атома галогена и алкила, или алкокси,
R2 представляет атом водорода или алкил, или аралкил,
или также R1 и R2 образуют вместе с атомом азота гетероцикл с 4-8 членами, содержащий 1-2 гетероатома, где члены, необходимые для замыкания гетероцикла, независимо выбраны из -CR15R16-, -O-, -S- или -NR17, где R15 и R16 независимо представляют, когда они имеются, атом водорода или алкил, и R17 представляет атом водорода или алкил, или аралкил;
R3 представляет атом водорода, атом галогена или алкил, галогеналкил, алкокси или алкилтио;
R4 представляет алкил, циклоалкил, циклоалкилалкил, циано, амино, -CH2-COOR18, -CH2-CO-NR19R20 или -CH2-NR21R22, или R4 представляет карбоциклический или гетероциклический арил, необязательно замещенный 1-4 заместителями, независимо выбранными из атома галогена и алкила, галогеналкила, алкокси, галогеналкокси или NR37R38, или также R4 представляет фенил, имеющий два заместителя, которые вместе образуют метилендиокси или этилендиокси,
R18 представляет атом водорода или алкил,
R19 представляет атом водорода, алкил или аралкил, арильная группа которого необязательно замещена 1-3 заместителями, независимо выбранными из группы, состоящей из атома галогена, алкила, галогеналкила, алкокси, галогеналкокси, гидрокси, нитро, циано, фенила, SO2NHR23 и NR24R25, где R23 представляет атом водорода или алкил, или фенил, и R24 и R25 независимо представляют алкил,
R20 представляет атом водорода или алкил,
или также R19 и R20 образуют вместе с атомом азота гетероцикл с 4-7 членами, содержащий 1-2 гетероатома, где члены, необходимые для замыкания гетероцикла, независимо выбраны из -CR26R27-, -O-, -S- или -NR28, где R26 и R27 независимо представляют, когда они имеются, атом водорода или алкил, и R28 представляет атом водорода или алкил, или аралкил, или также R28 представляет фенил, необязательно замещенный 1-3 заместителями, независимо выбранными из атома галогена и алкила, или алкокси,
R21 представляет атом водорода, алкил или аралкил, арильная группа которого необязательно замещена 1-3 заместителями, независимо выбранными из группы, состоящей из атома галогена, алкила, галогеналкила, алкокси, галогеналкокси, гидрокси, нитро, циано, фенила, SO2NHR29 и NR30R31, где R29 представляет атом водорода или алкил, или фенил, и R30 и R31 независимо представляют алкил,
R22 представляет атом водорода или алкил,
или также R21 и R22 образуют вместе с атомом азота гетероцикл с 4-7 членами, содержащий 1-2 гетероатома, где члены, необходимые для замыкания гетероцикла, независимо выбраны из -CR32R33-, -O-, -S- или -NR34, где R32 и R33 независимо представляют, когда они имеются, атом водорода или алкил, и R34 представляет атом водорода, алкил или аралкил, или также R34 представляет фенил, необязательно замещенный 1-3 заместителями, независимо выбранными из атома галогена и алкила, или алкокси,
R37 и R38 независимо выбраны из атома водорода и алкила, или R37 и R38 образуют вместе с атомом азота гетероцикл с 4-7 членами, содержащий 1-2 гетероатома, где члены, необходимые для замыкания гетероцикла, независимо выбраны из -CR39R40-, -O-, -S- или -NR41, где R39 и R40 независимо представляют, когда они имеются, атом водорода или алкил, и R41 представляет атом водорода или алкил; и
W представляет О или S;
или фармацевтически приемлемой соли соединения общей формулы (I) для получения лекарственного средства, предназначенного для ингибирования cdc25-фосфатаз и/или CD45-фосфатазы.
R1 представляет алкил, циклоалкил, алкоксиалкил, -(CH2)-X-Y, -(СН2)-Z-NR5R6 или -CHR35R36, и R2 представляет атом водорода или метил, этил или бензил, или также R1 и R2 образуют вместе с атомом азота гетероцикл с 4-8 членами, содержащий 1-2 гетероатома, где члены, необходимые для замыкания гетероцикла, независимо выбраны из -СН2-, -О- и -NR17, где R17 представляет метил или бензил;
R3 представляет атом водорода, атом галогена или алкил, алкокси или алкилтио;
R4 представляет алкил, -CH2-COOR18 или -CH2-CO-NR19R20, или -CH2-NR21R22, или также карбоциклический или гетероциклический арил, необязательно замещенный 1-4 заместителями, независимо выбранными из атома галогена и алкила, галогеналкила, алкокси или NR37R38.
2-метил-5-{[2-(4-морфолинил)этил]амино}-1,3-бензотиазол-4,7-дион;
5-{[2-(диметиламино)этил]амино}-2-метил-1,3-бензотиазол-4,7-дион;
5-{[6-(диметиламино)гексил]амино}-2-метил-1,6-бензотиазол-4,7-дион;
5-{[3-(диметиламино)-2,2-диметилпропил]амино}-2-метил-1,3-бензотиазол-4,7-дион;
2-метил-5-{[3-(4-метил-1-пиперазинил)пропил]амино}-1,3-бензотиазол-4,7-дион;
5-[(1-этилгексил)амино]-2-метил-1,3-бензотиазол-4,7-дион;
5-[(1-адамантилметил)амино]-2-метил-1,3-бензотиазол-4,7-дион;
2-метил-5-[(2-тиенилметил)амино]-1,3-бензотиазол-4,7-дион;
5-[(3-хлорбензил)амино]-2-метил-1,3-бензотиазол-4,7-дион;
2-метил-5-[4-пиридинилметил)амино]-1,3-бензотиазол-4,7-дион;
2-метил-5-(пропиламино)-1,3-бензотиазол-4,7-дион;
5-{[3-(1Н-имидазол-1-ил)пропил]амино}-2-метил-1,3-бензотиазол-4,7-дион;
4-{2-[(2-метил-4,7-диоксо-4,7-дигидро-1,3-бензотиазол-5-ил)амино]этил}бензолсульфонамид;
5-(4-бензил-1-пиперазинил)-2-метил-1,3-бензотиазол-4,7-дион;
или его фармацевтически приемлемую соль.
5-[(2-метоксиэтил)амино]-2-метил-1,3-бензотиазол-4,7-дион;
2-метил-5-[(2-пирролидин-1-илэтил)амино]-1,3-бензотиазол-4,7-дион;
2-метил-5-[(2-пиперидин-1-илэтил)амино]-1,3-бензотиазол-4,7-дион;
5-{[2-(диизопропиламино)этил]амино}-2-метил-1,3-бензотиазол-4,7-дион;
5-[(1-бензилпирролидин-3-ил)амино]-2-метил-1,3-бензотиазол-4,7-дион;
5-{[3-(диметиламино)пропил]амино}-2-метил-1,3-бензотиазол-4,7-дион;
2-метил-5-{[2-(1-метилпирролидин-2-ил)этил]амино}-1,3-бензотиазол-4,7-дион;
2-метил-5-{[3-(2-метилпиперидин-1-ил)пропил]амино}-1,3-бензотиазол-4,7-дион;
5-{[4-(диметиламино)бутил]амино}-2-метил-1,3-бензотиазол-4,7-дион;
5-{[5-(диметиламино)пентил]амино}-2-метил-1,3-бензотиазол-4,7-дион;
5-(2,3-дигидро-1Н-инден-1-иламино)-2-метил-1,3-бензотиазол-4,7-дион;
5-{бензил[2-(диметиламино)этил]амино}-2-метил-1,3-бензотиазол-4,7-дион;
2-метил-5-{[3-(метиламино)пропил]амино}-1,3-бензотиазол-4,7-дион;
5-[(3-аминопропил)амино]-2-метил-1,3-бензотиазол-4,7-дион;
6-хлор-5-{[2-(диметиламино)зтил]амино}-2-метил-1,3-бензотиазол-4,7-дион;
6-бром-5-{[2-(диметиламино)этил]амино}-2-метил-1,3-бензотиазол-4,7-дион;
6-(бутилтио)-5-{[2-(диметиламино)этил]амино}-2-метил-1,3-бензотиазол-4,7-дион;
5-{[2-(диметиламино)этил]амино}-2-(морфолин-4-илметил)-1,3-бензотиазол-4,7-дион;
5-{[2-(диметиламино)этил]амино}-2-[(4-фенилпиперазин-1-ил)метил]-1,3-бензотиазол-4,7-дион;
5-{[2-(диметиламино)этил]амино}-2-(пиперидин-1-илметил)-1,3-бензотиазол-4,7-дион;
5-{[6-(диметиламино)гексил]амино}-2-этил-1,3-бензоксазол-4,7-дион;.
2-этил-5-(4-метилпиперазин-1-ил)-1,3-бензоксазол-4,7-дион;
2-этил-5-[(1-этилгексил)амино]-1,3-бензоксазол-4,7-дион;
5-азокан-1-ил-2-этил-1,3-бензоксазол-4,7-дион;
2-этил-5-морфолин-4-ил-1,3-бензоксазол-4,7-дион;
5-{[2-(диметиламино)зтил]амино}-2-этил-6-метил-1,3-бензоксазол-4,7-дион;
5-{[2-(диметиламино)этил]амино}-2-фенил-1,3-бензоксазол-4,7-дион;
5-{[6-(диметиламино)гексил]амино}-2-фенил-1,3-бензоксазол-4,7-дион;
2-(2,6-дифторфенил)-5-[(2-пирролидин-1-илэтил)амино]-1,3-бензоксазол-4,7-дион;
2-[4-(диэтиламино)фенил]-5-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-дион;
2-[4-(диэтиламино)фенил]-5-[(2-пирролидин-1-илэтил)амино]-1,3-бензоксазол-4,7-дион;
2-(4-хлорфенил)-5-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-дион;
2-(4-хлорфенил)-5-{[3-(диметиламино)пропил]амино}-1,3-бензоксазол-4,7-дион;
2-(4-хлорфенил)-5-{[4-(диметиламино)бутил]амино}-1,3-бензоксазол-4,7-дион;
или его фармацевтически приемлемую соль.
трет-бутил метил{3-[(2-метил-4,7-диоксо-4,7-дигидро-1,3-бензотиазол-5-ил)амино]пропил}карбамат;
трет-бутил 3-[(2-метил-4,7-диоксо-4,7-дигидро-1,3-бензотиазол-5-ил)амино]пропилкарбамат;
6-{[6-(диметиламино)гексил]амино}-2-этил-1,3-бензоксазол-4,7-дион;
2-этил-6-(4-метилпиперазин-1-ил)-1,3-бензоксазол-4,7-дион;
2-этил-6-[(1-этилгексил)амино]-1,3-бензоксазол-4,7-дион;
6-азокан-1-ил-2-этил-1,3-бензоксазол-4,7-дион;
2-этил-6-морфолин-4-ил-1,3-бензоксазол-4,7-дион;
6-{[2-(диметиламино)этил]амино}-2-фенил-1,3-бензоксазол-4,7-дион;
6-{[6-(диметиламино)гексил]амино}-2-фенил-1,3-бензоксазол-4,7-дион;
2-(2,6-дифторфенил)-6-[(2-пирролидин-1-илэтил)амино]-1,3-бензоксазол-4,7-дион;
2-[4-(диэтиламино)фенил]-6-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-дион;
2-[4-(диэтиламино)фенил]-6-[(2-пирролидин-1-илэтил)амино]-1,3-бензоксазол-4,7-дион;
2-(4-хлорфенил)-6-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-дион;
2-(4-хлорфенил)-6-{[3-(диметиламино)пропил]амино}-1,3-бензоксазол-4,7-дион;
2-(4-хлорфенил)-6-{[4-(диметиламино)бутил]амино}-1,3-бензоксазол-4,7-дион;
2-(2-фторфенил)-5-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-дион;
2-(2-фторфенил)-6-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-дион;
2-(2-фторфенил)-5-[(2-пирролидин-1-илэтил)амино]-1,3-бензоксазол-4,7-дион;
2-(2-фторфенил)-6-[(2-пирролидин-1-илэтил)амино]-1,3-бензоксазол-4,7-дион;
2-(2-бромфенил)-5-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-дион;
2-(2-бромфенил)-6-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-дион;
2-(2-бромфенил)-5-[(2-пирролидин-1-илэтил)амино]-1,3-бензоксазол-4,7-дион;
2-(2-бромфенил)-6-[(2-пирролидин-1-илэтил)амино]-1,3-бензоксазол-4,7-дион;
2-(2-бромфенил)-5-{[3-(диметиламино)пропил]амино}-1,3-бензоксазол-4,7-дион;
2-(2-бромфенил)-6-{[3-(диметиламино)пропил]амино}-1,3-бензоксазол-4,7-дион;
2-(2-хлорфенил)-5-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-дион;
2-(2-хлорфенил)-6-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-дион;
2-(2-хлорфенил)-5-[(2-пирролидин-1-илэтил)амино]-1,3-бензоксазол-4,7-дион;
2-(2-хлорфенил)-6-[(2-пирролидин-1-илэтил)амино]-1,3-бензоксазол-4,7-дион;
2-(3-бромфенил)-5-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-дион;
2-(3-бромфенил)-6-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-дион;
2-(4-бромфенил)-5-[(2-пирролидин-1-илэтил)амино]-1,3-бензоксазол-4,7-дион;
2-(4-бромфенил)-6-[(2-пирролидин-1-илэтил)амино]-1,3-бензоксазол-4,7-дион;
2-(4-бромфенил)-5-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-дион;
2-(4-бромфенил)-6-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-дион;
2-(4-фторфенил)-5-[(2-пирролидин-1-илэтил)амино]-1,3-бензоксазол-4,7-дион;
2-(4-фторфенил)-6-[(2-пирролидин-1-илэтил)амино]-1,3-бензоксазол-4,7-дион;
5-{[2-(диметиламино)этил]амино}-2-(4-фторфенил)-1,3-бензоксазол-4,7-дион;
6-{[2-(диметиламино)этил]амино}-2-(4-фторфенил)-1,3-бензоксазол-4,7-дион;
5-[(1-бензилпирролидин-3-ил)амино]-2-(4-фторфенил)-1,3-бензоксазол-4,7-дион;
6-[(1-бензилпирролидин-3-ил)амино]-2-(4-фторфенил)-1,3-бензоксазол-4,7-дион;
5-{[3-(диметиламино)пропил]амино}-2-(4-фторфенил)-1,3-бензоксазол-4,7-дион;
6-{[3-(диметиламино)пропил]амино}-2-(4-фторфенил)-1,3-бензоксазол-4,7-дион;
2-(3,5-дифторфенил)-5-[(2-пирролидин-1-илэтил)амино]-1,3-бензоксазол-4,7-дион;
2-(3,5-дифторфенил)-6-[(2-пирролидин-1-илэтил)амино]-1,3-бензоксазол-4,7-дион;
2-(3,5-дифторфенил)-5-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-дион;
2-(3,5-дифторфенил)-6-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-дион;
2-(2,5-дифторфенил)-5-[(2-пирролидин-1-илэтил)амино]-1,3-бензоксазол-4,7-дион;
2-(2,5-дифторфенил)-6-[(2-пирролидин-1-илэтил)амино]-1,3-бензоксазол-4,7-дион;
2-(2,5-дифторфенил)-5-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-дион;
2-(2,5-дифторфенил)-6-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-дион;
2-(2,3-дифторфенил)-5-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-дион;
2-(2,3-дифторфенил)-6-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-дион;
2-(2,3-дифторфенил)-5-[(2-пирролидин-1-илэтил)амино]-1,3-бензоксазол-4,7-дион;
2-(2,3-дифторфенил)-6-[(2-пирролидин-1-илэтил)амино]-1,3-бензоксазол-4,7-дион;
2-(2,3-дифторфенил)-5-{[3-(диметиламино)пропил]амино}-1,3-бензоксазол-4,7-дион;
2-(2,3-дифторфенил)-6-{[3-(диметиламино)пропил]амино}-1,3-бензоксазол-4,7-дион;
5-[(2-пирролидин-1-илэтил)амино]-2-(3,4,5-трифторфенил)-1,3-бензоксазол-4,7-дион;
6-[(2-пирролидин-1-илэтил)амино]-2-(3,4,5-трифторфенил)-1,3-бензоксазол-4,7-дион;
5-{[2-(диметиламино)этил]амино}-2-(3,4,5-трифторфенил)-1,3-бензоксазол-4,7-дион;
6-{[2-(диметиламино)этил]амино}-2-(3,4,5-трифторфенил)-1,3-бензоксазол-4,7-дион;
5-[(2-пирролидин-1-илэтил)амино]-2-(2,3,4,5-тетрафторфенил)-1,3-бензоксазол-4,7-дион;
6-[(2-пирролидин-1-илэтил)амино]-2-(2,3,4,5-тетрафторфенил)-1,3-бензоксазол-4,7-дион;
5-{[2-(диметиламино)этил]амино}-2-(2,3,4,5-тетрафторфенил)-1,3-бензоксазол-4,7-дион;
6-{[2-(диметиламино)этил]амино}-2-(2,3,4,5-тетрафторфенил)-1,3-бензоксазол-4,7-дион;
5-{[2-(диметиламино)этил]амино}-2-[2-фтор-6-(трифторметил)фенил]-1,3-бензоксазол-4,7-дион;
6-{[2-(диметиламино)зтил]амино}-2-[2-фтор-6-(трифторметил)фенил]-1,3-бензоксазол-4,7-дион;
2-[2-фтор-6-(трифторметил)фенил]-5-[(2-пирролидин-1-илэтил)амино]-1,3-бензоксазол-4,7-дион;
2-[2-фтор-6-(трифторметил)фенил]-6-[(2-пирролидин-1-илэтил)амино]-1,3-бензоксазол-4,7-дион;
5-{[3-(диметиламино)пропил]амино}-2-[2-фтор-6-(трифторметил)фенил]-1,3-бензоксазол-4,7-дион;
6-{[3-(диметиламино)пропил]амино}-2-[2-фтор-6-(трифторметил)фенил]-1,3-бензоксазол-4,7-дион;
2-[2-хлор-5-(трифторметил)фенил]-5-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-дион;
2-[2-хлор-5-(трифторметил)фенил]-6-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-дион;
2-[2-хлор-5-(трифторметил)фенил]-5-[(2-пирролидин-1-илэтил)амино]-1,3-бензоксазол-4,7-дион;
2-[2-хлор-5-(трифторметил)фенил]-6-[(2-пирролидин-1-илэтил)амино]-1,3-бензоксазол-4,7-дион;
2-[2-хлор-5-(трифторметил)фенил]-5-{[3-(диметиламино)пропил]амино}-1,3-бензоксазол-4,7-дион;
2-[2-хлор-5-(трифторметил)фенил]-6-{[3-(диметиламино)пропил]амино}-1,3-бензоксазол-4,7-дион;
2-[2-хлор-6-фторфенил]-5-{[3-(диметиламино)пропил]амино}-1,3-бензоксазол-4,7-дион;
2-[2-хлор-6-фторфенил]-6-{[3-(диметиламино)пропил]амино}-1,3-бензоксазол-4,7-дион;
2-[2-хлор-6-фторфенил]-5-[(2-пирролидин-1-илэтил)амино]-1,3-бензоксазол-4,7-дион;
2-[2-хлор-6-фторфенил]-6-[(2-пирролидин-1-илэтил)амино]-1,3-бензоксазол-4,7-дион;
2-[3,4-диметоксифенил]-5-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-дион;
2-[3,4-диметоксифенил]-6-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-дион;
2-[2-бром-3-пиридил]-5-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-дион;
2-[2-бром-3-пиридил]-6-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-дион;
2-циклогексил-5-[(2-пирролидин-1-илэтил)амино]-1,3-бензотиазол-4,7-дион;
2-циклогексил-6-[(2-пирролидин-1-илэтил)амино]-1,3-бензотиазол-4,7-дион;
2-циклогексил-5-[(2-пирролидин-1-илэтил)амино]-1,3-бензотиазол-4,7-дион;
2-циклогексил-6-[(2-пирролидин-1-илэтил)амино]-1,3-бензотиазол-4,7-дион;
5-[(2-пирролидин-1-илэтил)амино]-2-тиен-2-ил-1,3-бензотиазол-4,7-дион;
6-[(2-пирролидин-1-илэтил)амино]-2-тиен-2-ил-1,3-бензотиазол-4,7-дион;
2-(2,5-дихлортиен-3-ил)-5-{[2-(диметиламино)этил]амино}-1,3-бензотиазол-4,7-дион;
2-(2,5-дихлортиен-3-ил)-6-{[2-(диметиламино)этил]амино}-1,3-бензотиазол-4,7-дион;
2-(2,5-дихлортиен-3-ил)-5-[(2-пирролидин-1-илэтил)амино]-1,3-бензотиазол-4,7-дион;
2-(2,5-дихлортиен-3-ил)-6-[(2-пирролидин-1-илэтил)амино]-1,3-бензотиазол-4,7-дион;
2-(2-фурил)-5-[(2-пирролидин-1-илэтил)амино]-1,3-бензотиазол-4,7-дион;
2-(2-фурил)-6-[(2-пирролидин-1-илэтил)амино]-1,3-бензотиазол-4,7-дион;
5-{[2-(диметиламино)этил]амино}-2-(2-метоксифенил)-1,3-бензотиазол-4,7-дион;
6-{[2-(диметиламино)этил]амино}-2-(2-метоксифенил)-1,3-бензотиазол-4,7-дион;
5-{[2-(диметиламино)этил]амино}-2-(2-фторфенил)-1,3-бензотиазол-4,7-дион;
6-{[2-(диметиламино)этил]амино}-2-(2-фторфенил)-1,3-бензотиазол-4,7-дион;
2-(2-фторфенил)-5-[(2-пирролидин-1-илэтил)амино]-1,3-бензотиазол-4,7-дион;
2-(2-фторфенил)-6-[(2-пирролидин-1-илэтил)амино]-1,3-бензотиазол-4,7-дион;
2-(4-фторфенил)-5-[(2-пирролидин-1-илэтил)амино]-1,3-бензотиазол-4,7-дион;
2-(4-фторфенил)-6-[(2-пирролидин-1-илэтил)амино]-1,3-бензотиазол-4,7-дион;
5-{[2-(диметиламино)этил]амино}-2-(4-фторфенил)-1,3-бензотиазол-4,7-дион;
6-{[2-(диметиламино)этил]амино}-2-(4-фторфенил)-1,3-бензотиазол-4,7-дион;
2-(2,6-дифторфенил)-5-[(2-пирролидин-1-илэтил)амино]-1,3-бензотиазол-4,7-дион;
2-(2,6-дифторфенил)-6-[(2-пирролидин-1-илэтил)амино]-1,3-бензотиазол-4,7-дион;
2-(2,6-дифторфенил)-5-{[2-(диметиламино)этил]амино}-1,3-бензотиазол-4,7-дион;
2-(2,6-дифторфенил)-6-{[2-(диметиламино)этил]амино}-1,3-бензотиазол-4,7-дион;
5-[[2-(диметиламино)этил](этил)амино]-2-метил-1,3-бензотиазол-4,7-дион;
5-[[2-(диметиламино)этил](метил)амино]-2-метил-1,3-бензотиазол-4,7-дион;
2-[2,6-дихлор-5-фтор-3-пиридил]-5-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-дион;
2-[2,6-дихлор-5-фтор-3-пиридил]-6-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-дион;
2-[2,6-дихлор-5-фтор-3-пиридил]-5-[(2-пирролидин-1-илэтил)амино]-1,3-бензоксазол-4,7-дион;
2-[2,6-дихлор-5-фтор-3-пиридил]-6-[(2-пирролидин-1-илэтил)амино]-1,3-бензоксазол-4,7-дион;
2-(2,4-дифторфенил)-5-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-дион;
2-(2,4-дифторфенил)-6-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-дион;
5-{[2-(диметиламино)этил]амино}-2-(2,3,4-трифторфенил)-1,3-бензоксазол-4,7-дион;
6-{[2-(диметиламино)этил]амино}-2-(2,3,4-трифторфенил)-1,3-бензоксазол-4,7-дион;
5-[(2-пирролидин-1-илэтил)амино]-2-(2,3,4-трифторфенил)-1,3-бензоксазол-4,7-дион;
6-[(2-пирролидин-1-илэтил)амино]-2-(2,3,4-трифторфенил)-1,3-бензоксазол-4,7-дион;
2-(3-фтор-4-метилфенил)-5-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-дион;
2-(3-фтор-4-метилфенил)-6-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-дион;
2-(3-фтор-4-метилфенил)-5-[(2-пирролидин-1-илэтил)амино]-1,3-бензоксазол-4,7-дион;
2-(3-фтор-4-метилфенил)-6-[(2-пирролидин-1-илэтил)амино]-1,3-бензоксазол-4,7-дион;
2-(4-хлорфенил)-5-{[2-(диметиламино)этил]амино}-1,3-бензотиазол-4,7-дион;
2-(4-хлорфенил)-6-{[2-(диметиламино)этил]амино}-1,3-бензотиазол-4,7-дион;
2-(4-хлорфенил)-5-[(2-пирролидин-1-илэтил)амино]-1,3-бензотиазол-4,7-дион;
2-(4-хлорфенил)-6-[(2-пирролидин-1-илэтил)амино]-1,3-бензотиазол-4,7-дион;
5-{[2-(диметиламино)этил]амино}-2-(2,3,4,5-тетрафторфенил)-1,3-бензотиазол-4,7-дион;
6-{[2-(диметиламино)этил]амино}-2-(2,3,4,5-тетрафторфенил)-1,3-бензотиазол-4,7-дион;
5-{[2-(диметиламино)этил]амино}-2-(3,4,5-трифторфенил)-1,3-бензотиазол-4,7-дион;
6-{[2-(диметиламино)этил]амино}-2-(3,4,5-трифторфенил)-1,3-бензотиазол-4,7-дион;
5-[(2-пирролидин-1-илэтил)амино]-2-(2,4,6-трифторфенил)-1,3-бензотиазол-4,7-дион;
6-[(2-пирролидин-1-илэтил)амино]-2-(2,4,6-трифторфенил)-1,3-бензотиазол-4,7-дион;
2-(1,3-бензодиоксол-5-ил)-5-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-дион;
2-(1,3-бензодиоксол-5-ил)-6-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-дион;
5-{[2-(диметиламино)этил]амино}-2-(4-этилфенил)-1,3-бензоксазол-4,7-дион;
6-{[2-(диметиламино)этил]амино}-2-(4-этилфенил)-1,3-бензоксазол-4,7-дион;
2-(4-этилфенил)-5-[(2-пирролидин-1-илэтил)амино]-1,3-бензоксазол-4,7-дион;
2-(4-этилфенил)-6-[(2-пирролидин-1-илэтил)амино]-1,3-бензоксазол-4,7-дион;
5-{[2-(диметиламино)этил]амино}-2-(2-фтор-6-метоксифенил)-1,3-бензоксазол-4,7-дион;
6-{[2-(диметиламино)этил]амино}-2-(2-фтор-6-метоксифенил)-1,3-бензоксазол-4,7-дион;
или фармацевтически приемлемую соль одного из них.

в которой
R1 представляет атом водорода или алкил, алкоксиалкил, алкилтиоалкил, циклоалкил, -(СН2)-Х-Y, - (СН2)-Z-NR5R6 или
-CHR35R36, в котором R35 и R36 образуют вместе с атомом углерода, к которому они присоединены, инданил или тетралинил, или также R35 и R36 образуют вместе с атомом углерода, к которому они присоединены, насыщенный гетероцикл, содержащий 5-7 членов и 1-2 гетероатома, выбранных из О, N и S, где атомы азота указанного гетероцикла необязательно замещены радикалами, выбранными из алкила и бензила,
R1 также может, когда W является О, представлять собой карбоциклический арил, необязательно замещенный 1-3 заместителями, независимо выбранными из атома галогена и алкила, галогеналкила или алкокси,
X представляет связь или нормальный, или разветвленный алкилен, содержащий 1-5 атомов углерода,
Y представляет насыщенную углеродсодержащую циклическую систему, содержащую 1-3 конденсированных кольца, независимо выбранных из колец с 3-7 членами, или Y представляет насыщенный гетероцикл, содержащий 1-2 гетероатома, независимо выбранных из О, N или S, и соединенный с радикалом X посредством N- или СН-члена, где указанный насыщенный гетероцикл, кроме того, содержит 2-6 дополнительных членов, независимо выбранных из -CHR7-, -СО-, -NR8-, -О- и -S-, где R7 представляет атом водорода или алкил, и R8 представляет атом водорода или алкил, или аралкил, или также Y представляет карбоциклический или гетероциклический арил, необязательно замещенный 1-3 заместителями, независимо выбранными из группы, состоящей из атома галогена, алкила, галогеналкила, алкокси, галогеналкокси, гидрокси, нитро, циано, фенила, SO2NHR9 и NR10R11, где R9 представляет атом водорода или алкил, или фенил, и R10 и R11 независимо представляют алкил,
Z представляет связь или нормальный, или разветвленный алкилен, содержащий 1-5 атомов углерода,
R5 и R6 независимо выбраны из атома водорода, алкила, аралкила или -(СН2)n-OH, в котором n представляет целое число от 1 до 6,
или R5 представляет алкоксикарбонил, галогеналкоксикарбонил или аралкоксикарбонил, и R6 представляет атом водорода или метил,
или также R5 и R6 образуют вместе с атомом азота гетероцикл с 4-7 членами, содержащий 1-2 гетероатома, где члены, необходимые для замыкания гетероцикла, независимо выбраны из
-CR12R13-, -O-, -S- и -NR14, где R12 и R13 независимо представляют, когда они имеются, атом водорода или алкил, и R14 представляет атом водорода или алкил, или аралкил, или также R14 представляет фенил, необязательно замещенный 1-3 заместителями, независимо выбранными из атома галогена и алкила, или алкокси,
R2 представляет атом водорода или алкил, или аралкил, или также R1 и R2 образуют вместе с атомом, азота гетероцикл с 4-8 членами, содержащий 1-2 гетероатома, где члены, необходимые для замыкания гетероцикла, независимо выбраны из -CR15R16-, -O-, -S-или -NR17, где R15 и R16 независимо представляют, когда они имеются, атом водорода или алкил, и R17 представляет атом водорода или алкил, или аралкил,
R3 представляет атом водорода, атом галогена или алкил, галогеналкил, алкокси или алкилтио,
R4 представляет алкил, циклоалкил, циклоалкилалкил, циано, амино, -CH2-COOR18, -CH2-CO-NR19R20 или -CH2-NR21R22, или R4 представляет карбоциклический или гетероциклический арил, необязательно замещенный 1-4 заместителями, независимо выбранными из атома галогена и алкила, галогеналкила, алкокси, галогеналкокси или NR37R38, или также R4 представляет фенил, имеющий два заместителя, которые вместе образуют метилендиокси или этилендиокси,
R18 представляет атом водорода или алкил,
R19 представляет атом водорода, алкил или аралкил, арильная группа которого необязательно замещена 1-3 заместителями, независимо выбранными из группы, состоящей из атома галогена, алкила, галогеналкила, алкокси, галогеналкокси, гидрокси, нитро, циано, фенила, SO2NHR23 и NR24R25, где R23 представляет атом водорода или алкил, или фенил, и R24 и R25 независимо представляют алкил,
R20 представляет атом водорода или алкил,
или также R19 и R20 образуют вместе с атомом азота гетероцикл с 4-7 членами, содержащий 1-2 гетероатома, где члены, необходимые для замыкания гетероцикла, независимо выбраны из
-CR26R27-, -O-, -S- или -NR28, где R26 и R27 независимо представляют, когда они имеются, атом водорода или алкил, и R28 представляет атом водорода или алкил, или аралкил, или также R28 представляет фенил, необязательно замещенный 1-3 заместителями, независимо выбранными из атома галогена и алкила, или алкокси,
R21 представляет атом водорода, алкил или аралкил, арильная группа которого необязательно замещена 1-3 заместителями, независимо выбранными из группы, состоящей из атома галогена, алкила, галогеналкила, алкокси, галогеналкокси, гидрокси, нитро, циано, фенила, SO2NHR29 и NR30R31, где R29 представляет атом водорода или алкил, или фенил, и R30 и R31 независимо представляют алкил,
R22 представляет атом водорода или алкил,
или также R21 и R22 образуют вместе с атомом азота гетероцикл с 4-7 членами, содержащий 1-2 гетероатома, где члены, необходимые для замыкания гетероцикла, независимо выбраны из
-CR32R33-, -O-, -S- или -NR34, где R32 и R33 независимо представляют, когда они имеются, атом водорода или алкил, и R34 представляет атом водорода, алкил или аралкил, или также R34 представляет фенил, необязательно замещенный 1-3 заместителями, независимо выбранными из атома галогена и алкила, или алкокси,
R37 и R38 независимо выбраны из атома водорода и алкила, или R37 и R38 образуют вместе с атомом азота гетероцикл с 4-7 членами, содержащий 1-2 гетероатома, где члены, необходимые для замыкания гетероцикла, независимо выбраны из -CR39R40-, -O-, -S- или -NR41, где R39 и R40 независимо представляют, когда они имеются, атом водорода или алкил, и R41 представляет атом водорода или алкил; и
W представляет О или S;
необходимо понимать, что, если W является S, и R4 представляет необязательно замещенный арил, то тогда R1 выбран из заместителей алкоксиалкила, алкилтиоалкила, циклоалкила, -(CH2)-X-Y и -(CH2)-Z-NR5R6,
или фармацевтически приемлемую соль данного соединения.
2-метил-5-{[2-(4-морфолинил)этил]амино}-1,3-бензотиазол-4,7-дион;
5-{[2-(диметиламино)зтил]амино}-2-метил-1,3-бензотиазол-4,7-дион;
5-{[6-(диметиламино)гексил]амино}-2-метил-1,3-бензотиазол-4,7-дион;
5-{[3-(диметиламино)-2,2-диметилпропил]амино}-2-метил-1,3-бензотиазол-4,7-дион;
2-метил-5-{[3-(4-метил-1-пиперазинил)пропил]амино}-1,3-бензотиазол-4,7-дион;
5-[(1-этилгексил)амино]-2-метил-1,3-бензотиазол-4,7-дион;
5-[(1-адамантилметил)амино]-2-метил-1,3-бензотиазол-4,7-дион;
2-метил-5-[(2-тиенилметил)амино]-1,3-бензотиазол-4,7-дион;
5-[(3-хлорбензил)амино]-2-метил-1,3-бензотиазол-4,7-дион;
2-метил-5-[(4-пиридинилметил)амино]-1,3-бензотиазол-4,7-дион;
2-метил-5-(пропиламино)-1,3-бензотиазол-4,7-дион;
5-{[3-(1Н-имидазол-1-ил)пропил]амино}-2-метил-1,3-бензотиазол-4,7-дион;
4-{2-[(2-метил-4,7-диоксо-4,7-дигидро-1,3-бензотиазол-5-ил)амино]этил}бензолсульфонамид;
5-(4-бензил-1-пиперазинил)-2-метил-1,3-бензотиазол-4,7-дион;
или его фармацевтически приемлемую соль.
5-[(2-метоксиэтил)амино]-2-метил-1,3-бензотиазол-4,7-дион;
2-метил-5-[(2-пирролидин-1-илэтил)амино]-1,3-бензотиазол-4,7-дион;
2-метил-5-[(2-пиперидин-1-илэтил)амино]-1,3-бензотиазол-4,7-дион;
5-{[2-(диизопропиламино)этил]амино}-2-метил-1,3-бензотиазол-4,7-дион;
5-[(1-бензилпирролидин-3-ил)амино]-2-метил-1,3-бензотиазол-4,7-дион;
5-{[3-(диметиламино)пропил]амино}-2-метил-1,3-бензотиазол-4,7-дион;
2-метил-5-{[2-(1-метилпирролидин-2-ил)этил]амино}-1,3-бензотиазол-4,7-дион;
2-метил-5-{[3-(2-метилпиперидин-1-ил)пропил]амино}-1,3-бензотиазол-4,7-дион;
5-{[4-(диметиламино)бутил]амино}2-метил-1,3-бензотиазол-4,7-дион;
5-{[5-(диметиламино)пентил]амино}-2-метил-1,3-бензотиазол-4,7-дион;
5-(2,3-дигидро-1Н-инден-1-иламино)-2-метил-1,3-бензотиазол-4,7-дион;
5-{бензил[2-(диметиламино)этил]амино}-2-метил-1,3-бензотиазол-4,7-дион;
2-метил-5-{[3-(метиламино)пропил]амино}-1,3-бензотиазол-4,7-дион;
5-[(3-аминопропил)амино]-2-метил-1,3-бензотиазол-4,7-дион;
6-хлор-5-{[2-(диметиламино)этил]амино}-2-метил-1,3-бензотиазол-4,7-дион;
6-бром-5-{[2-(диметиламино)этил]амино}-2-метил-1,3-бензотиазол-4,7-дион;
6-(бутилтио)-5-{[2-(диметиламино)этил]амино}-2-метил-1,3-бензотиазол-4,7-дион;
5-{[2-(диметиламино)этил]амино}-2-(морфолин-4-илметил)-1,3-бензотиазол-4,7-дион;
5-{[2-(диметиламино)этил]амино}-2-[(4-фенилпиперазин-1-ил)метил]-1,3-бензотиазол-4,7-дион;
5-{[2-(диметиламино)этил]амино}-2-(пиперидин-1-илметил)-1,3-бензотиазол-4,7-дион;
5-{[6-(диметиламино)гексил]амино}-2-этил-1,3-бензоксазол-4,7-дион;
2-этил-5-(4-метилпиперазин-1-ил)-1,3-бензоксазол-4,7-дион;
2-этил-5-[(1-этилгексил)амино]-1,3-бензоксазол-4,7-дион;
5-азокан-1-ил-2-этил-1,3-бензоксазол-4,7-дион;
2-этил-5-морфолин-4-ил-1,3-бензоксазол-4,7-дион;
5-{[2-(диметиламино) этил] амино}-2-этил-6-метил-1,3-бензоксазол-4,7-дион;
5-{[2-(диметиламино)этил]амино}-2-фенил-1,3-бензоксазол-4,7-дион;
5-{[6-(диметиламино)гексил]амино}-2-фенил-1,3-бензоксазол-4,7-дион;
2-(2,6-дифторфенил)-5-[(2-пирролидин-1-илэтил)амино]-1,3-бензоксазол-4,7-дион;
2-[4-(диэтиламино)фенил]-5-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-дион;
2-[4-(диэтиламино)фенил]-5-[(2-пирролидин-1-илэтил)амино]-1,3-бензоксазол-4,7-дион;
2-(4-хлорфенил)-5-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-дион;
2-(4-хлорфенил)-5-{[3-(диметиламино)пропил]амино}-1,3-бензоксазол-4,7-дион;
2-(4-хлорфенил)-5-{[4-(диметиламино)бутил]амино}-1,3-бензоксазол-4,7-дион;
или его фармацевтически приемлемую соль.
трет-бутил метил{3-[(2-метил-4,7-диоксо-4,7-дигидро-1,3-бензотиазол-5-ил)амино]пропил}карбамат;
трет-бутил 3-[(2-метил-4,7-диоксо-4,7-дигидро-1,3-бензотиазол-5-ил)амино]пропилкарбамат;
6-{[6-(диметиламино)гексил]амино}-2-этил-1,3-бензоксазол-4,7-дион;
2-этил-6-(4-метилпиперазин-1-ил)-1,3-бензоксазол-4,7-дион;
2-этил-6-[(1-этилгексил)амино]-1,3-бензоксазол-4,7-дион;
6-азокан-1-ил-2-этил-1,3-бензоксазол-4,7-дион;
2-этил-6-морфолин-4-ил-1,3-бензоксазол-4,7-дион;
6-{[2-(диметиламино)этил]амино}-2-фенил-1,3-бензоксазол-4,7-дион;
6-{[6-(диметиламино)гексил]амино}-2-фенил-1,3-бензоксазол-4,7-дион;
2-(2,6-дифторфенил)-6-[(2-пирролидин-1-илэтил)амино]-1,3-бензоксазол-4,7-дион;
2-[4-(диэтиламино)фенил]-6-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-дион;
2-[4-(диэтиламино)фенил]-6-[(2-пирролидин-1-илэтил)амино]-1,3-бензоксазол-4,7-дион;
2-(4-хлорфенил)-6-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-дион;
2-(4-хлорфенил)-6-{[3-(диметиламино)пропил]амино}-1,3-бензоксазол-4,7-дион;
2-(4-хлорфенил)-6-{[4-(диметиламино)бутил]амино}-1,3-бензоксазол-4,7-дион;
2-(2-фторфенил)-5-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-дион;
2-(2-фторфенил)-6-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-дион;
2-(2-фторфенил)-5-[(2-пирролидин-1-илэтил)амино]-1,3-бензоксазол-4,7-дион;
2-(2-фторфенил)-6-[(2-пирролидин-1-илэтил)амино]-1,3-бензоксазол-4,7-дион;
2-(2-бромфенил)-5-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-дион;
2-(2-бромфенил)-6-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-дион;
2-(2-бромфенил)-5-[(2-пирролидин-1-илэтил)амино]-1,3-бензоксазол-4,7-дион;
2-(2-бромфенил)-6-[(2-пирролидин-1-илэтил)амино]-1,3-бензоксазол-4,7-дион;
2-(2-бромфенил)-5-{[3-(диметиламино)пропил]амино}-1,3-бензоксазол-4,7-дион;
2-(2-бромфенил)-6-{[3-(диметиламино)пропил]амино}-1,3-бензоксазол-4,7-дион;
2-(2-хлорфенил)-5-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-дион;
2-(2-хлорфенил)-6-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-дион;
2-(2-хлорфенил)-5-[(2-пирролидин-1-илэтил)амино]-1,3-бензоксазол-4,7-дион;
2-(2-хлорфенил)-6-[(2-пирролидин-1-илэтил)амино]-1,3-бензоксазол-4,7-дион;
2-(3-бромфенил)-5-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-дион;
2-(3-бромфенил)-6-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-дион;
2-(4-бромфенил)-5-[(2-пирролидин-1-илэтил)амино]-1,3-бензоксазол-4,7-дион;
2-(4-бромфенил)-6-[(2-пирролидин-1-илэтил)амино]-1,3-бензоксазол-4,7-дион;
2-(4-бромфенил)-5-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-дион;
2-(4-бромфенил)-6-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-дион;
2-(4-фторфенил)-5-[(2-пирролидин-1-илэтил)амино]-1,3-бензоксазол-4,7-дион;
2-(4-фторфенил)-6-[(2-пирролидин-1-илэтил)амино]-1,3-бензоксазол-4,7-дион;
5-{[2-(диметиламино)этил]амино}-2-(4-фторфенил)-1,3-бензоксазол-4,7-дион;
6-{[2-(диметиламино)этил]амино}-2-(4-фторфенил)-1,3-бензоксазол-4,7-дион;
5-[(1-бензилпирролидин-3-ил)амино]-2-(4-фторфенил)-1,3-бензоксазол-4,7-дион;
6-[(1-бензилпирролидин-3-ил)амино]-2-(4-фторфенил)-1,3-бензоксазол-4,7-дион;
5-{[3-(диметиламино)пропил]амино}-2-(4-фторфенил)-1,3-бензоксазол-4,7-дион;
6-{[3-(диметиламино)пропил]амино}-2-(4-фторфенил)-1,3-бензоксазол-4,7-дион;
2-(3,5-дифторфенил)-5-[(2-пирролидин-1-илэтил)амино]-1,3-бензоксазол-4,7-дион;
2-(3,5-дифторфенил)-6-[(2-пирролидин-1-илэтил)амино]-1,3-бензоксазол-4,7-дион;
2-(3,5-дифторфенил)-5-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-дион;
2-(3,5-дифторфенил)-6-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-дион;
2-(2,5-дифторфенил)-5-[(2-пирролидин-1-илэтил)амино]-1,3-бензоксазол-4,7-дион;
2-(2,5-дифторфенил)-6-[(2-пирролидин-1-илэтил)амино]-1,3-бензоксазол-4,7-дион;
2-(2,5-дифторфенил)-5-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-дион;
2-(2,5-дифторфенил)-6-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-дион;
2-(2,3-дифторфенил)-5-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-дион;
2-(2,3-дифторфенил)-6-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-дион;
2-(2,3-дифторфенил)-5-[(2-пирролидин-1-илэтил)амино]-1,3-бензоксазол-4,7-дион;
2-(2,3-дифторфенил)-6-[(2-пирролидин-1-илэтил)амино]-1,3-бензоксазол-4,7-дион;
2-(2,3-дифторфенил)-5-{[3-(диметиламино)пропил]амино}-1,3-бензоксазол-4,7-дион;
2-(2,3-дифторфенил)-6-{[3-(диметиламино)пропил]амино}-1,3-бензоксазол-4,7-дион;
5-[(2-пирролидин-1-илэтил)амино]-2-(3,4,5-трифторфенил)-1,3-бензоксазол-4,7-дион;
6-[(2-пирролидин-1-илэтил)амино]-2-(3,4,5-трифторфенил)-1,3-бензоксазол-4,7-дион;
5-{[2-(диметиламино)этил]амино}-2-(3,4,5-трифторфенил)-1,3-бензоксазол-4,7-дион;
6-{[2-(диметиламино)этил]амино}-2-(3,4,5-трифторфенил)-1,3-бензоксазол-4,7-дион;
5-[(2-пирролидин-1-илэтил)амино]-2-(2,3,4,5-тетрафторфенил)-1,3-бензоксазол-4,7-дион;
6-[(2-пирролидин-1-илэтил)амино]-2-(2,3,4,5-тетрафторфенил)-1,3-бензоксазол-4,7-дион;
5-{[2-(диметиламино)этил]амино}-2-(2,3,4,5-тетрафторфенил)-1,3-бензоксазол-4,7-дион;
6-{[2-(диметиламино)этил]амино}-2-(2,3,4,5-тетрафторфенил)-1,3-бензоксазол-4,7-дион;
5-{[2-(диметиламино)этил]амино}-2-[2-фтор-6-(трифторметил)фенил]-1,3-бензоксазол-4,7-дион;
6-{[2-(диметиламино)этил]амино}-2-[2-фтор-6-(трифторметил)фенил]-1,3-бензоксазол-4,7-дион;
2-[2-фтор-6-(трифторметил)фенил]-5-[(2-пирролидин-1-илэтил)амино]-1,3-бензоксазол-4,7-дион;
2-[2-фтор-6-(трифторметил)фенил]-6-[(2-пирролидин-1-илэтил)амино]-1,3-бензоксазол-4,7-дион;
5-{[3-(диметиламино)пропил]амино}-2-[2-фтор-6-(трифторметил)фенил]-1,3-бензоксазол-4,7-дион;
6-{[3-(диметиламино)пропил]амино}-2-[2-фтор-6-(трифторметил)фенил]-1,3-бензоксазол-4,7-дион;
2-[2-хлор-5-(трифторметил)фенил]-5-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-дион;
2-[2-хлор-5-(трифторметил)фенил]-6-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-дион;
2-[2-хлор-5-(трифторметил)фенил]-5-[(2-пирролидин-1-илэтил)амино]-1,3-бензоксазол-4,7-дион;
2-[2-хлор-5-(трифторметил)фенил]-6-[(2-пирролидин-1-илэтил)амино]-1,3-бензоксазол-4,7-дион;
2-[2-хлор-5-(трифторметил)фенил]-5-{[3-(диметиламино)пропил]амино}-1,3-бензоксазол-4,7-дион;
2-[2-хлор-5-(трифторметил)фенил]-6-{[3-(диметиламино)пропил]амино}-1,3-бензоксазол-4,7-дион;
2-[2-хлор-6-фторфенил]-5-{[3-(диметиламино)пропил]амино}-1,3-бензоксазол-4,7-дион;
2-[2-хлор-6-фторфенил]-6-{[3-(диметиламино)пропил]амино}-1,3-бензоксазол-4,7-дион;
2-[2-хлор-6-фторфенил]-5-[(2-пирролидин-1-илэтил)амино]-1,3-бензоксазол-4,7-дион;
2-[2-хлор-6-фторфенил]-6-[(2-пирролидин-1-илэтил)амино]-1,3-бензоксазол-4,7-дион;
2-[3,4-диметоксифенил]-5-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-дион;
2-[3,4-диметоксифенил]-6-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-дион;
2-[2-бром-3-пиридил]-5-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-дион;
2-[2-бром-3-пиридил]-6-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-дион;
2-циклогексил-5-[(2-пирролидин-1-илэтил)амино]-1,3-бензотиазол-4,7-дион;
2-циклогексил-6-[(2-пирролидин-1-илэтил)амино]-1,3-бензотиазол-4,7-дион;
2-циклогексил-5-[(2-пирролидин-1-илэтил)амино]-1,3-бензотиазол-4,7-дион;
2-циклогексил-6-[(2-пирролидин-1-илэтил)амино]-1,3-бензотиазол-4,7-дион;
5-[(2-пирролидин-1-илэтил)амино]-2-тиен-2-ил-1,3-бензотиазол-4,7-дион;
6-[(2-пирролидин-1-илэтил)амино]-2-тиен-2-ил-1,3-бензотиазол-4,7-дион;
2-(2,5-дихлортиен-3-ил)-5-{[2-(диметиламино)этил]амино}-1,3-бензотиазол-4,7-дион;
2-(2,5-дихлортиен-3-ил)-6-{[2-(диметиламино)этил]амино}-1,3-бензотиазол-4,7-дион;
2-(2,5-дихлортиен-3-ил)-5-[(2-пирролидин-1-илэтил)амино]-1,3-бензотиазол-4,7-дион;
2-(2,5-дихлортиен-3-ил)-6-[(2-пирролидин-1-илэтил)амино]-1,3-бензотиазол-4,7-дион;
2-(2-фурил)-5-[(2-пирролидин-1-илэтил)амино]-1,3-бензотиазол-4,7-дион;
2-(2-фурил)-6-[(2-пирролидин-1-илэтил)амино]-1,3-бензотиазол-4,7-дион;
5-{[2-(диметиламино)этил]амино}-2-(2-метоксифенил)-1,3-бензотиазол-4,7-дион;
6-{[2-(диметиламино)этил]амино}-2-(2-метоксифенил)-1,3-бензотиазол-4,7-дион;
5-{[2-(диметиламино)этил]амино}-2-(2-фторфенил)-1,3-бензотиазол-4,7-дион;
6-{[2-(диметиламино)этил]амино}-2-(2-фторфенил)-1,3-бензотиазол-4,7-дион;
2-(2-фторфенил)-5-[(2-пирролидин-1-илэтил)амино]-1,3-бензотиазол-4,7-дион;
2-(2-фторфенил)-6-[(2-пирролидин-1-илэтил)амино]-1,3-бензотиазол-4,7-дион;
2-(4-фторфенил)-5-[(2-пирролидин-1-илэтил)амино]-1,3-бензотиазол-4,7-дион;
2-(4-фторфенил)-6-[(2-пирролидин-1-илэтил)амино]-1,3-бензотиазол-4,7-дион;
5-{[2-(диметиламино)этил]амино}-2-(4-фторфенил)-1,3-бензотиазол-4,7-дион;
6-{[2-(диметиламино)этил]амино}-2-(4-фторфенил)-1,3-бензотиазол-4,7-дион;
2-(2,6-дифторфенил)-5-[(2-пирролидин-1-илэтил)амино]-1,3-бензотиазол-4,7-дион;
2-(2,6-дифторфенил)-6-[(2-пирролидин-1-илэтил)амино]-1,3-бензотиазол-4,7-дион;
2-(2,6-дифторфенил)-5-{[2-(диметиламино)этил]амино}-1,3-бензотиазол-4,7-дион;
2-(2,6-дифторфенил)-6-{[2-(диметиламино)этил]амино}-1,3-бензотиазол-4,7-дион;
5-[[2-(диметиламино)этил](этил)амино]-2-метил-1,3-бензотиазол-4,7-дион;
5-[[2-(диметиламино)этил](метил)амино]-2-метил-1,3-бензотиазол-4,7-дион;
2-[2,6-дихлор-5-фтор-3-пиридил]-5-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-дион;
2-[2,6-дихлор-5-фтор-3-пиридил]-6-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-дион;
2-[2,6-дихлор-5-фтор-3-пиридил]-5-[(2-пирролидин-1-илэтил)амино]-1,3-бензоксазол-4,7-дион;
2-[2,6-дихлор-5-фтор-3-пиридил]-6-[(2-пирролидин-1-илэтил)амино]-1,3-бензоксазол-4,7-дион;
2-(2,4-дифторфенил)-5-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-дион;
2-(2,4-дифторфенил)-6-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-дион;
5-{[2-(диметиламино)этил]амино}-2-(2,3,4-трифторфенил)-1,3-бензоксазол-4,7-дион;
6-{[2-(диметиламино)этил]амино}-2-(2,3,4-трифторфенил)-1,3-бензоксазол-4,7-дион;
5-[(2-пирролидин-1-илэтил)амино]-2-(2,3,4-трифторфенил)-1,3-бензоксазол-4,7-дион;
6-[(2-пирролидин-1-илэтил)амино]-2-(2,3,4-трифторфенил)-1,3-бензоксазол-4,7-дион;
2-(3-фтор-4-метилфенил)-5-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-дион;
2-(3-фтор-4-метилфенил)-6-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-дион;
2-(3-фтор-4-метилфенил)-5-[(2-пирролидин-1-илэтил)амино]-1,3-бензоксазол-4,7-дион;
2-(3-фтор-4-метилфенил)-6-[(2-пирролидин-1-илэтил)амино]-1,3-бензоксазол-4,7-дион;
2-(4-хлорфенил)-5-{[2-(диметиламино)этил]амино}-1,3-бензотиазол-4,7-дион;
2-(4-хлорфенил)-6-{[2-(диметиламино)этил]амино}-1,3-бензотиазол-4,7-дион;
2-(4-хлорфенил)-5-[(2-пирролидин-1-илэтил)амино]-1,3-бензотиазол-4,7-дион;
2-(4-хлорфенил)-6-[(2-пирролидин-1-илэтил)амино]-1,3-бензотиазол-4,7-дион;
5-{[2-(диметиламино)этил]амино}-2-(2,3,4,5-тетрафторфенил)-1,3-бензотиазол-4,7-дион;
6-{[2-(диметиламино)этил]амино}-2-(2,3,4,5-тетрафторфенил)-1,3-бензотиазол-4,7-дион;
5-{[2-(диметиламино)этил]амино}-2-(3,4,5-трифторфенил)-1,3-бензотиазол-4,7-дион;
6-{[2-(диметиламино)этил]амино}-2-(3,4,5-трифторфенил)-1,3-бензотиазол-4,7-дион;
5-[(2-пирролидин-1-илэтил)амино]-2-(2,4,6-трифторфенил)-1,3-бензотиазол-4,7-дион;
6-[(2-пирролидин-1-илэтил)амино]-2-(2,4,6-трифторфенил)-1,3-бензотиазол-4,7-дион;
2-(1,3-бензодиоксол-5-ил)-5-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-дион;
2-(1,3-бензодиоксол-5-ил)-6-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-дион;
5-{[2-(диметиламино)этил]амино}-2-(4-этилфенил)-1,3-бензоксазол-4,7-дион;
6-{[2-(диметиламино)этил]амино}-2-(4-этилфенил)-1,3-бензоксазол-4,7-дион;
2-(4-этилфенил)-5-[(2-пирролидин-1-илэтил)амино]-1,3-бензоксазол-4,7-дион;
2-(4-этилфенил)-6-[(2-пирролидин-1-илэтил)амино]-1,3-бензоксазол-4,7-дион;
5-{[2-(диметиламино)этил]амино}-2-(2-фтор-6-метоксифенил)-1,3-бензоксазол-4,7-дион;
6-{[2-(диметиламино)этил]амино}-2-(2-фтор-6-метоксифенил)-1,3-бензоксазол-4,7-дион;
или фармацевтически приемлемую соль одного из них.
2-метил-5-{[2-(4-морфолинил)этил]амино}-1,3-бензотиазол-4,7-дион;
5-{[2-(диметиламино)этил]амино}-2-метил-1,3-бензотиазол-4,7-дион;
5-{[6-(диметиламино)гексил]амино}-2-метил-1,3-бензотиазол-4,7-дион;
5-{[3-(диметиламино)-2,2-диметилпропил]амино}-2-метил-1,3-бензотиазол-4,7-дион;
2-метил-5-{[3-(4-метил-1-пиперазинил)пропил]амино}-1,3-бензотиазол-4,7-дион;
5-[(1-этилгексил)амино]-2-метил-1,3-бензотиазол-4,7-дион;
5-[(1-адамантилметил)амино]-2-метил-1,3-бензотиазол-4,7-дион;
2-метил-5-[(2-тиенилметил)амино]-1,3-бензотиазол-4,7-дион;
5-[(3-хлорбензил)амино]-2-метил-1,3-бензотиазол-4,7-дион;
2-метил-5-[(4-пиридинилметил)амино]-1,3-бензотиазол-4,7-дион;
2-метил-5-(пропиламино)-1,3-бензотиазол-4,7-дион;
5-{[3-(1Н-имидазол-1-ил)пропил]амино}-2-метил-1,3-бензотиазол-4,7-дион;
4-{2-[(2-метил-4,7-диоксо-4,7-дигидро-1,3-бензотиазол-5-ил)амино]этил}бензолсульфонамид;
5-(4-бензил-1-пиперазинил)-2-метил-1,3-бензотиазол-4,7-дион;
или его фармацевтически приемлемую соль, и
фармацевтически приемлемый носитель.
5-[(2-метоксиэтил)амино]-2-метил-1,3-бензотиазол-4,7-дион;
2-метил-5-[(2-пирролидин-1-илэтил)амино]-1,3-бензотиазол-4,7-дион;
2-метил-5-[(2-пиперидин-1-илэтил)амино]-1,3-бензотиазол-4,7-дион;
5-{[2-(диизопропиламино)этил]амино}-2-метил-1,3-бензотиазол-4,7-дион;
5-[(1-бензилпирролидин-3-ил)амино]-2-метил-1,3-бензотиазол-4,7-дион;
5-{[3-(диметиламино)пропил]амино}-2-метил-1,3-бензотиазол-4,7-дион;
2-метил-5-{[2-(1-метилпирролидин-2-ил)этил]амино}-1,3-бензотиазол-4,7-дион;
2-метил-5-{[3-(2-метилпиперидин-1-ил)пропил]амино}-1,3-бензотиазол-4,7-дион;
5-{[4-(диметиламино)бутил]амино}2-метил-1,3-бензотиазол-4,7-дион;
5-{[5-(диметиламино)пентил]амино}-2-метил-1,3-бензотиазол-4,7-дион;
5-(2,3-дигидро-1Н-инден-1-иламино)-2-метил-1,3-бензотиазол-4,7-дион;
5-{бензил[2-(диметиламино)этил]амино}-2-метил-1,3-бензотиазол-4,7-дион;
2-метил-5-{[3-(метиламино)пропил]амино}-1,3-бензотиазол-4,7-дион;
5-[(3-аминопропил)амино]-2-метил-1,3-бензотиазол-4,7-дион;
6-хлор-5-{[2-(диметиламино)этил]амино}-2-метил-1,3-бензотиазол-4,7-дион;
6-бром-5-{[2-(диметиламино)этил]амино}-2-метил-1,3-бензотиазол-4,7-дион;
6-(бутилтио)-5-{[2-(диметиламино)этил]амино}-2-метил-1,3-бензотиазол-4,7-дион;
5-{[2-(диметиламино)этил]амино}-2-(морфолин-4-илметил)-1,3-бензотиазол-4,7-дион;
5-{[2-(диметиламино)этил]амино}-2-[(4-фенилпиперазин-1-ил)метил]-1,3-бензотиазол-4,7-дион;
5-{[2-(диметиламино)этил]амино}-2-(пиперидин-1-илметил)-1,3-бензотиазол-4,7-дион;
5-{[6-(диметиламино)гексил]амино}-2-этил-1,3-бензоксазол-4,7-дион;
2-этил-5-(4-метилпиперазин-1-ил)-1,3-бензоксазол-4,7-дион;
2-этил-5-[(1-этилгексил)амино]-1,3-бензоксазол-4,7-дион;
5-азокан-1-ил-2-этил-1,3-бензоксазол-4,7-дион;
2-этил-5-морфолин-4-ил-1,3-бензоксазол-4,7-дион;
5-{[2-(диметиламино)зтил]амино}-2-этил-6-метил-1,3-бензоксазол-4,7-дион;
5-{[2-(диметиламино)этил]амино}-2-фенил-1,3-бензоксазол-4,7-дион;
5-{[6-(диметиламино)гексил]амино}-2-фенил-1,3-бензоксазол-4,7-дион;
2-(2,6-дифторфенил)-5-[(2-пирролидин-1-илэтил)амино]-1,3-бензоксазол-4,7-дион;
2-[4-(диэтиламино)фенил]-5-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-дион;
2-[4-(диэтиламино)фенил]-5-[(2-пирролидин-1-илэтил)амино]-1,3-бензоксазол-4,7-дион;
2-(4-хлорфенил)-5-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-дион;
2-(4-хлорфенил)-5-{[3-(диметиламино)пропил]амино}-1,3-бензоксазол-4,7-дион;
2-(4-хлорфенил)-5-{[4-(диметиламино)бутил]амино}-1,3-бензоксазол-4,7-дион;
или его фармацевтически приемлемую соль, и
фармацевтически приемлемый носитель.
трет-бутилметил метил{3-[(2-метил-4,7-диоксо-4,7-дигидро-1,3-бензотиазол-5-ил)амино]пропил}карбамат;
трет-бутил 3-[(2-метил-4,7-диоксо-4,7-дигидро-1,3-бензотиазол-5-ил)амино]пропилкарбамат;
6-{[6-(диметиламино)гексил]амино}-2-этил-1,3-бензоксазол-4,7-дион;
2-этил-6-(4-метилпиперазин-1-ил)-1,3-бензоксазол-4,7-дион;
2-этил-6-[(1-этилгексил)амино]-1,3-бензоксазол-4,7-дион;
6-азокан-1-ил-2-этил-1,3-бензоксазол-4,7-дион;
2-этил-6-морфолин-4-ил-1,3-бензоксазол-4,7-дион;
6-{[2-(диметиламино)этил]амино}-2-фенил-1,3-бензоксазол-4,7-дион;
6-{[6-(диметиламино)гексил]амино}-2-фенил-1,3-бензоксазол-4,7-дион;
2-(2,6-дифторфенил)-6-[(2-пирролидин-1-илэтил)амино]-1,3-бензоксазол-4,7-дион;
2-[4-(диэтиламино)фенил]-6-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-дион;
2-[4-(диэтиламино)фенил]-6-[(2-пирролидин-1-илэтил)амино]-1,3-бензоксазол-4,7-дион;
2-(4-хлорфенил)-6-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-дион;
2-(4-хлорфенил)-6-{[3-(диметиламино)пропил]амино}-1,3-бензоксазол-4,7-дион;
2-(4-хлорфенил)-6-{[4-(диметиламино)бутил]амино}-1,3-бензоксазол-4,7-дион;
2-(2-фторфенил)-5-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-дион;
2-(2-фторфенил)-6-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-дион;
2-(2-фторфенил)-5-[(2-пирролидин-1-илэтил)амино]-1,3-бензоксазол-4,7-дион;
2-(2-фторфенил)-6-[(2-пирролидин-1-илэтил)амино]-1,3-бензоксазол-4,7-дион;
2-(2-бромфенил)-5-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-дион;
2-(2-бромфенил)-6-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-дион;
2-(2-бромфенил)-5-[(2-пирролидин-1-илэтил)амино]-1,3-бензоксазол-4,7-дион;
2-(2-бромфенил)-6-[(2-пирролидин-1-илэтил)амино]-1,3-бензоксазол-4,7-дион;
2-(2-бромфенил)-5-{[3-(диметиламино)пропил]амино}-1,3-бензоксазол-4,7-дион;
2-(2-бромфенил)-6-{[3-(диметиламино)пропил]амино}-1,3-бензоксазол-4,7-дион;
2-(2-хлорфенил)-5-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-дион;
2-(2-хлорфенил)-6-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-дион;
2-(2-хлорфенил)-5-[(2-пирролидин-1-илэтил)амино]-1,3-бензоксазол-4,7-дион;
2-(2-хлорфенил)-6-[(2-пирролидин-1-илэтил)амино]-1,3-бензоксазол-4,7-дион;
2-(3-бромфенил)-5-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-дион;
2-(3-бромфенил)-6-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-дион;
2-(4-бромфенил)-5-[(2-пирролидин-1-илэтил)амино]-1,3-бензоксазол-4,7-дион;
2-(4-бромфенил)-6-[(2-пирролидин-1-илэтил)амино]-1,3-бензоксазол-4,7-дион;
2-(4-бромфенил)-5-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-дион;
2-(4-бромфенил)-6-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-дион;
2-(4-фторфенил)-5-[(2-пирролидин-1-илэтил)амино]-1,3-бензоксазол-4,7-дион;
2-(4-фторфенил)-6-[(2-пирролидин-1-илэтил)амино]-1,3-бензоксазол-4,7-дион;
5-{[2-(диметиламино)этил]амино}-2-(4-фторфенил)-1,3-бензоксазол-4,7-дион;
6-{[2-(диметиламино)этил]амино}-2-(4-фторфенил)-1,3-бензоксазол-4,7-дион;
5-[(1-бензилпирролидин-3-ил)амино]-2-(4-фторфенил)-1,3-бензоксазол-4,7-дион;
6-[(1-бензилпирролидин-3-ил)амино]-2-(4-фторфенил)-1,3-бензоксазол-4,7-дион;
5-{[3-(диметиламино)пропил]амино}-2-(4-фторфенил)-1,3-бензоксазол-4,7-дион;
6-{[3-(диметиламино)пропил]амино}-2-(4-фторфенил)-1,3-бензоксазол-4,7-дион;
2-(3,5-дифторфенил)-5-[(2-пирролидин-1-илэтил)амино]-1,3-бензоксазол-4,7-дион;
2-(3,5-дифторфенил)-6-[(2-пирролидин-1-илэтил)амино]-1,3-бензоксазол-4,7-дион;
2-(3,5-дифторфенил)-5-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-дион;
2-(3,5-дифторфенил)-6-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-дион;
2-(2,5-дифторфенил)-5-[(2-пирролидин-1-илэтил)амино]-1,3-бензоксазол-4,7-дион;
2-(2,5-дифторфенил)-6-[(2-пирролидин-1-илэтил)амино]-1,3-бензоксазол-4,7-дион;
2-(2,5-дифторфенил)-5-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-дион;
2-(2,5-дифторфенил)-6-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-дион;
2-(2,3-дифторфенил)-5-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-дион;
2-(2,3-дифторфенил)-6-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-дион;
2-(2,3-дифторфенил)-5-[(2-пирролидин-1-илэтил)амино]-1,3-бензоксазол-4,7-дион;
2-(2,3-дифторфенил)-6-[(2-пирролидин-1-илэтил)амино]-1,3-бензоксазол-4,7-дион;
2-(2,3-дифторфенил)-5-{[3-(диметиламино)пропил]амино}-1,3-бензоксазол-4,7-дион;
2-(2,3-дифторфенил)-6-{[3-(диметиламино)пропил]амино}-1,3-бензоксазол-4,7-дион;
5-[(2-пирролидин-1-илэтил)амино]-2-(3,4,5-трифторфенил)-1,3-бензоксазол-4,7-дион;
6-[(2-пирролидин-1-илэтил)амино]-2-(3,4,5-трифторфенил)-1,3-бензоксазол-4,7-дион;
5-{[2-(диметиламино)этил]амино}-2-(3,4,5-трифторфенил)-1,3-бензоксазол-4,7-дион;
6-{[2-(диметиламино)этил]амино}-2-(3,4,5-трифторфенил)-1,3-бензоксазол-4,7-дион;
5-[(2-пирролидин-1-илэтил)амино]-2-(2,3,4,5-тетрафторфенил)-1,3-бензоксазол-4,7-дион;
6-[(2-пирролидин-1-илэтил)амино]-2-(2,3,4,5-тетрафторфенил)-1,3-бензоксазол-4,7-дион;
5-{[2-(диметиламино)этил]амино}-2-(2,3,4,5-тетрафторфенил)-1,3-бензоксазол-4,7-дион;
6-{[2-(диметиламино)этил]амино}-2-(2,3,4,5-тетрафторфенил)-1,3-бензоксазол-4,7-дион;
5-{[2-(диметиламино)этил]амино}-2-[2-фтор-6-(трифторметил)фенил]-1,3-бензоксазол-4,7-дион;
6-{[2-(диметиламино)этил]амино}-2-[2-фтор-6-(трифторметил)фенил]-1,3-бензоксазол-4,7-дион;
2-[2-фтор-6-(трифторметил)фенил]-5-[(2-пирролидин-1-илэтил)амино]-1,3-бензоксазол-4,7-дион;
2-[2-фтор-6-(трифторметил)фенил]-6-[(2-пирролидин-1-илэтил)амино]-1,3-бензоксазол-4,7-дион;
5-{[3-(диметиламино)пропил]амино}-2-[2-фтор-6-(трифторметил)фенил]-1,3-бензоксазол-4,7-дион;
6-{[3-(диметиламино)пропил]амино}-2-[2-фтор-6-(трифторметил)фенил]-1,3-бензоксазол-4,7-дион;
2-[2-хлор-5-(трифторметил)фенил]-5-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-дион;
2-[2-хлор-5-(трифторметил)фенил]-6-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-дион;
2-[2-хлор-5-(трифторметил)фенил]-5-[(2-пирролидин-1-илэтил)амино]-1,3-бензоксазол-4,7-дион;
2-[2-хлор-5-(трифторметил)фенил]-6-[(2-пирролидин-1-илэтил)амино]-1,3-бензоксазол-4,7-дион;
2-[2-хлор-5-(трифторметил)фенил]-5-{[3-(диметиламино)пропил]амино}-1,3-бензоксазол-4,7-дион;
2-[2-хлор-5-(трифторметил)фенил]-6-{[3-(диметиламино)пропил]амино}-1,3-бензоксазол-4,7-дион;
2-[2-хлор-6-фторфенил]-5-{[3-(диметиламино)пропил]амино}-1,3-бензоксазол-4,7-дион;
2-[2-хлор-6-фторфенил]-6-{[3-(диметиламино)пропил]амино}-1,3-бензоксазол-4,7-дион;
2-[2-хлор-6-фторфенил]-5-[(2-пирролидин-1-илэтил)амино]-1,3-бензоксазол-4,7-дион;
2-[2-хлор-6-фторфенил]-6-[(2-пирролидин-1-илэтил)амино]-1,3-бензоксазол-4,7-дион;
2-[3,4-диметоксифенил]-5-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-дион;
2-[3,4-диметоксифенил]-6-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-дион;
2-[2-бром-3-пиридил]-5-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-дион;
2-[2-бром-3-пиридил]-6-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-дион;
2-циклогексил-5-[(2-пирролидин-1-илэтил)амино]-1,3-бензотиазол-4,7-дион;
2-циклогексил-6-[(2-пирролидин-1-илэтил)амино]-1,3-бензотиазол-4,7-дион;
2-циклогексил-5-[(2-пирролидин-1-илэтил)амино]-1,3-бензотиазол-4,7-дион;
2-циклогексил-6-[(2-пирролидин-1-илэтил)амино]-1,3-бензотиазол-4,7-дион;
5-[(2-пирролидин-1-илэтил)амино]-2-тиен-2-ил-1,3-бензотиазол-4,7-дион;
6-[(2-пирролидин-1-илэтил)амино]-2-тиен-2-ил-1,3-бензотиазол-4,7-дион;
2-(2,5-дихлортиен-3-ил)-5-{[2-(диметиламино)этил]амино}-1,3-бензотиазол-4,7-дион;
2-(2,5-дихлортиен-3-ил)-6-{[2-(диметиламино)этил]амино}-1,3-бензотиазол-4,7-дион;
2-(2,5-дихлортиен-3-ил)-5-[(2-пирролидин-1-илэтил)амино]-1,3-бензотиазол-4,7-дион;
2-(2,5-дихлортиен-3-ил)-6-[(2-пирролидин-1-илэтил)амино]-1,3-бензотиазол-4,7-дион;
2-(2-фурил)-5-[(2-пирролидин-1-илэтил)амино]-1,3-бензотиазол-4,7-дион;
2-(2-фурил)-6-[(2-пирролидин-1-илэтил)амино]-1,3-бензотиазол-4,7-дион;
5-{[2-(диметиламино)этил]амино}-2-(2-метоксифенил)-1,3-бензотиазол-4,7-дион;
6-{[2-(диметиламино)этил]амино}-2-(2-метоксифенил)-1,3-бензотиазол-4,7-дион;
5-{[2-(диметиламино)этил]амино}-2-(2-фторфенил)-1,3-бензотиазол-4,7-дион;
6-{[2-(диметиламино)этил]амино}-2-(2-фторфенил)-1,3-бензотиазол-4,7-дион;
2-(2-фторфенил)-5-[(2-пирролидин-1-илэтил)амино]-1,3-бензотиазол-4,7-дион;
2-(2-фторфенил)-6-[(2-пирролидин-1-илэтил)амино]-1,3-бензотиазол-4,7-дион;
2-(4-фторфенил)-5-[(2-пирролидин-1-илэтил)амино]-1,3-бензотиазол-4,7-дион;
2-(4-фторфенил)-6-[(2-пирролидин-1-илэтил)амино]-1,3-бензотиазол-4,7-дион;
5-{[2-(диметиламино)этил]амино}-2-(4-фторфенил)-1,3-бензотиазол-4,7-дион;
6-{[2-(диметиламино)этил]амино}-2-(4-фторфенил)-1,3-бензотиазол-4,7-дион;
2-(2,6-дифторфенил)-5-[(2-пирролидин-1-илэтил)амино]-1,3-бензотиазол-4,7-дион;
2-(2,6-дифторфенил)-6-[(2-пирролидин-1-илэтил)амино]-1,3-бензотиазол-4,7-дион;
2-(2,6-дифторфенил)-5-{[2-(диметиламино)этил]амино}-1,3-бензотиазол-4,7-дион;
2-(2,6-дифторфенил)-6-{[2-(диметиламино)этил]амино}-1,3-бензотиазол-4,7-дион;
5-[[2-(диметиламино)этил](этил)амино]-2-метил-1,3-бензотиазол-4,7-дион;
5-[[2-(диметиламино)этил](метил)амино]-2-метил-1,3-бензотиазол-4,7-дион;
2-[2,6-дихлор-5-фтор-3-пиридил]-5-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-дион;
2-[2,6-дихлор-5-фтор-3-пиридил]-6-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-дион;
2-[2,6-дихлор-5-фтор-3-пиридил]-5-[(2-пирролидин-1-илэтил)амино]-1,3-бензоксазол-4,7-дион;
2-[2,6-дихлор-5-фтор-3-пиридил]-6-[(2-пирролидин-1-илэтил)амино]-1,3-бензоксазол-4,7-дион;
2-(2,4-дифторфенил)-5-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-дион;
2-(2,4-дифторфенил)-6-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-дион;
5-{[2-(диметиламино)этил]амино}-2-(2,3,4-трифторфенил)-1,3-бензоксазол-4,7-дион;
6-{[2-(диметиламино)этил]амино}-2-(2,3,4-трифторфенил)-1,3-бензоксазол-4,7-дион;
5-[(2-пирролидин-1-илэтил)амино]-2-(2,3,4-трифторфенил)-1,3-бензоксазол-4,7-дион;
6-[(2-пирролидин-1-илэтил)амино]-2-(2,3,4-трифторфенил)-1,3-бензоксазол-4,7-дион;
2-(3-фтор-4-метилфенил)-5-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-дион;
2-(3-фтор-4-метилфенил)-6-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-дион;
2-(3-фтор-4-метилфенил)-5-[(2-пирролидин-1-илэтил)амино]-1,3-бензоксазол-4,7-дион;
2-(3-фтор-4-метилфенил)-6-[(2-пирролидин-1-илэтил)амино]-1,3-бензоксазол-4,7-дион;
2-(4-хлорфенил)-5-{[2-(диметиламино)этил]амино}-1,3-бензотиазол-4,7-дион;
2-(4-хлорфенил)-6-{[2-(диметиламино)этил]амино}-1,3-бензотиазол-4,7-дион;
2-(4-хлорфенил)-5-[(2-пирролидин-1-илэтил)амино]-1,3-бензотиазол-4,7-дион;
2-(4-хлорфенил)-6-[(2-пирролидин-1-илэтил)амино]-1,3-бензотиазол-4,7-дион;
5-{[2-(диметиламино)этил]амино}-2-(2,3,4,5-тетрафторфенил)-1,3-бензотиазол-4,7-дион;
6-{[2-(диметиламино)этил]амино}-2-(2,3,4,5-тетрафторфенил)-1,3-бензотиазол-4,7-дион;
5-{[2-(диметиламино)этил]амино}-2-(3,4,5-трифторфенил)-1,3-бензотиазол-4,7-дион;
6-{[2-(диметиламино)этил]амино}-2-(3,4,5-трифторфенил)-1,3-бензотиазол-4,7-дион;
5-[(2-пирролидин-1-илэтил)амино]-2-(2,4,6-трифторфенил)-1,3-бензотиазол-4,7-дион;
6-[(2-пирролидин-1-илэтил)амино]-2-(2,4,6-трифторфенил)-1,3-бензотиазол-4,7-дион;
2-(1,3-бензодиоксол-5-ил)-5-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-дион;
2-(1,3-бензодиоксол-5-ил)-6-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-дион;
5-{[2-(диметиламино)этил]амино}-2-(4-этилфенил)-1,3-бензоксазол-4,7-дион;
6-{[2-(диметиламино)этил]амино}-2-(4-этилфенил)-1,3-бензоксазол-4,7-дион;
2-(4-этилфенил)-5-[(2-пирролидин-1-илэтил)амино]-1,3-бензоксазол-4,7-дион;
2-(4-этилфенил)-6-[(2-пирролидин-1-илэтил)амино]-1,3-бензоксазол-4,7-дион;
5-{[2-(диметиламино)этил]амино}-2-(2-фтор-6-метоксифенил)-1,3-бензоксазол-4,7-дион;
6-{[2-(диметиламино)этил]амино}-2-(2-фтор-6-метоксифенил)-1,3-бензоксазол-4,7-дион;
или фармацевтически приемлемую соль одного из них, и
фармацевтически приемлемый носитель.
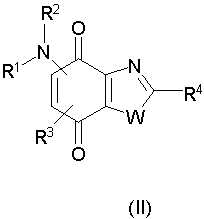
в которой
R1 представляет атом водорода или алкил, алкоксиалкил, алкилтиоалкил, циклоалкил, -(СН2)-Х-Y, - (СН2)-Z-NR5R6 или -CHR35R36, в котором R35 и R36 образуют вместе с атомом углерода, к которому они присоединены, инданил или тетралинил, или также R35 и R36 образуют вместе с атомом углерода, к которому они присоединены, насыщенный гетероцикл, содержащий 5-7 членов и 1-2 гетероатома, выбранных из О, N и S, где атомы азота указанного гетероцикла необязательно замещены радикалами, выбранными из алкила и бензила,
R1 также может, когда W является О, представлять собой карбоциклический арил, необязательно замещенный 1-3 заместителями, независимо выбранными из атома галогена и алкила, галогеналкила или алкокси,
X представляет связь или нормальный, или разветвленный алкилен, содержащий 1-5 атомов углерода,
Y представляет насыщенную углеродсодержащую циклическую систему, содержащую 1-3 конденсированных кольца, независимо выбранных из колец с 3-7 членами, или Y представляет насыщенный гетероцикл, содержащий 1-2 гетероатома, независимо выбранных из О, N или S, и соединенный с радикалом X посредством N- или СН-члена, где указанный насыщенный гетероцикл, кроме того, содержит 2-6 дополнительных членов, независимо выбранных из -CHR7-, -СО-, -NR8-, -О- и -S-, где R7 представляет атом водорода или алкил, и R8 представляет атом водорода или алкил, или аралкил, или также Y представляет карбоциклический или гетероциклический арил, необязательно замещенный 1-3 заместителями, независимо выбранными из группы, состоящей из атома галогена, алкила, галогеналкила, алкокси, галогеналкокси, гидрокси, нитро, циано, фенила, SO2NHR9 и NR10R11, где R9 представляет атом водорода или алкил, или фенил, и R10 и R11 независимо представляют алкил,
Z представляет связь или нормальный, или разветвленный алкилен, содержащий 1-5 атомов углерода,
R5 и R6 независимо выбраны из атома водорода, алкила, аралкила или -(СН2)n-OH, в котором n представляет целое число от 1 до 6,
или R5 представляет алкоксикарбонил, галогеналкоксикарбонил или аралкоксикарбонил, и R6 представляет атом водорода или метил,
или также R5 и R6 образуют вместе с атомом азота гетероцикл с 4-7 членами, содержащий 1-2 гетероатома, где члены, необходимые для замыкания гетероцикла, независимо выбраны из -CR12R13-, -O-, -S- и -NR14, где R12 и R13 независимо представляют, когда они имеются, атом водорода или алкил, и R14 представляет атом водорода или алкил, или аралкил, или также R14 представляет фенил, необязательно замещенный 1-3 заместителями, независимо выбранными из атома галогена и алкила, или алкокси,
R2 представляет атом водорода или алкил, или аралкил,
или также R1 и R2 образуют вместе с атомом азота гетероцикл с 4-8 членами, содержащий 1-2 гетероатома, где члены, необходимые для замыкания гетероцикла, независимо выбраны из -CR15R16-, -O-, -S- или -NR17, где R15 и R16 независимо представляют, когда они имеются, атом водорода или алкил, и R17 представляет атом водорода или алкил, или аралкил,
R3 представляет атом водорода, атом галогена или алкил, галогеналкил, алкокси или алкилтио;
R4 представляет алкил, циклоалкил, циклоалкилалкил, циано, амино, -CH2-COOR18, -CH2-CO-NR19R20 или -CH2-NR21R22, или R4 представляет карбоциклический или гетероциклический арил, необязательно замещенный 1-4 заместителями, независимо выбранными из атома галогена и алкила, галогеналкила, алкокси, галогеналкокси или NR37R38, или также R4 представляет фенил, имеющий два заместителя, которые вместе образуют метилендиокси или этилендиокси,
R18 представляет атом водорода или алкил,
R19 представляет атом водорода, алкил или аралкил, арильная группа которого необязательно замещена 1-3 заместителями, независимо выбранными из группы, состоящей из атома галогена, алкила, галогеналкила, алкокси, галогеналкокси, гидрокси, нитро, циано, фенила, SO2NHR23 и NR24R25, где R23 представляет атом водорода или алкил, или фенил, и R24 и R25 независимо представляют алкил,
R20 представляет атом водорода или алкил,
или также R19 и R20 образуют вместе с атомом азота гетероцикл с 4-7 членами, содержащий 1-2 гетероатома, где члены, необходимые для замыкания гетероцикла, независимо выбраны из
-CR26R27-, -O-, -S- или -NR28, где R26 и R27 независимо представляют, когда они имеются, атом водорода или алкил, и R28 представляет атом водорода или алкил, или аралкил, или также R28 представляет фенил, необязательно замещенный 1-3 заместителями, независимо выбранными из атома галогена и алкила, или алкокси,
R21 представляет атом водорода, алкил или аралкил, арильная группа которого необязательно замещена 1-3 заместителями, независимо выбранными из группы, состоящей из атома галогена, алкила, галогеналкила, алкокси, галогеналкокси, гидрокси, нитро, циано, фенила, SO2NHR29 и NR30R31, где R29 представляет атом водорода или алкил, или фенил, и R30 и R31 независимо представляют алкил,
R22 представляет атом водорода или алкил,
или также R21 и R22 образуют вместе с атомом азота гетероцикл с 4-7 членами, содержащий 1-2 гетероатома, где члены, необходимые для замыкания гетероцикла, независимо выбраны из -CR32R33-, -O-, -S- или -NR34, где R32 и R33 независимо представляют, когда они имеются, атом водорода или алкил, и R34 представляет атом водорода, алкил или аралкил, или также R34 представляет фенил, необязательно замещенный 1-3 заместителями, независимо выбранными из атома галогена и алкила, или алкокси,
R37 и R38 независимо выбраны из атома водорода и алкила, или R37 и R38 образуют вместе с атомом азота гетероцикл с 4-7 членами, содержащий 1-2 гетероатома, где члены, необходимые для замыкания гетероцикла, независимо выбраны из -CR39R40-, -O-, -S- или -NR41, где R39 и R40 независимо представляют, когда они имеются, атом водорода или алкил, и R41 представляет атом водорода или алкил; и
W представляет О или S;
необходимо понимать, что,
если W является S, и R4 представляет алкил, то тогда R1 не является атомом водорода или алкилом, или циклоалкилом, и/или R3 представляет атом водорода или алкил,
если W является S, и R4 представляет необязательно замещенный арил, то тогда R1 выбран из алкоксиалкила, алкилтиоалкила, циклоалкила, заместителей -(CH2)-X-Y и -(CH2)-Z-NR5R6;
или его соль.
2-метил-5-{[2-(4-морфолинил)этил]амино}-1,3-бензотиазол-4,7-дион;
5-{[2-(диметиламино)этил]амино}-2-метил-1,3-бензотиазол-4,7-дион;
5-{[6-(диметиламино)гексил]амино}-2-метил-1,3-бензотиазол-4,7-дион;
5-{[3-(диметиламино)-2,2-диметилпропил]амино}-2-метил-1,3-бензотиазол-4,7-дион;
2-метил-5-{[3-(4-метил-1-пиперазинил)пропил]амино}-1,3-бензотиазол-4,7-дион;
5-[(1-этилгексил)амино]-2-метил-1,3-бензотиазол-4,7-дион;
5-[(1-адамантилметил)амино]-2-метил-1,3-бензотиазол-4,7-дион;
2-метил-5-[(2-тиенилметил)амино]-1,3-бензотиазол-4,7-дион;
5-[(3-хлорбензил)амино]-2-метил-1,3-бензотиазол-4,7-дион;
2-метил-5-[(4-пиридинилметил)амино]-1,3-бензотиазол-4,7-дион;
2-метил-5-(пропиламино)-1,3-бензотиазол-4,7-дион;
5-{[3-(1Н-имидазол-1-ил)пропил]амино}-2-метил-1,3-бензотиазол-4,7-дион;
4-{2-[(2-метил-4,7-диоксо-4,7-дигидро-1,3-бензотиазол-5-ил)амино]этил}бензолсульфонамид;
5-(4-бензил-1-пиперазинил)-2-метил-1,3-бензотиазол-4,7-дион;
или его фармацевтически приемлемую соль.
5-[(2-метоксиэтил)амино]-2-метил-1,3-бензотиазол-4,7-дион;
2-метил-5-[(2-пирролидин-1-илэтил)амино]-1,3-бензотиазол-4,7-дион;
2-метил-5-[(2-пиперидин-1-илэтил)амино]-1,3-бензотиазол-4,7-дион;
5-{[2-(диизопропиламино)этил]амино}-2-метил-1,3-бензотиазол-4,7-дион;
5-[(1-бензилпирролидин-3-ил)амино]-2-метил-1,3-бензотиазол-4,7-дион;
5-{[3-(диметиламино)пропил]амино}-2-метил-1,3-бензотиазол-4,7-дион;
2-метил-5-{[2-(1-метилпирролидин-2-ил)этил]амино}-1,3-бензотиазол-4,7-дион;
2-метил-5-{[3-(2-метилпиперидин-1-ил)пропил]амино}-1,3-бензотиазол-4,7-дион;
5-{[4-(диметиламино)бутил]амино}-2-метил-1,3-бензотиазол-4,7-дион;
5-{[5-(диметиламино)пентил]амино}-2-метил-1,3-бензотиазол-4,7-дион;
5-(2,3-дигидро-1Н-инден-1-иламино)-2-метил-1,3-бензотиазол-4,7-дион;
5-{бензил[2-(диметиламино)зтил]амино}-2-метил-1,3-бензотиазол-4,7-дион;
2-метил-5-{[3-(метиламино)пропил]амино}-1,3-бензотиазол-4,7-дион;
5-[(3-аминопропил)амино]-2-метил-1,3-бензотиазол-4,7-дион;
6-хлор-5-{[2-(диметиламино)этил]амино}-2-метил-1,3-бензотиазол-4,7-дион;
6-бром-5-{[2-(диметиламино)этил]амино}-2-метил-1,3-бензотиазол-4,7-дион;
6-(бутилтио)-5-{[2-(диметиламино)этил]амино}-2-метил-1,3-бензотиазол-4,7-дион;
5-{[2-(диметиламино)этил]амино}-2-(морфолин-4-илметил)-1,3-бензотиазол-4,7-дион;
5-{[2-(диметиламино)этил]амино}-2-[(4-фенилпиперазин-1-ил)метил]-1,3-бензотиазол-4,7-дион;
5-{[2-(диметиламино)этил]амино}-2-(пиперидин-1-илметил)-1,3-бензотиазол-4,7-дион;
5-{[6-(диметиламино)гексил]амино}-2-этил-1,3-бензоксазол-4,7-дион;
2-этил-5-(4-метилпиперазин-1-ил)-1,3-бензоксазол-4,7-дион;
2-этил-5-[(1-этилгексил)амино]-1,3-бензоксазол-4,7-дион;
5-азокан-1-ил-2-этил-1,3-бензоксазол-4,7-дион;
2-этил-5-морфолин-4-ил-1,3-бензоксазол-4,7-дион;
5-{[2-(диметиламино)этил]амино}-2-этил-6-метил-1,3-бензоксазол-4,7-дион;
5-{[2-(диметиламино)этил]амино}-2-фенил-1,3-бензоксазол-4,7-дион;
5-{[6-(диметиламино)гексил]амино}-2-фенил-1,3-бензоксазол-4,7-дион;
2-(2,6-дифторфенил)-5-[(2-пирролидин-1-илэтил)амино]-1,3-бензоксазол-4,7-дион;
2-[4-(диэтиламино)фенил]-5-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-дион;
2-[4-(диэтиламино)фенил]-5-[(2-пирролидин-1-илэтил)амино]-1,3-бензоксазол-4,7-дион;
2-(4-хлорфенил)-5-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-дион;
2-(4-хлорфенил)-5-{[3-(диметиламино)пропил]амино}-1,3-бензоксазол-4,7-дион;
2-(4-хлорфенил)-5-{[4-(диметиламино)бутил]амино}-1,3-бензоксазол-4,7-дион;
или его фармацевтически приемлемую соль.
трет-бутил метил{3-[(2-метил-4,7-диоксо-4,7-дигидро-1,3-бензотиазол-5-ил)амино]пропил}карбамат;
трет-бутил 3-[(2-метил-4,7-диоксо-4,7-дигидро-1,3-бензотиазол-5-ил)амино]пропилкарбамат;
6-{[6-(диметиламино)гексил]амино}-2-этил-1,3-бензоксазол-4,7-дион;
2-этил-6-(4-метилпиперазин-1-ил)-1,3-бензоксазол-4,7-дион;
2-этил-6-[(1-этилгексил)амино]-1,3-бензоксазол-4,7-дион;
6-азокан-1-ил-2-этил-1,3-бензоксазол-4,7-дион;
2-этил-6-морфолин-4-ил-1,3-бензоксазол-4,7-дион;
6-{[2-(диметиламино)этил]амино}-2-фенил-1,3-бензоксазол-4,7-дион;
6-{[6-(диметиламино)гексил]амино}-2-фенил-1,3-бензоксазол-4,7-дион;
2-(2,6-дифторфенил)-6-[(2-пирролидин-1-илэтил)амино]-1,3-бензоксазол-4,7-дион;
2-[4-(диэтиламино)фенил]-6-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-дион;
2-[4-(диэтиламино)фенил]-6-[(2-пирролидин-1-илэтил)амино]-1,3-бензоксазол-4,7-дион;
2-(4-хлорфенил)-6-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-дион;
2-(4-хлорфенил)-6-{[3-(диметиламино)пропил]амино}-1,3-бензоксазол-4,7-дион;
2-(4-хлорфенил)-6-{[4-(диметиламино)бутил]амино}-1,3-бензоксазол-4,7-дион;
2-(2-фторфенил)-5-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-дион;
2-(2-фторфенил)-6-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-дион;
2-(2-фторфенил)-5-[(2-пирролидин-1-илэтил)амино]-1,3-бензоксазол-4,7-дион;
2-(2-фторфенил)-6-[(2-пирролидин-1-илэтил)амино]-1,3-бензоксазол-4,7-дион;
2-(2-бромфенил)-5-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-дион;
2-(2-бромфенил)-6-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-дион;
2-(2-бромфенил)-5-[(2-пирролидин-1-илэтил)амино]-1,3-бензоксазол-4,7-дион;
2-(2-бромфенил)-6-[(2-пирролидин-1-илэтил)амино]-1,3-бензоксазол-4,7-дион;
2-(2-бромфенил)-5-{[3-(диметиламино)пропил]амино}-1,3-бензоксазол-4,7-дион;
2-(2-бромфенил)-6-{[3-(диметиламино)пропил]амино}-1,3-бензоксазол-4,7-дион;
2-(2-хлорфенил)-5-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-дион;
2-(2-хлорфенил)-6-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-дион;
2-(2-хлорфенил)-5-[(2-пирролидин-1-илэтил)амино]-1,3-бензоксазол-4,7-дион;
2-(2-хлорфенил)-6-[(2-пирролидин-1-илэтил)амино]-1,3-бензоксазол-4,7-дион;
2-(3-бромфенил)-5-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-дион;
2-(3-бромфенил)-6-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-дион;
2-(4-бромфенил)-5-[(2-пирролидин-1-илэтил)амино]-1,3-бензоксазол-4,7-дион;
2-(4-бромфенил)-6-[(2-пирролидин-1-илэтил)амино]-1,3-бензоксазол-4,7-дион;
2-(4-бромфенил)-5-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-дион;
2-(4-бромфенил)-6-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-дион;
2-(4-фторфенил)-5-[(2-пирролидин-1-илэтил)амино]-1,3-бензоксазол-4,7-дион;
2-(4-фторфенил)-6-[(2-пирролидин-1-илэтил)амино]-1,3-бензоксазол-4,7-дион;
5-{[2-(диметиламино)этил]амино}-2-(4-фторфенил)-1,3-бензоксазол-4,7-дион;
6-{[2-(диметиламино)этил]амино}-2-(4-фторфенил)-1,3-бензоксазол-4,7-дион;
5-[(1-бензилпирролидин-3-ил)амино]-2-(4-фторфенил)-1,3-бензоксазол-4,7-дион;
6-[(1-бензилпирролидин-3-ил)амино]-2-(4-фторфенил)-1,3-бензоксазол-4,7-дион;
5-{[3-(диметиламино)пропил]амино}-2-(4-фторфенил)-1,3-бензоксазол-4,7-дион;
6-{[3-(диметиламино)пропил]амино}-2-(4-фторфенил)-1,3-бензоксазол-4,7-дион;
2-(3,5-дифторфенил)-5-[(2-пирролидин-1-илэтил)амино]-1,3-бензоксазол-4,7-дион;
2-(3,5-дифторфенил)-6-[(2-пирролидин-1-илэтил)амино]-1,3-бензоксазол-4,7-дион;
2-(3,5-дифторфенил)-5-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-дион;
2-(3,5-дифторфенил)-6-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-дион;
2-(2,5-дифторфенил)-5-[(2-пирролидин-1-илэтил)амино]-1,3-бензоксазол-4,7-дион;
2-(2,5-дифторфенил)-6-[(2-пирролидин-1-илэтил)амино]-1,3-бензоксазол-4,7-дион;
2-(2,5-дифторфенил)-5-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-дион;
2-(2,5-дифторфенил)-6-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-дион;
2-(2,3-дифторфенил)-5-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-дион;
2-(2,3-дифторфенил)-6-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-дион;
2-(2,3-дифторфенил)-5-[(2-пирролидин-1-илэтил)амино]-1,3-бензоксазол-4,7-дион;
2-(2,3-дифторфенил)-6-[(2-пирролидин-1-илэтил)амино]-1,3-бензоксазол-4,7-дион;
2-(2,3-дифторфенил)-5-{[3-(диметиламино)пропил]амино}-1,3-бензоксазол-4,7-дион;
2-(2,3-дифторфенил)-6-{[3-(диметиламино)пропил]амино}-1,3-бензоксазол-4,7-дион;
5-[(2-пирролидин-1-илэтил)амино]-2-(3,4,5-трифторфенил)-1,3-бензоксазол-4,7-дион;
6-[(2-пирролидин-1-илэтил)амино]-2-(3,4,5-трифторфенил)-1,3-бензоксазол-4,7-дион;
5-{[2-(диметиламино)этил]амино}-2-(3,4,5-трифторфенил)-1,3-бензоксазол-4,7-дион;
6-{[2-(диметиламино)этил]амино}-2-(3,4,5-трифторфенил)-1,3-бензоксазол-4,7-дион;
5-[(2-пирролидин-1-илэтил)амино]-2-(2,3,4,5-тетрафторфенил)-1,3-бензоксазол-4,7-дион;
6-[(2-пирролидин-1-илэтил)амино]-2-(2,3,4,5-тетрафторфенил)-1,3-бензоксазол-4,7-дион;
5-{[2-(диметиламино)этил]амино}-2-(2,3,4,5-тетрафторфенил)-1,3-бензоксазол-4,7-дион;
6-{[2-(диметиламино)этил]амино}-2-(2,3,4,5-тетрафторфенил)-1,3-бензоксазол-4,7-дион;
5-{[2-(диметиламино)этил]амино}-2-[2-фтор-6-(трифторметил)фенил]-1,3-бензоксазол-4,7-дион;
6-{[2-(диметиламино)этил]амино}-2-[2-фтор-6-(трифторметил)фенил]-1,3-бензоксазол-4,7-дион;
2-[2-фтор-6-(трифторметил)фенил]-5-[(2-пирролидин-1-илэтил)амино]-1,3-бензоксазол-4,7-дион;
2-[2-фтор-6-(трифторметил)фенил]-6-[(2-пирролидин-1-илэтил)амино]-1,3-бензоксазол-4,7-дион;
5-{[3-(диметиламино)пропил]амино}-2-[2-фтор-6-(трифторметил)фенил]-1,3-бензоксазол-4,7-дион;
6-{[3-(диметиламино)пропил]амино}-2-[2-фтор-6-(трифторметил)фенил]-1,3-бензоксазол-4,7-дион;
2-[2-хлор-5-(трифторметил)фенил]-5-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-дион;
2-[2-хлор-5-(трифторметил)фенил]-6-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-дион;
-2-[2-хлор-5-(трифторметил)фенил]-5-[(2-пирролидин-1-илэтил)амино]-1,3-бензоксазол-4,7-дион;
2-[2-хлор-5-(трифторметил)фенил]-6-[(2-пирролидин-1-илэтил)амино]-1,3-бензоксазол-4,7-дион;
2-[2-хлор-5-(трифторметил)фенил]-5-{[3-(диметиламино)пропил]амино}-1,3-бензоксазол-4,7-дион;
2-[2-хлор-5-(трифторметил)фенил]-6-{[3-(диметиламино)пропил]амино}-1,3-бензоксазол-4,7-дион;
2-[2-хлор-6-фторфенил]-5-{[3-(диметиламино)пропил]амино}-1,3-бензоксазол-4,7-дион;
2-[2-хлор-6-фторфенил]-6-{[3-(диметиламино)пропил]амино}-1,3-бензоксазол-4,7-дион;
2-[2-хлор-6-фторфенил]-5-[(2-пирролидин-1-илэтил)амино]-1,3-бензоксазол-4,7-дион;
2-[2-хлор-6-фторфенил]-6-[(2-пирролидин-1-илэтил)амино]-1,3-бензоксазол-4,7-дион;
2-[3,4-диметоксифенил]-5-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-дион;
2-[3,4-диметоксифенил]-6-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-дион;
2-[2-бром-3-пиридил]-5-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-дион;
2-[2-бром-3-пиридил]-6-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-дион;
2-циклогексил-5-[(2-пирролидин-1-илэтил)амино]-1,3-бензотиазол-4,7-дион;
2-циклогексил-6-[(2-пирролидин-1-илэтил)амино]-1,3-бензотиазол-4,7-дион;
2-циклогексил-5-[(2-пирролидин-1-илэтил)амино]-1,3-бензотиазол-4,7-дион;
2-циклогексил-6-[(2-пирролидин-1-илэтил)амино]-1,3-бензотиазол-4,7-дион;
5-[(2-пирролидин-1-илэтил)амино]-2-тиен-2-ил-1,3-бензотиазол-4,7-дион;
6-[(2-пирролидин-1-илэтил)амино]-2-тиен-2-ил-1,3-бензотиазол-4,7-дион;
2-(2,5-дихлортиен-3-ил)-5-{[2-(диметиламино)этил]амино}-1,3-бензотиазол-4,7-дион;
2-(2,5-дихлортиен-3-ил)-6-{[2-(диметиламино)этил]амино}-1,3-бензотиазол-4,7-дион;
2-(2,5-дихлортиен-3-ил)-5-[(2-пирролидин-1-илэтил)амино]-1,3-бензотиазол-4,7-дион;
2-(2,5-дихлортиен-3-ил)-6-[(2-пирролидин-1-илэтил)амино]-1,3-бензотиазол-4,7-дион;
2-(2-фурил)-5-[(2-пирролидин-1-илэтил)амино]-1,3-бензотиазол-4,7-дион;
2-(2-фурил)-6-[(2-пирролидин-1-илэтил)амино]-1,3-бензотиазол-4,7-дион;
5-{[2-(диметиламино)этил]амино}-2-(2-метоксифенил)-1,3-бензотиазол-4,7-дион;
6-{[2-(диметиламино)этил]амино}-2-(2-метоксифенил)-1,3-бензотиазол-4,7-дион;
5-{[2-(диметиламино)этил]амино}-2-(2-фторфенил)-1,3-бензотиазол-4,7-дион;
6-{[2-(диметиламино)этил]амино}-2-(2-фторфенил)-1,3-бензотиазол-4,7-дион;
2-(2-фторфенил)-5-[(2-пирролидин-1-илэтил)амино]-1,3-бензотиазол-4,7-дион;
2-(2-фторфенил)-6-[(2-пирролидин-1-илэтил)амино]-1,3-бензотиазол-4,7-дион;
2-(4-фторфенил)-5-[(2-пирролидин-1-илэтил)амино]-1,3-бензотиазол-4,7-дион;
2-(4-фторфенил)-6-[(2-пирролидин-1-илэтил)амино]-1,3-бензотиазол-4,7-дион;
5-{[2-(диметиламино)этил]амино}-2-(4-фторфенил)-1,3-бензотиазол-4,7-дион;
6-{[2-(диметиламино)этил]амино}-2-(4-фторфенил)-1,3-бензотиазол-4,7-дион;
2-(2,6-дифторфенил)-5-[(2-пирролидин-1-илэтил)амино]-1,3-бензотиазол-4,7-дион;
2-(2,6-дифторфенил)-6-[(2-пирролидин-1-илэтил)амино]-1,3-бензотиазол-4,7-дион;
2-(2,6-дифторфенил)-5-{[2-(диметиламино)этил]амино}-1,3-бензотиазол-4,7-дион;
2-(2,6-дифторфенил)-6-{[2-(диметиламино)этил]амино}-1,3-бензотиазол-4,7-дион;
5-[[2-(диметиламино)этил](этил)амино]-2-метил-1,3-бензотиазол-4,7-дион;
5-[[2-(диметиламино)этил](метил)амино]-2-метил-1,3-бензотиазол-4,7-дион;
2-[2,6-дихлор-5-фтор-3-пиридил]-5-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-дион;
2-[2,6-дихлор-5-фтор-3-пиридил]-6-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-дион;
2-[2,6-дихлор-5-фтор-3-пиридил]-5-[(2-пирролидин-1-илэтил)амино]-1,3-бензоксазол-4,7-дион;
2-[2,6-дихлор-5-фтор-3-пиридил]-6-[(2-пирролидин-1-илэтил)амино]-1,3-бензоксазол-4,7-дион;
2-(2,4-дифторфенил)-5-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-дион;
2-(2,4-дифторфенил)-6-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-дион;
5-{[2-(диметиламино)этил]амино}-2-(2,3,4-трифторфенил)-1,3-бензоксазол-4,7-дион;
6-{[2-(диметиламино)этил]амино}-2-(2,3,4-трифторфенил)-1,3-бензоксазол-4,7-дион;
5-[(2-пирролидин-1-илэтил)амино]-2-(2,3,4-трифторфенил)-1,3-бензоксазол-4,7-дион;
6-[(2-пирролидин-1-илэтил)амино]-2-(2,3,4-трифторфенил)-1,3-бензоксазол-4,7-дион;
2-(3-фтор-4-метилфенил)-5-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-дион;
2-(3-фтор-4-метилфенил)-6-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-дион;
2-(3-фтор-4-метилфенил)-5-[(2-пирролидин-1-илэтил)амино]-1,3-бензоксазол-4,7-дион;
2-(3-фтор-4-метилфенил)-6-[(2-пирролидин-1-илэтил)амино]-1,3-бензоксазол-4,7-дион;
2-(4-хлорфенил)-5-{[2-(диметиламино)этил]амино}-1,3-бензотиазол-4,7-дион;
2-(4-хлорфенил)-6-{[2-(диметиламино)этил]амино}-1,3-бензотиазол-4,7-дион;
2-(4-хлорфенил)-5-[(2-пирролидин-1-илэтил)амино]-1,3-бензотиазол-4,7-дион;
2-(4-хлорфенил)-6-[(2-пирролидин-1-илэтил)амино]-1,3-бензотиазол-4,7-дион;
5-{[2-(диметиламино)этил]амино}-2-(2,3,4,5-тетрафторфенил)-1,3-бензотиазол-4,7-дион;
6-{[2-(диметиламино)этил]амино}-2-(2,3,4,5-тетрафторфенил)-1,3-бензотиазол-4,7-дион;
5-{[2-(диметиламино)этил]амино}-2-(3,4,5-трифторфенил)-1,3-бензотиазол-4,7-дион;
6-{[2-(диметиламино)этил]амино}-2-(3,4,5-трифторфенил)-1,3-бензотиазол-4,7-дион;
5-[(2-пирролидин-1-илэтил)амино]-2-(2,4,6-трифторфенил)-1,3-бензотиазол-4,7-дион;
6-[(2-пирролидин-1-илэтил)амино]-2-(2,4,6-трифторфенил)-1,3-бензотиазол-4,7-дион;
2-(1,3-бензодиоксол-5-ил)-5-{[2-(диметиламино)этил]амино}-1,3-бензоксазол-4,7-дион;
2-(1,3-бензодиоксол-5-ил)-6-{[2-(диметиламино)этил]амине}-1,3-бензоксазол-4,7-дион;
5-{[2-(диметиламино)этил]амино}-2-(4-этилфенил)-1,3-бензоксазол-4,7-дион;
6-{[2-(диметиламино)этил]амино}-2-(4-этилфенил)-1,3-бензоксазол-4,7-дион;
2-(4-этилфенил)-5-[(2-пирролидин-1-илэтил)амино]-1,3-бензоксазол-4,7-дион;
2-(4-этилфенил)-6-[(2-пирролидин-1-илэтил)амино]-1,3-бензоксазол-4,7-дион;
5-{[2-(диметиламино)этил]амино}-2-(2-фтор-6-метоксифенил)-1,3-бензоксазол-4,7-дион;
6-{[2-(диметиламино)этил]амино}-2-(2-фтор-6-метоксифенил)-1,3-бензоксазол-4,7-дион;
или фармацевтически приемлемую соль, одного из них.
По пп.8, 12, 15, 20 установлен приоритет от 27.12.2001 согласно заявке 01 16889, FR.
По пп.9, 13, 16, 21 установлен приоритет от 25.07.2002 согласно заявке 01 16889, FR.
По пп.1-7, 10, 11, 14, 17-19, 22 установлен приоритет от 24.12.2002 согласно заявке PCT/FR02/04544.
| Печная вагонетка | 1987 |
|
SU1534275A1 |
| Прибор, замыкающий сигнальную цепь при повышении температуры | 1918 |
|
SU99A1 |
| ИНГИБИТОРЫ ФОСФАТАЗ cdc25 | 2001 |
|
RU2285521C2 |
Авторы
Даты
2008-06-20—Публикация
2002-12-24—Подача