Изобретение относится к синтетическим слоистым гидроксидам, а также к методам синтеза данного класса веществ.
Наиболее известен природный слоистый двойной гидроксокарбонат магния и алюминия - гидроталькит Mg6Al2(OH)16(CO3 2-)·4Н2O, аналогичные ему соединения называют гидроталькитоподобными. Данный класс соединений, относящийся к гидроксосолям, также называют слоистыми гидроксидами.
В природе существует слоистый двойной гидроксокарбонат магния и железа - пироаурит Mg6Al2(OH)16(CO3 2-)·4Н2O.
Элементарная ячейка слоистых гидроксидов описывается как октаэдр, в центре которого находится катион, а в вершинах - шесть атомов кислорода, октаэдры соединены в виде сетки и формируют слои, которые являются производными от структуры байерита. Изоморфное замещение двухзарядных катионов на трехзарядные приводит к возникновению избыточного положительного заряда, который компенсируется анионами в межслоевом пространстве. Данный класс веществ обладает гексагональной сингонией.
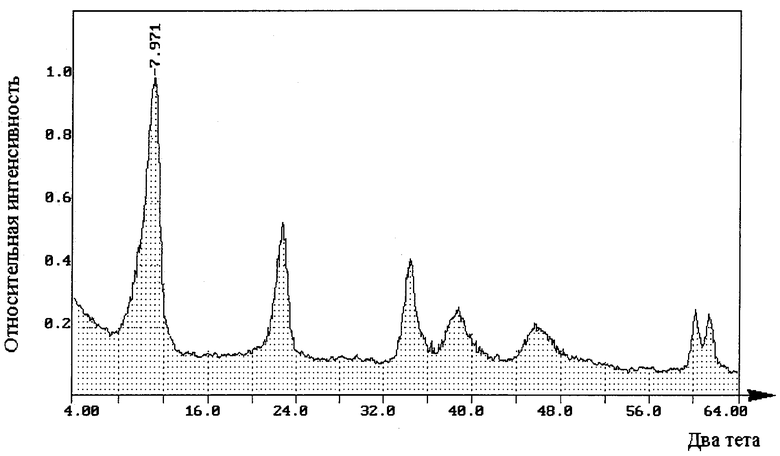
Для идентификации слоистой структуры гидроксидов используют рентгенофазовый анализ. Рентгеновские дифрактограммы слоистых гидроксидов имеют характерный вид: набор из 5 пиков, расстояние между которыми зависит от состава слоистого гидроксида, а интенсивность пиков убывает с увеличением угла дифракции два тета.
При больших углах (более 56°) имеется дуплет из шестого и седьмого пика, который также входит в характеристическую дифракционную картину для идентификации слоистой структуры.
Степень окристаллизованности вещества можно оценить по ширине пиков. Узкие интенсивные пики указывают на высокую степень кристалличности образцов, а также на однородность образцов и, следовательно, изотропность их физико-химических свойств.
Известны синтетические слоистые гидроксосоли с общей формулой
Mg(1-x)Mex(OH)2(A2-)x/2·nH2О, где Me - трехвалентный металл, а А2- -любой двухвалентный анион типа карбоната, сульфата и пр., например:
1. Известен синтетический магний-алюминиевый слоистый гидроксокарбонат и метод его получения (Елисеев А.А., Лукашин А.В., Вергетел А.А., Тарасов В.П., Третьяков Ю.Д. Исследование процессов кристаллизации слоистых двойных гидроксидов Mg-Al. // Доклады академии наук. - 2002. - т.387, - №6, - с.777-781).
Однако, судя по характеристике ширины пиков магний-алюминиевого слоистого гидроксокарбоната, представленной на рентгеновской дифрактограмме в упомянутом источнике, имеется разупорядочение анионов в межслоевом пространстве, т.е. образцы все-таки недостаточно кристаллизованы.
2. Известен также синтезированный гидроксосульфат магния-алюминия со слоистой структурой и метод его получения (Краснобаева О.Н., Носова Т.А., Елизарова Т.А., Данилов В.П. Двойные гидроксосульфаты магния-алюминия со слоистой структурой. // Ж. неорганической химии, 2001, - т.46, - №6, -с.899-902).
Приведенные рентгеновские дифрактограммы этих образцов имеют очень широкие и низкие пики, что свидетельствует о малой кристалличности образцов и неупорядоченности анионов.
3. В литературе упоминаются магний-скандиевые слоистые гидроксиды, но без указания на способ их получения (Rousselot I., Taviot-Gueho С., Besse J.-P. Synthesis and characterization of mixed Ga/Al-containing layered double hydroxides: study of their basic properties through the Knoevenagel condensation of benzaldehyde and ethyl cyanoacetate, and comparison to other LDHs // International Journal of Inorganic Materials, 1999, - V.1, - P.165-174, Reichele W.T. Synthesis of anionic clay minerals (mixed metal hydroxides, hydrotalcite). // Solid State lonics, 1986, - V. 22, - P.135-141).
Задача изобретения заключается в расширении арсенала уже известных синтезированных гидроталькитоподобных соединений с общей формулой Mg(1-x)Mex(OH)2(CO3)x/2·n Н2О, где в качестве трехвалентного металла Me - выступают одновременно алюминий и скандий, и создании способа получения такого соединения.
Техническим результатом является получение нового синтетического гидроталькитоподобного магний-скандий-алюминиевого соединения с улучшенными характеристиками, такими как высокая кристалличность и упорядоченность анионов в межслоевом пространстве.
Поставленная задача решается введением в состав слоистых гидроксидов одновременно двух трехвалентных катионов, а именно скандия и алюминия, что позволяет получить магний-скандий-алюминиевый слоистый гидроксид с формулой
Mg(1-x)ScyAlx-y(OH)2(CO3)x/2 · nH2О
где «y» меньше «х», а «х» не выше 0,4.
Смешанные слоистые гидроксиды, содержащие одновременно магний-алюминий-скандий, ранее не описаны ни в отечественной, ни в зарубежной литературе.
Введение в состав слоистых гидроксидов трехвалентного скандия позволило получить новое соединение, отличающееся хорошей закристаллизованностью и для которого характерна высокая упорядоченность анионов в межслоевом пространстве, что подтверждает рентгеновская дифрактограмма с высокими и узкими пиками (фиг.1).
Сопоставленный анализ с известными синтетическими слоистыми гидроксосолями показывает, что заявленное изобретение соответствует критериям «новизна» и «изобретательский уровень» по составу гидроталькитоподобного соединения с общей формулой Mg(1-x)Mex(OH)2(CO3)x/2·nH2О, где в качестве трехвалентного Me выступают одновременно алюминий и скандий:
- магний-скандий-алюминиевый слоистый гидроксид Mg(1-x)ScyAlx-y(OH)2(CO3)x/2·nH2О, причем «у» меньше «х», а «х» не выше 0,4 и имеющее характеристику дифракции рентгеновских лучей с высокими и узкими пиками (фиг.1), что свидетельствует о высокой кристалличности продукта и об упорядоченности анионов в межслоевом пространстве, соответственно данным, полученным при идентификации указанных слоистых гидроксидов путем проведения рентгенофазового анализа на рентгеновском дифрактометре ДРОН-3 (шаг сканирования по 2θ 0,5°; излучение CuKα).
Известен способ синтеза слоистых гидроксидов, например, гидроксосульфата магния-алюминия (Краснобаева О.Н., Носова ТА., Елизарова ТА., Данилов В.П. Двойные гидроксосульфаты магния-алюминия со слоистой структурой. // Ж. неорганической химии, 2001, - т.46, - №6, -с.899-902), включающий осаждение из 2N растворов сульфатов магния и алюминия раствором 2N гидроксида натрия при 50-70°С до рН 7,5-7,8, выдерживание смеси при 60-75°С на масляной бане в закрытых колбах в течение 2 недель, отделение осадков от раствора фильтрованием и промывку 50% водным раствором ацетона.
Данный способ обладает следующими недостатками: длительное термостатирование, использование для промывки ацетона, и при этом недостаточная кристаллизация конечного продукта и низкая упорядоченность анионов в межслоевом пространстве готового продукта.
Наиболее близким по существу является способ синтеза (Елисеев А.А., Лукашин А.В., Вергетел А.А., Тарасов В.П., Третьяков Ю.Д. Исследование процессов кристаллизации слоистых двойных гидроксидов Mg-Al. // Доклады академии наук. - 2002. - т.387, - №6, - с.777-781), включающий осаждение гидроталькитоподобных соединений из растворов нитратов магния и алюминия (Mg2+: Al3+=3:1, общая концентрация катионов 1М), раствором карбоната и гидроксида натрия ([СО3 2-]:[OH-]=1:6, общая концентрация анионов 3М), при постоянном значении рН 10,0±0,1, термостатирование при 80°С в течение 5 суток.
Недостатком данного способа является также длительность процесса, необходимость поддержания постоянного рН, при этом недостаточная кристаллизация и низкая упорядоченность анионов в межслоевом пространстве, что может являться причиной неоднородности физико-химических свойств готового продукта.
Предложенное изобретение от указанного способа, включающего осаждение гидроталькитоподобных соединений из раствора солей двухвалентного магния и трехвалентного металла раствором-осадителем, содержащим карбонат и гидроксид натрия, термостатирование выпавшего осадка, отличается тем, что:
раствор для осаждения содержит хлориды или нитраты металлов Mg2+ и Ме3+, причем в качестве трехвалентного металла используют одновременно алюминий Al3+ и скандий Sc3+;
концентрация как раствора для осаждения, так и раствора-осадителя не должна быть более 3М, т.к. повышение концентрации приводит к повышенной густоте реакционной смеси и невозможности из-за этого равномерного прохождения реакции по всему объему, что в конечном итоге препятствует получению необходимой гомогенности конечного продукта;
соотношение ионов в растворе для осаждения и в растворе-осадителе должно соответствовать: Me3+: Ме2+: [СО3 2-]:[ОН-]=1:3:1: 8, при этом нет необходимости поддерживать постоянный рН среды,
термостатирование проводят при 96-98°С в течение 2 суток, полученный осадок гидроталькитоподобного соединения трижды подвергают анионному обмену с Na2СО3, после промывают дистиллированной водой до отрицательной качественной реакции на ион Na+, сушку производят при 80-105°С.
Соответствие критериям «новизна» и «изобретательский уровень» предложенного способа получения заявленных слоистых гидроксидов подтверждают:
выявленная возможность использования в качестве трехвалентного металла одновременно алюминия Al3+ и скандия Sc3+ в виде [ScyAlx-y], где «у» меньше «х»,
проведение термостатирования при 96-98°С, что позволяет сократить длительность термостатирования до 2 суток. Снижение температуры ухудшает характеристику предложенного продукта, а повышение температуры термостатирования выше 100°С требует использования специального оборудования, т.е. дополнительных затрат. При указанной температуре уже через двое суток получают готовый продукт с высокими и узкими характеристическими пиками рентгеновских дифрактограмм, которые подтверждают высокое качество готового продукта, а именно гомогенность и изотропность физико-химических свойств.
Заявленное изобретение характеризует изображение, приведенное на чертеже, рентгеновская дифрактограмма магний-скандиево-алюминиевого слоистого гидроксида, полученного предложенным способом.
Примеры использования предложенного способа для получения нового магний-скандий-алюминиевого слоистого гидроксида Mg(1-x)ScyAlx-y(OH)2(CO3)x/2·nH2О.
Пример 1.
При синтезе магний-скандий-алюминиевого слоистого гидроксида к смеси растворов нитрата скандия, нитрата алюминия и нитрата магния, прикапывали со скоростью 3-5 мл/мин при комнатной температуре раствор-осадитель, который содержал гидроксид натрия и карбонат натрия. Общая концентрация солей металлов равна общей концентрации раствора-осадителя и составляет 2М. Навески веществ для приготовления растворов рассчитаны из соотношения: Ме3+: Mg2+: [ОН-]: [СО3 2-]=1:3:8:1, где в качестве трехвалентного металла выступают одновременно Al3+ и Sc3+ в соотношении 9:1.
Осажденные образцы термостатировали в маточном растворе при 96°С в течение двух суток.
Затем после охлаждения до комнатной температуры маточный раствор декантировали и осадок слоистого гидроксида подвергали анионному обмену с Na2СО3. Операцию повторили три раза. После отстаивания растворы декантировали и многократно промывали дистиллированной водой, пока качественная реакция на натрий не даст отрицательный результат. Образцы высушивали при 105°С.
Проведенный химический и термогравиметрический анализ позволили рассчитать химическую формулу полученного продукта: Mg0,682Al0,284Sc0,034(OH)2(CO3)0,159·0,83 Н2О, который имеет характеристику дифракции рентгеновских лучей с высокими и узкими пиками, представленную на чертеже.
Таким образом, предложенный способ позволяет за короткий промежуток времени получить хорошо закристаллизованные образцы нового гидроталькитоподобного магний - скандий - алюминиевого соединения с общей формулой Mg(1-x)Mex(OH)2(CO3)x/2·nH2О, где х не выше 0,4, а в качестве трехвалентного металла выступают одновременно скандий и алюминий в виде ScyAlx-y, где «у» меньше «х». Высокие и узкие характеристические пики рентгеновских дифрактограмм данного соединения говорят о гомогенности образцов и, следовательно, об изотропности их физико-химических свойств, что позволит найти им широкое применение.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ГИДРОТАЛЬКИТОПОДОБНЫХ СОЕДИНЕНИЙ | 2008 |
|
RU2361814C1 |
| СЛОИСТЫЙ ГИДРОКСИД СО СТРУКТУРОЙ ГИДРОТАЛЬКИТА, СОДЕРЖАЩИЙ НИКЕЛЬ В СТЕПЕНИ ОКИСЛЕНИЯ +3, И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2013 |
|
RU2540402C1 |
| Способ получения гидроталькитоподобных соединений | 2015 |
|
RU2611526C1 |
| Слоистый двойной гидроксид со структурой гидроталькита состава Ni/AlHo | 2022 |
|
RU2799181C1 |
| Способ получения слоистого гидроксида магния и алюминия | 2017 |
|
RU2678007C1 |
| Нанокомпозитный материал на основе титаната калия | 2021 |
|
RU2766089C1 |
| СПОСОБ ПОЛУЧЕНИЯ СЛОИСТОГО ДВОЙНОГО ГИДРОКСИДА, МОДИФИЦИРОВАННОГО ОРГАНИЧЕСКИМИ СОЕДИНЕНИЯМИ | 2006 |
|
RU2426688C2 |
| Способ получения кобальт-индиевого слоистого двойного гидроксида | 2024 |
|
RU2837869C1 |
| СПОСОБ ПОЛУЧЕНИЯ МАГНИТНОГО КОМПОЗИТА НА ОСНОВЕ МАГНИТНОГО ОКСИДА ЖЕЛЕЗА И СЛОИСТОГО ДВОЙНОГО ГИДРОКСИДА | 2017 |
|
RU2678024C1 |
| СПОСОБ ПОЛУЧЕНИЯ ОРГАНИЧЕСКИ МОДИФИЦИРОВАННОГО СЛОИСТОГО ДВОЙНОГО ГИДРОКСИДА | 2006 |
|
RU2424975C2 |
Изобретение относится к области химии, в частности к синтетическим слоистым гидроксидам общей формулы Mg(1-x)Mex(OH)2(CO3)x/2·nH2O где в качестве трехвалентного металла Me выступают одновременно скандий и алюминий в виде ScyAlx-y, причем «y» меньше «х», а «х» не выше 0,4. Способ заключается в том, что осаждают гидроталькитоподобное соединение из раствора солей двухвалентного магния и трехвалентных скандия и алюминия добавлением раствора-осадителя, содержащего гидроксид натрия и карбонат натрия, при этом общая концентрация солей металлов в растворе для осаждения, содержащем хлориды или нитраты металлов Mg2+, Al3+ и Sc3+, составляет не более 3 М, и общая концентрация раствора-осадителя составляет не более 3 М. Навески веществ для приготовления растворов для осаждения и раствора-осадителя рассчитывают из соотношения ионов в растворе: [Al3+ и Sc3+]:Mg2+:[ОН'']:[СО3 2'']=1:3:8:1. Термостатируют выпавший осадок в маточном растворе при 96-98°С в течение двух суток, затем охлаждают до комнатной температуры, маточный раствор с осадком слоистого гидроксида декантируют, затем трижды подвергают анионному обмену с Na2СО3, после отстаивания раствор декантируют и осадок промывают дистиллированной водой до получения отрицательного результата на наличие иона натрия. После чего производят сушку осадка при 80-105°С. Изобретение позволяет получить новое гидроталькитоподобное соединение. 2 н.п. ф-лы, 1 ил.
| WO 2005003034 A1, 13.01.2005 | |||
| СИНТЕТИЧЕСКИЙ МЕЙКСНЕРИТНЫЙ ПРОДУКТ (ВАРИАНТЫ) И СПОСОБ ЕГО ИЗГОТОВЛЕНИЯ | 1995 |
|
RU2155710C2 |
| Internet, STN, on the WEB, БД Chemical abstract, (CA), 133:143940, International Journal of Inorganic Materials, 1999, 1(2), 165-174 | |||
| Internet, STN, on the WEB, БД Chemical abstract, (CA), 130:75208, Journal of Materials Chemestry, 1998, 8(11), 2507-2514 | |||
| Internet, STN, on the WEB, БД | |||
Авторы
Даты
2008-08-10—Публикация
2006-10-10—Подача