Испрашивается приоритет в соответствии с временной заявкой на патент США №06/373766, поданной 19 апреля 2002, которая приведена здесь в качестве ссылки в полном объеме.
Область изобретения
Настоящее изобретение относится к способу снижения частоты сердечных сокращений при сведении к минимуму нежелательных побочных эффектов, который заключается во введении низких доз агониста рецептора аденозина A1 в сочетании с низкими дозами бета-блокатора, или блокатора кальциевых каналов, или сердечного гликозида.
Предпосылки изобретения
Аритмии представляют собой патологические сердечные ритмы, которые возникают либо в предсердии, либо в желудочках. Аритмии, возникающие в предсердии, называются предсердными аритмиями, и к ним относятся фибрилляция предсердий, трепетание предсердий и пароксизмальная предсердная тахикардия (PSVT). Аритмии, возникающие в желудочках, называются желудочковыми аритмиями и представляют собой группу расстройств различной этиологии, включая идиопатическую желудочковую тахикардию, фибрилляцию желудочков и хаотическую полиморфную желудочковую тахикардию (TdP). Аритмии могут варьировать от второстепенных, асимптоматических клинических признаков до угрожающих жизни патологий, в значительном проценте случаев они являются причиной смерти человека. Таким образом, желательно разработать способы, смягчающие эффекты аритмий.
В настоящее время существует большое количество противоаритмических препаратов, и их классификация дана ниже. К I классу противоартимических препаратов относятся блокаторы натриевых каналов; ко II классу относятся бета-блокаторы; к III классу относятся препараты с длительным действием (обычно блокаторы калиевых каналов); и к IV классу относятся блокаторы кальциевых каналов. Сердечные гликозиды, например препараты наперстянки, также являются эффективными препаратами для лечения аритмии, но начало их действия отсрочено по времени (приблизительно 30 минут) и их пик эффектов не регистрируется через ≥3-4 часов после введения. Кроме того, препараты наперстянки являются токсичными в дозах, близких к терапевтической дозе, что ограничивает применение этого соединения.
На самом деле, все вышеуказанные классы имеют большое количество ограничений. Например, бета-блокаторы, такие как пропранолол и эсмолол, и блокаторы кальциевых каналов, например верапамил, бепридил и дилтиазем, могут вызывать повышение давления, потенциально обладают отрицательными инотропными эффектами и к тому же могут вызывать новую аритмию, включая TdP.
Аденозин, который широко распространен в природе, является другим соединением, которое обладает противоаритмической активностью, благодаря своей способности при определенных уровнях доз замедлять проводимость в атрио-вентрикулярном узле. Антиаритмические эффекты аденозина обусловлены исключительно его взаимодействием с подтипом рецептора аденозина A1. Однако, хотя аденозин очень эффективен для снижения аритмии, одновременно с этим он также связывается с другими подтипами рецепторов аденозина (А2А, А2в и А3), что приводит к нежелательным подобным эффектам, таким как расширение сосудов, изменения в сердечном ритме, деградация тучных клеток и тому подобное. Аденозин также имеет короткий период полураспада (˜10 сек), что делает его неэффективным при лечении состояний, при которых необходимо длительное лечебное действие.
Соединения, которые являются агонистами рецепторов аденозина A1, хорошо известны. Например, новый класс агонистов, которые связываются с рецепторами аденозина A1 и эффективны при лечении аритмии, описан в патенте США No. 5789416 и в патенте США No. 10/194335, полное описание которых приведено здесь в качестве ссылки.
Эти соединения обладают высокой специфичностью в отношении подтипа рецептора аденозина A1, но как и все терапевтические соединения, могут потенциально вызывать побочные эффекты.
В целом, противоаритмические агенты имеют минимальную разницу между дозой, требуемой для получения желательного противоаритмического эффекта, и дозой, которая дает неблагоприятный эффект. Следовательно, было бы желательно разработать способ лечения аритмии, который был бы эффективен при низких дозах (или минимальных дозах) активного агента, таким образом, понижая вероятность побочных эффектов. Авторами было обнаружено, что при низких дозах агонисты рецептора аденозина A1, предпочтительно, частичные агонисты и, более предпочтительно, селективные агонисты рецептора аденозина A1, могут применяться в сочетании с низкими дозами бета-блокаторов, блокаторов кальциевого канала или сердечных гликозидов и обеспечивать эффективное лечение аритмии с минимальными побочными эффектами, характерными для бета-блокаторов, блокаторов кальциевого канала, сердечных гликозидов и агонистов рецептора аденозина A1, которые могут возникать при их самостоятельном применении. Также было обнаружено, что при низких дозах сочетания этих агентов действуют синергически, таким образом, еще сильней снижая вероятность побочных эффектов. Также было обнаружено, что сочетание агониста рецептора аденозина A1 с бета-блокатором может использоваться при лечении сердечной недостаточности, включая ишемическую болезнь сердца, застойную сердечную недостаточность, синдром сердечной недостаточности, повышенное давление и тому подобное.
Следовательно, новый и эффективный способ снижения частоты сердечных сокращений обеспечивает нормализацию синусового ритма без замедления синусового ритма и фактически не имеет нежелательных побочных эффектов, таких как изменение среднего артериального давления, кровяного давления, повышение сердечного ритма, TdP или других неблагоприятных эффектов.
Краткое описание изобретения
Объектом изобретения является эффективный способ снижения частоты сердечных сокращений у млекопитающих, при котором снижаются побочные эффекты. Таким образом, в соответствии с первым аспектом, настоящее изобретение относится к способу снижения частоты сердечных сокращений у млекопитающих, который заключается во введении терапевтически эффективной минимальной дозы агониста рецептора аденозина A1 в сочетании с терапевтически эффективной минимальной дозой бета-блокатора, блокатора кальциевых каналов, или сердечного гликозида млекопитающему, нуждающемуся в таком лечении.
В первом варианте осуществления агонист рецептора аденозина A1, который может быть использован согласно изобретению, представляет собой соединение формулы I:
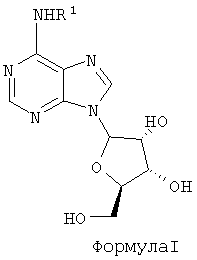
где
R1 представляет собой необязательно замещенную гетероциклическую группу, предпочтительно, моноциклическую. Эффективная доза предпочтительно находится в диапазоне 0,0001-0,05 мг/кг, более предпочтительно, 0,0005-0,02 мг/кг.
В предпочтительном варианте осуществления R1 представляет собой 3-тетрагидрофуранил, 3-тетрагидротиофуранил, 4-пиранил или 4-тиопиранил. Наиболее предпочтительным соединением формулы I является 6-(3-(R)-N-аминотетрагидрофуранил)пурин рибозид (здесь называемый CVT-510).
В другом варианте осуществления агонист рецептора аденозина А1, эффективный по данному изобретению, представляет собой соединение формулы II:
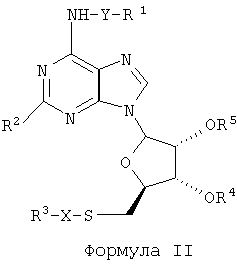
где
R1 представляет собой необязательно замещенный алкил, необязательно замещенный циклоалкил, необязательно замещенный арил или необязательно замещенный гетероарил;
R2 представляет собой водород, галоген, трифторметил, необязательно замещенный ацил или циано;
R3 необязательно представляет собой замещенный алкил, необязательно замещенный циклоалкил, необязательно замещенный арил; необязательно замещенный гетероарил или необязательно замещенную гетероциклическую группу,
R4 и R5 независимо представляют собой водород или необязательно замещенный ацил; и
X и Y независимо представляют собой ковалентную связь или необязательно замещенный алкилен.
Эффективная доза, предпочтительно, находится в диапазоне от 0,1 до 200 мг/кг, более предпочтительно, от 0,5 до 50 мг/кг.
Наиболее предпочтительным соединением формулы II является соединение, где R1 представляет собой 2-гидроксициклопентил, X и Y представляют собой ковалентные связи, R2, R3 и R4 представляют собой водород, и R5 представляет собой 2-фторфенил, наиболее предпочтительно, 2-{6-[((1R,2R)-2-гидроксициклопентил)амино]пурин-9-ил}(4S,5S,3R)-5-[(2-фторфенилтио)метил]оксолан-3,4-диол, называемый здесь CVT-3619.
Предпочтительные бета-блокаторы включают в себя атенолол, эсмолол, соталол и пропранолол. Более предпочтительным является эсмолол. Предпочтительная эффективная доза находится в диапазоне от 0,01 до 100 мг/кг, более предпочтительно, в диапазоне от 0,1 до 10 мг/кг.
Предпочтительные блокаторы кальциевых каналов включают в себя амлодипин, бепридил, дилтиазем, фелодипин, израдипин, никардипин, нифедипин, нимодипин и верапамил. Предпочтительная эффективная доза находится в диапазоне от 0,01 до 50 мг/кг, более предпочтительно, в диапазоне от 0,1 до 10 мг/кг.
Предпочтительные сердечные гликозиды включают в себя дигоксин и дигитоксин.
Одним из предпочтительных вариантов осуществления изобретения является способ снижения частоты сердечных сокращений у млекопитающих, который заключается во введении терапевтически эффективной минимальной дозы CVT-510 в сочетании с терапевтически эффективной минимальной дозой бета-блокатора, предпочтительно, эсмолола, атенолола, сотолола или пропранола, более предпочтительно, эсмолола, млекопитающим, нуждающимся в таком лечении.
Другим предпочтительным вариантом осуществления изобретения является способ снижения частоты сердечных сокращений у млекопитающих, который заключается во введении терапевтически эффективной минимальной дозы CVT-3619 и терапевтически эффективной минимальной дозы бета-блокатора, предпочтительно, эсмолола, атенолола, сотолола или пропранола, более предпочтительно, эсмолола, млекопитающим, нуждающимся в таком лечении.
Еще одним предпочтительным вариантом осуществления изобретения является способ снижения частоты сердечных сокращений у млекопитающего, который заключается во введении терапевтически эффективной минимальной дозы CVT-510, или терапевтически эффективной минимальной дозы CVT-3619, в сочетании с терапевтически эффективной минимальной дозой блокатора кальциевых каналов, предпочтительно, верапамила, млекопитающим, нуждающимся в таком лечении.
Третьим предпочтительным вариантом осуществления изобретения является способ снижения частоты сердечных сокращений у млекопитающих, который заключается во введении терапевтически эффективной минимальной дозы CVT-510, или терапевтически эффективной минимальной дозы CVT-3619, в сочетании с терапевтически эффективной минимальной дозой сердечного гликозида, предпочтительно, дигоксина, млекопитающим, нуждающимся в таком лечении.
В соответствии с другим аспектом изобретение относится к фармацевтической композиции, эффективной при лечении аритмий у млекопитающего, содержащей терапевтически эффективную минимальную дозу агониста рецептора аденозина А1 и терапевтически эффективную минимальную дозу бета-блокатора, и по крайней мере один фармацевтически приемлемый эксципиент.
Один из предпочтительных вариантов осуществления изобретения представляет собой фармацевтическую композицию для снижения частоты сердечных сокращений у млекопитающих, содержащую терапевтически эффективную минимальную дозу соединения формулы I, более предпочтительно, CVT-510, и терапевтически эффективную минимальную дозу бета-блокатора, предпочтительно, эсмолола, атенолола, сотолола или пропранола, более предпочтительно, эсмолола, у млекопитающих, нуждающихся в таком лечении. Доза соединения формулы I предпочтительно находится в диапазоне 0,0001-0,05 мг/кг, более предпочтительно, 0,0005-0,02 мг/кг, и доза бета-блокатора находится в диапазоне от 0,01 до 100 мг/кг, более предпочтительно, в диапазоне от 0,1 до 10 мг/кг.
Другим предпочтительным вариантом осуществления изобретения является фармацевтическая композиция для снижения частоты сердечных сокращений у млекопитающих, содержащая терапевтически эффективную минимальную дозу соединения формулы II, более предпочтительно, CVT-3619, и терапевтически эффективную минимальную дозу бета-блокатора, предпочтительно, эсмолола, атенолола, сотолола или пропранола, более предпочтительно, эсмолола, у млекопитающих, нуждающихся в таком лечении. Доза предпочтительно находится в диапазоне от 0,1 до 200 мг/кг, более предпочтительно, от 0,5 до 25 мг/кг, и доза бета-блокатора находится в диапазоне от 0,01 до 100 мг/кг, более предпочтительно, в диапазоне от 0,1 до 10 мг/кг.
В соответствии с еще одним аспектом изобретение относится к способу лечения сердечной недостаточности у млекопитающих, который заключается во введении терапевтически эффективной минимальной дозы агониста рецептора аденозина А1 в сочетании с терапевтически эффективной минимальной дозой бета-блокатора млекопитающим, нуждающимся в таком лечении.
Описание фигур
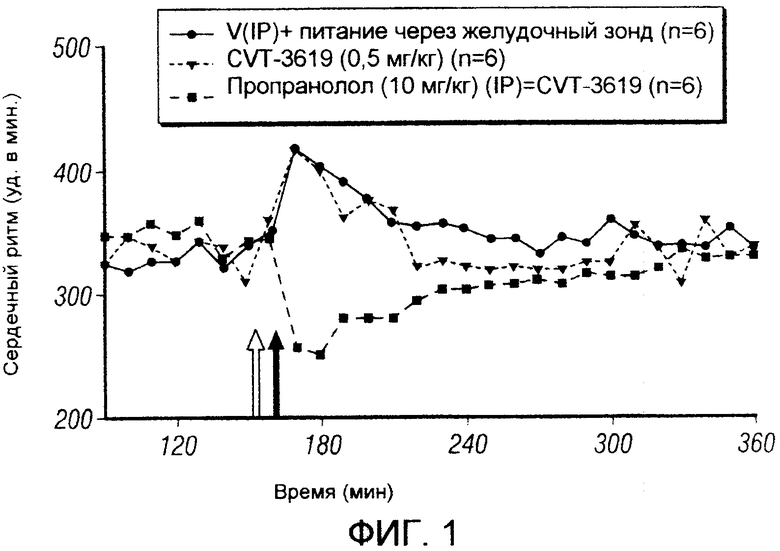
Фигура 1. Сравнение эффекта CVT-3619, вводимого самостоятельно, и CVT-3619, вводимого в сочетании с пропранололом, на сердечный ритм.
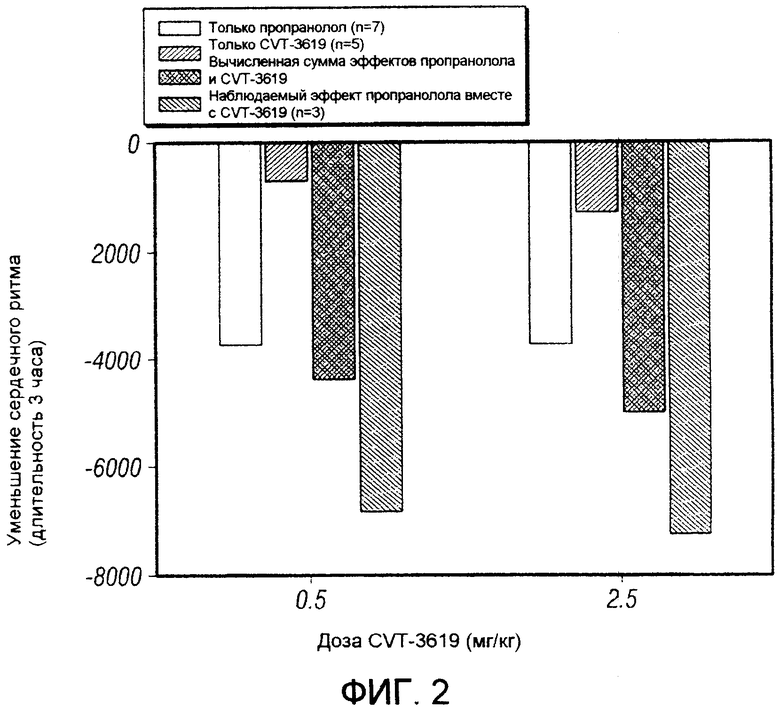
Фигура 2. Сравнение эффекта CVT-3619, вводимого самостоятельно, и CVT-3619, вводимого в сочетании с пропранололом, на сердечный ритм.
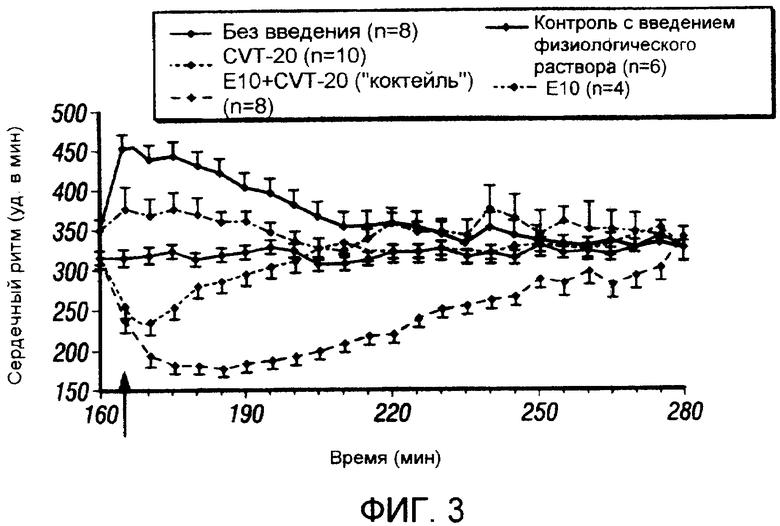
Фигура 3. Сравнение эффекта 20 мкг/кг CVT-510, 10 мг/кг эсмолола и сочетания 20 мкг/кг CVT-510 и 10 мг/кг эсмолола на сердечный ритм.
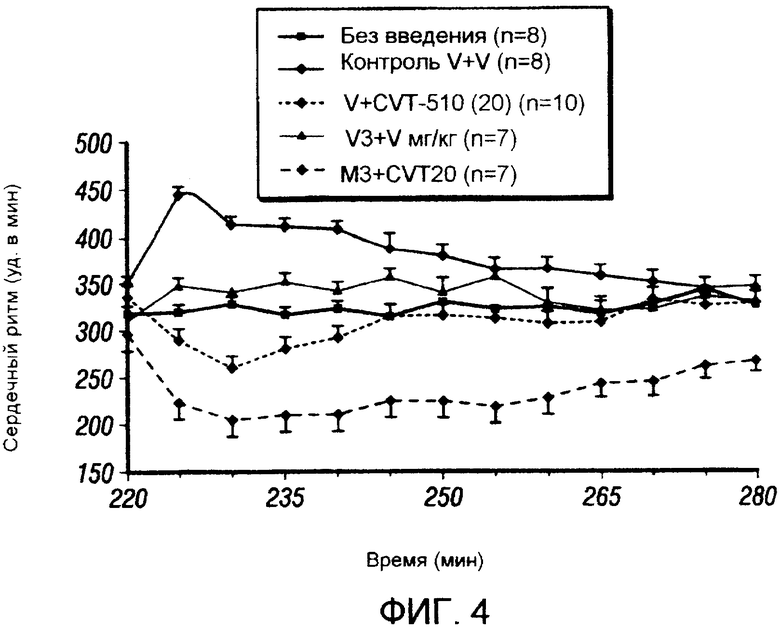
Фигура 4. Сравнение эффекта 20 мкг/кг CVT-510, 3 мг/кг эсмолола и сочетания 20 мкг/кг CVT-510 и 3 мг/кг эсмолола на сердечный ритм.
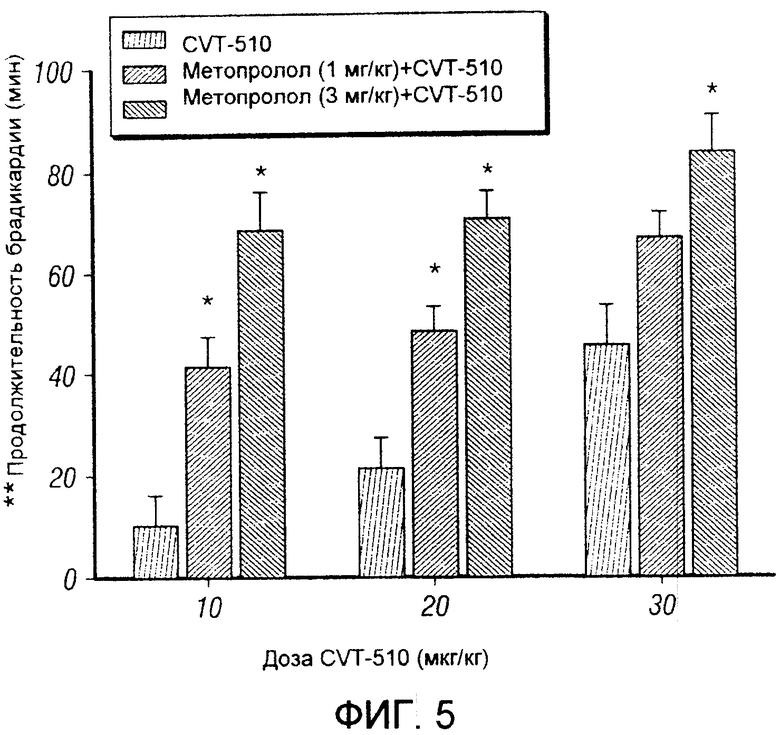
Фигура 5. Сравнение эффекта 10 мкг/кг, 20 мкг/кг и 30 мкг/кг доз CVT-510, 1 мкг/кг и 3 мг/кг эсмолола и сочетания 20 мкг/кг CVT-510, и 1, и 3 мг/кг эсмолола на продолжительность брадикардии.
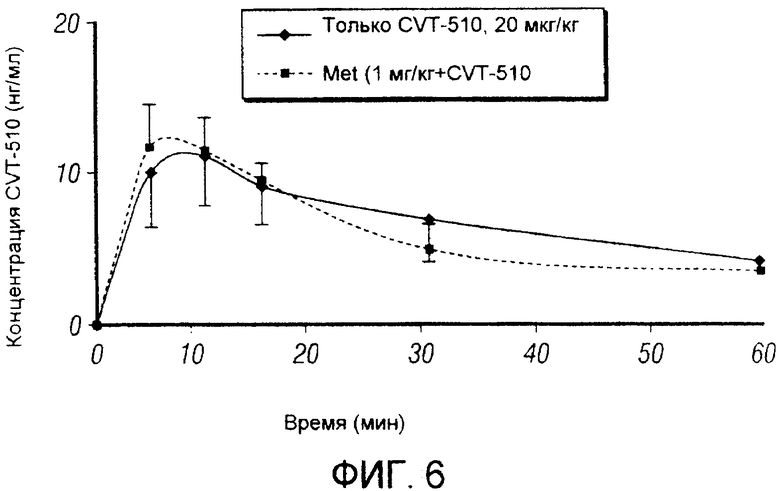
Фигура 6. Сравнение уровней плазмы при самостоятельном введении CVT-510 и сочетания CVT-510 и метопролола.
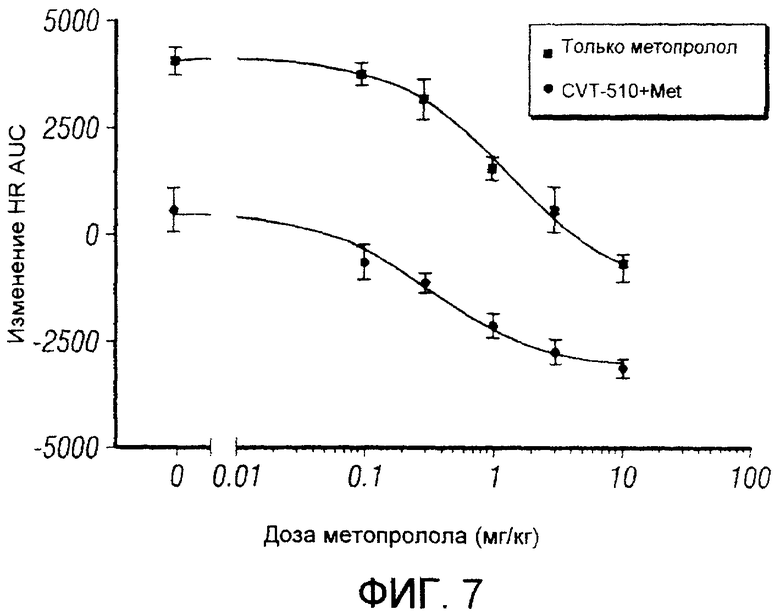
Фигура 7. Кривая доза-ответ для метопролола в отсутствие и присутствии CVT-510.
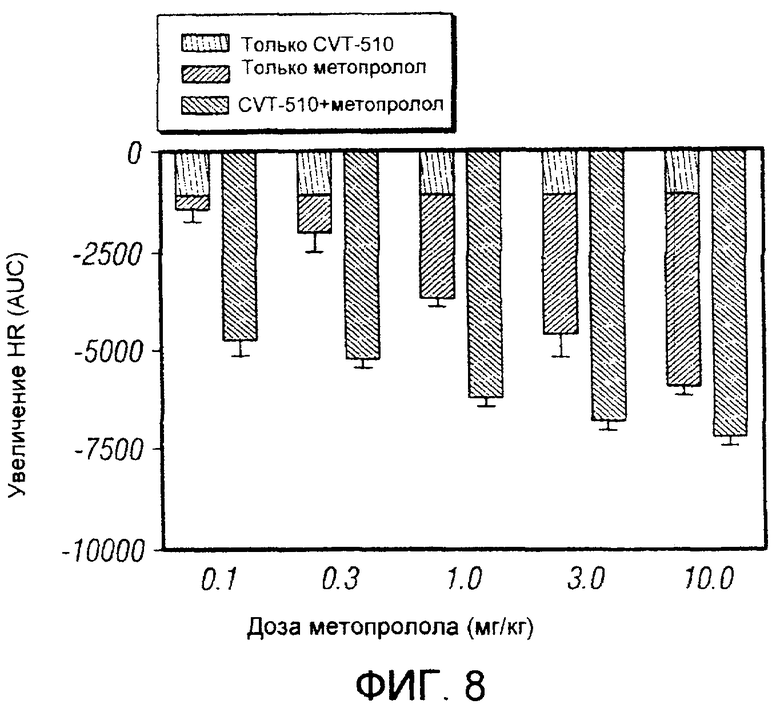
Фигура 8. На этой фигуре показаны данные фигуры 7.
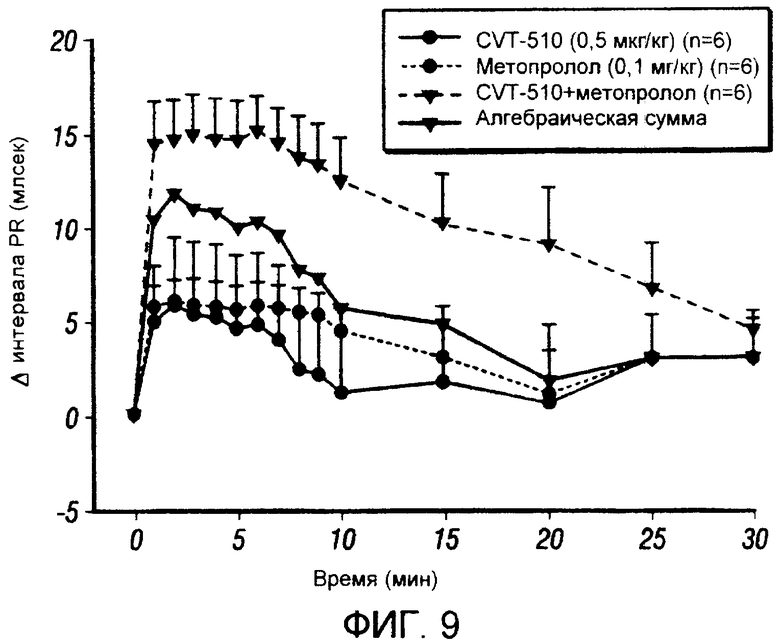
Фигура 9. Эффект CVT-510 (0,5 мкг/кг) и метопролола (0,1 мг/кг) при внутривенном введении болюса на интервал PR.
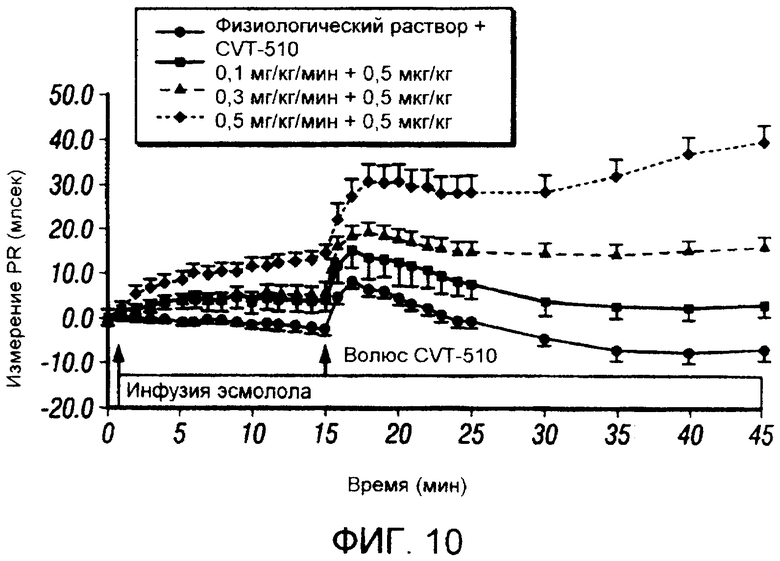
Фигура 10. Эффект CVT-510 (0,5 мкг/кг) и эсмолола на интервал PR.
Аббревиатуры
ВРМ: удары в минуту
HR: сердечный ритм
SH: стимул His (период времени для прохождения тока через AV узел)
PSVT: пароксизмальная предсердная тахикардия
Определения и общие характеристики
Как используется в настоящем описании, следующие слова и фразы обычно имеют значения, сформулированные ниже, если в рамках контекста, в котором они используются, не указано иного.
Термин «алкил» относится к монорадикальной разветвленной или неразветвленной насыщенной углеводородной цепи, содержащей от 1 до 20 атомов углерода. Примерами этого термина могут служить группы, такие как метил, этил, н-пропил, изо-пропил, н-бутил, изо-бутил, трет-бутил, н-гексил, н-децил, тетрадецил и тому подобное.
Термин «замещенный алкил» относится:
1) к алкильной группе, определенной выше, содержащей от 1 до 5 заместителей, предпочтительно, от 1 до 3 заместителей, выбранных из группы, включающей алкенил, алкинил, алкокси, циклоалкил, циклоалкенил, ацил, ациламино, ацилокси, амино, аминокарбонил, алкоксикарбониламино, азидо, циано, галоген, гидрокси, кето, тиокарбонил, карбокси, карбоксиалкил, арилтио, гетероарилтио, гетероциклилтио, тиол, алкилтио, арил, арилокси, гетероарил, аминосульфонил, аминокарбониламино, гетероарилокси, гетероциклил, гетероциклоокси, гидроксиамино, алкоксиамино, нитро, -SO-алкил, -SO-арил, -SO-гетероарил, -SO2-алкил, SO2-арил и -SO2-гетероарил. Если в определении не указано иного, все заместители могут быть, кроме того, необязательно замещены алкилом, алкокси, галогеном, CF3, амино, замещенным амино, циано, или -S(O)nR, где R представляет собой алкил, арил или гетероарил, и n равно 0, 1 или 2; или
2) к алкильной группе, определенной выше, которая прерывается 1-5 атомами или группами, независимо выбранными из кислорода, серы и -NRa-, где Ra выбран из водорода, алкила, циклоалкила, алкенила, циклоалкенила, алкинила, арила, гетероарила и гетероциклила. Все заместители могут быть, кроме того, необязательно замещены алкилом, алкокси, галогеном, CF3, амино, замещенным амино, циано или -S(O)nR, где R представляет собой алкил, арил или гетероарил, и n равно 0, 1 или 2; или
3) к алкильной группе, определенной выше, которая содержит от 1 до 5 заместителей, определенных выше, и прерывается 1-5 атомами или группами, определенными выше.
Термин «низший алкил» относится к монорадикальной разветвленной или неразветвленной насыщенной углеводородной цепи, содержащей от 1 до 6 атомов углерода. Примерами этого термина могут служить группы, такие как метил, этил, н-пропил, изо-пропил, н-бутил, изо-бутил, трет-бутил, н-гексил и тому подобное.
Термин «замещенный низший алкил» относится к низшему алкилу, определенному выше, содержащему от 1 до 5 заместителей, предпочтительно, от 1 до 3 заместителей, определенных выше для замещенного алкила, или к низшей алкильной группе, определенной выше, которая прерывается 1-5 атомами, как определено для замещенного алкила, или к низшей алкильной группе, определенной выше, которая содержит от 1 до 5 заместителей, определенных выше, и прерывается 1-5 атомами, как определено выше.
Термин «алкилен» относится к бирадикальной разветвленной или неразветвленной насыщенной углеводородной цепи, предпочтительно, содержащей от 1 до 20 атомов углерода, предпочтительно, от 1 до 10 атомов углерода, более предпочтительно, от 1 до 6 атомов углерода. Примерами этого термина могут служить группы, такие как метилен (-СН2-), этилен (-СН2СН2-), изомеры пропилена (например, -СН2СН2СН2- и -СН(СН3)СН2-) и тому подобное.
Термин «низший алкилен» относится к бирадикальной разветвленной или неразветвленной насыщенной углеводородной цепи, предпочтительно, содержащей от 1 до 6 атомов углерода.
Термин «замещенный алкилен» относится:
(1) к алкиленовой группе, как определено выше, содержащей от 1 до 5 заместителей, выбранных из группы, содержащей алкил, алкенил, алкинил, алкокси, циклоалкил, циклоалкенил, ацил, ациламино, ацилокси, амино, аминокарбонил, алкоксикарбониламино, азидо, циано, галоген, гидрокси, кето, тиокарбонил, карбокси, карбоксиалкил, арилтио, гетероарилтио, гетероциклилтио, тиол, алкилтио, арил, арилокси, гетероарил, аминосульфонил, аминокарбониламино, гетероарилокси, гетероциклил, гетероциклоокси, гидроксиамино, алкоксиамино, нитро, -SO-алкил, -SO-арил, -SO-гетероарил, -SO2-алкил, SO2-арил и -SO2-гетероарил. Если в определении не указано иного, все заместители могут быть, кроме того, необязательно замещены алкилом, алкокси, галогеном, CF3, амино, замещенный амино, циано или -S(O)nR, где R представляет собой алкил, арил или гетероарил, и n равно 0, 1 или 2; или
(2) к алкиленовой группе, как определено выше, которая прерывается 1-5 атомами или группами, независимо выбранными из кислорода, серы и NRa-, где Ra выбран из водорода, необязательно замещенного алкила, циклоалкила, циклоалкенила, арила, гетероарила и гетероциклила, или группами, выбранными из карбонила, карбоксиэфира, карбоксиамида и сульфонила; или
(3) к алкиленовой группе, как определено выше, которая содержит от 1 до 5 заместителей, как определено выше, и прерывается 1-20 атомами, как определено выше. Примерами замещенных алкиленов являются хлорметилен (-СН(Cl)-), аминоэтилен (-СН(NH2)СН2-), метиламиноэтилен (-СН(NHMe)СН2-), изомеры 2-карбоксипропилена (-СН2СН(СО2Н)СН2-), этоксиэтил (-СН2СН2O-СН2СН2-), этилметиламиноэтил (-CH2CH2N(СН3)СН2СН2-), 1-этокси-2-(2-этокси-этокси)этан (-СН2СН2O-СН2СН2-ОСН2СН2-ОСН2СН2-) и тому подобное.
Термин «аралкил» относится к арильной группе, ковалентно связанной с алкиленовой группой, где арил и алкилен такие, как определено здесь. «Необязательно замещенный аралкил» относится к необязательно замещенной арильной группе, ковалентно связанной с необязательно замещенной алкиленовой группой. Примерами таких аралкильных групп являются бензил, фенилэтил, 3-(4-метоксифенил)пропил и тому подобное.
Термин «алкокси» относится к группе R-O-, где R представляет собой необязательно замещенный алкил или необязательно замещенный циклоалкил, или R представляет собой группу -Y-Z, где Y представляет собой необязательно замещенный алкилен, и Z представляет собой необязательно замещенный алкенил, необязательно замещенный алкинил; или необязательно замещенный циклоалкенил, где алкил, алкенил, алкинил, циклоалкил и циклоалкенил такие, как определено выше. Предпочтительными алкоксигруппами являются алкил-О-, и они включают в себя, в качестве примера, метокси, этокси, н-пропокси, изо-пропокси, н-бутокси, трет-бутокси, втор-бутокси, н-пентокси, н-гексокси, 1,2-диметилбутокси и тому подобное.
Термин «алкилтио» относится к группе R-S-, где R такой, как определено выше для алкокси.
Термин «алкенил» относится к монорадикальной разветвленной или неразветвленной ненасыщенной углеводородной группе, предпочтительно, содержащей от 2 до 20 атомов углерода, более предпочтительно, от 2 до 10 атомов углерода и, еще более предпочтительно, от 2 до 6 атомов углерода и содержащей 1-6, предпочтительно, 1, двойную связь (винил). Предпочтительные алкенильные группы включают в себя этенил или винил (-СН=СН2), 1-пропилен или аллил (-СН2СН=СН2), изопропилен (-С(СН3)=СН2), бицикло[2.2.1]гептен и тому подобное. В случае, когда алкенил присоединен к азоту, двойная связь не может быть альфа по отношению к азоту азот.
Термин «низший алкенил» относится к алкенилу, как определено выше, содержащему от 2 до 6 атомов углерода.
Термин «замещенный алкенил» относится к алкенильной группе, как определено выше, содержащей от 1 до 5 заместителей, и предпочтительно от 1 до 3 заместителей, выбранных из группы, содержащей алкил, алкенил, алкинил, алкокси, циклоалкил, циклоалкенил, ацил, ациламино, ацилокси, амино, аминокарбонил, алкоксикарбониламино, азидо, циано, галоген, гидрокси, кето, тиокарбонил, карбокси, карбоксиалкил, арилтио, гетероарилтио, гетероциклилтио, тиол, алкилтио, арил, арилокси, гетероарил, аминосульфонил, аминокарбониламино, гетероарилокси, гетероциклил, гетероциклоокси, гидроксиамино, алкоксиамино, нитро, -SO-алкил, -SO-арил, -SO-гетероарил, -SO2-алкил, SO2-арил и -SO2-гетероарил. Все заместители могут быть, кроме того, необязательно замещены алкилом, алкокси, галогеном, CF3, амино, замещенным амино, циано или -S(O)nR, где R представляет собой алкил, арил или гетероарил, и n равно 0, 1 или 2.
Термин «алкинил» относится к монорадикальному ненасыщенному углеводороду, содержащему, предпочтительно, от 2 до 20 атомов углерода, более предпочтительно, от 2 до 10 атомов углерода и, еще более предпочтительно, от 2 до 6 атомов углерода, и содержащему, по крайней мере, 1 и, предпочтительно, 1-6 участков ацетиленовой (тройная связь) ненасыщенности. Предпочтительные алкинильные группы включают в себя этинил, (-С=СН), пропаргил (или пропинил, -С≡ССН3) и тому подобное. В случае, когда алкинил присоединен к азоту, тройная связь не может быть альфа по отношению к азоту.
Термин «замещенный алкинил» относится к алкинильной группе, как определено выше, содержащей от 1 до 5 заместителей, и, предпочтительно, от 1 до 3 заместителей, выбранных из группы, содержащей алкил, алкенил, алкинил, алкокси, циклоалкил, циклоалкенил, ацил, ациламино, ацилокси, амино, аминокарбонил, алкоксикарбониламино, азидо, циано, галоген, гидрокси, кето, тиокарбонил, карбокси, карбоксиалкил, арилтио, гетероарилтио, гетероциклилтио, тиол, алкилтио, арил, арилокси, гетероарил, аминосульфонил, аминокарбониламино, гетероарилокси, гетероциклил, гетероциклоокси, гидроксиамино, алкоксиамино, нитро, -SO-алкил, -SO-арил, -SO-гетероарил, -SO2-алкил, SO2-арил и -SO2-гетероарил. Все заместители могут быть, кроме того, необязательно замещены алкилом, алкокси, галогеном, CF3, амино, замещенным амино, циано или -S(O)nR, где R представляет собой алкил, арил или гетероарил, и n равно 0, 1 или 2.
Термин «аминокарбонил» относится к группе -C(O)NRR, где каждый R независимо представляет собой водород, алкил, арил, гетероарил, гетероциклил, или где обе группы R объединены с образованием гетероциклической группы (например, морфолино). Все заместители могут быть, кроме того, необязательно замещены алкилом, алкокси, галогеном, CF3, амино, замещенным амино, циано или -S(O)nR, где R представляет собой алкил, арил или гетероарил, и п равно 0, 1 или 2.
Термин «ациламино» относится к группе -NRC(O)R, где каждый R независимо представляет собой водород, алкил, арил, гетероарил или гетероциклил. Все заместители могут быть, кроме того, необязательно замещены алкилом, алкокси, галогеном, CF3, амино, замещенным амино, циано или -S(O)nR, где R представляет собой алкил, арил или гетероарил, и n равно 0, 1 или 2.
Термин «ацилокси» относится к группам -О(О)С-алкил, -O(O)С-циклоалкил, -O(O)С-арил, -О(O)С-гетероарил и -O(O)С-гетероциклил. Все заместители могут быть, кроме того, необязательно замещены алкилом, алкокси, галогеном, CF3, амино, замещенным амино, циано или -S(O)nR, где R представляет собой алкил, арил или гетероарил, и n равно 0, 1 или 2.
Термин «арил» относится к ароматической карбоциклической группе, содержащей от 6 до 20 атомов углерода и единичное кольцо (например, фенил) или множественные кольца (например, бифенил), или множественные конденсированные кольца (например, нафтил или антрил). Предпочтительные арилы включают в себя фенил, нафтил и тому подобное.
Если в определении не указано иного, арильные заместители, такие как арильные группы, могут быть необязательно замещены от 1 до 5 заместителями, предпочтительно, от 1 до 3 заместителями, выбранными из группы, состоящей из алкила, алкенила, алкинила, алкокси, циклоалкила, циклоалкенила, ацила, ациламино, ацилокси, амино, аминокарбонила, алкоксикарбониламино, азидо, циано, галоген, гидрокси, кето, тиокарбонила, карбокси, карбоксиалкила, арилтио, гетероарилтио, гетероциклилтио, тиола, алкилтио, арила, арилокси, гетероарила, аминосульфонила, аминокарбониламино, гетероарилокси, гетероциклила, гетероциклоокси, гидроксиамино, алкоксиамино, нитро, -SO-алкила, -SO-арила, -SO-гетероарила, -SO2-алкила, SO2-арила и -SO2-гетероарила. Все заместители, кроме того, могут быть необязательно замещены алкилом, алкокси, галогеном, CF3, амино, замещенным амино, циано или -S(O)nR, где R представляет собой алкил, арил или гетероарил, и n равно 0, 1 или 2.
Термин «арилокси» относится к группе арил-О-, где арильная группа такая, как определено выше, и включает в себя необязательно замещенные арильные группы такие, как определено выше. Термин «арилтио» относится к группе R-S-, где R такой, как определено для арила.
Термин «амино» относится к группе -NH2.
Термин «замещенный амино» относится к группе -NRR, каждый R независимо выбран из группы, состоящей из водорода, алкила, циклоалкила, карбоксиалкила (например, бенизилоксикарбонил), арил, гетероарил и гетероциклил, при условии, что обе R группы не являются водородом, или группы -Y-Z, где Y необязательно замещен алкиленом, и Z представляет собой алкенил, циклоалкенил, или алкинил. Все заместители могут быть, кроме того, необязательно замещены алкилом, алкокси, галогеном, CF3, амино, замещенным амино, циано или -S(O)nR, где R представляет собой алкил, арил или гетероарил, и n равно 0, 1 или 2.
Термин «карбоксиалкил» относится к группам -С(О)О-алкил, -С(О)О-циклоалкил, где алкил и циклоалкил, такие, как определено здесь, и могут быть, кроме того, необязательно замещены алкилом, алкенилом, алкинилом, алкокси, галогеном, CF3, амином, замещенным амином, циано или -S(O)nR, где R представляет собой алкил, арил, или гетероарил, и n равно 0, 1 или 2.
Термин «циклоалкил» относится к циклическим алкильным группам, содержащим от 3 до 20 атомов углерода и единичное циклическое кольцо или множественные конденсированные кольца. Такие циклоалкильные группы включают в себя, в качестве примера, единичные кольцевые структуры, такие как циклопропил, циклобутил, циклопентил, циклооктил и тому подобное, или множественные кольцевые структуры, такие как адамантил и бицикло[2.2.1]гептан, или циклические алкильные группы, с которыми конденсирована арильная группа, например индан, и тому подобное.
Термин «замещенный циклоалкил» относится к циклоалкильным группам, содержащим от 1 до 5 заместителей, и, предпочтительно, от 1 до 3 заместителей, выбранных из группы, состоящей из алкила, алкенила, алкинила, алкокси, циклоалкила, циклоалкенила, ацила, ациламино, ацилокси, амино, аминокарбонила, алкоксикарбониламино, азидо, циано, галогена, гидрокси, кето, тиокарбонила, карбокси, карбоксиалкила, арилтио, гетероарилтио, гетероциклилтио, тиола, алкилтио, арила, арилокси, гетероарила, аминосульфонила, аминокарбониламино, гетероарилокси, гетероциклила, гетероциклоокси, гидроксиамино, алкоксиамино, нитро, -SO-алкила, -SO-арила, -SO-гетероарила, -SO2-алкила, SO2-арила и -SO2-гетероарила. Все заместители могут быть, кроме того, необязательно замещены алкилом, алкокси, галогеном, CF3, амином, замещенным амином, циано или -S(O)nR, где R представляет собой алкил, арил или гетероарил, и n равно 0, 1 или 2.
Термин «галоген» относится к фтору, брому, хлору и йоду.
Термин «ацил» обозначает группу -C(O)R, где R представляет собой водород, необязательно замещенный алкил, необязательно замещенный циклоалкил, необязательно замещенный гетероциклил, необязательно замещенный арил и необязательно замещенный гетероарил.
Термин «гетероарил» относится к ароматической группе (то есть, незамещенной), содержащей от 1 до 15 атомов углерода и от 1 до 4 гетероатомов, выбранных из кислорода, азота и серы, по крайней мере, в одном кольце.
Если в определении гетероарильного заместителя не указано иного, то такие гетероарильные группы могут быть необязательно замещены от 1 до 5 заместителями, предпочтительно, от 1 до 3 заместителями, выбранными из группы, состоящей из алкила, алкенила, алкинила, алкокси, циклоалкила, циклоалкенила, ацила, ациламино, ацилокси, амино, аминокарбонила, алкоксикарбониламино, азидо, циано, галоген, гидрокси, кето, тиокарбонила, карбокси, карбоксиалкила, арилтио, гетероарилтио, гетероциклилтио, тиола, алкилтио, арила, арилокси, гетероарила, аминосульфонила, аминокарбониламино, гетероарилокси, гетероциклила, гетероциклоокси, гидроксиамино, алкоксиамино, нитро, -SO-алкила, -SO-арила, -SO-гетероарила, -SO2-алкила, SO2-арила и -SO2-гетероарила. Все заместители могут быть, кроме того, необязательно замещены алкилом, алкокси, галогеном, CF3, амино, замещенным амино, циано или -S(O)nR, где R представляет собой алкил, арил или гетероарил, и n равно 0, 1 или 2. Такие гетероарильные группы могут содержать единичное кольцо (например, пиридил или фурил) или множественные конденсированные кольца (например, индолизинил, бензотиазол или бензотиенил). Примеры азот-содержащих гетероциклов и гетероарилов включают в себя, но ими не ограничиваются, пиррол, имидазол, пиразол, пиридин, пиразин, пиримидин, пиридазин, индолизин, изоиндол, индол, индазол, пурин, хинолизин, изохинолизин, хинолин, фталазин, нафтилпиридин, хиноксалин, хиназолин, циннолин, птеридин, карбазол, карболин, фенантридин, акридин, фенантролин, изотиазол, феназин, изоксазол, феноксазин, фенотиазин, имидазолидин, имидазолин и тому подобное, а также N-алкокси азот-содержащие гетероарильные соединения.
Термин «гетероарилокси» относится к группе гетероарил-О-.
Термин «гетероциклил» относится к монорадикальной насыщенной или частично насыщенной группе, содержащей единичное кольцо или множественные конденсированные кольца и содержащей от 1 до 40 атомов углерода и от 1 до 10 гетероатомов, предпочтительно, от 1 до 4 гетероатомов, выбранных из азота, серы, фосфора и/или кислорода в кольце.
Если в определении гетероциклического заместителя не указано иного, такие гетероциклические группы могут быть необязательно замещены от 1 до 5 и, предпочтительно, от 1 до 3 заместителями, выбранными из группы, состоящей из алкила, алкенила, алкинила, алкокси, циклоалкила, циклоалкенила, ацила, ациламино, ацилокси, амино, аминокарбонила, алкоксикарбониламино, азидо, циано, галогена, гидрокси, кето, тиокарбонила, карбокси, карбоксиалкила, арилтио, гетероарилтио, гетероциклилтио, тиола, алкилтио, арила, арилокси, гетероарила, аминосульфонила, аминокарбониламино, гетероарилокси, гетероциклила, гетероциклоокси, гидроксиамино, алкоксиамино, нитро, -SO-алкила, -SO-арила, -SO-гетероарила, -SO2-алкила, SO2-арила и -SO2-гетероарила. Все заместители могут быть, кроме того, необязательно замещены алкилом, алкокси, галогеном, CF3, амино, замещенным амино, циано или -S(O)nR, где R представляет собой алкил, арил или гетероарил, и n равно 0, 1 или 2. Гетероциклические группы могут содержать единичное кольцо или множественные конденсированные кольца. Предпочтительные гетероциклические группы включают в себя тетрагидрофуранил, морфолино, пиперидинил и тому подобное.
Термин «тиол» относится к группе -SH.
Термин «замещенный алкилтио» относится к группе -S-замещенный алкил.
Термин «гетероарилтиол» относится к группе -S-гетероарил, где гетероарильная группа такая, как определено выше, включая необязательно замещенные гетероарильные группы, как также определено выше.
Термин «сульфоксид» относится к группе -S(O)R, где R представляет собой алкил, арил или гетероарил.
«Замещенный сульфоксид» относится к группе -S(O)R, где R представляет собой замещенный алкил, замещенный арил или замещенный гетероарил, как определено здесь.
Термин «сульфон» относится к группе -S(O)2R, где R представляет собой алкил, арил или гетероарил.
«Замещенный сульфон» относится к группе -S(O)2R, где R представляет собой замещенный алкил, замещенный арил или замещенный гетероарил, как определено здесь.
Термин «кето» относится к группе -С(О)-. Термин «тиокарбонил» относится к группе -C(S)-. Термин «карбокси» относится к группе -С(О)-ОН.
«Необязательный» или «необязательно» обозначает, что описанное вслед за этим событие или условие может возникать или может не возникать, и что описание включает в себя случаи, когда указанное событие или условие выполняется, и случаи, когда не выполняется.
Термин «соединение формулы I» и «соединение формулы II» включает в себя соединения, описанные в настоящем изобретении, и фармацевтически приемлемые соли, фармацевтически приемлемые сложные эфиры и пролекарства этих соединений.
Термин «терапевтически эффективное количество» относится к количеству активного ингредиента (A1-агониста, бета-блокатора, блокатора кальциевых каналов, сердечного гликозида), достаточному для лечебного действия, как определено выше, при введении млекопитающему, нуждающемуся в таком лечении. Терапевтически эффективное количество может варьировать в зависимости от пациента и состояния болезни, на которое направлено лечение, массы и возраста пациента, серьезности состояния болезни, способа введения и тому подобное, что может быть легко определено предписанием лечащего врача.
Термин «терапевтически эффективная минимальная доза» или «низкая доза» агониста аденозинового рецептора A1 относится к уровню доз агониста рецептора аденозина A1, который обычно считается более низким, чем терапевтически эффективное количество, определенное выше, но достаточное для эффективного лечения при введении в сочетании с «терапевтически эффективной минимальной дозой» или «низкой дозой» бета-блокатора, блокатора кальциевых каналов или сердечного гликозида.
Например, терапевтически эффективной минимальной дозой CVT-3619 является доза, которая обычно не считается эффективной для лечения аритмии, но в настоящей заявке рассматриваемая как эффективная для снижения частоты сердечных сокращений при введении в сочетании с терапевтически эффективной минимальной дозой бета-блокатора, вследствие синергизма эффекта, получаемого при сочетании A1-агониста с бета-блокатором. Терапевтически эффективная минимальная доза может варьировать в зависимости от пациента и болезненного состояния, на которое направлено лечение, массы и возраста пациента, серьезности болезненного состояния, способа введения и тому подобное, что может быть легко определено предписанием лечащего врача.
Терапевтически эффективную минимальную дозу агониста рецептора аденозина A1 вводят в «сочетании с» терапевтически эффективной минимальной дозой бета-блокатора, или блокатора кальциевых каналов, или сердечного гликозида. В этом контексте, слово «сочетание» обозначает, что дозы могут вводиться вместе в одно и то же время, например, одной таблеткой или раствором, или вводиться раздельно в одно и то же время, или вводиться в разное время.
Термин «лечение» обозначает любой тип лечения заболевания у млекопитающего, включая:
(i) профилактику заболевания, то есть, предотвращая развитие клинических симптомов заболевания;
(ii) ингибирование заболевания, то есть, задерживая развитие клинических симптомов; и/или
(iii) ослабляя заболевание, то есть, вызывая регрессию клинических симптомов.
Как используется здесь, термин «агонист» относится к способности соединения взаимодействовать с рецептором и вызывать максимальный эффект. Этот эффект известен как внутренняя активность. В отличие от агонистов, «частичные агонисты» взаимодействуют с рецепторами аденозина A1, но дают меньший ответ по сравнению с максимальным.
Термин «агонист рецептора аденозина A1» относится к агенту, который связывается с рецепторами аденозина А1, таким образом, вызывая отрицательный дромотропный эффект. Например, CVT-3619 является частичным агонистом A1-аденозинового рецептора и влияют на скорость проведения в AV узле. Он повышает сопротивляемость AV-узла и таким образом снижает частоту сокращения желудочков при предсердной тахиаритмии. Таким образом, действие агонистов A1 ингибирует высвобождение норэпинефрина из пресинаптических нервных окончаний и ингибирует поглощение норэпинефрина в пост-синаптических нервных окончаниях.
Термин «бета-блокатор» относится к агенту, который связывается с бета-адренергическим рецептором и ингибирует эффекты бета-адренергической стимуляции. Бета-блокаторы повышают проводимость в AV узле. Кроме того, бета-блокаторы снижают частоту сердечных сокращений, блокируя эффект норэпинефрина на пост-синаптические нервные окончания, которые контролируют сердечный ритм. Бета-блокаторы также снижают внутриклеточный обмен Са++, который ингибирует остаточную деполяризацию, вызывающую автоматизм. Примеры бета-блокаторов включают в себя атенолол, эсмолол, соталол, пропранолол, бопиндолол, картеолол, окспренолол, пенбутолол, карведилол, медроксалол, буциндолол, левобунолол, метипронолол, бетаксолол, целипролол и пропафенон.
Термин «блокатор кальциевых каналов» относится к агенту, блокирующему потенциалзависимые кальциевые каналы L-типа. Их используют для лечения сердечных заболеваний, включая сердечную аритмию, они влияют на скорость проводимости в AV узле. Примеры блокаторов кальциевых каналов включают в себя амлодипин, бепридил, дилтиазем, фелодипин, израдипин, никардипин, нифедипин, нимодипин и верапамил.
Термин «сердечный гликозид» относится к соединению, содержащему стероидные ядра и лактоновое ядро и обычно один или несколько остатков сахара. Их используют для лечения сердечных заболеваний, включая сердечную аритмию, они влияют на скорость проведения в AV узле. Примеры сердечных гликозидов включают в себя дигоксин и дигитоксин.
Термин «синергитический» эффект обозначает результат, получаемый при сочетании лекарственных препаратов, который больше результата, получаемого от каждого лекарственного препарата отдельно.
Во многих случаях соединения по изобретению способны образовывать кислые и/или щелочные соли в силу присутствия амино и/или карбоксильных групп или групп, подобных им. Термин «фармацевтически приемлемая соль» относится к соли, которая сохраняет биологическую эффективность и свойства соединений формулы I и которая является с биологической или с другой точки зрения подходящей. Фармацевтически приемлемые соли добавления оснований могут быть получены из неорганических и органических оснований. Соли, полученные из неорганических оснований, включают в себя, только для примера, соли натрия, калия, лития, аммония, кальция и магния. Соли, полученные из органических оснований, включают в себя, но ими не ограничиваются, соли первичных, вторичных и третичных аминов, таких как алкиламины, диалкиламины, триалкиламины, замещенные алкиламины, ди(замещенные алкил)амины, три(замещенные алкил)амины, алкениламины, диалкениламины, триалкениламины, замещенные алкениламины, ди(замещенные алкенил)амины, три(замещенные алкенил)амины, циклоалкиламины, ди(циклоалкил)амины, три(циклоалкил)амины, замещенные циклоалкиламины, дизамещенные циклоалкиламины, тризамещенные циклоалкиламины, циклоалкениламины, ди(циклоалкенил)амины, три(циклоалкенил)амины, замещенные циклоалкениламины, дизамещенные циклоалкениламины, тризамещенные циклоалкениламины, ариламины, диариламины, триариламины, гетероариламины, дигетероариламины, тригетероариламины, гетероциклические амины, дигетероциклические амины, тригетероциклические амины, смешанные ди- и три-амины, где, по крайней мере, два заместителя на амине являются различными и выбраны из группы, состоящей из алкила, замещенного алкила, алкенила, замещенного алкенила, циклоалкила, замещенного циклоалкила, циклоалкенила, замещенного циклоалкенила, арила, гетероарила, гетероциклической группы и тому подобное. Также к ним относятся амины, у которых два или три заместителя, вместе с азотом амино, образуют гетероциклическую или гетероарильную группу.
Специфические примеры подходящих аминов включают в себя, только в качестве примера, изопропиламин, триметиламин, диэтиламин, три(изопропил)амин, три(н-пропил)амин, этаноламин, 2-диметиламиноэтанол, трометамин, лизин, аргинин, гистидин, кофеин, прокаин, гидрабамин, холин, бетаин, этилендиамин, глюкозамин, N-алкилглюкамины, теобромин, пурины, пиперазин, пиперидин, морфолин, N-этилпиперидин и тому подобное.
Фармацевтически приемлемые соли добавления кислот могут быть получены из неорганических и органических кислот. Соли, полученные из неорганических кислот, включают в себя хлористоводородную кислоту, бромистоводородную кислоту, серную кислоту, азотную кислоту, фосфорную кислоту и тому подобное. Соли, полученные из органических кислот, включают в себя уксусную кислоту, пропионовую кислоту, гликолевую кислоту, пировиноградную кислоту, щавелевую кислоту, яблочную кислоту, малоновую кислоту, янтарную кислоту, малеиновую кислоту, фумаровую кислоту, винную кислоту, лимонную кислоту, бензойную кислоту, коричную кислоту, миндальную кислоту, метансульфоновую кислоту, этансульфоновую кислоту, п-толуолсульфоновую кислоту, салициловую кислоту и тому подобное.
Как используется здесь, «фармацевтически приемлемый носитель» или «фармацевтически приемлемый эксципиент» включает в себя любой или все растворители, дисперсионную среду, агенты покрытия, антибактериальные и противогрибковые агенты, изотонические агенты и агенты, задерживающие всасывание, и тому подобное. Использование такой среды и агентов с фармацевтически активными веществами хорошо известно в данное области. Исключая случаи, когда любая стандартная среда или агент несовместимы с активным ингредиентом, предполагается их применение в терапевтических композициях. В композиции также могут вводиться дополнительные активные вещества.
Термин «соединение формулы I» или «соединение формулы II» включает в себя соединения по изобретению, как описано, и фармацевтически приемлемые соли, фармацевтически приемлемые сложные эфиры и пролекарства таких соединений. Кроме того, соединения по изобретению могут иметь один или несколько асимметричных центров и могут быть получены в виде рацемической смеси или как отдельные энантиомеры или диастереоизомеры. Число стереоизомеров, присутствующих в любом данном соединении по изобретению, зависит от числа присутствующих асимметричных центров (возможно 2n стереоизомеров, где n равно числу асимметричных центров). Отдельные стереоизомеры могут быть получены разделением рацемической или нерацемической смеси промежуточных соединений на некоторых подходящих стадиях синтеза или разделением соединения формулы I или формулы II обычными способами. Отдельные стереоизомеры (включая отдельные энантиомеры и диастереоизомеры), а также рацемические и нерацемические смеси стереоизмеров входят в рамки настоящего изобретения, каждый из которых изображен структурами этого описания, если не указано иного.
«Изомеры» представляют собой различные соединения, которые имеют одинаковую молекулярную формулу.
«Стереоизомеры» представляют собой изомеры, различающиеся только по расположению атомов в пространстве.
«Энантиомеры» представляют собой пару стереоизомеров, которые не являются зеркальным отображением друг друга. Смесь 1:1 смеси пары энантиомеров представляет собой «рацемическую» смесь. Термин «(+)» используется для обозначения рацемической смеси, если уместно.
«Диастереоизомеры» представляют собой стереоизомеры, которые имеют по крайней мере два асимметричных атома, но не являются зеркальным отображением друг друга.
Абсолютная стереохимия определяется в соответствии с R-S системой Кана-Ингольда-Прелога.
Если соединение является чистым энантиомером, то стереохимия каждого хирального углерода может быть определена либо как R, либо как S. Растворенные соединения, чья абсолютная конфигурация неизвестна, обозначаются как (+) или (-), в зависимости от направления (право- или левостороннее), с которым они вращают плоскость поляризованного света при определенной длине волны соединения натрия D.
Фармацевтические композиции
Оба компонента по изобретению, агонист рецептора аденозина А1 и бета-блокатор, блокатор кальциевых каналов или сердечный гликозид, могут быть смешаны в виде фармацевтической композиции, содержащей физическую смесь этих двух компонентов, но вводятся, предпочтительно, в виде двух отдельных фармацевтических композиций. Такие отдельные композиции, предпочтительно, вводят одновременно, но также их можно вводить в разное время. Настоящее изобретение, следовательно, относится к фармацевтическим композициям, содержащим в качестве активного ингредиента один или два компонента, или их фармацевтически приемлемую соль или сложный эфир, и один или несколько фармацевтически приемлемых эксципиентов, носителей, включая инертные твердые разбавители и наполнители, разбавители, включая стерильный водный раствор и различные органические растворители, агенты, усиливающие проникновение, солюбилизаторы и адъюванты. Такие композиции получают способом, хорошо известным в фармацевтической области (см., например, Remington's Pharmaceutical Sciences, Mace Publishing Co., Philadelphia, PA 17th Ed. (1985) и «Modern Pharmaceutics», Marcel Dekker, Inc. 3rd Ed. (G.S.Banker & С.Т.Rhodes, Eds.).
Введение
Компоненты могут вводиться либо единичной, либо множественными дозами любым приемлемым способом введения агентов, имеющих сходное применение, например, как описано в патентах и патентных заявках, приведенных здесь в качестве ссылки, включая ректальный, буккальный, интраназальный и чрескожный пути, путем внутриартериальной инъекции, внутривенно, внутрибрюшинно, парентерально, внутримышечно, подкожно, перорально, местно, ингаляцией или посредством пропитанного или покрытого средства, такого как эндопротез сосуда, например, или цилиндрический полимер, вводимый в артерию.
Одним из способов введения является парентеральный путь, в частности, инъекция. Формы, в которых новые композиции по настоящему изобретению могут смешиваться для введения путем инъекции, включают в себя водные или масляные суспензии, или эмульсии, с кунжутным маслом, кукурузным маслом, хлопковым маслом или арахисовым маслом, а также эликсиры, маннит, декстроза, или стерильный водный раствор, и сходные фармацевтические носители. Водные растворы в физиологическом растворе также обычно используются для введения инъекций, но менее предпочтительны в контексте настоящего изобретения. Также могут быть использованы этанол, глицерин, пропиленгликоль, жидкий полиэтиленгликоль и тому подобное (и их применимые смеси), производные циклодекстрина и растительные масла. Подходящая текучесть может поддерживаться, например, используя агенты покрытия, таких как лецитин, поддерживая требуемый размер частиц в случае дисперсии, и используя поверхностно-активные вещества. Предупреждение действия микроорганизмов может осуществляться различными антибактериальными и противогрибковыми агентами, например, парабенами, хлорбутанолом, фенолом, сорбиновой кислотой, тимерозалом и тому подобное.
Стерильные растворы, вводимые инъекцией, получают введением компонента в требуемое количество соответствующего растворителя с другими различными ингредиентами, перечисленными выше, если требуется, с последующей стерилизацией фильтрацией. Обычно, дисперсии получают путем введения различных стерильных активных ингредиентов в стерильный носитель, который содержит основную дисперсионную среду и другие необходимые ингредиенты из ингредиентов, перечисленные выше. В случае стерильных порошков для получения стерильных растворов для инъекций, предпочтительными способами получения являются способы вакуумной сушки и сушки замораживанием, которые дают порошок активного ингредиента плюс любой дополнительный желательный ингредиент из раствора, предварительно стерилизованного фильтрацией.
Пероральное введение является другим путем введения компонентов. Введение может осуществляться посредством капсулы или таблетки с кишечно-растворимым покрытием, или тому подобное. При получении фармацевтической композиции, которая включает в себя по крайней мере одно соединение формулы I или II, активный ингредиент обычно разбавляют эксципиентом и/или вводят в такой носитель, который может быть в форме капсулы, саше, бумаги или другого контейнера. Если эксципиент служит разбавителем, то он может быть твердым, полутвердым или жидким веществом (как указано выше), который действует как транспортное средство, носитель или среда для активного ингредиента. Таким образом, композиции могут быть в форме таблеток, пилюль, лепешек, саше, эликсиров, суспензий, эмульсий, растворов, сиропов, аэрозолей (как в виде твердого вещества, так и в жидкой среде), мазей, содержащих, например, до 10% по массе активного соединения, мягких и твердых желатиновых капсул, стерильных растворов для инъекций и стерильных упакованных порошков.
Некоторые примеры подходящих эксципиентов включают в себя лактозу, декстрозу, сахарозу, сорбит, манит, крахмалы, гуммиарабик, фосфат кальция, альгинаты, трагакант, желатин, силикат кальция, микрокристаллическую целлюлозу, поливинилпирролидон, целлюлозу, стерильную воду, сироп и метилцеллюлозу. Кроме того, композиции также могут включать в себя: лубриканты, такие как тальк, стеарат магния и минеральное масло; смачивающие агенты; эмульгаторы и суспендирующие агенты; консерванты, такие как метил- и пропилгидроксибензоаты; подсластители и ароматизаторы.
Композиции по изобретению могут быть составлены таким образом, чтобы обеспечивать быстрое, длительное или замедленное высвобождение активного ингредиента после введения пациенту, с использованием процедур, известных в данной области. Системы доставки с контролируемым высвобождением препарата для перорального введения включают в себя системы осмотического насоса и растворяющиеся системы, содержащие резервуары, покрытые полимером, или композиции с полимерным основным веществом, в котором находится препарат. Примеры систем, контролирующих высвобождение, приведены в патентах США №№3845770; 4326525; 4902514 и 5616345. Другими композициями для использования в способах по настоящему изобретению являются устройства для доставки препарата («пластыри»). Такие чрескожные пластыри могут использоваться для постоянной или прерывистой инфузии соединений по настоящему изобретению в контролируемых количествах. Устройство и применение чрескожных пластырей для доставки фармацевтических агентов хорошо известно в данной области. См., например, патенты США №№5023252, 4992445 и 5001139. Такие пластыри могут быть сконструированы для длительной, прерывистой доставки фармацевтических агентов или доставки по потребности.
Композиции предпочтительно получают в единичной лекарственной форме. Термин «единичная лекарственная форма» относится к физически дискретным единицам, подходящим для единичного введения пациентам, человеку и другим млекопитающим, каждая единица содержит заранее определенное количество активного вещества, рассчитанным с тем, чтобы получить желаемый терапевтический эффект, объединенное с подходящим фармацевтическим эксципиентом (например, таблетка, капсула, ампула). Соединения формулы I и II эффективны в широком спектре доз, и обычно их вводят в фармацевтически эффективном количестве. Понятно, однако, что это фактически вводимое количество соединения формулы I может быть определено лечащим врачом с учетом существенных обстоятельств, включая условия лечения, выбранный путь введения, вводимое действующее соединение и его относительную активность, возраст, массу и реакцию отдельного пациента, тяжесть симптомов пациента и тому подобное.
Для получения твердых композиций, таких как таблетки, главный активный ингредиент смешивают с фармацевтическим эксципиентом с получением твердой смеси для таблетирования, содержащей гомогенную смесь соединения по настоящему изобретению. Под гомогенностью, относящейся к этой смеси для таблетирования, понимают, что активный ингредиент равномерно диспергирован в композиции так, чтобы композиция могла быть легко разделена на эквивалентные единичные лекарственные формы, такие как таблетки, пилюли и капсулы.
Таблетки или пилюли по настоящему изобретению могут быть покрыты или компаундированы иным образом с получением лекарственной формы, обеспечивающей благоприятное пролонгированное действие или защиту от кислотных условий в желудке. Например, таблетка или пилюля может содержать внутренний или наружный элемент, где последний находится в форме оболочки для внутреннего элемента. Два элемента могут быть разделены энтеросолюбильным слоем, который препятствует разрушению внутреннего элемента в желудке, что позволяет ему пройти в двенадцатиперстную кишку неповрежденным или замедлить высвобождение. Для получения таких энетросолюбильных слоев могут использоваться различные вещества или агенты покрытия, как вещества, включая разнообразное число полимерных кислот и разнообразные смеси полимерных кислот с такими веществами, например, гуммилак, цетиловый спирт и ацетат целлюлозы.
Композиции для ингаляции или вдувания включают в себя растворы и суспензии фармацевтически приемлемых, водных или органических растворителей, или их смеси, и порошки. Жидкие или твердые композиции могут содержать подходящие фармацевтически приемлемые эксципиенты, как описано выше. Предпочтительно, для местного или системного эффекта композиции вводят перорально или через нос. Композиции в предпочтительных фармацевтически приемлемых растворителях могут распыляться, используя инертный газ. Растворы для распыления могут вводиться путем ингаляции непосредственно из устройства для распыления или устройство для распыления может быть прикреплено к маске или дыхательному аппарату с перемежающимся положительным давлением. Композиции в виде растворов, суспензий или порошков могут вводиться, предпочтительно, перорально или назально, из устройств, которые обеспечивают доставку композиции соответствующим способом.
Нижеследующие примеры включены для демонстрации предпочтительных вариантов осуществления изобретения. Специалисту в данной области должно быть понятно, что способы, описанные в нижеследующих примерах, представляют собой способы, обнаруженные изобретателем, для оптимального осуществления изобретения, и таким образом могут быть рассмотрены как представляющие собой предпочтительные способы для его осуществления. Однако специалисту в данной области в свете настоящего описания должно быть понятно, что в конкретных вариантах осуществления может быть сделано много изменений, которые описаны и приводят к таким же или подобным результатам, не выходя за рамки сущности и объема изобретения.
Примеры
Бета-блокаторы, блокаторы кальциевых каналов и сердечные гликозиды по данному изобретению хорошо известны в данной области и являются коммерчески доступными. Соединения формулы I могут быть получены обычными способами, способом, описанным в патенте США №5789416, описание которого приведено здесь в качестве ссылки в полном объеме. Например, предпочтительное соединение CVT-510 получают нижеследующими способами.
Пример 1
А. Получение рибозида (3-(S)-аминотетрагидрофуранил)пурина
Стадия 1. Разделение 3-(S)-аминотетрагидрофурана
Смесь гидрохлорида 3-аминотетрагидрофурана (0,5 г, 4 ммоль) и хлорида (S)-(+)-10-камфорсульфонила (1,1 г, 4,4 ммоль) в пиридине (10 мл) перемешивали в течение 4 часов при комнатной температуре и затем концентрировали. Осадок растворяли в этилацетате и промывали 0,5 н. хлористоводородной кислотой, а затем бикарбонатом натрия и затем насыщенным солевым раствором. Органический слой сушили над сульфатом магния, фильтровали, и из фильтрата удаляли растворитель при пониженном давлении с получением 1,17 г коричневого масла, которое хроматографировали на силикагеле (25-70% этилацетат/гексан). Полученный белый твердый продукт повторно перекристаллизовывали из ацетона с получением (S)-камфорсульфоната 3-(S)-аминотетрагидрофурана.
Стадия 2. Получение гидрохлорида 3-(S)-аминотетрагидрофурана
(S)-Камфорсульфонат 3-(S)-аминотетрагидрофурана (170 мг, 0,56 ммоль) растворяли в концентрированной хлористоводородной кислоте/уксусной кислоте (каждого по 2 мл) и перемешивали в течение 20 часов при комнатной температуре. Реакционную смесь промывали три раза метиленхлоридом (10 мл), и объединенные экстракты концентрировали досуха при пониженном давлении с получением 75 мг 3-(S)-аминотетрагидрофурана, в виде белого твердого продукта.
Стадия 3. Получение рибозида6-(3-(S) -аминотетрагидрофуранил)пурина
Смесь рибозида 6-хлорпурина (30 мг, 0,10 ммоль), гидрохлорида 3-(S)-аминотетрагидрофурана (19 мг, 0,15 ммоль) и триэтиламина (45 мл, 0,32 ммоль) в метаноле (0,5 мл) нагревали до 80°С в течение 18 часов. Смесь охлаждали, концентрировали и хроматографировали 95/5 (метиленхлорид/метанол) с получением 8 мг рибозида 6-(3-(S)-аминотетрагидрофуранил)пурина в виде белого твердого продукта.
В. Получение рибозида (3-(R)-аминотетрагидрофуранил)пурина (CVT-510)
Аналогично, в соответствии с вышеописанными стадиями 1-3, но заменяя хлорид (S)-(+)-10-камфорсульфонила на хлорид (R)-(-)-10-камфорсульфонила, получали следующее соединение: рибозид 6-(3-(R)-аминотетрагидрофуранил)пурина (CVT-510).
Аналогично получали другие энантиомеры соединений формулы I.
Соединения формулы II могут быть получены обычными способами, способом, описанным в патенте США № 10/194335, описание которого приведено здесь в качестве ссылки в полном объеме. Например, предпочтительное соединение CVT-3619 получают нижеследующими способами.
Пример 2
Получение 6-(6-хлорпурин-9-ил)-2,2-диметилтетрагидрофуро[3,4-d][1,3]диоксол-4-ил]метанола
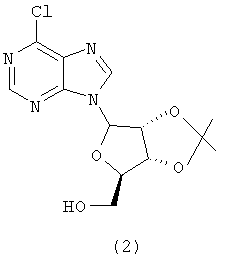
К раствору 2-(6-хлорпурин-9-ил)-5-гидроксиметилтетрагидрофуран-3,4-диола (соединение формулы (1)) (4,9 г, 17,1 ммоль) и 2,2-диметоксипропана (10,5 мл, 84,7 ммоль) в диметилформамиде (100 мл) добавляли п-толуолсульфоную кислоту (325 мг, 1,71 ммоль). После перемешивания в течение 24 часов при 70°С, реакционную смесь концентрировали в вакууме, и осадок очищали флэш-хроматографией на колонке (70% EtOAc/гексан) с получением 6-(6-хлорпурин-9-ил)-2,2-диметилтетрагидрофуро[3,4-d][1,3]диоксол-4-ил]метанола, соединения формулы (2), в виде не совсем белого твердого продукта (2), (3,8 г, 68%).
1H ЯМР (CDCl3) δ 1,4 (с, 3Н), 1,65 (с, 3Н), 3,8-4,0 (дд, 2Н), 4,6 (с, 1Н), 5,1-5,3 (м, 2Н), 6,0 (д, 1Н), 8,25 (с, 1Н), 8,8 (с, 1Н).
Пример 3
Получение 1-{[(2S, 1R, 4R, 5R)-4-(6-хлорпурин-9-ил)-7,7-диметил-3,6,8-триоксабицикло[3,3,0]окт-2-ил]метилтио}-2-фторбензола
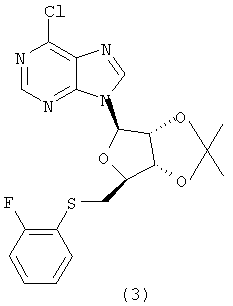
К раствору 6-(6-хлорпурин-9-ил)-2,2-диметилтетрагидрофуро[3,4-d][1,3]диоксол-4-ил]метанола, соединения формулы (2) (0,48 г, 1,47 ммоль) в 20 мл тетрагидрофурана добавляли трифенилфосфин (0,77 г, 2,94 ммоль) и диэтилазодикарбоксилат (0,47 мл, 2,94 ммоль), и смесь перемешивали в течение 5 минут. Затем добавляли 2-фтортиофенол (0,31 мл, 2,94 ммоль), и смесь перемешивали при кипячении с обратным холодильником. Через 72 часа кипячения с обратным холодильником, реакционную смесь концентрировали в вакууме, и осадок очищали флэш-хроматографией на колонке (20% EtOAc/гексаны) с получением 1-{[(2S,1R,4R,5R)-4-(6-хлорпурин-9-ил)-7,7-диметил-3,6,8-триоксабицикло[3.3.0]окт-2-ил]метилтио}-2-фторбензол, соединения формулы (3), в виде прозрачного вязкого масла (3), (0,25 г, ˜40%).
1Н ЯМР (CDCl3) δ 1,4 (с, 3Н), 1,6 (с, 3Н), 3,2 (м, 2Н), 4,6 (т, 1Н), 5,1 (м, 1Н), 5,5 (м, 1Н), 6,0 (д, 1Н), 7,0 (м, 2Н), 7,2 (м, 1Н), 7,4 (м, 1Н), 8,25 (с, 1Н), 8,75 (с, 1Н).
Пример 4
Получение (9-{(4S, 1R, 2R, 5R)-4-[(2-фторфенилтио)метил]-7,7-диметил-3,6,8-триоксабицикло[3,3,0]окт-2-ил]пурин-6-ил)циклопентиламина
К раствору 1-{[(2S,1R,4R,5R)-4-(6-хлорпурин-9-ил)-7,7-диметил-3,6,8-триоксабицикло[3.3.0]окт-2-ил]метилтио}-2-фторбензола, соединению формулы (3), (0,125 г, 2,86 ммоль) в 10 мл этанола и 1 мл триэтиламина, добавляли с избытком циклопентиламин, и смесь кипятили с обратным холодильником в атмосфере азота в течение 24 часов. Растворитель удаляли при пониженном давлении, и осадок очищали препаративной ТСХ, используя 1:1 EtOAc:гексаны с получением (9-{(4S, 1R, 2R, 5R)-4-[(2-фторфенилтио)метил]-7,7-диметил-3,6,8-триоксабицикло[3.3.0]окт-2-ил}пурин-6-ил)циклопентиламина, соединения формулы (4), в виде желтого масла (80 мг, 56%).
1H ЯМР (CDCl3) δ 1,4 (с, 3Н), 1,6 (с, 3Н), 1,6-2,4 (м, 6Н), 3,15-3,25 (м, 2Н), 4,1 (шир.с, 1Н), 4,4 (т, 1Н), 5,1 (м, 1Н), 5,5 (м, 1Н), 6,0 (д, 1Н), 6,2 (шир.с, 1Н), 7,0 (м, 2Н), 7,2 (м, 1Н), 7,4 (м, 1Н), 7,8 (с, 1Н), 8,25 (с, 1Н).
Пример 5
Получение (4S,5S,3R)-2-[6-(циклопентиламино)пурин-9-ил]-5-[(2-фторфенилтио)метил]оксолан-3,4-диола

(9-{(4S,1R,2R,5R)-4-[(2-фторфенилтио)метил]-7,7-диметил-3,6,8-триоксабицикло[3.3.0]окт-2-ил}пурин-6-ил)циклопентиламин, соединение формулы (4), (50 мг) растворяли в смеси уксусной кислоты (8 мл) и воды (2 мл) и нагревали при 90°С в течение 16 часов. Растворители удаляли при пониженном давлении, и осадок очищали препаративной ТСХ [метанолдихлорметан(1:9)] с получением (4S,5S,3R)-2-[6-(циклопентиламино)пурин-9-ил]-5-[(2-фторфенилтио)метил]оксолан-3,4-диола, соединения формулы I.
1Н ЯМР (CDCl3) δ 1,6-2,4 (м, 6Н), 3,15-3,25 (м, 2Н), 4,1 (шир.с, 1Н), 4,4-4,65 (м, 4Н), 6,0 (д, 1Н), 6,8 (шир.с, 1Н), 7,05 (м, 2Н), 7,2 (м, 1Н), 7,4 (м, 1Н), 7,8 (с, 1Н), 8,25 (с, 1Н).
Пример 6
Исследование бодрствующих крыс: (таблицы 1-7)
Способы
Крысы (Sprague Dawley), массой 300-400 г, были приобретены в лаборатории Simonsen laboratories. CVT-3619 растворяли в ДМСО и затем разводили физиологическим раствором. CVT-510 растворяли в физиологическом растворе. Кетамин был приобретен от Fort Dodge Animal Health, ксилазин от Bayer и ацепромазин малеат от Fermenta Animal Health Co. Метопролол и пропранолол были приобретены от SIGMA. Эсмолол получали из местной аптеки.
Телеметрические исследования
Для этих исследований крыс обследовали радиотелеметрическими датчиками (Data Sciences) по крайней мере за 3 недели до эксперимента. Животных анестезировали внутрибрюшинной инъекцией «коктейля» (1 мл/кг), содержащего кетамин (75 мг/мл), ксилазин (5 мг/мл) и ацепромазин (1 мг/мл). Через 20-30 минут после анестезии, проводили срединную лапаротомию. Датчик для записи ЭКГ, кровяного давления и температуры тела помещали в полость живота и закрепляли брюшными мышцами. Два электрокардиографических провода вводили подкожно - один в верную часть левого плеча, другой в правое бедро, и прикрепляли нитями. Сенсорный катетер, наполненный жидкостью, вводили в нисходящую аорту выше подвздошной бифуркации для измерения кровяного давления. Кончик телеметрического катетера помещали в брюшную аорту, каудальнее почечных артерий. После установки и проверки нормальной работы датчика и проводов, брюшную стенку зашивали. После восстановления после анестезии крыс помещали в клетки в зависимости от соответствующих введений в эксперименте. ЭКГ, кровяное давление и температуру записывали и сердечный ритм измеряли с помощью системы Dataquest ART Gold (Version 2.2; Data Sciences Intl). Система состояла из датчика, то есть биопотенциального сенсора (модель TL11M2-C50-PXT), приемников (модель RPC-1), объединяющей матрицы (ВСМ 100), персонального компьютера (Compaq DeskPro Series 3574) и программного обеспечения Dataquest 4. Сердечный ритм, кровяное давление и температуру измеряли с интервалом 5 минут. Каждая запись длилась 10 секунд и все сердечные циклы в этот период усредняли. Животным случайным путем вводили различные препараты после записи базисных данных в течение по крайней мере двух часов.
Имплантация осмотического насоса
Подгруппе животных были имплантированы осмотические насосы, содержание CVT-510, для комбинированных экспериментов. Через 7 дней или больше после имплантации радиотелеметрических датчиков для записи ЭКГ (L-2) и проверки нормальной работы датчиков, каждой крысе имплантировали осмотический мининасос Alzet. Под анестезией (смотри выше) и в стерильных условиях каждой крысе в межлопаточной области подкожно (ПК) имплантировали осмотический мининасос Alzet. Осмотические насосы наполняли либо носителем, либо CVT-510 (для введения дозы 20 мкг/кг/час).
Хирургическое введение катетеров для определения концентрации плазмы
Сонную артерию катетеризировали с получением серийных образцов крови для анализа концентрации CVT-510 в плазме. Животных анестезировали внутрибрюшинной инъекцией «коктейля» (1 мл/кг), содержащего кетамин (75 мг/мл), ксилазин (5 мг/мл) и ацепромазин (1 мг/мл). Через 20-30 минут после анестезии осуществляли срединный разрез в области шеи для доступа к внешней сонной артерии. Для катетера был сделан туннель, используя прямое рассечение в подкожной сумке на дорзальном участке шеи, где был сделан разрез. В сонную артерию вводили катетер 24 размера, отбирали образцы крови для определения уровней CVT-510 в плазме. Снаружи катетер привязывали на задней части шеи и небольшой кусок шовного материала завязывали узлом, оставляя оба конца длиной около 2 дюймов свободно выглядывать из-под кожи. Завязанный катетер втягивали под кожу для того, чтобы предохранить от вытаскивания крысой. Разрез затем обрабатывали физиологическим раствором, на рану накладывали зажимы и внутривенно вводили антибиотики (0,4 мл, 40 мг/мл раствор гентамицина). Животных оставляли восстанавливаться на по крайней мере 48 часов до осуществления эксперимента. В день эксперимента к прибору IV, 19 размера, наполненному 0,1% раствором гепарина, присоединяли разъем для введения инъекций и игольчатый конец вводили в катетеры. Животным вводили инъекцию либо физиологического раствора, либо метопролола за 1 час до инъекции CVT-510. В заранее определенные моменты времени из трубки в сонной артерии отбирали приблизительно 400 мкл крови, вливая вместо этого объема крови 400 мкл физиологического раствора. Отделяли плазму и хранили при -80°С для анализа уровней CVT-510.
Определение концентрации плазмы CVT-510
Анализ уровней CVT-510 в плазме осуществляли, как описано ниже. Коротко, 50 мкл образца плазмы осаждали в 400 мкл ацетонитрила:метанола (90:10), содержащего внутренний стандарт. Фильтраты упаривали досуха и восстанавливали в 100 мкл 90:10 воды:метанола. Концентрацию CVT-510 в отфильтрованных белковых осадках анализировали с помощью LC-MS-MS, используя систему Waters Alliance 2690 HPLC (Millford, MA), присоединенную к квадрупольному спектрометру Waters/Micromass Quattro Ultima Triple (Millford, MA). Калибровочные кривые строили по отношению площадей пиков исследуемого вещества и внутренних стандартов против концентрации, во всех случаях используя модель линейной регрессии взвешенных наименьших квадратов (1/Х).
Анализ данных
Замедление сердечного ритма, вызванное каждым введением, оценивали определением площади под кривой (AUC), используя для подсчетов метод трапецеидальных характеристик. Данными, используемыми для анализа, служила площадь под/над кривой, рассчитанная от изменений базовых данных (необрабатываемые животные). Данные анализировали по величине, а также длительности брадикардии, вызванной каждым введением. Значения AUC для различных доз каждой монотерапии сравнивали, используя односторонний анализ ANOVA, а затем с помощью теста Tukey для множественных препаратов. Для всех соединений важным уровнем был уровень с р<0,05.
Полученные в вышеописанных исследованиях результаты представлены на чертежах, описанных ниже.
На фигуре 1 показан эффект CVT-3619 (частичный агонист рецептора A1) на сердечный ритм вместе или без пропранолола у бодрствующих крыс с имплантированными телеметрическими радиодатчиками. При внутрибрюшинном введении только CVT-3619 с дозой 0/5 мг/кг эффект на сердечный ритм был минимальный. Однако при введении вместе с бета-блокатором (пропранолол, 10 мг/кг, внутрибрюшинно), наблюдалось значительное снижение сердечного ритма ниже основной линии по сравнению с введением только CVT-3619. Пропранолол вводили за 10 минут до инъекции CVT-3619.
На фигуре 2 показано суммирование данных, полученных у бодрствующих крыс с телеметрическими датчиками. Данные количественно оценивали по площади под кривой (AUC) и наличию снижения общего числа сердечных ударов в течение 2-часового периода времени, вызванного. введением только CVT-3619 (внутрибрюшинное введение) при двух различных дозах и в присутствии пропранолола (10 мг/кг, внутрибрюшинное введение за 10 минут до введения CVT-3619). Сочетание CVT-3619 и пропранолола оказывало синергетический эффект на сердечный ритм, тогда как эффект, наблюдаемый при сочетании, был гораздо сильнее, чем вычисленная сумма каждого агента отдельно.
На фигуре 3 показан эффект CVT-510 и эсмолола, вводимых самостоятельно и в виде смеси внутрибрюшинной инъекцией бодрствующим крысам с телеметрическими радиодатчиками. При введении CVT-510 с дозой, равной 20 мкг/кг, наблюдалось кратковременное снижение сердечного ритма ниже основного уровня, тогда как при введении эсмолола (10 мг/кг, внутрибрюшинно) небольшое снижение повышения сердечного ритма (вызванного взятием животного в руки). При введении сочетания двух агентов, эффект на сердечный ритм был гораздо выше. Сочетание не только повышало величину ответа, но также значительно увеличивало длительность брадикардии.
На фигуре 4 показан эффект CVT-510, вводимого самостоятельно, и эффект введения сочетания с бета-блокатором, метопролол, наблюдаемый на сердечный ритм у бодрствующих крыс с имплантированными телеметрическими радиодатчиками. CVT-510 (20 мкг/кг, внутрибрюшинно) понижал сердечный ритм в зависимости от дозы. В присутствии метопролола (3 мг/кг, внутрибрюшинно), сердечный ритм снижался на много сильнее.
Фигура 5. Продолжительность брадикардии, вызванной введением CVT-510, анализировали, наблюдая за временем восстановления сердечного ритма до 90% от уровня до введения препарата. Кроме увеличения значения брадикардии сочетание CVT-510 и метопролола давало значительное увеличение продолжительности брадикардии по сравнению с продолжительностью при введении только CVT-510.
Фигура 6: уровни CVT-510 в плазме, определяемые в отсутствие и присутствии метопролола в разных группах животных (фигура 6). Было обнаружено, что уровни CVT-510 в плазме были сходными в обеих группах, хотя замедление сердечного ритма, вызванное введением CVT-510, было больше в присутствии метопролола, что показывает, что метопролол не влияет на метаболизм CVT-510.
Фигура 7: Для дальнейшего исследования механизма взаимодействия CVT-510 и бета-блокаторов, осуществляли другую серию экспериментов, в которой дозу CVT-510 поддерживали постоянной, тогда как дозу метопролола изменяли. Сначала получали кривую полного ответа на введение только метопролола (доза 0,1-10 мг/кг, внутрибрюшинно) (фигура 7, символы ▪). Во второй части исследования животным подкожно имплантировали осмотический насос, содержащий CVT-510. CVT-510 высвобождался со скоростью 20 мкг/кг/час с получаемой концентрацией в плазме, равной 7,5±1 нг/мл. Кривую ответа на введение дозы метопролола строили для всех этих животных. В присутствии CVT-510 кривая ответа на введение дозы метопролола сдвигалась влево и вниз (фигура 7, символы •).
Фигура 8: На этой фигуре представлены данные, показанные на фигуре 7. Замедление сердечного ритма, вызванное CVT-510 и метопрололом, количественно оценивали, определяя площадь под кривой (AUC) для 60 минут каждого введения. Было обнаружено, что объединенный эффект CVT-510 и метопролола на сердечный ритм является синергетическим.
Фигуры 9-10: анализ анестезированных морских свинок
Самцов морских свинок массой 400-450 г получали из лаборатории Simonsen labs и размещали в лабораторном оборудовании для животных, имеющемся в институте. Животных анестезировали изофлураном в камерах для анестезии. После подтверждения (пощипывание подошвы), что животное анестезировано, животных интубировали эндотрахеальной трубкой и вентилировали смесью изофлурана и кислорода, используя аппарат для анестезии. Пользуясь стерильными инструментами и асептическим методом, вскрывали правую сонную артерию и вводили катетер для записи кровяного давления (ВР). Квадрипольный электронный катетер вводили через правую яремную вену и помещали в правом предсердии и желудочке для стимуляции предсердия и желудочка. Сердечный ритм задавали постоянной интенсивности (330-360 уд. в мин) для того, чтобы исключить различие сердечного ритма между животными. Другой катетер вводили в левую яремную вену и помещали в левом предсердии для введения препарата и физиологического раствора. Подкожные иглы использовали как стандарты элекрокардиографических проводов для записи электрокардиограммы (ECG). После завершения операции и инструментального вмешательства, свинок оставляли на 20 минут для уравновешивания до начала проведения эксперимента. Данные получали с помощью системы сбора данных Power Lab.
Фигура 9: Внутривенное введение CVT-510 (0,5 мкг/кг) и метопролола (0,1 мг/кг) в виде болюсов показало повышение интервала PR по 5 мсек каждой анестезированной морской свинки. Если два агента вводили в сочетании, то интервал PR повышался до 15 мсек. Этот синергетический эффект, который наблюдался, был больше, чем алгебраическая сумма эффекта каждого агента.
Фигура 10: Сходные результаты были получены при введении CVT-510 в присутствии с другим бета-блокатором эсмололом. Эсмолол вводили при трех различных уровнях инфузии. CVT-510 вводили через 15 минут после начала инфузии эсмолола. Эффект CVT-510 на интервал PR увеличивался с увеличением дозы эсмолола. Продолжительность эффекта значительно удлинялась в зависимости от дозы.
Таким образом, было показано, что сочетание бета-блокатора и агониста A1 приводит к синергическому эффекту на сердечный ритм у крыс и интервал PR у морских свинок. Объединенный эффект зависит от дозы каждого агента. То есть, сходные эффекты могут быть достигнуты, поддерживая один агент при постоянной концентрации и изменяя концентрацию другого. Были использованы различные пути введения препаратов и различные сочетания. Например, один препарат вводился за 10 минут до введения другого и через 1 час после введения другого. Препараты вводили в виде смеси или отдельно друга от друга в одно и то же время. Ответ изменялся по значению, но суммарный эффект был одинаковым. Было показано, что сочетание является эффективным при использовании полных агонистов рецепторов аденозина A1 и частичных агонистов рецепторов аденозина A1.
Было показано, что сочетание было эффективно в двух различных моделях.
1. Измерение сердечного ритма у бодрствующих крыс, который не является мишенью действия агонистов A1, но используется в качестве заместителя эффекта агонистов A1. Преимуществом этой модели является то, что высокий симпатический тон стимулировался во многих формах аритмии.
2. У анестезированных морских свинок для измерения интервала PR использовалась модель проведения в AV узле, который является агонистом A1. Однако симпатический тон был глухой на этой модели из-за анестезии.
| название | год | авторы | номер документа |
|---|---|---|---|
| ПУРИНРИБОЗИДЫ В КАЧЕСТВЕ АНТИАРИТМИЧЕСКИХ СРЕДСТВ | 2001 |
|
RU2248208C2 |
| СПОСОБЫ И КОМПОЗИЦИИ, ПОВЫШАЮЩИЕ ПЕРЕНОСИМОСТЬ ПАЦИЕНТОМ МЕТОДОВ ВИЗУАЛИЗАЦИИ МИОКАРДА | 2007 |
|
RU2459626C2 |
| ПРОИЗВОДНЫЕ 1,3-ДИГИДРОИМИДАЗОЛ-2-ТИОНА В КАЧЕСТВЕ ИНГИБИТОРОВ ДОФАМИН-БЕТА-ГИДРОКСИЛАЗЫ | 2008 |
|
RU2501796C2 |
| ЧАСТИЧНЫЕ И ПОЛНЫЕ АГОНИСТЫ АДЕНОЗИНОВЫХ РЕЦЕПТОРОВ А | 2003 |
|
RU2317994C2 |
| ЗАМЕЩЕННЫЕ ПИРАЗИНОПИРИМИДИНОНЫ КАК БЛОКАТОРЫ TRPA1 КАНАЛОВ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, СПОСОБЫ ИХ ПОЛУЧЕНИЯ И ПРИМЕНЕНИЯ | 2014 |
|
RU2603770C2 |
| АМИДЫ СИГМА-АМИНО-ГАММА-ГИДРОКСИ-ОМЕГА-АРИЛАЛКАНОВЫХ КИСЛОТ И ИХ ПРИМЕНЕНИЕ В КАЧЕСТВЕ ИНГИБИТОРОВ РЕНИНА | 2004 |
|
RU2425027C2 |
| ПЕПТИДНЫЕ КОМПОЗИЦИИ | 2014 |
|
RU2725150C2 |
| ЧАСТИЧНЫЕ И ПОЛНЫЕ АГОНИСТЫ АДЕНОЗИНОВЫХ РЕЦЕПТОРОВ A | 2003 |
|
RU2340623C2 |
| ПРОЛЕКАРСТВА АНТАГОНИСТОВ A РЕЦЕПТОРА АДЕНОЗИНА | 2006 |
|
RU2415858C2 |
| СПОСОБ ПРЕДОТВРАЩЕНИЯ И ЛЕЧЕНИЯ БОЛЕЗНИ ПЕЧЕНИ С ИСПОЛЬЗОВАНИЕМ АНТАГОНИСТОВ РЕЦЕПТОРА АДЕНОЗИНА A | 2007 |
|
RU2457842C2 |
Настоящая группа изобретений относится к медицине, а именно к кардиологии, и включает способ и фармацевтическую композицию, направленные на уменьшение числа сердечных сокращений у млекопитающих. Для этого вводят терапевтически эффективную дозу агониста рецептора аденозина A1, представляющего собой 6-(3-(R)-N-аминотетрагидрофуранил)пурин рибозида (CVT-510) или 2-{6-[((1R,2R)-2-гидроксициклопентил)амино]пурин-9-ил}(4S,5S,3R)-5-[(2-фторфенилтио)метил]оксолан-3,4-диола (CVT-3619), в сочетании с терапевтически эффективной минимальной дозой бета-блокатора. Это обеспечивает эффективное снижение частоты сердечных сокращений за счет синергического действия вводимых соединений при минимальных побочных эффектах. 2 н. и 20 з.п. ф-лы, 7 табл., 10 ил.
| SNOUDY S et al | |||
| ИНЕРЦИОННО-АККУМУЛЯТОРНОЕ ПРИСПОСОБЛЕНИЕ ДЛЯ АВТОМАТИЧЕСКОГО ОТКРЫВАНИЯ И ЗАКРЫВАНИЯ ВЕРТИКАЛЬНОГО КЛИНОВОГО ЗАТВОРА ОРУДИЙ | 1912 |
|
SU510A1 |
| Металлический водоудерживающий щит висячей системы | 1922 |
|
SU1999A1 |
| US 5789416, 04.08.1998 | |||
| Лекции по кардиологии под ред | |||
| Л.А.Бокерия, 2001, Издательство НЦССХ им | |||
| А.Н.Бакулева, с.152-165) | |||
| КУДРИН А.Н | |||
| Проблемы взаимодействия | |||
Авторы
Даты
2008-08-27—Публикация
2003-04-18—Подача