Это изобретение относится к периферически селективным ингибиторам дофамин-β-гидроксилазы, способу их получения и их применению в качестве лекарственных средств.
В последние годы интерес к разработке ингибиторов дофамин-β-гидроксилазы (DβH) сосредоточился на гипотезе, что ингибирование этого фермента может обеспечить существенные клинические улучшения у пациентов, страдающих от сердечнососудистых заболеваний, таких как гипертензия или хроническая сердечная недостаточность. Предложение использования ингибиторов DβH основано на их способности ингибировать биосинтез норадреналина за счет ферментативного гидроксилирования дофамина. Активация нейрогуморальных систем, главным образом симпатической нервной системы, представляет собой основное клиническое проявление застойной сердечной недостаточности (Parmley, W.W., Clinical Cardiology, 18: 440-445, 1995). Пациенты с застойной сердечной недостаточностью имеют повышенные концентрации норадреналина в плазме (Levine, Т.В. et al. , Am. J. Cardiol., 49: 1659-1666, 1982), увеличенный центральный симпатический отток (Leimbach, W.N. et al., Circulation, 73: 913-919, 1986) и увеличенный почечно-сердечный избыток норадреналина (Hasking, G.J. et al., Circulation, 73: 615-621, 1966). Длительное и избыточное воздействие норадреналина на миокард может привести к таким явлениям как понижающая регуляция кардиальных β1-адренорецепторов, коррекция левого желудочка, аритмия и некроз, каждое из которых может уменьшить функциональную целостность сердца. Пациенты с застойной сердечной недостаточностью, которые имеют высокие концентрации норадреналина в плазме, также имеют самый неблагоприятный долгосрочный прогноз (Conn, J.N. et al., N. Engl. J. Med., 311: 819-823, 1984). Более важное значение имеет наблюдение, что увеличенные концентрации норадреналина в плазме уже обнаруживаются у пациентов, не имеющих симптомов заболевания, без выраженной сердечной недостаточности, что помогает предсказать возможность смертельного исхода и возникновение заболевания (Benedict, C.R. et al., Circulation, 94: 690-697, 1996) . Активированный симпатический стимул не представляет собой, следовательно, просто клинический маркер застойной сердечной недостаточности, но может внести свой вклад в прогрессирующее ухудшение течения заболевания.
Ингибирование функции симпатического нерва антагонистами адренорецептора оказалось многообещающим подходом, однако существенная часть пациентов не переносит немедленного гемодинамического ухудшения, которое сопровождает воздействие β-блокатора (Pfeffer, М.А. et al., N. Engl. J. Med., 334: 1396-7, 1996). Альтернативная стратегия для непосредственного модулирования функции симпатического нерва состоит в том, чтобы уменьшить биосинтез норадреналина через ингибирование фермента DβH, ответственного за превращение дофамина в норадреналин в симпатических нервах. Этот подход имеет несколько преимуществ, включая постепенную модуляцию в противоположность резкому ингибированию симпатической системы, и увеличенное высвобождение дофамина, которое может улучшить почечную функцию, такую как почечная вазодилатация, диурез и натрийурез. Поэтому ингибиторы DβH могут обеспечить существенные преимущества по сравнению со стандартными β-блокаторами.
О нескольких ингибиторах DβH к настоящему времени сообщили в литературе. Примеры соединений раннего первого и второго поколения, такие как дисульфирам (Goldstein, M. et al., Life Sci., 3: 763, 1964) и диэтилдитиокарбамат (Lippmann, W. et al., Biochem. Pharmacol., 18: 2507, 1969) или фузаровая кислота (Hidaka, H. Nature, 231, 1971) и ароматические или алкильные тиомочевины (Johnson, G.A. et al, J. Pharmacol. Exp. Ther., 171: 80, 1970), как было обнаружено, имели низкую активность, показали низкую селективность к DβH и вызывали токсические побочные эффекты. Однако ингибиторы DβH третьего поколения, как обнаружили, имеют намного большую активность, такие как, например, непикастат (RS-25560-197, IC50 9 нМ) (Stanley, W.C., et al., Br. J. Pharmacol., 121: 1803-1809, 1997), который перешел на раннюю стадию клинических испытаний. Несмотря на преодоление некоторых проблем, связанных с первым и вторым поколением ингибиторов DβH, очень важным открытием стал тот факт, что непикастат пересекает гематоэнцефалический барьер (ГЭБ) и таким образом, может вызвать как центральные, так и периферические эффекты, и такая ситуация способна вызвать нежелательные и потенциально серьезные побочные эффекты лекарственного средства на ЦНС. Следовательно, остается неудовлетворительной клиническая потребность в сильнодействующем, нетоксичном и периферически селективном ингибиторе DβH, который можно применять для лечения определенных сердечно-сосудистых заболеваний. Ингибитор DβH с подобной или еще большей активностью, чем непикастат, но не оказывающий воздействия на ЦНС (неспособный пересекать ГЭБ), обеспечил бы существенное усовершенствование по сравнению со всеми ингибиторами DβH, описанными к настоящему времени в данной области техники.
Ингибиторы дофамин-β-гидроксилазы также раскрыты в WO95/29165. Кроме того, WO2004/033447 раскрывает ингибиторы дофамин-β-гидроксилазы, имеющие высокую активность и значительно уменьшенное проникновение в мозг, позволяющее получить сильные и периферически селективные ингибиторы DβH.
В настоящий момент авторы обнаружили новые соединения, которые представляют собой сильные ингибиторы дофамин-β-гидроксилазы, обладающие высокой активностью и значительно уменьшенным проникновением в мозг.
Согласно одному аспекту изобретения обеспечивают соединение формулы I:
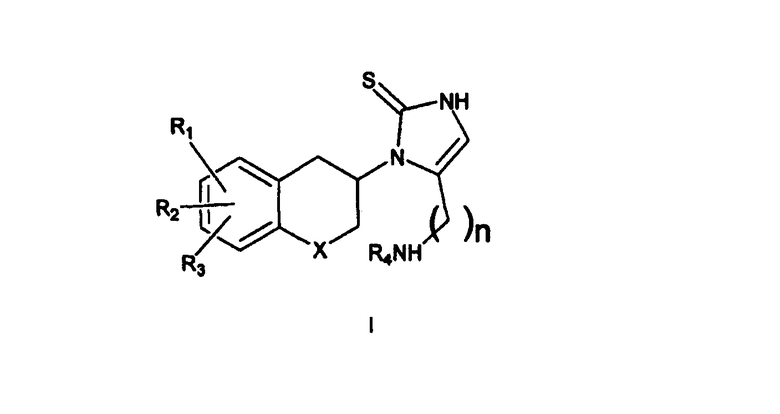
в которой R1, R2 и R3, одинаковые или различные, представляют собой водород, галоген, алкил, нитро, амино, алкилкарбониламино, алкиламино или диалкиламиногруппу; R4 представляет собой -алкиларил или -алкилгетероарил; X представляет собой CH2, атом кислорода или атом серы; n равно 2 или 3; включая его индивидуальные (R)- и (S)-энантиомеры или смеси энантиомеров; и включая его фармацевтически приемлемые соли и сложные эфиры, где термин «алкил» обозначает углеводородные цепи, прямые или разветвленные, содержащие от одного до шести атомов углерода, необязательно замещенные арилом, алкокси, галогеном, алкоксикарбонильной или гидроксикарбонильной группой; термин «арил» обозначает фенильную или нафтильную группу, необязательно замещенную алкилом, алкилокси, галогеном или нитрогруппой; термин «галоген» обозначает фтор, хлор, бром или йод; термин «гетероарил» обозначает гетероароматическую группу.
В предпочтительном варианте осуществления n=2.
В дальнейшем предпочтительном варианте осуществления X=O.
Предпочтительно, R4 представляет собой -CH2-арил или -CH2-гетероарил.
В одном варианте осуществления арильная группа R4 является незамещенной.
Арильная группа R4 может предпочтительно быть фенилом.
Предпочтительно, один из R1, R2 и R3 представляет собой водород, и другие представляют собой фтор.
Соединение формулы I можно представить в виде (R)- или (S)-энантиомера, или в виде смеси (R)- и (S)-энантиомеров в любых соотношениях, включая рацемат. Соединение формулы I наиболее предпочтительно состоит из R-энантиомера.
Соединение можно соответственно обеспечить в форме соли хлороводородной кислоты. Однако учитывая вторичную алифатическую аминогруппу, будет очевидно для специалиста в данной области техники, что другие соли кислот могут быть получены и находятся в рамках заявленного изобретения.
Согласно другому аспекту изобретения представлен способ получения индивидуальных (R)- и (S)-энантиомеров или смеси энантиомеров и фармацевтически приемлемых солей соединения формулы I, как описано выше, который включает взаимодействие индивидуальных (R)- или (S)-энантиомеров или смеси энантиомеров соединения формулы III
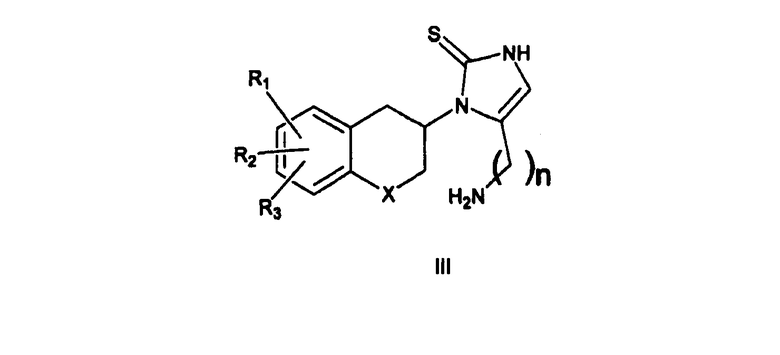
где X, R1, R2, R3 и n имеют значения, определенные для формулы I выше, с соединением формулы IV
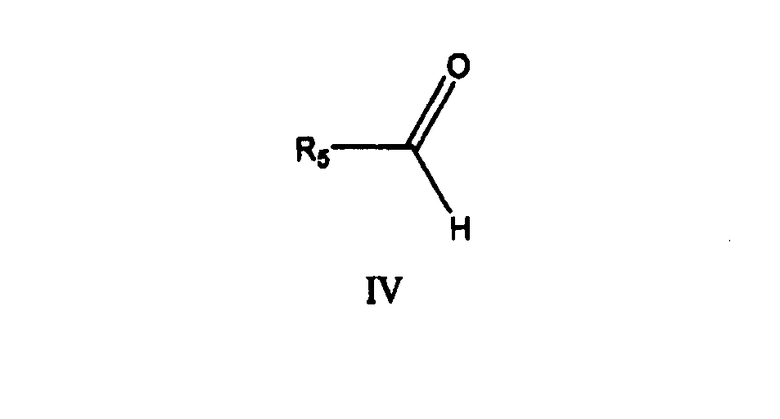
в которой R5 представляет собой арил или гетероарил, в котором термин «арил» обозначает фенильную или нафтильную группу, необязательно замещенную алкилом, алкилокси, галогеном или нитрогруппой; термин «галоген» обозначает фтор, хлор, бром или йод; термин «гетерил» обозначает гетероароматическую группу; в условиях восстановительного алкилирования.
Условия, необходимые для вышеупомянутого восстановительного алкилирования, будут очевидны специалисту в данной области техники.
Согласно наиболее предпочтительному варианту осуществления изобретения получают соединение формулы X:
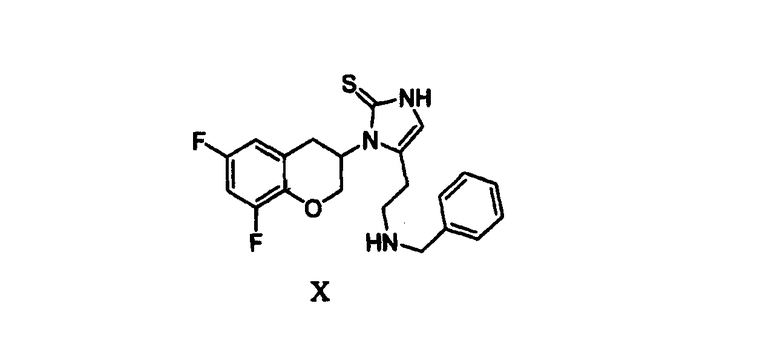
его (R)- или (S)-энантиомер, или смесь (R)- и (S)-энантиомера, или их фармацевтически приемлемые соли или сложные эфиры.
Соединение формулы X можно обеспечить в виде (R)- или (S)-энантиомера или в виде смеси (R)- и (S)-энантиомеров в любых соотношениях, включая рацемат. Предпочтительно, соединение формулы X обеспечивают в виде R-энантиомера, (R)-X:
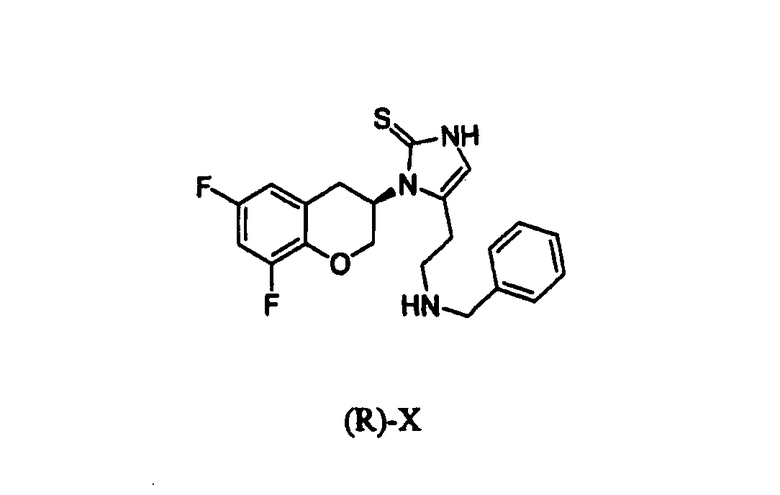
Соединение формулы X (или R-(X)), соответственно, предоставляют в виде соли хлороводородной кислоты. Однако учитывая вторичную алифатическую аминогруппу, будет очевидно для специалиста в данной области техники, что другие соли кислот могут быть получены и находятся в рамках заявленного изобретения.
Соединение формулы X можно получить, например, восстановительным алкилированием, обработкой (R)-5-(2-аминоэтил)-1-(6,8-дифторхроман-3-ил)-1,3-дигидроимидазол-2-тиона и бензальдегида в растворителе или смеси растворителей, таких как, например, метанол и дихлорметан, в присутствии восстанавливающего реагента, такого как, например, цианоборгидрид натрия, триацетоксиборгидрид натрия, боргидрид натрия и подобные, или водород в присутствии катализатора гидрирования. При желании, после выделения продукта реакции неочищенный продукт можно очистить с помощью колоночной хроматографии на силикагеле.
Согласно другому аспекту изобретения в нем обеспечивают фармацевтическую композицию, включающую терапевтически эффективное количество соединения, как описано выше, в комбинации с фармацевтически эффективным носителем.
Согласно дальнейшему аспекту изобретения в нем обеспечивают композицию, включающую терапевтически эффективное количество соединения, как описано выше, в комбинации с фармацевтически эффективным носителем и одним или более соединениями, выбранными из классов, описанных ниже.
В частности, соединения формулы I или X можно объединить с одним или более следующими классами соединений: диуретические средства; бета-адренергические антагонисты; альфа2-адренергические агонисты; альфа1-адренергические антагонисты; двойные бета- и альфа-адренергические антагонисты; блокаторы кальциевых каналов; активаторы калиевых каналов; антиаритмические средства; ингибиторы АПФ; антагонисты AT1-рецепторов; ингибиторы ренина; гиполипидемические средства, ингибиторы вазопептидазы; нитраты; антагонисты эндотелина; ингибиторы нейтральной эндопептидазы; антиангиотензиновые вакцины; вазодилататоры; ингибиторы фосфодиэстеразы; сердечные гликозиды; антагонисты серотонина; и агенты, действующие на ЦНС.
Наиболее пригодные диуретические средства включают
(1) Петлевые диуретические средства, в частности фуросемид, буметанид, этакриновую кислоту, торасемид, азосемид, музолимин, пиретанид, трипамид.
(2) Тиазидные диуретические средства, в частности бендрофлуметиазол, хлортиазид, гидрохлортиазид, гидрофлуметиазид, метилклотиазид, политиазид, трихлорметиазид.
(3) Тиазидподобные диуретические средства, в частности хлорталидон, индапамид, метозалон, квинетазон.
(4) Калийсберегающие диуретические средства, в частности амилорид, триамтерен.
(5) Антагонисты альдостерона, в частности спиролактон, канренон, эплеренон.
(6) Комбинации вышеупомянутых описанных диуретических средств.
Можно применять более чем одно из вышеупомянутых диуретических средств.
Наиболее пригодные бета-адренергические антагонисты включают тимолол, метопролол, атенолол, пропранолол, бисопролол, небиволол. Можно применять более чем один из вышеупомянутых бета-адренергических антагонистов.
Наиболее пригодные альфа2-адренергические агонисты включают клонидин, гуанабенз, гуанфацин. Можно применять более чем один из вышеупомянутых альфа2-адренергических агонистов.
Наиболее пригодные альфа1-адренергические антагонисты включают празозин, доксазозин, фентоламин. Можно применять более чем один из вышеупомянутых альфа1-адренергических антагонистов.
Наиболее пригодные двойные бета- и альфа-адренергические антагонисты (кроме упомянутых в другом месте в описании) включают карведилол, лабеталол. Можно применять более чем один из вышеупомянутых двойных бета- и альфа-адренергических антагонистов.
Активаторы калиевых каналов включают никорандил.
Наиболее пригодные блокаторы кальциевых каналов включают амлодипин, бепридил, дилтиазем, фелодипин, исрадипин, никардипин, нифедипин, нимодипин, нисолдипин, верапамил. Можно применять более чем один из вышеупомянутых блокаторов кальциевых каналов.
Антиаритмические средства, кроме упомянутых в другом месте в описании, включают блокаторы натриевых каналов, такие как хинидин, прокаинамид, дизопирамид, лидокаин, мексилетин, токаинид, фенитоин, энкаинид, флекаинид, морицизин и пропафенон; блокаторы калиевых каналов, такие как амиодарон, бретилий, ибутилид, дофетилид, азимилид, клофилиум, тедисамил, сематилид, соталол; и эсмолол, пропранолол, метопролол. Можно применять более чем одно из антиаритмических средств, упомянутых в описании,.
Наиболее пригодные ингибиторы АПФ включают бензеприл, каптоприл, эналаприл, фозиноприл, лизиноприл, имидаприл, моэксиприл, периндоприл, хинаприл, рамиприл, трандолаприл. Можно применять более чем один из вышеупомянутых ингибиторов АПФ.
Наиболее пригодные антагонисты AT1-рецепторов включают кандесартан, ирбесартан, лозартан, телмисартан, валзартан, эпросартан. Можно применять более чем один из вышеупомянутых антагонистов AT1-рецепторов.
Гиполипидемические средства включают статины, такие как аторвастатин, церивастатин, флувастатин, ловастатин, мевастатин, питавастатин, правастатин, розувастатин, симвастатин; секвестранты желчных кислот, такие как холестирамин, колестипол и колесевелам; ингибиторы абсорбции холестерина, такие как эзетимиб; фибраты, такие как фенофибрат, гемфиброзил; ниацин. Можно применять более чем одно из вышеупомянутых гиполипидемических средств.
Наиболее пригодные нитраты включают органические нитраты, такие как амилнитрит, нитроглицерин, изосорбид-динитрат, изосорбид-5-мононитрат, эритрит тетранитрат. Можно применять более чем один из вышеупомянутых органических нитратов.
Антагонисты эндотелина включают бозентан, ситаксентан. Можно применять более чем один из вышеупомянутых антагонистов эндотелина.
Наиболее пригодные вазодилататоры (кроме упомянутых в другом месте в описании) включают гидралазин, миноксидил, нитропруссид натрия, диазоксид. Можно применять более чем один из вышеупомянутых вазодилататоров.
Наиболее пригодные ингибиторы фосфодиэстеразы включают милринон, инамринон. Можно применять более чем один из вышеупомянутых ингибиторов фосфодиэстеразы.
Сердечные гликозиды включают аллокар, коррамедан, дигитоксин, дигоксин, ланоксин, пургоксин, цедиланид-D, кристодигин, ланоксикапс. Можно применять более чем один из вышеупомянутых сердечных гликозидов.
Антагонисты серотонина включают клозапин, локсапин, оланзапин, рисперидон, зипрасидон, ритансерин, кетансерин, амоксапин. Можно применять более чем один из вышеупомянутых антагонистов серотонина.
Агенты, действующие на ЦНС, кроме уже упомянутых в другом месте в этой спецификации, включают агонисты имидазолина, такие как моксонидин. Наиболее пригодный агент, действующий на ЦНС, представляет собой метилдопу.
Наиболее пригодные ингибиторы ренина включают алискирен, эналкирен, дитекирен, терлакирен, ремикирен, занкирен, ципрокирен. Можно применять более чем один из вышеупомянутых ингибиторов ренина.
Наиболее пригодные ингибиторы вазопептидазы включают омапатрилат, сампатрилат, гемопатрилат. Можно применять более чем один из вышеупомянутых ингибиторов вазопептидазы.
Другие фармацевтические средства, используемые при лечении сердечной недостаточности, можно также объединить с соединениями формулы I или X. Они включают активаторы кальция; ингибиторы редуктазы HMG CoA; антагонисты вазопрессина; антагонисты рецептора аденозина A1; агонисты атриального натрийуретического пептида (ANP); хелатирующие агенты; рецептор рилизинг-фактора кортикотропина; агонисты глюкагоноподобного пептида-1; ингибиторы натрий,калий-АТФазы; улучшенные прерыватели сшивания конечного продукта гликозилирования (AGE); ингибиторы смешанного неприлизин/эндотелин превращающего фермента (NEP/ECE); агонисты рецептора ноцицептина (ORL-1) (например, алпразолам); ингибиторы ксантиноксидазы; агонисты бензодиазепина; активаторы сердечного миозина; ингибиторы химазы; усилители транскрипции эндотелиальной синтазы оксида азота (ENOS); ингибиторы нейтральной эндопептидазы, такие как тиорфан.
Изобретение также предусматривает использование непикастата с классами соединений, описанных выше.
Для получения фармацевтических композиций соединений формулы I или X, инертные фармацевтически приемлемые носители примешивают к активным соединениям. Фармацевтически приемлемые носители могут быть или твердым веществом или жидкостью. Твердые лекарственные формы включают порошки, таблетки, дисперсные гранулы и капсулы. Носитель может быть одним или более веществами, которые могут также действовать как разбавители, ароматизирующие вещества, солюбилизаторы, смазывающие вещества, суспендирующие агенты, связывающие вещества или агенты, дезинтегрирующие таблетку; носитель может также быть капсулирующим соединением.
Предпочтительно, фармацевтическая композиция находится в стандартной лекарственной форме, например, упакованное лекарственное средство, упаковка, содержащая дискретные количества лекарственного средства, такие как пакетированные таблетки, капсулы и порошки в виалах или ампулах.
Дозировки могут быть различны в зависимости от потребностей пациента, степени заболевания и определенного соединения, которое применяют. Для удобства, полная ежедневная доза может быть разделена и вводиться частями в течение дня. Предполагается, что введение один или два раза в сутки будет наиболее подходящим. Определение соответствующей дозировки для определенной ситуации производится специалистом в данной области техники.
Согласно другому аспекту изобретения в нем обеспечивают соединение формулы I или формулы X, как описано выше, для применения в качестве лекарственного средства.
Согласно другому аспекту изобретения в нем обеспечивают применение соединения формулы I или формулы X, как описано выше, для получения лекарственного средства для лечения заболеваний, где восстановление в реакции гидроксилирования допамина в норадреналин имеет полезный терапевтический эффект.
Соединения формул I или X можно также использовать в сочетании с одним или более соединениями, выбранными из следующих классов соединений:
диуретические средства; бета-адренергические антагонисты; альфа2-адренергические агонисты; альфа1-адренергические антагонисты; двойные бета- и альфа-адренергические антагонисты; блокаторы кальциевых каналов; активаторы калиевых каналов; антиаритмические средства; ингибиторы АПФ; антагонисты AT1-рецепторов; ингибиторы ренина; гиполипидемические средства, ингибиторы вазопептидазы; нитраты; антагонисты эндотелина; ингибиторы нейтральной эндопептидазы; антиангиотензиновые вакцины; вазодилататоры; ингибиторы фосфодиэстеразы; сердечные гликозиды; антагонисты серотонина; агенты, действующие на ЦНС; активаторы кальция; ингибиторы редуктазы HMG CoA; антагонисты вазопрессина; антагонисты рецептора аденозина A1; агонисты атриального натрийуретического пептида (ANP); хелатирующие агенты; рецептор рилизинг-фактора кортикотропина; агонисты глюкагоноподобного пептида-1; ингибиторы натрий,калий-АТФазы; улучшенные прерыватели сшивания конечного продукта гликозилирования (AGE); ингибиторы смешанного неприлизин/эндотелин превращающего фермента (NEP/ECE); агонисты рецептора ноцицептина (ORL-1) (например, алпразолам); ингибиторы ксантиноксидазы; агонисты бензодиазепина; активаторы сердечного миозина; ингибиторы химазы; усилители транскрипции эндотелиальной синтазы оксида азота (ENOS); и ингибиторы нейтральной эндопептидазы, такие как тиорфан.
Используемый в настоящем описании термин «лечение» и вариации, такие как «лечить» или «лечащий», относится к любому режиму, который может принести пользу человеку или животному. Лечение может быть текущего состояния или может быть профилактическим (профилактическое лечение). Лечение может включать лечебный, смягчающий или профилактический эффекты. Лечение соединением формулы I или X в комбинации с одним из других классов соединений включает одновременное и последовательное введение этих двух или более лекарственных средств.
Согласно другому аспекту изобретения представлено применение соединения формулы I или формулы X, как описано выше, для получения лекарственного средства для лечения пациента с тревожными расстройствами.
Тревожные расстройства включают, но без ограничения, генерализованные тревожные расстройства, социальные тревожные расстройства, посттравматическое стрессовое расстройство, острое стрессовое расстройство, синдромы навязчивых состояний, расстройства панического типа, такие как приступы паники и фобии, такие как агорафобия, социальные фобии, специфические фобии. Другие тревожные расстройства, которые лечат, используя соединения настоящего изобретения, могут быть найдены на страницах 429-484 American Psychiatric Association: Diagnostic and Statistic Manual of Mental Disorders, 4th edition, Text Revision, Washington, DC, American Psychiatric Association, 2000 .
Согласно другому аспекту изобретения представлено применение соединения формулы I или формулы X, как описано выше, для получения лекарственного средства для лечения мигрени.
Согласно другому аспекту изобретения представлено применение соединения формулы I или формулы X, как описано выше, для получения лекарственного средства для лечения пациента, подверженного сердечно-сосудистым расстройством.
Согласно другому аспекту изобретения представлено применение соединения формулы I или формулы X, как описано выше, для получения лекарственного средства для лечения гипертензии или хронической или застойной сердечной недостаточности.
Согласно другому аспекту изобретения представлено применение соединения формулы I или формулы X, как описано выше, для получения лекарственного средства для лечения одного или большего количества следующих заболеваний: стенокардия, аритмия и циркуляторные нарушения, такие как феномен Рейно.
Согласно другому аспекту изобретения представлено применение соединения формулы I или формулы X, как описано выше, для получения лекарственного средства для применения в ингибировании дофамин-β-гидроксилазы.
Согласно другому аспекту изобретения представлен способ лечения тревожных расстройств, включающий введение
терапевтически эффективного количества соединения формулы I или формулы X, как описано выше, нуждающемуся в этом пациенту.
Согласно другому аспекту изобретения представлен способ лечения мигрени, включающий введение терапевтически эффективного количества соединения формулы I или формулы X, как описано выше, нуждающемуся в этом пациенту.
Согласно другому аспекту изобретения представлен способ лечения сердечно-сосудистых заболеваний, включающий введение терапевтически эффективного количества соединения формулы I или формулы X, как описано выше, нуждающемуся в этом пациенту.
Согласно другому аспекту изобретения представлен способ лечения гипертензии, включающий введение терапевтически эффективного количества соединения формулы I или формулы X, как описано выше, нуждающемуся в этом пациенту.
Согласно другому аспекту изобретения представлен способ лечения хронической или застойной сердечной недостаточности, включающий введение терапевтически эффективного количества соединения формулы I или формулы X, как описано выше, нуждающемуся в этом пациенту.
Согласно другому аспекту изобретения представлен способ лечения одного или большего количества следующих заболеваний: стенокардия, аритмия и циркуляторные нарушения, такие как феномен Рейно, включающий введение терапевтически эффективного количества соединения формулы I или формулы X, как описано выше, нуждающемуся в этом пациенту.
Вышеописанные способы лечения могут дополнительно включать одновременное или последовательное введение лекарственного средства из одного из следующих классов соединений:
диуретические средства; бета-адренергические антагонисты; альфа2-адренергические агонисты; альфа1-адренергические антагонисты; двойные бета- и альфа-адренергические антагонисты; блокаторы кальциевых каналов; активаторы калиевых каналов; антиаритмические средства; ингибиторы АПФ; антагонисты AT1-рецепторов; ингибиторы ренина; гиполипидемические средства, ингибиторы вазопептидазы; нитраты; антагонисты эндотелина; ингибиторы нейтральной эндопептидазы; антиангиотензиновые вакцины; вазодилататоры; ингибиторы фосфодиэстеразы; сердечные гликозиды; антагонисты серотонина; агенты, действующие на ЦНС; активаторы кальция; ингибиторы редуктазы HMG CoA; антагонисты вазопрессина; антагонисты рецептора аденозина A1; агонисты атриального натрийуретического пептида (ANP); хелатирующие агенты; рецептор рилизинг-фактора кортикотропина; агонисты глюкагоноподобного пептида-1; ингибиторы натрий,калий-АТФазы; улучшенные прерыватели сшивания конечного продукта гликозилирования (AGE); ингибиторы смешанного неприлизин/эндотелин превращающего фермента (NEP/ECE); агонисты рецептора ноцицептина (ORL-1) (например, алпразолам); ингибиторы ксантиноксидазы; агонисты бензодиазепина; активаторы сердечного миозина; ингибиторы химазы; усилители транскрипции эндотелиальной синтазы оксида азота (ENOS); и ингибиторы нейтральной эндопептидазы, такие как тиорфан.
Если не заявлено иначе, в этом описании термин «алкил» (используемый самостоятельно или в комбинации с другими частями) обозначает углеводородные цепи, прямые или разветвленные, содержащие от одного до шести атомов углерода, необязательно замещенные арилом, алкокси, галогеном, алкоксикарбонильной или гидроксикарбонильной группой; термин «арил» (используемый самостоятельно или в комбинации с другими частями) обозначает фенильную или нафтильную группу, необязательно замещенную алкилом, алкилокси, галогеном или нитрогруппой; и термин «галоген» обозначает фтор, хлор, бром или йод; термин «гетероарил» обозначает гетероароматическую группу. Кроме того, термины «алкокси» и «алкилокси» взаимозаменяемы, если иначе не обозначено.
Материалы и методы
Мыши-самцы NMRI были получены от Harlan-Interfauna (Испания) и помещены по 10 в клетку при контролируемых условиях окружающей среды (12 ч цикл день/ночь и комнатная температура 22±1°C). Обеспечивали свободный доступ к пище и водопроводной воде и эксперимент проводили в дневное время.
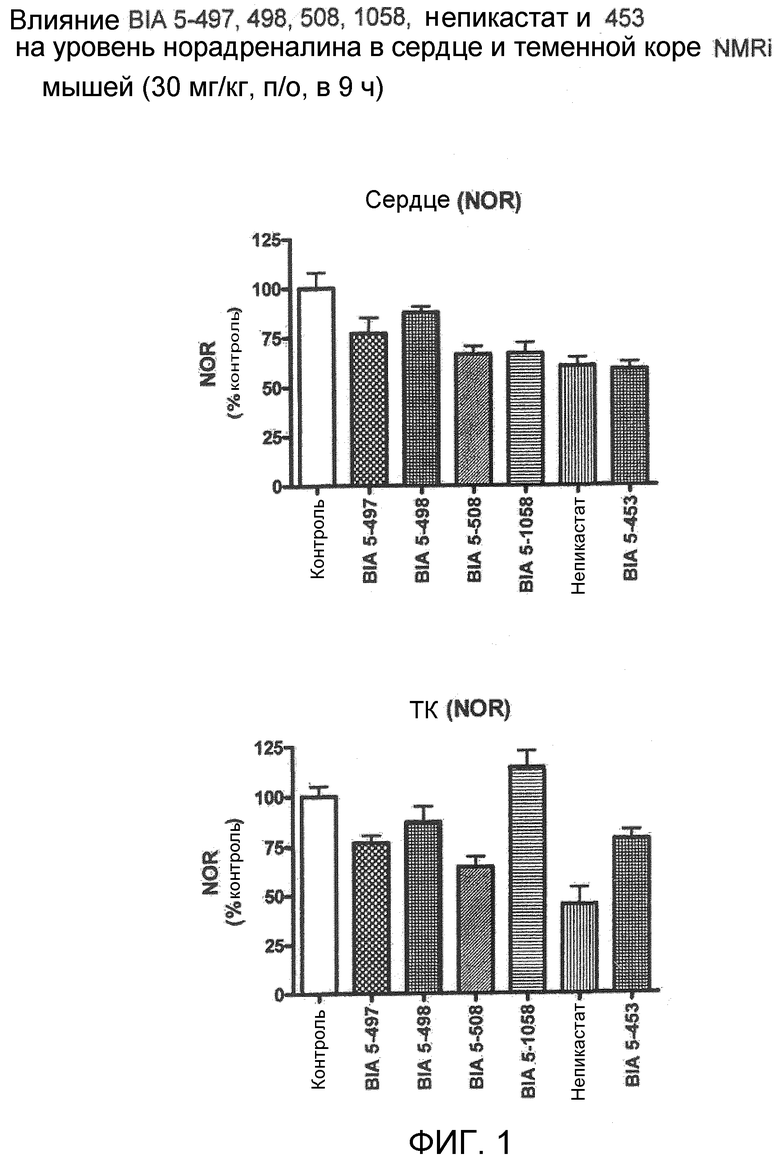
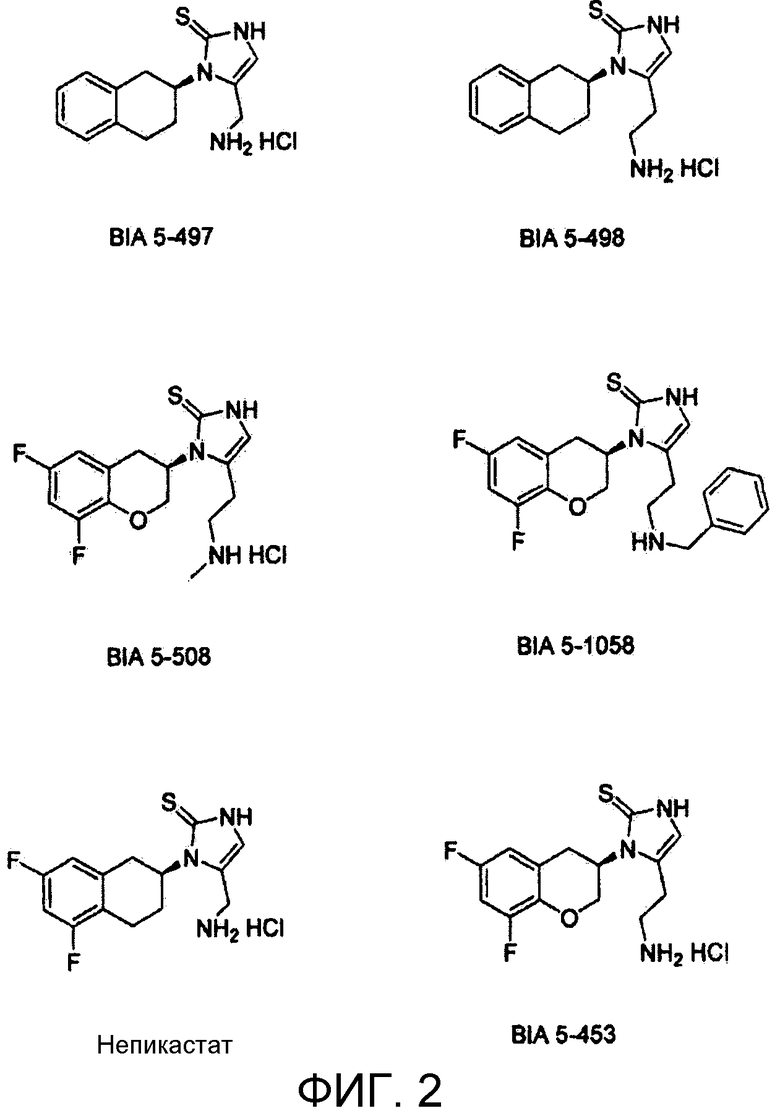
При времени = 0 ч, животным вводили любые тестируемые соединения (см. фиг.2) в заданной дозе или носитель (вода) перорально с помощью зонда. Через 9 ч после введения дозы животных умерщвляли путем декапитации и выделяли сердце (левое предсердие и левый желудочек) и мозг (теменная кора), взвешивали и хранили в объеме 0,2 М перхлорной кислоты в течение 12 ч при 4°C в темноте. После инкубирования результирующий супернатант собирали с помощью фильтрации инкубатов на центрифуге (0,2 мкМ/10 минут/~5000 оборотов в минуту, 4°C). Супернатант хранили замороженным при -80°C до анализа. Определение количества дофамина и норадреналина в супернатантах выполняли с помощью высокоэффективной жидкостной хроматографии с электрохимической детекцией.
Результаты
Как можно определить из фиг.1, соединение формулы X показало заметную селективность для сердца по сравнению с мозгом при сравнении с другими ингибиторами DβH известного уровня техники.
Далее ссылаются на прилагаемые чертежи, на которых
фиг.1 показывает влияние соединений на уровень норадреналина в сердце и теменной коре и
фиг.2 показывает структуры тестируемых соединений.
Примеры
Пример 1
(R)-5-(2-(бензиламино)этил)-1-(6,8-дифторхроман-3-ил)-1H-имидазол-2(3H)тион.
К (R)-5-(2-аминоэтил)-1-(6,8-дифторхроман-3-ил)-1,3-дигидроимидазол-2-тиону (2,36 г, 7,58 ммоль) и бензальдегиду (0,85 мл, 8,34 ммоль) в смеси метанола (15 мл) и дихлорметана (15 мл) добавляли цианоборгидрид натрия (0,67 г, 10,66 ммоль) при 20-25°C частями. Смесь перемешивали в течение 64 ч, гасили 1N HCl (12 мл) с перемешиванием, с последующим добавлением 3N NaOH (12 мл). Смесь экстрагировали ДХМ (100 мл), органическую фазу промывали солевым раствором (50 мл), высушивали (MgSO4) и выпаривали досуха. Остаток очищали на колонке с силикагелем, используя этилацетат и смесь этилацетата с метанолом (9:1) в качестве элюентов. Фракции, содержащие продукт, собирали, упаривали при пониженном давлении до около 20 мл, затем охлаждали на льду. Осадок собирали, промывали смесью этилацетат - петролейный эфир (1:1), высушивали на воздухе. Выход составлял 1,25 г (41%), продукт, имеющий т.пл. 188-90°C (2-пропанол-ДХМ).
Будет понятно, что описанное выше изобретение может быть изменено в объеме приложенной формулы изобретения.
| название | год | авторы | номер документа |
|---|---|---|---|
| ТЕРАПЕВТИЧЕСКОЕ ЛЕЧЕНИЕ МЕТАБОЛИЧЕСКОГО СИНДРОМА, ДИАБЕТА 2 ТИПА, ОЖИРЕНИЯ ИЛИ ПРЕДИАБЕТА | 2008 |
|
RU2467743C2 |
| ЛЕЧЕНИЕ ПОСТТРАВМАТИЧЕСКОГО СТРЕССОВОГО РАССТРОЙСТВА | 2008 |
|
RU2458691C2 |
| КОМБИНАЦИИ, СОДЕРЖАЩИЕ АНТИМУСКАРИНОВЫЕ СРЕДСТВА И БЕТА-АДРЕНЕРГИЧЕСКИЕ АГОНИСТЫ | 2010 |
|
RU2465902C2 |
| Производные 1,3-дигидроимидазол-2-тиона для применения в лечении легочной артериальной гипертензии и повреждения легкого | 2013 |
|
RU2718055C2 |
| КОМБИНАЦИИ, СОДЕРЖАЩИЕ АНТИМУСКАРИНОВЫЕ СРЕДСТВА И БЕТА-АДРЕНЕРГИЧЕСКИЕ АГОНИСТЫ | 2005 |
|
RU2379033C2 |
| ЛЕЧЕНИЕ ПСИХОЛОГИЧЕСКИХ СОСТОЯНИЙ С ПРИМЕНЕНИЕМ АНТАГОНИСТОВ M-МУСКАРИНОВЫХ РЕЦЕПТОРОВ | 2007 |
|
RU2477634C2 |
| ЛЕЧЕНИЕ ОЖИРЕНИЯ АНТАГОНИСТАМИ МУСКАРИНОВОГО РЕЦЕПТОРА М1 | 2007 |
|
RU2455981C2 |
| (R)-ПИРЛИНДОЛ И ЕГО ФАРМАЦЕВТИЧЕСКИ ПРИЕМЛЕМЫЕ СОЛИ ДЛЯ ПРИМЕНЕНИЯ В МЕДИЦИНЕ | 2014 |
|
RU2695607C2 |
| КОМБИНАЦИИ, СОДЕРЖАЩИЕ АНТИМУСКАРИНОВЫЕ СРЕДСТВА И БЕТА-АДРЕНЕРГИЧЕСКИЕ АГОНИСТЫ | 2005 |
|
RU2404771C2 |
| НОВЫЕ ПРИМЕНЕНИЯ | 2019 |
|
RU2836384C2 |
Данное изобретение относится к новым производным 1,3-дигидроимидазол-2-тиона формулы I:
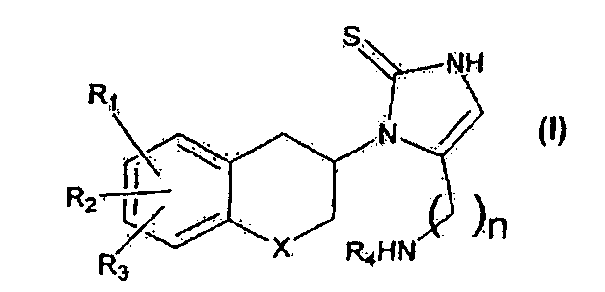
в которой R1, R2 и R3, одинаковые или различные, представляют собой водород или галоген; R4 представляет собой алкиларил; X представляет собой атом кислорода; n равно 2 или 3; его индивидуальные (R)-энантиомеры; или его фармацевтически приемлемые соли, где термин «алкил» обозначает углеводородные цепи, прямые или разветвленные, содержащие от одного до шести атомов углерода; термин «арил» обозначает фенильную или нафтильную группу; термин «галоген» обозначает фтор, хлор, бром или йод. Изобретение также относится к способу получения этих соединений, к фармацевтической композиции на их основе, обладающей ингибирующей активностью в отношении дофамин-бета-гидроксилазы, способам лечения различных сердечно-сосудистых заболеваний, таких как гипертензия и хроническая сердечная недостаточность, и применению соединений формулы 1 для получения лекарственных средств для лечения этих заболеваний. 20 н. и 12 з.п. ф-лы, 2 ил., 1 пр.
1. Соединение формулы I
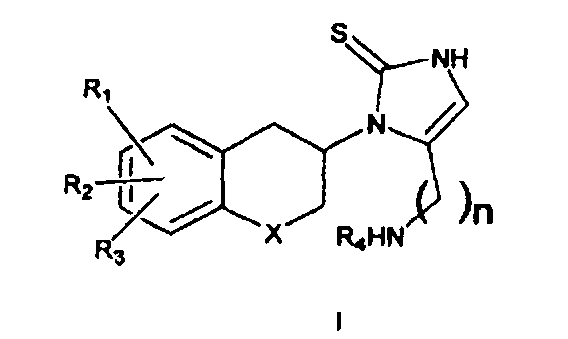
в которой R1, R2 и R3, одинаковые или различные, представляют собой водород или галоген; R4 представляет собой алкиларил; X представляет собой атом кислорода; n равно 2 или 3; его индивидуальные (R)-энантиомеры; или его фармацевтически приемлемые соли, где термин «алкил» обозначает углеводородные цепи, прямые или разветвленные, содержащие от одного до шести атомов углерода; термин «арил» обозначает фенильную или нафтильную группу; термин «галоген» обозначает фтор, хлор, бром или йод.
2. Соединение по п.1, в котором n равно 2.
3. Соединение по п.1, в котором R4 представляет собой -СН2-арил.
4. Соединение по п.1, в котором арильная группа R4 представляет собой фенил.
5. Соединение по п.1, в котором один из R1, R2 и R3 представляет собой водород, и другие представляют собой фтор.
6. Соединение по п.1, в котором указанное соединение состоит из R-энантиомера.
7. Соединение по п.1, представляющее собой гидрохлоридную соль соединения формулы I.
8. Способ получения индивидуального (R)-энантиомера и фармацевтически приемлемых солей соединения формулы I, включающий взаимодействие индивидуального (R)-энантиомера соединения Формулы III
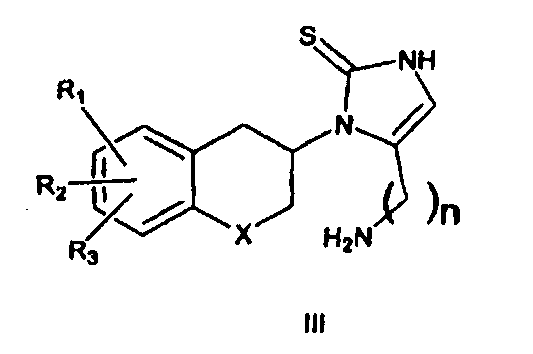
в которой X, R1, R2, R3 и n имеют значения, указанные по п.1, с соединением формулы IV
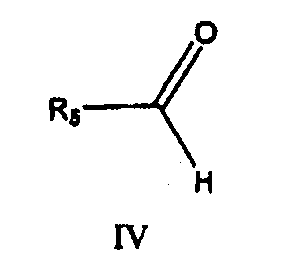
где R5 представляет собой арил, где термин «арил» обозначает фенильную или нафтильную группу; термин «галоген» обозначает фтор, хлор, бром или йод; в условиях восстановительного алкилирования.
9. Соединение формулы X
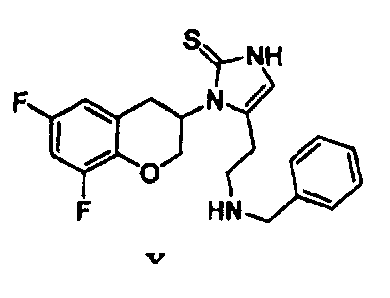
его (R)-энантиомер, или его фармацевтически приемлемые соли.
10. Соединение по п.9, представляющее собой гидрохлоридную соль соединения формулы X.
11. Способ получения соединения формулы X по п.9 или 10, включающий взаимодействие (R)-5-(2-аминоэтил)-1-(6,8-дифторохроман-3-ил)-1,3-дигидроимидазол-2-тиона и бензальдегида в условиях восстановительного алкилирования.
12. Способ по п.11, в котором восстановительное алкилирование проводят в присутствии восстанавливающего реагента.
13. Способ по п.12, в котором восстанавливающий реагент представляет собой цианоборгидрид натрия, триацетоксиборгидрид натрия, боргидрид натрия или водород в присутствии катализатора гидрирования.
14. Способ по любому из пп.9-13, в котором взаимодействие проводят в смеси метанола и дихлорметана.
15. Способ по п.11, который дополнительно включает стадию очистки.
16. Фармацевтическая композиция, обладающая ингибирующей активностью в отношении дофамин-бета-гидроксилазы, включающая терапевтически эффективное количество соединения по любому из пп.1-7, 9 или 10 в комбинации с фармацевтически эффективным носителем.
17. Соединение по п.9 или 10, предназначенное для применения в качестве лекарственного средства, обладающего ингибирующей активностью в отношении дофамин-бета-гидроксилазы.
18. Применение соединения по любому из пп.1-7, 9 или 10 для получения лекарственного средства для лечения расстройств, при которых снижение гидроксилирования дофамина до норадреналина имеет полезный терапевтический эффект.
19. Применение соединения по любому из пп.1-7, 9 или 10 для получения лекарственного средства для лечения пациента, подверженного тревожным расстройствам.
20. Применение соединения по любому из пп.1-7, 9 или 10 для получения лекарственного средства для лечения мигрени.
21. Применение соединения по любому из пп.1-7, 9 или 10 для получения лекарственного средства для лечения пациента, подверженного сердечно-сосудистым заболеваниям.
22. Применение соединения по любому из пп.1-7, 9 или 10 для получения лекарственного средства для лечения гипертензии.
23. Применение соединения по любому из пп.1-7, 9 или 10 для получения лекарственного средства для лечения хронической сердечной недостаточности.
24. Применение соединения по любому из пп.1-7, 9 или 10 для получения лекарственного средства для лечения застойной сердечной недостаточности.
25. Применение соединения по любому из пп.1-7, 9 или 10 для получения лекарственного средства для лечения одного или более из следующих заболеваний: стенокардии, аритмии и циркуляторных нарушений, таких как феномен Рейно.
26. Применение соединения по любому из пп.1-7, 9 или 10 для получения лекарственного средства для применения в ингибировании дофамин-β-гидроксилазы.
27. Способ лечения тревожных расстройств, в котором терапевтически эффективное количество соединения по любому из пп.1-7, 9 или 10 вводят нуждающемуся в этом пациенту.
28. Способ лечения мигрени, в котором терапевтически эффективное количество соединения по любому из пп.1-7, 9 или 10 вводят нуждающемуся в этом пациенту.
29. Способ лечения сердечно-сосудистых заболеваний, в котором терапевтически эффективное количество соединения по любому из пп.1-7, 9 или 10 вводят нуждающемуся в этом пациенту.
30. Способ лечения гипертензии, в котором терапевтически эффективное количество соединения по любому из пп.1-7, 9 или 10 вводят нуждающемуся в этом пациенту.
31. Способ лечения хронической или застойной сердечной недостаточности, в котором терапевтически эффективное количество соединения по любому из пп.1-7, 9 или 10 вводят нуждающемуся в этом пациенту.
32. Способ лечения одного или более из следующих заболеваний: стенокардия, аритмия и циркуляторные нарушения, такие как феномен Рейно, в котором терапевтически эффективное количество соединения по любому из пп.1-7, 9 или 10 вводят нуждающемуся в этом пациенту.
| WO 2004033447 А, 22.04.2004 | |||
| Beliaev A | |||
| at al, J | |||
| Medicinal Chemistry, 2006, v.49, no.3, p.1191-1197 | |||
| ПРОИЗВОДНЫЕ БЕНЗОКСАЗОЛОНА, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ И СПОСОБЫ ЛЕЧЕНИЯ | 2002 |
|
RU2279431C2 |
Авторы
Даты
2013-12-20—Публикация
2008-05-06—Подача