Настоящее изобретение относится к способу получения соли 5-[(R)-2-(5,6-диэтилиндан-2-иламино)-1-гидроксиэтил]-8-гидрокси-(1H)-хинолин-2-она без выделения его в виде свободного основания, которое является нестабильным в органических растворителях.
Соли 5-[(R)-2-(5,6-диэтилиндан-2-иламино)-1-гидроксиэтил]-8-гидрокси-(1H)-хинолинон-2-она являются селективными β-адренорецепторными агонистами с возможной бронхолитической активностью. Например, малеат 5-[(R)-2-(5,6-диэтилиндан-2-иламино)-1-гидроксиэтил]-8-гидрокси-(1H)-хинолинон-2-она особенно полезен для лечения астмы и COPD. Кроме того, было показано, что малеатная соль обладает очень длительным действием in vitro и in vivo.
В способе получения малеата 5-[(R)-2-(5,6-диэтилиндан-2-иламино)-1-гидроксиэтил]-8-гидрокси-(1H)-хинолинон-2-она эпоксид, такой как 8-замещенный окси-5-(R)-оксиранил-(1H)-хинолин-2-он [формула (I)], подвергают реакции с амином, таким как 2-амино-(5,6-диэтил)индан, с получением желаемого промежуточного соединения 5-[(R)-2-(5,6-диэтилиндан-2-иламино)-1-гидроксиэтил]-8-замещенного окси-(1H)-хинолин-2-она [формула (II)]. Однако реакция не является региоселективной и приводит к получению различных количеств региоизомера [формула (III)] и димера [формула (IV)].

Обычно указанная реакционная смесь содержит только от около 60 до 80% желаемого промежуточного соединения формулы (II). Кроме того, очень сложно провести очистку промежуточного соединения формулы (II) кристаллизацией без больших потерь выхода. Например, для такой очистки использовали хроматографию на силикагеле, однако, процедура хроматографии на силикагеле является длительной и требует больших объемов растворителей.
Существует потребность в разработке более эффективного способа получения солей 5-[(R)-2-(5,6-диэтилиндан-2-иламино)-1-гидроксиэтил]-8-гидрокси-(1H)-хинолинон-2-она, особенно для крупномасштабного производства, который привел бы к получению солей высокой энантиомерной чистоты и с высоким выходом.
Настоящее изобретение относится к способу получения соли 5-[(R)-2-(5,6-диэтилиндан-2-иламино)-1-гидроксиэтил]-8-гидрокси-(1H)-хинолин-2-она или его приемлемого сольвата, включающий:
(i) реакцию 8-замещенного окси-5-(R)-оксиранил-(1H)-хинолин-2-она формулы (I)

с 2-амино(5,6-диэтил)инданом с получением реакционной смеси, содержащей соединения формул (II), (III) и (IV)
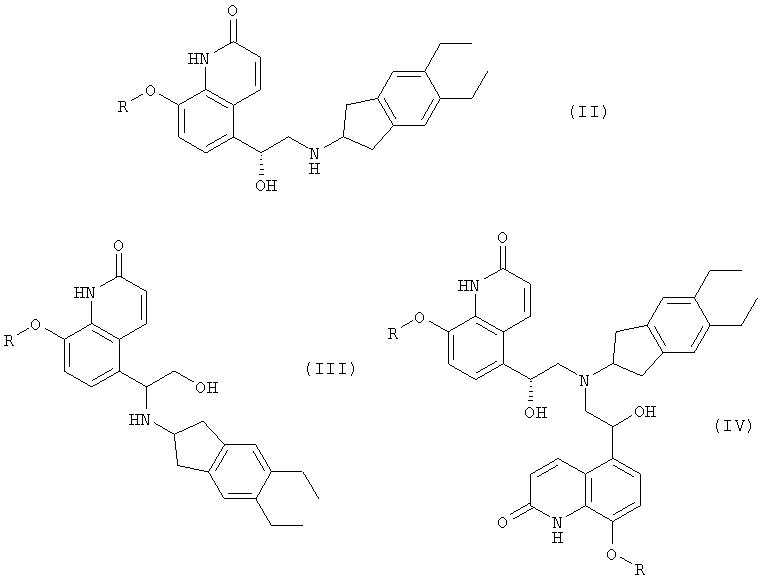
где R представляет собой защитную группу;
(ii) обработку реакционной смеси, полученной на стадии (i), кислотой в присутствии растворителя с получением соответствующей соли;
(iii) выделение и кристаллизацию соли формулы (V)
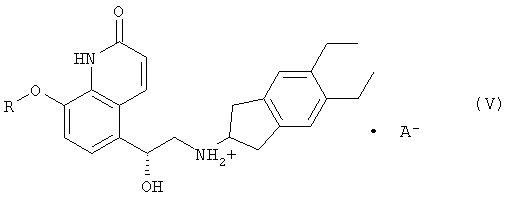
где R представляет собой защитную группу и А- представляет собой анион;
(iv) снятие защитной группы с соли формулы (V) в присутствии растворителя с получением соли формулы (VI)

где А- представляет собой анион, и
(v) обработку соли формулы (VI) кислотой в присутствии растворителя с получением соли 5-[(R)-2-(5,6-диэтилиндан-2-иламино)-1-гидроксиэтил]-8-гидрокси-(1H)-хинолин-2-она формулы (VII)

где Х- представляет собой анион.
Термины, используемые в описании, имеют следующие значения.
"Алкил" обозначает линейный или разветвленный алкил, который может представлять собой, например, С1-С10алкил, такой как метил, этил, н-пропил, изопропил, н-бутил, изобутил, вторбутил, трет-бутил, линейный или разветвленный пентил, линейный или разветвленный гексил, линейный или разветвленный гептил, линейный или разветвленный нонил или линейный или разветвленный децил. Предпочтительно алкил представляет собой С1-С4алкил.
"Арил" обозначает С6-С14арил, предпочтительно С6-С10арил, и может быть, например, замещен по крайней мере одной группой, выбранной из меркапто, диалкиламино, нитро, алкокси, галогена, кето, циано или их комбинаций. Предпочтительно арил представляет собой фенил.
"Алкокси" обозначает линейный или разветвленный алкокси и может представлять собой, например, С1-С10алкокси, такой как метокси, этокси, н-пропокси, изопропокси, н-бутокси, изобутокси, втор-бутокси, трет-бутокси или линейный или разветвленный пентокси, гексилокси, гептилокси, октилокси, нонилокси или децилокси. Предпочтительно алкокси представляет собой C1-С4алкокси.
"Алкенил" обозначает линейный или разветвленный алкенил, который может представлять собой, например, С2-С10алкенил, такой как винил, 1-пропенил, 2-пропенил, 1-бутенил, изобутенил, или линейный или разветвленный пентенил, гексенил, гептенил, октенил, ноненил или деценил. Предпочтительный алкенил представляет собой С2-С4алкенил.
"Циклоалкил" обозначает С3-С10циклоалкил, имеющий от 3 до 8 атомов углерода в кольце и может представлять собой, например, циклопропил, циклобутил, циклопентил, циклогексил, циклогептил или циклогептил, каждый из которых может быть замещен одной, двумя или более С1-С4алкильными группами, в частности метильными группами. Предпочтительно циклоалкил представляет собой С3-С6циклоалкил.
"Бензоциклоалкил" обозначает циклоалкил, например, одну из указанных выше С3-С10циклоалкильных групп, присоединенный по двум соседним атомам углерода к бензольному кольцу. Предпочтительно бензоциклоалкил представляет собой бензо-С5-С6циклоалкил, особенно бензоциклогексил (тетрагидронафтил).
"Циклоалкилалкил" обозначает С3-С10циклоалкилС1-С10алкил, где С3-С10циклоалкильная группа имеет от 3 до 8 атомов углерода в кольце и может представлять собой, например, одну из указанных выше С1-С10алкильных групп, в частности одну из С1-С4алкильных групп, замещенную одной из указанных выше С3-С10циклоалкильных групп. Предпочтительно циклоалкилалкил представляет собой С3-С6циклоалкилС1-С4алкил.
"Аралкил" обозначает линейный или разветвленный С6-С10арилС1-С10алкил и может представлять собой, например, одну из указанных выше С1-С10алкильных групп, в частности одну из С1-С4алкильных групп, замещенную фенилом, толилом, ксилилом или нафтилом. Предпочтительно аралкил представляет собой фенилС1-С4алкил, в частности бензил или 2-фенилэтил.
"Гетероциклический" обозначает моновалентную гетероциклическуюгруппу, имеющую вплоть до 20 атомов углерода и один, два, три или четыре гетероатома, выбранных из азота, кислорода и серы, где группа необязательно имеет алкильную, алкилкарбонильную, гидроксиалкильную, алкоксиалкильную или аралкильную группу, присоединенную к атому углерода или атому азота в кольце, и связана с остатком молекулы через атом углерода в кольце, и может представлять собой, например, группу, предпочтительно моноциклическую группу, с одним атомом азота, кислорода или серы, такую как пиррил, пиридил, пиперидил, фурил, тетрагидрофурил или тиенил, или группу, предпочтительно моноциклическую группу, с двумя гетероатомами, выбранными из азота, кислорода и серы, такую как имидазолил, пиримидинил, пиперазинил, оксазолил, изоксазолил, тиазолил, морфолинил или тиоморфолинил. Предпочтительно гетероцикл представляет собой моноциклическую группу, имеющую 5 или 6 атомов в кольце и один или два атома азота, или один атом азота и один атом кислорода в кольце и необязательно замещенный по атому азота в кольце С1-С4алкилом, гидроксиС1-С4алкилом, С1-С4алкилкарбонилом или фенилС1-С4алкилом.
"Гетероаралкил" обозначает линейный или разветвленный аралкил, например одну из указанных выше С6-С10арилС1-С10алкильных групп, замещенную одной или несколькими гетероциклическими группами.
"Галогеналкил" обозначает линейный или разветвленный алкил, например С1-С10алкил, такой как одна из указанных выше С1-С10алкильных групп, замещенный одним или несколькими, например одним, двумя или тремя атомами галогена, предпочтительно атомами фтора или хлора. Предпочтительно галогеналкил представляет собой С1-С4алкил, замещенный одним, двумя или тремя атомами фтора или хлора.
"Замещенная силильная группа" предпочтительно представляет собой силильную группу, замещенную по крайней мере одной указанной выше алкильной группой.
Во втором варианте осуществления изобретение относится к способу получения соли 5-[(R)-2-(5,6-диэтилиндан-2-иламино)-1-гидроксиэтил]-8-гидрокси-(1H)-хинолин-2-она или его приемлемого сольвата, включающий:
(а) реакцию 8-(замещенного окси)-5-галогенацетил-(1H)-хинолин-2-она с восстанавливающим агентом в присутствии хирального катализатора с получением 8-(замещенного окси)-5-((R)-2-галоген-1-гидроксиэтил)-(1H)-хинолин-2-она;
(б) обработку 8-(замещенного окси)-5-((R)-2-галоген-1-гидроксиэтил)-(1H)-хинолин-2-она с основанием в присутствии растворителя с получением 8-(замещенного окси)-5-(R)-оксиранил-(1H)-хинолин-2-она;
(в) реакцию 8-замещенного окси-5-(R)-оксиранил-(1H)-хинолин-2-она формулы (I)

с 2-амино(5,6-диэтил)инданом с получением реакционной смеси, содержащей соединения формул (II), (III) и (IV)
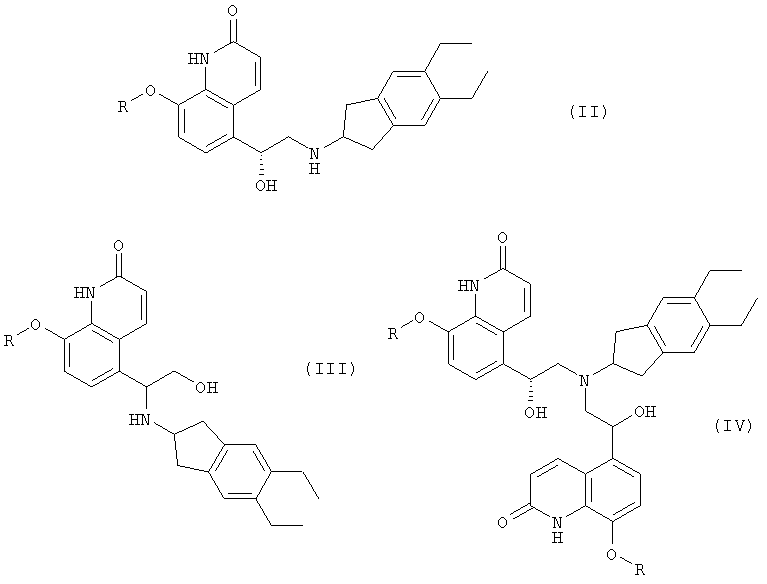
где R представляет собой защитную группу;
(г) обработку реакционной смеси, полученной на стадии (в), кислотой в присутствии растворителя с получением соответствующей соли;
(д) выделение и кристаллизацию соли формулы (V)
где R представляет собой защитную группу и А- представляет собой анион;
(е) снятие защитной группы с соли формулы (V) в присутствии растворителя с получением соли формулы (VI)

где А- представляет собой анион, и
(ж) обработку соли формулы (VI) кислотой в присутствии растворителя с получением соли 5-[(R)-2-(5,6-диэтилиндан-2-иламино)-1-гидроксиэтил]-8-гидрокси-(1H)-хинолин-2-она формулы (VII)

где X- представляет собой анион.
Настоящее изобретение относится к способу получения соли 5-[(R)-2-(5,6-диэтилиндан-2-иламино)-1-гидроксиэтил]-8-гидрокси-(1H)-хинолин-2-она или его приемлемого сольвата.
На первой стадии, стадии (i), 8-замещенный окси-5-(R)-оксиранил-(1H)-хинолин-2-он формулы (I)

подвергают реакции с 2-амино(5,6-диэтил)инданом с получением реакционной смеси, содержащей соединения формул (II), (III) и (IV)

где R представляет собой защитную группу.
Предпочтительными защитными группами являются фенольные защитные группы, известные специалисту в данной области техники. Более предпочтительно защитную группу выбирают из группы, состоящей из алкила, арила, алкокси, алкенила, циклоалкила, бензоциклоалкила, циклоалкилалкила, аралкила, гетероцикла, гетероаралкила, галогеналкила и замещенной силильной группы. Наиболее предпочтительно защитная группа представляет собой бензил или трет-бутилдиметилсилил.
Предпочтительно стадию (i) проводят в присутствии растворителя. Предпочтительные растворители включают спирты, например С1-6алкиловые спирты, такие как метанол, этанол, пропанол, бутанол и пентанол; алифатические С6-12углеводороды, например изооктан, гептан; диметилформамид; ароматические углеводороды, такие как толуол и бензол; ацетонитрил; гетероциклы, такие как тетрагидрофуран; диалкиловые эфиры, например диизопропиловый эфир, 2-метоксиэтиловый эфир и диэтиленовый эфир; диметилсульфоксид; тетрагидротиофен 1,1-диоксид, также известный как тетраметиленсульфон или как тетраметиленсульфолан; диалкилкарбонат, например диметилкарбонат и диэтилкарбонат; водные растворители, такие как вода; ионные жидкости и хлорированные растворители, такие как метиленхлорид. Также может использоваться комбинация растворителей. Более предпочтительно растворитель представляет собой 2-метоксиэтиловый эфир или бутанол.
Температуру, используемую на стадии (i), предпочтительно поддерживают от около 10°С до около 160°С. Более предпочтительно температуру поддерживают от около 30°С до около 120°С и наиболее предпочтительно от около 90°С до около 120°С.
Предпочтительно стадию (i) проводят с молярным избытком 2-амино(5,6-диэтил)индана относительно 8-замещенного окси-5-(R)-оксиранил-(1H)-хинолин-2-она. Предпочтительно от 1,05 мольного эквивалента до 3 мольных эквивалентов 2-амино(5,6-диэтил)индана используют относительно 8-замещенного окси-5-(R)-оксиранил-(1H)-хинолин-2-она. Наиболее предпочтительно от 1,1 мольного эквивалента до 1,5 мольного эквивалента 2-амино(5,6-диэтил)индана используют относительно 8-замещенного окси-5-(R)-оксиранил-(1H)-хинолин-2-она.
8-Замещенный окси-5-(R)-оксиранил-(1H)-хинолин-2-он предпочтительно представляет собой 8-фенилметокси-5-(R)-оксиранил-(1H)-хинолин-2-он. 5-[(R)-2-(5,6-Диэтилиндан-2-иламино)-1-гидроксиэтил]-8-замещенный окси-(1H)-хинолин-2-он предпочтительно представляет собой 5-[(R)-2-(5,6-диэтилиндан-2-иламино)-1-гидроксиэтил]-8-фенилметокси-(1H)-хинолин-2-он.
8-Замещенный окси-5-(R)-оксиранил-(1H)-хинолин-2-он может быть получен реакцией 8-(замещенного окси)-5-галогенацетил-(1H)-хинолин-2-она с восстанавливающим агентом в присутствии хирального катализатора с получением 8-(замещенного окси)-5-((R)-2-галоген-1-гидроксиэтил)-(1H)-хинолин-2-она; и обработкой 8-(замещенного окси)-5-((R)-2-галоген-1-гидроксиэтил)-(1H)-хинолин-2-она основанием в присутствии растворителя с получением 8-(замещенного окси)-5-(R)-оксиранил-(1H)-хинолин-2-она. Подробнее способ описан ниже.
На второй стадии, стадии (ii), реакционную смесь, полученную на стадии (i), обрабатывают кислотой в присутствии растворителя с получением соответствующей соли.
Предпочтительные растворители для применения на стадии (ii) включают спирты, например C1-6алкиловые спирты, такие как метанол, этанол, пропанол, бутанол и пентанол; алифатические С6-12углеводороды, например изооктан, гептан; диметилформамид; ароматические углеводороды, такие как толуол и бензол; ацетонитрил; гетероциклы, такие как тетрагидрофуран; диалкиловые эфиры, например диизопропиловый эфир, 2-метоксиэтиловый эфир и диэтиленовый эфир; диметилсульфоксид; тетрагидротиофен 1,1-диоксид, также известный как тетраметиленсульфон или как тетраметиленсульфолан; диалкилкарбонат, например, диметилкарбонат и диэтилкарбонат; водные растворители, такие как вода; ионные жидкости и хлорированные растворители, такие как метиленхлорид. Также может использоваться комбинация растворителей. Более предпочтительно растворитель представляет собой этанол.
Температуру, используемую на стадии (ii), предпочтительно поддерживают от около -10°С до около 160°С. Более предпочтительно температуру поддерживают от около 0°С до около 120°С и наиболее предпочтительно от около 0°С до около 75°С.
На третьей стадии, стадии (iii), соль формулы (V)

выделяют и кристаллизуют, где R представляет собой защитную группу и А- представляет собой анион. Анион соответствует кислоте, используемой на стадии (ii). Кислота, используемая на стадии (ii), предпочтительно представляет собой карбоновую кислоту, такую как бензойная кислота, малеиновая кислота, янтарная кислота, фумаровая кислота или винная кислота, ли минеральную кислоту, такую как хлороводородную кислоту. Наиболее предпочтительно кислота, используемая на стадии (ii), представляет собой бензойную кислоту.
Соль формулы (V) предпочтительно представляет собой бензоатную соль формулы (VIII)

где R представляет собой защитную группу.
Более предпочтительно бензоатная соль формулы (VIII) представляет собой бензоатную соль формулы (IX)
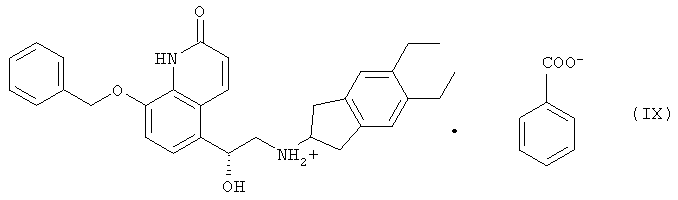
На четвертой стадии, стадии (iv), защитную группу соли формулы (V) удаляют в присутствии растворителя с получением соли формулы (VI)

где А- представляет собой анион.
Соль формулы (VI) предпочтительно представляет собой бензоатную соль формулы (X)

Снятие защитной группы известно специалисту в данной области техники и зависит от типа защитной группы. В одном варианте осуществления, где защитная группа представляет собой бензил, предпочтительным способом удаления бензильной группы в соли формулы (V) является обработка соли водородом в присутствии катализатора. Предпочтительные катализаторы включают палладий, гидроксид палладия, палладий на активированном угле, палладий на окиси алюминия, палладий на порошковом угле, платину, платину на активированном угле и никель Ренея™. Также возможна комбинация катализаторов. Наиболее предпочтительно катализатор представляет собой палладий на активированном угле.
В одном варианте осуществления, когда защитная группа представляет собой трет-бутилдиметилсилил, предпочтительным способом удаления трет-бутилдиметилсилильной группы в соли формулы (V) является обработка соли фторидом трет-бутиламмония или фторидом калия.
Растворитель, используемый на стадии (iv), предпочтительно выбирают из алкилацетата, например С1-6алкилацетатов, таких как этилацетат, изопропилацетат и бутилацетат; низших алкиламинов, например C1-6алкиламинов; спиртов, например, C1-6алкилспиртов, таких как метанол, этанол, пропанол, бутанол и пентанол; алифатических С6-12углеводородов, например изооктана, гептана, диметилформамида; ароматических углеводородов, таких как толуол и бензол; ацетонитрила; гетероциклов, таких как тетрагидрофуран; диалкиловых эфиров, например диизопропилового эфира, 2-метоксиэтилового эфира и диэтиленового эфира; кислоты, например уксусной кислоты, трифторуксусной кислоты и пропановой кислоты; водных растворителей, таких как вода; ионных жидкостей и хлорированных растворителей, таких как метиленхлорид. Также может использоваться комбинация растворителей. Более предпочтительно растворитель представляет собой уксусную кислоту или 2-пропанол.
Температуру, используемую на стадии (iv), предпочтительно поддерживают от около 0°С до около 70°С. Более предпочтительно температуру поддерживают от около 10°С до около 50°С и наиболее предпочтительно от около 10°С до около 30°С.
Соль формулы (VI) предпочтительно представляет собой бензоат 5-[(R)-2-(5,6-диэтилиндан-2-иламино)-1-гидроксиэтил]-8-фенилметоксигидрокси-(1H)-хинолин-2-она.
На пятой стадии, стадии (v), соль формулы (VI) обрабатывают кислотой в присутствии растворителя с получением соли формулы (VII)

где Х- представляет собой анион. Анион соответствует кислоте, используемой на стадии (v). Кислота, используемая на стадии (v), предпочтительно представляет собой карбоновую кислоту, такую как бензойная кислота, малеиновая кислота, янтарная кислота, фумаровая кислота или винная кислота. Наиболее предпочтительно кислота, используемая на стадии (v), представляет собой малеиновую кислоту.
Соль формулы (VII) предпочтительно выделяют фильтрацией. Соль формулы (VII) предпочтительно представляет собой малеат 5-[(R)-2-(5,6-диэтилиндан-2-иламино)-1-гидроксиэтил]-8-гидрокси-(1H)-хинолин-2-она формулы (XI)

Растворитель, используемый на стадии (v), предпочтительно выбирают из алкилацетата, например С1-6алкилацетатов, таких как этилацетат, изопропилацетат и бутилацетат; спиртов, например C1-6алкилспиртов, таких как метанол, этанол, пропанол, изопропанол, бутанол и пентанол; диметилформамида; ароматических углеводородов, таких как толуол и бензол; диалкилкетонов, например ацетона и метилизобутилкетона; ацетонитрила; гетероциклов, таких как тетрагидрофуран; диалкиловых эфиров, например диизопропилового эфира, 2-метоксиэтилового эфира и диэтиленового эфира; кислоты, такой как уксусная кислота и пропановая кислота; водных растворителей, таких как вода; ионных жидкостей и хлорированных растворителей, таких как метиленхлорид. Также могут использоваться комбинации растворителей. Более предпочтительно растворитель представляет собой этанол.
Температуру, используемую на стадии (v), предпочтительно поддерживают от около 0°С до около 70°С. Более предпочтительно, температуру поддерживают от около 10°С до около 60°С и наиболее предпочтительно от около 20°С до около 50°С.
Как указано выше, 8-замещенный окси-5-(R)-оксиранил-(1H)-хинолин-2-он может быть получен (а) реакцией 8-(замещенного окси)-5-галогенацетил-(1H)-хинолин-2-она с восстанавливающим агентом в присутствии хирального катализатора с получением 8-(замещенного окси)-5-((R)-2-галоген-1-гидроксиэтил)-(1H)-хинолин-2-она и затем (б) обработкой 8-(замещенного окси)-5-((R)-2-галоген-1-гидроксиэтил)-(1H)-хинолин-2-она основанием в присутствии растворителя с получением 8-(замещенного окси)-5-(R)-оксиранил-(1H)-хинолин-2-она.
Например, на стадии (а) 8-замещенный окси-5-галогенацетил-(1H)-хинолин-2-он подвергают реакции с восстанавливающим агентом в присутствии хирального катализатора с получением 8-замещенного окси-5-((R)-2-галоген-1-гидроксиэтил)-(1H)-хинолин-2-она формулы (XII)

где R представляет собой защитную группу и Х представляет собой галоген. Галоген выбирают из брома, хлора, фтора и йода. Предпочтительно галоген представляет собой хлор.
8-Замещенный окси-5-галогенацетил-(1H)-хинолин-2-он является коммерчески доступным или может быть получен галогенированием соответствующего метилкетона, например, с помощью процедуры, описанной в WO 95/25104. Метилкетон является коммерчески доступным или может быть получен с помощью процедуры, описанной в European Journal of Medicinal Chemistry, 1984, 19, 341-346.
Предпочтительно хиральный катализатор представляет собой оксазаборолидиновое соединение формулы (XIII)
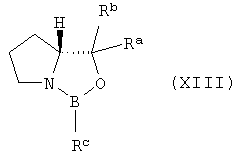
где Ra и Rb независимо выбраны из алифатического, циклоалифатического, циклоалифатического-алифатического, арильного или арилалифатического остатка. Предпочтительно Ra и Rb независимо выбраны из фенила, 4-метилфенила и 3,5-диметилфенила. Более предпочтительно Rа и Rb представляют собой фенил и
Rc выбран из алифатического, циклоалифатического, циклоалифатического-алифатического, арильного или арил-алифатического остатка, который, в каждом случае, может быть связан с полимером. Более предпочтительно Rc представляет собой метил.
Ra, Rb и Rc предпочтительно являются незамещенными, но могут быть замещены, например, одним или несколькими, например, двумя или тремя остатками, например, остатками, выбранными из C1-C7алкила, гидрокси, -O-СН2-О-, -СНО, C1-C7замещенного окси, С2-С8алканоилокси, галогена, например хлора или фтора, нитро, циано и CF3
Алифатические углеводородные остатки включают С1-C7алкил, С3-С7алкенил или, вторично, С2-С7алкинил. С2-С7Алкенил представляет собой, в частности, С3-С7алкенил и представляет собой, например, 2-пропенил или 1-, 2- или 3-бутенил. С3-С5Алкенил является предпочтительным. С2-С7Алкинил представляет собой, в частности, С3-С7алкинил и предпочтительно представляет собой пропинил.
Циклоалифатические остатки включают С3-C8циклоалкил или, вторично, С3-C8циклоалкенил. С3-C8циклоалкил предпочтительно представляет собой циклопентил или циклогексил. С3-C8Циклоалкенил представляет собой С3-С7циклоалкенил и предпочтительно представляет собой циклопент-2-енил и циклопент-3-енил или циклогекс-2-енил и циклогекс-3-енил.
Циклоалифатические-алифатические остатки включают С3-C8циклоалкил-C1-C7алкил, предпочтительно С3-С6циклоалкил-С1-C4алкил и особенно циклопропилметил.
Арильным остатком может быть, например, карбоциклический или гетероциклический ароматический остаток, в частности фенил или, в частности, подходящий 5- или 6-членный и моно- или мультициклический остаток, который имеет вплоть до четырех одинаковых или различных гетероатомов, таких как атомы азота, кислорода или серы, предпочтительно один, два, три или четыре атома азота, атома кислорода или атома серы. Подходящие 5-членные гетероарильные остатки включают моноаза-, диаза-, триаза-, тетрааза-, моноокса- или монотиациклические арильные радикалы, такие как пирролил, пиразолил, имидазолил, триазолил, тетразолил, фурил и тиенил, тогда как подходящими 6-членными остатками являются, в частности, пиридил. Подходящими мультициклическими остатками являются антраценил, фенантрил, бензо[1,3]диоксол или пиренил. Арильный остаток может быть монозамещен, например, NH2, ОН, SO3Н, СНО или дизамещен ОН или СНО и SO3Н.
Арил-алифатические остатки включают фенил-С1-С7алкил, фенил-С2-С7алкенил и фенил-С2-С7алкинил.
Подходящие полимеры включают полистирол (PS), поперечно сшитый PS (J), полиэтиленгликоль (PEG) или остаток силикагеля (Si). Примерами являются NH-Rd, где Rd представляет собой C(O)(CH2)n-PS или C(O)NH(CH2)n-PS, и -O-Si(Re)2(CH2)nRf, где n имеет значение 1-7, Re представляет собой C1-С6алкил, например этил, и Rf представляет собой полистирол, поперечно сшитый полистирол, полиэтиленгликоль или остаток силикагеля.
Восстанавливающий агент, который используется для восстановления 8-(замещенного окси)-5-галогенацетил-(1H)-хинолин-2-она, предпочтительно представляет собой борановый реагент, такой как боран-тетрагидрофурановый комплекс, боран-N,N-диэтиланилиновый комплекс или боран-метилсульфидный комплекс. Боран-тетрагидрофурановый комплекс является особенно предпочтительным. Оксазаборолидиновый хиральный катализатор предпочтительно представляет собой (R)-тетрагидро-1-метил-3,3-дифенил-(1Н,3H)-пирроло[1,2-с][1,3,2]оксазаборол, также известный как (R)-2-метил-CBS-оксазаборолидин (Me-CBS).
Предпочтительно растворитель используют на стадии (а). Предпочтительные растворители включают алкилацетат, например C1-6алкилацетаты, такие как этилацетат, изопропилацетат и бутилацетат; алкиламины, например C1-6алкиламины; низшие алкилспирты, например C1-6алкилспирты, такие как метанол, этанол, пропанол, изопропанол, бутанол и пентанол; алифатические С6-12углеводороды, например изооктан, гептан; диметилформамид; ароматические углеводороды, такие как толуол и бензол; ацетонитрил; гетероциклы, такие как тетрагидрофуран; диалкиловый эфир, например диизопропиловый эфир, 2-метоксиэтиловый эфир и диэтиленовый эфир; водные растворители, такие как вода; ионные жидкости и хлорированные растворители, такие как метиленхлорид. Также может использоваться комбинация растворителей. Предпочтительный растворитель для применения на стадии (а) представляет собой тетрагидрофуран.
Температуру, используемую на стадии (а), предпочтительно поддерживают от около -10°С до около 80°С. Более предпочтительно температуру поддерживают от около 0°С до около 50°С.
8-Замещенный окси-5-((R)-2-галоген-1-гидроксиэтил)-(1H)-хинолин-2-он предпочтительно представляет собой 8-фенилметокси-5-((R)-2-хлор-1-гидроксиэтил)-(1H)-хинолин-2-он.
Необязательно продукт 8-замещенного окси-5-((R)-2-галоген-1-гидроксиэтил)-(1H)-хинолин-2-она может быть очищен любым из способов, известным из уровня техники, таким как кристаллизация, и необязательно может проводиться в присутствии древесного угля.
На стадии (б) 8-замещенный окси-5-((R)-2-галоген-1-гидроксиэтил)-(1H)-хинолин-2-он обрабатывают основанием в присутствии растворителя с получением 8-замещенного окси-5-(R)-оксиранил-(1H)-хинолин-2-она. 8-Замещенный окси-5-(R)-оксиранил-(1H)-хинолин-2-он имеет формулу (I)

где R представляет собой защитную группу.
Предпочтительные основания включают этоксид натрия, гидроксид натрия, фосфат калия, карбонат калия, гидрокарбонат калия и карбонат цезия. Также может использоваться комбинация оснований. Наиболее предпочтительным основанием является карбонат калия.
Растворитель, используемый на стадии (б), предпочтительно выбирают из алкилацетата, например C1-6алкилацетатов, таких как этилацетат, изопропилацетат и бутилацетат; спиртов, например C1-6алкилспиртов, таких как метанол, этанол, пропанол, бутанол и пентанол; алифатических С6-12углеводородов, например изооктана, гептана; диметилформамида; ароматических углеводородов, таких как толуол и бензол; диалкилкетонов, например ацетона, метилизобутилкетона; ацетонитрила; гетероциклов, таких как тетрагидрофуран; диалкиловых эфиров, например диизопропилового эфира, 2-метоксиэтилового эфира и диэтиленового эфира; водных растворителей, таких как вода; ионных жидкостей и хлорированных растворителей, таких как метиленхлорид. Также могут использоваться комбинации растворителей. Предпочтительным растворителем для использования на стадии (б) является комбинация ацетона и воды.
Температуру, используемую на стадии (б), предпочтительно поддерживают от около 10°С до около 160°С. Более предпочтительно температуру поддерживают от около 30°С до около 80°С и наиболее предпочтительно от около 50°С до около 60°С.
8-Замещенный окси-5-(R)-оксиранил-(1H)-хинолин-2-он предпочтительно представляет собой 8-фенилметокси-5-(R)-оксиранил-(1H)-хинолин-2-он.
Необязательно продукт 8-замещенного окси-5-(R)-оксиранил-(1H)-хинолин-2-она может быть очищен любым из способов, известным из уровня техники, таким как кристаллизация.
Кристаллизация из толуола или ацетона является особенно предпочтительной, и необязательно может проводиться в присутствии древесного угля.
Настоящее изобретение иллюстрируется следующими примерами.
Пример 1
Получение бензоата 5-[(R)-2-(5,6-диэтилиндан-2-иламино)-1-гидроксиэтил]-8-фенилметокси-(1H)-хинолин-2-она
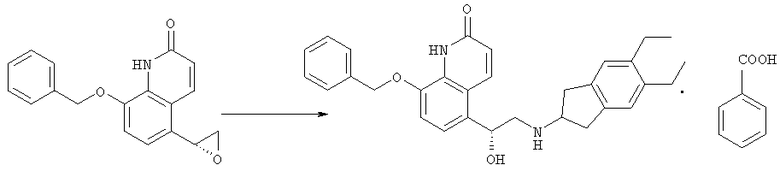
В 4-горлую колбу на 1 л, оборудованную механической мешалкой, термометром, дополнительной воронкой и обратным холодильником, загружали 30,89 г 2-амино-5,6-диэтилиндана и диметилового эфира диэтиленгликоля. К этому раствору добавляли 36,4 грамм 8-фенилметокси-5-(R)-оксиранил-1H-хинолин-2-она. Полученную суспензию нагревали до температуры 110°С и перемешивали при этой температуре в течение 15 часов. Полученный коричневый раствор охлаждали до 70°С. При 70°С добавляли 210 мл этанола и затем раствор 30,3 г бензойной кислоты в 140 мл этанола. Раствор охлаждали до 45-50°С и добавляли затравку. Суспензию охлаждали до 0-5°С.
Сырой бензоат 8-фенилметокси-5-[(R)-2-(5,6-диэтилиндан-2-иламино)-1-гидроксиэтил]-1H-хинолин-2-она выделяли фильтрацией и промывали 150 мл этанола тремя порциями. Влажный остаток на фильтре очищали перекристаллизацией из 1400 мл этанола, которая приводила к получению 50,08 г чистого бензоата 8-фенилметокси-5-[(R)-2-(5,6-диэтилиндан-2-иламино)-1-гидроксиэтил]-1H-хинолин-2-она в виде белого кристаллического порошка.
Пример 2
Получение малеата 5-[(R)-2-(5,6-диэтилиндан-2-иламино)-1-гидроксиэтил]-8-гидрокси-1H-хинолин-2-она
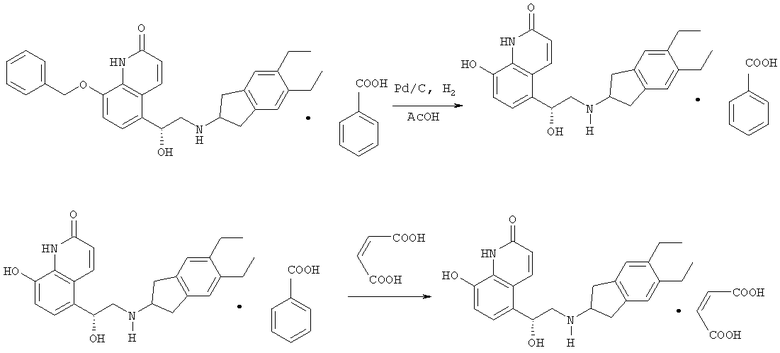
В сосуд на 1 л для гидрирования загружали 40 грамм бензоата 8-фенилметокси-5-[(R)-2-(5,6-диэтилиндан-2-иламино)-1-гидроксиэтил]-7H-хинолин-2-она и 400 мл уксусной кислоты. Добавляли палладий на угле 5% (5,44 г) и реакционную массу гидрировали в течение 2-8 часов до полного превращения в 5-[(R)-2-(5,6-диэтилиндан-2-иламино)-1-гидроксиэтил]-8-гидрокси-1Н-хинолин-2-он. Смесь отфильтровывали через вспомогательную фильтрующую присадку. Фильтрат концентрировали при 50-60°С в вакууме (100 мбар) до объема 70-90 мл. Этот остаток растворяли в 400 мл этанола и нагревали до 50-60°С. Добавляли раствор 11,6 г малеиновой кислоты в 24 мл этанола и в полученный прозрачный раствор добавляли затравку при внутренней температуре 50°С с суспензией 350 мг тонкоизмельченного 5-[(R)-2-(5,6-диэтилиндан-2-иламино)-1-гидроксиэтил]-8-гидрокси-1Н-хинолин-2-она в 20 мл изопропанола. Продукт кристаллизовали при медленном охлаждении до 0-5°С.
Фильтрация и промывание 50 мл этанола и затем 25 мл изопропанола приводили к получению 65 г сырого малеата 5-[(R)-2-(5,6-диэтилиндан-2-иламино)-1-гидроксиэтил]-8-гидрокси-1H-хинолин-2-она, который далее очищали кристаллизацией из 1,36 л этанола. После этого получали 24,3 г чистого малеата 5-[(R)-2-(5,6-диэтилиндан-2-иламино)-1-гидроксиэтил]-8-гидрокси-1H-хинолин-2-она в виде белого кристаллического порошка.
Пример 3
Чистота и выход различных солей 5-[(R)-2-(5,6-диэтилиндан-2-иламино)-1-гидроксиэтил]-8-замещенный окси-(1H)-хинолин-2-она
В 4-горлую колбу на 1 л, оборудованную механической мешалкой, термометром, дополнительной воронкой и обратным холодильником, загружали 30,89 г 2-амино-5,6-диэтилиндана и диметилового эфира диэтиленгликоля. К этому раствору добавляли 36,4 г 8-фенилметокси-5-(R)-оксиранил-1H-хинолин-2-она. Полученную суспензию нагревали до температуры 110°С и перемешивали при этой температуре в течение 15 часов. Полученный коричневый раствор охлаждали до 70°С.
Реакцию проводили следующим образом:
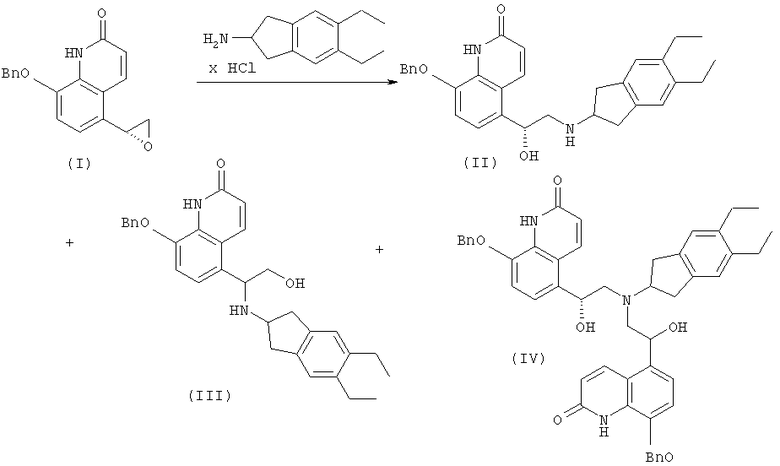
Как определено с помощью ВЭЖХ, реакционная смесь содержит 68,7% соединения формулы (II), 7,8% соединения формулы (III) и 12,4% соединения формулы (IV). Реакционную смесь делили на равные порции и каждую порцию отдельно обрабатывали кислотой, выбранной из бензойной кислоты, малеиновой кислоты, янтарной кислоты, фумаровой кислоты, винной кислоты и соляной кислоты. Результаты представлены в таблице
Как представлено в таблице, процентный выход основан на количестве 8-замещенного окси-5-(R)-оксиранил-(1H)-хинолин-2-она, и чистота основана на соли формулы (II) и определена с помощью ВЭЖХ.
Таким образом, неожиданно было обнаружено, что (а) выход соли 5-[(R)-2-(5,6-диэтилиндан-2-иламино)-1-гидроксиэтил]-8-гидрокси-(1H)-хинолин-2-она может быть существенно повышен при получении кислотной соли 5-[(R)-2-(5,6-диэтилиндан-2-иламино)-1-гидроксиэтил]-8-замещенный окси-(1H)-хинолин-2-она и (б) кислотная соль может быть превращена в соль 5-[(R)-2-(5,6-диэтилиндан-2-иламино)-1-гидроксиэтил]-8-гидрокси-(1H)-хинолин-2-она без выделения свободного основания 5-[(R)-2-(5,6-диэтилиндан-2-иламино)-1-гидроксиэтил]-8-гидрокси-(1H)-хинолин-2-она.
Пример 4
Получение 8-(фенилметокси)-5-((R)-2-хлор-1-гидроксиэтил)-(1H)-хинолин-2-она

В сухую на 3 л 4-горлую колбу, оборудованную механической мешалкой, термометром, дополнительной воронкой и обратным холодильником, загружали 50 г 8-(фенилметокси)-5-(α-хлорацетил)-(1H)-хинолин-2-она и 600 мл сухого ТГФ в атмосфере N2. Затем добавляли 15 мл 1 молярного раствора (R)-тетрагидро-1-метил-3,3-дифенил-(1H,3H)-пирроло[1,2-с][1,3,2]оксазаборола в толуоле. Смесь охлаждали до внутренней температуры 0-2°С и, поддерживая внутреннюю температуру 0-2°С, добавляли 153 мл 1 молярного раствора ВН3 в ТГФ в течение 1-2 часов. Реакционную смесь перемешивали еще в течение часа при внутренней температуре 0-2°С и затем гасили добавлением 65 мл метанола. Полученный раствор нагревали до 25°С и концентрировали до объема 250 мл (50°С/200 мбар). К этому концентрату добавляли смесь 713 мл воды и 37 г HCl (37%). В процессе добавления 8-(фенилметокси)-5-((R)-2-хлор-1-гидроксиэтил)-(1H)-хинолин-2-он осаждался в виде почти бесцветного осадка. Полученную суспензию перемешивали в течение 30 минут при 25°С, отфильтровывали и промывали 220 мл воды несколькими порциями. Сушка в вакуумной сушилке при 50°С в течение 12 часов приводила к получению 47,41 г 8-(фенилметокси)-5-((R)-2-хлор-1-гидроксиэтил)-(1H)-хинолин-2-она в виде светло-желтоватого порошка.
Пример 5
Получение 8-(фенилметокси)-5-(R)-оксиранил-(1H)-хинолин-2-она
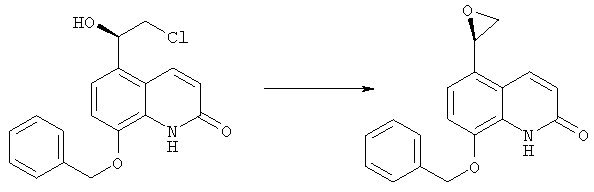
В 4-горлую колбу на 3 л, оборудованную механической мешалкой, термометром, дополнительной воронкой и обратным холодильником, загружали 50 г 8-(фенилметокси)-5-((R)-2-хлор-1-гидроксиэтил)-(1H)-хинолин-2-она, 52,42 г карбоната калия, 2500 мл ацетона и 25 мл воды. Смесь нагревали при перемешивании с обратным холодильником. Кипячение продолжали в течение 5-10 часов до полного превращения 8-фенилметокси-5-((R)-2-хлор-1-гидроксиэтил)-(1H)-хинолин-2-она в 8-фенилметокси-5-(R)-оксиранил-(1H)-хинолин-2-он. После окончания реакции горячую (45-50°С) реакционную смесь отфильтровывали для удаления неорганических солей. Остаток промывали несколькими порциями ацетона и объединенные маточный раствор и растворы ацетона концентрировали до объема 450 мл. К полученной суспензии добавляли 235 мл гептана при 25°С и затем суспензию охлаждали до внутренней температуры 0-2°С и перемешивали при этой температуре в течение 2-3 часов. Фильтрация и промывка приводили к получению сырого 8-фенилметокси-5-(R)-оксиранил-(1H)-хинолин-2-она, который перекристаллизовывали из толуола. После этого получали 36,7 г 8-(фенилметокси)-5-(R)-оксиранил-(1H)-хинолин-2-она в виде почти бесцветного твердого вещества.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ 5-(АЛЬФА-ГАЛОГЕНАЦЕТИЛ)-8-(ЗАМЕЩЕННЫЙ ОКСИ)-(1Н)-ХИНОЛИН-2-ОНОВ | 2004 |
|
RU2339621C2 |
| ЭНАНТИОСЕЛЕКТИВНЫЙ СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ ХИНОЛИНА | 2005 |
|
RU2383534C2 |
| СОЕДИНЕНИЯ, СПОСОБ ПОЛУЧЕНИЯ СОЕДИНЕНИЯ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 2000 |
|
RU2244709C2 |
| ПРОИЗВОДНЫЕ ХИНОЛИНОНА И СОДЕРЖАЩИЕ ИХ ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ | 2007 |
|
RU2449991C2 |
| КОМБИНАЦИИ ГЛИКОПИРРОЛАТА И АГОНИСТОВ В-2 АДРЕНОЦЕПТОРА | 2005 |
|
RU2388465C2 |
| ПРОИЗВОДНЫЕ 5-АМИНОЦИКЛИЛМЕТИЛОКСАЗОЛИДИН-2-ОНА | 2008 |
|
RU2492169C2 |
| ОРГАНИЧЕСКИЕ СОЕДИНЕНИЯ | 2001 |
|
RU2292890C2 |
| КОНДЕНСИРОВАННЫЕ ТРИАЗОЛАМИНЫ В КАЧЕСТВЕ МОДУЛЯТОРОВ Р2Х7 | 2010 |
|
RU2533122C2 |
| ПРОИЗВОДНЫЕ 2-ГИДРОКСИЭТИЛ-1Н-ХИНОЛИН-2-ОНА И ИХ АЗАИЗОСТЕРИЧЕСКИЕ АНАЛОГИ С АНТИБАКТЕРИАЛЬНОЙ АКТИВНОСТЬЮ | 2010 |
|
RU2540862C2 |
| АНТИБИОТИЧЕСКИЕ ПРОИЗВОДНЫЕ 2-ОКСО-ОКСАЗОЛИДИН-3, 5-ДИИЛА | 2012 |
|
RU2616609C2 |
Настоящее изобретение относится к способу получения соли 5-[(R)-2-(5,6-диэтилиндан-2-иламино)-1-гидроксиэтил]-8-гидрокси-(1Н)-хинолин-2-она, который включает в себя (i) реакцию 8-замещенного окси-5-(R)-оксиранил-(1Н)-хинолин-2-она формулы (I) с 2-амино-(5,6-диэтил)инданом с получением реакционной смеси, содержащей соединения формул (II), (III) и (IV), где R представляет собой защитную группу; (ii) обработку реакционной смеси, полученной на стадии (i), кислотой, выбранной из группы, состоящей из бензойной кислоты, малеиновой кислоты, янтарной кислоты, фумаровой кислоты, винной кислоты и хлороводородной кислоты, в присутствии растворителя с получением соответствующей соли; (iii) выделение и кристаллизацию соли формулы (V), где R представляет собой защитную группу и А- представляет собой анион; (iv) снятие защитной группы с соли формулы (V) в присутствии растворителя с получением соли формулы (VI), где А- представляет собой анион, и (v) обработку соли формулы (VI) кислотой, выбранной из группы, состоящей из бензойной кислоты, малеиновой кислоты, янтарной кислоты, фумаровой кислоты и винной кислоты, в присутствии растворителя с получением соли 5-[(R)-2-(5,6-диэтилиндан-2-иламино)-1-гидроксиэтил]-8-гидрокси-(1Н)-хинолин-2-она формулы (VII), где X- представляет собой анион. Технический результат: заявленный способ является альтернативой используемому в настоящее время промышленному способу получения соединения формулы (VII). 2 н. и 15 з.п. ф-лы, 1 табл.
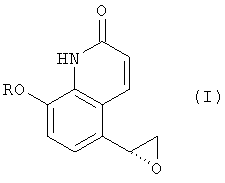


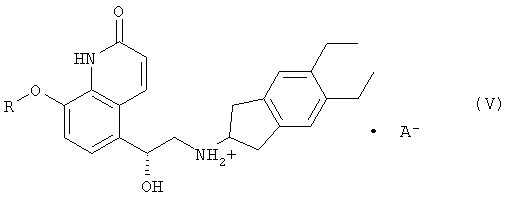


(i) реакцию 8-замещенного окси-5-(R)-оксиранил-(1Н)-хинолин-2-она формулы (I)

с 2-амино-(5,6-диэтил)-инданом с получением реакционной смеси, содержащей соединения формул (II), (III) и (IV)

где R представляет собой защитную группу;
(ii) обработку реакционной смеси, полученной на стадии (i), кислотой, выбранной из группы, состоящей из бензойной кислоты, малеиновой кислоты, янтарной кислоты, фумаровой кислоты, винной кислоты и хлороводородной кислоты, в присутствии растворителя с получением соответствующей соли;
(iii) выделение и кристаллизацию соли формулы (V)

где R представляет собой защитную группу и А- представляет собой анион;
(iv) снятие защитной группы с соли формулы (V) в присутствии растворителя с получением соли формулы (VI)

где А- представляет собой анион; и
(v) обработку соли формулы (VI) кислотой, выбранной из группы, состоящей из бензойной кислоты, малеиновой кислоты, янтарной кислоты, фумаровой кислоты и винной кислоты, в присутствии растворителя с получением соли 5-[(R)-2-(5,6-диэтилиндан-2-иламино)-1-гидроксиэтил]-8-гидрокси-(1Н)-хинолин-2-она формулы (VII)

где X- представляет собой анион.

(а) реакцию 8-(замещенного окси)-5-галогенацетил-(1Н)-хинолин-2-она с восстанавливающим агентом в присутствии хирального катализатора с получением 8-(замещенного окси)-5-((R)-2-галоген-1-гидроксиэтил)-(1Н)-хинолин-2-она; и
(б) обработку 8-(замещенного окси)-5-((R)-2-галоген-1-гидроксиэтил)-(1Н)-хинолин-2-она основанием в присутствии растворителя с получением 8-(замещенного окси)-5-(R)-оксиранил-(1Н)-хинолин-2-она.
(а) реакцию 8-(замещенного окси)-5-галогенацетил-(1Н)-хинолин-2-она с восстанавливающим агентом в присутствии хирального катализатора с получением 8-(замещенного окси)-5-((R)-2-галоген-1-гидроксиэтил)-(1Н)-хинолин-2-она;
(б) обработку 8-(замещенного окси)-5-((R)-2-галоген-1-гидроксиэтил)-(1Н)-хинолин-2-она основанием в присутствии растворителя с получением 8-(замещенного окси)-5-(R)-оксиранил-(1Н)-хинолин-2-она;
(в) реакцию 8-замещенного окси-5-(R)-оксиранил-(1Н)-хинолин-2-она формулы (I)

с 2-амино-(5,6-диэтил)-инданом с получением реакционной смеси, содержащей соединения формул (II), (III) и (IV)

где R представляет собой защитную группу;
(г) обработку реакционной смеси, полученной на стадии (в), кислотой, выбранной из группы, состоящей из бензойной кислоты, малеиновой кислоты, янтарной кислоты, фумаровой кислоты, винной кислоты и хлороводородной кислоты, в присутствии растворителя с получением соответствующей соли;
(д) выделение и кристаллизацию соли формулы (V)

где R представляет собой защитную группу и А- представляет собой анион;
(е) снятие защитной группы с соли формулы (V) в присутствии растворителя с получением соли формулы (VI)

где А- представляет собой анион; и
(ж) обработку соли формулы (VI) кислотой в присутствии растворителя с получением соли 5-[(R)-2-(5,6-диэтилиндан-2-иламино)-1-гидроксиэтил]-8-гидрокси-(1Н)-хинолин-2-она формулы (VII)

где X- представляет собой анион.
| ХИНОЛИНОВЫЕ КАРБОКСАМИДЫ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ | 1997 |
|
RU2170730C2 |
| US 4894219 A, 16.01.1990 | |||
| Способ определения степени иммунитета к кори у коревых доноров | 1947 |
|
SU75114A1 |
Авторы
Даты
2008-08-27—Публикация
2004-02-27—Подача