Область изобретения
Настоящее изобретение относится к новому способу приготовления твердой лекарственной формы десмопрессина или его фармацевтически приемлемой соли, а также к твердым лекарственным формам, предпочтительно таблеткам, получаемым указанным способом.
Предшествующий уровень техники
Десмопрессин, известный также как dDAVP, является нонапептидом и представляет собой терапевтически активный ингредиент (в виде ацетатной соли) в фармацевтическом продукте Minirin®, который имеется в продаже, inter alia, в виде назального спрея и таблеточного препарата. Десмопрессин главным образом применяют при лечении первичного ночного энуреза, то есть ночного недержания мочи, у детей, но он также разрешен для лечения никтурии и несахарного диабета. Первое появление на рынке таблеточного препарата состоялось в Швеции в 1987 году. Состав продаваемой таблеточной формы десмопрессина сохранился неизменным до настоящего времени.
Таблеточная форма десмопрессина впервые была описана, как изложено в патенте США 5047398. Полученные позже разрешения на торговлю относятся к таблетке, где среди прочего компоненты маннит, тальк и целлюлоза, приведенные в примерах в патенте США 5047398, заменены картофельным крахмалом. В дополнение к ацетату десмопрессина и картофельному крахмалу в настоящее время компонентами таблеток являются лактоза, поливинилпирролидон (PVP) и стеарат магния, которые совместно образуют гомогенную таблетку, приготавливаемую прессованием из гранулята. Эта композиция среди прочего описана на странице 28 в публикации WO 2003/094886 А1.
Поскольку десмопрессин является нонапептидом, содержащим дисульфидную связь, всегда следует учитывать его стабильность. Репрезентативными публикациями, направленными на проблему стабильности десмопрессина в фармацевтических препаратах, являются ЕР 1255557 А1, ЕР 752877 А1 и ЕР 740122 А1.
Содержащий десмопрессин гранулят до настоящего времени готовили способом влажной грануляции, включающим последовательность из нескольких стадий просеивания и перемешивания, осуществляемых при температуре и влажности окружающей среды, с последующей сушкой (сравни пример 1 в данном описании изобретения). Одной из задач этой процедуры является поддерживание усилий сдвига, которые могут оказывать влияние на десмопрессин в минимальной степени. Основной недостаток указанной процедуры заключается в том, что она требует довольно больших затрат времени и является трудоемкой.
В публикации WO 97/15297 А1 (примеры 6 и 10) описан способ влажной грануляции для приготовления трансбуккальной системы доставки десмопрессина.
Поскольку в качестве жидкости для грануляции для приготовления гранулята согласно предшествующему уровню техники используется смесь воды и этанола, получающаяся в результате этого таблетка неизбежно содержит остатки растворителей, в типичном случае 5-6% воды и 0,1% этанола (процент по массе). Полное удаление остатков растворителей посредством сушки является непрактичным, поскольку условия для полного высушивания твердых лекарственных форм имеют тенденцию быть либо чрезмерно дорогостоящими в промышленном масштабе, либо потенциально опасными в плане термического разрушения десмопрессина. Основной целью добавления этанола является сокращение продолжительности сушки (посредством образования азеотропной смеси).
В заявке США 2003/0091637 А1 раскрыто применение конкретного сополимера в качестве покрывающего агента для фармацевтического ядра. Фармацевтически активной основой может быть, например, пептидный гормон. Нанесение покрытия может быть осуществлено с использованием аппарата с псевдоожиженным слоем.
В упомянутой выше WO 2003/094886 А1 раскрыто приготовление таблеток, содержащих десмопрессин, с использованием традиционного способа влажной грануляции.
В WO 2004/096181 А2 (опубликованной 11 ноября 2004 года) приводятся примеры способа влажной грануляции для десмопрессина с использованием смеси вода/этанол 1:3 в качестве жидкости для грануляции. Данный способ характеризуется средним размером частиц эксципиента, выбранного для конкретной задачи.
Задачей настоящего изобретения является преодоление вышеупомянутых недостатков.
Краткое описание графических материалов
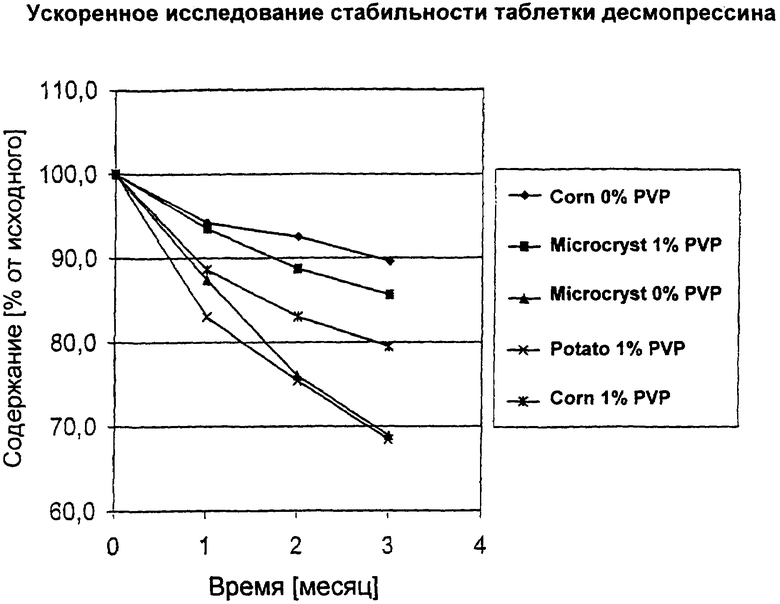
На чертеже показаны результаты ускоренного исследования стабильности различных таблеток, приготовленных прессованием из гранулята, изготовленного в соответствии с настоящим изобретением.
Описание сущности изобретения
Настоящее изобретение относится к способу приготовления твердой лекарственной формы десмопрессина или его фармацевтически приемлемой соли, включающему гранулирование десмопрессина и по меньшей мере одного эксципиента, выбранного из целлюлозы, крахмала и лактозы, либо их смеси в аппарате для грануляции в псевдоожиженном слое, причем получающийся десмопрессинсодержащий гранулят является пригодным для прессования в фармацевтически приемлемую таблетку. Более конкретно, такая обработка предусматривает условия, обеспечивающие перемешивание и действие усилия сдвига. Указанный процесс грануляции в типичном случае включает регулирование псевдоожижающего воздушного потока, температуры и продолжительности обработки.
Из стандартной литературы (смотри «Pharmaceutical Dosage Forms; Tablets», vol.1, pages 297-298, Eds. H.A. Lieberman, L. Lachman and J.B. Schwartz, Marcel Dekker, Inc., New York and Basel, 1989) известно, что условия, используемые при грануляции в псевдоожиженном слое, могут быть вредными, например для ферментов. Более конкретно, тепло и влага в совокупности с циркулирующим воздухом и частицами в процессе грануляции в псевдоожиженном слое создают значительные усилия сдвига и истирания с целью обеспечения гранулята, имеющего скользящие свойства, идеальные для прессования таблеток в промышленном масштабе и при промышленных скоростях. Такие скользящие свойства обусловлены получающейся в результате гладкой поверхностной структурой гранулята, подвергнутого воздействию указанных усилий сдвига и истирания.
Неожиданно оказалось, что такая чувствительная молекула, как десмопрессин, может выдерживать условия процесса грануляции в псевдоожиженном слое. Наиболее значительными преимуществами способа по настоящему изобретению являются небольшая по сравнению с традиционными процессами влажной грануляции продолжительность обработки и превосходные скользящие свойства для прессования получающегося в результате гранулята.
Грануляция в псевдоожиженном слое как таковая является традиционной технологией, и она широко описана в различной стандартной литературе, такой как «Pharmaceutical Dosage Forms; Tablets», vol.3, pages 27-29, Eds. H.A. Lieberman, L. Lachman and J.B. Schwartz, Marcel Dekker, Inc., New York and Basel, 1990 и «Pharmaceutics - The science of dosage form design» pages 625-627; Ed. M.E. Aulton, Churchill Livingstone, Edinburgh, London, Melbourne and New York 1988. Таким образом, подходящий выбор общих режимов работы оборудования и условий обработки обуславливается квалификацией специалиста в области производства фармацевтических препаратов. Примерами коммерческих поставщиков аппаратов, адаптированных для грануляции в псевдоожиженном слое, являются Aeromatic-Fielder AG, CH (Strea series) и Glatt GmbH, DE.
В предпочтительном воплощении настоящего способа указанный десмопрессинсодержащий гранулят готовят способом, включающим следующие стадии:
(1) приготовление порошка, содержащего по меньшей мере один эксципиент, выбранный из целлюлозы, крахмала и лактозы, либо их смесь, или состоящего по меньшей мере из одного из них;
(2) приготовление жидкости для грануляции, содержащей растворитель и десмопрессин или его фармацевтически приемлемую соль и, возможно, связующее вещество; и
(3) приведение в контакт указанной жидкости для грануляции, предпочтительно путем распыления, с указанным порошком внутри указанного аппарата, где псевдоожижающий воздушный поток и температуру и продолжительность обработки одновременно, и возможно также после завершения указанного приведения в контакт, регулируют так, чтобы обеспечить указанные перемешивание и действие усилия сдвига.
В типичном случае условия процесса грануляции в псевдоожиженном слое также предусматривают сушку во время проведения псевдоожижения, то есть также в продолжение указанной стадии (3). Таким образом, условия непрерывной обработки после указанного приведения в контакт предусматривают последующую сушку в дополнение к перемешиванию и действию усилия сдвига. В качестве примера операцию распыления при грануляции в псевдоожиженном слое в типичном случае проводят при постоянной скорости распыления в течение периода времени от 10 до 60 минут. Возможно, если желательны последующая сушка, перемешивание и/или действие усилия сдвига, то вслед за распылением условия непрерывной обработки могут продолжаться в течение от 10 до 240 мин.
Указанным растворителем предпочтительно является вода, что представляет собой особенно предпочтительный аспект настоящего изобретения. Заслуживает внимания тот факт, что применение воды в качестве единственного растворителя тем не менее сохраняет время сушки небольшим, тогда как риски взрывоопасности и воздействия органического растворителя сокращены, обеспечивая при этом получение гранулята требуемого качества. К тому же процесс грануляции упрощается в результате удаления компонента.
Псевдоожижающий воздушный поток относится к воздушному потоку, достаточному для достижения псевдоожижения порошка и полученного в результате гранулята в аппарате для грануляции в псевдоожиженном слое. Требуемый воздушный поток зависит от нескольких параметров, включая размер и плотность частиц. В качестве неограничивающего примера воздушный поток может находиться в диапазоне от 10 до 2500 м3/ч, предпочтительно от 20 до 1500 м3/ч. Различные масштабы производства в действительности будут требовать до некоторой степени различных псевдоожижающих воздушных потоков. Выбор оптимального потока для данного масштаба производства не является невыполнимой задачей для специалиста в данной области техники, так как машинное оборудование как таковое, необходимое для осуществления на практике настоящего изобретения, имеется в продаже и таким образом является общепринятым.
Указанная температура обработки в типичном случае находится в диапазоне от 25 до 80°С, предпочтительно от 30 до 60°С. Температурные диапазоны от 35 до 55°С и от 40 до 50°С также являются возможными.
Предпочтительно, чтобы продолжительность обработки находилась в диапазоне от 10 до 240 минут. На практике процесс в типичном случае считается завершенным, когда в образованном грануляте, который также сушат во время данного процесса, достигается содержание воды, по существу равное содержанию воды в указанном порошке, содержащем один эксципиент, выбранный из целлюлозы, крахмала и лактозы, либо их смесь.
Во многих случаях термины «эксципиент», «разбавитель» и «носитель» могут быть использованы взаимозаменяемо, и они могут относиться даже к одному и тому же веществу или к смеси подобных таких веществ. Надлежащее использование и понимание этих терминов хорошо известно специалистам в данной области техники.
В настоящем способе предпочтительно, чтобы указанный эксципиент, носитель или разбавитель был выбран из целлюлозы, крахмала и лактозы. Как он использован в данном описании изобретения, термин «целлюлоза» включает, взятую саму по себе либо в смеси, чистую целлюлозу, микрокристаллическую целлюлозу, карбоксиметилцеллюлозу, гидроксипропилметилцеллюлозу, а также другие ее варианты, которые могут быть использованы в фармацевтических препаратах.
Как он использован в данном описании изобретения, термин «крахмал» включает, взятый сам по себе либо в смеси, картофельный крахмал, пшеничный крахмал, кукурузный крахмал, рисовый крахмал и подвергнутые усилию сдвига и/или гидролизованные кислотой варианты вышеупомянутых типов крахмала, а также другие варианты крахмала, типичные для фармацевтических препаратов. Поскольку применение кукурузного крахмала неожиданно обеспечило получение наиболее стабильных таблеток (сравни пример 3), кукурузный крахмал является наиболее предпочтительным типом крахмала.
Используемым типом лактозы предпочтительно является лактоза-α-моногидрат.
Как указано выше, настоящая твердая лекарственная форма может возможно содержать по меньшей мере одну дополнительную добавку, в типичном случае выбранную из разрыхляющего агента, связующего вещества, смазывающего вещества, корригента, консерванта, красителя и любой подходящей их смеси. Примеры добавок, которые могут быть рассмотрены при практическом осуществлении настоящего изобретения, можно найти в «Handbook of Pharmaceutical Excipients»; Ed. A.H. Kibbe, 3rd Ed., American Pharmaceutical Association, USA and Pharmaceutical Press UK, 2000.
В предпочтительном воплощении настоящего способа указанный десмопрессинсодержащий гранулят прессуют в таблетку, предпочтительно в способе, при котором к указанному грануляту перед его прессованием добавляют смазывающее вещество.
Указанное смазывающее вещество в типичном случае выбрано из группы, состоящей из стеариновой кислоты, солей или сложных эфиров стеариновой кислоты, гидрогенизированных растительных масел, оксида магния, полиэтиленгликоля, лаурилсульфата натрия и талька и их смесей. Предпочтительно указанное смазывающее вещество выбрано из стеарата магния, стеарата кальция, стеарата цинка, глицерилпальмитостеарата и стеарилфумарата натрия и их смесей. Наиболее предпочтителен стеарат магния. Содержание смазывающего вещества в типичном случае составляет от 0,05 до 1,0, предпочтительно от 0,25 до 0,50 процента по массе для каждой единицы твердой лекарственной формы.
Практическое осуществление настоящего способа предпочтительно включает связующее вещество, например поливинилпирролидон (PVP). В типичном случае используют количество связующего вещества от 1 до 6 процентов по массе для каждой единицы твердой лекарственной формы.
В наиболее предпочтительном воплощении указанная твердая лекарственная форма не содержит энтеросолюбильного покрытия. Благодаря отсутствию энтеросолюбильного покрытия приготовление твердой лекарственной формы по настоящему изобретению дополнительно упрощается.
Окончательно приготовленная твердая лекарственная форма предпочтительно не содержит агент, оказывающий влияние на буферную емкость при рН от 2 до 6.
Способ по настоящему изобретению наиболее предпочтительно обеспечивает количество ацетата десмопрессина от 20 до 600 мкг на единицу твердой лекарственной формы.
Указанная твердая лекарственная форма предпочтительно выбрана из группы, состоящей из таблеток, гранулированного порошка, пастилки, облатки и оболочки капсулы. Наиболее предпочтительна таблетка.
Настоящая фармацевтическая композиция в твердой лекарственной форме в типичном случае представляет собой таблетку для перорального применения. Таблетка может быть изготовлена прессованием гранулята с использованием методик, хорошо разработанных в данной области техники. Примерами оборудования, подходящего для прессования таблеток, являются роторные прессы, поставляемые Elizabeth-Hata International, USA и Courtoy NV, BE. Для сравнительного обзора производства фармацевтических таблеток смотри «Tabletting» (N.A. Armstrong) в вышеупомянутом источнике информации «Pharmaceutics - The science of dosage form design», страницы 647-668.
Соответственно следующий аспект настоящего изобретения относится к твердой лекарственной форме, предпочтительно таблетке, которая может быть приготовлена способом, как он определен выше, изложенном как в общем, так и в конкретных воплощениях.
Далее следует более подробная иллюстрация настоящего изобретения. Ее не следует истолковывать как ограничение того, каким образом данное изобретение может быть применено на практике.
Экспериментальная часть
Пример 1 (предшествующий уровень техники): Приготовление таблетки, содержащей ацетат десмопрессина, посредством влажной грануляции
Лактозу (900 г, Pharmatose 150M; поставляется DMV, NL) и картофельный крахмал (550 г, AmylSolVät; поставляется Lyckeby Stärkelse AB, SE) смешивают в планетарном смесителе в течение 15 минут при комнатной температуре и просеивают через сито (1 мм). Готовят жидкость для грануляции, состоящую из воды (75 мл) и PVP (13,8 г, Kollidon® 25; поставляется BASF GmbH, DE), к которой добавляют ацетат десмопрессина (0,75 г; поставляется PolyPeptide Laboratories AB, SE) и этанол (225 г). Затем жидкость для грануляции постепенно добавляют к смеси лактоза/крахмал при перешивании в течение 20 минут с последующим перемешиванием в течение 10 минут при комнатной температуре. После просеивания (1,4 мм), сушки в течение приблизительно 20 часов при 40°С и дополнительного просеивания (1,4 мм) полученный гранулят смешивают со стеаратом магния (11,3 г; просеянный (1,0 мм); поставляется Peter Greven NV, NL) и затем прессуют с получением 7500 таблеток, используя таблеточную машину с одним пуансоном (Fette Exacta 1). В типичном случае изготовленная для продажи таблетка содержит 0,1 мг ацетата десмопрессина, имеет белый цвет и является выпуклой и овальной (6,8×9,6 мм) с толщиной 3-4 мм и целевой массой 192 мг. Она имеет гладкую поверхность без царапин или зазубренных краев и не демонстрирует тенденции к расслоению (так называемому кэппингу (capping)).
Пример 2: Приготовление таблетки, содержащей ацетат десмопрессина, посредством грануляции в псевдоожиженном слое
Лактозу (476,6 г; Granulac 140; поставляется Meggle AG, DE) и картофельный крахмал (294,6 г; М14; поставляется КМС, DK) подают в аппарат для грануляции в псевдоожиженном слое (Strea 1; поставляется Aeromatic Fielder AG, DE) и перемешивают в течение 2 минут в направленном вверх псевдоожижающем воздушном потоке (25 м3/ч) при установленной температуре 45°С. Жидкость для грануляции готовят, растворяя PVP (24 г, Povidone; поставляется BASF, DE) и ацетат десмопрессина (0,80 г; поставляется PolyPeptide Laboratories AB, SE) в воде (80 г). Затем жидкость для грануляции распыляют сверху вниз с постоянной скоростью в течение 15 минут на смесь лактоза/крахмал, в то же время подвергая последнюю воздействию направленного вверх псевдоожижающего воздушного потока (25 м3/ч) при температуре 45°С. После добавления всей жидкости для грануляции те же самые воздушный поток и температуру поддерживают в течение следующих 20 минут. Полученный сухой гранулят затем просеивают (1,0 мм) и перемешивают с порошкообразным стеаратом магния (4 г, просеян (1,0 мм); поставляется Peter Greven NV, NL) в течение 2 минут в традиционном смесителе (AR400E; поставляется EWREKA GmbH, DE) и затем прессуют с получением 4000 таблеток в ротационной машине для прессования с пуансоном (⊘ 8 мм) (Korsch XL 100; поставляется Korsch, DE) с целевой массой 200 мг. Этим способом получили таблетки с твердостью 5 кф (1 кф=9,81 Н), содержащие по 0,2 мг ацетата десмопрессина каждая. Таблетки имели гладкую поверхность без царапин или зазубренных краев, и не наблюдалось никакого кэппинга (capping).
Пример 3: Стабильность таблеток ацетата десмопрессина, приготовленных прессованием гранулята, полученного грануляцией в псевдоожиженном слое
Таблетки готовили согласно примеру 2, включая варианты с различным содержанием PVP (% масс./масс. от общей массы), и где картофельный крахмал (КМС М14) был заменен либо кукурузным крахмалом (White maize starch, С (star) PharmGel 03302; Cerestar Benelux В. V.), либо микрокристаллической целлюлозой (Avicel® PH 102; FMC BioPolymer). На чертеже изображены для сравнения следующие пять типов таблеток:
Таблетки хранили при 40°С и относительной влажности (RH) 75% в камерах искусственного климата. Содержание неповрежденного десмопрессина (исходное содержание 100% на момент времени 0 месяцев) регистрировали во времени, и результаты суммированы на чертеже. Для каждого типа таблеток исследовали по 20 таблеток, и показана средняя величина. Содержание десмопрессина регистрировали с использованием традиционной жидкостной хроматографии и УФ-спектроскопии (220 нм). В целом, применение кукурузного крахмала неожиданно обеспечило наиболее стабильные таблетки десмопрессина, полученные грануляцией в псевдоожиженном слое.
Все приведенные ссылки следует считать неотъемлемой частью настоящего описания.
| название | год | авторы | номер документа |
|---|---|---|---|
| ТВЕРДАЯ ЛЕКАРСТВЕННАЯ ФОРМА, СОДЕРЖАЩАЯ ДЕСМОПРЕССИН | 2004 |
|
RU2290945C2 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ ДЕСМОПРЕССИНА В ВИДЕ ТВЕРДОЙ ДОЗИРОВАННОЙ ЛЕКАРСТВЕННОЙ ФОРМЫ И СПОСОБ ЕЕ ИЗГОТОВЛЕНИЯ | 2004 |
|
RU2303439C2 |
| КОМПОЗИЦИЯ, СОДЕРЖАЩАЯ ДЕСМОПРЕССИН | 2007 |
|
RU2340351C1 |
| ЛЕКАРСТВЕННАЯ ФОРМА, СОДЕРЖАЩАЯ ДЕЗЛОРАТАДИН И СПОСОБ ЕЕ ИЗГОТОВЛЕНИЯ | 2013 |
|
RU2550958C2 |
| ДЕСМОПРЕССИН В ЛЕКАРСТВЕННОЙ ФОРМЕ, ДИСПЕРГИРУЕМОЙ ВО РТУ | 2003 |
|
RU2292903C2 |
| СТАБИЛЬНЫЙ ФАРМАЦЕВТИЧЕСКИЙ ПРЕПАРАТ, СОДЕРЖАЩИЙ АМЛОДИПИНА БЕЗИЛАТ И АТЕНОЛОЛ | 1998 |
|
RU2188636C2 |
| ГАЛЕНОВЫЙ СОСТАВ АЛИСКИРЕНА И ГИДРОХЛОРТИАЗИДА | 2007 |
|
RU2491058C2 |
| СПОСОБЫ МОКРОЙ ГРАНУЛЯЦИИ АЗИТРОМИЦИНА | 2002 |
|
RU2283651C2 |
| ДИСПЕРГИРУЕМЫЕ ТАБЛЕТКИ ДЕФЕРАСИРОКС | 2003 |
|
RU2338532C2 |
| ГАЛЕНОВЫ СОСТАВЫ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ | 2005 |
|
RU2384328C2 |
Изобретение относится к лекарственным средствам и касается способа приготовления твердой лекарственной формы десмопрессина или его фармацевтически приемлемой соли, включающего гранулирование указанного десмопрессина или его фармацевтически приемлемой соли и по меньшей мере одного эксципиента, выбранного из целлюлозы, крахмала и лактозы, либо их смеси в аппарате для грануляции в псевдоожиженном слое, причем получающийся гранулят, содержащий указанный десмопрессин, является пригодным для прессования в фармацевтически приемлемую таблетку. Предложенный способ позволяет получить стабильный препарат десмопрессина. 14 з.п. ф-лы, 1 ил.
а) приготовление порошка, содержащего по меньшей мере один эксципиент, выбранный из целлюлозы, крахмала и лактозы, либо их смесь;
б) приготовление жидкости для грануляции, содержащей растворитель и десмопрессин или его фармацевтически приемлемую соль и, возможно, связующее вещество; и
в) приведение в контакт указанной жидкости для грануляции с указанным порошком внутри указанного аппарата, где псевдоожижающий воздушный поток и температуру и продолжительность обработки одновременно регулируют так, чтобы обеспечить перемешивание и действие усилия сдвига.
| РАСТВОРЯЮЩИЕСЯ ВНУТРИ РОТОВОЙ ПОЛОСТИ ИЗДЕЛИЯ, СФОРМОВАННЫЕ ПРЕССОВАНИЕМ, И СПОСОБ ИХ ПРОИЗВОДСТВА | 1995 |
|
RU2147227C1 |
| US 6428812 В1, 06.08.2002 | |||
| WO 03094886 А2, 20.11.2003 | |||
| US 2002151474 А1, 17.10.2002. | |||
Авторы
Даты
2008-09-27—Публикация
2004-12-28—Подача