Изобретение относится к области медицины, в частности к фармацевтической промышленности, и описывает пероральную фармацевтическую композицию, выполненную в виде таблетки, включающую дезлоратадин и способ ее изготовления.
В течение последних лет во всем мире наблюдается значительный рост аллергических заболеваний. Аллергическими заболеваниями страдает каждый десятый житель Земли, а в некоторых регионах - каждый шестой. По официальной статистике в России аллергическим заболеваниями страдает от 10 до 15% населения. По данным ВОЗ, аллергические заболевания занимают 3 место по распространенности. За последнее десятилетие произошло удвоение заболеваемости аллергическим ринитом, бронхиальной астмой, атопическим дерматитом.
В этой связи, сегодня, представляется крайне актуальным создание эффективных, качественных и доступных противоаллергических лекарственных композиций и обеспечение высокой технологичности и производительности их производства.
Одним из наиболее эффективных действующих веществ для устранения аллергических симптомов различных этиологии является дезлоратадин. Химическое название дезлоратадина - 8-хлор-6,11-дигидро-11-(4-пиперидинилиден)-5Н-бензо[5,6]циклогепта[1,2-b]пиридин.
Дезлоратадин относится к группе блокаторов HI-гнетам иновых рецепторов длительного действия, является антигистаминным препаратом третьего поколения. Дезлоратадин подавляет высвобождение гистамина и лейкотриена С4 из тучных клеток, предупреждает развитие и облегчает течение аллергических реакций, обладает противоаллергическим, противозудным и противоэкссу дативным действием, уменьшает проницаемость капилляров, предупреждает развитие отека тканей, снимает спазм гладкой мускулатуры.
Одной из главных особенностей дезлоратадина является его высочайшая селективность и минимальный риск развития нежелательных реакций. Этот активный метаболит лоратадина характеризуется наибольшим сродством к H1-рецепторам - в 200 раз большим, чем фексофенадин, в 50 раз большим, чем лоратадин и цетиризин и в 3 раза большим, чем левоцетиризин. Поэтому дезлоратадин является более сильным обратным агонистом H1-рецепторов, что доказано как в клинических исследованиях, так и во врачебной практике (Anthes J., Richard С., West R. et al. Functional characteristics of desloratadine and other anhistamines in human Y1 receptors. Allergy, 2000, 55 (suppl. 63), S279 (Abstract 994); Henz В. The pharmacological profile of desloratadie: a review. Allergy, 2001, 56 (suppl. 65), 7-13.).
В частности, в рандомизированных двойных слепых плацебоконтролируемых исследованиях дезлоратадина при аллергическом рините с участием около 1 тыс.пациентов достоверно доказано, что дезлоратадин превосходит плацебо и уменьшает все основные симптомы ринита, в т.ч. заложенность носа. Установлено, что дезлоратадин - практически единственный блокатор H1-гистаминовых рецепторов, демонстрирующий в контролируемых исследованиях постоянный деконгестивный эффект. Дезлоратадин может применяться для лечения как сезонной, так и несезонной аллергии при реакциях на домашнюю пыль, пух, пыльцу растений, шерсть и перхоть животных, различные пищевые аллергены. Кроме того, в слепых плацебоконтролируемых многоцентровых исследованиях подтверждена эффективность дезлоратадина при хронической идиопатической крапивнице (Lorber R., Salmun L., Danzig M. Desloratadine is effective at relieving nasal congestion, as demonstrated in three placebo-controlled trials in patients with seasonal allergic rhinitis. New Trends in Allergy - V meeting, Davos, 2000; Nathan R. and the Desloradine Study Group. Desloratadine relieved nasal congestion in patients with seasonal allergic rhinitis. Annual meeting of American College of Allergy, Asthma and Immunology, Seattle, 2000.).
Дезлоратадин оказывает не только антигистаминный эффект, а также противовоспалительный и антиаллергический. Он блокирует также ряд других медиаторов, участвующих в развитии системного аллергического воспаления. Также препарат уменьшает проницаемость капилляров, предупреждает развитие отека тканей.
Кроме того, дезлоратадин не оказывает седативного эффекта, при приеме в терапевтических дозах не влияет на скорость психомоторных реакций и не усиливает угнетающее действие этанола на психомоторную функцию. Дезлорадатин определяется в плазме крови уже спустя 30 минут после приема, период полу выведения достигает 21-24 часа. Прием пищи не оказывает значимого влияния на всасывание препарата. Поэтому препарат можно принимать 1 раз/сутки независимо от приема пищи.
Таким образом, дезлоратадин значительно повышает качество жизни пациентов с аллергическими заболеваниями, причем, как показали популяционные исследования, даже в тех случаях, когда предшествующая терапия другими антигистаминными препаратами оказалась неэффективной.
Впервые формула дезлоратадина и его соли, способ его получения и фармацевтическая композиция с дезлоратадином в качестве активного вещества, были описаны в патенте US 4659716 с приоритетом от 15.02.1984 г. При этом был заявлен способ и состав получения лекарственной формы. Активное вещество смешивают с носителем, обладающим необходимыми связующими свойствами, в подходящих пропорциях и спрессовывают в нужную форму и размер. Порошки и таблетки в этом случае предпочтительно содержат от 5 до 20 процентов активного ингредиента. В качестве наполнителей предпочтительно используются: карбонат магния, стеарат магния, тальк, сахар, лактоза, пектин, декстрин, крахмал, желатин, метилцеллюлоза, натрий-карбоксиметилцеллюлоза, легкоплавкий воск, масло какао и т.д.
Из предшествующего уровня техники так же широко известны и применимы антигистаминные составы, включающие от 5 до 50 мг дезлоратадина или его фармацевтически приемлемой соли.
В частности известны составы препаратов Лордестин (Регистрационное удостоверение № ЛСР-006570/10, дата регистрации 09.07.2010 г.), Дезлоратадин Канон (Регистрационное удостоверение № ЛП-001853, дата регистрации 27.09.2012 г.), Дезлоратадин-Тева (Регистрационное удостоверение № ЛП-001627, дата регистрации 06.04.2012 г.) и другие. Данные препараты представлены на рынке в виде таблеток покрытых пленочной оболочкой, таблеток для рассасывания и сиропов.
Наиболее известным препаратом содержащим Дезлоратадин и широко представленным на рынке, является Эриус® (Регистрационное удостоверение № П N014704/02, дата регистрации 06.08.2010 г.), изготовленный в виде таблеток покрытых пленочной оболочкой, таблеток для рассасывания и сиропов. Указанные таблетки покрытые пленочной оболочкой, содержат следующие компоненты, мг:
Описывая кратко твердую лекарственную форму, такую как таблетированный препарат, обычно изготавливают путем прессования подходящего гранулята в нужную твердую лекарственную форму, причем гранулят состоит из нужных компонентов в виде смеси твердых частиц. Обычно такие частицы представляют собой терапевтически активный ингредиент, различные эксципиенты (наполнители), разрыхляющие агенты, смазывающие и связующие вещества, возможно вместе, например, с корригентом, консервантом и/или красителем. Имеющиеся в продаже таблетки Эриус® изготавливают в соответствии с таким общим протоколом, и такая таблетка была впервые раскрыта, как изложено в патенте US 4659716, сущность которого включена в данное описание изобретения посредством ссылки.
Таблетка Эриус®, представленная в настоящее время на рынке и, таким образом, производимая в промышленном масштабе, состоит из терапевтически активного ингредиента дезлоратадина вместе с кальция гидрофосфатом, целлюлозой микрокристаллической в качестве эксципиентов и, соответственно, подходящим количеством связующего и смазывающего вещества.
При любом прессовании гранулята, состоящего из смеси твердых частиц, в таблетки, существует общая необходимость в осуществлении операции прессования с наиболее высокой возможной скоростью при минимизации, в то же самое время износа механизма и с получением таблеток такого качества, которое соответствует регулирующим требованиям.
В настоящее время существует потребность в разработке более доступных и простых в производстве препаратов дезлоратадина, отличающихся высокой химико-физической стабильностью при хранении, соответствующих современным требованиям по качеству, изготовленных предпочтительно в виде твердой дозированной лекарственной формы, качественный и количественный состав которых обеспечит высокую производительность, технологичность с одновременной низкой себестоимостью производства, а также расширит арсенал противоаллергических препаратов отечественного производства.
Обнаружено, что сочетание в определенных соотношениях дисахарида - лактозы с полисахаридом - целлюлозой микрокристаллической, взятых с определенным размером частиц этих эксципиентов, неожиданно обеспечивает существенное повышение скорости в процессе изготовления, в то время как износ механизма и качество таблеток остаются по существу неизменными по сравнению с процессом промышленного производства, используемым до настоящего времени. По существу, соотношение компонентов и размер их частиц, о котором идет речь, по-видимому, влияет на сыпучесть частиц гранулята и их взаимное расположение в таблетке в процессе и после прессования так, что обеспечивает увеличенную общую производительность и, следовательно, скорость процесса изготовления таблетированного препарата дезлоратадина, а так же позволяет получать таблетки с достаточной механической прочностью при использовании меньшего усилия прессования, что позволяет экономить энергоресурсы.
В современных промышленных прессах производиться двустороннее сжатие порошка в матрице между двумя пуансонами. Исследователи считают, что механическая связь в таблетке обусловлена площадью контактирующих поверхностей, а также взаимным переплетением и зацеплением поверхностных выступов и неровностей частиц под давлением. В результате приложенного давления частицы сдвигаются и скользят по отношению друг к другу и вступают в более тесный контакт; симметричные скользят легче, чем шероховатые, но последние создают большее количество зацеплений и поэтому придают прессованной таблетке повышенную прочность. Благодаря экспериментальному подбору компонентов, частицы которых обладают перечисленными свойствами в оптимальных для процесса высокопроизводительного прессования соотношениях, авторам изобретения удалось решить поставленную задачу.
Более конкретно настоящее изобретение относится к фармацевтической композиции в виде твердой лекарственной формы, содержащей дезлоратадин или его фармацевтически приемлемую соль в качестве терапевтически активного ингредиента вместе с фармацевтически приемлемым эксципиентом, разбавителем или носителем, или их смесью, где по меньшей мере один из указанных эксципиентов, разбавителя и носителя в наиболее предпочтительном воплощении представляет собой дисахарид, более предпочтительно лактозу, а другой в наиболее предпочтительном варианте представляет собой полисахарид, более предпочтительно целлюлозу микрокристаллическую, причем средний размер частиц указанных веществ находится в интервале от 30 до 200 мкм. Причем массовое соотношение лактозы и целлюлозы микрокристаллической составляет от 8:1 до 2:1, а количество терапевтически активного вещества от 3 до 15%.
Правильное использование и понимание терминов эксцепиент, разбавитель, носитель не требует объяснений и полностью находится в пределах квалификации специалиста в области изготовления фармацевтических препаратов.
Фармацевтическая композиция по настоящему изобретению, возможно, может содержать по меньшей мере одну добавку, выбранную из разрыхлителя, смазывающего, связующего вещества, корригента, консерванта, красителя и их смеси. Где это приемлемо, также можно включать другие добавки. Типичные примеры разрыхлителей, смазывающих веществ (например, стеарат магния), связующих веществ (например, повидон), корригентов, консервантов и красителей, и подходящих их смесей, а также любых других традиционных добавок, которые могут быть рассмотрены специалистом в данной области, осуществляющим на практике настоящее изобретение, можно найти в "Handbook of Pharmaceutical Excipients"; Ed. A.H.Kibbe, 3rd Ed., American Pharmaceutical Association, USA, and Pharmaceutical Press UK, 2000, сущность которых включена в данное описание изобретения. В качестве примера, также применимого в практической реализации настоящего изобретения, можно упомянуть, что обычные количества смазывающих и связующих веществ, а также других традиционных технологических добавок имеют порядок менее 10% от массы фармацевтической композиции.
В состав имеющихся на рынке таблеток, изготавливаемых используемыми до настоящего времени способами, в качестве разбавителей входят кальция гидрофосфат, крахмал, целлюлоза микрокристаллическая. Такой состав, после изготовления из него гранулята или смеси, не позволяет получить скорость прессования превышающую 120000 таблеток в час на роторном одноручьевом прессе с 45 прессующими комлектами. По сравнению с этим способ по настоящему изобретению позволяет получить скорость прессования до приблизительно 200000 таблеток/ч включительно с нужным качеством таблеток и сохранить низкий уровень износа таблетирующего механизма.
В предпочтительном воплощении указанной фармацевтической композиции средний размер частиц находится в интервале от 30 до 200 мкм. В другом предпочтительном воплощении данный средний размер частиц находится в интервале от 90 до 180 мкм. В дополнительном предпочтительном воплощении указанный средний размер частиц лактозы находится в интервале от 150 до 200 мкм, а целлюлозы микрокристаллической от 70 до 110 мкм. В наиболее предпочтительном воплощении настоящего изобретения указанный средний размер частиц составляет для лактозы 70-80 мкм и для целлюлозы микрокристаллической 40-60 мкм (при измерении с помощью сита с использованием воздушной струи).
При измерении размера частиц при помощи сита с использованием воздушной струи воздух продувают через сито вверх от вращающейся щели так, что вещество на сите становится псевдоожиженным. В то же самое время к днищу сита прилагают отрицательное давление, которое удаляет мелкие частицы в собирающее устройство. Анализы размера и определение среднего размера частиц осуществляют путем удаления частиц с конца мелких частиц в распределении по размеру, последовательно используя одиночные сита. Дополнительные подробности смотрите также в "Particle Size Measurement", 5th Ed., p 178, vol.1; T.Allen, Chapman & Hall, London, UK, 1997. Для специалиста в данной области подобное измерение размера, таким образом, традиционно.
В предпочтительном воплощении в фармацевтической композиции присутствуют как указанный дисахарид, так и полисахарид. В данном конкретном воплощении массовое соотношение указанного дисахарида и полисахарида обычно составляет от 8:1 до 2:1, предпочтительно от 7:1 до 4:1 и более предпочтительно от 6:1 до 5:1.
Общее количество указанных эксципиента, разбавителя и носителя в совокупности обычно составляет от 75 до 96%, предпочтительно от 80% до 90% от массы фармацевтической композиции, причем оставшейся частью до 100% включительно является терапевтически активный ингредиент возможно вместе с вышеуказанными добавками, где последние предпочтительно представляют собой смазывающее, разрыхлюящее и связующее вещество.
Приведенные отношения долей компонентов и размеры их частиц, определены экспериментальным путем и могут быть обоснованы следующим образом. Лактоза является кристаллическим порошком, а целлюлоза микрокристаллическая обладает одновременно свойствами волокон и кристаллического порошка. Частицы лактозы обеспечивают смеси текучесть и скольжение частиц при уплотнении, частицы целлюлозы микрокристаллической увеличивают площадь контактирующих поверхностей.
При увеличении соотношения лактоза: целлюлоза микрокристаллическая более чем 8:1, процесс прессования для достижения достаточной прочности должен протекать при высоком давлении и небольшой скорости, а при уменьшении менее 2:1, уменьшается текучесть смеси и насыпная плотность до такой степени, что могут возникнуть проблемы с точностью дозирования веса порошка в матрицу при высокоскоростном прессовании. Несомненно, что на процесс прессования оказывает влияние и присутствие в смеси активного вещества. Авторами изобретения экспериментальным путем были определены пределы содержания дезлоратадина от 3 до 15%. Причем нижний предел в 3% обусловлен не свойствами порошка быть подвергнутому высокопроизводительному прессованию, а тем, что для таблеток содержащих приемлемое количество дезлоратадина экономически не целесообразно вводить в состав более 97% разбавителей.
Фармацевтической композицией в виде твердой лекарственной формы по настоящему изобретению обычно является таблетка, пригодная для перорального введения. Такая таблетка может быть покрыта оболочкой.
Композиция обычно содержит дезлоратадин в количестве от 3 до 50 мг на единицу твердой лекарственной формы. В качестве примера: типичная таблетка, содержащая 5 мг дезлоратадина, является белой или почти белой, цилиндрической двояковыпуклой формы диаметром 6 мм и массой 95 мг.
Соответственно, дополнительный аспект настоящего изобретения относится к способу изготовления фармацевтической композиции в виде твердой лекарственной формы, содержащей дезлоратадин в качестве терапевтически активного ингредиента, включающему стадии, на которых:
1) смешивают дезлоратадин и эксципиент, разбавитель или носитель, или их смеси, возможно, в присутствии увлажняющего агента, где, по меньшей мере два из указанных эксципиента, разбавителя и носителя представляет собой лактозу и целлюлозу микрокристаллическую, причем средний размер частиц составляет для лактозы 70-80 мкм и для целлюлозы микрокристаллической 40-60 мкм
2) формируют из полученной смеси гранулят, возможно в присутствии увлажняющего агента, подходящего для прессования в указанную твердую лекарственную форму;
3) возможно осуществляют указанное смешивание и/или формирование гранулята в присутствии по меньшей мере одной добавки, выбранной из разрыхлителя, смазывающего агента, связующего агента, корригента, консерванта, красителя и их смеси;
4) возможно сушат указанный гранулят;
5) прессуют указанный гранулят в твердую лекарственную форму.
6) возможно наносят на указанную твердую лекарственную форму пленочную оболочку.
Способ по настоящему изобретению как таковой можно осуществлять на практике, используя традиционное оборудование для изготовления фармацевтических препаратов, как только определены и включены конкретные компоненты. Гранулят, подходящий для прессования в таблетки, обычно имеет средний размер гранул по меньшей мере приблизительно 100 мкм. Отдельные гранулы с размером более 2 мм обычно не переносят на следующую стадию прессования.
В качестве неограничивающих примеров можно указать следующее оборудование для гранулирования: с псевдоожиженным твердым слоем и прямым нагревом, например поставляемое GEA/Collette NV, BE (серия UltimaPro™), Huttlin GmbH, DE (серия HDG), Diosna Dierks&Soehne GmbH, DE (серия VAC), Fluid Air Inc., US (серия Magnaflo®) и Vector Corp., US (серия GMX); с подвижным твердым слоем и непрямым теплообменом, включающее лопастные системы, ротационные системы и встряхивающие системы, которые поставляют, например, Jay go Inc., US (серии JRB и Novamix), Paul O. Abbe Inc., US (серии Rota-Cone, Rota-U, Rota Blade, Cylindrical Ribbon/Paddle, Plow и Sigma-blade), Forberg A/S, NO (серия Forberg II), Gemco Inc., US (серии D/3 Double Cone, V-Shape и Slant-Cone), LittlefordDay Inc., US (серии Double Arm, Day Nauta и Daymax), Patterson-Kelly, Harsco Corp., US (серия Р-К Solids Processor®), Diosna, как указанно выше (серии CCS и VAC), Romaco Zanchetta SpA, IT (серии Roto E, Roto D и Roto P) и L.B. Bohle Maschinen und Verfahren GmbH, DE (серии Granumator GMA и Vagumator VMA). Вышеуказанное оборудование обычно также обеспечивает сушку полученных гранул.
Соответственно, предпочтительно, чтобы указанное вещество представляло собой дисахарид, предпочтительно лактозу, и более предпочтительно лактозу - α - моногидрат. Указанный полисахарид предпочтительно представляет собой целлюлозу и более предпочтительно целлюлозу микрокристаллическую.
В способе по настоящему изобретению изготавливаемая твердая лекарственная форма обычно представляет собой пригодную для перорального введения таблетку. В качестве примера оборудования, на котором осуществляли процесс прессования таблеток, является роторный одноручьевой пресс с 45 прессующими комплектами и питателем с независимым приводом.
В предпочтительном воплощении способа по настоящему изобретению указанные стадии смешивания и формирования гранулята осуществляют в псевдоожиженном слое сушилки гранулятора.
Причем, как было указано выше, в составе фармацевтической композиции содержание активного действующего вещества, дезлоратадина, составляет от 3 до 15%, а количество антифрикционных, дезинтегрирующих, связывающих веществ (добавок) содержится в количестве от 1 до 10%. В качестве неограничивающих примеров, указанных добавок, широко применяемых и известных специалисту в области фармацевтической промышленности, можно указать магния стеарат, повидон и натрия кроскармеллозу. Предпочтительное количество действующего вещества и добавок, таким образом, может составлять от 4 до 25% от массы таблетки, более предпочтительно но не обязательно от 10 до 20%, однако наиболее предпочтительно, но вместе с тем не обязательно их содержание в количестве от 12 до 15%, но особенно предпочтительным является содержание активного вещества и добавок в количестве 13%.
Способ предпочтительно осуществляют таким образом, чтобы достигнуть максимальной прочности таблетки при оптимальном давлении для указанного состава и одновременно максимальной производительности на вышеуказанном прессе. Прочие качественные характеристики и показатели, при этом должны соответствовать, указанным в ГФ XI, вып.2, стр. 154-160 для указанной лекарственной формы. Причем, несмотря на допустимую ГФ прочность на истирание 97%, одной из задач по настоящему изобретению является достижение прочности на истирание в пределах 99,2-99,99% поскольку, как правило, уже при истирании менее 99,5% не вооруженным глазом видны сколы и дефекты материала.
Для достижения указанного результата, авторами настоящего изобретения были использованы различные комбинации составов, в частности комбинации наполнителей. Примеры и варианты, описывающие настоящее изобретение, более подробно приведены в таблице 1 и таблице 2. В таблице 1 приведены результаты испытаний различных вариантов составов. В таблице 2 указаны составы по каждому варианту из таблицы 1. Все варианты были произведены одинаковым способом, описанным ниже.
Специалисту в области изготовления фармацевтических препаратов известны термины, методы и способы определения, указанных в таблице 1 качественных характеристик, полученных таблеток и полностью находятся в пределах его квалификации.
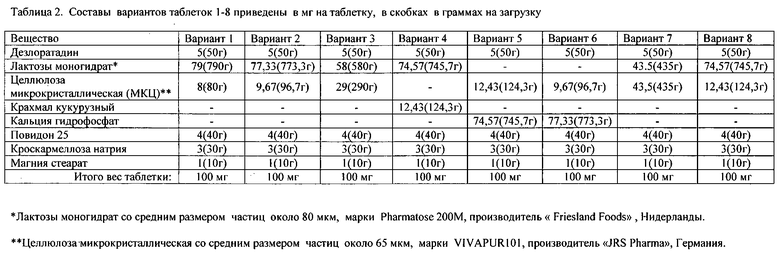
Как указано выше, предпочтительно получать из указанной полученной смеси гранулят со средним размером гранул по меньшей мере 100 мкм, предпочтительно в интервале от 100 мкм до 300 мкм.
В предпочтительном воплощении способа, как указанный дисахарид, так и полисахарид присутствуют на стадии смешивания. Тогда массовое соотношение указанного дисахарида и полисахарида обычно составляет от 8:1 до 2:1.
Способ предпочтительно осуществляют таким образом, что общее количество указанных эксципиентов, разбавителя и носителя в совокупности составляет от 75 до 96, предпочтительно от 80 до 90 процентов от массы фармацевтической композиции.
В наиболее предпочтительном воплощении используют дезлоратадин и смешивают его с указанными эксципиентом, разбавителем и/или носителем в количестве, которое в итоге обеспечивает содержание дезлоратадина в количестве от 3 до 50 мг на единицу твердой лекарственной формы.
Таким образом, Наиболее приемлемым составом и удивительным образом случайно подобранной комбинацией веществ, являющихся наполнителем лекарственной формы, является 8 вариант, указанный в таблице. Авторам настоящего изобретения, экспериментальным путем в результате многократных комбинаций составов и исследований качественных характеристик, полученных лекарственных форм, неожиданно удалось найти оптимальное соотношение компонентов, способ и технологию производства для получения наилучшего по качеству продукта при одновременно максимальной производительности.
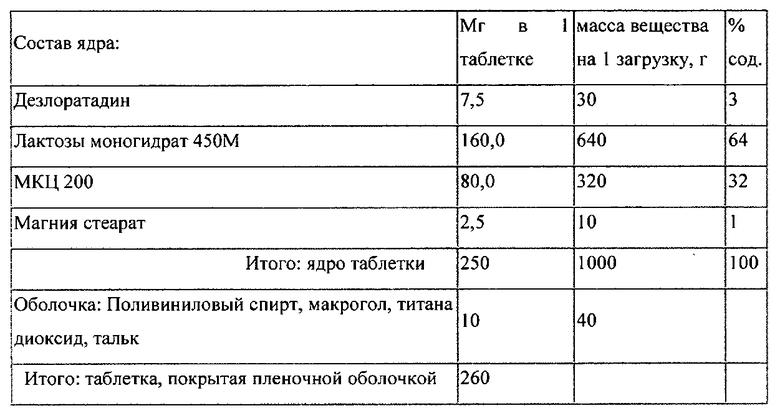
Наиболее предпочтительным, но не обязательным, является следующее содержание компонентов в мас. %:

Конкретный вариант наиболее предпочтительной рецептуры заявленного состава представлен в таблице 4.

Ниже приведены примеры изготовления таблеток, в которых использовались рецептуры, в соответствии с изобретением, а именно количество дезлоратадина от 3 до 15% и наполнителя от 75 до 96%, а так же показано использование лактозы и МКЦ со средним размером частиц от 30 до 200.
Примеры получения таблеток.
В приведенных примерах 1-4:
- при прессовании ядер производительность пресса составила 200-210 тысяч штук таблеток в час, отклонения в весе отдельных таблеток не превышали ±5% от средней массы;
- использованы марки наполнителей, характеризующиеся средним размером частиц:
лактозы моногидрат 450М со средним размером частиц около 30 мкм, марки Pharmatose 450М, производитель «Friesland Foods», Нидерланды,
лактозы моногидрат SD со средним размером частиц около 200 мкм, марки Fast Flo, производитель « Foremost Dr.», США,
МКЦ-105 со средним размером частиц около 30 мкм, марки VIVAPUR105, производитель «JRS Pharma», Германия,
МКЦ-200 со средним размером частиц около 200 мкм, марки Comprecel M200D+, производитель «MINGTAI», Тайвань.
Пример 1
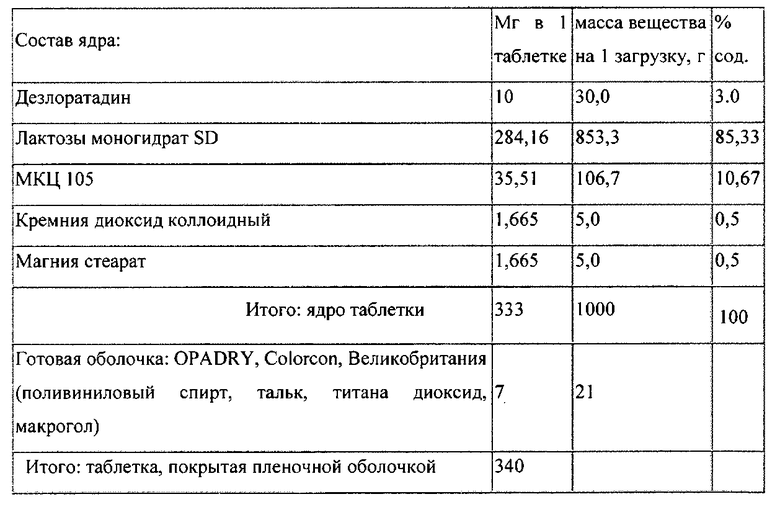
Дезлоратадин, лактозу и МКЦ перемешивают в лабораторном смесителе кубической формы, затем просеивают через сито с размером отверстий 0,63 мм и снова помещают в смеситель, добавляют кремния диоксид коллоидный и магния стеарат. Смесь просеивают еще раз через сито. Просеянную смесь прессуют с использованием прессинструмента диаметром 10 мм двояковыпуклой круглой цилиндрической формы. Получают ядра таблеток с прочностью на сдавливание 110-120Н и прочностью на истирание 99,4%, которые затем покрывают пленочной оболочкой, путем распыления водной суспензии на ядра, вращающиеся в перфорированном барабане.
Пример 2
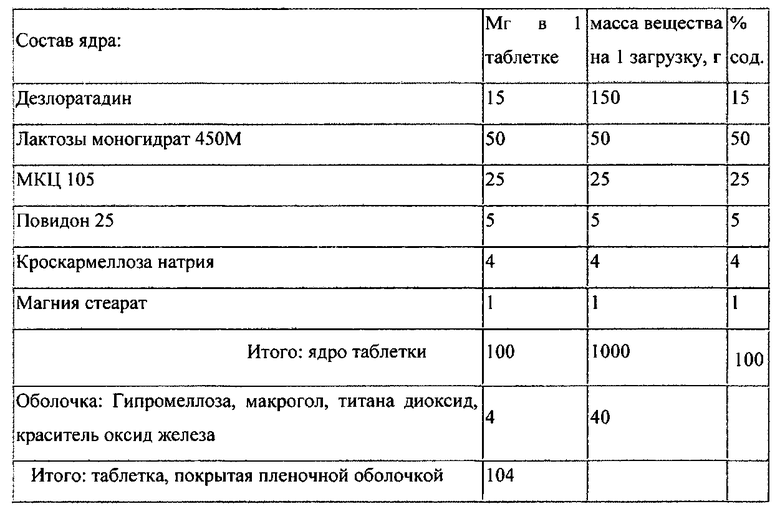
Дезлоратадин, лактозу, МКЦ и кроскармеллозу натрия, перемешивают в лопастном смесителе. Смесь гранулируют в псевдоожиженном слое лабораторной сушилки гранулятора путем распыления на нее чрез форсунку водного раствора повидона 25. После грануляции продукт сушат в этом же оборудовании до остаточной влажности 2-3%, затем добавляют магния стеарат и включают псевдоожижение на несколько секунд. Полученную смесь пропускают через сито 0,63 мм и прессуют из нее ядра таблеток диаметром 6 мм круглой цилиндрической двояковыпуклой формы. Прочность ядер на истирание составляет 99,8%, прочность на сдавливание 95-100Н.
Пример 3
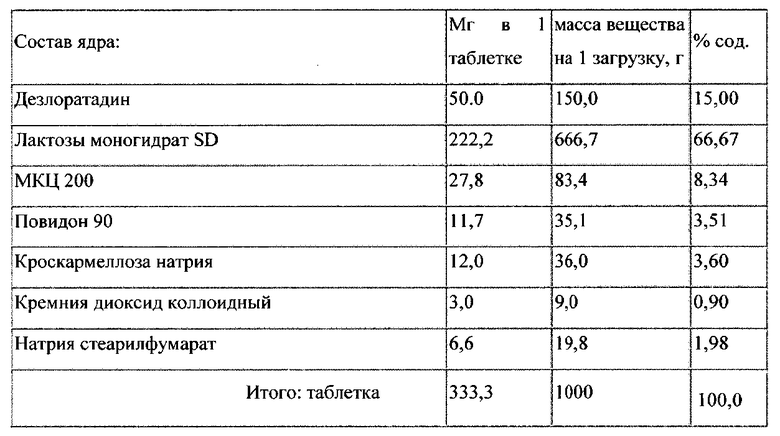
Дезлоратадин, лактозу, МКЦ, повидон, кроскармеллозу натрия, кремния диоксид коллоидный и натрия стеарилфумарат перемешивают в лопастном смесителе 30 сек. Смесь пропускают через коническую мельницу с установленной сеткой с диаметром отверстий около 2 мм. Просеянную смесь прессуют в таблетки капсулообразной формы, которые обладают прочностью на сдавливание 80-100Н и прочностью на истирание 99,5%..
Пример 4
Дезлоратадин, лактозу, МКЦ и половину магния стеарата, перемешивают в лопастном смесителе и пропускают через уплотнительные валки, уплотненный материал затем измельчают на конической мельнице, и перемешивают в смесителе с оставшейся частью магния стеарата. Из полученной смеси прессуют таблетки диаметром 9 мм круглой цилиндрической двояковыпуклой формы. Прочность ядер на истирание составляет 99,8%, прочность на сдавливание 70-85Н.
| название | год | авторы | номер документа |
|---|---|---|---|
| ДИСПЕРГИРУЕМАЯ В ВОДЕ ТАБЛЕТКА ДЕЗЛОРАТАДИНА И СПОСОБ ЕЕ ИЗГОТОВЛЕНИЯ | 2015 |
|
RU2631619C2 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, СОДЕРЖАЩАЯ ДЕЗЛОРАТАДИН (ВАРИАНТЫ) | 2013 |
|
RU2537169C1 |
| ХИМИЧЕСКИ- И ТЕРМОСТАБИЛЬНЫЕ ГОТОВЫЕ ФОРМЫ НОРАСТЕМИЗОЛА | 1998 |
|
RU2214245C2 |
| ТАБЛЕТКА, ПОЛУЧАЕМАЯ НЕПОСРЕДСТВЕННЫМ ПРЕССОВАНИЕМ, СОДЕРЖАЩАЯ 4-АМИНО-1-ГИДРОКСИБУТИЛИДЕН-1,1-БИСФОСФОНОВУЮ КИСЛОТУ В КАЧЕСТВЕ АКТИВНОГО ИНГРЕДИЕНТА | 2001 |
|
RU2279273C2 |
| ТВЕРДАЯ ЛЕКАРСТВЕННАЯ ФОРМА, СОДЕРЖАЩАЯ ДЕСМОПРЕССИН | 2004 |
|
RU2290945C2 |
| Таблетки ибупрофена натрия и способы изготовления фармацевтических композиций, включающих ибупрофен натрия | 2010 |
|
RU2715680C2 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ ДЕСМОПРЕССИНА В ВИДЕ ТВЕРДОЙ ДОЗИРОВАННОЙ ЛЕКАРСТВЕННОЙ ФОРМЫ И СПОСОБ ЕЕ ИЗГОТОВЛЕНИЯ | 2004 |
|
RU2303439C2 |
| КОМПОЗИЦИЯ И СПОСОБ ПРЯМОГО ПРЕССОВАНИЯ | 2005 |
|
RU2391097C2 |
| НЕ СОДЕРЖАЩИЕ ЛАКТОЗЫ, НЕГИГРОСКОПИЧНЫЕ И БЕЗВОДНЫЕ ФАРМАЦЕВТИЧЕСКИЕ ПРЕПАРАТЫ ДЕСКАРБОЭТОКСИЛОРАТАДИНА | 1998 |
|
RU2209627C2 |
| КОМПОЗИЦИЯ И СПОСОБ ПРЯМОГО ПРЕССОВАНИЯ | 2005 |
|
RU2766487C2 |
Изобретение относится к области медицины, в частности к фармацевтической промышленности, и описывает пероральную лекарственную форму, выполненную в виде таблетки, содержащую дезлоратадин в количестве от 3 до 15%, технологические добавки и фармацевтически приемлемый наполнитель. Технологические добавки состоят из кроскармеллозы натрия, магния стеарата и повидона. Наполнитель представляет собой смесь дисахарида лактозы и полисахарида целлюлозы микрокристаллической в соотношении от 2:1 до 8:1. Лактозу и целлюлозу микрокристаллическую используют со средним размером частиц от 30 до 200 мкм. При изготовлении таблетки дезлоратадин, лактозу и целлюлозу микрокристаллическую подвергают гранулированию. Изобретение обеспечивает уменьшение усилия прессования гранулята, повышение производительности технологического процесса при одновременном сохранении высокого качества таблеток. 8 з.п. ф-лы, 4 табл., 4 пр.
1. Лекарственная форма, содержащая дезлоратадин в качестве активного ингредиента в количестве от 3 до 15%, технологические добавки и фармацевтически приемлемый наполнитель, где наполнитель представляет собой смесь дисахарида лактозы и полисахарида целлюлозы микрокристаллической, взятых в соотношении от 2:1 до 8:1, при этом для изготовления лекарственной формы взвешенные дезлоратадин, лактозы моногидрат, целлюлозу микрокристаллическую перемешивают в смесителе, полученную смесь гранулируют, калибруют, опудривают и таблетируют, причем используют лактозу и целлюлозу микрокристаллическую со средним размером частиц от 30 до 200 мкм.
2. Лекарственная форма по п.1, где указанное соотношение находится в интервале от 4:1 до 7:1.
3. Лекарственная форма по п.1, где указанное соотношение находится в интервале от 5:1 до 6:1.
4. Лекарственная форма по п.1, где указанное соотношение составляет 6:1.
5. Лекарственная форма по п.1, где общее количество наполнителя составляет 75-96% от веса таблетки.
6. Лекарственная форма по п.1, где в составе указанных технологических добавок содержится кроскармеллоза натрия.
7. Лекарственная форма по п.1, где в составе указанных технологических добавок содержится магния стеарат.
8. Лекарственная форма по п.1, где в составе указанных технологических добавок содержится повидон.
9. Лекарственная форма по любому из пп.6-8, где указанные технологические добавки содержатся в количестве от 1 до 10%.
| Электрический насос | 1923 |
|
SU1627A1 |
| CN 102389404 A, 28.03.2012 | |||
| КОМБИНИРОВАННОЕ ГИПОТЕНЗИВНОЕ СРЕДСТВО | 2010 |
|
RU2444371C1 |
| ТАБЛЕТКА ИЗ АКТИВНОЙ ФАРМАЦЕВТИЧЕСКОЙ СУБСТАНЦИИ (ВАРИАНТЫ) И СПОСОБ ЕЕ ПОЛУЧЕНИЯ | 2009 |
|
RU2414888C1 |
| Н.Н.Жуйкова и др | |||
| "Комплексный наполнитель для прямого прессования на основе лактозы и микрокристаллической целлюлозы", Химико-фармацевтиеский журнал, 2010, | |||
Авторы
Даты
2015-05-20—Публикация
2013-04-23—Подача