Рассматриваемое применение
Настоящее изобретение касается открытия свойств сильнодействующего агониста мускариновых рецепторов дибензодиадипинового соединения N-десметилклозапина, 8-хлор-11-Q-пиперазинил)-5H-дибензо[b,e][1,4]диазепина, которое поддерживает клиническое применение данного лекарства в качестве превосходного терапевтического средства для лечения боли, глаукомы, слабоумия, аффективного заболевания и психоза.
Предпосылки изобретения
Физиологические действия гормон/нейротрансмиттер ацетилхолин опосредованы отчасти мускариновыми ацетилхолиновыми рецепторами. Мускариновые рецепторы включают семейство из пяти (M1-M5) трансмембранных белков, которые опосредуют медленную модулирующую передачу сигнала в клетках и тканях, экспрессирующих данные гены. Мускариновые рецепторы являются мишенями ряда терапевтически полезных агентов [1, 2]. Периферические мускариновые рецепторы опосредуют действия ацетилхолина в парасимпатической нервной системе. Периферическидействующие агонисты мускариновых рецепторов полезны терапевтически при снижении внутриглазного давления у пациентов с глаукомой [3]. Соединения, которые усиливают центральные действия ацетилхолина, а также центрально действующие агонисты мускариновых рецепторов, демонстрируют клиническую применимость при лечении ряда нейропсихиатрических заболеваний [1, 2, 4-7].
Действия ацетилхолина заканчиваются разрушением молекулы ацетилхолинэстеразными ферментами. Ингибирование данных ферментов в центральной нервной системе ведет к повышенным концентрациям ацетилхолина на мускариновых рецепторах. Разработан ряд ингибиторов ацетилхолинэстераз, которые находят рутинное клиническое применение в качестве агентов, повышающих познавательную функцию при слабоумии [4].
Ряд центрально действующих мускариновых агонистов является предметом клинического исследования. Показано, что один из них ксаномелин обладает эффективностью по регулированию психоза и родственных поведенческих нарушений, наблюдаемых у пациентов с болезнью Альцгеймера [5]. Кроме того, в настоящее время показано, что ксаномелин эффективен при лечении шизофрении [6]. Интересно, что он демонстрирует эффективность против позитивных и негативных симптомов и не вызывает вредных двигательных эффектов при начальных клинических исследованиях у шизофреников. Эти данные предполагают, что соединения со свойствами агонистов мускариновых рецепторов, вероятно, эффективны при лечении поведенческих нарушений, обычных для нейродегенеративного заболевания, такого как болезнь Альцгеймера, и в качестве антипсихотических средств для лечения психозов у людей, но только, если они допустимы в данной группе обследуемых пациентов. Кроме того, агонисты мускариновых рецепторов демонстрируют активность на доклинических моделях невропатических болезненных состояний [7].
Краткое содержание изобретения
Здесь раскрыто применение N-десметилклозапина для получения лекарственного средства для облегчения состояния психоза. В некоторых вариантах лекарственное средство подходит для введения человеку. В некоторых вариантах лекарственное средство вводят в виде единичной дозы. В других вариантах лекарственное средство вводят в виде многократных доз. В некоторых вариантах лекарственное средство содержит также дополнительный терапевтический агент. В некоторых вариантах дополнительный терапевтический агент выбран из группы, включающей селективные ингибиторы обратного захвата серотонина, ингибиторы обратного захвата норэпинефрина, агонисты дофамина, антипсихотические агенты и обратные агонисты серотонина 2A.
Также здесь раскрыто применение N-десметилклозапина для получения лекарственного средства для облегчения аффективных нарушений. В некоторых вариантах лекарственное средство подходит для введения человеку. В одном варианте аффективное нарушение является депрессией. В другом варианте аффективное нарушение является манией. В некоторых вариантах лекарственное средство вводят в виде единичной дозы. В других вариантах лекарственное средство вводят в виде многократных доз. В некоторых вариантах лекарственное средство также содержит дополнительный терапевтический агент. В некоторых вариантах дополнительный терапевтический агент выбран из группы, включающей селективные ингибиторы обратного захвата серотонина, ингибиторы обратного захвата норэпинефрина, агонисты дофамина, антипсихотические агенты и обратные агонисты серотонина 2A.
Также здесь раскрыто применение N-десметилклозапина для получения лекарственного средства для лечения слабоумия, в некоторых вариантах лекарственное средство подходит для введения человеку. В некоторых вариантах лекарственное средство вводят в виде единичной дозы. В других вариантах лекарственное средство вводят в виде многократных доз. В некоторых вариантах слабоумие проявляется как когнитивное нарушение. В некоторых вариантах слабоумие проявляется как поведенческое нарушение. В некоторых вариантах лекарственное средство содержит также дополнительный терапевтический агент. В некоторых вариантах дополнительный терапевтический агент выбран из группы, включающей селективные ингибиторы обратного захвата серотонина, ингибиторы обратного захвата норэпинефрина, агонисты дофамина, антипсихотические агенты и обратные агонисты серотонина 2А.
Также здесь раскрыто применение N-десметилклозапина для получения лекарственного средства для облегчения невропатической боли, в некоторых вариантах лекарственное средство подходит для введения человеку. В некоторых вариантах лекарственное средство вводят в виде единичной дозы. В других вариантах лекарственное средство вводят в виде многократных доз, в некоторых вариантах лекарственное средство также содержит дополнительный терапевтический агент. В некоторых вариантах дополнительный терапевтический агент выбран из группы, включающей селективные ингибиторы обратного захвата серотонина, ингибиторы обратного захвата норэпинефрина, агонисты дофамина, антипсихотические агенты и обратные агонисты серотонина 2А.
Также здесь раскрыто применение N-десметилклозапина для получения лекарственного средства для облегчения симптомов глаукомы. В некоторых вариантах лекарственное средство подходит для введения человеку. В некоторых вариантах лекарственное средство вводят в виде единичной дозы. В других вариантах лекарственное средство вводят в виде многократных доз. В различных вариантах симптомы глаукомы выбраны из группы, включающей повышенное внутриглазное давление, повреждение оптического нерва и уменьшенное поле зрения. В некоторых вариантах лекарственное средство содержит также дополнительный терапевтический агент. В некоторых вариантах дополнительный терапевтический агент выбран из группы, включающей селективные ингибиторы обратного захвата серотонина, ингибиторы обратного захвата норэпинефрина, агонисты дофамина, антипсихотические агенты и обратные агонисты серотонина 2А.
Также здесь раскрыт способ лечения психоза, включающий: идентификацию субъекта, страдающего от одного или нескольких симптомов психоза; и введение субъекту терапевтически эффективного количества N-десметилклозапина, посредством чего улучшается один или более симптомов психоза. В одном варианте субъект представляет собой человека. В некоторых вариантах терапевтически эффективное количество N-десметилклозапина вводят в виде единичной дозы. В других вариантах терапевтически эффективное количество N-десметилклозапина вводят в виде многократных доз. В одном варианте способ включает также введение субъекту дополнительного терапевтического агента. В одном варианте субъекту вводят дополнительный терапевтический агент после введения N-десметилклозапина. В другом варианте субъекту вводят дополнительный терапевтический агент до введения N-десметилклозапина. Еще в одном варианте субъекту вводят дополнительный терапевтический агент по существу одновременно с N-десметилклозапином. В некоторых вариантах дополнительный терапевтический агент выбран из группы, включающей селективные ингибиторы обратного захвата серотонина, ингибиторы обратного захвата норэпинефрина, агонисты дофамина, антипсихотические агенты и обратные агонисты серотонина 2А.
Также здесь раскрыт способ лечения аффективных нарушений, включающий: идентификацию субъекта, страдающего от одного или нескольких симптомов аффективного нарушения; и введение данному субъекту терапевтически эффективного количества N-десметилклозапина, посредством чего улучшается один или более симптомов аффективного нарушения. В одном варианте субъект является человеком. В одном варианте аффективное нарушение является депрессией. В другом варианте аффективное нарушение является манией. В некоторых вариантах терапевтически эффективное количество N-десметилклозапина вводят в виде единичной дозы. В других вариантах терапевтически эффективное количество N-десметилклозапина вводят в виде многократных доз. В одном варианте способ содержит также введение субъекту дополнительного терапевтического агента. В одном варианте субъекту вводят дополнительный терапевтический агент после введения N-десметилклозапина. В другом варианте субъекту вводят дополнительный терапевтический агент до введения N-десметилклозапина. Еще в одном варианте субъекту вводят дополнительный терапевтический агент по существу одновременно с N-десметилклозапином. В некоторых вариантах дополнительный терапевтический агент выбран из группы, включающей селективные ингибиторы обратного захвата серотонина, ингибиторы обратного захвата норэпинефрина, агонисты дофамина, антипсихотические агенты и обратные агонисты серотонина 2А.
Также здесь раскрыт способ лечения слабоумия, включающий: идентификацию субъекта, страдающего от одного или нескольких симптомов слабоумия; и введение указанному субъекту терапевтически эффективного количества N-десметилклозапина, посредством чего получают желательный клинический эффект. В одном варианте субъект является человеком. В некоторых вариантах терапевтически эффективное количество N-десметилклозапина вводят в виде единичной дозы. В других вариантах терапевтически эффективное количество N-десметилклозапина вводят в виде многократных доз. В одном варианте слабоумие проявляется как когнитивное нарушение. В другом варианте слабоумие проявляется как поведенческое нарушение. В одном варианте способ включает также введение субъекту дополнительного терапевтического агента.
В одном варианте субъекту вводят дополнительный терапевтический агент после введения N-десметилклозапина. В другом варианте субъекту вводят дополнительный терапевтический агент до введения N-десметилклозапина. Еще в одном варианте субъекту вводят дополнительный терапевтический агент по существу одновременно с N-десметилклозапином. В некоторых вариантах дополнительный терапевтический агент выбран из группы, включающей селективные ингибиторы обратного захвата серотонина, ингибиторы обратного захвата норэпинефрина, агонисты дофамина, антипсихотические агенты и обратные агонисты серотонина 2А.
Также здесь раскрыт способ лечения невропатической боли, включающий: идентификацию субъекта, страдающего от одного или нескольких симптомов невропатической боли; и введение указанному субъекту терапевтически эффективного количества N-десметилклозапина, посредством чего облегчают симптомы невропатической боли. В одном варианте субъект является человеком. В некоторых вариантах терапевтически эффективное количество N-десметилклозапина вводят в виде единичной дозы. В других вариантах терапевтически эффективное количество N-десметилклозапина вводят в виде многократных доз. В одном варианте способ включает также введение субъекту вводят дополнительного терапевтического агента. В одном варианте субъекту вводят дополнительный терапевтический агент после введения N-десметилклозапина. В другом варианте субъекту вводят дополнительный терапевтический агент до введения N-десметилклозапина. Еще в одном варианте субъекту вводят дополнительный терапевтический агент по существу одновременно с N-десметилклозапином. В некоторых вариантах дополнительный терапевтический агент выбран из группы, включающей селективные ингибиторы обратного захвата серотонина, ингибиторы обратного захвата норэпинефрина, агонисты дофамина, антипсихотические агенты и обратные агонисты серотонина 2А.
Также здесь раскрыт способ лечения глаукомы, включающий: идентификацию субъекта, страдающего от одного или нескольких симптомов глаукомы; и введение указанному субъекту терапевтически эффективного количества N-десметилклозапина, посредством чего облегчают симптомы глаукомы. В одном варианте субъект является человеком. В некоторых вариантах терапевтически эффективное количество N-десметилклозапина вводят в виде единичной дозы. В других вариантах терапевтически эффективное количество N-десметилклозапина вводят в виде многократных доз. В некоторых вариантах симптомы глаукомы выбраны из группы, включающей повышенное внутриглазное давление, повреждение оптического нерва и уменьшенное поле зрения. В одном варианте способ включает также введение субъекту дополнительного терапевтического агента. В одном варианте субъекту вводят дополнительный терапевтический агент после введения N-десметилклозапина. В другом варианте субъекту вводят дополнительный терапевтический агент до введения N-десметилклозапина. Еще в одном варианте субъекту вводят дополнительный терапевтический агент по существу одновременно с N-десметилклозапином. В некоторых вариантах дополнительный терапевтический агент выбран из группы, включающей селективные ингибиторы обратного захвата серотонина, ингибиторы обратного захвата норэпинефрина, агонисты дофамина, антипсихотические агенты и обратные агонисты серотонина 2А.
Также здесь раскрыта фармацевтическая композиция, содержащая фармацевтически эффективное количество N-десметилклозапина и дополнительный терапевтический агент. В некоторых вариантах дополнительный терапевтический агент выбран из группы, включающей селективные ингибиторы обратного захвата серотонина, ингибиторы обратного захвата норэпинефрина, агонисты дофамина, антипсихотические агенты и обратные агонисты серотонина 2А. В некоторых вариантах антипсихотический агент выбран из группы, включающей фенотиазин, фенилбутилпиперадин, дебензапин, бензизоксидил и соль лития. В некоторых вариантах антипсихотический агент выбран из группы, включающей хлорпромазин (Thorazine®), мезоридазин (Serentil®), прохлорперазин (Compazine®), тиоридазин (Mellaril®), галоперидол (Haldol®), пимозид (Orap®), клозапин (Clozaril®), локсапин (Loxitan®), оланзапин (Zyprexa®), кветиапин (Seroquel®), респеридон (Resperidal®), зипразидон (Geodon®), карбонат лития, арипипразол (Abilify), клозапин, клозарил, компазин, этрафон, геодон, халдол, инапсин, локситан, мелларил, мобан, наван, оланзапин (Zyprexa), орап, пермитил, проликсин, фенерган, кветиапин (Seroquel), реглан, риспердал, серентил, сероквел, стелазин, тарактан, торазин, триавил, трилафон, зипрекса и их фармацевтически приемлемые соли. В некоторых вариантах селективный ингибитор обратного захвата серотонина выбран из группы, включающей флуоксетин, флувоксамин, сертралин, пароксетин, циталопрам, эсциталопрам, сибутрамин, дулоксетин, венлафаксин и их фармацевтически приемлемые соли и пролекарства. В некоторых вариантах ингибитор обратного захвата норэпинефрина выбран из группы, включающей тиониксотин и ребоксетин. В некоторых вариантах агонист дофамина выбран из группы, включающей суматриптан, альмотриптан, наратриптан, фроватриптан, ризатриптан, зомитриптан, каберголин, амантадин, лизурид, перголид, ропинирол, прамипексол и бромокриптин. В одном варианте обратный агонист серотонина 2A представляет собой N-(1-метилпиперидин-4-ил)-N-(4-фторфенилметил)-N'-(4-(2-метилпропилокси)фенилметил)карбамид.
Краткое описание рисунков
На фиг.1 приведен график, показывающий результаты агонистической активности N-десметилклозапина на мускариновых ацетилхолиновых рецепторах M1 в (R-SAT)-исследованиях.
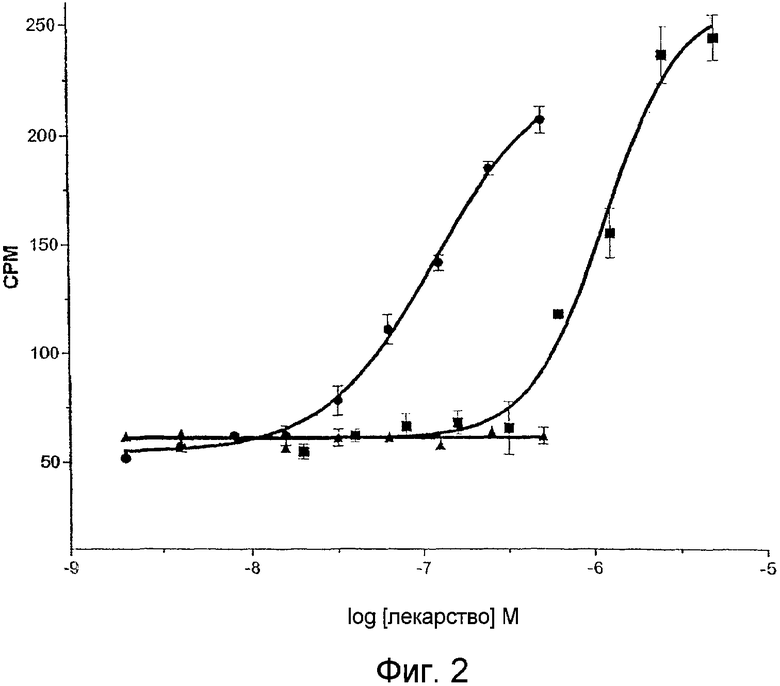
На фиг.2 приведен график, показывающий результаты агонистической активности N-десметилклозапина на мускариновых ацетилхолиновых рецепторах M1 в исследованиях с применением фосфатидилинозита.
На фиг.3 показаны фотографии активации MAP-киназы в гиппокампе крыс после парентерального введения N-десметилклозапина.
Подробное описание предпочтительного варианта
Определения
N-десметилклозапин, 8-хлор-11-(1-пиперазинил)-5H-дибензо[b,e][1,4]диазепин, определяют как соединение, имеющее молекулярную структуру, изображенную формулой (I).
"Агонист" определяют как соединение, которое повышает базовую активность рецептора (т.е. преобразование сигнала, опосредованное рецептором).
"Антагонист" определяют как соединение, которое конкурирует с агонистом или обратным агонистом за связывание с рецептором, блокируя тем самым влияние агониста или обратного агониста на рецептор. Однако антагонист (известный также как "нейтральный" антагонист) не оказывает влияния на неотъемлемую активность рецептора.
"Частичный агонист" определяют как агонист, который демонстрирует ограниченную или меньшую (чем полный агонист) активность, таким образом, что ему не удается активировать рецептор in vitro, функционируя как антагонист in vivo.
Термин "субъект" касается животного, предпочтительно млекопитающего и наиболее предпочтительно человека, который является объектом лечения, наблюдения или эксперимента.
Выражение "терапевтически эффективное количество" используют для указания количества активного соединения или фармацевтического агента, которое вызывает указанную биологическую или медицинскую реакцию. Данная реакция может происходить в ткани, системе, животном или человеке, который найден исследователем, ветеринаром, врачом или другим клиницистом и включает ослабление симптомов подлежащего лечению заболевания.
В некоторых вариантах раскрытый здесь способ включает введение субъекту терапевтически эффективного количества NDMC с целью лечения психоза.
В другом варианте способ включает введение субъекту терапевтически эффективного количества NDMC с целью лечения депрессии или мании.
Еще в одном варианте способ включает введение субъекту терапевтически эффективного количества NDMC с целью лечения психиатрических и других поведенческих нарушений, характерных для слабоумия или когнитивного нарушения любой природы.
Еще в одном варианте способ включает введение субъекту терапевтически эффективного количества NDMC с целью лечения невропатической боли.
Заявители настоящего изобретения представляют профили больших серий лекарств, которые находят применимость при лечении болезней человека благодаря функциональной активности на пяти подтипах мускариновых рецепторов человека. За исключением известных мускариновых лекарств только два исследованных агента (из числа более 500) демонстрируют активность агонистов мускариновых рецепторов. Один представляет собой нетипичное антипсихотическое средство клозапин [8]. Показано, что in vitro данное соединение обладает слабой активностью частичного агониста/антагониста на мускариновых рецепторах M1, M2 и M4 [9, 10], тогда как обычно полагают, что in vivo оно демонстрирует свойства антагониста мускариновых рецепторов. Другое соединение представляет собой рассматриваемый N-десметилклозапин.
Введение клозапина участвующим в исследовании людям дает в результате образование двух основных метаболитов N-десметилклозапина (NDMC) и клозапин-N-оксида [11]. Однако клозапин-N-оксид является полярным метаболитом, который быстро выделяется и, по-видимому, не вносит вклада в биологическую активность исходного соединения. Корреляция существует между дозой вводимого субъекту клозапина и уровнями в сыворотке всех фрагментов клозапина, кроме того, уровни NDMC могут варьироваться в широких пределах для индивидуальных субъектов [12]. Вообще NDMC составляет 40-75% общих концентраций клозапина в сыворотке при кинетиках в устойчивых состояниях у людей [13]. Имеются противоречивые данные, касающиеся способности NDMC проникать через гематоэнцефалический барьер и обеспечивать центрально-опосредованную активность [14, 15]. Данные наблюдения демонстрируют, что NDMC вводятся субъектам-людям обычным образом и хорошо переносятся. Имеются некоторые данные относительно молекулярных свойств NDMC. Показано, что NDMC обладает антагонистической активностью на рецепторах 5HT2C [16], но не сообщается данных по его взаимодействию с мускариновыми рецепторами.
Неожиданно и в отличие от родственных клозапину соединений обнаружено, что соединение N-десметилклозапин (NDMC) обладает недооцененной прежде функциональной активностью как агонист мускариновых рецепторов. Эксперименты ex vivo демонстрируют, что NDMC проходит гематоэнцефалический барьер и действует как агонист на центральных мускариновых рецепторах крыс. Данные наблюдения имеют практические применения, которые поддерживают применение NDMC в качестве антипсихотического средства, агента против маний, агента против слабоумия и в качестве терапевтического агента для лечения глаукомы или невропатической боли. Таким образом, в одном аспекте здесь раскрыт способ агонистического действия на активность мускаринового рецептора, включающий контакт данного рецептора с эффективным количеством NDMC. В другом аспекте здесь раскрыт способ лечения субъекта, страдающего от нарушения, связанного с мускариновыми рецепторами, включающий идентификацию нуждающегося в этом субъекта и введение данному субъекту терапевтически эффективного количества NDMC.
Выражение "нарушение, связанное с мускариновыми рецепторами" обозначает нарушение, симптомы которого облегчаются при агонистическом воздействии на мускариновые рецепторы.
В другом аспекте здесь раскрыт способ лечения у субъекта шизофрении или психоза любого происхождения, включающий идентификацию нуждающегося в этом субъекта и введение субъекту терапевтически эффективного количества NDMC. В некоторых вариантах способ включает введение субъекту фармакологически активной дозы NDMC с целью регулирования позитивных (галлюцинации и бред) и негативных (апатия, социальная самоизоляция, ангедония) симптомов шизофрении или родственного психоза.
В другом аспекте здесь раскрыт способ лечения у субъекта аффективных нарушений, включая глубокую депрессию, манию, биполярное нарушение и склонность к суициду, включающий идентификацию нуждающегося в этом субъекта и введение данному субъекту терапевтически эффективного количества NDMC. В некоторых вариантах способ включает введение субъекту фармакологически активной дозы NDMC с целью регулирования симптомов, наблюдаемых при глубокой депрессии или маниакальной депрессии.
В другом аспекте здесь раскрыт способ лечения у субъекта болезни Альцгеймера и родственных нейродегенеративных нарушений, включающий идентификацию нуждающегося в этом субъекта и введение данному субъекту терапевтически эффективного количества NDMC. В некоторых вариантах способ включает введение субъекту фармакологически активной дозы NDMC с целью улучшения познавательного дефицита и регулирования связанных с этим поведенческих аномалий, наблюдаемых при дегенеративном слабоумии.
В другом аспекте здесь раскрыт способ лечения у субъекта невропатической боли, включающий идентификацию нуждающегося в этом субъекта и введение данному субъекту терапевтически эффективного количества NDMC. В некоторых вариантах способ включает введение субъекту фармакологически активной дозы NDMC с целью регулирования дизестетических, гипералгических и других измененных ноцицептивных симптомов, наблюдаемых при невропатических болезненных состояниях независимо от их этиологии.
В другом аспекте здесь раскрыт способ лечения у субъекта глаукомы, включающий идентификацию нуждающегося в этом субъекта и введение субъекту терапевтически эффективного количества NDMC. В некоторых вариантах способ включает введение субъекту фармакологически активной дозы NDMC с целью регулирования повышенного внутриглазного давления, наблюдаемого при глаукоме, независимо от ее этиологии.
Неожиданно показано, что NDMC оказывает сильное агонистическое действие на мускариновые рецепторы человека. Кроме того, здесь раскрыто, что NDMC может проходить гематоэнцефалический барьер и функционировать in vivo как агонист мускариновых рецепторов, что определяют посредством активации MAP киназной активности в гиппокампе крыс. Молекулярные активности NDMC, которые идентифицированы настоящими способами, объединенные с известной клинической эффективностью соединений, которые обладают аналогичным молекулярным фармакологическим профилем, показывают, что NDMC можно применять для облегчения или лечения нарушений или состояний, связанных с психозом, аффективным заболеванием, дегенеративным слабоумием, глаукомой и невропатической болью.
Получение N-десметилклозапина (NDMC)
N-десметилклозапин (NDMC) имеет структуру, представленную формулой (I).
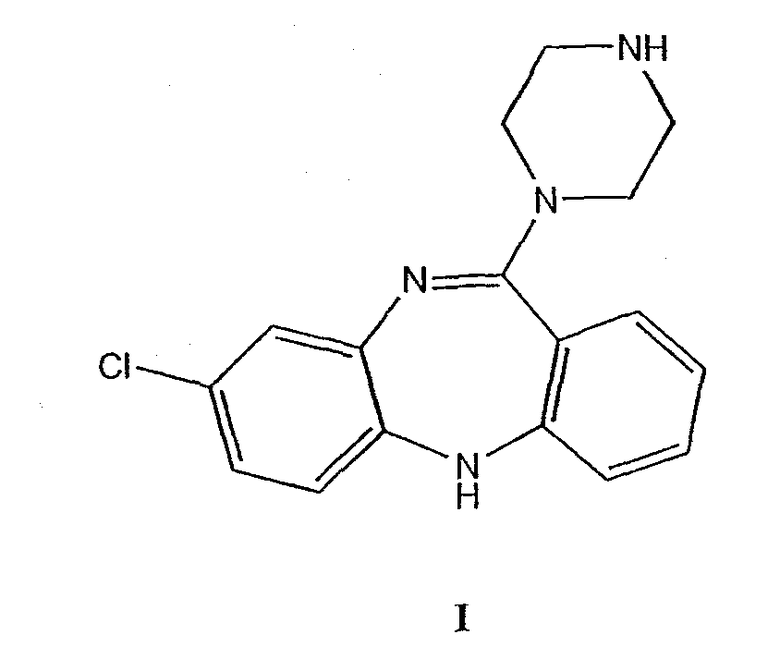
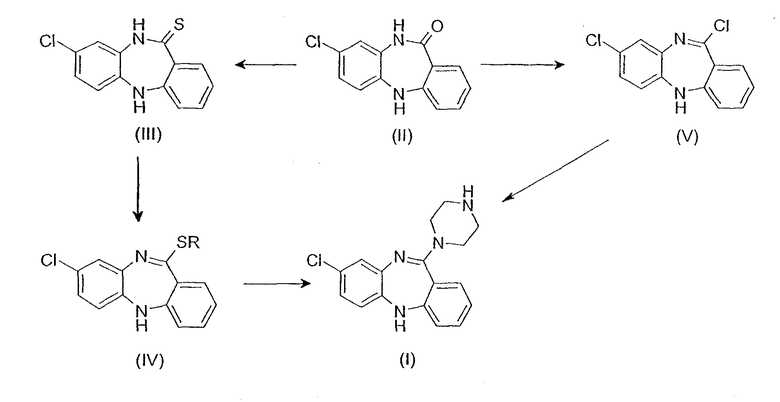
NDMC получают, как описано ранее [17]. Предшественник дибензодиазепинлактам (II) превращают в тиолактам (III), применяя пентасульфид фосфора с последующим алкилированием, например, диметилсульфатом с получением иминотиоэфира (IV). Аминолиз данного тиоэфира избытком пиперазина дает требуемый N-десметилклозапин (I). Иначе дибензодиазепинлактам (II) можно превратить в иминохлорид (V) посредством обработки агентом галогенирования, таким как пентахлорид фосфора, и продукт (V) превращают в N-десметилклозапин (I) взаимодействием с пиперазином.
NDMC можно приготовить в виде фармацевтических композиций, содержащих NDMC вместе с фармацевтически приемлемым разбавителем или наполнителем. Такие композиции можно приготовить подходящим образом и в соответствии с принятой практикой, например, как раскрыто в Remington's Pharmaceutical Sciences, Gennaro, Ed., Mack Publishing Co., Easton PA, 1990.
Преимущественно NDMC можно принимать в виде единичной дневной дозы или дневную дозу можно вводить в виде многократных доз (например, разделенными дозами два, три или четыре раза в день). Кроме того, соединение настоящего изобретения можно вводить в виде интраназальной формы посредством локального применения подходящих интраназальных носителей, или трансдермальными способами, или посредством локального применения глазных препаратов, или используя формы трансдермальных кожных пластырей, хорошо известные специалистам в данной области.
Схему приема NDMC можно выбрать в соответствии с различными факторами. Они включают тип, вид, возраст, вес, пол и медицинское состояние пациента; тяжесть подлежащего лечению состояния; способ приема препарата; почечную и печеночную функцию пациента и конкретное используемое соединение. Обычный лечащий врач может легко определить и прописать эффективное количество лекарства, необходимое для профилактики, противодействия или прекращения развития заболевания или нарушения, которое подлежит лечению.
Дневную дозу продуктов можно варьировать в широком диапазоне от 0,01 до 1000 мг в день для взрослого человека. Эффективное количество лекарства обычно обеспечивают при уровне дозы примерно от 0,0001 до 25 мг/кг массы тела в день. Предпочтительный диапазон составляет примерно от 0,001 до 10 мг/кг массы тела в день и особо предпочтительно примерно от 0,001 до 1 мг/кг массы тела в день. Данные соединения можно вводить по схеме от 1 до 4 раз в день.
NDMC можно применять сам по себе при подходящих дозах, определенных посредством рутинного исследования с целью получения оптимального фармакологического эффекта, минимизируя потенциальные токсические или другие нежелательные эффекты. Кроме того, полагают, что NDMC можно применять как дополнительную терапию с известными лекарствами с целью снижения необходимой дозы данных традиционных лекарств, уменьшая тем самым их побочные эффекты.
В некоторых вариантах NDMC вводят в комбинации с одним или несколькими дополнительными терапевтическими агентами. Дополнительные терапевтические агенты могут включать (но не ограничены этим) нейропсихиатрический агент. Используемое здесь выражение "нейропсихиатрический агент" касается соединения или комбинации соединений, которые воздействуют на нейроны в головном мозге прямо или косвенно или влияют на сигнал, передаваемый нейронам в головном мозге. Таким образом, нейропсихиатрические агенты могут воздействовать на психику пациента, т.е. настроение, восприятие, ноцицепцию, познавательную функцию, настороженность, память и др. В некоторых вариантах нейропсихиатрический агент может быть выбран из группы, включающей селективный ингибитор обратного захвата серотонина, ингибитор обратного захвата норэпинефрина, агонист дофамина, антипсихотический агент и обратные агонисты серотонина 2А.
В некоторых вариантах антипсихотический агент может быть выбран из группы, включающей фенотиазин, фенилбутилпиперадин, дебензапин, бензизоксидил и соль лития. Фенотиазиновая группа соединений может быть выбрана из группы, включающей хлорпромазин (Thorazine®), мезоридазин (Serentil®), прохлорперазин (Compazine®) и тиоридазин (Mellaril®). Фенилбутилпиперадиновая группа соединений может быть выбрана из группы, включающей галоперидол (Haldol®) и пимозид (Orap®). Дебензапиновая группа соединений может быть выбрана из группы, включающей клозапин (Clozaril®), локсапин (Loxitane®), оланзапин (Zyprexa®) и кветиапин (Seroquel®). Бензизоксидильная группа соединений может быть выбрана из группы, включающей респеридон (Resperidal®) и зипразидон (Geodon®). Соль лития может быть карбонатом лития. В некоторых вариантах антипсихотический агент может быть выбран из группы, включающей арипипразол (Abilify), клозапин, клозарил, компазин, этрафон, геодон, халдол, инапсин, локситан, мелларил, мобан, наван, оланзапин (Zyprexa), орап, пермитил, проликсин, фенерган, кветиапин (Seroquel), реглан, риспердал, серентил, сероквел, стелазин, тарактан, торазин, триавил, трилафон и зипрекса или их фармацевтически приемлемые соли.
В некоторых вариантах селективный ингибитор обратного захвата серотонина выбран из группы, включающей флуоксетин, флувоксамин, сертралин, пароксетин, циталопрам, эсциталопрам, сибутрамин, дулоксетин и венлафаксин и их фармацевтически приемлемые соли или пролекарства.
В других вариантах ингибитор обратного захвата норэпинефрина выбран из группы, включающей тиониксотин и ребоксетин.
В других вариантах агонист дофамина выбран из группы, включающей суматриптан, альмотриптан, наратриптан, фроватриптан, ризатриптан, зомитриптан, каберголин, амантадин, лизурид, перголид, ропинирол, прамипексол и бромокриптин.
В другом варианте обратный агонист серотонина 2A представляет собой N-(1-метилпиперидин-4-ил)-N-(4-фторфенилметил)-N'-(4-(2-метилпропилокси)фенилметил)карбамид.
В другом аспекте настоящее описание касается способа лечения нейропсихиатрических нарушений у пациента, включающего идентификацию нуждающегося в этом пациента и введение указанному пациенту терапевтически эффективного количества фармацевтической композиции, содержащей соединение формулы (I) и нейропсихиатрический агент. Еще в одном аспекте настоящее описание касается способа лечения у пациента нейропсихиатрического нарушения, включающего идентификацию нуждающегося в этом пациента и введение указанному пациенту терапевтически эффективного количества соединения формулы (I) и терапевтически эффективного количества нейропсихиатрического агента.
В некоторых вариантах NDMC и дополнительный терапевтический агент(ы) вводят почти одновременно. Такие варианты включают случаи, когда соединения находятся в одной и той же вводимой композиции, т.е. единая таблетка, пилюля или капсула, или единый раствор для внутривенной инъекции, или единый раствор для питья, или единое драже, или пластырь содержит данные соединения. Такие варианты также включают случаи, когда каждое соединение представляет собой отдельно принимаемую композицию, но пациенту назначают принимать данные отдельные композиции почти одновременно, т.е. одну пилюлю принимают сразу после другой, или инъекцию одного соединения делают сразу после инъекции другого соединения, и др.
В других вариантах сначала вводят один из NDMC и дополнительное терапевтическое соединение и во вторую очередь вводят другой из NDMC и дополнительное терапевтическое соединение. В данных вариантах пациенту можно вводить композицию, содержащую одно из соединений, и затем через некоторое время (несколько минут или несколько часов) вводить другую композицию, содержащую другое из указанных соединений. В данные варианты включены также случаи, когда пациенту вводят композицию, содержащую одно из соединений, обычным образом или постоянно, при этом он время от времени принимает композицию, содержащую другое соединение.
Определение функциональной фармакологической активности NDMC относительно данного рецептора можно осуществить, применяя различные методологии. В настоящее время предпочтительным исследованием является технология с отбором и амплификацией рецепторов (R-SAT), раскрытая в патенте США 5707798.
Определение функциональной фармакологической активности NDMC относительно данного рецептора можно осуществить, применяя различные методологии. Другим предпочтительным в настоящее время исследованием является PI гидролиз [18].
Оценку способности NDMC проникать через гематоэнцефалический барьер и вызывать ясную биологическую реакцию можно провести, применяя различные методологии. Предпочтительным в настоящее время исследованием является исследование с активацией MAP- киназы гиппокампа [19].
Настоящее изобретение раскрыто также в следующих примерах, которые никоим образом не предназначены для ограничения области данного изобретения, которая заявлена.
Пример 1
Функциональное исследование рецепторов - технологию с отбором и амплификацией рецепторов (R-SAT) применяют (главным образом, как раскрыто в патенте США 5707798) для исследования функциональных фармакологических свойств известных лекарств, включая многие их метаболиты. Данные эксперименты дают молекулярный профиль или «отпечатки пальцев» для каждого из данных агентов. Среди всех исследованных агентов только один NDMC демонстрирует сильную агонистическую активность относительно ацетилхолиновых рецепторов M1. На фиг.1 показано соотношение концентрация-реакция для клозапина (черные треугольники) и N-десметилклозапина (черные кружочки) по активации мускариновых рецепторов M1 человека. Данные получены из (R-SAT)-исследований, которые описаны ранее [20]. Данные представлены в виде графика как процент активации по отношению к полному агонисту мускариновых рецепторов карбахолу относительно концентрации лекарства. «Veh» обозначает носитель.
Как показано на фиг.1, клозапин демонстрирует высокую силу воздействия (pEC50 7,2), а также ограниченную характеристическую эффективность (относительная эффективность <25%) на рецепторах M1 человека. Клозапин, таким образом, определяют как слабый частичный агонист. Частичные агонисты не имеют достаточной позитивной характеристической активности для стимуляции рецептора аналогично полным агонистам. Таким образом, они ведут себя in vivo как антагонисты. В противоположность этому NDMC также демонстрирует высокую силу воздействия (pEC50 7,2) на рецепторах M1 человека, кроме того, он демонстрирует существенно большую позитивную характеристическую активность на рецепторах М1 (65% эффективность относительно карбахола), действуя как полный сильный агонист в (R-SAT)-исследованиях. Данная повышенная эффективность предполагает, что NDMC будет действовать in vivo как агонист, функциональный профиль отличается от профиля, наблюдаемого для клозапина.
Для подтверждения наблюдения, что NDMC демонстрирует повышенную агонистическую эффективность относительно рецепторов М1, проводят исследование PI гидролиза, результаты которого раскрыты на фиг.2 и в таблице 1. Данные фиг.2 получены из PI- исследований, которые описаны в [18]. На фиг.2 показано соотношение концентрация-реакция для карбахола (черные квадраты), клозапина (черные треугольники) и N-десметилклозапина (черные кружочки) по активации мускариновых рецепторов М1 человека. Данные представлены в виде графика как радиоактивность, измеренная в импульсах в минуту относительно концентрации лекарства.
В таблице 1 сила воздействия приводится как величины pEC50 и эффективность приводится как эффективность относительно полного агониста карбахола, в обоих случаях +/- стандартное отклонение, "n" обозначает количество экспериментальных определений. NDMC демонстрирует высокую силу воздействия как М1-агонист в данной системе (pEC50=7,0) при полной эффективности (>65% эффективность относительно карбахола). Таким образом, два различных функциональных исследования подтверждают, что NDMC обладает недооцененной ранее силой воздействия и активностью полного эффективного агониста на мускариновых ацетилхолиновых рецепторах М1 человека. Эта значительно большая позитивная характеристическая активность NDMC предполагает, что он ведет себя in vivo как агонист рецептора М1.
Клозапин и NDMC исследованы на остальных подтипах мускариновых рецепторов. Эти данные раскрыты в таблице 2. Данные таблицы 2 получены из (R-SAT)-исследований, которые описаны ранее [20]. Сила воздействия приведена как величины pEC50 и эффективность приведена как относительная эффективность полного агониста карбахола, в обоих случаях +/- стандартное отклонение. N обозначает количество экспериментальных определений.
вности
вности
вности
вности
NDMC демонстрирует повышенную характеристическую активность на всех пяти подтипах мускариновых рецепторов по сравнению с клозапином. Профиль NDMC на мускариновых рецепторах человека наиболее похож на профиль, наблюдаемый для исследовательского агента ксаномелина, при одном важном отличии - значительно меньшей эффективности на рецепторах m3 человека.
Для подтверждения аспектов данного молекулярного профиля in vivo и для оценки способности NDMC достигать центральной нервной системы NDMC вводят крысам парентерально и определяют активацию MAP киназной (MAPK) активности гиппокампа, опосредованной рецептором М1, это раскрыто на фиг.3. NDMC-обработка активирует MAPK в CA1 пирамидальных нейронах. Мышей C57BL6 обрабатывают подкожно носителем, N-десметилклозапином, клозапином или NDMC и скополамином (внутрибрюшинно) при дозах, указанных на фиг.3, и затем метят методом иммуногистохимии. При NDMC-обработке клеточные тела и проксимальные дендриты пирамидальных нейронов CA1 демонстрируют увеличенную фосфо-MAPK иммунореактивность по сравнению с обработкой носителем или клозапином. Кроме того, скополамин снижает NDMC-индуцированную активацию MAPK в CA1 области, что показательно для механизма, опосредованного мускариновыми рецепторами. Сильную активацию наблюдают при дозе 30 мг/кг. Это подтверждает, что NDMC проникает через гематоэнцефалический барьер и функционирует in vivo как агонист мускариновых рецепторов.
Цитированная литература
1. Eglen, R., M., Choppin, A. and Watson, N., (2001) Therapeutic opportunities from muscarinic receptor research. Trends Pharmacol. Sci. 22(8): 409-414.
2. Brown, J., H. and Taylor, P., (1996) Muscarinic receptor agonists and antagonists, in The pharmacological basis of therapeutics. Hardiman, J., G. and Limbird, L., E., editors, Mcgraw-Hill, New York, pp. 141-161.
3. Moroi, S., E. and Lichter, P., R. (1996) Ocular pharmacology, in The pharmacological basis of therapeutics. Hardiman, J., G., and Limbird, L., E., editors, Mcgraw-Hill, New York, pp. 1619-1647.
4. Davis, R E; Doyle, P D; Carroll, R T; Emmerling, M R; Jaen, J. Cholinergic therapies for Alzheimer's disease: Palliative or disease altering? Arzneimittel-Forschung, 45, 425-431, 1995.
5. Bodick, N., C., Offen, W., W., Levey, A., L, et., al. (1997) Effects of xanomeline, a selective muscarinic receptor agonist, on cognitive function and behavioral symptoms in Alzheimer's disease. Arch. Neurol, 54: 465-473.
6. Shekhar, A., Potter, W., Z., Lienemann, J., et. al. (2001) Efficacy of xanomeline, a selective muscarinic agonist, in treating schizophrenia: a double blind placebo controlled study. ACNP abstracts 135: 173.
7. Rodriquez, M.A., Whipple, В., Ocampo, G., et. al. (2002) Muscarinic agonists in neuropathic and nociceptive pain assays in rats. International Association for the Study of Pain's 10th World Congress, 1160-P76: 388.
8. Baldessarini, R., J., and Frankenburg, F., R. (1991) Clozapine. A novel antipsychotic agent. New. Engl. J. Med., 324(11): 746-754.
9. Olianis, M., C., Maullu, C., and Onali, P., (1999) Mixed agonist-antagonist properties of clozapine at different human cloned muscarinic receptor subtypes expressed in Chinese hamster ovary cells. Neuropsychopharmacology, 20(3): 263-270.
10. Zorn, S., H., Jones, S., В., Ward, К., М., and Liston, D., R. (1994) Clozapine is a potent and selective muscarinic m4 receptor agonist. Eur. J. Pharm. 269: R1-R2.
11. Janh, M., W., Grimsley, S., R., Gray, E., C., and Chang, W. (1993) Pharmacokinetic and pharmacodynamics of clozapine. Clin. Pharmacokinet. 24(2): 161-176.
12. Bondesson, U., and Lindstrom. L., H., (1988) Determination of clozapine and its N-desmethylated metabolite in plasma by use of gas chromatography-mass spectrometry with single ion detection. Psychopharmacology. 95: 472-475.
13. Centorrino, F., Baldessarini, R., J., Kando, J., C., et. al. (1994) Clozapine and metabolites: concentrations in serum and clinical findings during treatment of chronically psychotic patients. J. Clin. Psychopharmacol. 14: 119-125.
14. Baldessarini, R., J., Centorrino, F., Flood, J., G., et. al. (1993) Tissue concentrations of clozapine and its metabolites in the rat. Neuropsychopharmacology. 9(2): 117-124.
15. Weigmann, H., Hartter, S., Fischer, V., Dahmen, N., and Hiemke, C. (1999) Distribution of clozapine and desmethylclozapine between blood and brain in rats. European Neuropharmacology 9: 253-256.
16. Kuoppamaki, M., Syvalahti, E., and Hietala, J. (1993) Clozapine and N-desmethylclozapine are potent 5-HT1C receptor antagonists. Eur. J. Pharm. 245: 179-182.
17. Hunziker F. Fisher, E, and Scmutz, J. (1967) 11-amino-5H-dibenzo[b,e]-1,4-diazepine. Mitteilung uber siebenglienrige Heterocyclen. Helv. Chim. Acta, 50:1588-1599.
18. Jensen, A., A., Spalding, Т., A., Burstein E., S., et. al. (2000) Functional importance of the Ala(116)-Pro(136) region in the calcium-sensing receptor. Constitutive activity and inverse agonism in a family С G-protein-coupled receptor. J Biol Chem. 275(38): 29547-55.
19. Berkeley J., L., Gomeza J., Wess J., Hamilton S., E., Nathanson N., M., and Levey Al. (2001) M1 muscarinic acetylcholine receptors activate extracellular signal-regulated kinase in CA1 pyramidal neurons in mouse hippocampal slices. Mol. Cell Neurosci. 18(5): 512-24.
20. Weiner, D., M., Burstein, E., S., Nash, N., et. al. (2001) 5-hydroxytryptamine 2A receptor inverse agonists as antipsychotics. J Pharmacol Exp Ther., 299(1): 268-76.
| название | год | авторы | номер документа |
|---|---|---|---|
| СЕЛЕКТИВНЫЕ ОБРАТНЫЕ АГОНИСТЫ СЕРОТОНИНОВЫХ РЕЦЕПТОРОВ В КАЧЕСТВЕ ЛЕКАРСТВЕННЫХ СРЕДСТВ ПРИ ЗАБОЛЕВАНИИ | 2005 |
|
RU2442607C2 |
| НОВЫЕ ПРИМЕНЕНИЯ | 2019 |
|
RU2836384C2 |
| СЕЛЕКТИВНЫЕ ОБРАТНЫЕ АГОНИСТЫ СЕРОТОНИН 2А/2С РЕЦЕПТОРА, ПРИМЕНЯЕМЫЕ В КАЧЕСТВЕ ЛЕКАРСТВЕННЫХ СРЕДСТВ ПРИ НЕЙРОДЕГЕНЕРАТИВНЫХ ЗАБОЛЕВАНИЯХ | 2008 |
|
RU2465267C2 |
| СЕЛЕКТИВНЫЕ ОБРАТНЫЕ АГОНИСТЫ СЕРОТОНИН 2А/2С РЕЦЕПТОРА, ПРИМЕНЯЕМЫЕ В КАЧЕСТВЕ ЛЕКАРСТВЕННЫХ СРЕДСТВ ПРИ НЕЙРОДЕГЕНЕРАТИВНЫХ ЗАБОЛЕВАНИЯХ | 2004 |
|
RU2332401C2 |
| ЛЕЧЕНИЕ ОЖИРЕНИЯ АНТАГОНИСТАМИ МУСКАРИНОВОГО РЕЦЕПТОРА М1 | 2007 |
|
RU2455981C2 |
| ЛЕЧЕНИЕ ПСИХОЛОГИЧЕСКИХ СОСТОЯНИЙ С ПРИМЕНЕНИЕМ АНТАГОНИСТОВ M-МУСКАРИНОВЫХ РЕЦЕПТОРОВ | 2007 |
|
RU2477634C2 |
| ОРГАНИЧЕСКИЕ СОЕДИНЕНИЯ | 2015 |
|
RU2785871C2 |
| ОРГАНИЧЕСКИЕ СОЕДИНЕНИЯ | 2015 |
|
RU2728787C2 |
| ЛЕЧЕНИЕ ПОСТТРАВМАТИЧЕСКОГО СТРЕССОВОГО РАССТРОЙСТВА | 2008 |
|
RU2458691C2 |
| НОВЫЕ СПОСОБЫ | 2014 |
|
RU2682658C1 |
Предложено применение N-десметилклозапина для получения лекарственного средства, увеличивающего уровень активности мускаринового рецептора для облегчения состояния или лечения шизофрении. N-десметил-клозапин - метаболит клозапина, применяемого для лечения шизофрении. Показано, что N-десметилклозапин отличает от клозапина более сильная активация мускариновых рецепторов, в том числе действие на М3- и М5- мускариновые рецепторы (клозапин не действует на последние), способность проникать в центральную нервную систему через гемато-энцефалический барьер. 9 з.п. ф-лы, 3 ил., 2 табл.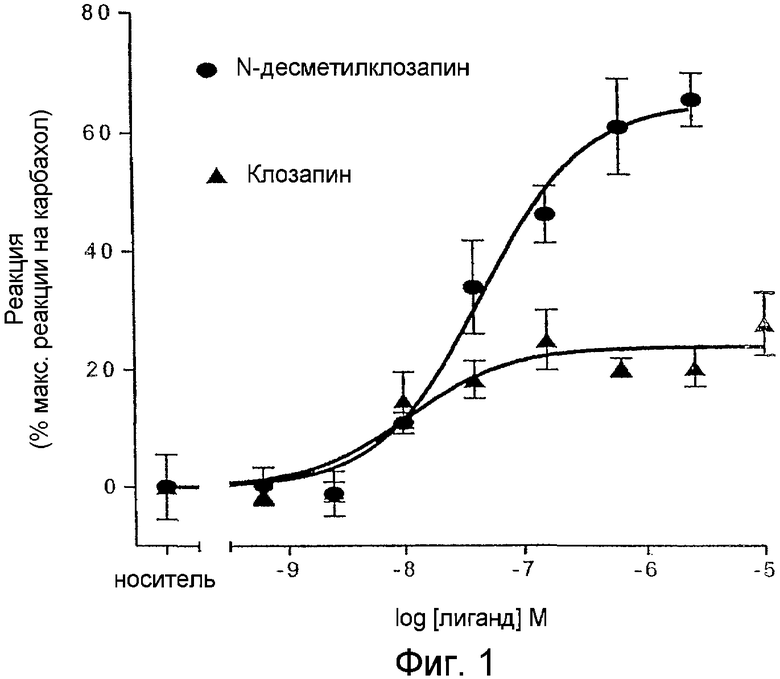
| Young C.D | |||
| et al | |||
| Effects of desmethylclozapine on Fos protein expression in the forebrain: in vivo biological activity of the clozapine metabolite | |||
| Neuropsychopharmacology | |||
| Способ и аппарат для получения гидразобензола или его гомологов | 1922 |
|
SU1998A1 |
| Руководство по медицине «THE MERCK MANUAL» | |||
| - M.: Мир, 1997, т.2, с.77-78 | |||
| Bilder R.M | |||
| et al | |||
| Neurocognitive effects of clozapine, olanzapine, | |||
Авторы
Даты
2008-10-27—Публикация
2004-01-21—Подача