Изобретение относится к области медицины и может быть использовано для лечения нарушения обмена веществ, иммунитета, сердечно-сосудистой системы, дерматологических, инфекционных, паразитарных, опухолевых, неспецифических воспалительных и аллергических заболеваний у взрослых и детей.
Известны способы лечения заболеваний при помощи фотодинамической терапии (Weishaupt K.R., Dougherty Т.О., Potter W.R. Purified hematoporphyrine derivative for diagnosis and treatment of tumors, and method, PCT, WO 84/01382, 1984, p.1-25), основанные на сочетании фототоксического и/или фотомодифицирующего эффекта лекарственного препарата (токсического и/или модифицирующего действия на клетку и ткань при его взаимодействии со светом) с накоплением препарата преимущественно в патологически измененной клетке или ткани. К фотодинамической терапии также относится действие лазерного излучения на клетки крови в присутствии фотосенсибилизатора (ФС) (Proc. SPIE, 5973 (2005), OX-1-7, Photoditazine mediated chemosensitized blood photomodification. Advanced tumors treatment preliminary results. M.L.Gelfond, D.L.Vassiliev) и антимикробная фотодинамическая терапия (Лазерная медицина, 6(1) (2002) 32-38. Антимикробная фотодинамическая терапия. Н.Е.Васильев А.П.Огиренко; Journal of Antimicrobal Chemotherapy. Photodynamic antimicrobial Chemotherapy. 42 (1998) 13-28. M.Wainwright).
Эти способы по типу действия делятся на фототоксические и фотомодифицирующие. При фототоксическом действии происходит разрушение клеток и некроз ткани вследствие непосредственного контакта фотосенсибилизатора, кислорода и света с клетками тканей и сосудов (локальное действие с радиусом около 20 нм для «Фотофрина II» (ФII)). Этот радиус связан со временем жизни активной частицы кислорода в клеточном окружении (около 48 наносекунд для ФII), типом и концентрацией ФС (Phys. Med. Biol. 50 (2005) 2597-2616, Characterization of Photofrin photobleaching for singlet oxygen dose estimation during photodynamic therapy of MLL cells in vitro, Jonathan S. Dysart and Michael S. Patterson; J. Photochem. PhotobioL, B: Biol., 6 (1990), 343-344. On the diffusion length of singlet oxygen in cells and tissues. J. Moan). При фотомодифицирующем действии в результате фотохемомодификации клеточных маркеров патологической ткани активируются антигенпрезентирующие клетки и клетки с опухолеспецифической памятью и формируется иммунный ответ, иногда сопровождающийся активным противоопухолевым иммунным ответом, разрушающим опухоли, обнаруженные иммунной системой вдали от первичного очага совместного действия ФС, кислорода и света (Proc. SPIE 4961 (2003) 1-9, Specific anti-tumor immune response with photodynamic therapy mediated by benzoporphyrin derivative and chlorin (e6), Ana P. Castano, Faten Gad, Touqir Zahra, Michael R.Hamblin).
При проведении ФДТ могут осуществляться и оба механизма одновременно (Медицинская иммунология. Иммунологические аспекты фотодинамической терапии, 5-6 (2003) 507-518. Н.Е.Васильев, Е.Д.Даниленко, Г.М.Сысоева).
Однако такие способы лечения требуют однократного, а часто и многократного облучения светом очага заболевания (например, опухоли) или крови. Для этого к очагу заболевания требуется подвести свет. Это, во-первых, требует точного знания места нахождения очага заболевания, что затруднительно даже при высокоразвитой диагностике и требует сложной аппаратуры (одновременное использование УЗИ, компьютерной и ЯМР-томографии, анализов крови и биопсий), поэтому в современной онкологии остро стоит проблема выявления первичной опухоли у пациента. Во-вторых, для подведения света (за исключением случаев, когда очаг заболевания расположен на коже) необходимо использование эндоскопа либо внутритканевой или внутрисосудистой инвазии, что связано с дополнительным дорогостоящим оборудованием, медицинским хирургическим стационаром и неудобствами для пациента.
Как наиболее близкий к предлагаемому, известен также способ, согласно которому любой из ФС - мероцианин 540, ФII или нафталимид - активируют светом вне пробирки (ex vitro), затем добавляют предактивированный ФС к культуре вирусов герпеса или иммунодефицита человека, либо раковых клеток различных линий, что ведет к инактивации вирусов и ингибированию пролиферативной активности раковых клеток на 70-90%. в то время как 85% нормальных лейкоцитов крови человека выживают (Eur J Cancer (1990) 26(5), 551-553. Preactivation - a novel antitumour and antiviral approach. K.S.Gulliya, T.Chanh, J.Newman, S.Pervaiz, J.L.Matthews). Роль в повреждающем действии в нем отводится опухолеспецифическим метастабильным продуктам деградации этих ФС наряду с продуктами окисления других молекул, которые образуются под действием света, причем для проявления биологической активности ФС дальнейшая световая экспозиция уже не требуется.
Недостатком данного способа является его лабораторный характер: вплоть до настоящего времени отсутствует клиническая методика для его применения у людей по причинам, приведенным ниже (The FASEB Journal (2001); 15 612-617. Reactive oxygen-dependent production of novel photochemotherapeutic agents. S.Pervaiz). Основным недостатком является то, что предложенный в способе ФС ФII обладает невысокой опухолевой специфичностью как на клеточных культурах, так и в экспериментах на животных-опухоленосителях и у людей. У животных для модельных поверхностных форм рака отношение накопления в опухоли к нормальной ткани составляет 0,8 для кожи над опухолью. 1,1 для кожи вокруг опухоли, и 2 для мышечной ткани (Photochem. Photobiol. (1989) 50, 221-228. Distribution and elimination of Photon-in II in mice. D.A.Bellnier, Y.-K.Ho. R.K.Padney, J.R.Missert and T.J.Dougherty). У людей при различных формах рака с локализацией в брюшной полости отношение накопления в опухоли к нормальной ткани составляет в среднем 1,6, максимальное - 2,3 (Clinical Cancer Research, 12, (2006) 5464-5470. Photofnn Uptake in the Tumor and Normal Tissues of Patients Receiving Intraperitoneal Photodynamic Therapy. S.M.Hahn, M.E.Putt, J.Metz, D.B.Shin, E. Rickter, C.Menon, D.Smith, E.Glatstein, D.L.Fraker and Т.М.Busch). Мероцианин 540 способен накапливаться в оболочке и структурах раковых клеток (Biochim Biophys Acta (2005) 1722(1) 51-59. Merocyanine 540-sensitized photokilling of leukemia cells: role of post-irradiation chain peroxidation of plasma membrane lipids as revealed by nitric oxide protection. М.Zareba, М.Niziolek. W.Korytowski, A.W.Girotti), но, будучи красителем для цитологии, мероцианин 540 не используется в клинической медицине из-за высокой генотоксичности и фототоксичности для здоровых тканей in vivo (Toxicol Lett (2000) 115, 53-61. Photocytotoxic and DNA damaging effect of temoporfin (mTHPC) and merocyanine 540 (MC540) on nasopharyngeal carcinoma cell. C.M.Yow, N.K.Mak, S.Szeto, J.Y.Chen, Y.L.Lee, N.H.Cheung, D.P.Huang, A.W.Leung). Нафталимид опухолеспецифичностью не обладает.
Данные факты превращают упомянутый способ при применении у человека в аналог традиционной химиотерапии опухолей, не отличающийся новизной.
Задачей настоящего изобретения является предложение способа дистанционного и избирательного воздействия на очаг опухолевого, инфекционного, паразитарного, дерматологического, иммунологического или аллергического заболевания, на источник нарушения обмена веществ или работы сердечно-сосудистой системы, пригодного для клинического применения.
Не все очаги заболеваний, например опухоли, могут быть подвергнуты лечению методом ФДТ из-за распространенности процесса или недоступности для лазерного воздействия (например, множественные метастазы или метастазы в лимфатические узлы средостения или брюшной полости). Кроме того, многие пациенты по различным причинам не могут быть подвергнуты классическим методам лечения - лучевому, хирургическому или химио-, антибиотикотерапии. Таким пациентам врачи рекомендуют только симптоматическое лечение.
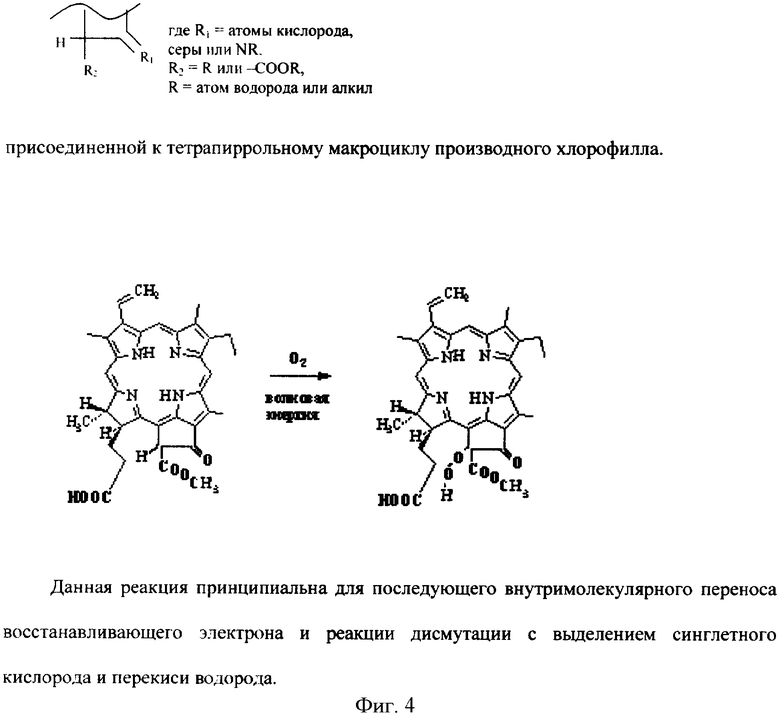
Поставленная задача решена путем создания способа, который заключается во введении ФС предварительно или одномоментно с введением подвергнутого действию волновой энергии в присутствии кислорода, причем в качестве ФС используют производные хлорофилла, содержащие по отдельности или вместе в одном или в нескольких соединениях, составляющих композицию, группы: 15-карбоксиметил-, 3-винил-, 15-формил-, 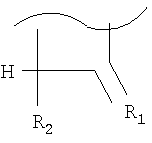
где R1 = атомы кислорода,
серы или NR,
R2=R или -COOR,
R = атом водорода или алкил
Задачей настоящего изобретения также является достижение в способе лечения высокой воспроизводимости, простоты, отсутствия токсичности для здоровых органов, тканей и систем организма, химической стабильности предактивированной формы ФС в течение, по крайней мере, нескольких дней, совокупности физико-химических и биологических свойств ФС, которые обеспечат его эффективность при терапии.
Предлагаемое изобретение принципиально отличается от всех известных как по способу воздействия на очаг заболевания, по выбору хлоринов в качестве фотосенсибилизаторов, так и по воздействию на них волновой энергии вне организма человека (в отличие, например, от внутрисосудистого и надсосудистого облучения светом фотосенсибилизатора, циркулирующего в крови). При ФДТ происходит совместное действие кислорода, света и ФС на биологический объект, а в предлагаемом изобретении - разнесенное во времени (кислород и волновая энергия действуют на ФС, а затем окисленная форма ФС - на дистанционный биологический объект). По типу проявляемого действия на организм данный способ можно отнести к фотомодифицирующим и увеличивающим специфические распознающие функции иммунной системы и назвать «фотоиммунотерапией» (ФИТ).
Сущность способа заключается в том, что ФС перед введением в организм активируют излучением в присутствии кислорода, причем в качестве ФС применяют производные хлорофилла, содержащие по отдельности или вместе, в одном или в нескольких составляющих композицию соединениях группы 15-карбоксиметил-, 3-винил, 15-формил-, 
где R1 = атомы
кислорода,
серы или NR,
R2=R или -COOR,
R = атом водорода или алкил
а в качестве излучения - волновую энергию мощностью 0,1-20000 Вт в дозе 1-100000 Дж.
Кроме того. в способе в качестве примера композиции из вышеупомянутых ФС используют лекарственный препарат «Радахлорин®» (РХ), содержащий хлорин е6 (13-карбокси-17-[2-карбоксиэтил]-15-карбоксиметил-17,18-транс-дигидро-3-винил-8-этил-2,7,12,18-тетраметилпорфирин) (содержит группы 15-карбоксиметил-, 3-винил-)
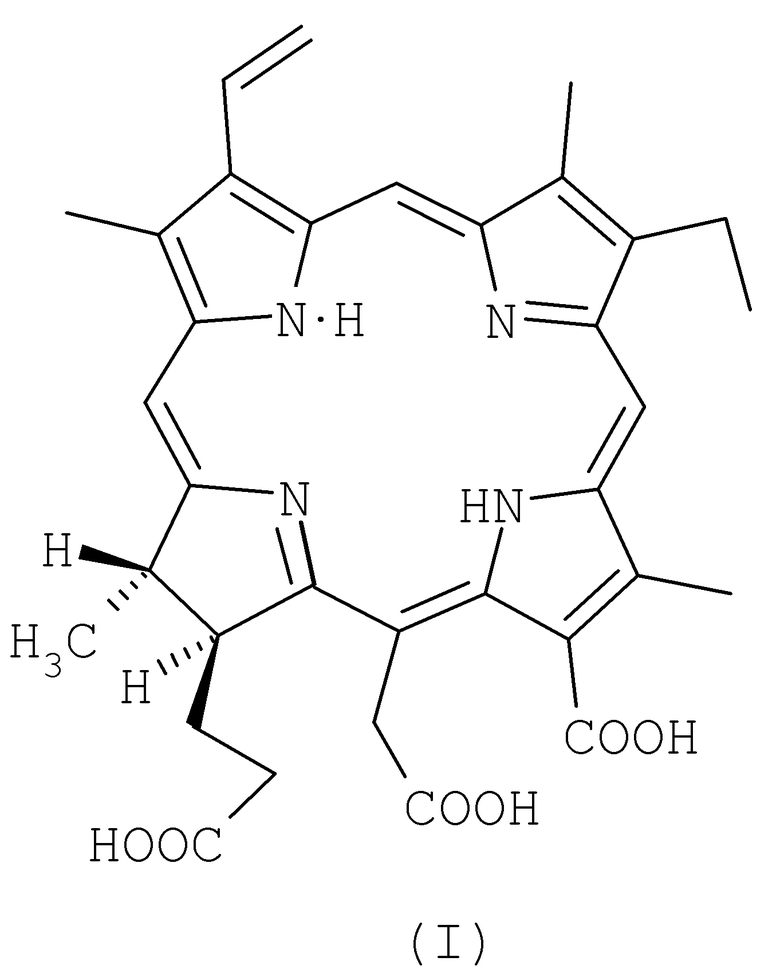
в количестве 80-90%, пурпурин 5 (13-карбокси-17-[2-карбоксиэтил]-15-формил-17,18-транс-дигидро-3-винил-8-этил-2,7,12,18-тетраметилпорфирин) (содержит группу 15-формил-)
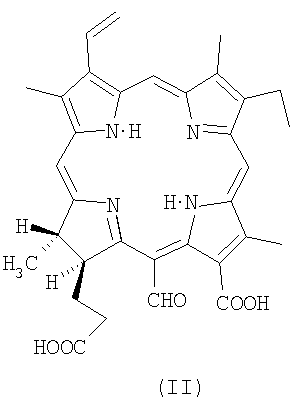
в количестве 5-20%, а также пурпурин 18-хлорин р6 (13-карбокси-17-[2-карбоксиэтил]-15-карбокси-17,18-транс-дигидро-3-винил-8-этил-2,7,12,18-тетраметилпорфирин)
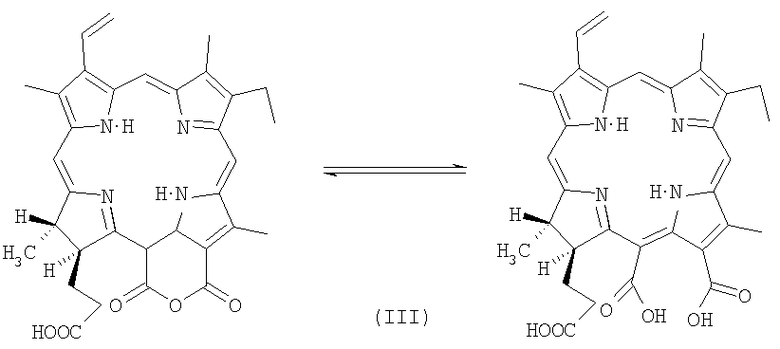
в количестве - остальное, так что указанные компоненты образуют композицию, а в лекарственных формах могут быть использованы их соли со щелочными металлами и азотосодержащими соединениями.
Кроме того, в способе используют медицинский лазер «ЛАХТА-МИЛОН®», излучающий волновую энергию длиной волны любой (или по две любых единовременно) в ряду 635, 662, 670, 690, 798, 808, 920, 960, 975, 1060, 1260, 1300, 1470, 1530, 1750 нм, мощностью от 1 до 18 Вт в непрерывном режиме или импульсами от 1 до 1000 мс (с паузами от 1 до 1000 мс).
Указанный способ реализуется с помощью стандартного медицинского оборудования для облучения ФС (лазеров, ламп накаливания, светодиодных, люминесцентных, газоразрядных ламп, источников радио-, магнитного и ультразвукового излучения, волноводов - кварцевых и других, как оснащенных, так и не оснащенных цилиндрическими диффузорами), для введения активированного ФС в организм человека (капельниц, шприцев, ультразвуковых и других ингаляционных приборов).
В способе производные хлорофилла используются в связи с их малой токсичностью (Использование лазеров для диагностики и лечения заболеваний. Научно-информационный сборник - приложение к бюллетеню «Лазер-информ» (2001) 3, 34-40. Оценка биологических свойств новых фотосенсибилизаторов хлоринового ряда. А.В.Решетников, А.В.Иванов, О.Ю.Абакумова, А.Т.Градюшко, И.Д.Залевский, А.В.Карменян, В.П.Лаптев, Н.П.Неугодова) и высокой избирательностью накопления в очагах патологических процессов (опухолях, абсцессах, инфицированных тканях, атеросклеротических бляшках и т.п.) (Optical Methods for Tumor Treatment and Detection: Mechanisms and Techniques in Photodynamic Therapy IX. - T.J.Dougherty, ed., Vol.3909, 131-137 (2000). One more PDT application of chlorin е6. A.V.Ivanov, A.V.Reshetnickov, G.V.Ponomarev). А именно, на моделях опухолей экспериментальных животных при введении производного хлорофилла в дозе 20 мг/кг через 0,5-5 часов после введения отношение концентрации хлорина в опухоли к концентрации в нормальной ткани варьировало от 3 до 40, а по коже и мышцам соответственно составило 4 и 3, что превышает терапевтический индекс ФII в аналогичном способе лечения соответственно в 3,6 и 2 раза. При лечении рака кожи у людей флюоресцентная контрастность накопления препарата РХ, содержащего производные хлорофилла, дозой 1,2 мг/кг (опухоль/кожа) варьировала от 3/1 до 6/1, что по максимальному возможному значению превышает терапевтический индекс ФII в аналогичном способе лечения в 2,6 раза (Российский Биотерапевтический Журнал (2004) 1, 77-82. Фотодинамическая терапия и флюоресцентная диагностика с фотосенсибилизатором «Радахлорин®» у больных раком кожи. Е.Г.Вакуловская. А.В.Решетников, И.Д.Залевский, Ю.В.Кемов; Current research on Laser Use in Oncology 2000-2004, A.V.Ivanov, M.A.Kazaryan, eds., Proceedings of SPIE (2005) 5973, 81-86. Photodynamic therapy and fluorescent diagnostics of head and neck cancer with second-generation photosensitizers. E.G.Vakulovskaya). Однако для предлагаемого способа принципиально не столько большее терапевтическое отношение для РХ, сколько отсутствие у него значительного сродства к коже, слизистым оболочкам и паренхимальным органам, благодаря чему он выводится из организма на 96% за 24 часа (при этом оставшееся количество удерживается патологически измененными тканями до 6 суток). ФII же выводится из нормальных тканей в течение 2,5-3 месяцев, и его активация в этот период дневным светом может привести к системному токсическому действию на организм пациента.
В способе мощность и дозы волновой энергии предложены в диапазоне 0,1-20000 Вт, 1-100000 Дж. Это связано с тем, что мощность менее 0,1 Вт делает процедуру слишком длительной, а мощности выше 20 кВт технически малодоступны, и их невозможно в настоящее время использовать в условиях медицинского стационара. Дозы излучения менее 1 Дж на дозу ФС недостаточно для его активации, а доза свыше 100 кДж приводит к фотообесцвечиванию ФС и к потере его свойств.
В способе предлагаются производные хлорофилла, содержащие по отдельности или вместе в одном или в нескольких составляющих композицию соединениях группы 15-карбоксиметил-, 3-винил-, 15-формил-, 
где R1 = атомы кислорода,
серы или NR,
R2=R или -COOR,
R = атом водорода или алкил
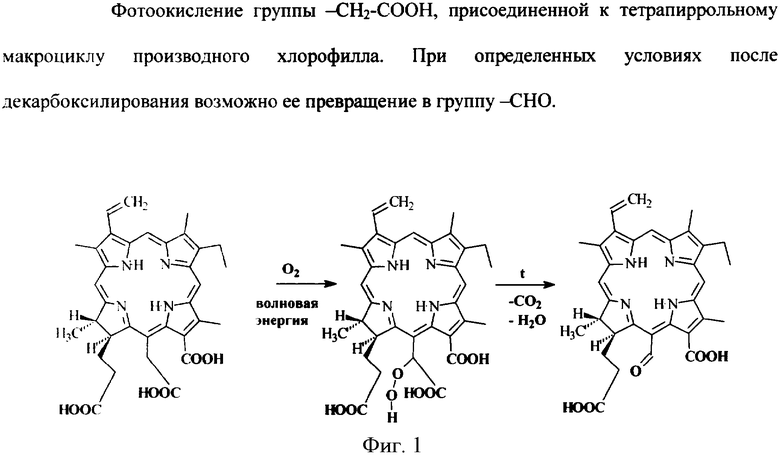
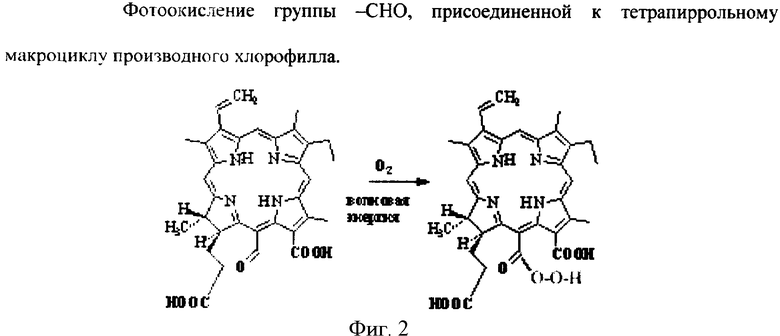
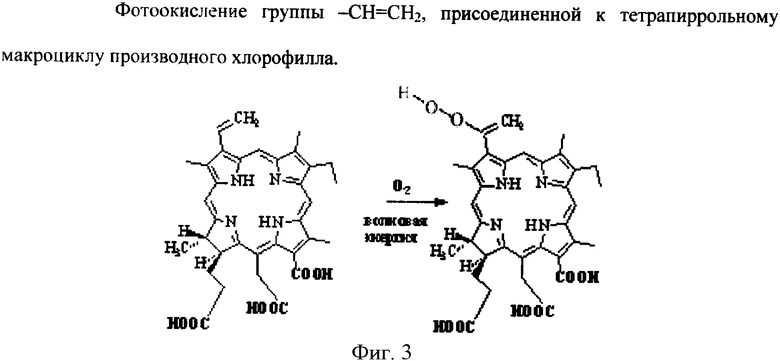
Известно, что для образования синглетного кислорода (1О2) необходимо наличие молекул ФС, при помощи которых происходит передача энергии фотонов молекулам кислорода. Известно также, что эффективными ФС образования 1О2 являются основные пигменты фотосинтеза, например производные хлорофиллов. Синглетным кислородом (1О2) называют электронно-возбужденные молекулы О2, находящиеся на одном из двух синглетных уровней - lg+ и lg. Таким образом, 1О2 отличается от других активных форм кислорода (радикалов О2 -, НОО, ОН или перекиси водорода Н2О2) тем, что для его получения требуется лишь поглощение энергии без химической модификации кислородных молекул. Данными многих исследований доказано, что lg - состояние 1О2 приводит к пероксидазным реакциям. Упомянутые в способе группы с точки зрения их химических свойств способны к химическим превращениям по схемам, изображенным на Фиг.1-4.
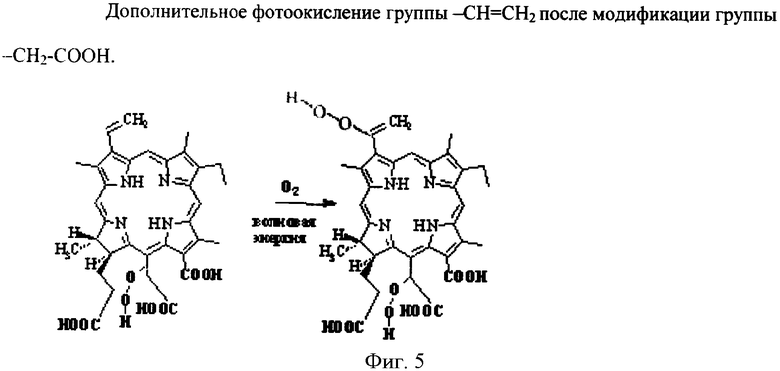
И далее каждое из четырех веществ способно присоединить вторую молекулу кислорода. Это демонстрируется для одного вещества схемой, приведенной на Фиг.5. Для других веществ присоединение второй молекулы кислорода по группе -СН=СН2 протекает аналогично. Данная реакция принципиальна для последующего внутримолекулярного переноса восстанавливающего электрона и реакции дисмутации с выделением синглетного кислорода и перекиси водорода.
При этом р-электронные молекулярные орбитали ядра порфина (18-π-электронная ароматическая система) стабилизируют супероксид-анионы, образующиеся в результате действия на ФС волновой энергии, приводя к химической устойчивости активированной формы ФС в течение, по крайней мере, нескольких дней.
Перекиси, образующиеся под воздействием света и кислорода из упомянутых выше групп, присоединенных непосредственно к ароматической системе производных хлорофилла, стабилизированные наличием порфинового макроцикла и потому долгоживущие, после введения в организм человека накапливаются по свойству, присущему производным хлорина е6, в очагах опухолевого, инфекционного, паразитарного, дерматологического, иммунологического или аллергического заболевания, могут переносить атом кислорода, гидроксил-радикал, либо электрон как друг на друга, так и на биомолекулы оболочек патологически измененных клеток (ПИК) или микроорганизмов.
Модифицированные синглетным кислородом (окисленные) группы атомов 15-карбоксиметил- и 3-винил-, 15-формил- и 3-винил-, 
где R1 = атомы кислорода,
серы или NR,
R2=R или -COOR,
R = атом водорода или алкил
и 3-винил-, соединенные с ароматическим ядром порфина, при межмолекулярном (Фиг.1-4) (либо внутримолекулярном - Фиг.5) переносе восстанавливающего электрона способны к превращениям, аналогичным известной схеме дисмутации супероксид-аниона, в результате которой могут высвобождаться синглетный кислород (который ранее присоединился к молекуле производного хлорофилла в процессе ее активации излучением) и перекись водорода:
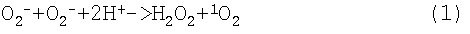
При реакции супероксид-аниона и перекиси водорода образуется гидроксил-радикал:
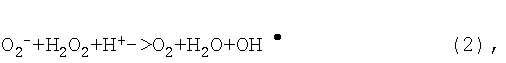
который при реакции с супероксид анионом образует вновь синглетный кислород:
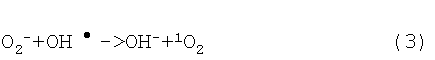
Таким образом, продуктами реакции могут являться кислород, вода, гидроксид-анион и синглетный кислород (который по окислительной способности уступает только гидроксил-радикалу).
Кислород и синглетный кислород далее при некоторых условиях могут также приводить к образованию озона и атомарного кислорода:

Эти перекиси как самого ФС, так и субстратов, которые ассоциируются с ним и также окисляются, превращаясь в кислородсодержащие радикалы, могут существовать, по данным хемилюминесценции, от минут до десятков часов и могут являться важными факторами фотоиммунотерапии (ФИТ), дополнительными к собственно перекисям ФС, накопившимся в очаге заболевания.
Таким образом, на оболочках всех ПИК под действием перекисей и прочих активных форм кислорода (суммарно-АФК) происходит фотохемомодификация молекул, отвечающих за функцию передачи и распознавания сигналов, вследствие чего клетки становятся узнаваемыми для иммунной системы организма, которая лучше распознает и подавляет патологический процесс. Гибель измененных клеток приводит к подаче сигнала на стволовые клетки человека, являющихся своеобразными «запасниками» организма, инициирующими образование новых клеток (например, в случае массовых повреждений тканей). На месте разрушенных клеток появляются новые, здоровые клетки. Одновременно происходит активация обменных процессов в клетках, повышается уровень иммунной защиты организма в целом. Аналогичное действие оказывается и на патогенную микрофлору.
Действие РХ не проявляется на уровне генов, что исключает генетические модификации. Отсутствие стимуляции деления малодифференцированных (раковых) клеток дополнительно доказано экспериментами на животных. Это подтвердили и иммунологические исследования - рост иммунорегуляторного индекса Т4/Т8 и рост иммуноглобулина А, который свидетельствует об адекватном завершении иммунного ответа именно на мембраносвязанные клеточные маркеры разрушаемых ПИК (Реологические свойства крови у больных с лимфогранулематозом в процессе и после курса химиотерапии. Влияние Радахлорофилла. Материалы 22 симпозиума по реологии Реологического общества им. Г.В.Виноградова. 21-26 июня 2004 г. г. Валдай. Стр.41. А.В.Решетников, Н.А.Горбунова, Л.И.Ершова, З.М.Лиховецкая, Т.А.Балакина Г.Н.Курбакова, М.Л.Маркова, Н.Н.Цыба).
Наряду с увеличением специфичности системного (гуморального) иммунного ответа действие предлагаемого способа реализуется также на уровне подавления патологического очага путем прямой активации мононуклеаров крови (макрофагов). Известно, что возможно стимулировать макрофаги действием 5-аминофталгидразида («Галавита»), в основе стимулирующего действия может лежать механизм гиперпродукции супероксидного анион-радикала (Российский биотерапевтический журнал (2005) 4/4, 44-49. In vivo и In vitro индуцируемые эффекты Галавита на хемилюминесцентную активность мононуклеаров крови онкологических и неонкологических больных. А.Ф.Цыб, М.А.Каплан, В.Н.Петров, Л.И.Крикунова, В.Н.Медведев, И.А.Смирнова), являющегося также одним из возможных продуктов активации РХ волновой энергией. Активированные макрофаги действуют на опухолевые и бактериальные клетки либо цитотоксически, либо фагоцитарно. Их действие, однако, как и активированного ФС в предлагаемом способе, связывают с продукцией АФК, а также интерферона, интерлейкинов, фактора некроза опухолей, протеаз, гидролаз и пр. (цит. по ibid.).
Способ может быть применен для лечения онкологических заболеваний, повышает качество жизни и в 33% случаев может повысить операбельность опухоли (состояние пациентов после проведения процедуры значительно улучшилось, что позволило провести хирургическое удаление опухоли).
Существо изобретения можно пояснить следующими примерами. Использовалось лекарственное средство «Радахлорин», раствор для внутривенного введения, 0,35% (Регистрационное удостоверение № ЛС-001868 от 04.08.2006). Приведенные в способе ФС входят в состав данного лекарственного средства либо в качестве основных компонентов, либо в виде возможных примесных соединений.
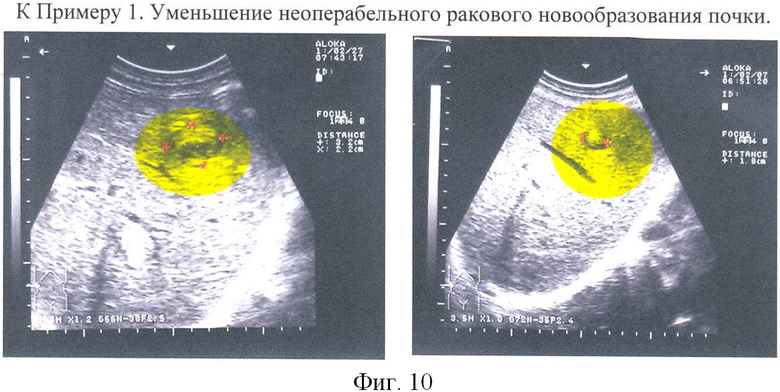
Пример 1. Онкологические заболевания. Способ показан для:
1. Пациентов в стадии рака Т3-Т4 при противопоказанности других методов лечения либо при рекомендации согласно стандартным протоколам только симптоматическго лечения;
2. Совмещения с проведением классической ФДТ с целью усиления эффекта;
3. Предоперационной подготовки при раке любой локализации и невозможности проведения классической ФДТ;
4. Абластики в послеоперационном периоде.
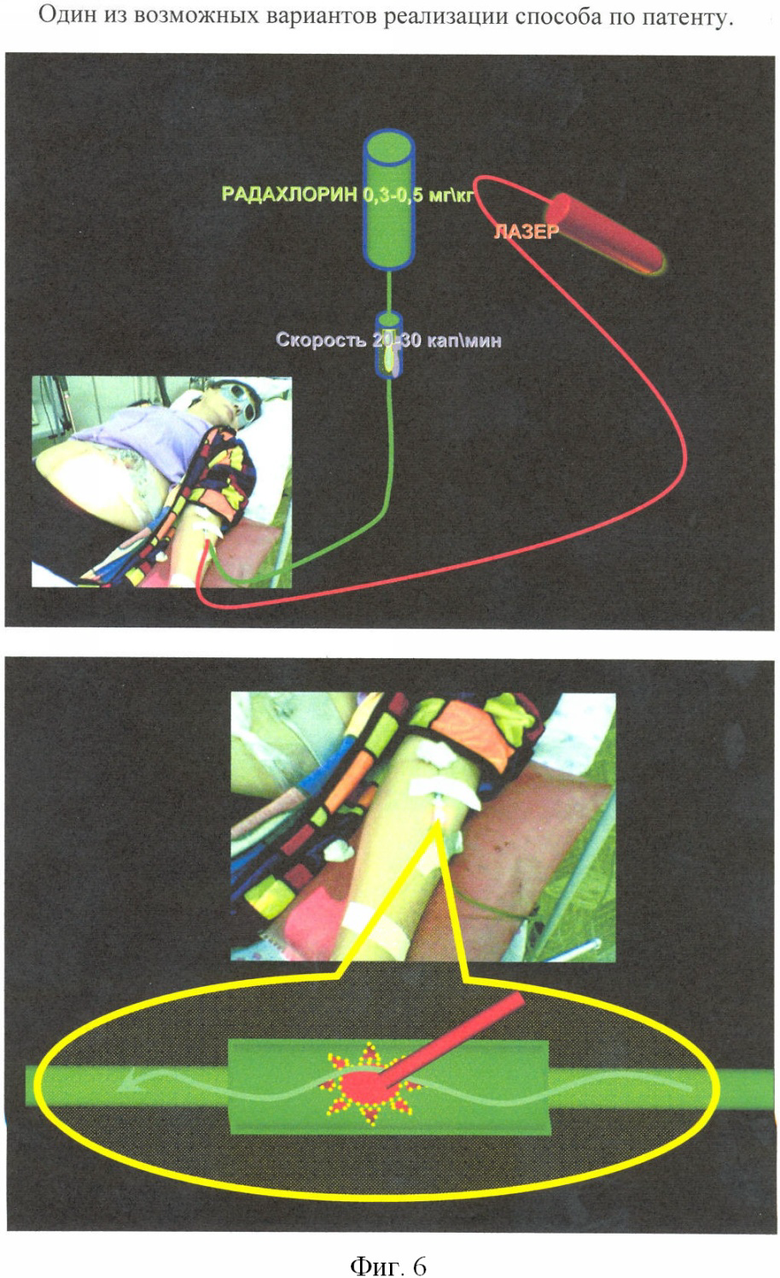
ФС в дозе 0,5 мг/кг разводится на 200,0 мл физиологического раствора и через капельницу подключается к периферической вене пациента стандартным способом. Скорость капельного введения составляет 40-60 кап./мин. Время капельного введения составляет 40-60 мин. Одновременно с началом капельного введения стерильный одноразовый световод вводится в просвет капельницы посредством пункции канюли иглы и осуществляется активация раствора ФС волновой энергией в присутствии кислорода.
Возможен также вариант активации непосредственно во флаконе с раствором ФС с последующим его инъекционым или инфузионным введением в организм пациента.
Фиг.6 и 7 демонстрируют реализацию способа в этом примере.
До, через 1-2 и 5-7 дней после проведения вышеуказанной процедуры пациентам производились лабораторные клинические исследования. Данные Табл.1 демонстрируют эффективность способа, изменения биохимических и клинических лабораторных показателей, свидетельствуя о его безопасности для состояния и транзиторности. В полном соответствии с концепцией фармакокинетики ФС отмечается повышение печеночных трансаминаз на 1-2 день и нормализация на 5-7 день, нормализация сахара в крови, транзиторное повышение билирубина.
В исследование включен 21 пациент с различными формами злокачественных опухолей. Всем пациентам показано симптоматическое лечение онкологами по разным причинам.
ФС активировали светом предварительно или одномоментно с его введением в организм источником волновой энергии - лазером - мощностью 0,1-20000 Вт, в дозе 1-100000 Дж в присутствии кислорода воздуха:
Пациенты 1-3: ФС активировали лазером с длиной волны 662 нм для хлорина с группами атомов 15-карбоксиметил- и 3-винил- (хлорин e6) мощностью 0,1 Вт в дозе 1 Дж в капельнице.
Пациенты 4-6: ФС активировали лазером с длиной волны 665 нм для хлорина с группами атомов 15-формил- и 3-винил- (пурпурин 5) мощностью 2 Вт в дозе 5000 Дж/мл во флаконе препарата.
Пациенты 7-9: ФС активировали лазером с длиной волны 635 нм мощностью 1 Вт в дозе 1000 Дж для хлоринов с группами атомов 3-винил- и

где R1 = атомы кислорода,
серы или NR,
R2=R или -COOR,
R = атом водорода или алкил
Пациенты 10-12: ФС активировали лазером с длиной волны 2500-4200 нм с импульсами длиной 0,5 мкс для композиции «Радахлорин», мощностью в импульсе 10000 Вт (пауза 3 мкс, суммарная продолжительность энергетического воздействия 100 мкс, продолжительность всего процесса активации 0,7 с) в дозе 1 Дж.
Пациенты 13-15: ФС активировали лазером с длиной волны 5000-6000 нм с импульсами длиной 0,5 мкс для композиции «Радахлорин», мощностью в импульсе 20000 Вт (пауза 3 мкс, суммарная продолжительность энергетического воздействия 5 с, продолжительность всего процесса активации 35 с) в дозе 100000 Дж.
Пациенты 16-18: ФС активировали лазером с длиной волны 662 нм для хлорина с группами атомов 15-карбоксиметил- и 3-винил- (хлорин е6) мощностью 2,5 Вт в дозе 25000 Дж (непрерывное излучение в течение 10000 с).
Пациенты 19-21: ФС активировали лазером с длиной волны 1750 нм для композиции «Радахлорин», мощностью 1 Вт в дозе 5000 Дж (импульс 1 с, пауза 1 с, время активации 5000 с, продолжительность облучения 10000 с).
Таблица 1 эффектов применения метода у 21 пациента демонстрирует наличие неполного эффекта в 33% случаев (уменьшение опухоли более чем на 50%) и частичного эффекта в 38% случаев (уменьшение опухоли менее чем на 50%). Таким образом, в 71% случаев получен положительный клинический эффект (улучшено качество жизни) у пациентов, которым в соответствии с общим состоянием и стандартами лечения онкологических заболеваний показано только «симптоматическое лечение» (то есть никакого лечения). В 33% случаев процедура позволила настолько улучшить клиническое состояние пациентов, что они были подвергнуты условно-радикальному хирургическому удалению опухоли.
Процедура не имеет осложнений, хорошо переносится.
Результаты были документированы рентгенограммами, фотографиями, данными УЗИ, историями болезни.
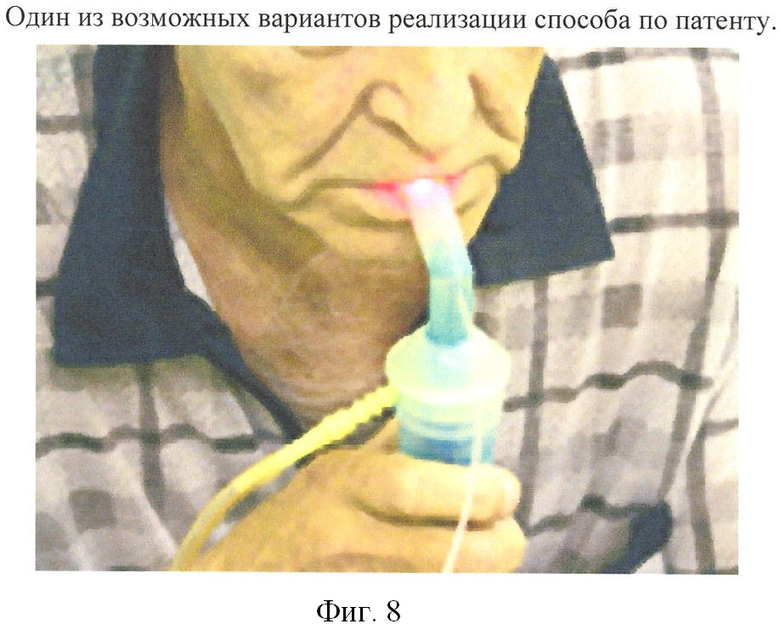
Пример 2. Туберкулез. ФС активировали лазером с длиной волны 662 нм с для композиции «Радахлорин», мощностью волнового излучения 2 Вт в дозе 1000 Дж в присутствии кислорода воздуха. Фиг.8 демонстрирует реализацию способа в этом примере.
Долговременным результатом лечения явилось торможение процессов развития легочного фиброза, что выявлено в течение 3-летнего наблюдения по сравнению с контрольной группой пациентов и что выражалось в отсутствии снижения основных показателей функции внешнего дыхания.
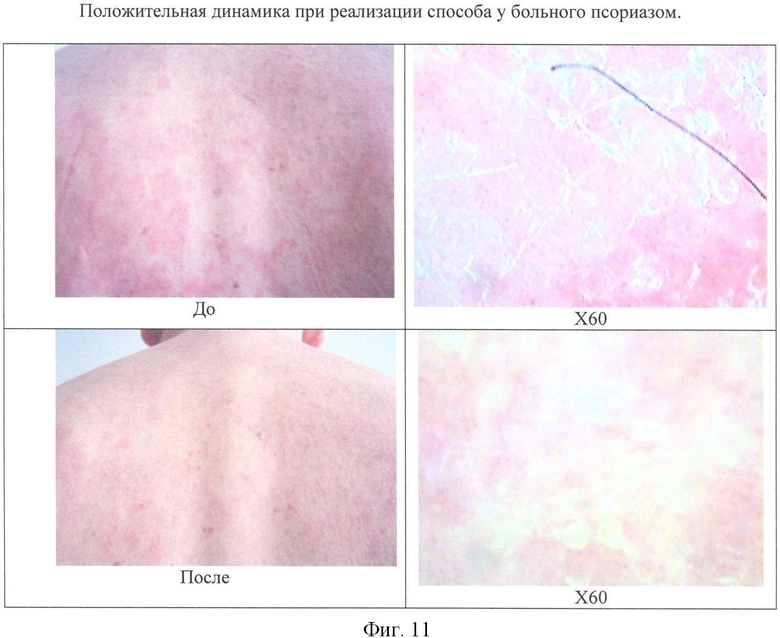
Пример 3. Псориаз. Пероральное введение ФС, активированного волновым излучением. В качестве ФС использовали БАД «Фотостим» (Регистрационное удостоверение МЗ РФ №005730.Р.643.04.2003), представляющий собой глицериновый раствор производного хлорофилла, содержащего вместе, в одном соединении, группы 3-винил-, 15-карбоксиметил-. Данный раствор ФС активировали во флаконе волновым излучением диодной лампы «Елан» с длиной волны 664 нм в присутствии кислорода воздуха плотностью мощности 12 мВт/см2 (расстояние 25 см) в течение 3600 с (световая доза 43,2 Дж). Пациент принимал активированный ФС по 5 мл в течение 20 дней. Через 10 дней приема отмечалось уменьшение инфильтрации и побледнение псориатических папул и бляшек. Через 1 мес наблюдалось уменьшение инфильтрации псориатических папул и бляшек, уменьшение шелушения и появление по периферии элементов псевдоатрофического венчика Воронова, что говорит о положительной динамике на фоне проводимого консервативного лечения (Фиг.11).
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ЛАЗЕРНОГО ЛЕЧЕНИЯ ХРОНИЧЕСКОГО ТОНЗИЛЛИТА С ПРИМЕНЕНИЕМ ФОТОСЕНСИБИЛИЗАТОРА | 2007 |
|
RU2379073C2 |
| СПОСОБ ФОТОДИНАМИЧЕСКОГО ЛЕЧЕНИЯ ОСТРОГО И ХРОНИЧЕСКОГО ГНОЙНОГО ГАЙМОРИТА | 2002 |
|
RU2228775C1 |
| ФОТОСЕНСИБИЛИЗАТОР И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2001 |
|
RU2183956C1 |
| СПОСОБ ЛЕЧЕНИЯ ВНУТРИГЛАЗНЫХ НОВООБРАЗОВАНИЙ БОЛЬШОГО РАЗМЕРА | 2005 |
|
RU2303965C2 |
| СПОСОБ ФОТОДИНАМИЧЕСКОЙ ТЕРАПИИ ВНУТРИГЛАЗНЫХ НОВООБРАЗОВАНИЙ | 2005 |
|
RU2290150C2 |
| СПОСОБ СНИЖЕНИЯ ПОВЕРХНОСТНОЙ ДОЗЫ ОФТАЛЬМОАППЛИКАТОРА ПРИ ПРОВЕДЕНИИ БРАХИТЕРАПИИ ВНУТРИГЛАЗНЫХ НОВООБРАЗОВАНИЙ | 2005 |
|
RU2303966C2 |
| СПОСОБ ФОТОДИНАМИЧЕСКОЙ ТЕРАПИИ И ЭЛЕКТРОХИМИЧЕСКОЙ ДЕСТРУКЦИИ МЕЛАНОМЫ ХОРИОИДЕИ | 2006 |
|
RU2303964C1 |
| СПОСОБ ФОТОДИНАМИЧЕСКОЙ ТЕРАПИИ И ХИРУРГИЧЕСКОГО УДАЛЕНИЯ МЕЛАНОМЫ ХОРИОИДЕИ | 2006 |
|
RU2305518C1 |
| СПОСОБ ПОДГОТОВКИ К ПЕРЕСАДКЕ РОГОВИЦЫ ПРИ ВАСКУЛЯРИЗИРОВАННЫХ БЕЛЬМАХ РОГОВИЦЫ | 2005 |
|
RU2299713C1 |
| СПОСОБ ЛЕЧЕНИЯ НЕОВАСКУЛЯРНОЙ ГЛАУКОМЫ | 2005 |
|
RU2289374C1 |


Изобретение относится к медицине и может быть использовано для фотоиммунотерапии фотосенсибилизатором, активируемым волновой энергией вне организма человека. Для этого в качестве ФС применяют производные хлорофилла. Активацию ФС светом проводят в присутствии кислорода предварительно или одномоментно с его введением в организм источниками волновой энергии. При этом мощность излучения 0,1-20000 Вт, доза 1-100000 Дж. Способ позволяет увеличить специфичность гуморального иммунного ответа, подавить патологический очаг, активировать обменные процессы в клетках, повысить уровень иммунной защиты организма в целом, повысить качество жизни, повысить операбельность опухоли. 2 з.п. ф-лы, 11 ил., 1 табл.
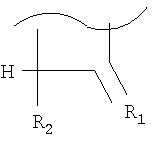
где R1 = атомы кислорода, серы или NR,
R2=R или -COOR,
R = атом водорода или алкил,
а активацию ФС светом проводят в присутствии кислорода предварительно или одномоментно с его введением в организм источниками волновой энергии мощностью 0,1-20000 Вт, в дозе 1-100000 Дж.
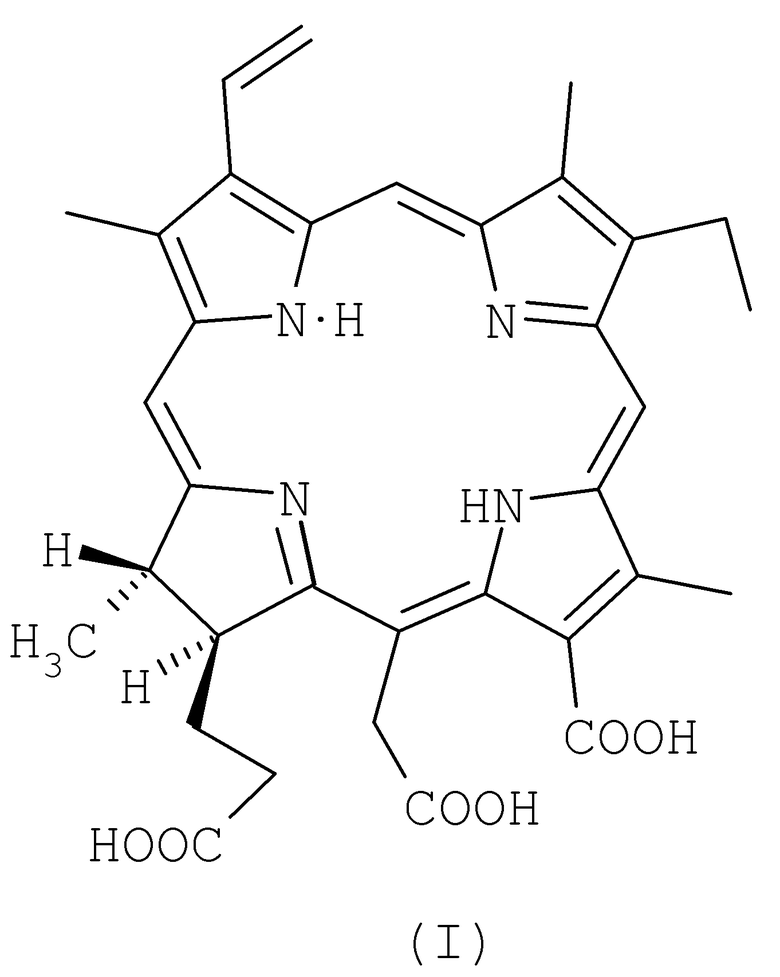
в количестве 80-90%, пурпурин 5 (13-карбокси-17-[2-карбоксиэтил]-15-формил-17,18-транс-дигидро-3-винил-8-этил-2,7,12,18-тетраметилпорфирин) (содержит группу 15-формил-)
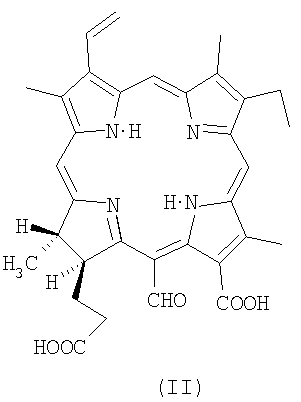
в количестве 5-20%, а также пурпурин 18-хлорин р6 (13-карбокси-17-[2-карбоксиэтил]-15-карбокси-17,18-транс-дигидро-3-винил-8-этил-2,7,12,18-тетраметилпорфирин)
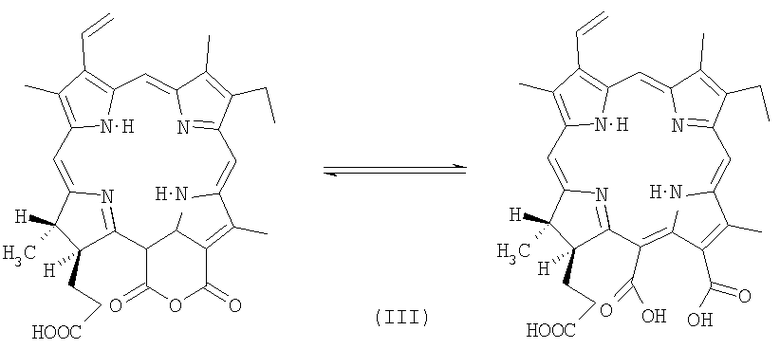
в количестве - остальное так, что указанные компоненты образуют композицию, а в лекарственных формах могут быть использованы их соли со щелочными металлами и азотосодержащими соединениями.
| ФОТОСЕНСИБИЛИЗАТОР И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2004 |
|
RU2276976C2 |
| ФОТОСЕНСИБИЛИЗАТОР И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2001 |
|
RU2183956C1 |
| СПОСОБ ТРАНСЭТЕРИФИКАЦИИ ДЛЯ ПОЛУЧЕНИЯ СИНТЕТИЧЕСКОГО ПРОИЗВОДНОГО ХЛОРОФИЛЛА ИЛИ БАКТЕРИОХЛОРОФИЛЛА | 2000 |
|
RU2250905C2 |
| RU 2000133104 A, 10.11.2002 | |||
| US 5330741 A, 19.07.1994 | |||
| СИПЛИВЫЙ В.И | |||
| Приспособление для точного наложения листов бумаги при снятии оттисков | 1922 |
|
SU6A1 |
| Вестник офтальмологии, 2005, т.121, №5, с.19-21 | |||
| GULLIYA | |||
Авторы
Даты
2009-02-10—Публикация
2006-11-30—Подача