ПРЕДПОСЫЛКИ ИЗОБРЕТЕНИЯ
Область изобретения
Изобретение относится к областям медицины, здравоохранения, иммунологии, молекулярной биологии и вирусологии.
Связанная область
Артериальное кровяное давление у млекопитающих контролируется по большей части биохимическим каскадом, известным как ренин-ангиотензиновая система (RAS). Он инициируется высвобождением ренина из эпителиоидных клеток юкстагломерулярного аппарата почки после падения артериального кровяного давления. Ренин ферментативно расщепляет пептид ангиотензиноген (аминокислотная последовательность: Asp-Arg-Val-Tyr-Ile-His-Pro-Phe-His-Leu-Val-Ile-His-Asn, SEQ ID NO: 15), который секретируется в сыворотку печенью. Данное расщепление приводит к образованию декапептида ангиотензина I (аминокислотная последовательность: Asp-Arg-Val-Tyr-Ile-His-Pro-Phe-His-Leu, SEQ ID NO: 16). Ангиотензин-превращающий фермент (АСЕ), который находится в эндотелии легких, за секунды отщепляет две С-концевые аминокислоты ATI с образованием ангиотензина II (аминокислотная последовательность: Asp-Arg-Val-Tyr-Ile-His-Pro-Phe, SEQ ID NO: 17). В то время как ангиотензин I является в организме очень короткоживущим и не имеет или имеет очень слабую сосудосуживающую активность, ангиотензин II оказывает сильное действие на систему циркуляции, а также на эндокринную систему. Повышенные концентрации активированного RAS ангиотензина II вызывают суживание сосудов, задержку почками солей и воды, причем оба данных эффекта вносят вклад в повышенное артериальное давление (гипертензию), которое может приводить к повреждению сердечно-сосудистой системы. Возможными клиническими проявлениями гипертензии являются инсульт, инфаркт, застойная сердечная недостаточность, почечная недостаточность или кровоизлияние в сетчатку.
Согласно данным U.S.Centers for Disease Control and Prevention (CDC), застойная сердечная недостаточность является основным хроническим заболеванием лиц старшего возраста и вызывает в США примерно 260000 смертей за год. В 1'995 г.из-за случаев сердечной недостаточности программой страхования здоровья (Medicare) было выплачено $3,4 миллиарда. Хотя для лечения гипертензии доступны лекарственные средства, контролировать гипертензию удается только примерно у половины подвергнутых лечению пациентов с гипертензией. Частично это является следствием отсутствия соблюдения больным режима и схем лечения или неэффективности использованных лекарственных средств.
Современное лечение гипертензии включает вмешательство в систему RAS с использованием небольших органических молекул. Основными мишенями являются ренин, АСЕ и рецепторы ангиотензина II. Ингибиторы АСЕ включают лизиноприл®, каптоприл® и эналаприл®, однако, данные лекарственные средства не являются полностью эффективными. Во-первых, оказывается, что они не полностью блокируют активность АСЕ, и, во-вторых, воздействию подвергается образование посредством АСЕ других биологически активных пептидов, включая брадикинин, что нежелательно. Данные лекарственные средства могут индуцировать побочные эффекты, такие как сухой кашель и гипотензивный эффект первой дозы с головокружением и возможным обмороком. Антагонисты рецептора ангиотензина II включают лозартан®, валсартан® и исбесафтан®, которые специфично воздействуют на рецептор ангиотензина ATI; поэтому они блокируют основные сосудосуживающие эффекты ангиотензина II и лучше переносятся, но не влияют на другие действия ангиотензиновых гормонов. Однако антагонисты рецептора ангиотензина, как и ингибиторы АСЕ, требуют приема на регулярной основе, часто в течение длительных периодов, таких как большая часть взрослой жизни, что, по крайней мере, частично объясняет плохое соблюдение больным режима и схем лечения. Поэтому существует явная потребность в лекарственных средствах для лечения гипертензии, которые были бы эффективными, хорошо бы переносились и сопровождались бы хорошим соблюдением больным режима и схем лечения.
Предполагаемый подход к лечению или профилактике заболеваний или нарушений, связанных с активностью гормона, представляет собой нейтрализацию эффектов гормона в организме пациента путем иммунотерапии, например, путем иммунизации пациента против данного гормона или ферментов, участвующих в его образовании, так что активность данного гормона нейтрализуется или его концентрации снижаются за счет специфических антител против гормона или фермента. Такие антитела могут вводиться путем пассивной иммунизации, или они могут генерироваться in situ путем активной иммунизации с использованием иммуногена, основанного на гормоне или связанном с ним ферменте.
Осуществимость вакцинации против компонентов RAS с целью модуляции гипертензии показана на экспериментальных животных (для обзора см. Michel, Am. Heart J. 117:756 (1989)). Вакцинация против ренина была эффективной для понижения кровяного давления, однако, животные страдали от аутоиммунного нефрита (Michel et al., Circulation 81:1899 (1990); Lo et al., Hypertension 16:80 (1990)). Количество данных по активной иммунизации против гомологичного АСЕ очень ограничено. В одном из сообщений описана вакцинация кроликов, но только 1 из 50 животных характеризовалось детектируемым уровнем антител против АСЕ (Softer, Fed. Proc. 42:2735 (1983)). Пассивный перенос иммунной сыворотки против АСЕ может снижать кровяное давление у кроликов, но ведет к иммуноаллергической реакции с отеком легким, возможно, поскольку АСЕ экспрессируется в мембраносвязанной форме в легких (Cadwell, FEBS Lett. 63:82 (1976)). Не доступны сообщения об активной иммунизации против ангиотензиногена, однако, в некоторых исследованиях анализировалась осуществимость вакцинации против ангиотензина-I и ангиотензина-II. В двух исследованиях сообщается об эффекте на кровяное давление (Christlieb, J. Clin. Invest. 48:1506 (1969); Gardiner, Br. J. Pharmacol. 129:1178 (2000)) у вакцинированных животных, и не отмечалось аутоиммунитета. Однако множество исследований по вакцинации ангиотензиновыми пептидами имели отрицательные результаты, возможно, потому что индуцированные титры антител против ангиотензиновых пептидов были слишком низкими, или потому что специфичность индуцированных антител не была оптимальной. Вероятно, что вакцина, которая направлена только на ангиотензин II, не имеет такого эффекта на RAS, как вакцина, которая индуцирует антитела против ангиотензина II, а также против ангиотензина I и, возможно, также против их предшественника ангиотензиногена.
В WO 98/58952 описано лечение конъюгатом, содержащим ангиотензин I, конъюгированный со столбнячным анатоксином, что ведет к индукции специфичных в отношении ангиотензина антител у крыс, при использовании совместно с адъювантом, таким как гидроксид алюминия. Адъюванты часто являются токсичными или по крайней мере вызывают раздражение. Из адъювантов для применения у человека разрешены только минеральные соли (гидроксид алюминия, фосфат алюминия, фосфат кальция) и виросомы. Чаще всего для людей используется адъювант гидроксид алюминия (алюминиевые квасцы). Хотя он считается безопасным, он остается в организме в течение длительного периода времени, характеризуясь депонированием. Последствия такого депонирования пока изучены слабо, поэтому в будущих вакцинах следует пробовать избегать применения алюминиевых квасцов без утраты иммуногенности вакцины.
Таким образом, в данной области сохраняется потребность в предоставлении конъюгатов, приводящих к индукции высоких титров антител даже в отсутствие адъювантов.
КРАТКОЕ ИЗЛОЖЕНИЕ СУЩНОСТИ ИЗОБРЕТЕНИЯ
В настоящее время авторы изобретения разработали мощные иммуногены для индукции антител, специфичных в отношении ангиотензиногена, ангиотензина I или ангиотензина II (совместно обозначенных здесь, как «ангиотензиновые пептиды»), которые эффективны даже без применения адъювантов и которые обеспечивают in vivo продукцию антител, которые специфично направлены на один или несколько ангиотензиновых пептидов, таких как ангиотензиноген, ангиотензин I или ангиотензин II. Иммуногены состоят из ангиотензиновых пептидных составляющих, которые связаны с вирусоподобными частицами (VLP). Это приводит к образованию высокоиммуногенного повторяющегося антигенного мотива, способного стимулировать образование антител даже без применения адъювантов. В зависимости от аминокислотной последовательности использованных ангиотензиновых пептидных составляющих индуцируются высокие титры антител, и, более того, они могут специфично индуцироваться против N- или С-концов ангиотензиногена, ангиотензина I или ангиотензина II. Это обеспечивает специфичную направленность против только одного вида ангиотензиновых пептидов или их комбинации. Таким образом, иммуногены по настоящему изобретению могут использоваться в иммунотерапевтическом подходе для борьбы с состояниями, ассоциированными с повышенными концентрациями ангиотензина II, продуцированного RAS.
Данные конъюгаты и конъюгаты по изобретению могут индуцировать антитела, которые связываются более чем с одним видом ангиотензиновых пептидов, одновременно блокируя таким образом все близкие ангиотензины, причем не подразумевается, что это явление ограничено какой-либо конкретной теорией действия или механизма. Альтернативно, индуцированные антитела могут специфично связываться с С-концом ангиотензиногена, ангиотензина I или ангиотензина II. В данных условиях, индуцированные антитела блокируют активацию ангиотензиногена или ангиотензина I ренином или АСЕ, соответственно. Тем не менее, протеазы, отличные от АСЕ или ренина, такие как эндопептидазы и аминопептидазы, могут разрушать ангиотензиноген, ангиотензин I или ангиотензин II с N-конца, предотвращая таким образом накопление связанного с антителом интактного ангиотензиногена, ангиотензина I или ангиотензина II.
Таким образом, по изобретению предоставлены иммуногены, которые содержат один или несколько ангиотензиновых пептидов или пептидных составляющих или их производных, связанных с одной или несколькими коровыми частицами, предпочтительно, с одной или несколькими вирусоподобными частицами (VLP) с образованием конъюгатов, имеющих структуру упорядоченных или повторяемых мотивов. Коровые частицы, содержащие один участок связывания, и ангиотензиновые пептиды или их производные, содержащие второй участок связывания, ассоциированы через указанные первый и второй участки связывания с образованием таких упорядоченных или повторяемых мотивов. Взаимодействие между первым и вторым участками может быть непосредственным, или в нем может участвовать, по крайней мере, одна другая молекула, например, линкер.
В одном из осуществлений первый участок связывания присущ коровой частице от природы. Альтернативно, первый участок связывания добавляется путем химического присоединения или с использованием рекомбинантных способов. Предпочтительные первые участки связывания содержат аминогруппы, карбоксильные группы или сульфгидрильные группы. Предпочтительные аминокислоты, содержащие второй участок связывания, выбраны из лизина, аргинина, цистеина, аспарагиновой кислоты, глутаминовой кислоты, тирозина и гистидина. Особенно предпочтительными являются остатки лизина.
Подходящими вторыми участками связывания на ангиотензиновых пептидах или их производных являются амин, амид, карбоксильная или сульфгидрильная группы. Имеется много разнообразных соединений, которые были разработаны для обеспечения перекрестного связывания пептидов/белков или конъюгации белка с дериватизированными молекулами путем образования ковалентной связи с реакционноспособной группой белковой молекулы коровой частицы.
Коровые частицы с первым участком связывания по изобретению включают любую частицу, подходящую для образования упорядоченных повторяющихся мотивов. В некоторых осуществлениях такие коровые частицы включают вирусоподобные частицы (VLP), бактериофаг, частицы, подобные вирусу бактериофагу, пили, и тому подобное. В некоторых осуществлениях они представляют собой VLP из HBcAg, бактериофаговые VLP и пили I типа. Изобретение также относится к вариантным формам коровых частиц, которые сохраняют способность образовывать упорядоченную повторяющуюся структуру. Вариантные формы включают рекомбинантные и природные формы, и мутантные формы коровых частиц. В некоторых осуществлениях мутантные формы коровых частиц включают те, в которых тип первого участка связывания или некоторого количества указанных участков отличается от первоначального. Особенно предпочтительным является изменение числа остатков лизина на коровой частице.
В некоторых осуществлениях конъюгаты по изобретению содержат ангиотензиновые пептидные составляющие, которые химически связаны с вирусоподобными частицами (VLP). Это приводит к образованию высокоиммуногенного повторяющегося мотива антигенов, который способен стимулировать образование антител даже без применения адъювантов. В зависимости от аминокислотной последовательности применяемых ангиотензиновых пептидных составляющих индуцируются высокие титры антител, и, более того, они могут специфично индуцироваться против N- или С-концов ангиотензиногена, ангиотензина I или ангиотензина II. Это обеспечивает специфичную направленность против только одного вида ангиотензиновых пептидов или их комбинации. Иммуногены по изобретению могут использоваться в иммунотерапевтическом подходе для борьбы с состояниями, ассоциированными с повышенными концентрациями ангиотензина II, продуцированного RAS.
Таким образом, настоящее изобретение относится к конъюгатам, содержащим коровую частицу и один или несколько ангиотензиновых пептидов или ангиотензиновых пептидных составляющих, подходящих для применения при индукции иммуных ответов. Изобретение также относится к конъюгатам, включающим такие конъюгаты по изобретению и один или несколько дополнительных компонентов, таких как один или несколько наполнителей или носителей, предпочтительно, один или несколько фармацевтически приемлемых наполнителей или носителей. Конъюгаты и конъюгаты по изобретению включают вакцинные конъюгаты или конъюгаты с дополнительными фармацевтически приемлемыми наполнителями или адъювантами, или без них. Например, настоящее изобретение также относится к вакцинным конъюгатам, содержащим иммунологически эффективное количество одного или нескольких данных конъюгатов или конъюгатов по настоящему изобретению вместе с фармацевтически приемлемым разбавителем, носителем или наполнителем. В дальнейшем осуществлении вакцина, кроме того, содержит по крайней мере, один адъювант, такой как алюминиевые квасцы или неполный адъювант Фрейнда. Изобретение также относится к способам иммунизации и/или лечения животного, предпочтительно, млекопитающего, такого как человек, предусматривающим введение данному животному иммунологически эффективного количества конъюгатов, конъюгатов или вакцин по изобретению с индукцией таким образом иммунного ответа против данных конъюгатов. Животных можно подходящим образом иммунизировать данными конъюгатами или конъюгатами по изобретению любым известным в данной области путем введения, включая, в качестве не ограничивающих примеров, подкожный, внутримышечный, интраназальный, внутрикожный, внутривенный, чрескожный, пероральный пути введения, введение через слизистые оболочки или введение непосредственно в лимфатический узел. Интраназальная иммунизация представляет собой особенно подходящий путь; данный тип введения не только приводит к образованию высоких титров антител, включая IgA, как это показано в примерах, но также за счет избежания болезненных процедур иммунизации (например, внутримышечной) является более приемлемым для пациента и ведет к улучшенному соблюдению больным режима и схем лечения.
Конъюгаты и конъюгаты по изобретению индуцируют иммунный ответ, включая продукцию антител. Поэтому еще в одном осуществлении данное изобретение относится к способам продукции антител против одного или нескольких ангиотензиновых пептидов или ангиотензиновых пептидных составляющих. Такие антитела по изобретению могут использоваться для лечения или профилактики физических нарушений, ассоциированных с RAS, и для детекции ангиотензиновых пептидов или ангиотензиновых пептидных составляющих, например, в способах диагностики физических нарушений, ассоциированных с присутствием одного или нескольких компонентов RAS в тканях или циркуляторном русле животного.
В связанных осуществлениях изобретение относится к профилактике или лечению заболеваний, нарушений или состояний ассоциированных с RAS, включая, в качестве не ограничивающих примеров, инсульт, инфаркт, застойную сердечную недостаточность, почечную недостаточность, кровоизлияние в сетчатку и тому подобное. Иммунизация данными конъюгатами или конъюгатами по изобретению приводит к иммунному ответу против одного или нескольких ангиотензиновых пептидов или ангиотензиновых пептидных составляющих, так что иммунные молекулы, особенно антитела, связываются с ангиотензиновыми пептидами или с ангиотензиновыми пептидными составляющими. Пассивный перенос антител также может использоваться для лечения и профилактики нарушений, ассоциированных с RAS.
Авторами настоящего изобретения обнаружено, что конъюгаты ангиотензиновых пептидов или ангиотензиновых пептидных составляющих, присоединенных к вирусоподобным частицам (VLP), индуцируют высокоспецифичные в отношении ангиотензина антитела IgG. Поэтому настоящее изобретение относится к терапевтическому средству лечения физических нарушений, ассоциированных с RAS, которое в особо предпочтительном осуществлении основано на упорядоченных и повторяемых конъюгатах VLP-ангиотензиновый пептид/составляющая. Данное терапевтическое средство способно индуцировать высокие титры антиангиотензиновых антител у вакцинированного животного. Высокие титры антител индуцируются даже в отсутствие адъювантов и охватывают не только субтип IgG, но также субтип IgA. Более того, неожиданно данное терапевтическое средство не ассоциировано с индукцией потенциально патогенного иммунного ответа, такого как воспаление. Терапевтические конъюгаты по изобретению содержат, по крайней мере, один ангиотензиновый пептид или ангиотензиновую пептидную составляющую и VLP, предпочтительно VLP РНК-фага, или, по крайней мере, ангиотензиновый пептид или ангиотензиновую пептидную составляющую и альтернативную коровую частицу, такую как HBcAg или пили.
Другие осуществления настоящего. изобретения будут понятны обычному специалисту в свете имеющейся в данной области информации, следующих чертежей и описания изобретения, а также формулы изобретения.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
Фигура 1 представляет собой анализ методом ELISA антител IgG, специфичных в отношении пептида Angio 1 и ангиотензина II, в сыворотке мышей, иммунизированных пептидами Angio 1, Angio 2, Angio 3 или Angio 4, конъюгированными с белком капсида Qβ.
Фигура 2 представляет собой анализ методом ELISA антител IgG, специфичных в отношении пептида Angio 2 и ангиотензина I, в сыворотке мышей, иммунизированных пептидами Angio 1, Angio 2, Angio 3 или Angio 4, конъюгированными с белком капсида Qβ.
Фигура 3 представляет собой анализ методом ELISA антител IgG, специфичных в отношении пептида Angio 1 и ангиотензина II, в сыворотке мышей, иммунизированных пептидами Angio 5, Angio 6, Angio 7, Angio 8 или Angio 9, конъюгированными с белком капсида Qβ.
Фигура 4 представляет собой анализ методом ELISA антител IgG, специфичных в отношении пептида Angio 2 и ангиотензина I, в сыворотке мышей, иммунизированных пептидами Angio 5, Angio 6, Angio 7, Angio 8 или Angio 9, конъюгированными с белком капсида Qβ.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Определения
В последующем описании интенсивно используется ряд терминов, используемых в области молекулярной биологии, иммунологии и медицины. Для обеспечения более ясного и непротиворечивого понимания описания и формулы изобретения, включая объем, в котором даны такие термины, предоставлены следующие не ограничивающие определения.
Активная иммунизация. Используемый в данном описании термин «активная иммунизация» относится к индукции иммунного ответа у субъекта, обычно животного, вызванной введением иммуногена, вакцины, антигена или конъюгата ангиотензиновый пептид-носитель. Пассивная иммунизация, наоборот, означает обеспечение у субъекта иммунитета путем переноса указанному субъекту иммунных молекул или клеток.
Альфавирус. Используемый в данном описании термин «альфавирус» относится к любому из РНК-вирусов, входящих в состав рода Alphavirus. Описание представителей данного рода содержится в Strauss and Strauss, Microbiol. Rev., 58:491-562 (1994). Примеры альфавирусов включают вирус Аура, вирус Бебару, вирус Кабассу, вирус Чикунгунья, вирус восточного энцефаломиелита лошадей, вирус Форт-Морган, вирус Гета, вирус Кызыл-Агача, вирус Майоаро, вирус Миддлебурга, вирус Мукамбо, вирус Ндуму, вирус Пиксуна, вирус Тонате, вирус Тринити, вирус Уна, вирус западного энцефаломиелита лошадей, вирус Уатароа, вирус Синдбис (SIN), вирус леса Семлики (SFV), вирус венесуэльского энцефаломиелита лошадей (VEE) и вирус Росс-Ривер.
Аминокислотный линкер. «Аминокислотный линкер», также называемый в данной.спецификации «линкером», при использовании в данном описании осуществляет ассоциацию антигена или антигенной детерминанты со вторым участком связывания, или, более предпочтительно, уже включает или содержит второй участок связывания, обычно, но необязательно, в виде одного аминокислотного остатка, предпочтительно, остатка цистеина. Используемый в данном описании термин «аминокислотный линкер», однако, не подразумевает, что данный аминокислотный линкер состоит исключительно из аминокислотных остатков, даже если аминокислотный линкер, состоящий из аминокислотных остатков, является предпочтительным осуществлением по настоящему изобретению. Аминокислотные остатки аминокислотного линкера, предпочтительно, состоят из встречающихся в природе аминокислот или неприродных аминокислот, известных в данной области, полностью из L-аминокислот или полностью из D-аминокислот, или их смесей. Однако аминокислотный линкер, содержащий молекулу с сульфгидрильной группой или остаток цистеина, также относится к настоящему изобретению. Такая молекула предпочтительно содержит С1-С6-алкильную, циклоалкильную (С5, С6), арильную или гетероарильную группу. Однако, в дополнение к аминокислотному линкеру, линкер, предпочтительно содержащий C1-С6-алкильную, циклоалкильную (С5, С6), арильную или гетероарильную группу и не содержащий какой(-их)-либо аминокислоты(-т), также будет входить в объем настоящего изобретения. Ассоциация между антигеном или антигенной детерминантой или, необязательно,.вторым участком связывания и аминокислотным линкером, предпочтительно, осуществляется посредством, по крайней мере, одной ковалентной связи, более предпочтительно, посредством, по крайней мере, одной пептидной связи.
Ангиотензиновая пептидная составляющая. Используемый в данном описании термин «ангиотензиновая пептидная составляющая» относится к любой составляющей, независимо от того, имеет или нет данная составляющая биологическую активность нативного ангиотензина in vivo (например, природную гормональную активность в отношении рецепторов, включая ангиотензин I и II), которая способна действовать как иммуномиметик природных ангиотензиновых пептидов (т.е. которая иммунологически имитирует ангиотензин, так что генерируются антитела, которые связываются с нативными ангиотензиновыми пептидами). Таким образом, данная составляющая может подходящим образом содержать ангиотензиновый пептид, предпочтительно, ангиотензиноген, ангиотензин I (декапептид формулы Asp-Arg-Val-Tyr-Ile-His-Pro-Phe-His-Leu, SEQ ID NO: 16) или ангиотензин II (октапептид формулы Asp-Arg-Val-Tyr-Ile-His-Pro-Phe, SEQ ID NO: 17), или его функционально эквивалентный вариант. Следовательно, «ангиотензиновая пептидная составляющая» охватывает «ангиотензиновый пептид», как данный термин определен в данном описании. Такие функционально эквивалентные варианты могут включать модификации последовательности ангиотензина I или II с единичной или множественными аминокислотными заменами, добавлениями или делециями, и также последовательности, где аминокислотные остатки химически модифицированы, но которые, несмотря на это, сохраняют иммуногенную активность ангиотензина. Такие функционально (или иммунологически) эквивалентные варианты могут иметь место как природные биологические вариации, или они могут быть получены с использованием известных и стандартных способов, например, химического синтеза или модификации, мутагенеза, например, сайт-специфического или случайного мутагенеза, и т.д. Для целей данного определения ключевой чертой, касающейся модификации, является то, что ангиотензиновый пептид сохраняет способность действовать как иммуномиметик нативного ангиотензина. Так, например, аминокислота может быть замещена другой, которая сохраняет физико-химическую характеристику ангиотензинового пептида или его эпитопа(-ов), например, в плане плотности заряда, гидрофильности/гидрофобности, размера и конфигурации, и потому сохраняет иммунологическую структуру. Варианты «добавления» могут включать N- или С-концевые приращения, а также вставки внутри последовательности одной или нескольких аминокислот. Делеции могут иметь место внутри последовательности или могут представлять собой укорочения с N- или С-концов. Предпочтительными мутантными формами с делецией являются те, что обеспечивают индукцию антител против N- или, предпочтительно, С-конца. Такие антитела могут предотвращать образование активного ангиотензина II, но при этом оставлять возможность для деградации связанного с антителом ангиотензиногена, ангиотензина I или ангиотензина II.
Ангиотензиновый пептид. Используемый в данном описании термин «ангиотензиновый пептид» охватывает все, предпочтительно природные, ангиотензиновые пептиды и их функционально эквивалентные варианты. Следовательно, «ангиотензиновый пептид» может считаться подмножеством термина «ангиотензиновая пептидная составляющая», как это определено в данном описании. На практике, определение того, является ли данный вариант ангиотензинового пептида (или ангиотензиновой пептидной составляющей) «функциональным эквивалентом», предпочтительно, нативного ангиотензинового пептида, может осуществляться разнообразными способами анализа для определения биологической активности ангиотензинового пептида. Некоторые из данных способов анализа описаны здесь, а другие хорошо известны обычному специалисту в данной области.
Антитело. Используемый в данном описании термин «антитело» относится к молекулам, способным связываться с эпитопом или антигенной детерминантой. Подразумевается, что данный термин охватывает целые антитела и их антигенсвязывающие фрагменты, включая одноцепочечные антитела. Такие антитела включают антигенсвязывающие фрагменты антител человека и охватывают, в качестве неограничивающих примеров, Fab, Fab' и F(ab')2, Fd, одноцепочечные Fv (scFv), одноцепочечные антитела, связанные дисульфидной связью Fv (sdFv) и фрагменты, содержащие VL- или VH-домен. Антитела могут происходить из любого животного, включая птиц и млекопитающих. Предпочтительно, антитела происходят от млекопитающих, например, из человека, мыши, кролика, козы, морской свинки, верблюда, лошади и тому подобного, или других подходящих животных, таких как куры. Используемый в данном описании термин «человеческие» антитела охватывают антитела, характеризующиеся аминокислотной последовательностью человеческого иммуноглобулина, и охватывают антитела, выделенные из библиотек имуноглобулинов человека или из животных, трансгенных по одному или нескольким человеческим иммуноглобулинам и не экспрессирующих эндогенные иммуноглобулины, как описано, например в патенте США № 5939598, описание которого включено сюда полностью в качестве ссылки.
Антиген. Используемый в данном описании термин «антиген» относится к молекуле, способной связываться с антителом или с Т-клеточным рецептором (TCR), если презентируется молекулами МНС. Используемый в данном описании термин «антиген» также охватывает Т-клеточные эпитопы. Т-клеточный эпитоп распознается Т-клеточным рецептором в связи с МНС класса I, который присутствует на всех клетках организма кроме эритроцитов, или с МНС класса II, присутствующим на клетках иммунной системы и, в частности, на антигенпредставляющих клетках. Данное событие распознавания ведет к активации Т-клеток и последующему запуску эффекторных механизмов, таких как пролиферация Т-клеток, секреция цитокинов, секреции перфоринов и т.д. Кроме того, антиген способен распознаваться иммунной системой и/или способен индуцировать гуморальный иммунный ответ и/или клеточный иммунный ответ, что ведет к активации В- и/или Т-лимфоцитов. Это, однако, по крайней мере в некоторых случаях может требовать того, чтобы антиген содержал или был связанным с эпитопом ТH-клеток и был представлен в адъюванте. Антиген может содержать один или несколько эпитопов. (В- и Т-эпитопов). Специфическая в отношении антигена реакция означает, что антиген предпочтительно взаимодействует с соответствующим ему антителом или TCR, обычно высокоселективным образом, и не взаимодействует с множеством других антител или TCR, которые могут индуцироваться другими антигенами. Используемые здесь антигены также могут представлять собой смесь различных индивидуальных антигенов.
Антигенная детерминанта. Подразумевается, что используемый в данном описании термин «антигенная детерминанта» относится к той части антигена, которая специфично распознается В- или Т-лимфоцитами. В-лимфоциты реагируют на чужеродные антигенные детерминанты путем продукции антител, в то время как Т-лимфоциты являются медиаторами клеточного иммунитета. Таким образом, антигенные детерминанты или эпитопы являются теми частями антигена, которые распознаются антителами или, в связи с МНС, Т-клеточными рецепторами. Антигенная детерминанта содержит один или несколько эпитопов. Аллергены также служат в качестве антигенов у позвоночных животных.
Ассоциация. Используемый в данном описании термин «ассоциация» в применении к первому и второму участкам связывания относится к связыванию с первым и вторым участками связывания, которое предпочтительно осуществляется посредством, по крайней мере, одной непептидной связи. Природа ассоциации может быть ковалентной, ионной, гидрофобной, полярной, или представлять собой любую их комбинацию, предпочтительно, природа ассоциации является ковалентной.
Участок связывания, первый. Используемое в данном описании выражение «первый участок связывания» относится к элементу коровой частицы природного или неприродного происхождения, с которым может ассоциировать второй участок связывания, локализованный на антигене или антигенной детерминанте. Первый участок связывания может представлять собой белок, полипептид, аминокислоту, пептид, сахар, полинуклеотид, природный или синтетический полимер, вторичный метаболит или соединение (биотин, флуоресцеин, ретинол, дигоксигенин, ионы металлов, фенилметилсульфонилфторид), или их комбинацию, или их химическую реакционноспособную группу. Первый участок связывания обычно и предпочтительно локализован на поверхности коровой частицы, предпочтительно, такой как вирусоподобная частица. Множественные первые участки связывания присутствуют на поверхности коровой и вирусоподобной частицы, соответственно, обычно в повторяемой конфигурации.
Участок связывания, второй. Используемое в данном описании выражение «второй участок связывания» относится к элементу, ассоциированному с антигеном или антигенной детерминантой, с которым может ассоциировать первый участок связывания, локализованный на поверхности коровой частицы и вирусоподобной частицы, соответственно. Второй участок связывания антигена или антигенной детерминанты может представлять собой белок, полипептид, пептид, сахар, полинуклеотид, природный или синтетический полимер, вторичный метаболит или соединение (биотин, флуоресцеин, ретинол, дигоксигенин, ионы металлов, фенилметилсульфонилфторид), или их комбинацию, или их химическую реакционноспособную группу. По крайней мере, один второй участок связывания присутствует на антигене или антигенной детерминанте. Термин «антиген или антигенная детерминанта с, по крайней мере, одним вторым участком связывания», таким образом, относится к антигену или антигенной конструкции, содержащим, по крайней мере, антиген или антигенную детерминанту и второй участок связывания. Однако, в особенности для второго участка связывания неприродного происхождения, т.е. он не встречается в данном антигене или антигенной детерминанте в природе, данный антиген или антигенная конструкция содержат «аминокислотный линкер».
Связанный. Используемый в данном описании термин «связанный» относится к связыванию или присоединению, которое может быть ковалентным, например, образованным путем химического связывания, или нековалентным, например, представлять собой ионные взаимодействия, гидрофобные взаимодействия, водородные связи и т.д. Ковалентные связи могут быть, например, сложноэфирными, эфирными, фосфоэфирными, амидными, пептидными, имидными, связями между углеродом и серой, связями между углеродом и фосфором, и тому подобным. Термин «связанный» охватывает такие термины, как «объединенный», «слитый» и «присоединенный», и шире их.
Покровный(-ые) белок(-и). Используемый в данном описании термин «покровный(-ые) белок(-и)» относится к белку(-ам) бактериофага или РНК-фага, способному(-ым) включаться в состав капсида бактериофага или РНК-фага при его сборке. Однако, при ссылке на конкретный генный продукт гена покровного белка РНК-фагов используется термин «СР». Например, конкретный генный продукт гена покровного белка РНК-фага Qβ указывается как «СР Qβ«, причем «покровные белки» бактериофага Qβ включают «СР Qβ«, а также белок А1. Капсид бактериофага Qβ в основном составлен из СР Qβ, с небольшим содержанием белка А1. Сходным образом, покровный белок VLP Qβ состоит главным образом из СР Qβ с небольшим содержанием белка А1.
Коровая частица. Используемый в данном описании термин «коровая частица» относится к ригидной структуре с присущей ей повторяемой организацией. Коровая частица, как этот термин используется в данном описании, может являться продуктом синтетического процесса или продуктом биологического процесса.
Эффективное количество. Используемый в данном описании термин «эффективное количество» относится к количеству, необходимому или достаточному для реализации требуемого биологического эффекта. Эффективное количество композиции является тем количеством, с которым достигается выбранный результат, и такое количество может быть определено в порядке рутинной работы специалиста в данной области. Например, эффективное количество для лечения иммунодефицита может быть тем количеством, которое необходимо для активации иммунной системы, что приведет к развитию антигенспецифического иммунного ответа после воздействия антигена. Данный термин также синонимичен термину «достаточное количество».
Эффективное количество для любого конкретного применения может варьировать в зависимости от таких факторов, как заболевание или состояние, подлежащее лечению, конкретная композиция, подлежащая введению,. размер субъекта и/или тяжесть заболевания или состояния. Обычный специалист в данной области может эмпирически определить эффективное количество конкретной композиции по настоящему изобретению без необходимости избыточного экспериментирования.
Эпитоп. Используемый в данном описании термин «эпитоп» относится к основному элементу или наименьшей единице распознавания индивидуальным антителом или Т-клеточным рецептором и, таким образом, к конкретному домену, области или молекулярной структуре, с которой связывается указанное антитело или Т-клеточный рецептор. Антиген может состоять из множества эпитопов, в то время как гаптен обычно может содержать мало эпитопов.
Слияние. Используемый в данном описании термин «слияние» относится к комбинации аминокислотных последовательностей различного происхождения в одну полипептидную цепь путем комбинации в одну рамку считывания кодирующих их нуклеотидных последовательностей. Термин «слияние» без сомнения охватывает внутренние слияния, т.е. вставки последовательностей другого происхождения в полипептидную цепь, в дополнение к слиянию с одного из ее концов.
Гетерологичная последовательность. Используемый в данном описании термин «гетерологичная последовательность» относится к второй последовательности нуклеиновой кислоты или белка, которая в норме не находится в указанной нуклеиновой кислоте или белке, и обычно искусственно добавлена к данной последовательности для наделения ее определенными свойствами. В одном из примеров гетерологичные аминокислоты могут быть добавлены к рекомбинантным капсидным белкам для целей очистки белка, или для функционирования в качестве первого участка связывания.
Иммунный ответ. Используемый в данном описании термин «иммунный ответ» относится к любому действию иммунной системы субъекта, которое направлено против некоторой молекулы или соединения, таких как антиген. У млекопитающих иммунный ответ включает активности клеток и продукцию растворимых молекул, таких как цитокины и антитела. Таким образом, данный термин включает гуморальный иммунный ответ и/или клеточный иммунный ответ, которые ведут к активации или пролиферации В- и/или Т-лимфоцитов. Однако в некоторых осуществлениях иммунные ответы могут быть мало интенсивными и подлежат детекции лишь с использованием по крайней мере одного соединения по настоящему изобретению. «Иммуногенное средство» относится к средству, используемому для стимуляции иммунной системы живого организма, так что одна или несколько функций иммунной системы усиливаются и направляются на иммуногенное средство. «Иммуногенный полипептид» представляет собой полипептид, который вызывает клеточный и/или гуморальный иммунный ответ, сам по себе, или в связи с носителем в присутствии или в отсутствие адъюванта.
Иммунная девиация. Используемый в данном описании термин иммунная девиация относится к стимуляции иммунного ответа иной природы по сравнению с предсуществующим иммунным ответом. Например, у субъекта, характеризующегося иммунным ответом ТH2 против аллергена, так что продуцируются антитела IgE после воздействия данного аллергена, по осуществлениям настоящего изобретения может индуцироваться развитие иммунного ответа ТH1 против данного аллергена. Такой ответ ТH1 будет противодействовать индуцирующему аллергию ответу ТH2 и таким образом будет облегчать течение аллергического заболевания.
Средство иммунотерапии. Используемый в данном описании термин «средство иммунотерапии» относится к конъюгату для лечения заболеваний, нарушений или состояний. Более конкретно, данный термин используется для ссылки на способ лечения, где благоприятный иммунный ответ генерируется вакцинацией.
Иммунологически эффективное количество. Используемый в данном описании термин «иммунологически эффективное количество» относится к количеству конъюгата, достаточному для индукции у субъекта иммунного ответа, при введении его данному субъекту. Количество конъюгата, достаточное для того, чтобы оно было иммунологически эффективным, варьирует в зависимости от многих факторов, включая конъюгат, наличие других компонентов конъюгата (например, адъювантов), антиген, путь иммунизации, субъект, предсуществующий иммунный или физиологический статус, и т.д.
Выделенный. При использовании в данном описании термина «выделенный» в отношении молекулы данный термин означает, что молекула удалена из своего природного окружения. Например, полинуклеотид или полипептид, встречающийся в природе в живом организме, не является «выделенным», но тот же полинуклеотид или полипептид, отделенный от сосуществующих с ним в природном состоянии веществ, является «выделенным». Далее, молекулы рекомбинантной ДНК, содержащиеся в векторе, считаются выделенными для целей настоящего изобретения. Выделенные молекулы РНК включают продукты РНК-репликации in vivo или in vitro молекул ДНК и РНК. Выделенные молекулы нуклеиновой кислоты кроме того включают синтетически продуцированные молекулы. Кроме того, векторные молекулы, содержащиеся в рекомбинантных клетках хозяина, также являются выделенными. Таким образом, не все «выделенные» молекулы должны быть «очищенными».
Средство иммунотерапии. Используемый в данном описании термин «средство иммунотерапии» относится к конъюгату, который содержит иммунные молекулы и/или вызывает иммунный ответ, для лечения заболеваний или нарушений.
Субъект. Используемый в данном описании термин «субъект» относится к многоклеточным организмам и включает как растения, так и животные. Предпочтительными многоклеточными организмами являются животные, более предпочтительно, позвоночные, даже более предпочтительно, млекопитающие и, наиболее предпочтительно, люди.
Низкий или не подлежащий детекции. Используемое в данном описании выражение «низкий или не подлежащий детекции» при использовании в отношении к уровню генной экспрессии относится к уровню экспрессии, который значительно ниже того, который наблюдается при максимальной индукции данного гена (например, по крайней мере, в пять раз ниже), или не подлежит легкой детекции способами, использованными в последующем разделе примеров.
Лектин. Используемый в данном описании термин «лектин» означает белки, полученные, в частности, из семян бобовых растений, но также из многих разных растительных и животных источников, в которых имеются участки связывания для специфичных моно- и олигосахаридов. Примеры включают конканавалин А и агглютинин зародыша пшеницы, которые широко используются в качестве аналитических и препаративных средств при изучении гликопротеина.
Мимеотоп. Используемый в данном описании термин «мимеотоп» относится к веществу, которое индуцирует иммунный ответ на антиген или антигенную детерминанту. В общем, термин «мимеотоп» используется со ссылкой на конкретный антиген. Например, пептид, который вызывает продукцию антител к фосфолипазе А2 (PLA2), представляет собой мимеотоп антигенной детерминанты, с которой связываются данные антитела. Мимеотоп может обладать существенным структурным сходством или проявлять структурные характеристики антигена или антигенной детерминанты, иммунный ответ на которые он индуцирует, а может и не характеризоваться этим. Способы получения и идентификации мимеотопов, которые индуцируют иммунные ответы к конкретным антигенам или антигеннным детерминантам, известны в данной области и описаны здесь в другом месте.
Мутеин. Используемый в данном описании термин «мутеин» относится к белку или полипептиду, отличающемуся одной или несколькими аминокислотами от заданного полипептида сравнения (например, природного, дикого типа и т.д.).
Природное происхождение. Используемый в данном описании термин «природное происхождение» означает, что целый компонент или его часть не являются синтетическими и существуют или продуцируются в природе. Предпочтительно, используемый в данном описании термин «природное происхождение» означает, что целый компонент не является синтетическим и существует или продуцируется в природе.
Неприродный. Используемый в данном описании термин в основном означает нечто, возникшее не в природе, более конкретно, данный термин означает нечто, созданное руками человека.
Неприродный молекулярный каркас. Используемая в данном описании фраза «неприродный молекулярный каркас» относится к любому продукту, созданному руками человека, который служит, обеспечивая ригидный и повторяющийся мотив первых участков связывания. В идеале, но не обязательно, данные первые участки связывания находятся в геометрическом порядке. Неприродный молекулярный каркас может быть органическим или неорганическим и может синтезироваться химически или в биологическом процессе, частично или полностью. Неприродный молекулярный каркас состоит из (а) коровой частицы природного или неприродного происхождения; и (b) по крайней мере одного первого участка связывания. Используемый в данном описании термин «неприродное происхождение» в основном означает нечто, возникшее не в природе или синтетически, более конкретно, данный термин означает нечто, созданное руками человека.
Упорядоченный и повторяемый мотив антигенов или антигенных детерминант. Используемый в данном описании термин «упорядоченный и повторяемый мотив антигенов или антигенных детерминант» в основном относится к повторяющейся структуре антигенов или антигенных.детерминант, обычно и предпочтительно характеризующейся однородным пространственным расположением антигенов или антигенных детерминант по отношению к коровой частице и вирусоподобной частице, соответственно. В одном из осуществлений изобретения повторяющаяся структура может представлять собой геометрическую структуру. Типичными и предпочтительными примерами подходящих упорядоченных и повторяемых мотивов антигенов и антигенных детерминант являются те, которые характеризуются строго повторяемым паракристаллическим упорядочиванием антигенов или антигенных детерминант, предпочтительно с разбивкой по 0,5-30 нанометров, предпочтительно, 5-15 нанометров.
Пассивная иммунизация. Используемый в данном описании термин «пассивная иммунизация» относится к введению животному любым путем продуцированных зкзогенно иммунных молекул (например, антител) или клеток (например, Т-клеток). Пассивная иммунизация отличается от «активной» иммунизации, где иммунитет достигается путем введения субъекту иммуногена, вакцины, антигена или конъюгата гаптен-носитель, чтобы вызвать иммунный ответ.
Пили. Используемый в данном описании термин «пили» («пиль» в единственном числе) относится к внеклеточным структурам бактериальных клеток, состоящим из белковых мономеров (например, мономеров пилина), которые организованы в упорядоченные и повторяемые структуры. Кроме того, пили представляют собой структуры, вовлеченные в такие процессы, как присоединение бактериальной клетки к поверхностному рецептору клетки-хозяина, генный обмен между клетками и распознавание клетка-клетка. Примеры пилей включают пили 1 типа, Р-пили, F1C-пили, S-пили и 987Р-пили. Дополнительные примеры пилей приведены здесь в другом месте.
Структура, подобная пилям. Используемое в данном описании выражение «структура, подобная пилям» относится к структурам, имеющим характеристики, сходные с таковыми пилей, и составленным из мономеров белка. Одним из примеров «структуры, подобной пилям» является структура, образованная бактериальной клеткой, которая экспрессирует модифицированные белки пилины, не образующие упорядоченные и повторяемые мотивы, по существу идентичные таковым природных пилей.
Полипептид. Используемый в данном описании термин «полипептид» относится к полимеру, состоящему из аминокислотных остатков, в основном, из природных аминокислотных остатков, связанных вместе через пептидные связи. Полипептид не обязательно может быть ограничен по длине и охватывает как белки, так и пептиды. Пептид представляет собой полипептид размером обычно от пяти до примерно 50 аминокислот, или состоит из любого количества аминокислот в данном общем интервале. Однако пептид может быть более длинным, например, до 120-150 аминокислот.
Белок. Используемый в данном описании термин белок относится к полипептиду размером, в общем, превышающим примерно 5 или более, 10 или более, 20 или более, 25 или более, 50 или более, 75 или более, 100 или более, 200 или более, 500 или более, 1000 или более, 2000 или более аминокислот. Белки в основном характеризуются определенной трехмерной структурой, хотя и не обязательно, и они часто обозначаются, как обладающие укладкой, в отличие от пептидов или полипептидов, которые зачастую не обладают определенной трехмерной структурой, но вместо этого могут принимать большое количество различных конформаций, и обозначаются как не имеющие укладки. Однако пептиды могут также обладать определенной трехмерной структурой.
Очищенный. Когда используемый в данном описании термин «очищенный» используется в отношении молекулы, это означает, что концентрация подлежащей очистке молекулы повышена по сравнению с молекулами, ассоциированными с ней в ее природном окружении, или в окружении, в котором она была продуцирована, обнаружена или синтезирована. Встречающиеся в природе молекулы включают белки, нуклеиновые кислоты, липиды и сахара, но обычно не включают воду, буферы и реагенты, добавленные для поддержания целостности или обеспечения очистки указанной молекулы. Например, даже если мРНК растворяют в водном растворе во время колоночной хроматографии на олиго-dT, молекулы мРНК очищаются данной хроматографией, если встречающиеся в природе нуклеиновые кислоты и другие биологические молекулы не связываются с колонкой и отделяются от указанных молекул мРНК. По данному определению вещество может быть чистым на 5% или более, на 10% или более, на 20% или более, на 30% или более, на 40% или более, на 50% или более, на 60% или более, на 70% или более, на 80% или более, на 90% или более, на 95% или более, на 98% или более, на 99% или более, или на 100%, при рассмотрении относительно примесей к нему.
Рецептор. Используемый в данном описании термин «рецептор» относится к белкам или гликопротеинам, или их фрагментам, способным взаимодействовать с другой молекулой, называемой лигандом. Лиганд может принадлежать к любому классу биохимических или химических соединений. Рецептор не обязательно является мембраносвязанным белком. Растворимые белки, например, такие как мальтозосвязывающий белок или ретинолсвязывающий белок, также являются рецепторами.
Остаток. Используемый в данном описании термин «остаток» означает конкретную аминокислоту в полипептидном остове или боковой цепи.
Рекомбинантная клетка-хозяин. Используемый в данном описании термин «рекомбинантная клетка-хозяин» относится к клетке-хозяину, в которую введены одна или несколько молекул нуклеиновой кислоты по настоящему изобретению. Клетки-хозяева включают эукариотические клетки, например, клетки млекопитающих, насекомых, растений, птиц, дрожжей; и прокариотические клетки, например, Е. coli, B. subtilis и т.д.
Рекомбинантный вирус. Используемое в данном описании выражение «рекомбинантный вирус» относится к вирусу, который генетически модифицирован руками человека. Данное выражение охватывает любой вирус, известный в данной области. Более конкретно, выражение относится к альфавирусу, генетически модифицированному руками человека, и наиболее конкретно, выражение относится к вирусу Синдбис, генетически модифицированному руками человека.
РНК-фаг. Используемый в данном описании термин «РНК-фаг» относится к РНК-вирусам, инфицирующим бактерии, более конкретно, к одноцепочечным РНК-вирусам с плюс-цепью, инфицирующим бактерии.
Вектор. Используемый в данном описании термин «вектор» относится к средству (например, плазмиде или вирусу), используемому для переноса генетического материала в клетку-хозяина. Вектор может быть составлен из ДНК или РНК.
Вирусоподобная частица (VLP). Используемый в данном описании термин «вирусоподобная частица» относится к структуре, напоминающей вирусную частицу. Более того, вирусоподобная частица по данному изобретению не способна к репликации и неинфекционна вследствие того, что она лишена вирусного генома или его части, в особенности, его компонентов, относящихся к репликации и инфекции. Вирусоподобная частица по изобретению может содержать нуклеиновую кислоту, отличную от ее генома. Типичное и предпочтительное осуществление вирусоподобной частицы по настоящему изобретению представляет собой вирусный капсид, такой как вирусный капсид соответствующего вируса, бактериофага или РНК-фага. Термины «вирусный капсид» или «капсид», используемые в данном описании взаимозаменяемо, относятся к комплексу макромолекул, составленному из вирусных белковых субъединиц. Типично и предпочтительно вирусные белковые субъединицы объединяются в вирусный капсид, и капсид, соответственно, характеризуется структурой с присущей ему повторяемой организацией, где указанная структура обычно является сферической или трубчатой. Например, капсиды РНК-фагов или HBcAg имеют сферическую форму с икосаэдрической симметрией. Используемый в данном описании термин «капсидоподобная структура» относится к макромолекулярному комплексу, составленному из вирусных белковых субъединиц, напоминающему капсид по морфологии в определенном выше смысле, но отклоняющемуся от структуры обычного симметричного комплекса при сохранении существенной степени упорядоченности и повторяемости.
Вирусоподобная частица бактериофага. Используемый в данном описании термин «вирусоподобная частица бактериофага» относится к вирусоподобной частице, по структуре напоминающей бактериофаг, являющейся не способной к репликации, неинфекционной и лишенной, по крайней мере, гена или генов, кодирующих механизм репликации бактериофага, и обычно также лишенной гена или генов, кодирующих белок или белки, ответственные за присоединение вируса к клетке-хозяину или проникновение в нее. Данное определение, однако, также охватывает вирусоподобные частицы бактериофагов, в которых указанные выше ген или гены пока присутствуют, но являются неактивными, что поэтому также ведет к образованию нереплицирующихся и неинфекционных вирусоподобных частиц бактериофага.
VLP из покровного белка РНК-фага. Капсидная структура, образованная из самопроизвольного объединения 180 субъединиц покровного белка РНК-фага и необязательно содержащая РНК хозяина, обозначается как «VLP из покровного белка РНК-фага». Конкретным примером является VLP из покровного белка Qβ. В данном конкретном случае VLP из покровного белка Qβ может образовываться исключительно из субъединиц СР Qβ (генерируемых путем экспрессии гена СР Qβ, содержащего, например, стоп-кодон ТАА, препятствующий какой-либо экспрессии более длинного белка А1 путем супрессии, см. Kozlovska, Т.М., et al., Intervirology 39: 9-15 (1996)), или может дополнительно содержать субъединицы белка А1 при сборке капсида.
Вирусная частица. Используемый в данном описании термин «вирусная частица» относится к морфологической форме вируса. В некоторых типах вирусов она содержит геном, окруженный белковым капсидом, другие имеют дополнительные структуры (например, оболочки, отростки и т.д.).
Один. Когда в данном описании используется выражение «один», оно означает «по крайней мере, один» или «один или несколько», кроме случаев, когда это обозначено иначе.
При использовании в данном описании ссылки на любое численное значение термин «примерно» означает интервал ±10% от установленного значения (например, «примерно 50°С» охватывает интервал температур от 4°С до 55°С включительно; сходным образом, «примерно 100 мМ» охватывает интервал концентраций от 90 мМ до 110 мМ включительно).
Обзор
В настоящее время авторами разработаны мощные иммуногены для индукции антител, специфичных в отношении ангиотензиновых пептидов, которые эффективны даже без применения адъювантов и которые могут обеспечить специфичное воздействие на ангиотензиноген, ангиотензин I или ангиотензин II. Данные иммуногены состоят из ангиотензиновых пептидных составляющих, которые связаны с вирусоподобными частицами (VLP) или другими коровыми частицами, такими как бактериальные пили или подобные пилям частицы. Это приводит к получению высокоиммуногенного повторяемого мотива антигенов, который способен стимулировать образование антител даже без применения адъювантов. В зависимости от аминокислотной последовательности использованных ангиотензиновых пептидных составляющих индуцируются высокие титры антител, и, более того, они могут индуцироваться специфично против N- или С-концов ангиотензиногена, ангиотензина I или ангиотензина II. Это обеспечивает специфичное воздействие только на один вид ангиотензиновых пептидов или на их комбинацию. Иммуногены по настоящему изобретению могут, таким образом, использоваться в иммунотерапевтическом подходе для борьбы с состояниями, ассоциированными с повышенными концентрациями ангиотензиновых пептидных составляющих, особенно ангиотензина II и его производных, продуцируемых RAS.
Получение конъюгатов по изобретению, т.е. связывание одной или нескольких ангиотензиновых пептидных составляющих с коровой частицей (например, VLP), достигается путем присоединения, фиксации, слияния или другого типа связывания, включая ковалентные и нековалентные связи. В одном из осуществлений VLP содержит первый участок связывания, органическая молекула содержит второй участок связывания. Ассоциация с органической молекулой происходит путем непосредственного соединения первого и второго участков связывания, или их соединения посредством третьей молекулы. Участки связывания могут иметь место в природе или могут быть введены.
Иммунизация животных конъюгатами ангиотензиновых пептидных составляющих и коровых частиц или конъюгатами, содержащими такие конъюгаты по изобретению, индуцируют сильный иммунный ответ на экспонированные ангиотензиновые пептидные составляющие. Следовательно, данные конъюгаты и конъюгаты по изобретению могут использоваться для стимуляции иммунного ответа против различных ангиотензиновых пептидных составляющих или их производных и, таким образом, для применения у животных. Настоящее изобретение также относится к вакцине, включающей иммунологически эффективное количество одного или нескольких конъюгатов или конъюгатов по настоящему изобретению вместе с фармацевтически приемлемым разбавителем, носителем или наполнителем. Конъюгаты и конъюгаты по настоящему изобретению могут использоваться для вакцинирования животных против одной или нескольких ангиотензиновых пептидных составляющих или их производных. Вакцинация может осуществляться для профилактических и терапевтических целей, или для обеих. В связанном аспекте для лечения, профилактики или диагностики заболевания, состояния или нарушения могут использоваться иммунные молекулы, такие как антитела, генерированные против таких конъюгатов или конъюгатов. Такие антитела, конъюгаты и конъюгаты по изобретению также могут использоваться в качестве компонентов для наборов.
Таким образом, в одном из аспектов настоящего изобретение относится к конъюгатам одной или нескольких ангиотензиновых пептидных составляющих с носителем в конъюгате упорядоченная и повторяющаяся ангиотензиновая пептидная составляющая - носитель и к способам получения таких конъюгатов. Изобретение также относится к конъюгатам, включающим по крайней мере один такой конъюгат по изобретению и, по крайней мере, один другой компонент, подходящим образом, по крайней мере, один наполнитель или носитель и, в частности, по крайней мере один фармацевтически приемлемый наполнитель или носитель. Конъюгаты и конъюгаты по изобретению могут использоваться для индукции иммунного ответа против ангиотензиновых пептидных составляющих. Такой иммунный ответ может использоваться для получения антител, которые применяются для терапевтических, профилактических и диагностических целей.
Конъюгаты по настоящему изобретению содержат высоко упорядоченные и повторяемые мотивы одной или нескольких ангиотензиновых пептидных составляющих. Мотивы конъюгатов по данному аспекту изобретения включают (а) коровую частицу, содержащую первый участок связывания и (b) ангиотензиновую пептидную составляющую, содержащую второй участок связывания, где элементы (а) и (b) ассоциированы через первый и второй участки связывания с образованием указанных упорядоченных и повторяемых мотивов ангиотензиновых пептидных составляющих.
Коровые частицы, подходящим образом используемые в данных конъюгатах и конъюгатах по изобретению, могут быть природными и неприродными. Природные коровые частицы, используемые в данных конъюгатах и конъюгатах по изобретению, включают вирусные частицы, вирусоподобные частицы и пили. Белки данных природных коровых частиц могут быть природными или рекомбинантными. Первые участки связывания на коровых частицах могут иметь место в природе или могут вводиться химическими или рекомбинантными средствами. Ангиотензиновые пептидные составляющие, используемые в данных конъюгатах и конъюгатах по изобретению, являются теми, которые подходят для индукции иммунного ответа против различных компонентов RAS (т.е. различные ангиотензиновые пептидные составляющие или их производные), включая в качестве не ограничивающих примеров ангиотензиновый пептид, предпочтительно, те, что содержат или, альтернативно, состоят из последовательности ангиотензиногена, ангиотензина I (декапептид формулы Asp-Arg-Val-Tyr-Ile-His-Pro-Phe-His-Leu, SEQ ID NO: 16) или ангиотензина II (октапептид формулы Asp-Arg-Val-Tyr-Ile-His-Pro-Phe, SEQ ID NO: 17), или ее фрагментов, или ее функционально эквивалентных вариантов, включая ангиотензиновые пептидные составляющие, упоминаемые в другом месте описания. Второй участок связывания на ангиотензиновой пептидной составляющей может иметь место в природе или быть введен. Взаимодействие между первым и вторым участками может быть непосредственным, или может включать, по крайней мере, одну молекулу, например, линкер. Более того, перекрестно связывающие молекулы могут использоваться по настоящему изобретению для ассоциации первого и второго участков связывания. Перекрестно связывающие молекулы обычно используются в дополнение к линкеру.
Конъюгаты и конъюгаты по изобретению являются неожиданно эффективными для индукции иммунного ответа, особенно антител, против различных ангиотензиновых пептидных составляющих. Таким образом, они могут использоваться в конъюгатах, подходящих для иммунизации животных для терапии или профилактики заболеваний, нарушений или состояний, ассоциированных с RAS, включая в качестве неограничивающих примеров гипертензию, инсульт, инфаркт, застойную сердечную недостаточность, почечную недостаточность или геморрагию сетчатки. Антитела, продуцируемые путем иммунизации конъюгатами и конъюгатами по изобретению, также могут использоваться для терапевтических и профилактических целей.
В других осуществлениях изобретение относится к способам лечения и профилактики заболевания, задействующим конъюгаты и конъюгаты по изобретению. Еще в одном осуществлении настоящее изобретение относится к наборам, подходящим для диагностики и скрининга.
Конъюгаты упорядоченных и повторяемых мотивов
Настоящее изобретение относится к конъюгатам и конъюгатам конъюгатов, содержащим упорядоченный и повторяемый мотив одной или нескольких ангиотензиновых пептидных составляющих. Более того, настоящее изобретение подходящим образом позволяет специалисту-практику конструировать упорядоченные и повторяемые мотивы для различных целей и, предпочтительно, индуцировать иммунный ответ против одной или нескольких ангиотензиновых пептидных составляющих или их производных.
Конъюгаты по настоящему изобретению по существу содержат, или, альтернативно, состоят из двух элементов: (1) неприродный молекулярный каркас и (2) по крайней мере, одна ангиотензиновая пептидная составляющая, по крайней мере, одним вторым участком связывания, способным к ассоциации посредством, по крайней мере, одной связи с указанным первым участком связывания.
Неприродный молекулярный каркас содержит или, альтернативно, состоит из: (а) коровой частицы, выбранной из группы, состоящей из (1) коровой частицы неприродного происхождения и (2) коровой частицы природного происхождения; и (b) по крайней мере, одного первого участка связывания, соединенного с указанной коровой частицей, по крайней мере, одной ковалентной связью. Коровые частицы, используемые в конъюгатах, конъюгатах и способах изобретения, включают неорганические молекулы, вирусные частицы, вирусоподобные частицы и бактериальные пили. Ангиотензиновые пептидные составляющие, используемые в конъюгатах, конъюгатах и способах изобретения, имеют, по крайней мере, один второй участок связывания, который выбран из группы, состоящей из (а) участка связывания, не встречающегося в природе в ангиотензиновой пептидной составляющей; и (b) участка связывания, не встречающегося в природе в ангиотензиновой пептидной составляющей.
Настоящее изобретение относится к упорядоченному и повторяемому мотиву путем ассоциации второго участка связывания с первым участком связывания путем, по крайней мере, одной связи. Таким образом, ангиотензиновая пептидная составляющая и неприродный молекулярный каркас объединены за счет данной ассоциации первого и второго участка связывания с образованием упорядоченного и повторяемого антигенного мотива.
Специалист-практик может специфично сконструировать ангиотензиновую пептидную составляющую и второй участок связывания, так что расположение всех составляющих, связанных с неприродным молекулярным каркасом или, в некоторых осуществлениях, с коровой частицей, будет однородным. Например, можно поместить единственный второй участок связывания на ангиотензиновую пептидную составляющую, обеспечивая таким конструированием то, что все ангиотензиновые пептидные составляющие, которые присоединены к неприродному молекулярному каркасу, позиционированы однородным путем. В одном из таких аспектов настоящего изобретения одну или несколько дополнительных аминокислот (приводящих к образованию не встречающегося в природе второго участка связывания) добавляют с С- или N-конца последовательностей ангиотензиновых пептидных составляющих, в частности, для обеспечения ориентированной и упорядоченной ассоциации с коровой частицей по настоящему изобретению. Таким образом, изобретение относится к удобному средству размещения любой ангиотензиновой пептидной составляющей на неприродном молекулярном каркасе в определенном порядке и способом, который образует повторяемую структуру.
Как будет ясно обычным специалистам в данной области, конкретные осуществления изобретения включают применение технологий рекомбинантной нуклеиновой кислоты, таких как клонирование, полимеразная цепная реакция, очистка ДНК и РНК, экспрессия рекомбинантных белков в прокариотических и эукариотических клетках и т.д. Такие методологии хорошо известны специалистам в данной области и могут подходящим образом обнаруживаться в опубликованных руководствах по лабораторным методам (например, Sambrook, J. et al., eds., MOLECULAR CLONING, A LABORATORY MANUAL, 2nd. edition, Cold Spring Harbor Laboratory Press, Cold Spring Harbor, N.Y. (1989); Ausubel, F. - et al., eds., CURRENT PROTOCOLS IN MOLECULAR BIOLOGY, John H. Wiley & Sons, Inc. (1997)). Основные лабораторные методы для работы с культурами ткани клеточных линий (Celis, J., ed., CELL BIOLOGY, Academic Press, 2nd edition, (1998)), и основанные на антителах технологии (Harlow, E. and Lane, D., «Antibodies: A Laboratory Manual,» Cold Spring Harbor Laboratory, Cold Spring Harbor, N.Y. (1988); Deutscher, M.P., «Guide to Protein Purification», Meth. Enzymol. 128, Academic Press San Diego (1990); Scopes, R.K., «Protein Purification Principles and Practice», 3 ed., Springer-Verlag, New York (1994)) также адекватно описаны в литературе, все источники которой включены сюда в качестве ссылки.
Более того, технологии присоединения органических молекул к аминокислотам и средства для получения производных ангиотензиновых пептидных составляющих, содержащих подходящие вторые участки связывания, такие как участки, необходимые для воплощения изобретения, хорошо известны специалистам в данной области. Такие методологии могут быть найдены в книгах по химии и публикациях, примеры которых приведены ниже и включены сюда в качестве ссылки; патент США № 5876727; WO 99/61054; Isomura, S. et al. J. Org. Chem. 66: 4115-4121 (2001); Matsushita, H. et al. Biochem. Biophys. Res. Comm. 57: 1006-1010. (1974); Langone, J.L. and Van Vunakis, H., Methods Enzymol. 84: 628-640 (1982); Wong, Chemistry of Protein Conjugation and Cross-Linking. CRC Press, Inc., Boca Raton, Fla (1991).
Коровые частицы и неприродные молекулярные каркасы
В одном из осуществлений настоящее изобретение относится к способам получения упорядоченного и повторяемого мотива одного или нескольких ангиотензиновых пептидных составляющих. По изобретению это осуществляется путем ассоциации коровой частицы, к которой присоединяется один или несколько ангиотензиновых пептидных составляющих посредством первого и второго участков связывания.
Таким образом, одним из элементов конкретных конъюгатов и конъюгатов по настоящему изобретению является неприродный молекулярный каркас, содержащий или, альтернативно, состоящий из коровой частицы и первого участка связывания. Более конкретно, неприродный молекулярный каркас содержит или, альтернативно, состоит из (а) коровой частицы природного или неприродного происхождения и (b) по крайней мере, одного первого участка связывания, присоединенного к коровой частице по крайней мере одной ковалентной связью.
Коровые частицы. В одном из осуществлений настоящего изобретения коровая частица представляет собой синтетический полимер, жидкую мицеллу или металл. Такие коровые частицы известны в данной области, что обеспечивает основу, на которой строится новый неприродный молекулярный каркас по изобретению. Например, коровые частицы из синтетического полимера или из металла описаны в патенте США № 5770380 и патенте США № 5334394, которые включены сюда полностью в качестве ссылки. Подходящие металлы включают в качестве не ограничивающих примеров хром, рубидий, железо, цинк, селен, никель, золото, серебро, платину. Подходящие керамические материалы включают в качестве не ограничивающих примеров диоксид кремния, диоксид титана, оксид алюминия, оксид рутения и оксид олова. Коровые частицы по данному осуществлению могут состоять из органических материалов, охватывающих в качестве не ограничивающих примеров углерод и подходящие полимеры, включая полистирол, нейлон и нитроцеллюлозу. В случае надокристаллических частиц могут использоваться частицы, состоящие из оксида олова, диоксида титана или углерода (алмаза). Липидные мицеллы для применения по настоящему изобретению получают любыми средствами, известными в данной области; например, по Baiselle and Millar (Biophys. Chem. 4:355-361 (1975)), или Corti et al. (Chem. Phys. Lipids 38:197 - 214 (1981)), или Lopez et al. (FEBS Lett. 426:314-318 (1998)), или Topchieva and Karezin (J. Colloid Interface Sci. 213:29-35 (1999)), или Morein et al, (Nature 308: 457-460 (1984)), которые включены сюда полностью в качестве ссылки.
В одном из осуществлений изобретения коровая частица продуцируется в биологическом процессе, который может быть природным и неприродным. Например, вирусы и бактериальные пили или структуры, подобные пилям, образуются из белков, которые организованы в повторяемые и упорядоченные структуры. Поэтому настоящее изобретение относится к конъюгатам, конъюгатам и способам, включающим пригодные коровые частицы, которые включают в качестве не ограничивающих примеров вирус, вирусоподобную частицу, бактериальный пиль, фаг, вирусную капсидную частицу и их фрагменты. В некоторых таких осуществлениях белки могут быть рекомбинантными.
В некоторых осуществлениях коровая частица неприродного молекулярного каркаса включает вирус, бактериальный пиль, структуру, образованную из бактериального пилина, бактериофаг, вирусоподобную частицу, вирусную капсидную частицу или их рекомбинантную форму. Любой вирус, известный в данной области, характеризующийся упорядоченной и повторяемой структурой покровных и/или коровых белков, может быть выбран для применения по данным способам, в конъюгатах и в конъюгатах по изобретению в качестве неприродного молекулярного каркаса. Не ограничивающие примеры подходящих вирусов охватывают вирус Синдбис и другие альфавирусы, рабдовирусы (например, вирус везикулярного стоматита), пикорнавирусы (например, человеческий риновирус, вирус Аичи), тогавирусы (например, вирус краснухи), ортомиксовирусы (например, вирус Тогото, вирус Баткен, вирус чумы домашней птицы), полиомавирусы (например, полиомавирус ВК, полиомавирус JC, птичий полиомавирус BFDV), парвовирусы, ротавирусы, бактериофаг Qβ, бактериофаг R17, бактериофаг М11, бактериофаг МХ1, бактериофаг NL95, бактериофаг fr, бактериофаг GA, бактериофаг SP, бактериофаг MS2, бактериофаг f2, бактериофаг РР7, бактериофаг АР205, вирус Норволк, вирус ящура, ретровирус, вирус гепатита В, вирус табачной мозаики, вирус Флок-Хауз и человеческий папилломавирус (например, см. таблицу 1 в Bachman, М.F. and Zinkernagel, R.M., Immunol. Today 17: 553-558 (1996)). В более конкретных типовых осуществлениях настоящего изобретения коровая частица может содержать или, альтернативно, состоять из рекомбинантных белков ротавируса, рекомбинантных белков вируса Норволк, рекомбинантных белков альфавируса, рекомбинантных белков, которые образуют бактериальные пили или подобные пилям структуры, рекомбинантных белков вируса ящура, рекомбинантных белков ретровируса, рекомбинантных белков вируса гепатита В (например, HBcAg), рекомбинантных белков вируса табачной мозаики, рекомбинантных белков вируса Флок-Хауз и рекомбинантных белков человеческого папилломавируса.
Коровая частица, используемая в конъюгатах, конъюгатах и способах по изобретению, может, кроме того, содержать или, альтернативно, состоять из одного или нескольких фрагментов таких белков, а также вариантов таких белков, которые сохраняют способность ассоциировать друг с другом с образованием упорядоченных и повторяемых мотивов антигенов или антигенных детерминант. Например, как описано в принадлежащей настоящим заявителям ожидающей решения заявке на выдачу патента США № 10/050902 (поданной 18 января 2002 г., и ее описание включено сюда полностью в качестве ссылки), коровые частицы могут быть образованы из вариантных форм человеческого HBcAg, которые заметно отличаются от частицы дикого типа по идентичности и сходству аминокислотной последовательности и по длине последовательности. Например, аминокислотная последовательность HBcAg вирусов гепатита В, которые инфицируют снежных гусей и уток, существенно отличается от таковой HBcAg вирусов, инфицирующих млекопитающих, так что затруднено выравнивание данных белков. Однако оба вируса сохраняют способность к формированию коровых структур, подходящих для образования упорядоченных повторяемых мотивов антигенов. Сходным образом, HBcAg может сохранять способность образовывать мультимерные частицы, обычно вирусные, после удаления N-концевых лидерных последовательностей, дальнейших делеций, замен или добавлений к последовательности. Способы, которые могут использоваться для определения того, образуют ли белки такие структуры, охватывают гель-фильтрацию, электрофорез в агарозном геле, центрифугирование в градиенте сахарозы и электронную микроскопию (например, Koschel, M. et al., J. Virol 73:2153-2160 (1999)).
Первые участки связывания. Природные или неприродные коровые частицы, используемые в конъюгатах, конъюгатах и способах по настоящему изобретению, в основном содержат компонент, включающий первый участок связывания, который привязан к природной или неприродной коровой частице, по крайней мере, одной ковалентной связью. Элемент, включающий первый участок связывания, связывается с коровой частицей не случайным образом, что обеспечивает участок образования ядра для создания упорядоченного и повторяемого мотива. В идеале, но не обязательно данный элемент ассоциирован с коровой частицей в геометрическом порядке. Первый участок связывания может быть природной частью коровой частицы, такой как экспонированный на поверхность аминокислотный остаток, подходящий для присоединения второго участка связывания. Например, лизин и цистеин могут образовывать непептидные связи за счет реакционноспособных групп на аминокислоте. Альтернативно, элемент, содержащий первый участок связывания, может вводиться в коровую частицу путем химического связывания или путем конструирования рекомбинантных молекул. Первый участок связывания может представлять собой любой элемент, связанный с коровой частицей, по крайней мере, одной ковалентной связью, или данный участок может находиться на данном элементе.
Первый участок связывания может содержать или, альтернативно, может состоять из белка, полипептида, пептида, аминокислоты (т.е. остатка белка, полипептида или пептида), сахара, полинуклеотида, природного или синтетического полимера, вторичного метаболита или соединения (биотин, флуоресцеин, ретинол, дигоксигенин, ионы металлов, фенилметилсульфонилфторид), или их комбинации, или их реакционноспособной химической группы. В более конкретном осуществлении первый участок связывания содержит антиген, антитело или фрагмент антитела, биотин, авидин, стрептавидин, рецептор, лиганд рецептора, лиганд, связывающий лиганд белок, взаимодействующий путем лейциновой застежки полипептид, аминогруппу, химическую группу, реакционноспособную в отношении аминогруппы; карбоксильную группу, химическую группу реакционноспособную в отношении карбоксильной группы, сульфгидрильную группу, химическую группу, реакционноспособную в отношении сульфгидрильной группы, или их комбинацию.
В одном из осуществлений изобретения используется генная инженерия вируса для создания слияния между упорядоченным и повторяемым вирусным оболочечным белком и элементом, содержащим первый участок связывания, который включает гетерологичный белок, пептид, антигенную детерминанту или реакционноспособный аминокислотный остаток по выбору. В конструирование неприродного молекулярного каркаса могут вовлекаться другие генетические манипуляции, известные в данной области; например, может быть предпочтительным ограничение способности рекомбинантного вируса к репликации посредством генной мутации. Вирусный белок, выбранный для слияния с белком, содержащим первый участок связывания, должен характеризоваться организованной и повторяемой структурой. Такая организованная и повторяемая структура включает паракристаллические организованные структуры с разбивкой, равной 0,5-30 нм, предпочтительно, 5-15 нм, на поверхности вируса. Создание данного типа белка слияния приводит к появлению множественных, упорядоченных и повторяемых первых участков связывания на поверхности вируса. Таким образом, упорядоченная и повторяемая организация первых. участков связывания, полученная в результате этого, будет являться отражением обычной организации нативного вирусного белка.
Как будет понятно обычным специалистам в данной области, первый участок связывания может быть любым подходящим белком, полипептидом, сахаром, полинуклеотидом, пептидом (аминокислотой), природным или синтетическим полимером, вторичным метаболитом или их комбинацией, или их частью, и он может служить для специфического связывания антигена или антигенной детерминанты по выбору с неприродным молекулярным каркасом. В одном из осуществлений участок связывания представляет собой белок или пептид, который может быть выбран из известных в данной области. Например, первый участок связывания может представлять собой лиганд, рецептор, лектин, авидин, стрептавидин, биотин, зпитоп, такой как метка НА или Т7, Мус, Мах, иммуноглобулиновые домены и любую другую аминокислотную последовательность, известную в данной области, которая может использоваться в качестве первого участка связывания.
Обычным специалистам в данной области будет далее понятно, что в другом осуществлении изобретения первый участок связывания может быть создан во вторую очередь после создания элемента, несущего первый участок связывания (например, белка или полипептида), задействованного при конструировании слияния с капсидным белком в одной рамке считывания. Например, для слияния с оболочечным белком может использоваться белок с аминокислотной последовательностью, о которой известно, что она гликозилируется специфичным образом, и добавленная в результате сахарная группа может затем служить в качестве первого участка связывания вирусного каркаса путем связывания лектина, служащего в качестве вторичного участка связывания антигена. Альтернативно, последовательность может быть биотинилирована in vivo, и радикал биотина может служить в качестве первого участка связывания по изобретению, или последовательность может подвергаться химической модификации по различным аминокислотным остаткам in vitro, причем модификация служит в качестве первого участка связывания.
В одном из конкретных осуществлений изобретения первый участок связывания представляет собой белковый домен с лейциновой застежкой JDN-FOS, который подвергнут слиянию в рамку считывания с капсидным (коровым) белком вируса гепатита В (HBcAg). Однако специалисту в данной области будет ясно, что другие вирусные капсидные белки могут быть задействованы при конструкции белка слияния для локализации первого участка связывания в неприродном молекулярном каркасе по изобретению. Например, в других осуществлениях изобретения первый участок связывания выбирают так, чтобы он представлял собой остаток лизина или цистеина, который подвергнут слиянию в рамку с HBcAg. Также всем специалистам в данной области будет ясно, что другие вирусные капсидные или вирусоподобные частицы могут быть задействованы при конструкции белка слияния для локализации первого участка связывания на неприродном молекулярном каркасе по изобретению.
Вирусные частицы. В одном из осуществлений изобретения неприродный молекулярный каркас представляет собой рекомбинантный альфавирус и, более конкретно, рекомбинатный вирус Синдбис. Некоторые представители семейства альфавирусов, Синдбис (Xiong, С.et al., Science 243:1188-1191 (1989); Schlesinger, S., Trends Biotechnol. 11:18-22 (1993)), вирус леса Семлики (SFV) (Liljestöm, P. & Garoff, H., Bio/Technology 9: 1356-1361 (1991)) и другие (Davis, N.L. et al., Virology 171:189-204 (1989)) привлекли существенное внимание в плане применения в качестве основанных на вирусах экспрессирующих векторов для ряда различных белков (Lundstrom, К., Curr. Opin. Biotechnol. 8:578-582 (1997); Liljeström, P., Curr. Opin. Biotechnol. 5:495-500 (1994)) и в качестве кандидатов для разработки вакцин. Было описано применение альфавирусов для экспрессии гетерологичных белков и разработки вакцин (см. патенты США № 5766602; 5792462; 5739026; 5789245 и 5814482 все описания которых включены сюда полностью в качестве ссылки). Конструирование альфавирусного каркаса по данному аспекту изобретения может быть выполнено средствами, в основном известными в.области технологии рекомбинантной ДНК, как описано в указанных выше статьях, которые включены сюда в качестве ссылки. Различные рекомбинантные клетки-хозяева могут использоваться для продукции основанной на вирусах коровой частицы для присоединения одной или нескольких ангиотензиновых пептидных составляющих.
Для инфекции клеток-хозяев также могут использоваться упакованные последовательности РНК. Данные упакованные последовательности РНК могут быть введены в клетки-хозяева путем добавления их к культуральной среде. Например, получение неинфекционных альфавирусных частиц описано в некоторых источниках, включая «Sindbis Expression System», Version С (Invitrogen Corporation, Carlsbad CA; Catalog No.K750-1).
Когда в качестве рекомбинантных клеток-хозяев для продукции основанных на вирусе коровых частиц используют клетки млекопитающих, данные клетки главным образом выращиваются в культуре ткани. Способы выращивания клеток в культуре хорошо известны в данной области (см., например., Celis, J., ed., CELL BIOLOGY, Academic Press, 2nd edition, (1998); Sambrook, J. et al., eds., MOLECULAR CLONING, A LABORATORY MANUAL, 2nd. edition, Cold Spring Harbor Laboratory Press, Cold Spring Harbor, N.Y. (1989); Ausubel, F. et al., eds., CURRENT PROTOCOLS IN MOLECULAR BIOLOGY, John H. Wiley & Sons, Inc. (1997); Freshney, R., CULTURE OF ANIMAL CELLS, Alan R. Liss, Inc. (1983)).
Таким образом, изобретение относится к основанным на вирусах коровым частицам, которые содержат или, альтернативно, состоят из вируса, вирусоподобной частицы, фага, вирусной капсидной частицы или их рекомбинантных форм. Обычные специалисты в данной области обладают знаниями, необходимыми для получения таких коровых частиц и присоединения к ним первых участков связывания. Продукция частиц, подобных вирусу гепатита В, в частности, тех, что собираются или самопроизвольно собираются из HBcAg, и капсидных частиц вируса кори в качестве коровых частиц, описана в примерах от 17 до 22 WO 00/32227, полностью включенной сюда в качестве ссылки. В таких осуществлениях домен белка с лейциновой застежкой JUN или домен белка с лейциновой застежкой FOS могут использоваться в качестве первого участка связывания для неприродного молекулярного каркаса по изобретению. Обычному специалисту в данной области известны способы конструирования коровых частиц вируса гепатита В, несущих подвергнутый слиянию в ту же рамку считывания пептид, несущий реакционноспособный остаток лизина, и ангиотензиновых пептидных составляющих, несущих присоединенный генетически остаток цистеина, в качестве первого и второго участков связывания, соответственно.
В других осуществлениях коровые частицы, используемые в конъюгатах по изобретению, состоят из капсидного (корового) белка вируса гепатита В (HBcAg), фрагмента HBcAg или другого белка или пептида, который может образовывать вирусоподобные частицы, представляющие собой упорядоченные структуры, которые модифицированы так, что число свободных остатков цистеина элиминировано или снижено. Zhou et al. (J. Virol. 66:5393-5398 (1992)) продемонстрировали, что HBcAg, которые модифицированы, так что удалены присутствующие в природе остатки цистеина, сохраняют способность ассоциировать и образовывать мультимерные структуры. Таким образом, коровые частицы, подходящие для применения в конъюгатах по изобретению, включают те, что содержат модифицированный HBcAg или его фрагменты, в котором один или несколько присутствующих в природе остатков цистеина подвергнуты делеции или заменены другим аминокислотным остатком (например, остатком серина). В одном из осуществлений изобретения модифицированный HBcAg, содержащий аминокислотную последовательность, представленную в SEQ ID NO: 1, или ее часть, используют для получения неприродных молекулярных каркасов. В частности, модифицированные HBcAg, подходящие для использования при воплощении изобретения, включают белки, в которых один или нескольких остатков цистеина в положениях, соответствующих положениям 48, 61, 107 и 185 белка, характеризующегося аминокислотной последовательностью, представленной в SEQ ID NO: 1, подвергнуты делеции или замещены другими аминокислотными остатками (например, остатком серина). Как понятно специалисту в данной области, цистеиновые остатки в сходных положениях вариантов HBcAg, характеризующихся аминокислотными последовательностями, которые отличаются от той, что представлена в SEQ ID NO: 1, также могут подвергаться делеции или замещаться другими аминокислотными остатками. Затем модифицированные варианты HBcAg могут использоваться для получения вакцинных конъюгатов по изобретению.
В некоторых обстоятельствах (например, при использовании гетеробифункционального перекрестно связывающего реагента для присоединения одной или нескольких ангиотензиновых пептидных составляющих к неприродному молекулярному каркасу) наличие свободных остатков цистеина в HBcAg, как полагают, приводит к ковалентному присоединению к коровым частицам токсичных компонентов, а также перекрестному связыванию мономеров с образованием неопределенных видов молекул. Далее, во многих случаях данные токсические компоненты могут не детектироваться путем анализов, проводимых с конъюгатами по изобретению. Это происходит потому, что ковалентное присоединение токсических компонентов к неприродному молекулярному каркасу приводит к образованию группы различных видов молекул, в которых токсические компоненты присоединены к различным остаткам цистеина или, в некоторых случаях, к нецистеиновым остаткам HBcAg. Иными словами, не каждый свободный остаток цистеина каждого HBcAg будет ковалентно связан с токсичными компонентами. Далее, во многих случаях ни один из остатков цистеина конкретных HBcAg не будет связан с токсичными компонентами. Таким образом, наличие данных токсичных компонентов может быть трудным для детекции, поскольку они будут присутствовать в смешанной группе молекул. Введение субъекту видов HBcAg, содержащих токсические компоненты, однако, может привести к потенциально опасным побочным реакциям.
В данной области хорошо известно, что свободные остатки цистеина могут участвовать в некоторых химических побочных реакциях. Данные побочные реакции охватывают обмены дисульфидных групп, реакции с химическими веществами или метаболитами, которые, например, инъецируют или формулируют при комбинированной терапии с другими веществами, или прямое окисление и реакция с нуклеотидами после воздействия УФ-излучения. Таким образом могут генерироваться токсичные аддукты, особенно, в контексте того факта, что HBcAg обладают выраженной тенденцией к связыванию нуклеиновых кислот. Детекция таких токсических продуктов в конъюгатах антиген-капсид будет затруднена при использовании капсидов, полученных с использованием HBcAg, содержащих свободные цистеины и гетеробифункциональные перекрестные линкеры, поскольку будет генерироваться набор продуктов, сильно различающихся по молекулярной массе. Таким образом, токсичные аддукты будут распределяться между многими видами молекул, которые по отдельности могут присутствовать в низкой концентрации, но вместе достигать токсичных концентраций.
В свете вышесказанного, одним из преимуществ применения HBcAg в вакцинных конъюгатах, которые были модифицированы, так что были удалены присутствующие в природе остатки цистеина, является то, что число участков, с которыми могут связываться токсичные виды молекул при присоединении к неприродному молекулярному каркасу ангиотензиновых пептидных составляющих, будет снижено, или они будут вовсе удалены. Далее, высокая концентрация перекрестного линкера может использоваться для продукции сильно модифицированных частиц без неблагоприятной продукции множества неопределенных перекрестно связанных видов мономеров HBcAg (например, разнородной смеси перекрестно связанных мономерных HBcAg).
Был идентифицирован ряд встречающихся в природе вариантов HBcAg, подходящих для применения при воплощении по настоящему изобретению. Yuan et al., (J. Virol. 73:10122-10128 (1999)), например, описывают варианты, в которых остаток изолейцина в положении, соответствующем положению 97 в SEQ ID NO: 1, замещен остатком лейцина или остатком фенилаланина. Аминокислотные последовательности некоторых вариантов HBcAg, а также некоторых вариантов предшественников корового антигена вируса гепатита В, представлены в отчетах GenBank AAF121240, AF121239, Х85297, Х02496, Х85305, Х85303, AF151735, Х85259, Х85286, Х85260, Х85317, Х85298, AF043593, М20706, Х85295, Х80925, Х85284, Х85275, Х72702, Х85291, Х65258, Х85302, М32138, Х85293, Х85315, U95551, Х85256, Х85316, Х85296, АВ033559, Х59795, Х8529, Х85307, Х65257, Х85311, Х85301, Х85314, Х85287, Х85272, Х85319, АВ010289, Х85285, АВ010289, AF121242, М90520, Р03153, AF110999 и М95589, описания которых включены сюда полностью в качестве ссылки. Данные варианты HBcAg отличаются по аминокислотной последовательности в некоторых положениях, включая аминокислотные остатки, которые соответствуют аминокислотным остаткам, расположенным в положениях 12, 13, 21, 22, 24, 29, 32, 33, 35, 38, 40, 42, 44, 45, 49, 51, 57, 58, 59, 64, 66, 67, 69, 74, 77, 80, 81, 87, 92, 93, 97, 98, 100, 103, 105, 106, 109, 113, 116, 121, 126, 130, 133, 135, 141, 147, 149, 157, 176, 178, 182 и 183 в SEQ ID NO: 1.
Дальнейшие варианты HBcAg, подходящие для применения в композициях по изобретению, и те, которые могут быть далее модифицированы по раскрытию данной спецификации, описаны в WO 00/198333, WO 00/177158 и WO 00/214478, включенных сюда полностью в качестве ссылок.
HBcAg, подходящие для применения по настоящему изобретению, могут происходить из любого организма при условии, если они могут ассоциировать с образованием упорядоченного и повторяемого мотива антигенов. Процессированные обычным образом HBcAg (т.е. те, что не содержат лидерных последовательностей) используют в качестве вакцинных конъюгатов по изобретению. Настоящее изобретение включает вакцинные конъюгаты, а также способы применения данных конъюгатов, в которых используются описанные выше вариантные HBcAg для получения неприродных молекулярных каркасов. Кроме того, в объем изобретения входят добавочные варианты HBcAg, способные ассоциироваться с образованием димерных или мультимерных структур. Таким образом, изобретение, кроме того, относится к вакцинным конъюгатам, включающим полипептиды HBcAg, содержащие или, альтернативно, состоящие из аминокислотных последовательностей, которые, по крайней мере, примерно на 80%, примерно на 85%, примерно на 90%, примерно на 95%, примерно на 97% или примерно на 99% идентичны любой аминокислотной последовательности из указанных выше аминокислотных последовательностей, включая SEQ ID NO: 1, и к формам данных белков, которые были процессированы, где следует, с целью удаления N-концевой лидерной последовательности.
То, характеризуется ли аминокислотная последовательность полипептида аминокислотной последовательностью, которая, по крайней мере, примерно на 80%, примерно на 85%, примерно на 90%, примерно на 95%, примерно на 97% или примерно на 99% идентична одной из представленных выше аминокислотных последовательностей, или ее части, можно определить широко используемыми компьютерными программами, такими как программа Bestfit. При использовании Bestfit или любой другой программы выравнивания последовательностей для определения того, является ли конкретная последовательность, например, примерно на 95% идентична аминокислотной последовательности сравнения по настоящему изобретению, параметры устанавливают так, что процентная доля идентичности вычисляется по всей длине аминокислотной последовательности сравнения, и что допустимы разрывы в гомологии до 5% от общего количества аминокислотных остатков в последовательности сравнения. Таким образом, могут проводиться сравнения между аминокислотной последовательностью HBcAg SEQ ID NO: 1 и другого HBcAg. При сравнении белков, которые относительно сходны, ссылка на аминокислотный остаток варианта HBcAg, находящийся в положении, которое соответствует конкретному положению в SEQ ID NO: 1, указывает аминокислотный остаток, который присутствует в том положении в аминокислотной последовательности, представленной в SEQ ID NO: 1. Гомология между данными вариантами HBcAg среди вирусов гепатита В, которые инфицируют млекопитающих, по большей части является достаточно высокой, так что специалисту в данной области будет не очень трудно анализировать аминокислотную последовательность, представленную в SEQ ID NO: 1, и таковую для конкретного варианта HBcAg, и идентифицировать «соответствующие» аминокислотные остатки. Например, при сравнениях между SEQ ID NO: 1 и аминокислотной последовательностью HBcAg, происходящего из вируса, который инфицирует североамериканских лесных сурков, легко понять, что в данной последовательности присутствует вставка из трех аминокислот между аминокислотными остатками 155 и 156 SEQ ID NO: 1.
Однако, если выравнивание затруднено, специалист в данной области может распознать значимость конкретных аминокислот или мотивов в последовательности. Например, аминокислотная последовательность HBcAg из человеческих вирусов отличается от таковой от утиных вирусов, так что выравнивание затруднено, однако, специалист в данной области сможет распознать консервативные остатки цистеина, которые могли бы быть замещены другим аминокислотным остатком или подвергнуты делеции перед их включением в вакцинные конъюгаты по изобретению.
В одном из осуществлений, остатки цистеина в положениях 48 и 107 белка, характеризующегося аминокислотной последовательностью, представленной в SEQ ID NO: 1, делетируют или замещают другими аминокислотными остатками, но цистеин в положении 61 остается на месте. Кроме того, модифицированный полипептид затем используют для получения вакцинных конъюгатов по изобретению.
Препарат предпочтительных вирусоподобных частиц вируса гепатита В, который может использоваться по настоящему изобретению, описан, например, в WO 00/32227, и там, в частности, в примерах с.17 по 19 и с 21 по 24, а также в WO 01/85208, и там, в частности, в примерах с 17 до 19, с 21 до 24, в 31 и 41, и в ожидающей решения заявке на выдачу патента США № 10/050902, поданной правопреемником настоящего изобретения 18 января 2002 г. В последней заявке он упоминается, в частности, в примере 23, 24, 31 и 51. Все три документа включены сюда полностью в качестве ссылки.
Как установлено в примере 31 заявки на выдачу патента США 10/050902, поданной правопреемником настоящего изобретения 18 января 2002 г., остатки цистеина в положениях 48 и 107, доступных для растворителя, могут удаляться, например, путем сайт-направленного мутагенеза. В одном из таких примеров было обнаружено, что двойной мутант HBcAg Cys-48-Ser, Cys-107-Ser, сконструированный, как описано в одновременно ожидающей решения заявке на выдачу патента США 10/050902, поданной 18 января 2002 г. (которая включена сюда полностью в качестве ссылки), может экспрессироваться в Е. coli.
Как описано выше, удаление свободных остатков цистеина снижает число участков, где токсичные компоненты могут связываться с HBcAg, и также приводит к элиминации участков, где может произойти перекрестное связывание остатков лизина и цистеина одной или соседних молекул HBcAg. Цистеин в положении 61, участвующий в формировании димера и образующий дисульфидный мостик с цистеином в положении 61 другого HBcAg, обычно оставляют интактным для стабилизации димеров HBcAg и мультимеров по изобретению. Эксперименты по перекрестному связыванию, проведенные на (1) HBcAg, содержащих свободные остатки цистеина, и (2) HBcAg, остатки цистеина которых были лишены реакционной способности с помощью иодацетамида, показали, что свободные остатки цистеина HBcAg ответственны за перекрестное связывание между HBcAg за счет взаимодействий между дериватизированными с помощью гетеробифункционального перекрестного линкера боковыми цепями лизина и свободными остатками цистеина. Также было обнаружено, что перекрестное связывание субъединиц HBcAg приводит к образованию типов молекул с высокой молекулярной массой неопределенного размера, которые не могут быть разрешены при помощи электрофореза в SDS-полиакриламидном геле.
Когда ангиотензиновую пептидную составляющую присоединяют к неприродному молекулярному каркасу через остаток лизина, может быть предпочтительна замена или делеция одного или нескольких присутствующих в природе остатков лизина, находящихся в положениях, соответствующих положениям 7 и 96 в SEQ ID NO: 1, а также других остатков лизина, присутствующих в вариантах HBcAg. Элиминация данных остатков лизина приводит к удалению участков связывания ангиотензиновых пептидных составляющих, которые могли бы разрушить упорядоченный мотив, и улучшает качество и однородность конечного вакцинного конъюгата.
Во многих случаях элиминации обоих присутствующих в природе остатков лизина в положениях, соответствующих положениям 7 и 96 в SEQ ID NO: 1, другой остаток лизина вводят в HBcAg в качестве участка связывания ангиотензиновой пептидной составляющей. Способы вставки такого остатка лизина установлены, например, в одновременно ожидающей решения заявке на выдачу патента США 10/050902, поданной 18 января 2002 г., и там, в частности, в примере 23 заявки на выдачу патента США 10/050902 (которая включена сюда полностью в качестве ссылки). Часто является предпочтительным введение остатка лизина в HBcAg, где, например, изменяют оба присутствующих в природе остатка лизина в положениях, соответствующих положениям 7 и 96 в SEQ ID NO: 1, и добиваются присоединения ангиотензиновой пептидной составляющей к неприродному молекулярному каркасу с использованием гетеробифункционального перекрестно-связывающего агента.
Как было показано, С-конец HBcAg направляет ядерную локализацию данного белка (Eckhardt et al., J. Virol. 65:575-582 (1991)). Далее, эта область белка, как также полагают, дает HBcAg способность связывать нуклеиновые кислоты.
В некоторых осуществлениях вакцинные конъюгаты по настоящему изобретению содержат HBcAg, которые обладают активностью в плане связывания нуклеиновой кислоты (например, те, что содержат присутствующий в природе связывающий нуклеиновую кислоту домен HBcAg). HBcAg, содержащие один или несколько связывающих нуклеиновую кислоту доменов, могут использоваться для получения вакцинных конъюгатов, которые проявляют повышенную активность в плане стимуляции Т-клеток. Таким образом, вакцинные конъюгаты по настоящему изобретению включают конъюгаты, которые содержат HBcAg, обладающие активностью в плане связывания нуклеиновой кислоты. Кроме того, включаются вакцинные конъюгаты, в которых HBcAg связаны с нуклеиновой кислотой, а также применение таких конъюгатов для протоколов вакцинирования. Данные HBcAg могут связываться с нуклеиновыми кислотами перед введением субъекту или могут связывать нуклеиновые кислоты после введения.
Дальнейшие HBcAg, подходящие для применения при воплощении настоящего изобретения, включают мутанты, укороченные по N- и С-концам, и мутеины, аминокислотные последовательности которых содержат или, альтернативно, состоят из аминокислотных последовательностей, которые, по крайней мере, примерно на 80%, примерно на 85%, примерно на 90%, примерно на 95%, примерно на 97% или примерно на 99% идентичны последовательностям описанных выше укороченных мутантов.
Как описано выше, в некоторых осуществлениях настоящего изобретения остаток лизина вводят в качестве первого участка связывания в полипептид, который образует неприродный молекулярный каркас. В предпочтительных осуществлениях вакцинные конъюгаты по изобретению получают с использованием HBcAg, включающего или, альтернативно, состоящего из аминокислот 1-144, или аминокислот 1-149, или аминокислот 1-185 из SEQ ID NO: 1, которые модифицируют, так что аминокислоты, соответствующие положениям 79 и 80, замещены пептидом, имеющим аминокислотную последовательность Gly-Gly-Lys-Gly-Gly (SEQ ID NO:32), и остатки цистеина в положениях 48 и 107 подвергнуты делеции или замещены другим аминокислотным остатком, в то время как цистеин в положении 61 остается на месте.
Настоящее изобретение, кроме того, включает вакцинные конъюгаты, включающие фрагменты HBcAg, содержащие или, альтернативно, состоящие из аминокислотной последовательности, отличной от той, что представлена в SEQ ID NO: 1, из которой удален остаток цистеина, не имеющийся в соответствующем положении в SEQ ID NO: 1.
Вакцинные конъюгаты по изобретению могут включать смеси различных HBcAg. Таким образом, данные вакцинные конъюгаты могут состоять из HBcAg, которые различаются по аминокислотной последовательности. Например, могут быть получены вакцинные конъюгаты, содержащие HBcAg «дикого типа», и модифицированный HBcAg, в котором изменена (например, подвергнута делеции, вставлена или заменена) одна или несколько аминокислот.
Настоящее изобретение, кроме того, относится к вакцинным конъюгатам, в которых неприродный молекулярный каркас получают с использованием HBcAg, подвергнутого слияния с другим белком. Как описано выше, одним из примеров такого белка слияния является белок слияния HBcAg/FOS. Другие примеры белков слияния HBcAg, подходящие для применения в вакцинных конъюгатах по изобретению, включают белки слияния, где добавлена аминокислотная последовательность, которая способствует образованию и/или стабилизации димеров и мультимеров HBcAg. Данная дополнительная аминокислотная последовательность может быть слита с С-концом HBcAg. Одним из примеров такого белка слияния является белок слияния HBcAg со спиральным районом GCN4 Saccharomyces cerevisiae, который образует гомодимеры путем нековалентных взаимодействий, которые могут использоваться для получения и стабилизации димеров и мультимеров HBcAg.
В одном из осуществлений изобретение относится к вакцинным конъюгатам, полученным с использованием белков слияния HBcAg, содержащих HBcAg или его фрагмент, с полипептидом GCN4 (SEQ ID NO: 5, PAALKRARNEAARRSRARKLQRMKQLEDKVEELLSKNYHLENEVARLKK), присоединенным с С-конца. Данный полипептид GCN4 может.также подвергаться слиянию с N-конца HBcAg.
Белки слияния HBcAg/гомологичный src домен 3 (SH3) также могут использоваться для получения вакцинных конъюгатов по изобретению. Домены SH3 являются относительно небольшими доменами, обнаруженными в ряде белков и наделенными способностью взаимодействовать с особыми богатыми пролином последовательностями в белковых партнерах по связыванию (см. McPherson, Cell Signal 11:229-238 (1999). Белки слияния HBcAg/SH3 могут использоваться несколькими способами. Во-первых, домен SH3 может образовывать первый участок связывания, который взаимодействует со вторым участком связывания на ангиотензиновой пептидной составляющей. Сходным образом, богатая пролином аминокислотная последовательность может быть добавлена к HBcAg и использована в качестве первого участка связывания для основанного на домене SH3 второго участка связывания ангиотензиновой пептидной составляющей. Во-вторых, домен SH3 может ассоциироваться с богатыми пролином районами, введенными в HBcAg. Таким образом, домены SH3 и богатые пролином участки взаимодействия с SH3 могут быть встроены в один и тот же или разные HBcAg. и использованы для образования и стабилизации димеров и мультимеров по изобретению.
Как доказано приведенным выше примером, специалисту в данной области известно, как получить молекулярный каркас, включающий коровые частицы и первый участок связывания, из HBcAg и происходящих из HBcAg мутеинов. За счет применения известных в данной области способов и рутинного экспериментирования специалисту в данной области будет понятно, как сходным образом использовать для конструирования молекулярного каркаса другие вирусы.
Как представлено здесь в другом месте, вирусные капсиды могут применяться для (1) презентации одной или нескольких ангиотензиновых пептидных составляющих и (2) получения вакцинных конъюгатов по изобретению. Особенно подходящими при воплощении изобретения являются вирусные капсидные белки, также указанные в данном описании как «покровные белки», которые после экспрессии образуют капсиды или подобные капсидам структуры. Так, данные капсидные белки могут образовывать коровые частицы и неприродные молекулярные каркасы. Как правило, данные капсиды или подобные капсидам структуры образуют упорядоченные и повторяемые мотивы, которые могут использоваться для презентации антигенных детерминант и получения вакцинных конъюгатов по изобретению.
Одна или несколько (например, одна, два, три, четыре, пять и т.д.) ангиотензиновых пептидных составляющих могут присоединяться любым числом способов к одному или нескольким (например, к одному, двум, трем, четырем, пяти и т.д.) белкам, которые образуют вирусные капсиды или подобные капсидам структуры (например, покровные белки бактериофагов), а также другие белки. Например, ангиотензиновые пептидные составляющие могут присоединяться к коровым частицам с использованием первого и второго участков связывания. Далее, один или несколько (например, один, два, три, четыре, пять и т.д.) гетеробифункциональных перекрестных линкеров могут использоваться для присоединения одного или нескольких ангиотензиновых пептидных составляющих к одному или нескольким белкам, которые образуют вирусные капсиды или подобные капсидам структуры.
Вирусные капсидные белки или их фрагменты могут использоваться, например, для получения коровых частиц и вакцинных конъюгатов по изобретению. Покровные белки бактериофага Qβ, например, могут рекомбинантно зкспрессироваться в Е. coli. Далее, после такой экспрессии данные белки спонтанно образуют капсиды, которые представляют собой вирусоподобные частицы. Кроме того, данные капсиды образуют упорядоченные и повторяемые мотивы антигенов, которые могут использоваться при презентации ангиотензиновых пептидных составляющих и получения вакцинных конъюгатов.
В предпочтительном осуществлении вирусоподобная частица содержит, по существу, состоит или, альтернативно, состоит из рекомбинантных белков РНК-фага или их фрагментов. Предпочтительно, РНК-фаг выбирают из группы, состоящей из: а) бактериофага Qβ; b) бактериофага R17; с) бактериофага fr; d) бактериофага GA; е) бактериофага SP; f) бактериофага MS2; g) бактериофага M11; h) бактериофага МХ1; i) бактериофага NL95; k) бактериофага f2; l) бактериофага РР7 и m) бактериофага АР205.
В другом предпочтительном осуществлении настоящего изобретения вирусоподобная частица содержит или, альтернативно, по существу, состоит, или, альтернативно, состоит из рекомбинантных белков РНК-бактериофага Qβ, или РНК-бактериофага fr, или РНК-бактериофага АР205, или их фрагментов.
Конкретные примеры покровных белков бактериофагов, которые могут использоваться для получения конъюгатов по изобретению, включают покровные белки РНК-бактериофагов, таких как бактериофаг Qβ (SEQ ID NO: 3; база данных PIR, инвентарный номер VCBPQβ, относящийся к СР Qβ, и SEQ ID NO: 4; инвентарный номер ААА16663, относящийся к белку А1 Qβ) бактериофаг R17 (инвентарный номер PIR VCBPR7), бактериофаг fr (инвентарный номер PIR VCBPFR), бактериофаг GA (инвентарный номер GenBank NP-040754), бактериофаг SP (инвентарный номер GenBank CAA30374, относящийся к СР SP, и инвентарный номер, относящийся к белку А1 SP), бактериофаг MS2 (инвентарный номер PIR VCBPM2), бактериофаг М11 (инвентарный номер GenBank AAC06250), бактериофаг МХ1 (инвентарный номер GenBank AAC14699), бактериофаг NL95 (инвентарный номер GenBank AAC14704), бактериофаг f2 (инвентарный номер GenBank P03611), бактериофаг РР7, бактериофаг АР205 (SEQ ID NO: 12). Как понятно специалисту в данной области, любой белок, образующий капсиды или капсидоподобные структуры, может использоваться для получения вакцинных конъюгатов по изобретению. Более того, белок А1 бактериофага Qβ (инвентарный номер Genbank AAA16663 (SEQ ID NO: 4)) или его укороченные с С-конца формы, лишенные, по крайней мере, примерно 100, примерно 150 или примерно 180 аминокислот с его С-конца, могут входить в состав собранного капсида покровных белков Qβ. Белок А1 также может быть слит с элементом, содержащим первый участок связывания, для связывания ангиотензиновых пептидных составляющих, содержащих второй участок связывания. В основном процентную долю белка А1 по отношению к белку СР Qβ при сборке капсида ограничивают для обеспечения образования капсида.
Покровный белок Qβ, как было обнаружено, также самопроизвольно организуется в капсиды при экспрессии в Е. coli (Kozlovska TM. et al., GENE 137: 133-137 (1993)). Полученные капсиды или вирусоподобные частицы характеризовались экосаэдрической структурой, подобной фаговому капсиду, с диаметром 25 нм и квазисимметрией Т=3. Кроме того, разрешена кристаллическая структура фага Qβ. Капсид содержит 180 копий покровного белка, которые связаны в ковалентные пентамеры и гексамеры дисульфидными связями (Golmohammadi, R. et al., Structure 4:543-5554 (1996)). Другие покровные белки РНК-фагов, как было показано, также самоорганизуются после экспрессии в бактериальном хозяине (Kastelein, RA. et al., Gene 23: 245-254 (1983), Kozlovskaya, TM. et al., Dokl. Akad. Nauk SSSR 287:452-455 (1986), Adhin, MR. et al., Virology 170:238-242 (1989), Ni, CZ., et al., Protein Sci. 5:2485-2493 (1996), Priano, С et al., J. Mol. Biol. 249: 283-297 (1995)). Капсид фага Qβ содержит в дополнение к покровному белку так называемый белок считывания А1 и белок созревания А2. А1 генерируется путем подавления в стоп-кодоне UGA и характеризуется длиной 329 аминокислот. Капсид из рекомбинантного покровного белка фага Qβ, использованного по изобретению, лишен белка лизиса А2 и, содержит РНК хозяина. Покровный белок РНК-фагов представляет собой РНК-связывающий белок и взаимодействует с стеблевой петлей сайта связывания рибосомы гена репликазы, действуя как репрессор трансляции во время жизненного цикла вируса. Известны последовательность и структурные элементы взаимодействия (Witherell, GW. & Uhlenbeck, ОС.Biochemistry 28:71-76 (1989); Lim F. et al., J, Biol. Chem. 271:31839-31845 (1996)). В общем, известно, что данная стеблевая петля и РНК участвуют в сборке вируса (Golmohammadi, R. et al., Structure 4: 543-5554 (1996)).
После экспрессии в Е. coli N-концевой метионин покровного белка Qβ обычно удаляется, как наблюдали авторы настоящего изобретения посредством N-концевого секвенирования по Эдману, описанного в Stoll, Е. et al. J. Biol. Chem. 252: 990-993 (1977). VLP, составленные из покровных белков Qβ, где не удален N-концевой метионин, или VLP, состоящие из смеси покровных белков Qβ, где N-концевой метионин отщеплен или присутствует, также входят в объем настоящего изобретения.
В дальнейшем предпочтительном осуществлении настоящего изобретения вирусоподобная частица содержит, или, альтернативно, по существу состоит, или, альтернативно, состоит.из рекомбинантных белков РНК-фага АР205 или их фрагментов.
Геном АР205 состоит из белка созревания, покровного белка, репликазы и двух открытых рамок считывания, не присутствующих в родственных фагах; гена лизиса и открытой рамки считывания, играющей роль в трансляции гена созревания (Klovins, J., et al., J Gen. Virol. 83:1523-33 (2002)). Покровный белок АР205 может экспрессироваться из плазмиды рАР283-58 (SEQ ID NO: 11), которая является производным pQb10 (Kozlovska, Т.М. et al., Gene 137: 133-37 (1993)) и которая содержит сайт связывания рибосомы АР205. Альтернативно, покровный белок АР205 может быть клонирован в pQb185, ниже сайта связывания рибосомы, присутствующего в векторе. Оба подхода ведут к экспрессии белка и образованию капсидов, как описано в одновременно находящейся на рассмотрении предварительной заявке на выдачу патента США №60/396126, поданной 17 июля 2002 г., которая включена сюда полностью в качестве ссылки, и, в частности, как описано в примере 2 указанной патентной заявки. Векторы pQb10 и рQb185 представляют собой векторы, происходящие от вектора pGEM, и экспрессия клонированных генов в данных векторах контролируется промотором trp (Kozlovska, Т.М. et al., Gene 137: 133-37 (1993)). Плазмида рАР283-58 (SEQ ID NO: 11) содержит предполагаемый сайт связывания рибосомы АР205 в следующей последовательности, который располагается ниже сайта XbaI и непосредственно выше стартового кодона ATG покровного белка АР205: tctagaATTTTCTGCGCACCCATCCCGGGTGGCGCCCAAAGTGAGGAAAATCACatg (основания 77-133 SEQ ID NO: 34). Вектор pQbl85 содержит последовательность Шайна-Дальгарно ниже сайта XbaI и выше стартового кодона (tctagraTTAACCCAACGCGTAGGAG TCAGGCCatg, последовательность Шайна-Дальгарно подчеркнута, SEQ ID NO: 18).
В дальнейшем предпочтительном осуществлении настоящего изобретения вирусоподобная частица содержит или, альтернативно, по существу состоит, или, альтернативно, состоит из рекомбинантных покровных белков РНК-фага АР205, или их фрагментов.
Данное предпочтительное осуществление настоящего изобретения, таким образом, включает покровные белки АР205, которые образуют капсиды. Такие белки рекомбинантно экспрессируют или получают из природных источников. Покровные белки АР205, продуцируемые в бактериях, спонтанно образуют капсиды, что подтверждают электронной микроскопией (ЭМ) и иммунодиффузией. Структурные свойства капсида, образованного покровным белком АР205 (SEQ ID NO: 12), и тех, что образуются покровным белком РНК-фага АР205, практически неразличимы при наблюдении с помощью ЭМ. VLP AP205 высоко иммуногенны и могут быть связаны с антигенами и/или антигенными детерминантами для получения вакцинных конструкций, презентирующих антигены и/или антигенные детерминанты, ориентированные повторяемым образом. Против презентированных таким образом антигенов генерируются высокие титры, что указывает на доступность связанных антигенов и/или антигенных детерминант для взаимодействия с молекулами антитела и на их иммуногенность.
В дальнейшем предпочтительном осуществлении настоящего изобретения вирусоподобная частица содержит, или, альтернативно, по существу состоит, или, альтернативно, состоит из рекомбинантных мутантных покровных белков РНК-фага АР205, или их фрагментов.
Способные к сборке мутантные формы VLP AP205, включающие покровные белки АР205 с заменой пролина в положении 5 на треонин (SEQ ID NO: 13), также могут использоваться при воплощении изобретения, что приведет к дальнейшему предпочтительному осуществлению изобретения. Данные VLP, VLP AP205, происходящие из природных источников, или вирусные частицы АР205 могут быть связаны с антигенами для продукции упорядоченных повторяемых мотивов антигенов по настоящему изобретению.
Мутантный покровный белок Р5-Т АР205 может экспрессироваться с плазмиды рАР281-32 (SEQ ID NO: 14), которая является непосредственным производным от pQb185 и которая содержит мутантный ген покровного белка АР205 вместо гена покровного белка Qβ. Векторами для экспрессии покровного белка АР205 трансфицируют Е. coli для экспрессии покровного белка АР205.
Способы экспрессии покровного белка и мутантного покровного белка, соответственно, приводящие к самопроизвольной сборке VLP, описаны в одновременно находящейся на рассмотрении предварительной заявке на выдачу патента США № 60/396126, поданной 17 июля 2002 г., которая включена сюда полностью в качестве ссылки. Подходящие. штаммы Е. coli включают в качестве не ограничивающих примеров Е. coli K802, JM 109, RR1. Подходящие векторы и штаммы, и их комбинации могут идентифицироваться путем тестирования экспрессии покровного белка и мутантного покровного белка, соответственно, посредством SDS-PAGE, и образования и сборки капсида необязательно вначале путем очистки капсида гель-фильтрацией и затем путем их тестирования в анализе иммунодиффузии (тест Оухтерлони) или электронной микроскопией (Kozlovska, Т.М. et al., Gene 137: 133-37 (1993)).
Покровные белки АР205, экспрессируемые с векторов рАР283-58 и рАР281-32, могут быть лишены начальной аминокислоты метионина вследствие процессинга в цитоплазме Е. coli. Расщепленные, нерасщепленные формы VLP AP205 или их смеси представляют собой дальнейшие осуществления настоящего изобретения.
В дальнейшем предпочтительном осуществлении настоящего изобретения вирусоподобная частица содержит, или, альтернативно, по существу состоит, или, альтернативно, состоит из смеси рекомбинантных покровных белков РНК-фага АР205 или их фрагментов, и рекомбинантных мутантных покровных белков РНК-фага АР205 или их фрагментов.
В дальнейшем предпочтительном осуществлении настоящего изобретения вирусоподобная частица содержит, или, альтернативно, по существу состоит, или, альтернативно, состоит из фрагментов рекомбинантных покровных белков или рекомбинантных мутантных покровных белков РНК-фага АР205.
Фрагменты рекомбинантного покровного белка АР205, способные к самопроизвольной сборке в VLP и капсид, соответственно, также могут использоваться при воплощении настоящего изобретения. Данные фрагменты могут генерироваться путем делеции, внутренней или с концов покровного белка и мутантного покровного белка, соответственно. Вставки в последовательность покровного белка и мутантного покровного белка или слияния с последовательностью покровного белка и мутантного покровного белка антигенных последовательностей, совместимые со сборкой в VLP, представляют собой дальнейшие осуществления изобретения и ведут к образованию химерных покровных белков АР205 и частиц, соответственно. Исход вставок, делеций и слияний с последовательностью покровного белка и то, совместимы ли они со сборкой в VLP, может определяться путем электронной микроскопии.
Частицы, образованные покровным белком АР205, фрагментами покровного белка и химерными покровными белками, описанными выше, могут быть выделены в чистой форме путем комбинации стадий фракционирования путем преципитации и стадий очистки путем гель-фильтрации, например, с использованием колонок Sepharose CL-4B, Sepharose CL-2B, Sepharose CL-6B и их комбинаций, как описано в одновременно находящейся на рассмотрении предварительной заявке на выдачу патента США № 60/396126, поданной 17 июля 2002 г., которая включена сюда полностью в качестве ссылки. Другие способы выделения вирусоподобных частиц известны в данной области и могут использоваться для выделения вирусоподобных частиц (VLP) бактериофага АР205. Например, применение ультрацентрифугирования для выделения VLP дрожжевого ретротранспозона Ту описано в патенте США № 4918166, включенном сюда полностью в качестве ссылки.
По настоящему изобретению одна или несколько ангиотензиновых пептидных составляющих могут связываться с одной субъединицей капсида покровных белков РНК-фагов. Возможность присоединять различные ангиотензиновые пептидные составляющие к субъединице капсида покровного белка РНК-фагов и, в частности, капсида Qβ обеспечивает генерирование плотного мотива ангиотензиновых пептидных составляющих. Другие вирусные капсиды могут использоваться для ковалентного присоединения ангиотензиновых пептидных составляющих путем химического перекрестного связывания, как, например, HBcAg, модифицированный в его главной иммунодоминантной области остатком лизина (MIR; WO 00/32227). Расстояние между выступами (соответствующими MIR) HBcAg составляет 50 Å (Wynne, SA. et al., Mol Cell 3:771-780 (1999)), и поэтому не может быть образован мотив ангиотензиновых пептидных составляющих с расстояниями короче 50 Å.
Капсиды из покровного белка Qβ презентируют на своей поверхности определенное число остатков лизина с определенной топологией, где три остатка лизина направлены внутрь капсида и взаимодействуют с РНК, а четыре других остатка лизина экспонированы на внешнюю часть капсида. Данные определенные свойства способствуют присоединению ангиотензиновых пептидных составляющих на внешнюю часть частицы, но не на внутреннюю часть, где остатки лизина взаимодействуют с РНК. Капсиды из покровных белков других РНК-фагов также характеризуются определенным числом остатков лизина на своей поверхности и ограниченной топологией данных остатков лизина. Другим преимуществом капсидов, происходящих из РНК-фагов, является их высокая экспрессия в бактериях, которая обеспечивает продукцию больших количеств материала по доступной цене.
Другой характеристикой капсида из покровного белка Qβ является его стабильность. Субъединицы Qβ связаны друг с другом дисульфидными мостиками, ковалентно связывающими субъединицы. Капсидный белок Qβ также проявляет необычную устойчивость к органическим растворителям и денатурирующим агентам. Авторами настоящего изобретения неожиданно обнаружено, что такие высокие концентрации ДМСО и ацетонитрила, как примерно 30%, и такие высокие концентрации гуанидина, как примерно 1 М, могут использоваться без нарушения стабильности или способности образовывать мотивы ангиотензиновых пептидных составляющих. Таким образом, данные органические растворители могут использоваться для присоединения гидрофобных молекул, таких как некоторые ангиотензиновые пептидные. составляющие. Высокая стабильность капсида из покровного белка Qβ является важной характеристикой, относящейся к его применению для иммунизации и вакцинации млекопитающих и, в частности, людей. Устойчивость данного капсида к органическому растворителю дает возможность для связывания тех ангиотензиновых пептидных составляющих или их производных, которые не растворимы в водных буферах.
Вставка остатка цистеина в N-концевую β-шпильку покровного белка РНК-фага MS-2 описана в патенте США № 5698424, который включен сюда полностью в качестве ссылки. Однако авторами настоящего изобретения отмечено, что наличие экспонированных свободных остатков цистеина в капсиде может приводить к олигомеризации капсидов путем образования дисульфидных мостиков. Другие связи, рассмотренные в указанном выше патенте США, относятся к образованию дисульфидных мостиков между ангиотензиновыми пептидными составляющими и частицей Qβ. Такие связи неустойчивы к воздействию молекул, содержащих сульфгидрильную связь.
Взаимодействие между исходным дисульфидным мостиком, образованным остатком цистеина на Qβ, и антигеном, содержащим свободную сульфгидрильную группу, приводит к образованию видов молекул, содержащих сульфгидрил, отличных от ангиотензиновой пептидной составляющей. Данные вновь образованные, содержащие сульфгидрил виды молекул могут взаимодействовать с другими дисульфидными мостиками, присутствующими на частице, и так устанавливается равновесие. После взаимодействия с дисульфидным мостиком, образованным на частице, ангиотензиновая пептидная составляющая может образовывать дисульфидный мостик с остатком цистеина на частице или с остатком цистеина на молекуле уходящей группы, которая образовывала исходный дисульфидный мостик на частице. Более того, описан другой способ связывания, где используется гетеробифункциональный перекрестный линкер, взаимодействующий с цистеином на частице Qβ с одной стороны, и с остатком лизина на ангиотензиновой пептидной составляющей с другой стороны, что может приводить к случайной ориентации ангиотензиновых пептидных составляющих на частице.
Кроме того, авторами настоящего изобретения отмечено, что в отличие от капсида из покровных белков Qβ и Fr рекомбинантный MS-2, описанный в патенте США 5698424, по существу, свободен от нуклеиновых кислот, в то время как внутрь двух упомянутых выше капсидов упакована РНК.
Здесь авторами настоящего изобретения описаны новые и изобретенные конъюгаты и конъюгаты, обеспечивающие образование плотных мотивов ангиотензиновых пептидных составляющих с вариабельной плотностью. ангиотензиновых эпитопов в конъюгатах. Авторами настоящего изобретения показано, что за счет присоединения ангиотензиновых пептидных составляющих к VLP может достигаться очень высокая плотность эпитопов. Кроме того, плотность и разбивка ангиотензиновых пептидных составляющих может модифицироваться путем изменения числа и типа остатков с подходящим первым участком связывания. Например, в одновременно ожидающей решения заявке на выдачу патента США № 10/050902, поданной 18 января 2002 г., описан мутантный покровный белок Qβ с дополнительными остатками лизина, подходящими для получения мотивов более высокой плотности, чем наблюдается с использованием покровного белка Qβ дикого типа. Далее, в указанной выше заявке также описаны конъюгаты, подходящие для одновременной презентации нескольких антигенов с подходящей разбивкой, и конъюгаты с добавлением дополнительных молекул, с усилением растворимости или с модификацией капсида подходящим и предпочтительным образом. Другие мутантные покровные белки Qβ, образующие капсиды, которые представляют собой вирусоподобные частицы, описаны в одновременно ожидающей решения заявке на выдачу патента США №10/050902 и являются подходящими для получения композиций по изобретению. В частности, в случаях, где растворимость ангиотензиновых пептидных составляющих и основанного на Qβ антигенного мотива ангиотензиновых пептидов определяет лимит количества ангиотензиновых пептидных составляющих, которые могут присоединяться к вирусоподобной частице Qβ, могут использоваться мутанты, в которых остатки лизина замещены аргининами, которые не обладают той же реакционной способностью, что остатки лизина. При получении данных композиций высокая концентрация ангиотензиновой пептидной составляющей или ангиотензиновой пептидной составляющей, модифицированной так, чтобы она содержала второй участок связывания, может использоваться для достижения полной реакции с остатками лизина на мутантных Qβ-вирусоподобных частицах без образования потенциально нерастворимых частиц с большим количеством присоединенных ангиотензиновых пептидных составляющих, как в случае использования частицы,. подобной вирусу Qβ дикого типа.
Была определена кристаллическая структура некоторых РНК-бактериофагов (Golmohammadi, R. et al., Structure 4:543-554 (1996)). С использованием такой информации специалист в данной области легко сможет идентифицировать экспонированные на поверхность остатки и модифицировать покровные белки бактериофага, так что может быть встроен один или несколько реакционноспособных аминокислотных остатков. Таким образом, специалист в данной области легко может генерировать и идентифицировать модифицированные формы покровных белков бактериофагов, которые могут использоваться при воплощении изобретения. Таким образом, для получения вакцинных конъюгатов по настоящему изобретению могут использоваться варианты белков, которые образуют капсиды или подобные капсидам структуры (например, покровные белки бактериофага Qβ, бактериофага R17, бактериофага fr, бактериофага GA, бактериофага SP и бактериофага MS2).
Хотя последовательность обсуждаемых выше вариантных белков отличается от их дубликатов дикого типа, данные вариантные белки в основном сохраняют способность образовывать капсиды или подобные капсидам структуры. Таким образом, изобретение далее относится к вакцинным конъюгатам, которые содержат варианты белков, которые образуют капсиды или подобные капсидам структуры, а также к способам. получения таких вакцинных конъюгатов, индивидуальных белковых субъединиц, используемых для получения таких вакцинных конъюгатов. Так, в объем изобретения входят вариантные формы белков дикого типа, которые образуют упорядоченные и повторяемые мотивы (например, варианты белков, которые образуют капсиды или подобные капсидам структуры) и сохраняют способность ассоциировать и образовывать капсиды и подобные капсидам структуры. Обычно, С- и N-концевые укороченные варианты сохраняют способность образовывать вирусоподобные частицы. В результате, вариантные формы, содержащие делецию, добавление или замену, химерные формы и встречающиеся в природе варианты представляют собой подходящие компоненты по настоящему изобретению.
Бактериальные пили и белок пилин. В других осуществлениях бактериальный пилин, часть бактериального пилина или белок слияния, который содержит бактериальный пилин или его часть, используют для получения вакцинных конъюгатов по изобретению. Примеры белков пилинов включают пилины, продуцируемые Escherichia coli, Haemophilus influenzae, Neisseria meningitidis, Neisseria gonorrhoeae, Caulobacter crescentus, Pseudomonas stutzeri и Pseudomonas aeruginosa. Аминокислотные последовательности белков пилинов, подходящие для применения по настоящему изобретению, включают те, что установлены в отчетах GenBank AJ000636, AJ132364, AF229646, AF051814, AF051815 и Х00981, полное описание которых включено сюда в качестве ссылки.
Белки бактериального пилина главным образом процессируются с удалением N-концевых лидерных последовательностей перед экспортом белков в бактериальную периплазму. Далее, что понятно специалисту в данной области, белки бактериального пилина, используемые для получения вакцинных конъюгатов по изобретению, в основном не будут содержать присутствующей в природе лидерной последовательности.
Одним из конкретных примеров белка пилина, подходящего для применения по настоящему изобретению, является Р-пилин Е. coli (отчет GenBank AF237482). Примером пилина типа-1 Е. coli, подходящего для применения по изобретению, является пилин, характеризующийся аминокислотной последовательностью, установленной в отчете GenBank P04128 (SEQ ID NO: 2), которая кодируется нуклеотидной последовательностью, установленной в отчете GenBank M27603. Полные описания данных отчетов GenBank включены сюда в качестве ссылки. Опять для получения вакцинных конъюгатов по изобретению используется зрелая форма указанных выше белков.
Бактериальные пилины или части пилинов, подходящие для применения при воплощении настоящего изобретения, в основном могут ассоциировать с образованием неприродных молекулярных каркасов. Способы получения пилей и структур, подобных пилям, in vitro известны в данной области. Bullitt et al., Proc. Natl. Acad. Sci. USA 93:12890-12895 (1996), например/ описывают реконституцию in vitro субъединиц Р-пилей E. coli. Далее, Eshdat et al. (J. Bacteriol. 148:308-314 (1981)) описывают способы, подходящие для диссоциации пилей типа-1 Е. coli и реконституции пилей. В кратком изложении данные способы следующие: пили диссоциируют за счет инкубации при 37°С в насыщенном гуанидина гидрохлориде. Белки пилины затем очищают хроматографией, после чего димеры пилина формируют путем диализа против 5 мМ трис(гидроксиметил)аминометана гидрохлорида (рН 8,0). Eshdat et al. также обнаружили, что димеры пилина повторно объединяются с образованием пилей при диализе против 5 мМ трис(гидроксиметил)аминометана гидрохлорида (рН 8,0), содержащего 5 мМ MgCl2.
Далее, с использованием, например, общепринятых способов генной инженерии и модификации белка, белки пилины могут модифицироваться так, чтобы они содержали первый участок связывания, к которому присоединяется ангиотензиновая пептидная составляющая, через второй участок связывания. Альтернативно, ангиотензиновые пептидные составляющие могут быть непосредственно связаны через второй участок связывания с аминокислотными остатками, которые присутствуют на данных белках в природе. Данные модифицированные белки пилины могут затем использоваться для иммунизирующих конъюгатов по изобретению.
Бактериальные белки пилины, используемые для получения конъюгатов по изобретению, могут модифицироваться способом, сходным с тем, что описан здесь для HBcAg. Например, остатки цистеина и лизина могут подвергаться делеции или замене на другие аминокислотные остатки, и к данным белкам могут быть добавлены первые участки связывания. Далее, белки пилины могут экспрессироваться в модифицированной форме или могут быть химически модифицированы после экспрессии. Сходным образом, интактные пили могут собираться от бактерий и затем модифицироваться химически.
В другом осуществлении пили или подобные пилям структуры собирают от бактерий (например, Е. coli) и используют для образования вакцинных конъюгатов по изобретению. Одним из примеров пилей, подходящих для получения вакцинных конъюгатов, является пиль типа-1 Е. coli, который образуется из мономеров пилина, обладающих. аминокислотной последовательностью, представленной в SEQ ID NO: 2.
В данной области известно несколько способов сбора бактериальных пилей. Например, Bullitt and Makowski (Biophys. J. 74:623-632 (1998)) описывают способ очистки пиля для сбора Р-пилей Е. coli. По данному способу пили срезают с Е. coli с повышенным количеством пилей, содержащей плазмиду Р-пилей, и очищают путем солюбилизации и преципитацией MgCl2 (1,0 М). В одновременно ожидающей решения заявке на выдачу патента США № 10/050902, поданной 18 января 2002 г., описаны сбор и очистка пилей типа-I от бактерий, которые продуцируют пили в природе, или от тех, в которые был введен вектор, кодирующий оперон fim, ответственный за продукцию пилей.
После сбора пили и подобные пилям структуры могут модифицироваться различными путями. Например, к пилям может добавляться первый участок связывания, к которому может присоединяться одна или несколько ангиотензиновых пептидных составляющих посредством второго участка связывания. Другими словами, бактериальные пили и подобные пилям структуры могут собираться и модифицироваться с образованием неприродных молекулярных каркасов.
Пили и подобные пилям структуры также можно модифицировать путем связывания ангиотензиновых пептидных составляющих в отсутствие неприродного первого участка связывания. Например, антигены или антигенные детерминанты могут связываться с встречающимися в природе остатками цистеина или остатками лизина. В таких случаях высокая упорядоченность и повторяемость встречающегося в природе аминокислотного остатка будет направлять связывание ангиотензиновых пептидных составляющих с пилями и подобными пилям структурами. Например, пили или подобные пилям структуры могут связываться со вторыми участками связывания ангиотензиновых пептидных составляющих с использованием гетеробифункционального перекрестно-связывающего агента.
Когда структуры, которые синтезируются организмами в природе (например, пили), используют для получения вакцинных конъюгатов по изобретению, часто будет предпочтительным генетическое конструирование данных организмов с тем, чтобы они продуцировали структуры, имеющие требуемые характеристики. Например, при использовании пилей типа-1 Е. coli, E. coli, из которой отбирают данные пили, может модифицироваться так, что она будет продуцировать структуры с конкретными характеристиками. Примеры возможных модификаций белков-пилинов включают вставку одного или нескольких остатков лизина, делецию или замену одного или нескольких присутствующих в природе остатков лизина и делецию или замену одного или нескольких присутствующих в природе остатков цистеина (например, остатков цистеина в позициях 44 и 84 в SEQ ID NO: 2).
Далее могут проводиться дополнительные модификации генов пилина, которые приводят к образованию продуктов экспрессии, содержащих первый участок связывания, отличный от остатка лизина (например, домен FOS или JUN). Подходящие первые участки связывания, конечно, в основном ограничены теми, которые не предотвращают образование из белков пилинов пилей или подобных пилям структур, подходящих для применения в вакцинных конъюгатах по настоящему изобретению. Способность рекомбинантных белков пилинов образовывать пили может определяться рядом способов, включая электронную микроскопию.
Гены пилина, которые находятся в бактериальных клетках в природе, могут модифицироваться in vivo (например, путем гомологичной рекомбинации), или гены пилина с конкретными характеристиками могут встраиваться в данные клетки. Например, гены пилина могут вводиться в бактериальные клетки в качестве компонента реплицируемого клонирующего вектора или вектора, который встраивается в бактериальную хромосому. Встроенные гены пилина могут также связываться с последовательностями регуляции контроля экспрессии (например, оператором lac).
Во многих случаях, пили или подобные пилям структуры, применяемые в вакцинных конъюгатах по настоящему изобретению, состоят из одного типа субъединиц пилина. Однако конъюгаты по изобретению также включают вакцины, содержащие пили и подобные пилям структуры, образованные из гетерогенных субъединиц пилина. Пили или подобные пилям структуры, состоящие из идентичных субъединиц, в основном могут использоваться, поскольку ожидается, что они образуют структуры, представляющие высокоупорядоченные и повторяемые антигенные мотивы.
Второй участок связывания. Препараты молекулярных каркасов с упорядоченными и повторяемыми мотивами предоставлены так, что они включают конъюгаты капсидов из покровных белков РНК-фагов с высокой плотностью эпитопов. Природа ангиотензиновой пептидной составляющей и природа и локализация второго участка связывания на данной составляющей являются важными факторами, которые могут воздействовать на средства, доступные для конструирования конъюгатов по изобретению, и на эффективность данных конъюгатов для индукции иммунного ответа, что может быть ясно обычному специалисту в данной области.
Предпосылки для конструирования второго участка связывания включают выбор положения, в котором он должен быть присоединен, встроен или, в общем, сконструирован или связан. Специалисту в данной области известно, как найти руководство по выбору положения для второго участка связывания, и многие факторы могут считаться имеющими отношение к данному решению. Химическая и/или кристаллическая структура ангиотензиновой пептидной составляющей может предоставить информацию о доступности доменов молекулы, подходящей для связывания. Доступность реакционноспособного домена для растворителя может быть ограничительным фактором для кинетики химического связывания с первым участком связывания. Должны быть доступны группы, подходящие для связывания, такие как сульфгидрильные остатки. В основном, в случае, когда иммунизация ангиотензиновой пептидной составляющей способствует ингибированию взаимодействия ангиотензиновой пептидной составляющей, которая также может представлять собой аутоантиген, с его природными лигандами, такими как субстрат или рецептор, второй участок связывания добавляется так, что он обеспечивает образование антител против участка взаимодействия с природными лигандами. Таким образом, локализация второго участка связывания выбирается так, что избегается стерическое препятствие от второго участка связывания или какого-либо содержащего его аминокислотного линкера. В дальнейших осуществлениях требуется ответ в виде антител, направленных на участок, отличный от участка взаимодействия антигена с его природным лигандом. В таких осуществлениях второй участок связывания может быть выбран так, что он предотвращает образование антител против участка связывания антигена с его природными лигандами. Другие рассматриваемые факторы включают природу ангиотензиновой пептидной составляющей, ее биохимические свойства, такие как pI, распределение заряда, дальнейшая модификация. В основном, предпочтительными являются гибкие линкеры.
Другие критерии выбора положения второго участка связывания включают состояние олигомеризации ангиотензиновой пептидной составляющей, сайт олигомеризации, присутствие кофактора и наличие экспериментального доказательства, раскрывающего участки в структуре составляющей и последовательности, где модификация составляющей совместима с ее функционированием или с получением антител, распознающих данную составляющую и, предпочтительно, блокирующих функцию ангиотензиновой пептидной составляющей. В некоторых осуществлениях одну или несколько дополнительных аминокислот (приводящих к образованию не встречающегося в природе второго участка связывания) добавляют или с С- или с N-конца последовательностей ангиотензиновых пептидных составляющих для обеспечения, в частности, ориентированной и упорядоченной ассоциации ангиотензиновой пептидной составляющей с вирусоподобной частицей согласно настоящему изобретению.
Особенно предпочтительным способом присоединения полипептидных антигенов к VLP, и, в частности, к капсидам из покровных белков РНК-фагов, является связывание остатка лизина на поверхности капсида из покровных белков РНК-фага с остатком сульфгидрильной группы на антигене, таким как находящийся в остатках цистеина. Сходным образом, свободные сульфгидрильные группы на ангиотензиновых пептидных составляющих могут также представлять собой эффективные участки связывания. Там, где окисленные сульфгидрильные группы должны быть в восстановленном состоянии для функционирования в качестве второго участка связывания, может достигаться восстановление, например, при помощи DTT, ТСЕР или β-меркаптоэтанола.
По настоящему изобретению, эпитопная плотность на капсиде из покровных белков РНК-фага может модулироваться путем выбора перекрестного линкера и других условий реакции. Например, перекрестные линкеры Sulfo-GMBS и SMPH позволяют достигать высокой эпитопной плотности. На получение производных положительно влияет высокая концентрация реагентов, и для того, чтобы контролировать количество антигенов, связанных с капсидными белками РНК-фага, и в особенности с капсидным белком Qβ, может использоваться манипуляция условиями реакции. Кроме того, количество первых участков связывания на коровой частице является другим фактором, влияющим на плотность мотива ангиотензиновой пептидной составляющей. В одном из осуществлений настоящего изобретения, авторы настоящего изобретения предоставляют мутантный покровный белок Qβ с дополнительными остатками лизина, подходящий для получения мотива с более высокой плотностью.
В самых предпочтительных осуществлениях ангиотензиновая пептидная составляющая включает один второй участок связывания или один реакционноспособный участок связывания, способный к ассоциации с первыми участками связывания на коровой частице и на VLP или субъединицах VLP, соответственно. Это обеспечивает определенное и однородное связывание и ассоциацию, соответственно, по крайней мере, одного, но типично более одного, предпочтительно более 10, 20, 40, 80, 120 антигенов с коровой частицей и VLP, соответственно. Предоставление одного второго участка связывания или одного реакционноспособного участка связывания на антигене, таким образом, обеспечивает единственный и однородный тип связывания и ассоциации, соответственно, приводя к образованию очень высоко упорядоченного и повторяемого мотива. Например, если связывание и ассоциация, соответственно, осуществлены посредством взаимодействия с лизином (в качестве первого участка связывания) и цистеином (в качестве второго участка связывания), то это обеспечивает то, по данному предпочтительному осуществлению изобретения, что только один остаток цистеина на антиген, независимо от того, присутствует ли этот остаток цистеина на антигене природно или неприродно, способен к связыванию и ассоциации, соответственно, с VLP и с первым участком связывания на коровой частице, соответственно.
В дальнейшем предпочтительном осуществлении изобретения ковалентной является непептидная связь.
В некоторых осуществлениях, для инженерии второго участка связывания на антигене требуется слияние аминокислотного линкера, содержащего подходящую в качестве второго участка связывания аминокислоту по описанию данного изобретения. Поэтому, в предпочтительном осуществлении настоящего изобретения аминокислотный линкер связывается с антигеном или антигенной детерминантой посредством, по крайней мере, одной ковалентной связи. Предпочтительно, аминокислотный линкер включает или, альтернативно, состоит из второго участка связывания. В дальнейшем предпочтительном осуществлении аминокислотный линкер включает сульфгидрильную группу или остаток цистеина. В другом предпочтительном осуществлении аминокислотным линкером является цистеин. Выше уже упоминались некоторые критерии выбора аминокислотного линкера так же, как и дальнейшие предпочтительные осуществления аминокислотного линкера по изобретению.
В дальнейшем предпочтительном осуществлении изобретения, по крайней мере, один антиген или антигенная детерминанта, а именно. молекула ангиотензинового белка, объединяется с коровой частицей и с вирусоподобной частицей, соответственно. Как отмечено выше, VLP обычно формируется, по крайней мере, из одной субъединицы, собирающейся в VLP. Таким образом, снова в дальнейшем предпочтительном осуществлении изобретения антиген или антигенная детерминанта, предпочтительно, по крайней мере, одна ангиотензиновая пептидная составляющая, объединяется, по крайней мере, с одной субъединицей вирусоподобной частицы или со способным включаться в VLP белком, с образованием химерного слияния VLP-субъединица - ангиотензиновая пептидная составляющая.
Слияние ангиотензиновых пептидных составляющих может осуществляться посредством вставки в последовательность субъединицы VLP, или посредством слияния либо с N-, либо С-концом VLP-субъединицы, либо способных включаться в VLP белком. В дальнейшем, при ссылке на белки слияния пептидов с субъединицей VLP подразумевается слияние либо концов последовательности субъединицы, либо внутренняя вставка пептида в последовательность субъединицы.
Слияние может также осуществляться посредством вставки последовательности ангиотенэиновой пептидной составляющей в разновидность субъединицы VLP, где была удалена часть последовательности субъединицы, что далее обозначается как укороченные мутанты. У укороченных мутантов могут быть N- или С-концевые или внутренние делеции части последовательности субъединицы VLP. Например, конкретный HBcAg VLP с делецией, например, с 79 по 81 аминокислотный остаток является укороченным мутантом с внутренней делецией. Слияние ангиотенэиновой пептидной составляющей или с N- или С-концом VLP-субъединиц укороченных мутантов также приводит к осуществлениям изобретения. Подобным образом, слияние эпитопа с последовательностью субъединицы VLP также может осуществляться путем замены, где, например, для конкретного HBcAg VLP аминокислоты 79-81 заменяются на инородный эпитоп. Таким образом, слияние, как обозначено в дальнейшем, может осуществляться путем вставки последовательности ангиотензиновой пептидной составляющей в последовательность субъединицы VLP, посредством замены части последовательности субъединицы VLP на последовательность ангиотензиновой пептидной составляющей или путем комбинации делеции, замены или вставок.
Химерные белки, ангиотензиновая пептидная составляющая - VLP-субъединица, в основном, будут способны самопроизвольно объединяться в VLP. VLP, представляющие слитые со своими субъединицами эпитопы, также здесь обозначаются как химерные VLP. Как указано, вирусоподобная частица включает или, альтернативно, состоит, по крайней мере, из одной субъединицы VLP. В дальнейшем осуществлении изобретения вирусоподобная частица включает или, альтернативно, состоит из смеси химерных субъединиц VLP и нехимерных субъединиц VLP, а именно субъединиц VLP, не имеющих с ними слитого антигена, приводя к образованию так называемых мозаичных частиц. Это может быть благоприятно для обеспечения образования и сборки в VLP. В данных осуществлениях соотношение химерных VLP-субъединиц может быть 1, 2, 5, 10, 20, 30, 40, 50, 60, 70, 80, 90, 95% или выше.
Фланкирующие аминокислотные остатки могут добавляться либо к концу последовательности пептида, либо к эпитопу, сливаемому с любым из концов последовательности субъединицы VLP, либо в качестве внутренней вставки такой пептидной последовательности в последовательность субъединицы VLP. Остатки глицина и серина являются особенно благоприятными для того, чтобы использоваться во фланкирующих последовательностях, добавляемых к ангиотензиновой пептидной составляющей, подвергаемой слиянию. Остатки глицина привносят дополнительную гибкость, которая может уменьшить потенциально дестабилизирующий эффект слияния инородной последовательности с последовательностью субъединицы VLP.
В конкретном осуществлении изобретения VLP является VLP из корового антигена гепатита В. Были описаны белки слияния или с N-концом HBcAg (Neyrinck, S. et al., Nature Med. 5: 1157-1163 (1999)) или со вставками в так называемой главной иммунодоминантной области (MIR) (Pumpens, P. and Grens, E., Intervirology 44: 98-114 (2001), WO 01/98333), и они являются предпочтительными осуществлениями изобретения. Также были описаны встречающиеся в природе варианты HBcAg с делециями в MIR (Pumpens, P. and Grens, E., Intervirology 44: 98-114 (2001), которые включены сюда полностью в качестве ссылки), и слияния с N- или С-концом, так же как и вставки в положение MIR, соответствующее месту делеции по сравнению с HBcAg дикого типа, являются дальнейшими осуществлениями изобретения. Также были описаны слияния с С-концом (Pumpens, P. and Grens, E., Intervirology 44: 98-114 (2001)). Специалисты в данной области легко обнаружат руководство, как, используя классические молекулярно-биологические методы, конструировать белки слияния (Sambrook, J. et al., eds., Molecular Cloning, A Laboratory Manual, 2nd. edition, Cold Spring Habor Laboratory Press, Cold Spring Harbor, N.Y. (1989), Ho et al., Gene 77: 51 (1989)). Были описаны векторы и плазмиды, кодирующие HBcAg и белки слияния HBcAg и пригодные для экспрессии HBcAg и белков слияния HBcAg (Pumpens, P. & Grens, E. Intervirology 44: 98-114 (2001), Neyrinck, S. et al., Nature Med. 5: 1157-1163 (1999)), и они могут использоваться в воплощении изобретения. Также авторы настоящего изобретения описывают посредством примера (пример 6) вставку эпитопа в MIR HBcAg, приводящую к образованию химерного самопроизвольно объединяющегося HBcAg. Важным фактором для оптимизации эффективности самопроизвольного объединения и представления эпитопов, которые будут вставлены в MIR HBcAg, является выбор участка вставки, так же как количество аминокислот, которые будут удалены из последовательности HBcAg внутри MIR при вставке (Pumpens, P. and Grens, E., Intervirology 44: 98-114 (2001); ЕР 421635; US 6231864), или, другими словами, какие аминокислоты из HBcAg должны заменяться новым эпитопом. Например, была описана замена 76-80, 79-81, 79-80, 75-85 или 80-81 аминокислот HBcAg на инородные эпитопы (Pumpens, P. and Grens, E., Intervirology 44: 98-114 (2001); ЕР0421635; US 6231864). HBcAg содержит длинный конец из аргинина (Pumpens, P. and Grens, E., Intervirology 44: 98-114 (2001)), который несущественен для сборки в капсид и способен к связыванию нуклеиновых кислот (Pumpens, P. and Grens, E., Intervirology 44: 98-114 (2001)). Оба HBcAg, или включающие, или не имеющие такой конец из аргинина, являются осуществлениями изобретения.
В дальнейшем предпочтительном осуществлении изобретения VLP является VLP РНК-фага. Основные покровные белки РНК-фагов при экспрессии в бактерии, и в особенности в Е. coli, самопроизвольно собираются в. VLP. Конкретные примеры покровных белков бактериофагов, которые могут использоваться для создания композиций по изобретению, содержат покровные белки РНК-бактериофагов, таких как бактериофаг Qβ (SEQ ID NO: 3; база данных PIR, инвентарный номер VCBPQβ, относящийся к GP Qβ, и SEQ ID NO: 4; инвентарный номер ААА16663, относящийся к белку A1 Qβ) и бактериофаг fr (SEQ ID NO: 33; инвентарный номер PIRVCBPFR).
В наиболее предпочтительном осуществлении, по крайней мере, одна ангиотензиновая пептидная составляющая слита с покровным белком Qβ. Были описаны конструкции белков слияния, где эпитопы сливались с С-концом укороченной формы белка A1 Qβ или вставлялись в белок A1 (Kozlovska, Т.М., et al., Intervirology, 39: 9-15 (1996)). Белок A1 образуется путем суппрессии в стоп-кодоне UGA и имеет длину в 329 а.к. или 328 а.к., если принимать во внимание отщепление N-концевого метионина. Обычно отщепление N-концевого метионина перед аланином (второй аминокислоты, кодируемой, геном СР Qβ) имеет место у Е. coli, и то же самое происходит в случае с N-концом покровных белков СР Qβ. Часть гена А1, 3' от амбер-кодона UGA, кодирует продление СР, которое имеет в длину 195 аминокислот. Вставка, по крайней мере, одной ангиотензиновой пептидной составляющей в положение между 72 и 73 продления СР приводит к дальнейшим осуществлениям изобретения (Kozlovska, Т.М., et al., Intervirology 39: 9-15 (1996)). Слияние ангиотензиновой пептидной составляющей с С-концом укороченного с С-конца белка A1 Qβ приводит к дальнейшим предпочтительным осуществлениям настоящего изобретения. Например, Kozlovska et al. (Intervirology, 39: 9-15 (1996)) описали слияния белков A1 Qβ, где эпитоп слит с С-концом укороченного в положении 19 продления СР Qβ.
Как описано у Kozlovska et al. (Intervirology, 39: 9-15 (1996)) для сборки частиц, представляющих слитые эпитопы, типично необходимо наличие и слияния белок А1 - ангиотензиновая пептидная составляющая, и СР дикого типа для образования мозаичной частицы. Несмотря на это, осуществления, включающие вирусоподобные частицы, и, таким образом, в особенности, VLP из покровного белка РНК-фага Qβ, которые формируются исключительно из субъединиц VLP, имеющих, по крайней мере, одну слитую с ней ангиотензиновую пептидную составляющую, также находятся в области настоящего изобретения.
Продукция мозаичных частиц может осуществляться рядом способов. Kozlovska et al., Intervirolog, 39: 9-15 (1996) описали два способа, которые оба могут использоваться в воплощении изобретения. В первом подходе эффективное представление слитых эпитопов на VLP опосредовано экспрессией плазмиды, кодирующей слияние белка A1 Qβ, содержащее стоп-кодон UGA, между СР и продлением СР, в штамме E. coli, несущем плазмиду, кодирующую клонированную UGA-супрессорную тРНК, что приводит к трансляции UGA-кодона в Тгр (плазмида pISM3001 (Smiley В. К., et al., Gene 134: 33-40 (1993))). В другом подходе стоп-кодон гена СР модифицируется в UAA, и вторая плазмида, экспрессирующая слияние белка А1 и ангиотензиновой пептидной составляющей, трансформируется совместно. Вторая плазмида кодирует разного вида резистентность к антибиотикам и начало репликации согласовано с первой плазмидой (Kozlovska, Т.М., et al., Intervirology 39: 9-15 (1996)). В третьем подходе СР и слияние белка А1 с ангиотензиновой пептидной составляющей кодируется бицистронным способом, функционально связанным с таким промотором, как промотор Тгр, как описано на фиг.1 у Kozlovska et al., Intervirology 39: 9-15 (1996).
В дальнейшем осуществлении ангиотензиновая пептидная составляющая встраивается между 2 и 3 аминокислотой (нумерация отщепленного СР, то есть оттуда, откуда отщеплен N-концевой метионин) СР fr, таким образом, приводя к образованию белка слияния ангиотензиновой пептидной составляющей с СР fr. Были описаны полезные для воплощения настоящего изобретения векторы и экспрессионные системы для конструкции и экспрессии самопроизвольно собирающихся в VPL белков слияния СР fr (Pushko P. et al., Prot. Eng. 6: 883-891 (1993)). В конкретном осуществлении последовательность ангиотензиновой пептидной составляющей встраивают в разновидность делеции после аминокислоты 2, где были удалены остатки 3 и 4 СР fr (Pushko P. et al., Prot. Eng.6: 883-891 (1993)).
Также было описано слияние эпитопов в N-концевой выступающей β-шпильке покровного белка MS-2 РНК-фага и последующее представление слитого эпитопа на самопроизвольно собирающейся VLP из MS-2 РНК-фага (WO 92/13081), и слияние ангиотензиновой пептидной составляющей путем вставки или замещения внутри покровного белка MS-2 РНК-фага также попадает в область настоящего изобретения.
В другом осуществлении настоящего изобретения ангиотензиновые пептидные составляющие слиты с капсидным белком папилломавируса. В более конкретном осуществлении ангиотензиновые пептидные составляющие слиты с основным капсидным белком L1 бычьего папилломавируса типа 1 (BPV-1). Были описаны векторы и экспрессионные системы для конструкции и экспрессии белков слияния BPV-1 в системах клеток бациловирус/насекомое (Chackerian, В. et al., Proc. Natl. Acad. Sci. USA 96: 2373-2378 (1999), WO 00/23955). Замена аминокислот 130-136 в L1 BPV-1 на ангиотензиновую пептидную составляющую приводит к образованию белка слияния L1 BPV-1 и ангиотензиновой пептидной составляющей, который является предпочтительным осуществлением настоящего изобретения. Было описано клонирование в бациловирусный вектор и экспрессия в инфицированных бациловирусом клетках Sf9, и это может использоваться в воплощении изобретения (Chackerian, В. et al., Proc. Natl. Acad. Sci. USA 96: 2373-2378 (1999), WO 00/23955). Очистка собранных частиц, представляющих слитые ангиотензиновые пептидные составляющие, может выполняться рядом способов, таких, как например, гель-фильтрация или ультрацентрифугирование в градиенте сахарозы (Chackerian,, В. et al., Proc. Natl. Acad. Sci. USA 96: 2373-2378 (1999), WO 00/23955).
В дальнейшем осуществлении настоящего изобретения, ангиотензиновые пептидные составляющие сливают с белком Ту, способным внедряться в VLP из Ту. В более конкретном осуществлении, ангиотензиновые пептидные составляющие сливают с p1 или с капсидным белком, кодируемым геном TYA (Roth, J.F., Yeast 16: 785-795 (2000)). Дрожжевые ретротранспозоны Ty1, 2, 3 и 4 были выделены из Saccharomyces Serevisiae, в то время как ретротранспозон Tf1 был выделен из Schizosaccharomyces Pombae (Boeke, J.D. and Sandmeyer, S. В., «Yeast Transposable elements», in The molecular and Cellular Biology of the Yeast Saccharomyces: Genome dynamics, Protein Synthesis, and Energetics., p.193, Cold Spring Harbor Laboratory Press (1991)). Ретротранспозоны Ty1 и 2 относятся к классу элементов растений и животных copia, в то время как Ту3 принадлежит семейству ретротранспозонов gypsy, которые относятся к ретровирусам растений и животных. В ретротранспозоне Ty1 белок p1, также обозначаемый как Gag или как капсидный белок, имеет в длину 440 аминокислот. Р1 расщепляется во время созревания VLP в положении 408, приводя к образованию белка р2, существенному компоненту VLP.
Были описаны белки слияния для p1 и векторы для экспрессии вышеуказанных белков слияния в дрожжах (Adams, S. E., et al., Nature 329: 68-70 (1987)). Так, например, ангиотензиновая пептидная составляющая может быть слита с p1 посредством встраивания кодирующей ангиотензиновую пептидную составляющую последовательности в сайт BamH1 плазмиды рМА5620 (Adams, S.Е., et al., Nature 329: 68-70 (1987)). Клонирование кодирующей инородный эпитоп последовательности в вектор рМА5620 приводит к экспрессии белков слияния, включающих аминокислоты 1-381 p1 Ty1-15, слитых у C-конца с N-концом инородного эпитопа. Подобным образом, N-концевое слияние ангиотензиновых пептидных составляющих или внутренняя вставка в последовательность p1 или замена части последовательности p1 также находится в объеме изобретения. Вставка ангиотензиновых пептидных составляющих в последовательность Ту между аминокислотами 30-31, 67-68, 113-114 и 132-133 белка p1 Ту (ЕР0677111), в особенности, приводит к предпочтительному осуществлению изобретения.
Дальнейшими VLP, подходящими для слияния ангиотензиновых пептидных составляющих, являются, например, ретровирусоподобные частицы (WO9630523), Gag HIV2 (Kang, Y.С, et al., Biol. Chem. 380: 353-364 (1999)), вирус мозаики вигны (Taylor, К.M. et al., Biol. Chem. 380: 387-392 (1999)), VLP VP2 парвовируса (Rueda, P. et al., Virology 263: 89-99 (1999)), HBsAg (US 4722840, EP0201416B1).
Примеры химерных VLP, подходящих для воплощения изобретения, также описаны в Intervirology 39: 1 (1996). Дальнейшими примерами VLP, рассматриваемыми для использования по изобретению, являются: HPV-1, HPV-6, HPV-11, HPV-16, HPV-18, HPV-33, HPV-45, CRPV, COPV, GAG HIV, вирус табачной мозаики. Также могут быть изготовлены вирусоподобные частицы SV-40, вируса полиомы, аденовируса, вируса простого герпеса, ротавируса и Норуолкского вируса, и химерные VLP из тех VLP также находятся в области настоящего изобретения.
Перекрестное связывание. Способы связывания ангиотензиновой пептидной составляющей с коровой частицей хорошо известны работающим в данной области обычным профессионалам, и существует большое количество ссылок для помощи таким профессионалам (например, Sambrook, J. et al., eds., MOLECULAR CLONING, A LABORATORY MANUAL, 2nd. edition, Cold Spring Harbor Laboratory Press, Cold Spring Harbor, N.Y. (1989); Ausubel, F. et al., eds., CURRENT PROTOCOLS IN MOLECULAR BIOLOGY, John H. Wiley & Sons, Inc. (1997); Celis, J., ed., CELL BIOLOGY, Academic Press, 2nd edition, (1998); Harlow, E. and Lane, D., «Antibodies: A Laboratory Manual,» Cold Spring Harbor Laboratory, Cold Spring Harbor, N.Y. (1988), все из которых включены сюда полностью в качестве ссылок.
В данном описании представлены различные способы достижения ассоциации коровой частицы и ангиотензиновой пептидной составляющей, и они в дальнейшем описаны в одновременно ожидающей решения заявке на выдачу патента США № 10/050902, поданной 18 января 2002 года, которая полностью включена сюда в качестве ссылки. Способы включают белковые домены с лейциновой застежкой JUN и FOS, которые используются в качестве первого и второго участков связывания по изобретению, соответственно.
Предпочтительные осуществления настоящего изобретения включают связывание неприродного молекулярного каркаса и ангиотензиновой пептидной составляющей путем химического перекрестного связывания. Существует широкий диапазон соединений, которые разработаны для осуществления перекрестного связывания белков/пептидов или для конъюгации белков с дериватизированными молекулами, например, ангиотензиновыми пептидными составляющими. Они включают в качестве неограничивающих примеров активные сложные эфиры производных карбоновых кислот (активированные соединения), смешанные ангидриды, ацилгалиды, ацилазиды, алкилгалиды, N-малеимиды, иминовые сложные эфиры, изоцианаты и изотиоцианаты, которые известны специалистам в данной области. Они способны образовывать ковалентную связь с реакционноспособной группой молекулы белка. В зависимости от активационной группы, реакционноспособной группой является аминогруппа остатка лизина на молекуле белка или тиоловая группа белка-носителя или модифицированная молекула белка-носителя, которые, взаимодействуя, приводят к образованию амидной, аминной, тиоэфирной, амидин-мочевинной или тиомочевинной связи. Специалисты в данной области могут определить дальнейшие подходящие активационные группы, например, в таких основных справочных руководствах, как Protein Conjugation and Cross-Linking (Wong (1991) CRC Press, Inc., Boca Raton, Fla.). Большинство реагентов взаимодействуют предпочтительно с группами боковых цепей лизина.
В некоторых осуществлениях, ангиотензиновая пептидная составляющая связывается с коровой частицей путем химического перекрестного связывания с использованием гетеробифункционального перекрестного линкера. В данной области известно несколько гетеробифункциональных перекрестных линкеров. В одном из осуществлений гетеробифункциональный перекрестный линкер содержит функциональную группу, которая может взаимодействовать с аминогруппой боковой цепи остатка лизина коровой частицы, и функциональную группу, которая может взаимодействовать с остатком цистеина или с присутствующей сульфгидрильной группой, которая за счет восстановления стала доступной для реакции, или была сконструирована на ангиотензиновой пептидной составляющей и также, необязательно, за счет восстановления стала доступной для реакции. Первой стадией процедуры, называемой дериватизацией, является реакция коровой частицы с перекрестным линкером. Продуктом этой реакции является активированная коровая частица, также называемая активированным носителем. На второй стадии, не прореагировавший перекрестный линкер удаляется при помощи обычных способов, таких как гель-фильтрация или диализ. На третьей стадии антиген (например, ангиотензиновая пептидная составляющая) взаимодействует с активированной коровой частицей, и эта стадия называется стадией связывания. Не прореагировавший антиген может, необязательно, удаляться на четвертой стадии.
В альтернативном осуществлении ангиотензиновая пептидная составляющая дериватизируется при помощи активного радикала, подходящего для перекрестного связывания с первым участком связывания, образуя активированную ангиотензиновую пептидную составляющую. Такая дериватизация может происходить с использованием выделенной ангиотензиновой пептидной составляющей или посредством химического синтеза. Затем активированная ангиотензиновая пептидная составляющая взаимодействует с коровой частицей таким образом, что происходит связывание.
В данной области известно несколько гетеробифункциональных перекрестных линкеров. Они включают перекрестные линкеры SMPH (Pierce), Sulfo-MBS, Sulfo-EMCS, Sulfo-GMBS, Sulfo-SIAB, Sulfo-SMPB, Sulfo-SMCC, SVSB, SIA и другие перекрестные линкеры, доступные, например в Pierce Chemical Company (Рокфорд, Иллинойс, США), несущие одну функциональную группу, взаимодействующую с аминогруппами, и одну функциональную группу, взаимодействующую с остатками SH. Все вышеупомянутые перекрестные линкеры приводят к образованию тиоэфирной связи. Другой класс перекрестных линкеров, подходящих для воплощения изобретения, характеризуется введением при связывании дисульфидной связи между ангиотензиновой пептидной составляющей и коровой частицей. Перекрестные линкеры, принадлежащие к этому классу, включают, например, SPDP и Sulfo-LC-SPDP (Pierce). Как хорошо известно по реакционной теории из области органической химии, на степень дериватизации коровой частицы с помощью перекрестного линкера можно влиять, изменяя такие экспериментальные условия, как концентрация каждого из взаимодействующих партнеров, избыток одного реагента над другим, рН, температура и ионная сила. Для соответствия с требованиями к вакцинам, степень связывания, то есть количество ангиотензиновых пептидных составляющих на носитель, может регулироваться при помощи изменения описанных выше экспериментальных условий. Растворимость ангиотензиновой пептидной составляющей может налагать ограничение на количество антигенов, которые могут связаться с каждой субъединицей, и в тех случаях, где полученная вакцина нерастворима, уменьшение количества антигенов на субъединицу является благоприятным.
В одном из конкретных осуществлений химическим агентом является гетеробифункциональный агент перекрестного связывания N-гидроксисукцинимидный сложный эфир ε-малеимидокапроновой кислоты (Tanimori et al., J. Pharm. Dyn. 4: 812 (1981); Fujiwara et al., J Immunol. Meth. 45: 195 (1981)), который содержит (1) сукцинимидную группу, взаимодействующую с аминогруппами, и (2) малеимидную группу, взаимодействующую с группами SH. Гетерологичыый белок или полипептид первого участка связывания может конструироваться так, чтобы он содержал один или несколько остатков лизина, которые будут служить реакционноспособными радикалами для сукцинимидной части гетеробифункционального агента перекрестного связывания. После химического связывания с остатками лизина гетерологичного белка малеимидная группа гетеробифункционального агента перекрестного связывания будет доступна для взаимодействия с SH-группой остатка цистеина на антигене или антигенной детерминанте. В этом случае для изготовления антигена или антигенной детерминанты может требоваться конструирование сульфгидрильного остатка в качестве второго участка связывания для того, чтобы он смог взаимодействовать со свободной малеимидной группировкой на агенте перекрестного связывания, связанного с первым участком связывания неприродного молекулярного каркаса. Таким образом, гетеробифункциональный агент перекрестного связывания в таком случае связывается с первым участком связывания неприродного молекулярного каркаса и соединяет каркас со вторым участком связывания ангиотензиновой пептидной составляющей.
Другие способы связывания ангиотензиновой пептидной составляющей с коровой частицей включают способы, где ангиотензиновая пептидная составляющая перекрестно связывается с коровой частицей с использованием карбодиимидных связей. Они включают EDC карбодиимид(1-(3-диметиламинопропил)-3-этилкарбодиимида гидрохлорид) и NHS. В одном из способов EDC смешивается с ангиотензиновой пептидной составляющей, содержащей свободную карбоновую кислоту, амино- или амидо- радикал, затем добавляется к белковому носителю. В других способах радикал присоединяется к коровой частице с использованием такого гомобифункционального перекрестного линкера, как глутаральдегид, DSG, BM[PEO]4, BS3 (Pierce Chemical Company, Рокфорд, Иллинойс, США) или другие известные гомобифункциональные перекрестные линкеры с функциональными группами, взаимодействующими с аминогруппами или карбоксильными группами коровой частицы.
Дополнительные способы перекрестного связывания и перекрестные линкеры, подходящие для связывания гаптена с коровой частицей и вирусоподобной частицей, соответственно, так же, как и руководство по проведению реакций связывания и по использованию химических перекрестных линкеров, и процедуры химического перекрестного связывания можно обнаружить у Hermanson, G.Т. в Bioconjugate Techniques, Academic Press Inc., San Diego, CA, USA.
Дальнейшие способы связывания коровой частицы с ангиотензиновой пептидной составляющей включают способы, где коровая частица биотинилируется, а составляющая сливается со стрептавидином, или способы, где биотинилируются и составляющая, и коровая частица. В этом случае ангиотензиновая пептидная составляющая может сначала связываться со стрептавидином или авидином при помощи корректирования соотношения составляющей и стрептавидина таким образом, чтобы свободные участки связывания оставались еще доступными для связывания коровой частицы, которая добавляется на следующей стадии. Альтернативно, все компоненты могут смешиваться при реакции «в одной колбе». Другие пары лиганд-рецептор, где доступна растворимая форма рецептора и лиганда и они способны перекрестно связываться с коровой частицей или ангиотензиновой пептидной составляющей, могут использоваться в качестве связывающих агентов для связывания ангиотензиновой пептидной составляющей с коровой частицей.
Ангиотензиновые пептидные составляющие
Таким образом, в одном из аспектов, изобретение предоставляет упорядоченные, повторяемые мотивы ангиотензиновых пептидных составляющих, подходящих для иммунизации против таких составляющих. Предпочтительными ангиотензиновыми пептидными составляющими являются ангиотензиновые пептидные составляющие, включающие, или, альтернативно, состоящие из последовательности, или ее фрагментов, ангиотензиногена, ангиотензина I или ангиотензина II. Как отмечено выше, одна или несколько дополнительных аминокислот может соответствующим образом добавляться либо к С-, либо к N-концу последовательностей ангиотензиновых пептидных составляющих для того, чтобы обеспечить в особенности ориентированную и упорядоченную ассоциацию ангиотензиновой пептидной составляющей с коровой частицей.
Предпочтительными ангиотензиновыми пептидными составляющими для использования в конъюгатах и конъюгатами по изобретению являются ангиотензиновые пептидные составляющие и конъюгаты, включающие или, альтернативно, состоящие из полноразмерной последовательности ангиотензиногена, ангиотензина I или ангиотензина II. Ангиотензиновые пептидные составляющие предпочтительно включают или, альтернативно, состоят из полноразмерной последовательности ангиотензина II, такой как CGGDRVYIHPF (SEQ ID NO: 19, обозначенной здесь как «Angio 1»; аминокислоты, добавленные к последовательности ангиотензинового пептида, выделены курсивом) или полноразмерной последовательности ангиотензина I, такой как CGGDRVYIHPFHL (SEQ ID NO: 20, «Angio 2»), DRVYIHPFHLGGC (SEQ ID NO: 21, «Angio 3») и CDRVYIHPFHL (SEQ ID NO: 22, «Angio 4»). Дальнейшими предпочтительными осуществлениями являются осуществления ангиотензиновых пептидных составляющих, которые включают или, альтернативно, состоят только из фрагмента последовательностей ангиотензиногена, ангиотензина I или ангиотензина II. Некоторые из таких осуществлений включают ангиотензиновые пептидные составляющие, которые включают или, альтернативно, состоят, по крайней мере, из трех аминокислот с С-концов ангиотензиновых пептидов и, в альтернативном осуществлении, ангиотензиновых пептидов, из которых были удалены, по крайней мере, четыре аминокислоты с N-концов. Другими связанными осуществлениями являются такие осуществления, полученные из ангиотензина I, как CHPFHL (SEQ ID NO: 23, «Angio 5») и CGPFHL (SEQ ID NO: 24, «Angio 6»), или такие осуществления, полученные из ангиотензина II, как CYIHPF (SEQ ID NO: 25, «Angio 7»), CGIHPF (SEQ ID NO: 26, «Angio 8») и CGGHPF (SEQ ID NO: 27, «Angio 9»).
Дополнительные осуществления настоящего изобретения используют ангиотензиновые пептидные составляющие, которые включают или, альтернативно, состоят, по крайней мере, из трех аминокислот с N-концов ангиотензиновых пептидов и для которых, в дальнейшем предпочтительном осуществлении, по крайней мере, четыре, предпочтительно, пять аминокислот были удалены с С-концов ангиотензиновых пептидов. Другими связанными осуществлениями являются DRVYIGGC (SEQ ID NO: 28, «Angio 13»), DRVYGGC (SEQ ID NO: 29, «Angio 14») и DRVGGC (SEQ ID NO: 30, «Angio 15»).
Однако обычным специалистам в данной области будет понятно, что упомянутые выше примеры ангиотензиновых пептидных составляющих являются не ограничивающими примерами, и что количество и природа аминокислот, добавляемых для связывания либо к С-, либо к N-концу, может изменяться.
По настоящему изобретению не является необходимым, чтобы иммунизирующая ангиотензиновая пептидная составляющая включала полную интактную молекулу любой конкретной ангиотензиновой пептидной составляющей. Подходящие иммунные ответы на интересующие ангиотензиновые пептидные составляющие могут вызываться с использованием фрагментов ангиотензиновых пептидных составляющих или их производных, мутантов или мутеинов.
Изобретение включает различные участки связывания и средства связывания ангиотензиновой пептидной составляющей с коровой частицей, не ограничивающие примеры которых описаны здесь в другом месте. Предпочтительные участки и средства связывания могут также определяться специалистами на основе прежнего опыта, теории и путем определенного экспериментирования.
Конъюгаты, вакцины и способы использования
Таким образом, изобретение предоставляет конъюгаты, которые могут использоваться для предотвращения и/или ослабления заболеваний или состояний, ассоциированных с одним или несколькими компонентами RAS, особенно с одним или несколькими ангиотензиновыми пептидными составляющими. Изобретение в дальнейшем предоставляет способы вакцинации для предотвращения и/или ослабления заболеваний или состояний у субъектов, в частности, у таких животных, как млекопитающие, и, в частности, человек. В предпочтительном осуществлении конъюгаты и конъюгаты по изобретению стимулируют иммунный ответ, приводящий к продукции иммунных молекул, включающих антитела, которые связываются с одной или несколькими ангиотензиновыми пептидными составляющими. Изобретение в дальнейшем предоставляет способы вакцинации для предотвращения и/или ослабления заболеваний или состояний, ассоциированных с RAS, у субъектов.
Природа или тип иммунного ответа не является ограничивающим фактором данного описания. Желаемый результат терапевтического или профилактического иммунного ответа может изменяться в соответствии с заболеванием, согласно хорошо известным в данной области принципам. Без намерения ограничить настоящее изобретение последующими объяснениями механизмов можно сказать, что конъюгаты по изобретению могут индуцировать антитела, которые связывают более одного вида ангиотензиновых пептидов, таким образом блокируя одновременно все значимые виды ангиотензина. Альтернативно, индуцированные антитела могут специфически связываться С-концом ангиотензиногена, ангиотензина I или ангиотензина II. При данных условиях, индуцированные антитела будут блокировать активацию ангиотензиногена или ангиотензина I посредством ренина или АСЕ, соответственно. Тем не менее, протеазы, отличные от АСЕ или ренина, такие как эндопептидазы и аминопептидазы, могут осуществлять деградацию ангиотензиногена, ангиотензина I или ангиотензина II с N-конца, предотвращая таким образом накопление связанного с антителом интактного ангиотензиногена, ангиотензина I или ангиотензина II.
К тому же, возможно желательно стимулировать различные типы иммунного ответа в зависимости от заболевания и согласно известным в данной области принципам. Например, хорошо известно, что некоторые иммунные ответы более свойственны конкретному антигену, чем другие иммунные ответы. Некоторые иммунные ответы являются, на самом деле, несоответствующими и могут вызывать такую патологию, как патологичное воспаление.
На природу иммунного ответа может влиять природа антигена, способ введения в тело, доза, дозировочный режим, повторяемая природа антигена, исходное состояние организма и сигнальные факторы иммунной системы. Такая информация хорошо известна в данной области. По существу, иммунный ответ может быть адаптирован посредством применения и известной в данной области теории, и общепринятого экспериментирования.
Кроме того, изобретение включает использование разных коровых частиц во время курса вакцинации против ангиотензиновых пептидных составляющих. Субъекты, которые проявили напряженный иммунный ответ против таких коровых частиц, как, например, пили, могут иммунизироваться конъюгатами, включающими ту же самую ангиотензиновую пептидную составляющую, но на других коровых частицах.
Данные конъюгаты настоящего изобретения обеспечивают особые новые и неожиданные преимущества в качестве компонентов фармацевтических конъюгатов, индуцирующих иммунный ответ, и, особенно, в качестве вакцин против одной или нескольких ангиотензиновых пептидных составляющих, хотя и не предполагается, что это связано с какой-либо теорией. Другие известные в данной области носители, включающие БСА, гемоцианин морского блюдечка, столбнячный анатоксин, бактериальные белки внешней мембраны, холерный токсин и экзотоксин A Pseudomonas aeruginosa, могут быть неподходящими для использования у субъектов, в особенности, у человека. Вышеупомянутые носители могут индуцировать аллергические реакции или стимулировать патологические иммунные ответы (например, холерный токсин, KLH, БСА). Вышеупомянутые носители могут требовать наличия адъювантов, таких как полный адъювант Фрейнда, в настоящий момент считающийся неподходящим для использования у людей. Ряд носителей могут быть компонентами имеющихся вакцин (например, столбнячный анатоксин, холерный, токсин, экзотоксин А). Как таковой, субъект может обладать высоким уровнем существующего до иммунизации иммунитета к этим носителям, так что иммунизация конъюгатом носитель-антиген вызовет относительно более сильный иммунный ответ на носитель, чем на новый антиген. По этим причинам, индивидуально или в целом, конъюгаты или конъюгаты по настоящему изобретению представляют полезное усовершенствование вышеописанных белков-носителей.
При использовании осуществлений изобретения, одна или несколько ангиотензиновых пептидных составляющих, конъюгированных с коровыми частицами, могут захватываться антиген-представляющими клетками и таким образом стимулировать Т-клетку, помогающую индуцировать иммунные ответы. Ответы клеток Т-хэлперов можно подразделить на ответы клеток Т-хэлперов типа 1 (ТH1) и типа 2 (ТH2) (Romagnani, Immunol. Today 18: 263-266 (1997)). Клетки ТH1 секретируют интерферон-гамма и другие цитокины, которые запускают продукцию антител IgG1-3 в В-клетках. В отличие от них, необходимым цитокином, продуцируемым клетками ТH2, является IL-4, который стимулирует В-клетки продуцировать IgG4 и IgE. Во многих экспериментальных системах выработка ответов ТH1 и ТH2 является взаимно исключающей, поскольку клетки ТH1 подавляют индукцию клеток ТH2 и наоборот. Таким образом, антигены, которые вызывают напряженный ответ ТH1, одновременно подавляют выработку ответов ТH2 и, следовательно, продукцию антител IgE. Интересно, что практически все вирусы индуцируют в организме хозяина ответ ТH1 и не способны запускать продукцию антител IgE (Coutelier et al., J. Exp.Med. 165: 64-69 (1987)). Антитела изотипа IgE являются важными компонентами аллергических реакций. Тучные клетки связывают антитела IgE на своей поверхности и высвобождают гистамины и другие медиаторы аллергического ответа при связывании специфического антигена с молекулами IgE, связанными на поверхности тучных клеток. Типичный изотипный профиль ответов ТH1 не ограничивается живыми вирусами, но также наблюдается для инактивированных или рекомбинантных вирусных частиц (Lo-Man et al., Eur. J. Immunol. 28: 1401-1407 (1998)). Таким образом, с использованием процесса по изобретению (например, AlphaVaccine Technology) вирусные частицы могут нести различные ангиотензиновые пептидные составляющие и могут использоваться для иммунизации. За счет конечной «вирусной структуры» мотива, будет вызываться ответ ТH1, будут продуцироваться «защитные» антитела IgG1-3, и продукция антител IgE, которая вызывает аллергические реакции, будет предотвращена. Таким образом, изобретение включает конъюгаты, способные индуцировать предпочтительные иммунные ответы, в особенности, ответы типа ТH1. Далее, изобретение включает использование конъюгатов по изобретению для противодействия аллергическим реакциям, индуцированным альтернативными вакцинами против интересующих антигенов.
Дальнейшей благоприятной характерной чертой изобретения является то, что ангиотензиновые пептидные составляющие могут предоставляться на частицах в систематических повторяемых мотивах, которые способны вызывать эффективные иммунные ответы как с, так и без помощи Т-клеток. Эта характерная черта изобретения особенно благоприятна.
В отличие от отдельных белков вирусы вызывают быстрые и эффективные иммунные ответы в отсутствие любых адъювантов как с помощью, так и без помощи Т-клетки (Bachmann & Zinkernagel, Ann. Rev. Immunol: 15: 235-270 (1997)). Хотя вирусы часто состоят из нескольких белков, они способны индуцировать гораздо более напряженный иммунный ответ, чем их отдельные компоненты. Известно, что для В-клеточных ответов одним из решающих факторов иммуногенности вирусов является повторяемость и порядок поверхностных эпитопов. Многие вирусы демонстрируют квазикристаллическую поверхность, которая представляет систематический мотив эпитопов, который эффективно перекрестно связывает специфичные для эпитопа иммуноглобулины на В-клетках (Bachmann & Zinkernagel, Immunol. Today 17: 553-558 (1996)). Такое перекрестное связывание поверхностных иммуноглобулинов на В-клетках является сильным активационным сигналом, который непосредственно индуцирует клеточный цикл и продукцию антител IgM. Далее, такие активированные В-клетки способны активировать клетки Т-хэлперы, которые, в свою очередь, индуцируют переключение продукции антител с IgM на IgG в В-клетках и образование долгосрочной В-клеточной памяти - цели любой вакцинации (Bachmann & Zinkernagel, Ann. Rev. Immunol. 15: 235-270 (1997)). Настоящее изобретение предоставляет один из способов улучшить эффективность вакцинации путем увеличения степени повторяемости ангиотензиновой пептидной составляющей, которая будет использоваться для иммунизации, посредством связывания ангиотензиновой пептидной составляющей с коровой частицей. Как отмечалось ранее, изобретение предусматривает конъюгаты, включающие коровую частицу, модифицированную так, чтобы изменить количество и/или расположение организующей основы.
Обычным специалистам в данной области должно быть понятно, что когда конъюгаты вводятся субъекту, они могут быть конъюгатами, которые содержат соли, буферы, адъюванты или другие вещества, которые требуются для увеличения эффективности конъюгатов. Примеры подходящих для использования в приготовлении фармацевтических конъюгатов материалов предоставлены в многочисленных источниках, включающих REMINGTON'S PHARMACEUTICAL SCIENCES (Osol, A, ed., Mack Publishing Co., (1990)).
Конъюгаты по изобретению являются, как говорят, «фармакологически приемлемыми», если их введение может переноситься получающим их субъектом. Далее, конъюгаты по изобретению будут вводиться в «терапевтически эффективном количестве» (то есть, в количестве, которое обеспечивает требуемый физиологический эффект).
Для индукции иммунного ответа конъюгаты настоящего изобретения могут вводиться животным, соответственно, млекопитающим, таким как человек, различными известными в данной области способами, но, обычно, будут вводиться путем инъекции, инфузии, ингаляции, перорального введения или другими подходящими физическими способами. Конъюгаты могут, альтернативно, вводиться внутримышечно, внутривенно, через слизистые оболочки, чрескожно или подкожно. Компоненты конъюгатов для введения включают стерильные водные (например, физиологический раствор) или неводные растворы и суспензии. Примерами неводных растворителей являются пропиленгликоль, полиэтиленгликоль, такие растительные масла, как оливковое масло, и подходящие для инъекции органические сложные эфиры, такие как этилолеат. Носители или окклюзионная повязка могут использоваться для увеличения проницаемости кожи и повышения абсорбции антигена.
Дальнейшие осуществления изобретения включают иммунные молекулы, получаемые путем иммунизации конъюгатами по изобретению. Иммунные молекулы включают антитела и Т-клеточные рецепторы. Такие иммунные молекулы могут использоваться у вакцинированных субъектов для связывания с мишенью одной или нескольких ангиотензиновых пептидных составляющих. Также иммунные молекулы могут использоваться при переносе другому субъекту, не иммунизированному против конъюгатов или конъюгатов по изобретению, посредством этого «пассивно» передавать иммунитет. В одном из осуществлений иммунной молекулой является антитело. Моноклональное антитело, подходящее для связывания одной или нескольких ангиотензиновых пептидных составляющих, может переноситься субъекту для осуществления терапии или профилактики.
Изобретение также включает использование антител, продуцированных при иммунизации конъюгатами или конъюгатами по изобретению, в наборах для определения одной или нескольких ангиотензиновых пептидных составляющих при иммунноанализах (например, ELISA). В связанном осуществлении повторяемые упорядоченные мотивы ангиотензиновых пептидных составляющих могут использоваться для определения антител против таких составляющих в анализах связывания. Другие осуществления изобретения включают процесс продукции конъюгатов по изобретению и способы медицинского лечения с использованием таких конъюгатов, особенно, для лечения одного или нескольких физических заболеваний, ассоциированных с RAS, таких как гипертензия, удар, инфаркт, застойная сердечная недостаточность, почечная недостаточность или кровоизлияние в сетчатку.
Обычным специалистам в связанных областях будет понятно, что другие подходящие модификации и адаптации способов и применений, описанных здесь, без труда очевидны и могут быть выполнены, не отступая от объема изобретения или его осуществления. На настоящий момент, подробно описав настоящее изобретение, то же самое будет более ясно понятным при ссылке на следующие примеры, которые включены сюда только с целью иллюстрации и не предназначены для ограничения изобретения.
ПРИМЕРЫ
ПРИМЕР 1: Связывание пептидов, полученных из ангиотензина I и ангиотензина II, с Qβ и иммунизация мышей полученными в результате конъюгатами
А. Продукция конъюгатов
Следующие ангиотензиновые пептидные составляющие были химически синтезированы: CGGDRVYIHPF (SEQ ID NO: 19, «Angio 1»), CGGDRVYIHPFHL (SEQ ID NO: 20, «Angio 2»), DRVYIHPFHLGGC (SEQ ID NO: 21, «Angio 3»), CDRVYIHPFHL (SEQ ID NO: 22, «Angio 4»), CHPFHL (SEQ ID NO: 23, «Angio 5»), CGPFHL (SEQ ID NO: 24, «Angio 6»), CYIHPF (SEQ ID NO: 25, «Angio 7»), CGIHPF (SEQ ID NO: 26, «Angio 8»), CGGHPF (SEQ ID NO: 27, «Angio 9»), DRVYIGGC (SEQ ID NO: 28, «Angio 13»), DRVYGGC (SEQ ID NO: 29, «Angio 14») и DRVGGC (SEQ ID NO: 30, «Angio 15»). Они использовались для химического связывания с Qβ, как описано в дальнейшем.
Для пептидов Angio 1-Angio 4: раствор объемом 5 мл капсидного белка Qβ в концентрации 2 мг/мл в 20 мМ Hepes, 150 мМ NaCl, pH 7,4, в течение 30 минут подвергали взаимодействию с 507 мкл раствора Sulfo-MBS (Pierce) в H2О в концентрации 13 мг/мл при температуре 25°С на вращающемся шейкере. Впоследствии, реакционный раствор дважды диализовали в течение 2 часов против 2 л 20 мМ Hepes, 150 мМ NaCl, pH 7,4, при температуре 4°С. Отдиализованную реакционную смесь объемом 665 мкл затем подвергали взаимодействию с 2,8 мкл каждого из соответствующих 100 мМ маточных растворов пептидов (в DMSO) в течение двух часов при температуре 25°С на вращающемся шейкере. Впоследствии, реакционную смесь диализовали 2×2 часа против 2 литров 20 мМ Hepes, 150 мМ NaCl, pH 7,4, при температуре 4°С.
Для пептидов Angio 5-9 и Angio 13-15: раствор объемом 3 мл капсидного белка Qβ в концентрации 2 мг/мл в 20 мМ Hepes, 150 мМ NaCl, pH 7,2, в течение 50 минут подвергали взаимодействию с 86 мкл раствора 100 мМ SMPH (сукцинимидил-6-(β-малеимидопропионоамидогексаноат, Pierce) в DMSO при температуре 25°С на вращающемся шейкере. Впоследствии, реакционный раствор дважды диализовали в течение 2 часов против 2 л 20 мМ Hepes, 150 мМ NaCl, pH 7,2 при температуре 4°С. Отдиализованную реакционную смесь объемом 514 мкл затем подвергали взаимодействию с 3,6 мкл каждого из соответствующих 100 мМ маточных растворов пептидов (в DMSO) в течение 4 часов при температуре 25°С на вращающемся шейкере. Впоследствии, реакционную смесь диализовали 2×2 часа против 2 литров 20 мМ Hepes, 150 мМ NaCl, pH 7,2, при температуре 4°С.
Б. Иммунизация
Самки мышей Balb/c были вакцинированы одним из девяти производных ангиотензинового пептида, связанных с капсидным белком Qβ, без добавления адъюванта. 50 мкг (вакцины Angio 1-4 с Qβ) или 20 мкг (вакцины Angio 5-9 с Qβ) общего белка каждого образца растворяли в PBS до объема 200 мкл и подкожно вводили (100 мкл с двух сторон брюшка) на 0 день и 14 день. У мышей забирали кровь ретроорбитально на 21 день, и их сыворотку анализировали с использованием специфичного для ангиотензина анализа ELISA.
Следует отметить, что человеческая и мышиная последовательности ангиотензиновых пептидов идентично соответствуют одна другой. Следовательно, иммунизация человека или мыши вакцинами или конъюгатами, соответственно, включающими ангиотензиновые пептидные составляющие в качестве антигенных детерминант по изобретению, является вакцинацией против аутоантигенов.
ПРИМЕР 2: Анализ ELISA сывороток мышей, вакцинированных пептидами, полученными из ангиотензина I и ангиотензина II, связанных с Qβ
Производные пептидов Angio 1-Angio 9 и Angio 13-15, полученные, как описано в примере 1, каждый по отдельности связывали с бычьей РНКазой A (Sigma), используя химический перекрестный линкер sulfo-SPDP. На планшеты для ELISA сорбировали в течение ночи при температуре 4°С связанные с РНКазой препараты в концентрации 10 мкг/мл в сорбирующем буфере (0,1 М NaH2СО3, рН 9,6). Альтернативно, ангиотензин I или ангиотензин II (SIGMA) разводили в том же самом сорбирующем буфере до концентрации 200 мкг/мл. Планшеты блокировали блокирующим буфером (2% бычий сывороточный альбумин (БСА) в PBS (рН 7,4)/0,05% Tween 20) в течение 2 часов при температуре 37°С, отмывали в PBS (pH 7,4)/0,05% Tween 20 и затем инкубировали в течение 2 часов при комнатной температуре с последовательно разведенными в блокирующем буфере мышиными сыворотками. Планшеты отмывали в PBS (рН 7,4)/0,05% Tween 20 и затем инкубировали с меченным пероксидазой хрена антителом козы против IgG мыши в концентрации 1 мкг/мл (Jackson ImmunoResearch) в течение 1 часа при комнатной температуре. Планшеты отмывали в PBS (рН 7, 4)/0,05% Tween 20 и добавляли субстратный раствор (0,066 М Na2HPO4, 0,035 М лимонной кислоты (рН 5,0)+0,4 мг OPD (1,2-фенилендиамина дигидрохлорид)+0,01% Н2О2). После 10 минут цветную реакцию останавливали 5% H2SO4 и считывали поглощение при длине волны 450 нм.
В качестве контроля также тестировали сыворотки тех же самых мышей до иммунизации. Контрольные эксперименты ELISA с использованием сывороток мышей, иммунизированных неродственными пептидами, перекрестно связанным с Qβ или другими носителями, показали, что определенные антитела были специфичны для соответствующих пептидов. Титры ELISA рассчитывали как величину, обратную разбавлению сыворотки, которое дает половину от максимального сигнала в ELISA (50% максимальной оптической плотности).
РЕЗУЛЬТАТЫ:
На фигуре 2 показаны анализы ELISA антител IgG, специфичных для пептида Angio 2 и ангиотензина I, в сыворотках мышей, иммунизированных пептидами Angio 1-4, связанными с капсидным белком Qβ. Qβ-Angio 1, Qβ-Angio 2, Qβ-Angio 3 и Qβ-Angio 4, как использовано на фигурах, обозначают вакцину, введенную мышам, от которых получали сыворотки, согласно указанному выше определению ангиотензиновых пептидов. Самки мышей Balb/c были подкожно вакцинированы 50 мкг вакцины в PBS в 0 день и 14 день. Антитела IgG в сыворотках мышей, вакцинированных Qβ-Angio 1, Qβ-Angio 2, Qβ-Angio 3 и Qβ-Angio 4, измеряли на 21 день против пептида Angio 2, связанного с РНКазой А, и против ангиотензина I. В качестве контроля также анализировали сыворотки до иммунизации. Результаты для указанных разведений сывороток показаны как оптическая плотность при длине волны 450 нм. Среднее значение для трех мышей (включая стандартные отклонения) показано для Angio 2. Среднее значение для двух мышей показаны для ангиотензина I. У всех вакцинированных мышей выработались специфичные IgG-антитела против пептида Angio 2, так же как и против ангиотензина I, хотя мыши, иммунизированные пептидом Angio 2, Angio 3 или Angio 4, показали более высокие титры, чем мыши, вакцинированные пептидом Angio 1, что соответствует большему подобию пептидов Angio 2, Angio 3 и Angio 4 ангиотензину I.
На фигуре 1 показаны анализы ELISA IgG-антител, специфичных для пептида Angio 1 и ангиотензина II, в сыворотках мышей, иммунизированных пептидами Angio 1-4, связанными с капсидным белком Qβ. Qβ-Angio 1, Qβ-Angio 2, Qβ-Angio 3 и Qβ-Angio 4, как использовано на фигурах, обозначают вакцину, введенную мышам, от которых получали сыворотки, согласно указанному выше определению ангиотензиновых пептидов. Самки мышей Balb/c были подкожно вакцинированы 50 мкг вакцины в PBS в 0 день и 14 день. Антитела IgG в сыворотках мышей, вакцинированных Qβ-Angio 1, Qβ-Angio 2, Qβ-Angio 3 и Qβ-Angio 4, измерялись на 21 день против пептида Angio 1, связанного с РНКазой А, и против ангиотензина II. В качестве контроля также анализировались сыворотки до иммунизации. Результаты для указанных разведений сывороток показаны как оптическая плотность при длине волны 450 нм. Среднее значение для трех мышей (включая стандартные отклонения) показано для Angio 1. Среднее значение для двух мышей показано для ангиотензина II. У всех вакцинированных мышей выработались специфичные антитела IgG против пептида Angio 1, так же как и против ангиотензина II, хотя мыши, иммунизированные пептидом Angio 1, показали более высокие титры, что соответствует большему подобию пептида Angio 1 ангиотензину II.
На фигуре 4 показаны анализы ELISA антител IgG, специфичных для пептида Angio 2 и ангиотензина I, в сыворотках мышей, иммунизированных пептидами Angio 5-9, связанными с капсидным белком Qβ. Qβ-Angio 5, Qβ-Angio 6, Oβ-Angio 7, Qβ-Angio 8 и Qβ-Angio 9, как использовано на фигурах, обозначают вакцину, введенную мышам, от которых получались сыворотки, согласно указанному выше определению ангиотензиновых пептидов. Самки мышей Balb/c были подкожно вакцинированы 20 мкг вакцины в PBS в 0 день и 14 день. Антитела IgG в сыворотках мышей, вакцинированных Qβ-Angio 4, Qβ-Angio 5, Qβ-Angio 6, Qβ-Angio 7, Qβ-Angio 8 и Qβ-Angio 9, измерялись на 21 день против пептида Angio 2, связанного с РНКазой А, и против ангиотензина I. Результаты для указанных разведений сывороток показаны как оптическая плотность при длине волны 450 нм. Для каждой из двух мышей показаны средние значения. Две мыши, вакцинированные Qβ-Angio 8 и Qβ-Angio 9, показали очень низкие или неспецифичные титры против пептида Angio 2, так же как и против ангиотензина I, указывая на то, что эти два типа вакцин индуцировали антитела, которые, главным образом, были специфичны для С-конца ангиотензина II, а не для ангиотензина I (смотри также Фиг.3).
На фигуре 3 показаны анализы ELISA антител IgG, специфичных для пептида Angio 1 и ангиотензина II, в сыворотках мышей, иммунизированных пептидами Angio 5-9, связанными с капсидным белком Qβ. Qβ-Angio 5, Qβ-Angio 6, Qβ-Angio 7, Qβ-Angio 8 и Qβ-Angio 9, как использовано на фигурах, обозначают вакцину, введенную мышам, от которых получались сыворотки, согласно указанному выше определению ангиотензиновых пептидов. Самок мышей Balb/c вакцинировали подкожно 20 мкг вакцины в PBS на сутки 0 и сутки 14. Антитела IgG против пептида Angio 1, связанного с РНКазой А, и против ангиотензина II в сыворотках мышей, вакцинированных Qβ-Angio 4, Qβ-Angio 5, Qβ-Angio 6, Qβ-Angio 7, Qβ-Angio 8 и Qβ-Angio 9, измеряли на сутки 21. Результаты для указанных разведений сыворотки показаны в виде оптической плотности при 450 нм. Каждое значение показано как среднее от двух мышей. Две мыши, вакцинированные Qβ-Angio 5 и Qβ-Angio 6, проявляли очень низкие специфические титры против пептида Angio 1, а также против ангиотензина II, или данные титры отсутствовали, что указывает на индукцию данными двумя типами вакцин антител, которые наиболее специфичны к С-концу ангиотензина I, но не к ангиотензину II (см, также фиг.4).
В таблице 1 суммирован анализ путем ELISA сывороток от мышей, вакцинированных пептидами Angio 1-9, связанными с Qβ. Средние титры ELISA от 21 суток рассчитывали, как описано в примере 2.
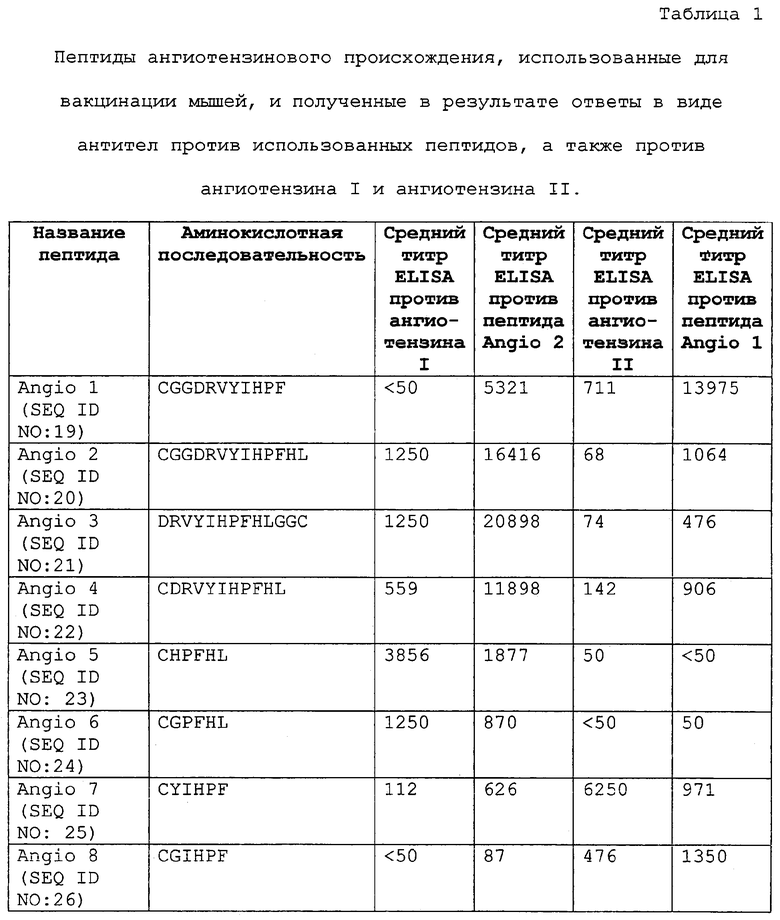
Все результаты по Angio 5 и Angio 6 показывают, что пептиды могут индуцировать антитела, которые селективно распознают ангиотензин I. Более того, результаты по Angio 7-9 показывают, что могут индуцироваться антитела, которые селективно распознают антиотезин II, но не ангиотезин I. Поскольку антиотезин I и II различаются 2 аминокислотами только на С-конце, тогда как оставшиеся 8 аминокислот идентичны, данные результаты демонстрируют, что все антитела, индуцированные Angio 5 или Angio 6, избирательно распознают С-конец ангиотензина I, и что антитела, индуцированные Angio 7-9, и, в особенности, Angio 8-9, селективно распознают С-конец ангиотензина II. Таким образом, общие 8 аминокислот не распознаются и, в частности, не распознается общий N-конец. Это указывает, что N-конец не погружен внутрь антител при их связывании, и поэтому доступен для протеаз.
Присоединение ангиотензиновой пептидной составляющей к VLP, иммунизация и демонстрация эффективности на экспериментальной модели гипертензии
Ангиотензиновая пептидная составляющая CGGDRVYIHPF («Ангио 1») была синтезирована с помощью твердофазного метода синтеза.
Присоединение Ангио 1 к VLP Qβ и АР205
Ангио 1, ангиотензиновую пептидную составляющую, присоединяли к VLP РНК-бактериофага Qβ и АР205 в соответствии со способом примера 1.
Таким образом, сначала VLP взаимодействовали с 10- или 20- кратным избытком (относительно концентрации мономеров белка оболочки) гетеробифункционального перекрестно-сшивающего агента SMPH (Pierce). Не прореагировавший перекрестно-сшивающий агент удаляли путем диализа, и полученные таким образом производные VLP затем взаимодействовали с 8- или 20-кратным избытком (снова относительно концентрации мономеров белка оболочки) ангиотензиновых пептидных составляющих в течение двух часов при комнатной температуре. Конъюгаты ангиотензиновой пептидной составляющей и VLP, полученные таким образом, затем диализировали для удаления свободных несвязанных ангиотензиновых пептидных составляющих. Конъюгацию ангиотензиновой пептидной составляющей и VLP определяли LDS-PAGE, осуществляемым в восстанавливающих условиях (12% Nu-Page гели, Invitrogen). Концентрацию белка вакцины определяли методом Брадфорда (Bradford). Полученные таким образом конъюгаты ангиотензиновой пептидной составляющей и VLP в дальнейшем обозначены как «Qβ-Ангио 1» и «АР205-Ангио 1».
Иммунизация мышей Qβ-Ангио 1
На 0 и 14 день мышам Balb/c (n=5) подкожно вводили 100 мкг вакцины Qβ-Ангио 1 без адъюванта. На 21 день у животных брали кровь для определения титра антител против иммунизированного пептида с помощью ELISA.
ELISA
Конъюгаты РНКаза-пептид получали сначала реакцией РНКазы с перекрестно-сшивающим агентом SPDP (Pierce, Rockford, IL), а затем с пептидом Ангио 1. Конъюгаты РНКаза-пептид наносили на плашки для ELISA в количестве 10 мкг/мл в карбонатном буфере в течение ночи при 4°С. После блокирования сыворотки 2% раствором BSA в PBS/Tween, ее инкубировали в течение двух часов на плашке и визуализировали с помощью конъюгата HRP козла против IgG крысы (Jackson Immunoresearch, West Grove, PA).
Результаты, представленные на фигуре 1, показывают, что вакцина индуцирует высокие титры антител против иммунизированной ангиотензиновой пептидной составляющей, и что ответ является специфичным, так как значение титра в сыворотке до иммунизации было ниже 1:100. Таким образом, вакцина способна индуцировать высокие титры антител против ангиотензиновой пептидной составляющей, которая в данном контексте является аутоантигеном и, поэтому, нарушает аутотолерантность.
Фиг.1 Иммуногенность вакцины Qβ-Ангио 1 у мышей. Мышей (n=5) иммунизировали на 0 и 14 день 100 мкг вакцины. Титры антител измеряли с помощью ELISA против Ангио 1 (группа Qβ-Ангио 1), присоединенной к РНКазе. Титры выражали как разведение сыворотки, при которой возможно полумаксимальное связывание в анализе (OD 50%). Сыворотка перед иммунизацией давала сигнал минимально выше фонового и была обозначена как титр 1:100, самое маленькое разведение сыворотки, используемое в анализе. Линии ошибок соответствуют стандартной ошибке усреднения.
Эффективность вакцины на моделях гипертензии у животных
Оценку эффективности у крыс SHR проводили, осуществляя измерение давления крови на хвосте с помощью манжеты
Крысам со спонтанной гипертензией (SHR) подкожно вводили 400 мкг Qβ-Ангио 1, или Qβ с гидроксидом алюминия. На 14 и 28 день животных аналогичным образом ревакцинировали тем же количеством. Измеряли титры антител в сыворотке, полученной на 0, 7, 14, 21 и 28 день. Дополнительной группе крыс ежедневно с питьевой водой давали активный агент сравнения, рамиприл (1 мг/кг массы тела). Артериальное давление крови измеряли на 9, 16, 23 и 30 день методом измерения давления на хвосте с помощью манжеты (Pressure Meter LE-5000 Series, Letica, Cornella (Barcelona), Spain). Во время измерения животных помещали в удерживающее устройство. Систолическое давление крови (SBP) рассчитывали как медиану 25 показателей для каждого животного в конкретный период времени. На 23 и 30 день SBP у животных, вакцинированных Qβ-Ангио 1, было значительно ниже давления животных контрольной группы, получавших Qβ (фигура 2А). На 30 день разница между давлением в контрольной группе, получавшей Qβ, составила 1 мм рт.ст. (р<0.01). Вакцина вызывала повышение титров антител (фигура 2В) и, следовательно, нарушала аутотолерантность к ангиотензину II, который в данном контексте является аутоантигеном. Авторы наблюдали обратную корреляцию между титром антител и давлением крови (r=-0,54, р=0,006, для титра ln против SBP, корреляция среди животных). Таким образом, эти данные показывают, что иммунный ответ, вызванный ангиотензиновой пептидной составляющей, присоединенной к Qβ, вызывает снижение давления крови у крыс с SHR, что говорит об эффективности этой вакцины в качестве средства для лечения гипертензии. Более того, корреляция между повышением титра антител и снижением давления крови подтверждается механизмом действия, основанного на блокировании ангиотензина антителами, образование которых индуцировано применением вакцины.
Фигура 2. Эффект вакцинации на SBP у крыс с SHR, осуществляли измерением давления крови на хвосте с помощью манжеты. Группы крыс с SHR (n=8) иммунизировали на 0, 14 и 28 день Qβ-Ангио 1 (ромбы), Qβ (закрашенные треугольники) или вводили рамиприл (квадраты), как описано. SBP измеряли на хвосте с помощью манжеты и определяли титр антител с помощью ELISA.
А. Эффект вакцинации на SBP. SBP записывали для каждого животного на 9, 16, 23 и 30 день. Данные представлены как среднее значение для каждой группы, и линии, ошибок соответствуют стандартной ошибке усреднения. С помощью ONEWAY ANOWA с использованием процедуры Дунетта на 30 день было зафиксировано статистически значимое снижение давления, на 21 мм рт.ст., в группе Qβ-Ангио 1 (р<0,01) по сравнению с группой VLP.
В. Титры антител у вакцинированных крыс. Титры IgG против Ангио 1 измеряли в сыворотке иммунизированных крыс с SHR, взятых на 0, 7, 14, 21 и 28 день. Титры до иммунизации составили 1:100, на столбчатых диаграммах указано среднее геометрическое титров для групп, и линии ошибок соответствуют стандартной ошибке усреднения.
Оценку эффективности у крыс с SHR проводили с помощью телеметрической аппаратуры.
Крыс с SHR подкожно вакцинировали 400 мкг Qβ-Ангио 1, или 400 мкг Qβ с гидроксидом алюминия на 1, 15 и 43 день. Аналогичные инъекции осуществляли на 29 день, при этом использовали АР205-Ангио 1 и АР205 вместо аналога с Qβ. Вакцина АР205-Ангио 1 обладает той же плотностью эпитопов, что и аналог с Qβ. Четвертой группе животных с 1 по 28 день ежедневно перорально с помощью зонда вводили ингибитор АСЕ (эналаприл) в количестве 10 мг/кг массы тела. В течение эксперимента дозу последовательно снижали. В группе, получающей Qβ-Ангио 1/АР205-Ангио 1, собирали образцы крови и измеряли титры антител. Постоянно измеряли давление крови телеметрической аппаратурой. Каждые 24 часа в течение каждого 12-часового периода дня и ночи рассчитывали медиану 48 показателей. Для статистического анализа значение давления крови вычитали из базисного значения.
Для точности авторы представляют только данные дневного периода, так как результаты ночных периодов были эквивалентны. Снижение давления крови в группе, получающей Qβ-Ангио 1/АР205-Ангио 1, впервые достигло статистически значимого значения на 46 и 47 день (по сравнению с группой Qβ/AP205, фигура 3А). Впоследствии, статистически значимое снижение SBP по сравнению с контрольной группой, получающей Qβ/AP205, было зафиксировано с 57 по 79 день, исключая 62, 63 и 68 день. В период с 57 по 79 день в группе, получающей Qβ-Ангио 1/АР205-Ангио 1, среднее значение SBP было на 15 мм рт.ст. ниже по сравнению с контрольной группой, получающей Qβ/AP205 (p<0,01, таблица 1). В этот период также было снижено среднее артериальное давление (MAP) на 7% (р<0,05) или -10 мм рт.ст. (таблица 1). Разница в 5 мм рт.ст. диастолического давления (DBP) (таблица 1) не имела статистической значимости (р>0,05). Таким образом, иммунизация вакцинами Qβ-Ангио 1 и АР205-Ангио 1 давала стойкое снижение давления крови в течение более 35 дней после ревакцинации. Титры антител, специфических в отношении ангиотензина II, в группе, получавшей Qβ-Ангио 1/АР205-Ангио 1, достигали максимума на 42 день, позже, чем в эксперименте с измерением давления на хвосте с помощью манжеты, и оставалось высоким до конца эксперимента (фигура 3А). Давление крови испытуемой группы и контрольной группы стало расходиться после возникновения высокого титра антител, что согласуется с предполагаемым механизмом действия вакцины. Наконец, ни в одной из испытуемых групп не было обнаружено значительного изменения сердечного ритма.
Фигура 3. Эффект вакцинации на ВР у крыс с SHR, контролируемый с помощью телеметрической аппаратуры. Крыс с SHR иммунизировали на 1, 15, 29 и 43 день Qβ/AP205 (n=7), Qβ-Ангио 1/АР205-Ангио 1, (n=8), как описано. SBP измеряли с помощью телеметрической аппаратуры, а титры антител определяли с помощью ELISA. Одной группе (n=7) вводили эналаприл.
А. Эффект вакцинации на SBP. Значение SBP усредняли в каждой группе. Для ясности показаны данные только для группы, получавшей Qβ-Ангио 1/АР205-Ангио 1, (квадраты) и группы, получавшей Qβ (ромбы). Линии ошибок соответствуют стандартной ошибке усреднения. Значимые различия (р<0,05) группы, получавшей Qβ-Ангио 1/АР205-Ангио 1, и группы, получавшей Qβ/AP205, были зарегистрированы на 46 и 47 день и на 57-79 день (отмечены скобкой), исключая 62, 63 и 68 день (TWO-WAY ANOVA для повторных измерений с использованием процедуры Дунетта).
В. Титры антител у вакцинированных крыс. Титры антител IgG измеряли в сыворотке, полученной в 0 день, на 14, 28, 42, 56 и 70 день, против Ангио 1. Титр до иммунизации составлял 1:100. На столбчатых диаграммах указано среднее геометрическое титров для групп, и линии ошибок соответствуют стандартной ошибке усреднения.
Средние значения SBP, MAP и DBP в мм рт.ст. рассчитывали в период с 1 по 56 день и с 57 по 79 день и прибавляли значение базовой линии. С 57 по 79 день было отмечено изменение значений артериального давления крови в группе, получавшей Qβ-Ангио 1/АР205-Ангио 1, по сравнению с контрольной группой, получавшей Qβ/AP205, или на 1-56 день между группой, получавшей эналаприл, и группой, получавшей Qβ/AP205 (введение высокой дозы эналаприла). *р≤0,01 по сравнению с Qβ/AP205. Данные анализировали в процентах: 7% снижение (р<0,05). Данные анализировали в абсолютных переменных: пороговое значение значимости по сравнению с Qβ/AP205 при 95% доверительном пределе = -11 мм рт.ст.
Доклинические данные токсикологической безопасности и данные фазы I клинических испытаний на людях, получаемых Qβ-Ангио 1
Приведенные ниже данные были получены при применении «Qβ-Ангио 1», то есть композиций, содержащих VLP РНК-бактериофага Qβ, к которому присоединена пептидная молекула ангиотензина CGGDRVYIHPF («Ангио 1»).
Доклинические данные токсикологической безопасности
Доклинические исследования токсичности осуществляли в соответствии с рекомендациями ICH по доклинической оценке безопасности фармацевтических средств, полученных биотехнологическими способами, и с рекомендациями по доклиническим фармацевтическим и токсикологическим исследованиям вакцин. Исследования осуществляли в соответствии с принципами добросовестной лабораторной практики в контрактной научно-исследовательской организации с экспертизой токсичности вакцины.
Исследования токсичности Qβ-Ангио 1 у крыс с нормальным давлением не выявили случаев местной или системой токсичности при однократном или многократном введении вакцины вместе или без гидроксида алюминия. Гистиоцитарная реакция в местах инъекции была отмечена у животных, получавших Qβ-Ангио 1 вместе с гидроксидом алюминия, и соответствовала ожидаемой реакции при введении такого адъюванта. В частности, не было обнаружено следов воспаления в почках, что указывает на отсутствие депонирования воспалительных иммунных комплексов.
Фаза I клинических испытаний у человека
План исследования
Целью рандомизированного, плацебо контролируемого, двойного слепого исследования в фазу I испытаний было оценить безопасность, толерантность и фармакодинамический эффект (иммуногенность) вакцины, содержащей Qβ-Ангио 1. В исследовании оценивали режим одной дозы, состоящий из подкожной инъекции 100 мкг Qβ-Ангио 1 или плацебо, в смеси с гидроксидом алюминия. Двенадцать индивидуумов принимали активный препарат и четыре - плацебо. Индивидуумы находились в клинике 24 часа после введения дозы, и их обследовали на безопасность и толерантность препарата на 1, 2, 3 и 4 неделю. Фармакодинамический эффект (образование антител) измеряли на 1, 2, 3, 4, 8 и 16 неделю. Перед началом исследования протокол и другие соответствующие документы были согласованы с комиссией по этическим нормам, и исследование проводилось в соответствии с рекомендациями ICH GCP и Хельсинской декларацией (1964) и последними пересмотрами. Каждый индивидуум дал письменное согласие на участие в испытании.
Измерение иммунных комплексов
Концентрацию активированных факторов комплемента (С3а, С5а) и иммунных комплексов определяли с помощью анализов BD Biosciences (Heidelberg, Germany) и OSTEOmedical (Bünde, Germany), соответственно.
Индивидуумов наблюдали в течение 4 недель после вакцинации. Вакцинация Qβ-Ангио 1 переносилась хорошо. У четырнадцати из 16 индивидуумов наблюдались местные побочные эффекты (АЕ), такие как покраснение, отек, боль и уплотнение на месте инъекции. Все побочные эффекты были умеренными. Головную боль одного из индивидуумов (в активную фазу лечения) учли как вероятный побочный эффект лечения. Все другие системные АЕ (один индивидуум жаловался на заложенность носа и еще один на боль в горле), а также симптомы одного из индивидуума (в активную фазу лечения), который ощущал боль в спине в результате грыжи межпозвоночного диска и перенесенной операции, не сочли связанными с приемом препарата. Как и предполагалось, у указанных здоровых добровольцев с нормальным давлением не наблюдалось значительного изменения давления. Сердечный ритм и данные 12-канальной ЭКГ оставались без изменений, а лабораторные показатели не имели клинически значимых отклонений от нормальной области значений и, в частности, изменений клинических химических показателей, указывающих на заболевание почек.
Образование антител, вызванное вакцинацией, отслеживали на 0 неделе (перед введением дозы) и на 1, 2, 3, 4, 8 и 16 неделе. У двух добровольцев в фазе активного лечения были потеряны образцы на 1, 2, 3, 8 и 16 неделе и на 3, 8 и 16 неделе, соответственно. Все добровольцы, получавшие Qβ-Ангио 1, давали высокие титры IgG против ангиотензина II в течение 2 недель иммунизации (n=12). Титры достигали максимума на 3 неделе и уменьшались со средним значением времени полувыведения 19 дней (n=10, 95% CI [12-25], фиг.1). У добровольцев, получавших плацебо, не было обнаружено визуализируемое образование антител против ангиотензина II (n=4).
Индукция антител против эндогенного ангиотензина II теоретически могла приводить к образованию иммунных комплексов. Поэтому, авторы измерили исходный уровень концентрации иммунных комплексов, содержащих C1, C3, IgM, IgA или IgG, и на 7 и 14 день после иммунизации. Не было обнаружено никаких изменений уровней иммунных комплексов. Аналогично, не было обнаружено изменений уровней С3а и С5а в сыворотке относительно исходного уровня на 7 и 14 день после иммунизации. Qβ-Ангио 1 был высокоиммуногенным у людей и не вызывал никаких признаков воспаления или образования иммунных комплексов.
Фигура 4. Ангиотензин II-специфические IgG титры у здоровых добровольцев после единичной иммунизации Qβ-Ангио 1. Анти-ангиотензин II IgG титры 16 здоровых добровольцев определяли с помощью ELISA. Столбчатые диаграммы обозначают среднее геометрическое титров у индивидуумов с 95% доверительным интервалом. Титры индивидуумов, получавших активный препарат, показаны в виде закрашенных столбчатых диаграмм. У всех индивидуумов, получавших плацебо (n=4, не закрашенные столбчатые диаграммы), наблюдали титры ниже нижнего предела количественных показателей, установленного как 1:30.
Плотность связывания ангиотензиновых пептидов в CYT006-AngQb
Среднее число пептидов ангиотензина II на мономер Qβ определяли, используя восстановительный LDS-PAGE, окрашивая Кумасси синим. Не провзаимодействовавший мономер Qβ мигрировал с приблизительным молекулярным весом (MW) 16,2±0,3 кДа. После взаимодействия определяли число полос с большим молекулярным весом (фиг., ниже). Эти полосы соответствовали мономеру Qβ, связанному с одним, двумя, тремя, четырьмя, пятью или шестью ангиотензиновыми пептидами, при этом мономеры Qβ без ангиотензинового пептида не определялись
Для оценки плотности связывания использовали относительную интенсивность полос кластеров. Сумму относительной интенсивности полос мономера Qβ, связанного с одним, двумя, тремя, четырьмя, пятью или шестью ангиотензиновыми пептидами, умножали на соответствующее число пептидов, что соответствовало средней плотности связывания. В семи различных партиях ангиотензиновые пептиды AngQb 2.9-3.1 были связаны с мономерами Qβ. Так как Qβ VLP содержит 18 0 мономеров, то AngQb VLP содержит от 522 до 558 ангиотензиновых пептидов на VLP.
Фигура 5: Плотность связывания CYT006-AngQb, определенная с помощью LDS-PAGE/Кумасси Синий
Линии: (1) маркер Sigma 66 LMW; (2) Qβ эталонный стандарт IS018, партия QBP014; (3/4) CYT006-AngQb партия QAN005.
При том, что настоящее изобретение полностью описано с некоторыми подробностями, приведенными для иллюстрации и примера для целей ясности понимания, специалисту в данной области очевидно, что то же может быть осуществлено путем модификации или изменения изобретения в широком и эквивалентном интервале условий, композиций и других параметров без воздействия на объем изобретения или его каких-либо предпочтительных осуществлений, и что такие модификация или изменения подразумеваются как охваченные объемом прилагаемой формулы изобретения.
Все публикации, патенты и патентные заявки, упомянутые в данной спецификации, указывают на уровень знания специалистов в области, к которой относится данное изобретение, и включены сюда в качестве ссылки в той же степени, как если бы каждая отдельная публикация, патент или патентная заявка была бы конкретно и отдельно указана как включенная в качестве ссылки.



















| название | год | авторы | номер документа |
|---|---|---|---|
| КОНЪЮГАТЫ ГРЕЛИН-НОСИТЕЛЬ | 2003 |
|
RU2325202C2 |
| АНТИГЕННЫЕ МАТРИЦЫ ДЛЯ ЛЕЧЕНИЯ ЗАБОЛЕВАНИЯ КОСТЕЙ | 2002 |
|
RU2322258C2 |
| КОМПОЗИЦИЯ ДЛЯ ИММУНИЗАЦИИ (ВАРИАНТЫ), СПОСОБ ЕЕ ПОЛУЧЕНИЯ И ПРИМЕНЕНИЕ ДЛЯ ЛЕЧЕНИЯ АЛЛЕРГИЧЕСКИХ ЭОЗИНОФИЛЬНЫХ ЗАБОЛЕВАНИЙ | 2002 |
|
RU2319503C2 |
| КОНЪЮГАТЫ ПЕПТИДА Melan-A, АНАЛОГА ВИРУСОПОДОБНОЙ ЧАСТИЦЫ | 2004 |
|
RU2351362C2 |
| МОЛЕКУЛЯРНЫЕ МАССИВЫ АНТИГЕНОВ | 2003 |
|
RU2324704C2 |
| КОНЪЮГАТЫ ГАПТЕН-НОСИТЕЛЬ И ИХ ПРИМЕНЕНИЕ | 2003 |
|
RU2326693C2 |
| КОМПОЗИЦИЯ И СПОСОБ ДЛЯ ИММУНИЗАЦИИ, СПОСОБ ПРОДУЦИРОВАНИЯ НЕПРИРОДНОГО, УПОРЯДОЧЕННОГО И ПОВТОРЯЮЩЕГОСЯ МАССИВА АНТИГЕНОВ | 2002 |
|
RU2294211C2 |
| КОМПОЗИЦИЯ И СПОСОБ ДЛЯ ИММУНИЗАЦИИ, СПОСОБ ПРОДУЦИРОВАНИЯ НЕПРИРОДНОГО, УПОРЯДОЧЕННОГО И ПОВТОРЯЮЩЕГОСЯ МАССИВА АНТИГЕНОВ И ОБОЛОЧЕЧНЫЙ БЕЛОК | 2002 |
|
RU2295973C2 |
| БЕЛКИ, СЛИТЫЕ С КОШАЧЬИМ АЛЛЕРГЕНОМ, И ИХ ПРИМЕНЕНИЕ | 2006 |
|
RU2414239C2 |
| КОНЪЮГАТЫ ИНТЕРЛЕЙКИНА-1 И ИХ ПРИМЕНЕНИЕ | 2006 |
|
RU2441067C2 |
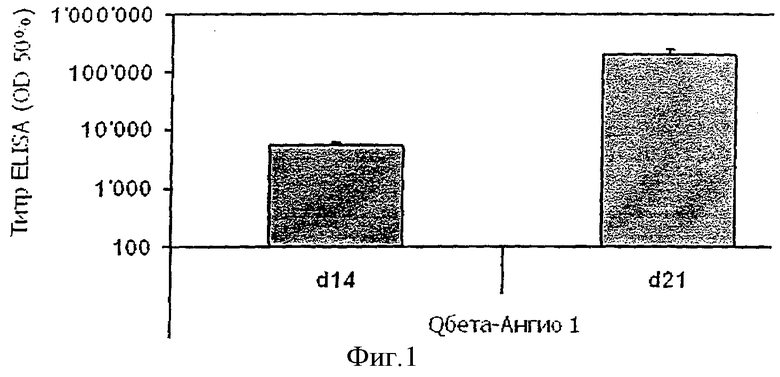
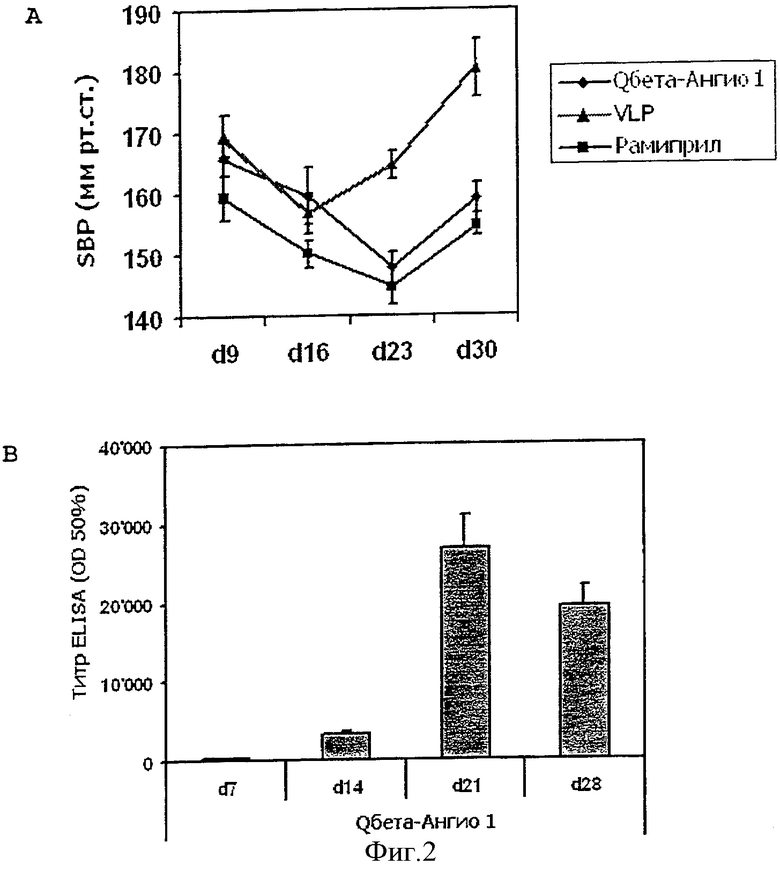
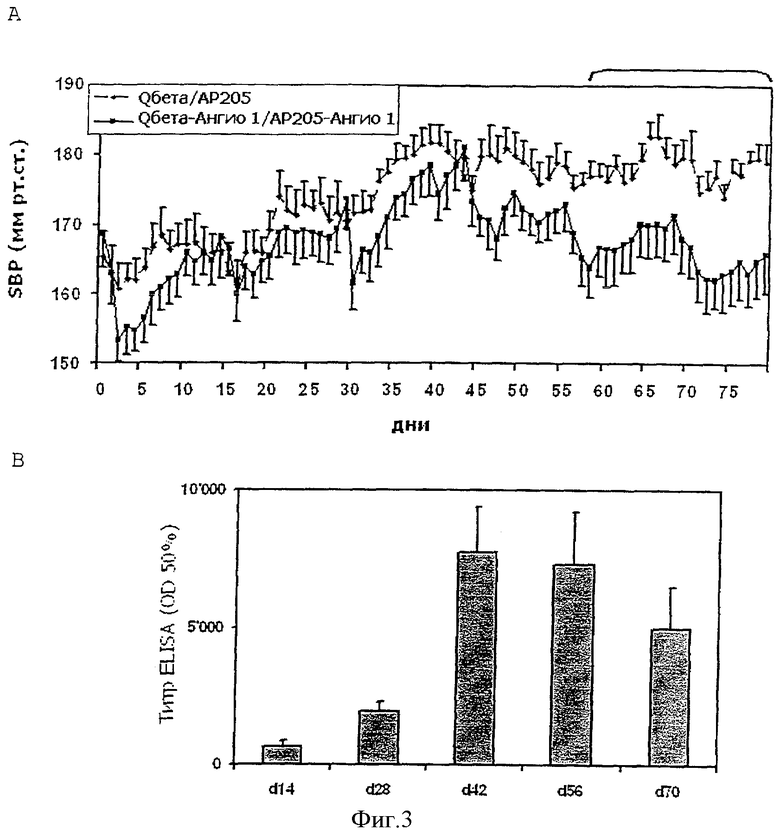
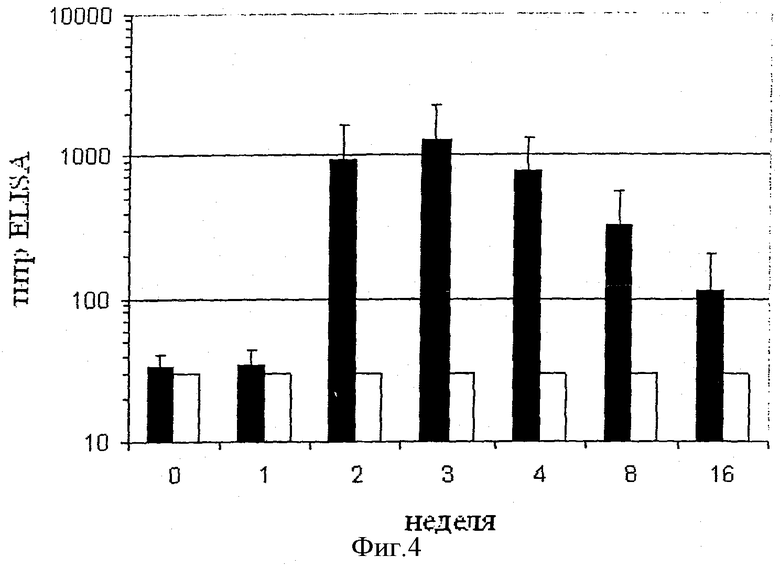
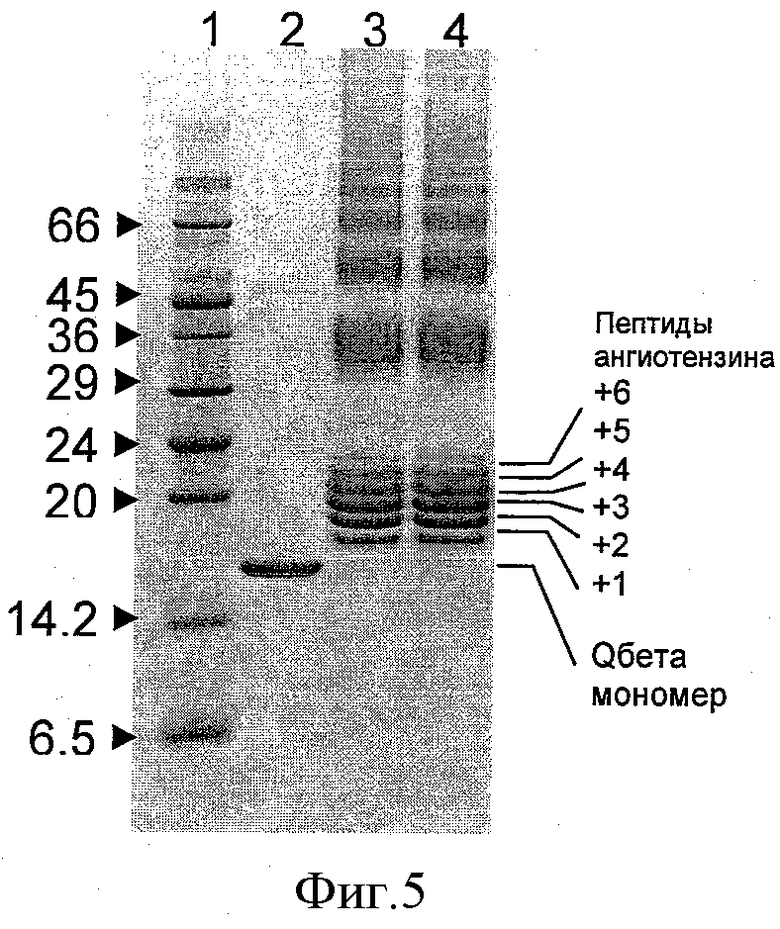
Изобретение относится к области генной инженерии, конкретно к иммуногенным конъюгатам, и может быть использовано для лечения и профилактики состояний, ассоциированных с активируемой ренином ангиотензиновой системой. Посредством непептидной ковалентной связи конъюгируют вирусоподобную частицу РНК-бактериофага с ангиотензиновой пептидной составляющей. Полученный конъюгат ангиотензиновой пептидной составляющей с носителем используют для иммунизации. Изобретение позволяет получить упорядоченный и повторяемый конъюгат ангиотензиновой пептидной составляющей с носителем. 5 н. и 24 з.п. ф-лы, 5 ил., 2 табл.
(a) носитель по крайней мере с одним первым участком связывания, и
(b) по крайней мере одну ангиотензиновую пептидную составляющую по крайней мере с одним вторым участком связывания,
где указанный носитель содержит коровую частицу, которая представляет собой вирусоподобную частицу РНК-бактериофага, и,
где указанный второй участок связывания связан с указанным первым участком связывания посредством по меньшей мере одной непептидной ковалентной связи и образует упорядоченный и повторяемый конъюгат ангиотензиновой пептидной составляющей с носителем.
a) бактериофага Qβ;
b) бактериофага R17;
c) бактериофага fr;
d) бактериофага GA;
e) бактериофага SP;
f) бактериофага MS2;
g) бактериофага M11;
h) бактериофага МХ1;
i) бактериофага NL95;
j) бактериофага f2;
k) бактериофага АР205; и
l) бактериофага РР7.
a) аминокислотной последовательности SEQ ID NO: 6;
b) аминокислотной последовательности SEQ ID NO: 7;
c) аминокислотной последовательности SEQ ID NO: 8;
d) аминокислотной последовательности SEQ ID NO: 9; и
e) аминокислотной последовательности SEQ ID NO: 10.
a) CGGDRVYIHPF (SEQ ID NO: 19);
b) CGGDRVYIHPFHL (SEQ ID NO: 20);
c) DRVYIHPFHLGGC (SEQ ID NO: 21);
d) CDRVYIHPFHL (SEQ ID NO: 22);
e) CHPFHL (SEQ ID NO: 23);
f) CGPFHL (SEQ ID NO: 24);
g) CYIHPF (SEQ ID NO: 25);
h) CGIHPF (SEQ ID NO: 26); и
i) CGGHPF (SEQ ID NO: 27).
Приоритет по пунктам:
| GARDINER S.M | |||
| et al | |||
| Active immunization with angiotensin I peptide analogue vaccines selectively reduces the pressor effects of exogenous angiotensin I in conscious rats, Br | |||
| J | |||
| Pharmacol., 2000, v.129, n.6, p.1178-1182 | |||
| WO 9858952 A1, 30.12.1998 | |||
| Культиватор для поверхностной обработки пара | 1928 |
|
SU32227A1 |
| CHACKERIAN B | |||
| et al | |||
| Кипятильник для воды | 1921 |
|
SU5A1 |
Авторы
Даты
2009-03-27—Публикация
2002-10-07—Подача