Изобретение относится к медицине, точнее к сосудистой хирургии, и может найти применение при операциях по прямой реваскуляризации конечностей.
Атеросклероз, по данным Всемирной Организации Здравоохранения за последние 5 лет, продолжает оставаться главной причиной смертности среди взрослого населения планеты. Облитерирующий атеросклероз сосудов нижних конечностей является одним из наиболее частых и опасных проявлений атеросклероза, который в 95% случаев ведет к инвалидизации населения. В настоящее время заболеваемость облитерирующим атеросклерозом сосудов нижних конечностей составляет от 3% до 20% к 70 годам жизни. На аутопсиях находят поражения до 50% просвета магистральных артерий нижних конечностей еще у 15% мужчин и 5% женщин. Необходимо заметить, что до 50% пациентов с симптомной формой заболевания не обращаются за медицинской помощью, поэтому цифры могут быть несколько другими в сторону увеличения частоты встречаемости рассматриваемой патологии.
На сегодняшний момент нуждаемость больных облитерирующим атеросклерозом в оперативном лечении ежегодно составляет в развитых странах 600 человек на 1 млн. населения. В то же время мировая статистика показывает, что на фоне активно развивающейся реконструктивной сосудистой хирургии еще 500 человек на 1 млн. населения нуждается в ампутации нижних конечностей в течение года. Летальность при данных видах вмешательств остается еще достаточно высокой, что обусловлено в первую очередь генерализованностью атеросклеротических поражений и плохим соматическим состоянием пациентов. Почти 40% пациентов, перенесших ампутацию по поводу терминальных стадий заболевания, погибает в первый год жизни после калечащей операции - по данным разных авторов, летальность составляет 10%, через год еще 25-30%.
Артериальные конструкции, создаваемые в ходе оперативного лечения, имеют ограниченный срок функционирования. Так, по данным различных авторов, кумулятивная проходимость аортобедренных шунтов через 5 лет составляет от 70% до 74%, окклюзии бедренно-подколенных шунтов от 20 до 40% в сроки от 3 до 5 лет. Поэтому рано или поздно для большого числа пациентов либо требуются повторные реконструктивные вмешательства, либо они теряют конечности. Причиной этого, как правило, является развитие облитераций в зоне дистальных анастомозов либо пластик. Конструкция тромбируется, ишемия конечности возвращается, порой в более выраженных проявлениях, что ведет к необходимости выполнения ампутаций. Поэтому все более актуальной становится проблема улучшения качества реконструктивных операций на магистральных артериях конечностей как главного метода лечения этого заболевания на стадиях выраженных манифестаций патологических проявлений и осложнений, а также определение тактики лечения таких больных.
Известен способ определения показаний к оперативному лечению больных облитерирующим заболеванием нижних конечностей путем изучения регионарной гемодинамики [С.В.Иванов, В.Э.Кудряшов, Ю.В.Белов // Сравнительная информативность допплерографических показателей скорости кровотока и давления в оценке степени ишемии нижних конечностей. - Хирургия, - 1995. - N6. - с.11-13]. Он заключается в том, что больным проводят допплерографическую оценку линейной скорости кровотока, объемного кровотока, а также с помощью аппарата Рива-Роччи и ультразвукового датчика неинвазивно определяют регионарное артериальное давление (на дистальных артериях нижних конечностей) и артериальное давление на плече, принимая его за системное. Анализируя полученные данные, интерпретируют их следующим образом: градиент (перепад, разность) регионарного артериального давления (АД) на различных сегментах характеризует уровень сопротивления артериального русла конечности, а соотношение величин регионарного артериального давления и системного АД, называемое плече-лодыжечным индексом, отражает степень тяжести периферической артериальной недостаточности. Величина объемного кровотока в конечности также косвенно характеризует уровень сопротивления артериального русла. Линейная скорость кровотока отражает прежде всего локальную морфологическую ситуацию в сосудистом русле в месте измерения. На основе анализа этих данных авторы делают вывод о состоянии регионарной гемодинамики и при значениях плече-лодыжечного индекса ниже 0,5 ставят показания к оперативному лечению.
Этот способ явился первым объективно отражающим в цифровой форме состояние кровообращения нижних конечностей, но тем не менее он не лишен серьезных недостатков.
Во-первых, величина объемного кровотока по сосуду является расчетной величиной, в основе которой лежат округленные данные о диаметре артерии, а также данные о линейной скорости кровотока, зависящие от внутрисосудистого рельефа проксимальнее, дистальнее и в месте измерения.
Во-вторых, определение градиента артериального давления не совсем корректно, так как за системное берется АД на плечевой артерии (не всегда артериальное русло верхних конечностей достоверно отражает системное давление: атеросклероз, удаленность от аортального кольца, анатомические особенности в строении магистральных сосудов конкретного индивидума). Кроме того, артериальное давление у "входа" в сосудистое русло нижней конечности не обязательно должно соответствовать системному АД по причинам наличия атеросклеротических и иных (аневризматическая трансформация, патологическая извитость артерий) препятствий на пути кровотока от аортального кольца до конечности, а также самой длины этого пути.
В-третьих, способ, объективно отражая состояние кровоснабжения тканей конечности и перфузионную достаточность магистрального артериального кровотока (перфузионное давление в магистральных артериях, его соотношение с системным АД, количественную характеристику притока крови к тканям нижних конечностей в виде объемного кровотока), позволяет принять решение о необходимости оперативной коррекции перфузии тканей, но тем не менее не дает возможности объективно оценить периферическое сопротивление в артериальном русле нижних конечностей после операции, что затрудняет определение хирургической тактики послеоперационного лечения пациента. Эта тактика и определяет в первую очередь показания к дополнительной реваскуляризации нижнего этажа артериального русла конечности. Именно эти дополнительные вмешательства, выполненные своевременно, обеспечивают адекватное кровообращение в конечности и значительно удлиняют продолжительность «жизни» создаваемой конструкции. Таким образом, этот способ не позволяет достоверно спрогнозировать развитие возможного атеросклеротического процесса с учетом изменившихся в ходе операции гемодинамических условий и не может лежать в основе определения тактики лечения больных в послеоперационном периоде.
Известен способ определения показаний к проведению хирургической коррекции нарушений регионарной гемодинамики при реконструктивных операциях на артериях нижних конечностей (Майстренко Д.Н., Майстренко А.Д. Патент РФ N2239373 на «Способ определения показаний к проведению хирургической коррекции нарушений регионарной гемодинамики при реконструктивных операциях на артериях нижних конечностей), при котором производят измерения АД непосредственно в исследуемой артерии после реваскуляризации конечности одновременно с записью ЭКГ. Артериальное давление регистрируют после выполнения реваскуляризации непосредственно в исследуемой артерии инвазивно при свободном кровотоке и после пережатия ее дистальнее места исследования, регистрируют в том и другом случаях барограммы, определяют площади под их кривыми за один сердечный цикл, находят разность их значений и если она более 1,0 кПА×с предполагают локальную баротравму сосудистой стенки, вызывающую избыточную пролиферацию эндотелия, а также неудовлетворительные условия локального кровотока, приводящие к преждевременному патологическому внутрисосудистому тромбозу, что требует гемодинамической хирургической коррекции.
Регистрация АД непосредственно в исследуемой артерии после реваскуляризации конечности характеризует объективную картину, сложившуюся после запуска кровотока по вновь созданному в ходе операции пути, что позволяет своевременно скорректировать тактику лечения больного уже на интраоперационном этапе. Однако инвазивность способа, а также возможность его применения только во время операции не позволяют проводить исследование в динамике во время диспансерного мониторинга за пациентом. Таким образом, использование такого способа, как и вышеописанного, не дает возможности корректировать лечебный процесс в отдаленном послеоперационном периоде, когда с течением времени меняются условия регионарной гемодинамики.
Наиболее близким к предлагаемому является способ определения тактики хирургического лечения больных облитерирующим атеросклерозом путем диагностики нарушений регионарной гемодинамики в послеоперационном периоде за счет определения мощности потока крови в исследуемой артерии после реваскуляризации конечности [Майстренко Д.Н., Майстренко А.Д. Патент РФ №2270609 на «Способ определения показаний к проведению коррекции нарушений регионарной гемодинамики после реконструктивных операций на артериях нижних конечностей»]. Способ заключается в том, что непосредственно в исследуемой артерии методом ультразвуковой допплерографии определяют значение начальной скорости кровотока в систолу (V0), максимальное значение линейной скорости кровотока (V1), минимальное значение линейной скорости кровотока (V2), а также время (t1) между изменением скорости от V0 до V1, время (t2) изменения скорости от V1 до V2 и по формуле М=100%-(V2 2-V1 2)t1/(V1 2-V0 2)t2×100% находят показатель коэффициента потери мощности потока крови (М) и при его значении более 65% считают целесообразной коррекцию регионарной гемодинамики.
Определение абсолютных значений линейных скоростей кровотока, времени ускорения и замедления, а также их оценка позволяют косвенно судить о состоянии периферического артериального русла и о кровообращении в нем. V0 дает лишь косвенное субъективное представление о сопротивлении дистального русла, V1 отражает степень стеноза артерии в месте исследования, V2 - диастолический компонент регионарного кровотока - субъективный показатель наличия повышенного периферического сопротивления в сосуде. Накопление этих данных и сопоставление их с клиническими наблюдениями за пациентами убедили авторов в малой информативности этих показателей. Наиболее важным для реконструктивной сосудистой хирургии объективным показателем, который в численной форме отражает периферическое сопротивление, является мощность потока крови. Сопротивление периферического артериального русла обусловлено множеством составляющих компонентов: анатомическими особенностями (наличием и выраженностью перитоков и коллатералей), емкостью сосудистого русла, локализацией и выраженностью атеросклеротического поражения артерий, условиями гемодинамики (давлением на входе в артериальное русло нижних конечностей, соотношением фаз анте- и ретроградных потоков крови по сосудам), реологией и т.д. Авторы работы считают, что, используя коэффициент потери мощности потока крови, можно не учитывать роль каждого из этих составляющих факторов, условившись определять интегральное регионарное периферическое сопротивление дистальнее места измерения, поскольку фактическая роль каждого конкретного составляющего фактора сопротивления не имеет практической значимости, в то время как значение их совокупного влияния на гемодинамику трудно переоценить. Кроме того, определение коэффициента потери мощности на одном и том же участке артерии позволяет свести к минимуму погрешности, связанные с учетом диаметра артерии, измерение которого в реальных условиях всегда является приблизительным. Таким образом, авторами работы был создан способ определения достаточно объективного показателя, отражающего сопротивление периферического русла (М или в дальнейшем КПМ).
Опытным путем, на основании наблюдений за отдаленными результатами оперированных пациентов, им удалось показать, что значение коэффициента потери мощности потока крови более 65% требует гемодинамической хирургической коррекции. При значениях коэффициента потери мощности потока крови менее 65% дополнительная хирургическая коррекция гемодинамики в исследуемом бассейне не требуется. Последующее проведение консервативной вазоактивной терапии обязательно в обоих вариантах лечения.
Авторы считают, что регистрация линейной скорости кровотока, определение его ускорения и вычисление показателя коэффициента потери мощности потока крови, отражающего локальное сопротивление непосредственно в исследуемой артерии после реваскуляризации конечности, характеризует объективную картину, сложившуюся после запуска кровотока по вновь созданному в ходе операции пути, что позволяет своевременно скорректировать лечебный процесс и определить тактику послеоперационного ведения больного практически на всем этапе диспансерного наблюдения за пациентом.
Кроме того, определение коэффициента потери мощности потока крови проксимальнее и дистальнее места хирургической операции на артериальном русле пациента позволяет по разнице его значений на входе и выходе из зоны операции оценивать гемодинамические характеристики самой искусственной конструкции (аутовенозного шунта, синтетического протеза, участка пластики артерии). Это очень важно в прогностическом плане, так как это дает возможность выбора оптимальной для конкретного больного и конкретной анатомической ситуации варианта хирургического лечения.
Таким образом, нахождение коэффициента потери мощности (КПМ) потока крови определяет показания к дополнительной реваскуляризации нижнего этажа артериального русла, наложению артериовенозной фистулы, что обеспечивает адекватное кровообращение в конечности и удлиняет продолжительность «жизни» созданной конструкции. Иными словами, КПМ свидетельствует о том, что необходима ли больному коррекция регионарной гемодинамики в момент операции по прямой реваскуляризации конечности и в послеоперационном периоде.
Как свидетельствуют вышеприведенные способы, в том числе и прототип, показанием к хирургической коррекции регионарного сопротивления при облитерирующем атеросклерозе сосудов нижних конечностей является определение значения того или иного индекса, характеризующего состояние регионарной гемодинамики, причем, определение их производится после операции по прямой реваскуляризации конечностей. А поскольку создаваемые при ее выполнении артериальные конструкции достаточно быстро тромбируются и ишемия возвращается, зачастую в более выраженных проявлениях, большое число больных, в первую очередь пожилых людей, не решается на повторное хирургическое вмешательство, обеспечивающее дополнительную реваскуляризацию артериального русла несмотря на то, что именно она обеспечивает адекватное кровообращение и удлиняет «жизнь» созданных на первом этапе операции конструкций. Вместе с тем, в настоящее время не существует неинвазивного способа, определяющего в предоперационном периоде адекватную тактику лечения облитерирующего атеросклероза сосудов нижних конечностей.
Задача настоящего изобретения состояла в разработке одноэтапного способа лечения облитерирующего атеросклероза сосудов нижних конечностей на основе предоперационного определения денситометрии скелетных мышц нижних конечностей.
Эта задача решена тем, что в известном способе лечения облитерирующего атеросклероза сосудов нижних конечностей, включающем реконструкцию магистрального артериального русла и формирование дистальной артериовенозной фистулы с последующей консервативной вазоактивной терапией, согласно изобретению, предварительно выполняют компьютерную или магнитно-резонансную томографию скелетной мускулатуры нижней конечности (конечностей), определяют плотность мышечной ткани задних групп мышц голени, а формирование дистальной артериовенозной фистулы осуществляют непосредственно после завершения реконструкции магистрального артериального русла при плотности мышечной ткани задних групп мышц голени, менее или равной 40 HU, по данным компьютерной томографии (КТ) или соотношении сигнал/шум, равном или более 10 условных единиц, по данным магнитно-резонансной томографии (МРТ), выполненной на аппарате Magnetom vision с напряженностью магнитного поля 1,5 Тс.
Известно, что длительность функционирования создаваемых при операциях по прямой реваскуляризации конечностей артериальных конструкций ограничена в среднем 2-5 годами, после чего больному предстоит повторное реконструктивное вмешательство либо потеря конечности.
Реконструктивными операциями по поводу облитерирующего атеросклероза мы занимаемся в течение многих лет. Целью наших научных исследований является улучшение результатов реконструктивных операций при этом грозном заболевании. В последние годы в ходе нашей работы обследовано 192 пациента, 36 из которых попали в исследование после повторных оперативных вмешательств. Нами были отслежены результаты больных, дисциплинированно принимавших антикоагулянты и дезагреганты, прописанные лечащим врачом. Средний возраст пациентов составил 58,4+4,2 лет. Из них 12 были женщины, остальные - мужчины. До операции стадия заболевания составляла 67,9% IIб, 25,8% III, 6,3% IV. Сопутствующую патологию имели: гипертоническая болезнь II стадии 89,1%, ИБС 86,9%, язвенная болезнь желудка 18,7% больных.
Все пациенты были обследованы самыми современными методами, включая выполнение КТ, МРТ ангиографии и позитронной эмиссионной томографии (ПЭТ) (до и после операции). Оценивали периферическое сосудистое сопротивление с определением КПМ на 7 сутки после операции, используя разработанную нами ранее формулу: КПМ=100%-((V2 2-V1 2)t1/(V1 2-V0 2)t2×100%, где V1 - максимальные показатели линейной скорости кровотока, V2 - минимальные значения линейной скорости кровотока, V0 - линейная скорость кровотока в систолу, t1 - время изменения линейных скоростей кровотока от V0 до V1, t2 - время изменения показателя линейной скорости кровотока от V1 до V2.
Нам удалось выявить корреляцию между повышением показателя определяемого нами коэффициента потери мощности (КПМ) в оперированной конечности с отрицательными отдаленными результатами реконструктивных операций в течение 12 месяцев наблюдения.
Эти результаты позволили нам предположить, что повышение КПМ имеет множество причин. Помимо особенностей внутрисосудистого рельефа в магистральных артериях конечностей, их анатомических особенностей, а также особенностей атеросклеротических поражений, имеет значение и состояние микроциркуляции, зависящее в свою очередь от состояния самой скелетной мускулатуры конечности. Мы отметили, что у ряда больных, имеющих худшие результаты лечения, имела место гипотрофичность скелетной мускулатуры нижних конечностей. Проведенное нами гистологическое исследование этих мышц показало соединительно-тканное перерождение их.
Одновременно были проанализированы данные МРТ и КТ, характеризующие скелетную мускулатуру нижних конечностей.
Мы сопоставили эти данные с данными КПМ, которые представлены в таблице.
Как видно из приведенных данных, имеется статистически достоверная связь между состоянием скелетной мускулатуры и уровнем КПМ.
С целью уточнения влияния на значение КПМ у больных процесса некротизации части скелетной мускулатуры во время выраженных приступов перемежающейся хромоты, эквивалентной инфаркту, и дальнейшего миосклероза, мы провели исследования ПЭТ у части обследуемых в ходе нашей работы больных. Полученные данные не могут ввиду малочисленности быть обработаны статистически, однако представляют прекрасный иллюстративный материал. Полученные данные представлены на фиг.1 (пациент, у которого артериальное русло нижних конечностей без гемодинамически значимого поражения - контроль) и фиг.2 (больной с выраженным облитерирующим атеросклерозом сосудов нижних конечностей IV ст. Синдром Лериша. Субокклюзия правой глубокой артерии бедра. Билатеральная окклюзия поверхностных бедренных артерий. Критическая ишемия правой голени и стопы. Трофическая язва правой голени в нижней трети). У больного (фиг.2) на правой нижней конечности видно отсутствие признаков метаболизма мягких тканей после восстановленного кровообращения в этой конечности, что свидетельствует о соединительно-тканном перерождении ее скелетной мускулатуры. На фиг.3-4 приведены гистологические препараты тех же больных. Сравнение их демонстрирует перерождение мышц у больного пациента (фиг.4).
Полученные в ходе нашей работы данные позволили нам сделать вывод о том, что облитерирующий атеросклероз сосудов нижних конечностей не только многостадийное поражение магистральных артерий конечностей, но и последовательный патологический процесс поражения скелетной мускулатуры конечностей, ведущий на фоне гипоксии тканей к соединительно-тканному перерождению мышц, сопровождающийся редукцией микроциркуляторного русла и проявляющийся повышением периферического сосудистого сопротивления, который ранее мы оценивали по значению КПМ. Указанные процессы, по нашим данным, ведут, с одной стороны, к прогрессированию атерогенеза за счет повышения роли гемодинамических нарушений, а, с другой стороны, ограничивают сроки эффективного функционирования созданных в ходе операций конструкций.
Наличие достоверной информации о периферическом сосудистом сопротивлении (определяемом в послеоперационном периоде) позволяет прогнозировать клинические результаты хирургического лечения с высокой долей вероятности. Данные же о состоянии скелетной мускулатуры конечностей и соответственно микроциркуляторного русла (при найденных нами количественных значениях их) свидетельствуют о необходимости инвазивного лечения больных и требуется ли больному одновременное наложение артериовенозной фистулы.
Выполнение приведенных выше исследований побудило нас проводить больным облитерирующим атеросклерозом сосудов нижних конечностей дооперационное исследование плотности скелетных мышц и при их значении, равном или менее 40 HU, по данным КТ, или равном или более 10 условных единиц, по данным МРТ (Magnetom vision с напряженностью магнитного поля 1,5 Тс.), выполнять шунтирование с одновременным формированием артериовенозной фистулы.
Именно найденные нами показатели плотности скелетной мускулатуры пораженной конечности, характеризующие, как свидетельствуют наши исследования, периферическое сопротивление магистрального русла, являются показанием к интраоперационному формированию разгрузочных артериовенозных фистул.
Сущность способа поясняется примерами.
ПРИМЕР 1. Больной Н., 1953 г. рождения, поступил в клинику Центрального научно-исследовательского рентгенорадиологического института (ЦНИРРИ) 04.11.2003 г. с диагнозом: облитерирующий атеросклероз сосудов нижних конечностей II б ст.
Из анамнеза: весной 1998 г. в областной клинической больнице (СПб) больному было выполнено аортобедренное бифуркационное шунтирование. Осенью 1998 г. там же выполнено аутовенозное бедренноподколенное шунтирование слева. Коэффициент потери мощности после оперативного вмешательства составлял 68,9%. Конструкция функционировала 2 года. В 2001 г. - состояние после тромбоза аутовенозного бедренно-подколенного шунта слева. От оперативного вмешательства больной отказался.
При поступлении в клинику ЦНИРРИ больному выполнены МРТ ангиография, МРТ денситометрия мышц левой голени. Плотность скелетной мускулатуры в задней группе мышц левой голени составила 12,3 у.е., что являлось показанием к хирургической коррекции повышенного периферического сопротивления путем формирования дистальной артериовенозной фистулы.
10.11.2003 г. больному выполнено оперативное вмешательство: бедренно-подколенное дистальное шунтирование слева синтетическим протезом "GORE-TEX". Симультантно формирование дистальной артериовенозной фистулы между a. Tibialis anterior и сопровождающей веной в нижней трети левой голени. МРТ ангиография контроль-конструкция функционирует, в т.ч. фистула. При УЗДГ контроле отмечено низкое периферическое сопротивление кровотоку по шунту с высокой линейной скоростью кровотока. КПМ 44,7%. У больного исчезла перемежающаяся хромота. При УЗДГ-контроле плече-лодыжечный индекс (ЛПИ) увеличился с 0,36 до операции до 0,78 после операции (при ЛПИ>0,5 кровообращение в нижней конечности считается компенсированным).
Больной выписан с хорошим клиническим результатом. Пациент получает стандартную антикоагулянтную терапию Варфарином 2 табл. на ночь под контролем MHO (международные нормализованные отношения - отношение протромбинового индекса (ПТИ) стандартной сыворотки к ПТИ сыворотки больного).
Наблюдение за больным продолжается до настоящего времени - состояние его удовлетворительное (без отрицательного результата). Больной периодически получает курсы вазоактивной консервативной терапии: Вазапростан 60 мкг на 200 мл физиологического раствора внутривенно капельно N 10 2 раза в год. Созданная ему в 2003 г. конструкция функционирует уже в течение 4-х с лишним лет.
ПРИМЕР 2. Больной И., 1949 г.рождения, поступил в ЦНИРРИ 15.09.2002 г. с диагнозом: облитерирующий атеросклероз сосудов нижних конечностей II б ст. Окклюзия бедренно-подколенного сегмента слева.
Больному выполнено КТ ангиография, КТ денситометрия мышц левой голени. Плотность скелетной мускулатуры в задней группе мышц левой голени составила 47 HU, по данным МРТ 8,8 у.е., что свидетельствовало об отсутствии показаний к гемодинамической хирургической коррекции.
22.09.2002 г. больному выполнено оперативное вмешательство: аутовенозное бедренно-подколенное шунтирование слева (реверс). МРТ ангиография контроль-конструкция функционирует. При УЗДГ контроле отмечено низкое периферическое сопротивление кровотоку по шунту с высокой линейной скоростью кровотока. КПМ 56,8%. У больного исчезла перемежающаяся хромота. При УЗДГ-контроле плече-лодыжечный индекс увеличился с 0,27 до операции (при ЛПИ<0,3 кровообращение в конечности считается декомпенсированным) до 0,72 после операции (при ЛПИ>0,5 - компенсированное). Больной выписан с хорошим клиническим результатом. Пациент получает стандартную антикоагулянтную терапию Варфарином 2 табл. на ночь под контролем MHO.
Наблюдение за больным до настоящего времени (более 5 лет) без отрицательного результата. Больной не получает вазоактивной консервативной терапии.
К настоящему времени оперативные вмешательства на основе дооперационного определения плотности скелетных мышц выполнены у 56 пациентов, наблюдение за которыми составляет уже 7 лет, из них у 26 одновременно с реконструкцией магистрального артериального русла формировалась дистальная артериовенозная фистула. При этом лишь у одного пациента имело место возвращение ишемии конечности, но и у него по объективной причине (больной отказался от приема антикоагулянтов - стандартного обязательного условия после реконструктивной операции). Все остальные больные продолжают наблюдаться и находятся в удовлетворительном состоянии.
Предлагаемый способ по сравнению с известными имеет ряд существенных преимуществ.
1. Впервые обеспечивает определение адекватной тактики лечения больных с облитерирующим атеросклерозом сосудов нижних конечностей в дооперационном периоде (на стадии обследования больного), что не может дать ни один из известных способов.
2. Обеспечивает создание у больных оптимальных гемодинамических условий для функционирования формируемых во время операции сосудистых конструкций, обеспечивая их долголетнюю адекватную работу и предотвращая тем самым необходимость выполнения в последующем калечащей операции.
3. Позволяет прогнозировать клинические результаты хирургического лечения с высокой долей вероятности.
Способ разработан в отделе интервенционной терапии ЦНИРРИ, прошел клиническую апробацию у 56 пациентов с положительным результатом.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ формирования артериовенозной фистулы для профилактики нарушения проходимости магистральных артерий нижних конечностей | 2021 |
|
RU2780929C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ПОКАЗАНИЙ К ПРОВЕДЕНИЮ ХИРУРГИЧЕСКОЙ КОРРЕКЦИИ НАРУШЕНИЙ РЕГИОНАРНОЙ ГЕМОДИНАМИКИ ПРИ РЕКОНСТРУКТИВНЫХ ОПЕРАЦИЯХ НА АРТЕРИЯХ НИЖНИХ КОНЕЧНОСТЕЙ | 2004 |
|
RU2239373C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ПОКАЗАНИЙ К ПРОВЕДЕНИЮ КОРРЕКЦИИ НАРУШЕНИЙ РЕГИОНАРНОЙ ГЕМОДИНАМИКИ ПОСЛЕ РЕКОНСТРУКТИВНЫХ ОПЕРАЦИЙ НА АРТЕРИЯХ НИЖНИХ КОНЕЧНОСТЕЙ | 2005 |
|
RU2270609C1 |
| СПОСОБ ХИРУРГИЧЕСКОЙ КОРРЕКЦИИ НАРУШЕНИЙ РЕГИОНАРНОЙ ГЕМОДИНАМИКИ ПРИ ОБЛИТЕРИРУЮЩИХ ЗАБОЛЕВАНИЯХ АРТЕРИЙ КОНЕЧНОСТЕЙ | 2001 |
|
RU2189785C1 |
| СПОСОБ ДИАГНОСТИКИ НАРУШЕНИЙ РЕГИОНАРНОЙ ГЕМОДИНАМИКИ ПРИ ОПЕРАЦИИ ПРЯМОЙ РЕВАСКУЛЯРИЗАЦИИ КОНЕЧНОСТИ | 2001 |
|
RU2198583C1 |
| СПОСОБ ПЛАСТИКИ ТИБИОПЕРОНЕАЛЬНОГО СТВОЛА ПРИ СУБТОТАЛЬНОЙ ОККЛЮЗИИ ВЕТВЕЙ ПОДКОЛЕННОЙ АРТЕРИИ ПРИ ПРОВЕДЕНИИ ТРОМБОЭКТОМИИ ИЛИ БЕДРЕННО-ПОДКОЛЕННОГО ШУНТИРОВАНИЯ | 2023 |
|
RU2815343C1 |
| Способ комбинированной хирургической стимуляции неоангиогенеза хронической ишемии нижних конечностей | 2018 |
|
RU2703395C1 |
| Комбинированный способ лечения пациентов с критической ишемией нижних конечностей | 2023 |
|
RU2796189C1 |
| СПОСОБ ВОССТАНОВЛЕНИЯ МАГИСТРАЛЬНОГО АРТЕРИАЛЬНОГО КРОВОТОКА НИЖНИХ КОНЕЧНОСТЕЙ | 2015 |
|
RU2601698C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ФУНКЦИОНИРОВАНИЯ БЕДРЕННО-ТИБИАЛЬНОЙ РЕКОНСТРУКЦИИ ПОСЛЕ ШУНТИРУЮЩИХ ОПЕРАЦИЙ | 2014 |
|
RU2576082C1 |
Изобретение относится к области медицины, а именно к сосудистой хирургии. Предварительно выполняют компьютерную или магнитно-резонансную томографию скелетной мускулатуры нижней конечности (конечностей). Определяют плотность мышечной ткани задних групп мышц голени, а формирование дистальной артериовенозной фистулы осуществляют непосредственно после завершения реконструкции магистрального артериального русла при плотности мышечной ткани задних групп мышц голени, равной или менее 40 HU, по данным компьютерной томографии, или соотношении сигнал/шум, равном или более 10 условных единиц, по данным магнитно-резонансной томографии, выполненной на аппарате Magnetom vision с напряженностью магнитного поля 1,5 Тс. Способ расширяет арсенал средств для определения адекватной тактики лечения облитерирующего атеросклероза сосудов нижних конечностей. 4 ил., 1 табл.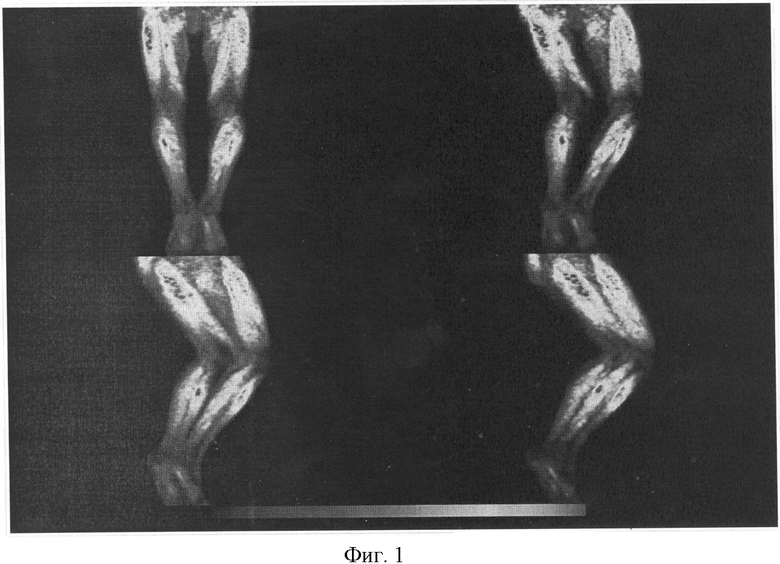
Способ лечения облитерирующего атеросклероза сосудов нижних конечностей, включающий реконструкцию магистрального артериального русла и формирование дистальной артериовенозной фистулы с последующей консервативной вазоактивной терапией, отличающийся тем, что предварительно выполняют компьютерную или магнитно-резонансную томографию скелетной мускулатуры нижней конечности (конечностей), определяют плотность мышечной ткани задних групп мышц голени, а формирование дистальной артериовенозной фистулы осуществляют непосредственно после завершения реконструкции магистрального артериального русла при плотности мышечной ткани задних групп мышц голени, равной или менее 40 HU, по данным компьютерной томографии, или соотношении сигнал/шум, равном или более 10 условных единиц, по данным магнитно-резонансной томографии, выполненной на аппарате Magnetom vision с напряженностью магнитного поля 1,5 Тс.
| СПОСОБ ОПРЕДЕЛЕНИЯ ПОКАЗАНИЙ К ПРОВЕДЕНИЮ КОРРЕКЦИИ НАРУШЕНИЙ РЕГИОНАРНОЙ ГЕМОДИНАМИКИ ПОСЛЕ РЕКОНСТРУКТИВНЫХ ОПЕРАЦИЙ НА АРТЕРИЯХ НИЖНИХ КОНЕЧНОСТЕЙ | 2005 |
|
RU2270609C1 |
| СПОСОБ ОЦЕНКИ ЭФФЕКТИВНОСТИ СОСУДИСТОЙ РЕКОНСТРУКЦИИ У БОЛЬНЫХ С КРИТИЧЕСКОЙ ИШЕМИЕЙ НИЖНИХ КОНЕЧНОСТЕЙ | 2006 |
|
RU2310376C1 |
| US 7313428, 25.12.2007 | |||
| ЕВГРАФОВ А.И | |||
| Оценка состояния периферического русла нижних конечностей в выборе показаний к реконструктивным сосудистым вмешательствам при облитерирующем атеросклерозе, автореф | |||
| дисс., 2005, с.4-21 | |||
| HEIJENBROK-KAL M.H | |||
| et al | |||
| Lower extremity arterial disease: | |||
Авторы
Даты
2009-07-20—Публикация
2008-03-24—Подача