Область техники, к которой относится изобретение
Настоящее изобретение касается способа ферментации и культивирования для получения иммуностимулятора, который безопасен при добавлении в лекарственные препараты, препараты для животных, квазилекарства, косметику, продукты питания, функциональные продукты питания, кормовые продукты и моющие средства для млекопитающих, включая людей (особенно домашних животных, домашних питомцев и т.п.), птиц (особенно выращиваемых цыплят, домашних птиц и т.п.), амфибий, рептилий, рыб (особенно выращиваемых рыб, домашних рыбок и т.п.) и беспозвоночных, способа получения экстракта ферментированного растения, экстракта ферментированного растения, содержащего иммуностимулятор, полученный способом ферментации и культивирования, порошка, содержащего иммуностимулятор, полученный из экстракта ферментированного растения, и композиции экстракта ферментированного растения, содержащей экстракт ферментированного растения.
Предшествующий уровень техники
Актуальной проблемой является обеспечение предотвращения заболевания и способов терапии, включая технологию профилактики инфицирования млекопитающих, включая человека (особенно домашних животных, домашних питомцев и т.п.), птиц (особенно выращиваемых цыплят, домашних птиц и т.п.), амфибий, рептилий, рыб (особенно выращиваемых рыб, домашних рыбок и т.п.) и беспозвоночных. Более того, для достижения этого чрезвычайно необходимы способы без использования химических реагентов, без загрязнения окружающей среды, без получения резистентных бактерий и накапливания в человеческом организме. Авторы настоящего изобретения уже обнаружили для перечисленных выше проблем, что иммуностимуляторы растительного происхождения, такие как водный экстракт пшеницы, надежно предотвращают заболевание и имеют терапевтический эффект (патентный документ 1, непатентный документ 1). Также для достижения указанного выше эффекта авторы настоящего изобретения установили, что существует возможность использовать низкомолекулярные липополисахариды, полученные из Pantoea agglomerans, который является симбиотической бактерией для пшеницы (непатентный документ 2). При этом недавние исследования показали, что различные вещества в дополнение к липополисахаридам проявляют иммунопотенциирующий (иммуностимулирующий) эффект, и это множество натуральных материалов, содержащих иммуностимулятор, привлекло внимание.
Технология ферментации с использованием микроорганизмов используется обычно не только в пищевой промышленности, но также и в более широких областях. Ферментация широко применялась для получения спиртов, включая вина, получения соусов из сои и паст из бобов сои, продуктов ферментации молока, таких как сыры, и для получения лекарственных препаратов. Существует много микроорганизмов, используемых для этих видов ферментации, и примерами являются дрожжи рисового солода (гриб) и молочные бактерии, но редки случаи применения грамотрицательных бактерий. В основном ферментация является явлением, при котором органическая материя разлагается под действием микроорганизма, и подразумевает, в широком смысле, образование микроорганизмом полезного вещества (непатентный документ 3). Примеры использования микроорганизмов в ферментации включают виноделие. Виноделие является технологией ферментации с использованием адгезии дрожжей к кожице винограда и ее продуктом является спирт. В технологии ферментации с использованием микроорганизма известны использование как таковых грамотрицательных бактерий, ферментации метана с использованием метановых бактерий, уксусной ферментации с использованием уксусных грибков и ферментации этанола (ферментация текилы) из корневища американской агавы, с применением Zymomonas mobilis, но едва ли известна ферментация культуры с использованием съедобного растения в качестве материала и микроорганизма, характеризующегося симбиотическим взаимодействием с растением, и данный иммуностимулятор никогда не привлекал внимания как продукт ферментации. Кроме того, способ ферментации и культивирования с целью получения иммуностимулятора никогда не привлекал внимания.
При этом, при проведении ферментации с помощью микроорганизма, в основном, существуют условия питания для роста микроорганизма, которым ферментируемый субстрат должен соответствовать. То есть присутствие веществ, потребляемых микроорганизмом в качестве питательных веществ, необходимо, например в качестве источников углерода содержатся в достаточном количестве моносахариды, такие как глюкоза и фруктоза. Следовательно, фрукты, такие как богатый фруктозой виноград, могут быть использованы в качестве субстрата ферментации без проведения какой-либо обработки. Однако в других случаях необходима предварительная обработка, такая как нагревание и обработка ферментом для ферментации данным микроорганизмом. Например, вышеуказанный Zymomonas mobilis представляет собой микроорганизм, применяемый для ферментации текилы. В этом случае полисахариды, полученные из корневищ американской агавы, которая не является съедобным растением, преобразуют в ферментируемые моносахариды нагреванием, и далее моносахариды ферментируются микроорганизмом с получением спирта в качестве продукта ферментации. Следовательно, когда создают культуру ферментации с помощью обычного микроорганизма, полисахариды, такие как крахмал, не приемлемы в качестве субстрата ферментации. Например, описан факт, что Pantoea agglomerans не может разлагать крахмал (непатентный документ 4).
Авторы изобретения показали, что активный компонент для потенцирования иммунитета содержится в водном экстракте пшеничной муки (непатентный документ 5). Авторы изобретения также показали, что активные компоненты содержатся в пищевых зернах (пшеница, рис), водорослях (бурых водорослях, ламинарии, hijiki (brown alga) и красных водорослях) и бобах (соевых бобах и фасоли адзуки) (непатентный документ 6). Что касается биологической активности, было обнаружено, что эти объекты имеют профилактическое действие в отношении болезней человека и мышей (диабета, гиперлипидемии, атопического дерматита, рака) и могут быть эффективными в профилактике инфекций у рыб, ракообразных и цыплят (патентный документ 1, непатентный документ 1). Однако для возможности ожидания вышеуказанного эффекта действия водного экстракта пшеничной муки необходимо принимать внутрь пшеничную муку в большом количестве.
При этом Pantoea agglomerans является бактерией, которая живет симбиотически взаимодействуя с пшеницей, и, как полагают, является применимой в культивировании пшеницы, так как бактерия обеспечивает пшеницу фосфором и азотом (непатентный документ 7). Также Pantoea agglomerans откладывается не только на пшенице, но и на эпидермисе груш и яблок. В Европе было показано, что болезни гниения, вызванные грибами, могут быть предотвращены в момент оседания этой бактерии, и преимущественным было развитие использования этой бактерии в качестве экологически безвредного нетоксичного фунгицида (непатентный документ 8). Было определено, что симбиоз является «явлением, при котором чужеродные организмы живут вместе. В этом случае традиционно подразумевается сохранение поведенчески или физиологически близкого взаимодействия. Следовательно, под эту концепцию не попадает проживание только в одной и той же среде обитания. Симбиоз классифицируется и делится на различные категории в зависимости от смысла жизнедеятельности и важности симбиотического партнера, устойчивости взаимодействия и пространственного расположения симбиотического партнера. В основном, симбиоз в широком смысле делится на три типа, мутуализм, комменсализм и паразитизм на основе присутствия или отсутствия пользы/вреда симбиотического партнера» (непатентный документ 9). Известно, что Pantoea agglomerans отделена от пшеницы в каких-либо регионах и каких-либо типах (непатентный документ 5) и также отделена от фруктов (непатентные документы 10, 11). Было показано, что Pantoea agglomerans защищает растения от грибков или других бактерий за счет продукции антибиотиков (непатентные документы 12, 13) и осуществляет фиксацию фосфора и азота (непатентный документ 7). Следовательно, полагают, что Pantoea agglomerans всегда присутствует в растениях и играет роль, приносящую пользу растениям. Таким образом, характер ее жизнедеятельности определяется как «симбиоз», но не «паразитизм». Кроме того, авторы показали, что активный компонент для потенцирования иммунитета содержится в Pantoea agglomerans. Также авторы обнаружили, что низкомолекулярный липополисахарид, полученный из этой бактерии, имеет профилактическое действие в отношении заболеваний человека и мышей (диабета, гиперлипидемии, атопического дерматита, рака) и эффективен для профилактики инфекции у рыб, ракообразных и цыплят (патентный документ 3, непатентный документ 2).
В таком случае авторы прониклись идеей создания способа получения экстракта ферментированного растения, с использованием Pantoea agglomerans в качестве способа получения безопасного и недорогого иммуностимулятора. То есть авторы изобретения сфокусировались на (1) недорогом культивировании Pantoea agglomerans, используя среду, содержащую основные белковые компоненты, включенные в раствор для культивирования, полученный из растений, так же как и компонент, ферментирующий растение, и (2) получении материалов обогащенных Pantoea agglomerans, содержащимся в растении или продукте ферментации, таким образом, получая лекарственные препараты, препараты для животных, квазилекарства, косметику, функциональные продукты питания, продукты питания, кормовые продукты и моющие средства для млекопитающих, включая людей (особенно домашних животных, домашних питомцев и т.п.), птиц (особенно выращиваемых цыплят, домашних птиц и т.п.), амфибий, рептилий, рыб (особенно выращиваемых рыб, домашних рыбок и т.п.) и беспозвоночных. Однако это не означает, что микроорганизм, живущий в симбиотическом взаимодействии с растением, может напрямую использовать растительные компоненты, например материал из съедобного растения в качестве субстрата для ферментации. Например, пшеничная мука является сложным органическим веществом, состоящим из крахмала и ему подобных веществ, присутствующих в зернах пшеницы, но выделенная Pantoea agglomerans, которая является симбиотическим микроорганизмом внешней оболочки пшеницы, не имеет с ней прямого контакта. Таким образом, с помощью симбиотического взаимодействия пшеницы и микроорганизма нельзя показать, может ли Pantoea agglomerans ферментировать пшеницу и быть культивируемым с использованием пшеницы или нет. Действительно, неизвестны и совсем не опубликованы данные о способности Pantoea agglomerans ассимилировать пшеничную муку. Напротив, на основании общеизвестных фактов было описано, что Pantoea agglomerans не может использовать пшеничный крахмал в качестве субстрата для ферментации.
Глюциды, содержащиеся в растениях, часто сохраняются в виде крахмала, и это примечательно для съедобных растений, в частности пищевых зерен. Обычно микроорганизмы не имеют функции, в которой крахмал ассимилируется в высокой степени. В связи с этим стало известно, что часть факультативных грамотрицательных бактерий может ферментировать крахмал. Например, известно, что Erwinia способна ассимилировать крахмал. Однако в этой ферментации, когда ферментируется крахмал, подразумевается использование амилазной активности микроорганизма путем добавления микроорганизма, культивированного в большом количестве, в другую оптимальную среду, и никогда не предполагалось, что культура сама по себе создается с использованием крахмала и в связи с этим осуществляется ферментация. В традиционной технологии данная технология соответствует объективной ферментации только для эффективного использования амилазной активности микроорганизма и не планируется выращивать микроорганизм с использованием крахмала в качестве субстрата. При этом в примерах настоящего изобретения описывается, что ферментируемый продукт производится в дополнение к выращиванию микроорганизма, используя крахмал в качестве единственного источника углерода, и настоящее изобретение значительно отличается от традиционной технологии тем, что в настоящем примере имеет место не только ферментация, но также ферментация и культивирование.
С другой стороны, если определенный микроорганизм сохраняет свою функцию разложения крахмала, это напрямую не означает, что микроорганизм может расти, используя в качестве субстрата крахмал. По окончании культивирования, в случае достижения также роста микроба, количество добавляемого микроорганизма крайне мало. В этом случае, даже если микроорганизм имеет слабо выраженную амилазную активность, эта активность слишком слаба для достаточного разложения субстрата и рост микроорганизма не достигается. Действительно, было установлено, что многие микроорганизмы не могут расти, используя крахмал в качестве единственного источника углерода.
Однако если ферментация и культивирование могут быть осуществлены с использованием Pantoea agglomerans в среде, содержащей пшеничную муку в качестве основного компонента для образования экстракта ферментированного растения (здесь и далее экстракт ферментированного растения, получаемый ферментацией и культивированием Pantoea agglomerans в среде, содержащей пшеничную муку в качестве основного компонента, соответствует экстракту ферментированной пшеницы), содержащего в большом количестве недорогой иммуностимулятор, то в качестве конкретных примеров должны быть обеспечены лекарственные препараты, препараты для животных, квазилекарства, косметика, продукты питания, функциональные продукты питания, кормовые продукты и моющие средства, которые не загрязняют окружающую среду, безопасны и эффективны для профилактики инфекции у людей и в области животноводства и водных культур. Настоящее изобретение было выполнено за счет использования факта открытия того, что Pantoea agglomerans рос с использованием пшеничной муки в качестве субстрата в представленном выше контексте и за счет интенсивного проведения многих экспериментов.
Термин экстракт ферментированного растения, вводимый настоящим изобретением, является дженериковым, который включает сам культуральный раствор, полученный осуществлением ферментации и культивирования, жидкий компонент, полученный разделением твердого вещества/жидкости этого культурального раствора, и жидкий компонент, полученный воздействием процесса экстракции на твердый компонент, полученный разделением твердого вещества/жидкости, и так далее. Таким образом, экстракт ферментированного растения включает сам культуральный раствор, полученный способом ферментации и культивирования в соответствии с настоящим изобретением, и все экстракты, которые могут быть получены с использованием всего или части культурального раствора. Хотя, конечно, само собой разумеется, что данный экстракт ферментированного растения может быть обработан высушиванием, как в случае порошка экстракта ферментированного растения, или растворением экстракта ферментированного растения с получением оптимальной концентрации в подходящем растворе, например растворе фосфатного буфера, включая нормальный солевой раствор.
[патентный документ 1] японская нерассмотренная патентная заявка № Н3-218466
[патентный документ 2] японская нерассмотренная патентная заявка № Н8-198902
[патентный документ 3] WO 00/57719
[патентный документ 4] японская нерассмотренная патентная заявка № Н6-78756
[патентный документ 5] японская нерассмотренная патентная заявка № Н4-187640
[патентный документ 6] японская нерассмотренная патентная заявка № Н4-49240
[патентный документ 7] японская нерассмотренная патентная заявка № Н4-99481
[патентный документ 8] японская нерассмотренная патентная заявка № Н5-155778
[непатентный документ 1] Inagawa, H. et al., Biotherapy 5(4), p617-621, 1991
[непатентный документ 2] Soma, G. et al., «Tumor necrosis Factor: Molecular and Cellular Biology and Clinical Relevance» p203-220, 1993
[непатентный документ 3] Yamada, T. et al., «Seibutsugaku Jiten» 3rd ed., p1021, 1983
[непатентный документ 4] Gavini, F. et al., Int. J. Syst. Bacteriol., 39), p337-345, 1989
[непатентный документ 5] Nishizawa, T. et al., Chem. Pharm. Bull., 40(2), p479-483, 1992
[непатентный документ 6] Inagawa, H. et al., Chem. Pharm. Bull., 40(4), p994-997, 1992
[непатентный документ 7] Neilson A. H., J. Appl. Bacteriol., 46(3), p483-491, 1979
[непатентный документ 8] Nunes, C. et al., Int. J. Food Microbiol., 70(1-2), p53-61, 2001
[непатентный документ 9] Yamada, T. et al., «Seibutsugaku Jiten» 3rd ed., p287-288, 1983
[непатентный документ 10] Nunes, C. et al., J. Appl. Microbiol., 92(2), p247-255, 2002
[непатентный документ 11] Asis C. A. Jr. et al., Lett. Appl. Microbiol., 38(1), p19-23, 2004
[непатентный документ 12] Vanneste J. L. et al., J. Bacteriol., 174(9), p2785-2796, 1992
[непатентный документ 13] Kearnes L. P. et al., Appl. Environ. Microbiol., 64(5), p1837-1844, 1998
Описание изобретения
Проблема, решаемая данным изобретением
Как уже было описано, иммуностимуляторы часто содержатся в самих растениях и часто являются компонентами или продуктами микроорганизмов, которые живут в симбиотическом взаимодействии с растениями. Следовательно, для получения иммуностимулятора из натурального продукта, безопасного при приеме, следует экстрагировать данный компонент непосредственно из съедобных растений (например, limulus-положительный гликолипид, патентный документ 1) или эффективно культивировать микроорганизм, который живет в симбиотическом взаимодействии со съедобным растением, для получения его компонента или продукта (например, низкомолекулярные липополисахариды. Патентный документ 2). Однако содержание иммуностимулятора в съедобном растении крайне мало, очень большое количество пищи должно быть усвоено для того, чтобы можно было ожидать иммуностимулирующий эффект при потреблении пищи, и, в основном, не легко сохранить потребленное количество иммуностимулятора в соответствующем виде. Таким образом, не следует ожидать его воздействия. Более того, экстракция иммуностимулятора из растения и использование его в качестве пищи или лекарства связано с большими затратами и имеет невысокую практическую значимость.
При этом при фокусировании на микроорганизмах, которые живут в симбиотическом взаимодействии с растением, Pantoea agglomerans, который является симбиотической бактерией пшеницы, содержит в качестве компонента низкомолекулярный липополисахарид, эффективный для иммуностимуляции. Однако до настоящего времени для экстракции низкомолекулярного липополисахарида было необходимо культивировать Pantoea agglomerans, используя дорогую среду, в которой основной белок, содержащийся в среде, имеет животное происхождение, например NZ амин, триптон или казамино кислоты. Следовательно, было затруднительно недорого обеспечить высокодоступный иммуностимулятор. Одновременно, не может быть отклонена вероятность неизвестных вредных веществ, например, тех, что содержатся в животных, зараженных губчатой энцефалопатией крупного рогатого скота (BSE).
В свете вышеуказанных проблем целью настоящего изобретения является обеспечение способа ферментации и культивирования, в котором иммуностимулятор может быть получен недорого и эффективно, используя безопасные материалы, экстракт ферментированного растения, полученного данным способом, порошок экстракта ферментированного растения, полученный из экстракта ферментированного растения, и композиция экстракта ферментированного растения, содержащая порошок экстракта ферментированного растения.
Средства решения данной проблемы
Способ ферментации и культивирования настоящего изобретения, включающий в себя ферментацию материала, полученного из съедобного растения и содержащего глюциды, основным компонентом которых является полисахарид, с факультативной анаэробной грамотрицательной бактерией, которая живет в симбиотическом взаимодействии именно с растением, и одновременное культивирование факультативной анаэробной грамотрицательной бактерии.
Ферментация и культивирование могут быть осуществлены простым способом ферментации крахмала как источника углерода с факультативной анаэробной грамотрицательной бактерией.
Желательно, чтобы факультативная анаэробная грамотрицательная бактерия представляла собой факультативную анаэробную бациллу.
Желательно, чтобы факультативная анаэробная бацилла принадлежала семейству Enterobacteraceae.
Желательно, чтобы факультативная анаэробная бацилла принадлежала роду Pantoea, Serratia или Enterobacter.
Используя факультативную анаэробную бациллу Pantoea agglomerans, возможно сделать крахмал источником углерода.
Также желательно, чтобы съедобное растение было выбрано из хлебных зерен, морских водорослей, бобов и их смеси.
Также желательно, чтобы съедобное растение представляло собой пищевое зерно и материал из пищевого зерна, выбранный из пшеничной муки, рисового порошка, порошка пшеничных отрубей, рисовых отрубей и осадка от саке. В частности, так как пшеничная мука содержит глютен в качестве источника белков, существует возможность ферментировать и культивировать даже без использования материала животного происхождения.
Желательно, чтобы съедобным растением была морская водоросль и материал, получаемый из морской водоросли, выбранный из порошка бурой водоросли, порошка «mekabu» (спорофилл Undaria pinnatifida) и порошка ламинарии.
Когда съедобным растением являются бобы и материалом, получаемым из бобов, являются отходы брожения бобов, данный материал содержит большое количество белка. Таким образом, существует возможность эффективно ферментировать и культивировать даже без использования материала животного происхождения.
Экстракт ферментированного растения данного изобретения получают способом ферментации и культивирования.
Порошок экстракта ферментированного растения данного изобретения получают из экстракта ферментированного растения.
Композиция экстракта ферментированного растения данного изобретения содержит экстракт ферментированного растения или порошок экстракта ферментированного растения.
Композиции экстракта ферментированного растения могут быть выбраны из лекарственных препаратов, препаратов для животных, квазилекарств, косметики, продуктов питания, функциональных продуктов питания, кормовых продуктов и моющих средств.
Желательно, чтобы экстракт ферментированного растения имел следующие физико-химические свойства.
Экстракт ферментированного растения проявляет способность к активации макрофагов даже в присутствии полимиксина В. Экстракт ферментированного растения имеет иммуностимулирующий эффект.
Желательно, чтобы факультативная анаэробная грамотрицательная бактерия представляла собой бациллу, принадлежащую роду Pantoea, и съедобное растение было выбрано из хлебных зерен, морских водорослей, бобов и их смеси.
Желательно, чтобы факультативная анаэробная грамотрицательная бактерия представляла собой Pantoea agglomerans, и съедобное растение было выбрано из хлебных зерен, морских водорослей, бобов и их смеси.
Желательно, чтобы материал, полученный из хлебного зерна, выбирали из пшеничной муки, рисового порошка, порошка пшеничных отрубей, рисовых отрубей и осадка от саке.
Желательно, чтобы материал, полученный из морской водоросли, выбирали из порошка бурой водоросли, порошка mekabu и порошка ламинарии.
Эффект изобретения
В соответствии с настоящим изобретением ввиду того, что культивирование осуществляют в среде, не содержащей компонентов животного происхождения, не существует загрязнения примесями животного происхождения. Следовательно, не существует возможности загрязнения неизвестными вредными веществами, например, полученными из BSE-носителей, и существует возможность создания в высшей степени безопасного и недорогого способа получения экстракта ферментированного растения, способного удовлетворить потребности различных назначений и безопасно и недорого обеспечить экстракт ферментированного растения или порошок экстракта ферментированного растения, содержащий иммуностимулятор. Более того, возможно обеспечить культуральный раствор, иммуностимулятор, экстракт и порошок экстракта и дополнительные лекарственные препараты, препараты для животных, квазилекарства, косметику, продукты питания, функциональные продукты питания, кормовые продукты и моющие средства, содержащие экстракт или порошок экстракта.
Никогда не предполагалось и отсутствуют факты исследований традиционной технологии ферментации, касающиеся того, что ферментация и культивирование могут быть осуществлены простым способом, так что именно материал, полученный из съедобного растения, ферментируется факультативной анаэробной грамотрицательной бактерией, которая живет в симбиотическом взаимодействии с растением и одновременно культивируется факультативная анаэробная грамотрицательная бактерия.
Это может быть использовано, если TNF продуцируется макрофагами или нет (индукционная активность TNF) в качестве индикатора того, что конкретное вещество проявляет иммуностимулирующий эффект. Более того, иммуностимулирующий эффект может быть количественно оценен с помощью измерения количества производимого TNF. Таким образом, продукция TNF макрофагами была оценена с использованием limulus-положительного растительного гликолипида, полученного из Pantoea agglomerans. Продукция TNF макрофагами была остановлена обработкой полимиксином В и в случае limulus-положительного растительного гликолипида, полученного из пшеничной муки, и в случае низкомолекулярного липополисахарида, полученного из Pantoea agglomerans. Однако во многих примерах было показано, что даже когда экстракт ферментированного растения обрабатывали полимиксином В, TNF продуцировался макрофагами. Это показывает, что экстракт ферментированного растения, полученный ферментацией и культивированием, имеет иммуностимулирующий эффект, качественно отличный от иммуностимулирующих эффектов компонентов самого растения, которое являлось материалом, и самого микроорганизма, использованного для ферментации.
Краткое описание чертежа
Чертеж - рисунок, демонстрирующий ингибирующий эффект на присутствие koi герпеса за счет кормового продукта, содержащего экстракт ферментированной пшеницы.
Наилучший режим применения изобретения
Соответствующие воплощения настоящего изобретения будут описаны в деталях ниже.
I. Существенным признаком получения экстракта ферментированного растения является использование Pantoea agglomerans.
В настоящем изобретении авторами было обнаружено впервые, что Pantoea agglomerans может расти, непосредственно используя в качестве источника углерода крахмал, и, используя Pantoea agglomerans, был создан способ для недорогого получения экстракта ферментированной пшеницы, обильно содержащего в качестве продукта ферментации и продукта культивирования иммуностимулятор. Этот способ может обеспечить экологически безвредные и безопасные квазилекарства, косметику, продукты питания, функциональные продукты питания и кормовые продукты, эффективные для профилактики инфекций у людей, и в животноводстве, и в водной культуре.
1. Выделение Pantoea agglomerans
Когда пшеничную муку суспендируют в воде и супернатант наносят на L-бульонную агаровую среду и культивируют, появляются колонии микроорганизмов. В этих колониях микроорганизмы идентифицируются стандартными методами. Например, те, что имеют свойства, одинаковые со стандартной Pantoea agglomerans, выбирают отбором колоний, которые окрашиваются как грамотрицательные, положительны в реакции анаэробного метаболизма глюкозы и отрицательны в отношении оксидазной активности и при использовании ID-теста (Nissui Pharmaceutical Co., Ltd). Стандартная Pantoea agglomerans доступна из Института физических и химических исследований, Биоресурсного центра (непатентный документ 4). В следующем описании процентное соотношение является значением по массе, если не определено иначе.
2. Оценка иммуностимулирующей активности
В настоящих воплощениях в качества индикатора иммуностимулирующего эффекта, который проявляет экстракт ферментированной пшеницы, оценивалась способность активации макрофагов путем оценки продукции макрофагами TNF.
3. Низкомолекулярный липополисахарид, полученный из Pantoea agglomerans
Что касается одного из активных компонентов, иммуностимулируемых ферментацией и культивированием с использованием Pantoea agglomerans, ожидалось, что он содержит низкомолекулярный липополисахарид, полученный из Pantoea agglomerans. Низкомолекулярные липополисахариды имеют особо выраженную безопасность и исключительную биологическую активность по сравнению с обычно используемыми высокомолекулярными липополисахаридами (обычными липополисахаридами). Таким образом, измерялось содержание низкомолекулярного липополисахарида. Низкомолекулярные липополисахариды подробно описаны в патентном документе 2. Настоящие примеры касаются экстракта ферментированной пшеницы, но настоящее изобретение не подразумевает, что используемое растение ограничено пшеницей и что используемый иммуностимулятор ограничен низкомолекулярными липополисахаридами.
Pantoea agglomerans может быть культивирована и с использованием общеизвестного способа (патентный документ 2, непатентный документ 8), но основные компоненты белков, содержащихся в культуральной среде, имеют животное происхождение, и стоимость среды высока. Более того, когда животному дают функциональные продукты питания и функциональные кормовые продукты или вводят подкожно, заражение примесями животного происхождения, именно имеющими отношение к BSE, является проблемой безопасности продуктов питания, и дополнительно, производство становится дорогим и способ не имеет практической значимости. Таким образом, в качестве результата расширенного исследования для получения безвредного и недорогого натурального продукта, имеющего иммуностимулирующее действие, авторы настоящего изобретения создали способ ферментации и культивирования с использованием Pantoea agglomerans для получения экстракта ферментированной пшеницы, как это показано в примерах. Основным компонентом белка, содержащегося в культуральной среде, обычно был белок животного происхождения, а в настоящем изобретении - белок растительного происхождения. Обычно продукт, полученный разложением белка, такого как казеин, полученный из коровьего молока с помощью расщепляющего фермента, добавляли в культуральный раствор. В этом случае себестоимость литра среды составляла 250 йен, а при использовании пшеничной муки себестоимость составляет, примерно, 16 йен. Никогда не осуществлялась ферментация с целью значительного концентрирования и синергистического слияния иммуностимулирующей активности растения и микроорганизма в их симбиотическом взаимодействии.
Содержание данного изобретения будет описано ниже в виде примеров, но настоящее изобретение не ограничено применением Pantoea agglomerans, в качестве микроорганизма, пшеницы, в качестве съедобного растения, или муки, в качестве материала, описанных в настоящих примерах. Настоящее изобретение может быть также применено к материалу, полученному обычным способом из других съедобных растений, обильно содержащих иммуностимулятор, например бурых водорослей, хлебных зерен (материалом, полученным из хлебных зерен, является пшеничная мука, рисовый порошок, порошок пшеничных отрубей, рисовые отруби или осадок от саке), морских водорослей (материалом, полученным из морских водорослей, является порошок морских водорослей, порошок mekabu или порошок ламинарии) и бобов (материалом, полученным из бобов, являются отходы брожения бобов). Хорошо известно, что в этих растениях содержатся белки и сахара. Эти растения могут быть использованы для ферментации и культивирования с применением Pantoea agglomerans. Общеизвестно то, что природные бактерии, например, бактерии, относящиеся к роду Serratia или Enterobacter, живут в симбиотическом взаимодействии с этими растениями (непатентный документ 4). Само собой разумеется, что микроорганизмы, используемые для данной ферментации, включают факультативные анаэробные грамотрицательные бактерии, которые живут в симбиотическом взаимодействии с этими растениями.
II. Краткое изложение основных моментов настоящего изобретения
(1) Экстракт ферментированной пшеницы, сам по себе, как субстанция, имеющая иммуностимулирующее действие, создается путем соединения пшеницы, Pantoea agglomerans, которая является симбиотической бактерией, и продуктов ферментации, их комбинирование является новым, но настоящее изобретение этим не ограничивается.
(2) Новым является получение экстракта ферментированного растения с применением Pantoea agglomerans, которая является грамотрицательной бактерией, но настоящее изобретение этим не ограничивается.
III. Конкретный способ получения экстракта ферментированной пшеницы
(1) Pantoea agglomerans выделяют из пшеничной муки стандартным способом (непатентный документ 1). Будучи однажды выделенной и идентифицированной, эта бактерия может храниться в 50% глицерине.
(2) Готовят 0,05-5% раствор соли, 0,005-1 молярный фосфатный буфер, или смешанный солевой раствор (0,5-10% раствор фосфата натрия, 0,05-5% раствор дигидрофосфата калия, 0,05-5% раствор хлорида натрия, 0,05-5% раствор хлорида аммония).
(3) Пшеничную муку суспендируют в воде в концентрации 0,05-10%.
(4) Готовят 0,2-3 молярный раствор хлорида магния.
(5) Готовят 0,2-3 молярный раствор хлорида кальция.
(6) Растворы с (2) по (5), в некоторых случаях, стерилизуют автоклавированием и т.п.
(7) Растворы со (2) по (5) смешивают в соответствующих количествах и добавляют воду для создания суспензии, содержащей 0,1-5% пшеничной муки. В некоторых случаях pH нейтрализуют добавлением раствора щелочи или кислоты.
(8) В некоторых случаях пшеничный крахмал может быть частично расщеплен добавлением от 10 до 50000 единиц амилазы на литр среды в (7) и инкубированием при температуре от 10 до 80°С в течение от 1 до 24 часов.
(9) Pantoea agglomerans, выделенную в (1), добавляют в (7) или (8).
(10) (9) ферментируют при температуре от 1 до 40°С. В некоторых случаях ферментационная емкость может просто стоять или быть встряхиваемой. Альтернативно, перемешивание может быть осуществлено каждые несколько часов.
(11) (10) ферментируется в течение от 6 часов до одной недели. По мере прохождения ферментации раствор пшеничной муки приобретает желтый цвет.
(12) Необязательно может быть добавлен раствор щелочи для нейтрализации pH во время ферментации (11) или могут быть добавлены суспензия пшеничной муки или неорганические соли.
(13) Ферментация заканчивается, и твердый компонент собирают в виде осадка центрифугированием (1000-5000 об/мин, 10-60 минут). Осадок может быть непосредственно использован в качестве продукта ферментации пшеничной муки для кормовых продуктов или в качестве сырья для смешивания с кормовым материалом.
(14) В случае получения экстракта ферментированной пшеницы (13) суспендируют в воде или солевом буфере, который затем нагревают при температуре от 80 до 140°С в течение от 10 минут до 6 часов. Твердый компонент может быть удален центрифугированием или фильтрованием. Вода или буфер могут быть добавлены снова к удаленному осадку для повторной экстракции с нагреванием в течение нескольких раз.
(15) Экстракт ферментированной пшеницы, полученный в (14), может быть далее просто очищен, в зависимости от предполагаемых нужд. Таким образом, осадок образуется, когда соль, такую как хлорид натрия, в конечной концентрации 0,05-1 моль/л добавляют к экстракту (14), и далее добавляют растворитель, такой как этанол, от одного до трехкратного количества по отношению к количеству экстракта. Осадок может быть собран центрифугированием. Осадок может быть далее промыт растворителем, таким как этанол. При высушивании осадка может быть получен порошок.
А. ПРИМЕРЫ, ОТНОСЯЩИЕСЯ К СПОСОБУ ПОЛУЧЕНИЯ ЭКСТРАКТА ФЕРМЕНТИРОВАННОЙ ПШЕНИЦЫ
Пример 1
Исследование роста Pantoea agglomerans в среде, содержащей пшеничную муку
Для того чтобы подтвердить, является ли Pantoea agglomerans природной симбиотической бактерией для пшеницы, способной расти, используя пшеничную муку в качестве источника углерода, оценивался рост Pantoea agglomerans в среде, содержащей пшеничную муку.
(1) Готовили М9 агаровую среду, содержащую 0,5% пшеничной муки в качестве источника углерода.
(2) Одну колонию Pantoea agglomerans брали с поверхности агаровой среды LB и суспендировали в 1 мл фосфатного буфера. Далее разбавляли в 10-10000 раз, и 0,1 мл каждой аликвоты высевали на М9 агаровую среду (1).
(3) После культивирования при 37°С в течение 6 дней наблюдалось наличие колоний. Как результат, наблюдали примерно 300 колоний в чашке Петри, в которую высевали 0,1 мл 10000-кратного разбавления.
Это подтверждает, что Pantoea agglomerans может использовать пшеничную муку в качестве источника углерода.
Пример 2
Получение экстракта ферментированной пшеницы
(1) Дистиллированную воду (5 мл) добавляли к 0,5 г пшеничной муки для суспендирования, 0,1 мл супернатанта добавляли к L-бульонной агаровой среде и культивировали при 37°С в течение ночи.
(2) Желтые колонии выделяли, бактерию идентифицировали стандартными способами, выделяли Pantoea agglomerans, суспендировали в 50% растворе глицерина и хранили в морозильной камере. Часть исходного вещества наносили на LB-агаровую среду, оставляли при 37°С для получения независимой колонии Pantoea agglomerans.
(3) В 2-литровую колбу добавляли 64 г гидрофосфата натрия гептагидрата, 15 г дигидрофосфата калия, 2,5 г хлорида натрия, и 5 г хлорида аммония, и очищенную воду для получения общего объема, равного 1 литр (смешанный раствор неорганических солей). Очищенную воду добавляли к 13,1 г дигидрата хлорида магния для получения общего объема, равного 100 мл (раствор хлорида магния). Очищенную воду добавляли к 11,1 г хлорида кальция для получения общего объема, равного 100 мл (раствор хлорида кальция). Очищенную воду (4 л) добавляли в 5-литровую коническую колбу (очищенная вода). Указанные выше растворы и очищенную воду стерилизовали автоклавированием (TOMY BS-325, 120°С в течение 20 минут).
(4) Пшеничную муку (24 г) (Nisshin Flour Milling Co., Ltd.) добавляли в 1-литровую коническую колбу и добавляли очищенную воду для получения общего объема, равного 600 мл. После такого же автоклавирования добавляли 3 мг α-амилазы (SIGMA, Bacillus, ферментная активность 1500-3000 единиц на мг белка), и нагревали на водяной бане при 65°С в течение 12 часов (раствор пшеничной муки, обработанный амилазой).
(5) Полученные растворы и подобные им в количествах, представленных в таблице 1, помещали в 3-литровую стерилизованную колбу Sakaguchi для получения среды, содержащей пшеничную муку.
(6) Приготовление инокулята: Одну колонию Pantoea agglomerans, выделенную из пшеничной муки в (2), добавляли к 10 мл среды, содержащей пшеничную муку (5), предварительно приготовленную с тем же составом, и ферментировали с помощью слабого перемешивания при 37°С в течение ночи (12-15 часов) для получения инокулята для ферментации пшеничной муки.
(7) Все количество (6) добавили к (5) и ферментировали при 37°С 20-30 часов с перемешиванием. Измеряли pH ферментируемого раствора и доводили до рН 7 добавлением водного раствора аммиака. В стерильных условиях 150 мл раствора пшеничной муки обрабатывали амилазой и в него добавляли 37,5 мл смешанного раствора неорганических солей и сходным образом ферментировали 20-30 часов. Следующее действие было повторено для достижения общего времени ферментации 65-80 часов.
(8) Раствор ферментированной пшеничной муки центрифугировали (Hitachi, высокоскоростная центрифуга с охлаждением, SCR-20B, 5000 об/мин, 20 минут, 4°С) и осадок собирали.
(9) К осадку (8) добавляли фосфатный буфер, который затем суспендировали для получения общего объема 100 мл, каждую аликвоту по 33 мл переносили в 50-миллилитровую центрифужную пробирку, и проводили экстракцию с нагреванием на кипящей водяной бане в течение 30 минут. После окончания нагревания раствор охлаждали до комнатной температуры и центрифугировали (Hitachi, высокоскоростная центрифуга с охлаждением, SCR-20B, 10000 об/мин, 20 минут, 20°С). После центрифугирования декантацией в другую пробирку собирали 82 мл супернатанта бледно-желтого цвета.
(10) Раствор хлорида натрия (8,9 мл, 5 моль) добавляли к 80 мл супернатанта в (9). Когда в раствор было добавлено 178 мл этанола, появилась белая взвесь. Раствор оставили в морозильной камере (-90°С) в течение ночи и затем раствор центрифугировали (Hitachi, высокоскоростная центрифуга с охлаждением, SCR-20B, 10000 об/мин, 20 минут, 4°С). Осадок получали удалением супернатанта. После добавления к осадку 10 мл 70% этанола и последующего суспендирования раствор центрифугировали (Hitachi, высокоскоростная центрифуга с охлаждением, SCR-20B, 10000 об/мин, 20 минут, 20°С) и осадок промывали. Осадок высушивали на воздухе и растворяли в дистиллированной воде с получением 11 мл экстракта ферментированной пшеницы.
(11) Измерение сухой массы: 0,3 мл переносили в предварительно взвешенную 1,5 мл пластиковую пробирку, и после замораживания с помощью лиофилизатора была проведена лиофилизация, и масса составила 7,45 мг. Следовательно, масса сухого экстракта ферментированной пшеницы в (10) составил 24,8 мг на 1 мл раствора и 273 мг на общее количество 11 мл.
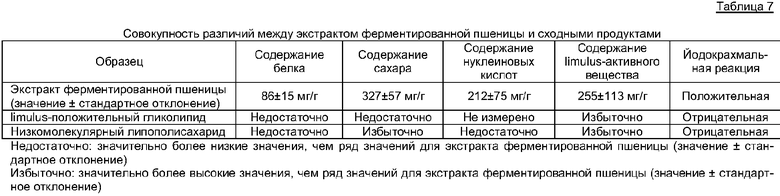
(12) Экстракт ферментированной пшеницы был произведен 8 раз независимо этим же способом, и количество белка в каждом образце было измерено методом Бредфорда, используя в качестве стандартного белка бычий сывороточный альбумин (БСА). В качестве объектов сравнения использовались limulus-положительный гликолипид (патентный документ 1) и низкомолекулярный липополисахарид (патентный документ 2). Результаты измерений представлены в таблице 2. В таблицах 2-5 и 7 числовое значение для экстракта ферментированной пшеницы представлено как содержание мг на 1 г массы, полученной высушиванием экстракта ферментированной пшеницы, полученного в вышеуказанном (10).
(13) Измерение содержания сахара: содержание сахара оценивали с помощью фенолсульфатного метода, используя глюкозу в качестве стандартного сахара. Результаты измерения показаны в таблице 3.
(14) Измерение содержания нуклеиновых кислот: оценивалось поглощение образца разбавленного в 100 раз при длине волны 210-340 нм. Максимальное содержание подсчитывали, используя значение, полученное вычитанием поглощения при 320 нм из поглощения при 260 нм и 50 мкг на единицу оптической плотности поглощения ДНК. Результаты измерения показаны в таблице 4.
(15) Измерение содержания limulus-активного вещества с помощью limulus-анализа: для измерения использовалась Toxi-color system Seikagaku Corporation и Seikagaku Corporation Et-1 в качестве стандартного limulus-активного вещества. Результаты измерения показаны в таблице 5.
(16) Йодокрахмальная реакция: 1 н. йодный реагент (10 мл воды добавляли к 12,7 г йода и 25 г йодида калия, тщательно перемешивали, и затем добавляли воду до 100 мл) разбавляли в 200 раз водой при использовании. Этот раствор (5 мкл) добавляли к 0,1 мл экстракта ферментированной пшеницы, предварительно растворенного с получением концентрации 1 мг/мл, и тщательно перемешивали. В растворе экстракта ферментированной пшеницы немедленно развилась окраска от светло-пурпурного до темно-пурпурного (положительная реакция). В limulus-положительном гликолипиде и низкомолекулярном липополисахариде эта же процедура не индуцировала развитие окраски (отрицательная реакция). Вышеуказанные результаты сведены в таблице 6.
Как очевидно из вышеуказанных результатов, экстракт ферментированной пшеницы отличается от limulus-положительного гликолипида и низкомолекулярного липополисахарида по содержанию белка, сахаров, нуклеиновых кислот (кроме limulus-положительного гликолипида, так как для него нет данных), по содержанию limulus-положительного вещества и йодокрахмальной реакции, и ясно, что настоящее вещество является новым. Вышеуказанные результаты просто суммированы в таблице 7. Таким образом, экстракт ферментированной пшеницы в настоящих примерах является новым и отличным от limulus-положительного гликолипида и низкомолекулярного липополисахарида в том, что проявляет следующие физико-химические свойства. Экстракт ферментированной пшеницы демонстрирует содержание белка 5-15%, содержание сахара 20-45%, содержание нуклеиновых кислот 10-35% и содержание limulus-положительного вещества 10-40% и положителен в йодокрахмальной реакции и проявляет способность активации макрофагов даже в присутствии полимиксина В.
Пример 3
Иммуностимулирующее действие экстракта ферментированной пшеницы
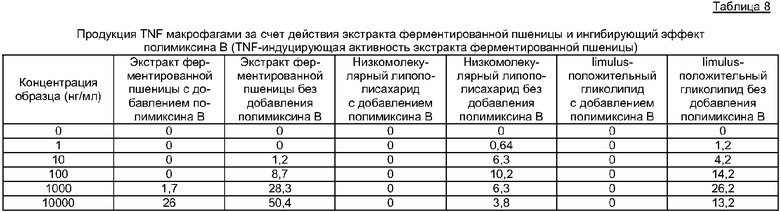
Клеточную линию острой миелогенной лейкемии, ТНР-1 (1×106/250 мкл, среду RPMI1640, содержащую 10% эмбриональной телячьей сыворотки), использованную в качестве человеческих макрофагов, помещали в 48-луночный планшет и предварительно культивировали в течение 30 минут. Далее 250 мкл среды (конечный объем 500 мкл) добавляли таким образом, что конечная концентрация каждого образца составила 1-10000 нг/мл. К образцам добавляли полимиксин В (12,5 мкг/мл). После культивирования в течение 4 часов собирали культуральные супернатанты и клетки. Активность TNF в супернатанте измерялась тестом цитотоксичности, используя L-929. Результаты показаны в таблице 8. Макрофаги продуцировали TNF даже в присутствии полимиксина В за счет действия экстракта ферментированной пшеницы, но низкомолекулярный липополисахарид и limulus-положительный гликолипид в присутствии полимиксина В не могли повлиять на синтез TNF макрофагами. Исходя из этого, очевидно, что экстракт ферментированной пшеницы имеет биологическую активность, отличную от тех, что имеют низкомолекулярный липополисахарид и limulus-положительный гликолипид.
В. ПРИМЕР ИСПОЛЬЗОВАНИЯ ЭКСТРАКТА ФЕРМЕНТИРОВАННОЙ ПШЕНИЦЫ В КОРМОВЫХ ПРОДУКТАХ
Пример 4
Кормовой продукт для выращиваемых цыплят, содержащий экстракт ферментированной пшеницы (эффект ингибирования смертности в области разведения бройлеров в масштабном исследовании)
Производили кормовой продукт, содержащий 430 мкг/кг экстракта ферментированной пшеницы, полученного в примере 2. Коммерческие бройлерные цыплята использовались в количестве 5500-6000 цыплят в группе. В контрольной тест-группе давали кормовой продукт, не содержащий экстракт ферментированной пшеницы. Кормовой продукт, содержащий экстракт ферментированной пшеницы, давали цыплятам в возрасте 3-х недель после вылупления и вводили каждый день до достижения возраста 7 недель. Количество мертвых цыплят подсчитывали каждый день. Цыплята, которые не соответствовали стандарту при перевозке, выбраковывались. Результаты показаны в таблице 9. Показатель удаления в тест-группе составил 1,9% (кормовой продукт, содержащий экстракт ферментированной пшеницы), который был низок, и 3,3% - в контрольной группе. Уровень выживаемости в тест-группе составил 98,1% и 96,7% - в контрольной группе. Таким образом, наблюдалось увеличение уровня выживаемости, равное 1,4%. Был осуществлен тест значительного различия количества реально перевозимых цыплят и числа удаленных цыплят между тест-группой и контрольной группой, и наблюдалось значимое отличие р<0,0001 в Х2 тесте. На основе указанного выше был показан эффект защиты от инфекции за счет кормового продукта, содержащего экстракт ферментированной пшеницы, в выращивании бройлеров.
Пример 5
Кормовой продукт для выращиваемых рыб, содержащий экстракт ферментированной пшеницы (эффект предотвращения инфицирования у желтохвоста, тест на открытом воздухе)
Для оценки эффекта предотвращения инфицирования тестом на открытом воздухе примерно 5200 желтохвостов на группу кормили кормовым продуктом, содержащим экстракт ферментированной пшеницы, полученный в примере 2. Результаты показаны в таблице 10. Уровень смертности из-за Streptococcus в контрольной группе составил 4,8%. В группе, в которой принимали 100 мкг/кг/день (на массу тела 1 кг и на один день) (тест-группа), смертность, как наблюдалось, значительно снизилась (р<0,00001) по сравнению с группой, не принимавшей указанного кормового продукта (контрольной группой).
Пример 6
Кормовой продукт для выращиваемых рыб, содержащий экстракт ферментированной пшеницы (эффект предотвращения инфицирования koi герпес)
(1) Карп: исследовался черный карп с массой тела 70 г. Тест проводили в группе, содержащей 20 карпов.
(2) Получение вируса koi герпеса: добавляли 10 мл сбалансированного буферного солевого раствора Хэнка к 1 г бронхов карпа, умершего от инфицирования koi герпесом, и гомогенизировали, фильтровали через фильтр с диаметром пор 0,45 мкм, и фильтрат становился раствором вируса.
(3) Инфицирование вирусом koi герпеса: указанный выше фильтрат (600 мкл/100 г массы тела) вводили внутрибрюшинно.
(4) Приготовление кормового продукта, содержащего экстракт ферментированной пшеницы: экстракты ферментированной пшеницы, полученные в примере 2, смешивали с коммерчески доступным кормовым продуктом в концентрации 0, 5, 10 и 20 мг/кг.
(5) Способ кормления: каждый кормовой продукт в количестве 1% от массы тела давали один раз в день. Это соответствует 0, 50, 100 или 200 мкг/кг массы тела/в день в терминах количества экстракта ферментированной пшеницы.
(6) Эксперимент: Кормовой продукт, содержащий экстракт ферментированной пшеницы, давали в течение недели, затем карпа инфицировали вирусом, и далее кормовой продукт, содержащий экстракт ферментированной пшеницы, давали в течение 10 дней. Наблюдали уровень выживаемости карпа в течение 10 дней после инфицирования вирусом. Результат представлен на чертеже.
Все карпы к концу шестого дня умирали в группе, в которой не давали экстракт ферментированной пшеницы. При этом было показано, что в группах, в которых давали экстракт ферментированной пшеницы, уровень выживаемости был значительно выше на 10 день после инфицирования (метод Каплана-Мейера, логарифмический ранговый критерий, процент риска составил 0,01% или менее). В частности, уровень выживаемости, равный 65%, был показан в группе, в которой давали 100 мкг/кг массы тела/день экстракта ферментированной пшеницы.
С. ПРИМЕНЕНИЕ ПРИМЕРОВ ЭКСТРАКТА ФЕРМЕНТИРОВАННОЙ ПШЕНИЦЫ В КОСМЕТИКЕ И В ПОЛУЧЕНИИ МОЮЩИХ СРЕДСТВ
Пример 7
Получение крема для рук, содержащего экстракт ферментированной пшеницы
Для получения мази примерно 10% экстракт ферментированной пшеницы, полученный в примере 2, смешивали с мазью жирорастворимого субстрата 1 в композиции, описанной в таблице 11.
Пример 8
Получение увлажняющего крема, содержащего экстракт ферментированной пшеницы
1. Приготовление увлажняющего крема, содержащего экстракт ферментированной пшеницы
Компоненты представлены в таблице 12. Комбинацию А нагревали и растворяли при 70°С, комбинацию В перемешивали в очищенной воде в количестве 1/4 и нагревали/растворяли при 70°С, и комбинацию С перемешивали в очищенной воде в количестве 1/4 и нагревали/растворяли при 70°С, и добавляли в комбинацию А. Смесь тщательно перемешивали гомогенизатором и затем охлаждали до 40°С. Затем добавляли комбинацию D и рН доводили до 6,8. Далее добавляли оставшуюся очищенную воду и экстракт ферментированной пшеницы, полученный в примере 2 в соответствующем количестве, и тщательно перемешивали для получения молочка. Экстракт ферментированной пшеницы предварительно растворяли в очищенной воде до концентрации 5 мг/мл и 0,1 мл добавляли к 100 г молочка.
2. Эффект увлажняющего крема, содержащего экстракт ферментированной пшеницы
Этот крем был использован 43 мужчинами и женщинами, и был проведен анкетный опрос. В результате, касательно увлажняющего эффекта, 18 человек ответили, что имел место определенный увлажняющий эффект, 18 человек ответили, что имел место легкий увлажняющий эффект, 2 человека ответили, что не было увлажняющего эффекта, и 5 человек не ответили (критерий знака одного образца: р<0,0001). Касательно эффекта улучшения при действии на шершавую кожу 6 человек ответили, что крем был определенно эффективен, 13 человек ответили, что крем был слегка эффективен, никто не ответил, что крем был неэффективен, и 24 человека не ответили (критерий знака одного образца: р<0,0001). Касательно ухудшения состояния кожи после применения крема никто из людей не отметил ухудшения. Этот крем использовался 4-мя людьми с умеренными атопическими симптомами, и был проведен анкетный опрос. Касательно улучшения состояния атопического дерматита 3 человека ответили, что крем был определенно эффективен, и один человек ответил, что крем был слегка эффективен (критерий знака одного образца: р<0,125). Кроме того, один человек ответил, что рубцы от угрей быстро проходили. Этот крем был использован 9 мужчинами после бритья, и был проведен анкетный опрос. Восемь мужчин ответили, что крем был эффективен в уменьшении боли после бритья, профилактике сухости и быстром заживлении порезов (критерий знака одного образца: р<0,01). Кроме того, этот крем использовался 2 людьми с возрастными симптомами «застывших плеч» путем нанесения на плечо для уменьшения боли. Один человек сказал, что крем был эффективен.
Кроме того, этот крем использовался пациентами с ожогами. У пациентов, имеющих в равной степени ожоговые травмы на коже обеих рук, на одну руку наносили крем, содержащий экстракт ферментированной пшеницы, а на другую руку - крем, не содержащий экстракт ферментированной пшеницы. Рука обработанная кремом, содержащим экстракт ферментированной пшеницы, очевидно заживала быстрее. Этот крем использовался у 10 пациентов с ожоговыми травмами, включая описанный случай. Следовательно, во всех местах, обработанных кремом, содержащим экстракт ферментированной пшеницы, раны заживали быстрее, чем в местах, обработанных кремом, не содержащим экстракт ферментированной пшеницы (точная сходимость по вероятности Фишера: р<0,0001). Из указанного выше было показано, что экстракт ферментированной пшеницы проявлял терапевтический эффект в отношении ожоговых травм.
Пример 9
Получение лосьона для кожи, содержащего экстракт ферментированной пшеницы
1. Приготовление лосьона для кожи, содержащего экстракт ферментированной пшеницы
Использованные компоненты показаны в таблице 13. Экстракт ферментированной пшеницы, полученный в примере 2, был предварительно растворен с получением концентрации 5 мг/мл в очищенной воде, и 0,1 мл добавляли к 100 г лосьона для кожи.
2. Эффекты лосьона для кожи, содержащего экстракт ферментированной пшеницы
Этот лосьон для кожи использовали 5 женщин, и был проведен анкетный опрос. В результате, 3 женщины ответили, что они почувствовали хорошее увлажняющее действие и 2 женщины ответили, что почувствовали обычное увлажняющее действие. Никто из женщин не имел проблем с кожей.
Пример 10
Получение моющего средства, содержащего экстракт ферментированной пшеницы
Моющее средство, содержащее экстракт ферментированной пшеницы, было получено для улучшения функций организма. Основные компоненты моющего средства показаны в таблице 14.
Моющее средство, содержащее экстракт ферментированной пшеницы, готовили добавлением 110 мкг экстракта ферментированной пшеницы, полученного в примере 2, к вышеуказанным компонентам. Моющее средство, содержащее экстракт ферментированной пшеницы, и моющее средство, не содержащее экстракт ферментированной пшеницы, произвольно давали 102 субъектам, которые затем использовали их в ванне (160-200 литров) до принятия ванны, и был проведен анкетный опрос [(1) степень нагрева организма, (2) ощущение холода после ванны, (3) эффект снятия усталости, (4) легкость засыпания, (5) степень снятия ощущения «застывших плеч», (6) эффект мышечной боли, (7) эффект нервной боли, (8) эффект боли в пояснице, (9) эффект чувствительности к низким температурам, (10) эффект улучшения дерматомикоза ступни, (11) эффект улучшения состояния сухой кожи, (12) эффект в отношении атопического дерматита]. В результате, наблюдалось 7% или более улучшение по сравнению с контролем в (1) степени нагрева тела (10%), (2) сложность ощущения холода после ванны (7,9%), (6) эффект в отношении мышечной боли (13%), (8) эффект боли в пояснице (16%), (9) эффект чувствительности к низким температурам (10%) и (11) эффект улучшения состояния сухой кожи (7,3%) (тест Mantel-Haenszel: р<0,04). Из вышеуказанных результатов наблюдались эффекты в отношении болей и улучшения нагрева тела при применении экстракта ферментированной пшеницы в качестве моющего средства.
D. ПРИМЕНЕНИЕ ПРИМЕРА ЭКСТРАКТА ФЕРМЕНТИРОВАННОЙ ПШЕНИЦЫ К КОРМОВЫМ ПРОДУКТАМ
Пример 11
Получение конфет, содержащих экстракт ферментированной пшеницы
(1) В качестве исходных материалов смешивали гранулированный сахар, крахмальную патоку, смесь воды и экстракта ферментированной пшеницы, полученного в примере 2, в соотношении 5:5:5:1 и готовили нагреванием от 120 до 160°С.
(2) Конфеты получали охлаждением смеси, полученной в (1), в стальной емкости для охлаждения, вытягиванием для получения формы палочки и формованием зерен массой, примерно, 1 г.
Данные конфеты в соответствующем количестве помещали в 20 мл воды и растворяли нагреванием. Количество липополисахарида, активного компонента экстракта ферментированной пшеницы, измеряли в данном растворе, и, следовательно, содержание составило 4,6 мкг/г. Эти конфеты употребляли 6 мужчин и женщин, которые простудились и имели боль в горле. После этого был проведен анкетный опрос касательно боли в горле. Касательно боли в горле все 6 человек чувствовали уменьшение боли в горле (критерий знака одного образца: р<0,03).
Пример 12
Получение функционального продукта, разрушающего алкоголь, содержащего экстракт ферментированной пшеницы
Экстракт ферментированной пшеницы, полученный в примере 2, смешивали с коммерчески доступным продуктом, функциональным продуктом, разрушающим алкоголь, и оценивали, наблюдалось ли новое действие, выражаемое в облегчении фарингодинии, или нет.
Коммерчески доступный продукт: торговая марка «Nonde oiki»
Компоненты представлены в таблице 15.
Настоящий «Nonde oiki» содержит экстракт аmachazuru (Gynostemma pentaphylla) и экстракт зеленого чая, но только в количестве, примерно, 0,002 мкг на порцию липополисахарида, который является одним из активных компонентов экстракта растения. Следовательно, ожидается, что продукт приобретет новое действие за счет добавления соответствующего количества экстракта ферментированной пшеницы, который обильно содержит липополисахарид. Желательно комбинировать от 1 до 30 мкг на 2 г порции липополисахарида, который является одним из активных компонентов экстракта ферментированной пшеницы (от 5 до 150 мкг в случае экстракта ферментированной пшеницы). Таким образом, сначала был произведен продукт, в котором совмещается 50 мкг экстракта ферментированной пшеницы в одной порции. В процессе производства Nonde oiki добавляли 2,5 мг экстракта ферментированной пшеницы на 100 г продукта. В результате получали новый продукт, который содержал 50 мкг экстракта ферментированной пшеницы на 2 г продукта.
Анализируя 20 взрослых мужчин и женщин, которые жаловались на фарингодинию после выпивки и пения под караоке, 10-ти человекам давали традиционный «Nonde oiki» и «Nonde oiki», содержащий экстракт ферментированной пшеницы соответственно и оценивали усиление действия разрушения алкоголя, которое является общеизвестным, и эффект облегчения фарингодинии. Сразу после этого был проведен анкетный опрос относительно эффекта смягчения фарингодинии. В результате, наблюдалось уменьшение фарингодинии у 8 из 10 человек, которые принимали «Nonde oiki», содержащий экстракт ферментированной пшеницы, против 2 человек, которые принимали традиционный «Nonde oiki». Таким образом, наблюдалось статистически значимое различие (точная сходимость по вероятности Фишера: р<0,0001) по сравнению с контролем.
Е. ПРИМЕР, КАСАЮЩИЙСЯ МЕДИЦИНСКОЙ ПОЛЬЗЫ ЭКСТРАКТА ФЕРМЕНТИРОВАННОЙ ПШЕНИЦЫ
Пример 13
Получение раствора глицерина, содержащего экстракт ферментированной пшеницы (терапевтический эффект в отношении атопического дерматита)
50%-ный раствор глицерина, содержащий 50 мкг/мл экстракта ферментированной пшеницы, полученного в примере 2, давали 2 или 3 раза в день с дозировкой от 2 до 3 мл на одно введение 9 пациентам женского и мужского пола с устойчивым атопическим дерматитом (возраст от 25 до 34), где наблюдались сыпь на лице, ладонях, ногах, по всему телу, шее, руках и спине и субъективные симптомы были от умеренных до сильно выраженных. Субъективные симптомы (зуд) классифицировались на слабые, умеренные и выраженные на основе жалоб пациентов. После срока от двух недель до двух месяцев после начала применения пациентов посещали снова и эффекты оценивались. В результате, случаи полного ответа (значительного улучшения сыпи и практически полного исчезновения субъективных симптомов) составило 4 (44%), случаи частичного ответа (легкого улучшения сыпи и уменьшения субъективных симптомов) составило 4 (44%), случаи отсутствия ответа были равны одному (11%) и случаев ухудшения не было (критерий знака одного образца: р<0,03). Из указанного выше результата уровень эффективности был определен как равный 89%.
Пример 14
Обезболивающий эффект экстракта ферментированной пшеницы
Экстракт ферментированной пшеницы, полученный в примере 2, растворяли в дистиллированной воде и по 0,2 мл вводили мышам перорально с использованием зонда. После 90 минут мышам внутрибрюшинно вводили 0,7% уксусную кислоту. После наблюдения за мышами в течение 5 минут подсчитывали число выгибаний, вызванных в течение 30 минут. Результаты приведены в таблице 16 в виде количества каждого образца, необходимого для ингибирования 30% числа выгибаний, при использовании в качестве контроля дистиллированной воды. Когда эффективное действие низкомолекулярного липополисахарида из Escherichia coli было равно 1, эффективное действие экстракта ферментированной пшеницы было равно 7, демонстрируя, что экстракт ферментированной пшеницы имел прекрасный обезболивающий эффект.
Пример 15
Ингибирующий эффект экстракта ферментированной пшеницы в отношении атопического дерматита
Для оценки влияния экстракта ферментированной пшеницы в отношении атопического дерматита была введена модель аллергии 1-го типа. Внутривенно вводили антидинитрофенил-моноклональные антитела (1 мкг/мышь) самцам мышей линии BALB/c (3-4 мыши в группе). После одного часа внутрикожно вводили экстракт ферментированной пшеницы, полученный в примере 2 (абдоминальная область) (4 мкг/мышь), или перорально (100 мкг/мышь). После дополнительного часа 20 мкл раствора ацетона и оливкового масла, смешанных в соотношении (4:1), содержащего 0,25% динитрофторбензола, наносили в качестве аллергена на поверхность и обратную сторону ушной раковины мыши. Толщина ушной раковины оценивалась с использованием калибромера спустя 1, 2, 24 и 48 часов после нанесения. Значение (∆), полученное вычитанием толщины непосредственно перед нанесением, являлось степенью отека. Эффект введения лекарства оценивали с помощью уровня ингибирования, полученного с помощью следующей формулы в ингибировании ранней стадии реакции, наблюдаемой один час спустя после введения аллергена, и отсроченной реакции, индуцируемой после 24 часов. Уровень ингибирования = (1-∆ отека ушной раковины после введения лекарства/∆ отека ушной раковины в контроле×100). Результаты представлены в таблице 17. Как это следует из таблицы, экстракт ферментированной пшеницы ингибировал аллергическую реакцию и при внутрикожном, и при пероральном введении.
Пример 16
Эффект предотвращения инфицирования экстракта ферментированной пшеницы
Для оценки эффекта предотвращения инфицирования экстракта ферментированной пшеницы вводилась инфекционная модель метициллин-устойчивого Staphylococcus aureus (MRSA). Внутрибрюшинно вводили циклофосфамид (CY, 200 мг/кг) самцам мышей линии BALB/c (в возрасте 6-8 недель) (10 на группу), и после 5 дней вводили внутрикожно экстракт ферментированной пшеницы, полученный в примере 2. После 3 часов внутривенно вводили MRSA (3×107 колониеобразующих единиц (КОЕ)) и оценивалось количество дней выживания. Результаты представлены в таблице 18. Как видно из таблицы, экстракт ферментированной пшеницы проявлял эффект предотвращения инфицирования со статистически значимым отличием (тест Х2: р<0,001) по сравнению с контрольной группой, получавшей солевой раствор.
Пример 17
Терапевтический эффект экстракта ферментированной пшеницы в отношении метастизирующего рака
Для оценки терапевтического эффекта экстракта ферментированной пшеницы в отношении метастазирующего рака вводилась модель метастаз в легких клеток линии Meth A. Внутривенно вводили раковые клетки Meth A (1×105 клеток) самцам мышей линии BALB/c (в возрасте 6-8 недель) (10 на группу) и после 12 дней вводили внутрикожно в течение 4 дней подряд экстракт ферментированной пшеницы, полученный в примере 2. Двадцать дней спустя после пересадки клеток проводили аутопсию, легкое извлекали и фиксировали формалином. Легкое наблюдали невооруженным глазом и подсчитывали количество узлов. Результаты представлены в таблице 19. Как видно из таблицы, экстракт ферментированной пшеницы проявлял терапевтический эффект в отношении метастазирующего рака легких Meth A со статистически значимым отличием (t-тест: р<0,001) по сравнению с контрольной группой, получавшей солевой раствор.
F. ПРИМЕРЫ, КАСАЮЩИЕСЯ ЭКСТРАКТА ОТХОДОВ БРОЖЕНИЯ БОБОВ
Пример 18
Получение экстракта отходов брожения бобов
(1) 1,0 л воды, 0,2 г дигидрофосфата калия, 1,15 г гидрофосфата натрия, 8 г обычной соли и 0,2 г хлорида калия добавляли в 2-литровую коническую колбу.
(2) Высушенные отходы брожения бобов (20 г) добавляли к (1).
(3) (2) стерилизовали автоклавированием.
(4) Приготовление инокулята: одну колонию Pantoea agglomerans, выделенную из пшеничной муки, добавляли к 5 мл 2%-ной среды отходов брожения бобов, предварительно приготовленной с таким же составом, и ферментировали при 37°С в течение ночи (15 часов) с аккуратным перемешиванием для приготовления инокулята для ферментации отходов брожения бобов.
(5) Общее количество (4) добавляли к (3) и ферментировали при 37°С в течение 48 часов аккуратным перемешиванием.
(6) Раствор экстракта отходов брожения бобов (5) экстрагировали нагреванием при 120°С в течение 20 минут в автоклаве. Центрифугировали (Kubota 8800, 2000 об/мин, 10 минут) и супернатант собирали для получения экстракта отходов брожения бобов.
(7) Определение сухого веса: 0,3 мл переносили в 1,5 мл пластиковую пробирку, предварительно взвешенную, и после замораживания лиофилизацию осуществляли с помощью лиофилизатора, и далее вес составил 5,97 мг. Следовательно, сухой вес экстракта отходов брожения бобов (6) составил 19,9 мг на 1 мл раствора и 19,9 г на общее количество 1000 мл.
(8) Количество белка определяли в образце, разбавленном в 10 раз с помощью метода Бредфорда с использованием БСА в качестве стандартного белка. Результаты представлены в таблице 15.
(9) Определение содержания нуклеиновых кислот: определялось поглощение при длине волны 210-340 нм образца, разбавленного в 100 раз. Максимальное содержание определяли, используя значение, полученное вычитанием поглощения при 320 нм из поглощения при 260 нм и 50 мкг на единицу оптической плотности поглощения ДНК.
(10) Определение содержание сахара: содержание сахара определяли фенол-сульфатным методом, используя в качестве стандартного сахара глюкозу.
(11) Определение limulus-активного вещества limulus-анализом: для определения использовалась система Тoxi-color, обеспечиваемая Seikagaku Corporation, и Seikagaku Corporation Et-1 использовалась в качестве стандартного limulus-активного вещества. Результаты представлены в таблице 20.
Пример 19
Иммуностимулирующий эффект экстракта отходов брожения бобов
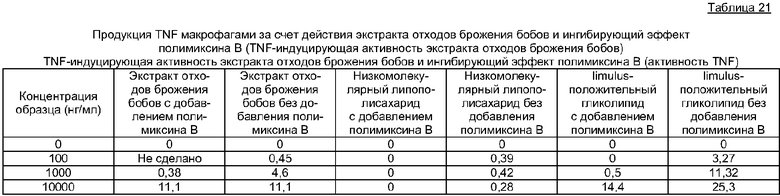
Клеточную линию острой миелогенной лейкемии ТНР-1 (1×106/250 мкл среды RPMI1640, содержащей 10% эмбриональной телячьей сыворотки), использованную в качестве человеческих макрофагов, помещали в 48-луночный планшет и предварительно культивировали в течение 30 минут. Далее 250 мкл среды (конечный объем 500 мкл) добавляли таким образом, что конечная концентрация каждого образца составила 100-10000 нг/мл. Образцы снабжали группой, содержащей полимиксин В (12,5 мкг/мл) (не группой, содержащей полимиксин В только при 100 нг/мл). После культивирования в течение 4 часов собирали супернатанты культур и клетки. Активность TNF в супернатанте измеряли с помощью теста цитотоксичности, используя L-929. Результаты представлены в таблице 21. Макрофаги продуцировали TNF даже в присутствии полимиксина В под влиянием экстракта отходов брожения бобов, но в присутствии полимиксина В, макрофаги не могли продуцировать TNF под влиянием низкомолекулярного липополисахарида. Из этого очевидно, что экстракт отходов брожения бобов имеет биологическую активность, отличную от той, что имеется у низкомолекулярного липополисахарида.
G. ПРИМЕРЫ, КАСАЮЩИЕСЯ ЭКСТРАКТА ФЕРМЕНТИРОВАННОГО РИСОВОГО ПОРОШКА
Пример 20
Получение экстракта ферментированного рисового порошка
(1) 1,0 л воды, 0,2 г дигидрофосфата калия, 1,15 г гидрофосфата натрия, 8 г обычной соли и 0,2 г хлорида калия добавляли в 2-литровую коническую колбу.
(2) Высушенный рисовый порошок (20 г) добавляли к (1).
(3) (2) стерилизовали автоклавированием.
(4) Приготовление инокулята: одну колонию Pantoea agglomerans, выделенную из пшеничной муки, добавляли к 5 мл 2%-ной среды рисового порошка, предварительно приготовленной с таким же составом, и ферментировали при 37°С в течение ночи (15 часов) с аккуратным перемешиванием для приготовления инокулята для ферментации рисового порошка.
(5) Общее количество (4) добавляли к (3) и ферментировали при 37°С в течение 72 часов аккуратным перемешиванием.
(6) Раствор ферментированного рисового порошка (5) экстрагировали нагреванием при 120°С в течение 20 минут в автоклаве. Центрифугировали (Kubota 8800, 2000 об/мин, 10 минут) и супернатант собирали для получения экстракта ферментированного рисового порошка.
(7) Определение содержания limulus-активного вещества limulus-анализом: для определения использовалась система Тoxi-color, обеспечиваемая Seikagaku Corporation, и Seikagaku Corporation Et-1 использовалась в качестве стандартного limulus-активного вещества. Содержание limulus-активного вещества в экстракте ферментированного рисового порошка составило 1,7 мкг/мл.
Пример 21
Иммуностимулирующий эффект экстракта ферментированного рисового порошка
Клеточную линию острой миелогенной лейкемии ТНР-1 (1×106/250 мкл среды RPMI1640, содержащей 10% эмбриональной телячьей сыворотки), использованную в качестве человеческих макрофагов, помещали в 48-луночный планшет и предварительно культивировали в течение 30 минут. Далее 250 мкл среды (конечный объем 500 мкл) добавляли таким образом, что конечная концентрация каждого образца составила 100-10000 нг/мл. Образцы снабжали группой, содержащей полимиксин В (12,5 мкг/мл). После культивирования в течение 4 часов собирали супернатанты культур и клетки. Активность TNF в супернатантах измеряли с помощью теста цитотоксичности, используя L-929. Результаты представлены в таблице 22. Макрофаги продуцировали TNF даже в присутствии полимиксина В под влиянием экстракта ферментированного рисового порошка, но в присутствии полимиксина В макрофаги не могли продуцировать TNF под влиянием низкомолекулярного липополисахарида. Из этого очевидно, что экстракт ферментированного рисового порошка имеет биологическую активность, отличную от тех, что имеются у низкомолекулярного липополисахарида и limulus-положительного гликолипида.
(нг/мл)
с добавлением полимиксина В
без добавления полимиксина В
Н. ПРИМЕРЫ, КАСАЮЩИЕСЯ ЭКСТРАКТА ФЕРМЕНТИРОВАННЫХ БУРЫХ ВОДОРОСЛЕЙ
Пример 22
Получение экстракта ферментированных бурых водорослей mekabu
(1) 1,0 л воды, 0,2 г дигидрофосфата калия, 1,15 г гидрофосфата натрия, 8 г обычной соли и 0,2 г хлорида калия добавляли в 2-литровую коническую колбу.
(2) Высушенные бурые водоросли mekabu (20 г) добавляли к (1).
(3) (2) стерилизовали автоклавированием.
(4) Приготовление инокулята: одну колонию Pantoea agglomerans, выделенную из пшеничной муки, добавляли к 5 мл 2%-ной среды бурых водорослей mekabu, предварительно приготовленной с таким же составом, и ферментировали при 37°С в течение ночи (15 часов) с аккуратным перемешиванием для приготовления инокулята для ферментации бурых водорослей mekabu.
(5) Общее количество (4) добавляли к (3) и ферментировали при 37°С в течение 72 часов аккуратным перемешиванием.
(6) Раствор ферментированных бурых водорослей mekabu (5) экстрагировали нагреванием при 120°С в течение 20 минут в автоклаве. Центрифугировали (Kubota 8800, 2000 об/мин, 10 минут) и супернатанты собирали для получения экстракта ферментированных бурых водорослей mekabu.
(7) Определение содержания limulus-активного вещества limulus-анализом: для определения использовалась система Тoxi-color, обеспечиваемая Seikagaku Corporation, и Seikagaku Corporation Et-1 использовалась в качестве стандартного limulus-активного вещества. Содержание limulus-активного вещества в экстракте ферментированных бурых водорослей mekabu составило 132 мкг/мл.
Пример 23
Иммуностимулирующее действие экстракта ферментированных бурых водорослей mekabu
Клеточную линию острой миелогенной лейкемии ТНР-1 (1×106/250 мкл среды RPMI1640, содержащей 10% эмбриональной телячьей сыворотки), использованную в качестве человеческих макрофагов, помещали в 48-луночный планшет и предварительно культивировали в течение 30 минут. Далее 250 мкл среды (конечный объем 500 мкл) добавляли таким образом, что конечная концентрация каждого образца составила 1-10000 нг/мл. Образцы снабжали группой, содержащей полимиксин В (12,5 мкг/мл). После культивирования в течение 4 часов собирали супернатанты культур и клетки. Активность TNF в супернатантах измеряли с помощью теста цитотоксичности, используя L-929. Результаты представлены в таблице 23. Макрофаги продуцировали TNF даже в присутствии полимиксина В под влиянием экстракта ферментированных бурых водорослей mekabu, но в присутствии полимиксина В макрофаги не могли продуцировать TNF под влиянием низкомолекулярного липополисахарида. Из этого очевидно, что экстракт ферментированных бурых водорослей mekabu имеет биологическую активность, отличную от той, что имеется у низкомолекулярного липополисахарида и limulus-положительного гликолипида.
Промышленная применимость
В соответствии с настоящим изобретением становится возможным недорого производить экстракт ферментированного растения, который является безопасным иммуностимулятором. Экстракт ферментированного растения, полученный таким образом, может быть использован в лекарственных препаратах, лекарственных препаратах для животных, квазилекарствах, косметике, продуктах питания, функциональных продуктах питания, кормовых продуктах и моющих средствах для млекопитающих, включая людей (особенно домашних животных, домашних питомцев и т.п.), птиц (особенно выращиваемых цыплят, домашних птиц и т.п.), амфибий, рептилий, рыб (особенно выращиваемых рыб, домашних рыбок и т.п.) и беспозвоночных.
Способ предусматривает приготовление питательной среды, содержащей растительный материал, ферментацию растительного материала с анаэробной грамотрицательной бактерией и одновременное культивирование бактерии на среде с получением экстракта ферментированного растительного материала. При этом экстракцию осуществляют водой или солевым буфером. Также проводят необязательное высушивание экстракта с получением порошка экстракта. В качестве растительного материала используют съедобный растительный материал, содержащий углеводы, преимущественно полисахарид. При этом грамотрицательная бактерия существует в симбиозе только с указанным растительным материалом. Также предложено применение экстракта и порошка ферментированного растительного материала для получения лекарственных препаратов, лекарственных препаратов для животных, квазилекарств, косметики, продуктов питания, в том числе функциональных, кормов и моющих средств. Изобретение обеспечивает получение продуктов с иммуностимулирующим действием. 5 н. и 12 з.п. ф-лы, 1 ил., 23 табл.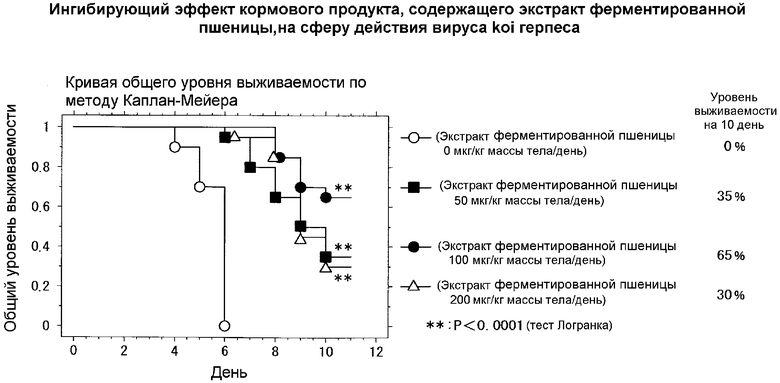
1. Способ ферментации растительного материала и культивирования бактерий для получения экстракта ферментированного растительного материала, включающий приготовление питательной среды, содержащей растительный материал, ферментацию растительного материала с факультативной анаэробной грамотрицательной бактерией и одновременное культивирование бактерии на среде с последующим получением экстракта с помощью воды или солевого буфера и, необязательно, высушиванием полученного экстракта, причем растительный материал получают из съедобного растительного материала, содержащего углеводы, основным компонентом которых является полисахарид, а указанная бактерия существует в симбиозе только со съедобным растительным материалом.
2. Способ по п.1, где указанный материал является всецело съедобным.
3. Способ по п.1, где в качестве источника углерода используют крахмал.
4. Способ по п.1, где указанной факультативной анаэробной грамотрицательной бактерией является бацилла.
5. Способ по п.4, где указанная факультативная анаэробная бацилла принадлежит семейству Enterobacteriaceae.
6. Способ по п.4, где указанная факультативная анаэробная бацилла принадлежит роду Pantoea, Serratia или Enterobacter.
7. Способ по п.4, где указанная факультативная анаэробная бацилла является Pantoea agglomerans.
8. Способ по любому из пп.1-7, где указанный съедобный растительный материал выбран из зернового продукта, морских водорослей или бобов.
9. Способ по п.8, где указанный съедобный растительный материал является зерновым продуктом и указанный материал, полученный из зернового продукта, выбирают из пшеничной муки, рисового порошка, порошка пшеничных отрубей, рисовых отрубей и осадка от саке.
10. Способ по п.8, где указанный съедобный растительный материал является морскими водорослями и указанный материал, получаемый из морской водоросли, выбирают из порошка бурой водоросли, порошка "mekabu" и порошка ламинарии.
11. Способ по п.8, где указанным съедобным растительным материалом являются бобы и материалом, получаемым из бобов, являются отходы брожения бобов.
12. Экстракт ферментированного растительного материала, полученный способом по п.1.
13. Экстракт ферментированного растительного материала по п.12 проявляет физико-химические свойства, которые заключаются в способности к активации макрофагов даже в присутствии полимиксина В.
14. Экстракт ферментированного растительного материала по п.12 или 13, который имеет иммуностимулирующую активность.
15. Порошок экстракта ферментированного растительного материала, полученный из экстракта ферментированного растительного материала по п.12.
16. Применение экстракта ферментированного растительного материала по п.12 для получения лекарственных препаратов, лекарственных препаратов для животных, квазилекарств, косметики, продуктов питания, функциональных продуктов питания, кормовых продуктов и моющих средств.
17. Применение порошка экстракта ферментированного растительного материала по п.15 для получения лекарственных препаратов, лекарственных препаратов для животных, квазилекарств, косметики, продуктов питания, функциональных продуктов питания, кормовых продуктов и моющих средств.
| Приспособление для точного наложения листов бумаги при снятии оттисков | 1922 |
|
SU6A1 |
| ПРИСПОСОБЛЕНИЕ ДЛЯ АВТОМАТИЧЕСКОГО СОБИРАНИЯ НА ПРОВОЛОЧНЫЕ РАМКИ СКОБОК, ВЫХОДЯЩИХ ИЗ АВТОМАТИЧЕСКОГО ШТАМПОВОЧНОГО СТАНКА | 1938 |
|
SU57719A1 |
Авторы
Даты
2009-10-20—Публикация
2004-09-22—Подача