Изобретение относится к новым циклопентильным производным следующей общей формулы I:

где Х означает метилен, кислород, серу или NR7-группу;
R1 означает линейную или разветвленную С1-С8-алкильную, или С3-С8-алкениленовую, или С3-С8-алкиниленовую цепь, необязательно замещенную CF3, фенилом, фенокси или нафтилом, причем ароматические кольца необязательно замещены одной или более С1-С4-алкильными группами, атомами галогенов, трифторметильными, гидроксильными или С1-С4-алкоксильными группами;
R2, R3 независимо означают водород, С1-С3-алкильную цепь, галоген, трифторметил, гидроксил или С1-С4-алкоксил;
R4, R5, R6, R7 независимо означают водород или С1-С6-алкил;
и их фармацевтически приемлемым солям, которые эффективны в качестве модуляторов натриевого и/или кальциевого канала и, следовательно, пригодны для предотвращения, облегчения и лечения широкого спектра патологий, включая, но не ограничиваясь этим, неврологические, психиатрические, сердечно-сосудистые, воспалительные, глазные, урологические, метаболические и желудочно-кишечные заболевания, где вышеуказанные механизмы описываются как играющие патологическую роль.
Предпосылки создания изобретения
Химические предпосылки
В патенте ФРГ 2624290 раскрываются 2-аминоциклоалканкарбоновые кислоты и их производные общей формулы:

где R1 означает гидроксил или NR4R5-группу, R2 и R3 означают водород, алкил, аралкил, арил или ацил, R4 и R5 означают водород, С1-С8-алкил, аралкил, арил или гетероарил, и их применение в качестве аналгетических, жаропонижающих и анестезирующих средств.
Биологические предпосылки
Хорошо известно, что натриевые каналы играют важную роль в нейронной сети за счет быстрой передачи электрических импульсов через клетки и клеточные сети, координируя таким образом процессы более высокого уровня в порядке от перемещения до познания. Эти каналы представляют собой большие трансмембранные белки, которые способны к изменению между различными состояниями для облегчения селективной проницаемости ионов натрия. Для этого процесса необходим потенциал, чтобы деполяризовать мембрану, и, следовательно, эти каналы являются потенциалзависимыми. В последние несколько лет глубже стали понимать натриевые каналы и взаимодействие с ними лекарственных средств.
Установлено, что целый ряд лекарственных средств, имеющих неизвестный механизм действия, на самом деле модулирует проводимость натриевого канала, включая местные анестезирующие средства, антиаритмические средства класса I и противосудорожные средства. Блокаторы нейронного натриевого канала находят применение для лечения эпилепсии (фенитоин и карбамазепин), маниакально-депрессивного психоза (ламотригин), для предотвращения нейродегенеративного заболевания и для уменьшения невропатической боли. Различные противоэпилептические лекарственные средства, стабилизирующие нейронную возбудимость, эффективны при невропатической боли (габапентин).
Кроме того, увеличение экспрессии или активности в случае натриевого канала также наблюдают на некоторых моделях воспалительной боли, что наводит на мысль об участии натриевых каналов в формировании воспалительной боли.
Кальциевые каналы охватывают мембрану, состоящую из множества субъединиц белка, которые позволяют контролировать поступление ионов кальция из внеклеточной жидкости в клетки. Как правило, кальциевые каналы являются потенциалзависимыми и относятся к потенциалчувствительным кальциевым каналам (VSCC). VSCC обнаружены во всей нервной системе млекопитающего, где они регулируют такие разнообразные виды активности, как клеточная возбудимость, высвобождение медиатора, внутриклеточный метаболизм, нейросекреторная активность и экспрессия гена. Все «возбудимые» клетки у животных, такие как нейроны центральной нервной системы (CNS), периферические нервные клетки и клетки мышц, включая клетки скелетных мышц, сердечных мышц и венозные и артериальные гладкомышечные клетки, имеют потенциалзависимые кальциевые каналы. Кальциевые каналы играют главную роль в регуляции внутриклеточных уровней ионов кальция, которые важны для жизнеспособности и функции клеток. Внутриклеточные концентрации ионов кальция вовлекаются в целый ряд таких необходимых для жизни процессов у животных, как высвобождение нейромедиаторов, сокращение мышц, электрокардиостимуляторная активность и секреция гормонов. Полагают, что кальциевые каналы важны при некоторых болезненных состояниях. Целый ряд соединений, приемлемых для лечения различных сердечно-сосудистых заболеваний у млекопитающих, включая людей, проявляют свое полезное действие путем модулирования функций потенциалзависимых кальциевых каналов, присутствующих в сердечной и/или сосудистой гладкой мышце. Соединения с активностью против кальциевых каналов также опосредуют лечение боли. В частности, полагают, что кальциевые каналы N-типа (Cav 2.2), ответственные за регуляцию нейромедиаторов, играют существенную роль в ноцицептивной трансмиссии, что обусловлено их распределением в ткани, а также следует из результатов некоторых фармакологических исследований.
Эта гипотеза подтверждена в клинике при использовании цинокотида, пептида, получаемого из яда морской улитки, Conus Magus. Ограничение в терапевтическом применении этого пептида заключается в том, что его нужно вводить людям внутриоболочечно (Bowersox S.S. и Luther R., Toxicon, 1998, 36, 11, 1651-1658).
В совокупности эти полученные данные показывают, что соединения, блокирующие натриевый и/или кальциевый канал, имеют высокий терапевтический потенциал в отношении предотвращения, облегчения и лечения широкого спектра патологий, включая неврологические, психиатрические, сердечно-сосудистые, урологические, метаболические и желудочно-кишечные заболевания, где вышеуказанные механизмы описываются как играющие патологическую роль.
Существует множество статей и патентов, раскрывающих модуляторы или антагонисты натриевого канала и/или кальциевого канала для лечения или модулирования плеторы расстройств, как, например, их применение в качестве местных анестезирующих, противоаритмических, противорвотных средств, антиманиакальных депрессантов, агентов для лечения униполярной депрессии, сердечно-сосудистых заболеваний, энуреза, диареи, воспалительных заболеваний, эпилепсии, нейродегенеративных состояний, смерти нейронов, антиконвульсации, невропатической боли, мигрени, острой гипералгезии и воспаления, почечного заболевания, аллергии, астмы, спазма бронхов, дисменореи, спазма пищевода, глаукомы, нарушений мочевых путей, нарушений моторики пищеварительного тракта, преждевременных родов, ожирения. Далеко неполный перечень представлен ниже.
Широкий и полный обзор известного уровня техники представлен в WO 03/057219 (и данные там ссылки); дальнейший подбор известного уровня техники представлен в следующих ссылках: Alzheimer C., Adv. Exp. Med. Biol., 2002, 513, 161-181; Vanegas H., Schaible H., Pain, 2000, 85, 9-18; патент США № 5051403; патент США № 5587454; патент США № 5863952; патент США № 6011035; патент США № 6117841; патент США № 6362174; патент США № 6380198; патент США № 6420383; патент США № 6458781; патент США № 6472530; патент США № 6518288; патент США № 6521647; WO 97/10210; WO 03/018561.
Описание данного изобретения
Настоящее изобретение относится к новым соединениям формулы I:

где
Х означает метилен, кислород, серу или NR7-группу;
R1 означает линейную или разветвленную С1-С8-алкильную, или С3-С8-алкениленовую, или С3-С8-алкиниленовую цепь, необязательно замещенную CF3, фенилом, фенокси или нафтилом, причем ароматические кольца необязательно замещены одной или более С1-С4-алкильными группами, атомами галогенов, трифторметильными, гидроксильными или С1-С4-алкоксильными группами;
R2, R3 независимо означают водород, С1-С3-алкильную цепь, галоген, трифторметил, гидроксил или С1-С4-алкоксил;
R4, R5, R6, R7 независимо означают водород или С1-С6-алкил;
и их фармацевтически приемлемым солям.
Соединения согласно данному изобретению пригодны в качестве модуляторов натриевого и/или кальциевого канала.
Заместители R1-Х, R2 и R3 у фенильного кольца могут быть в любом положении. Фармацевтически приемлемые соли соединений формулы I включают аддитивные соли неорганических кислот, например соляной кислоты, бромоводородной кислоты, серной кислоты и фосфорной кислоты, или органических кислот, например уксусной кислоты, пропионовой кислоты, бензойной кислоты, коричной кислоты, миндальной кислоты, салициловой кислоты, гликолевой кислоты, молочной кислоты, щавелевой кислоты, яблочной кислоты, малеиновой кислоты, малоновой кислоты, фумаровой кислоты, винной кислоты, лимонной кислоты, и тому подобное.
Предпочтительными соединениями согласно данному изобретению являются соединения формулы I, где Х означает кислород, метилен, NH или NCH3, R1 означает
С1-С8-алкильную цепь, необязательно замещенную CF3, фенилом или феноксигруппой, где ароматическое кольцо в R1 необязательно замещено одним или двумя атомами галогена или метоксигруппой или трифторметильной группой, R2 и R3 означают водород, метил, метокси, фтор, хлор или бром, R4, R5 и R6 означают водород или метил.
Примерами конкретных соединений согласно данному изобретению являются:
амид 2-(2-бензилоксибензиламино)циклопентанкарбоновой кислоты;
амид 2-(3-бензилоксибензиламино)циклопентанкарбоновой кислоты;
амид 2-(4-бензилоксибензиламино)циклопентанкарбоновой кислоты;
амид 2-[2-(2-фторбензилокси)бензиламино]циклопентан-карбоновой кислоты;
амид 2-[3-(2-фторбензилокси)бензиламино]циклопентанкарбоновой кислоты;
амид цис-2-[3-(2-фторбензилокси)бензиламино]циклопентанкарбоновой кислоты;
амид 2-[4-(2-фторбензилокси)бензиламино]циклопентанкарбоновой кислоты;
амид 2-[4-(2-фторбензилтио)бензиламино]циклопентанкарбоновой кислоты;
амид 2-[4-(2-фторбензиламино)бензиламино]циклопентанкарбоновой кислоты;
амид 2-[2-(2-фторбензилокси)-3-фторбензиламино]циклопентанкарбоновой кислоты;
амид 2-[4-(2-фторбензилокси)-3-фторбензиламино]циклопентанкарбоновой кислоты;
амид 2-[2-(2-фторбензилокси)-3-хлорбензиламино]циклопентанкарбоновой кислоты;
амид 2-[4-(2-фторбензилокси)-3-хлорбензиламино]циклопентанкарбоновой кислоты;
амид 2-[4-(2-фторбензилокси)-3-бромбензиламино]циклопентанкарбоновой кислоты;
амид 2-[4-(2-фторбензилокси)-2-метоксибензиламино]циклопентанкарбоновой кислоты;
амид 2-[4-(2-фторбензилокси)-3-метоксибензиламино]циклопентанкарбоновой кислоты;
амид 2-[4-(2-фторбензилокси)-3,5-диметилбензиламино]циклопентанкарбоновой кислоты;
амид цис-2-[4-(2-фторбензилокси)-3,5-диметилбензиламино]циклопентанкарбоновой кислоты;
и все их стереоизомеры и/или фармацевтически приемлемые соли.
Соединения согласно данному изобретению и их соли можно получать по способу, включающему:
а) взаимодействие соединений формулы II:

где R1, R2, R3 и Х имеют значения, как определено выше,
с соединениями формулы III, в присутствии восстановителя:

где R4, R5 и R6 такие, как определено выше; таким образом получая соединение формулы I; или
b) взаимодействие соединений формулы IV:
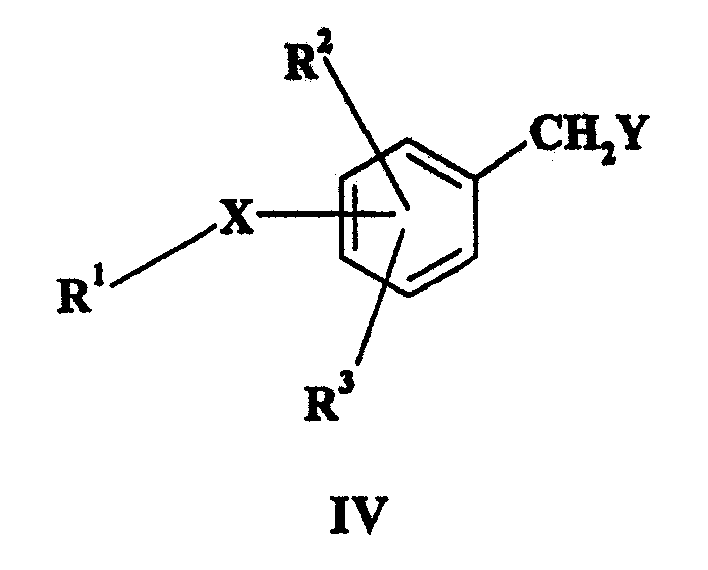
где R1, R2, R3 и Х имеют значения, как определено выше, и Y означает атом галогена или О-ЕWG-группу, где ЕWG означает электроноакцепторную группу, подобную, например, мезильной, тозильной или трифторацетильной группам, способным трансформировать кислород, с которым они связаны, в хорошую удаляемую группу,
с соединениями формулы III, таким образом получая соединение формулы I; или
с) взаимодействие соединения формулы Ia:
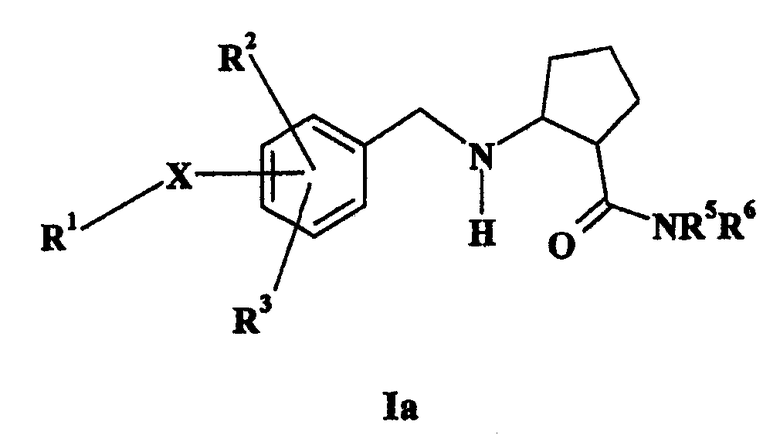
где R1, R2, R3, R5, R6 и Х такие, как определено выше, с соединениями формулы V или VI:

где Y и R4 такие, как определено выше; и R8 означает водород или С1-С5-алкил, таким образом получая соединение согласно данному изобретению, в котором R4 означает С1-С6-алкил;
и, если желательно, превращение соединения согласно данному изобретению в другое соединение и/или, если желательно, превращение соединения в фармацевтически приемлемую соль и/или, если желательно, превращение соли в свободное соединение и/или, если желательно, разделение смеси изомеров соединений согласно данному изобретению на отдельные изомеры.
Соединения II, III, IV, V и VI являются коммерчески доступными или их получают из коммерчески доступных соединений, используя хорошо известные способы.
Взаимодействия соединений формулы II с соединениями формулы III и соединений формулы Ia с соединениями формулы VI, приводящие к соединениям формулы I, представляют собой реакцию восстановительного аминирования, которую можно осуществлять в соответствии с хорошо известными методиками. По предпочтительному воплощению данного изобретения эту реакцию можно осуществлять в атмосфере азота, в таком подходящем органическом растворителе, как спирт, например низший алканол, в частности метанол, или в ацетонитриле, или в тетрагидрофуране, при температуре в диапазоне от примерно 0оС до примерно 80оС, в присутствии восстановителя, причем наиболее подходящим является боргидрид натрия или цианоборгидрид натрия. Иногда для облегчения протекания реакции к реакционной смеси можно добавлять изопропилат титана IV и молекулярные сита.
В соединении формул IV и V галогеном предпочтительно является бром или иод. Реакции алкилирования соединения формулы IV с помощью соединения формулы III и соединения формулы Ia с помощью соединения формулы V можно осуществлять в таком подходящем органическом растворителе, как спирт, например, метанол, этанол или изопропанол, в частности в этаноле, при температуре в диапазоне от примерно 0оС до примерно 50оС.
Когда в соединениях согласно настоящему изобретению и их промежуточных продуктах присутствуют группы, необходимые для защиты перед тем, как подвергать их проиллюстрированным выше реакциям, они могут быть защищены перед введением в реакцию и затем подвергнуты снятию защиты в соответствии с хорошо известными способами.
Фармакология
Соединения согласно данному изобретению обладают аффинностью к сайтам связывания кальциевого и/или натриевого каналов, как показано, используя селективные радиолиганды при исследованиях in vitro в отношении связывания.
Соединения согласно данному изобретению являются блокаторами потенциалзависимых натриевых каналов и/или кальциевых каналов. Следовательно, эти соединения вытесняют 3Н-батрахотоксин (ВТХ) с высокой аффинностью из сайта связывания в натриевом канале при IC50 в области низких микромолярных значений или субмикромолярных значений. Подобным образом соединения вытесняют 3Н-нитрендипин из сайта связывания в кальциевом канале при IC50 в области низких микромолярных или, наиболее обычно, субмикромолярных значений, а также ингибируют приток кальция, вызываемый через кальциевые каналы за счет клеточной деполяризации.
Такие вещества проявляют «зависимость при использовании», когда натриевые каналы блокированы, то есть максимальная блокировка натриевых каналов достигается только после его повторной стимуляции. Следовательно, вещества предпочтительно связываются с многократно активированными натриевыми каналами. В результате вещества способны активироваться предпочтительно в тех областях организма, которые являются патологически сверхстимулируемыми, как проиллюстрировано «пэтч-кламп» экспериментами (W.A. Catteral, Trends Pharmacol. Sci., 8, 57-65, 1987), показывающими, что соединения согласно данному изобретению блокируют электростимулированный натриевый канал «зависимым при использовании» образом.
В результате этих механизмов действия соединения согласно данному изобретению in vivo эффективны при пероральном введении от 0,1 до 100 мг/кг в широком диапазоне моделей животных и, в частности, в MES-тесте электроиндуцированных конвульсий, на формалиновой модели стойкой боли и на каррагенановой модели воспаления.
Потенциалзависимую блокировку кальциевых и/или натриевых каналов соединениями согласно настоящему изобретению обнаруживают с помощью базирующегося на флуоресценции анализа притока кальция и электрофизиологических исследований.
Активность, модулирующую кальциевый канал N-типа активность циклопентильных производных общей формулы I, измеряют посредством базирующегося на флуоресценции анализа притока кальция.
Активность, модулирующую натриевый канал циклопентильных производных общей формулы I, измеряют посредством электрофизиологических анализов, с использованием двухэлектродного способа фиксации потенциала (TEVC), овоцитов Xenopus, экспрессирующих натриевый канал Nav 1.3.
Принимая во внимание вышеописанные механизмы действия, соединения согласно настоящему изобретению приемлемы для лечения или профилактики невропатической боли. Синдромы невропатической боли включают, но не ограничиваясь этим, диабетическую невропатию, ишиас, неспецифическую боль нижней части спины, боль при рассеянном склерозе, фибромиалгию, связанную с ВИЧ невропатию, невралгию, такую как постгерпетическая невралгия и тригеминальная невралгия, и боль, возникающую вследствие физической травмы, ампутации, ракового заболевания, токсинов или хронических воспалительных состояний.
Соединения согласно данному изобретению также пригодны для лечения хронической боли. Хроническая боль включает, но не ограничиваясь этим, хроническую боль, вызываемую воспалением или связанным с воспалением состоянием, остеоартритом, ревматоидным артритом или последствиями этого заболевания, сильным повреждением или травмой, и включает боль в верхней и нижней частях спины (возникающую в результате систематического, регионального или первичного заболевания позвоночника (такого как радикулопатия)), костную боль (обусловленную остеоартритом, остеопорозом, метастазом костей или неизвестными причинами), боль в области таза, боль, связанную с повреждением спинного мозга, кардиальную боль грудной клетки, некардиальную боль грудной клетки, центральную постинсультную боль, миофасциальную боль, раковую боль, боль при СПИДе, серповидно-клеточную боль, гериатрическую боль или боль, вызываемую цефалгией, синдромом височно-нижнечелюстного сустава, подагрой, фиброзом или сдавлением плечевого сплетения и подключичной артерии прикрепляемых мышцами в области первого ребра и ключицы.
Соединения по данному изобретению также пригодны для лечения острой боли (вызываемой сильным повреждением, заболеванием, спортивно-медицинскими травмами, запястным синдромом, ожогами, скелетно-мышечными растяжениями и нагрузками, мышечно-сухожильной нагрузкой, болевыми шейно-плечевыми синдромами, диспепсией, язвой желудка, язвой двенадцатиперстной кишки, дисменореей, эндометриозом или хирургическим вмешательством (таким как операция на открытом сердце или шунтирование)), постоперационной боли, боли при почечно-каменной болезни, боли желчного пузыря, боли от желчного конкремента, боли при акушерстве или зубной боли.
Соединения согласно данному изобретению также пригодны для лечения мигрени, а именно головная боль типа напряжения, трансформирующая мигрень или прогрессирующая головная боль, «гистаминовая» головная боль, а также вторичных головных болей, происходящих от инфекций, метаболических нарушений или других системных заболеваний, и других типах сильных головных болей, а именно пароксизмальной гемикрании и тому подобного, возникающих в результате ухудшения вышеописанных первичных и вторичных головных болей.
Соединения согласно данному изобретению также пригодны для лечения неврологических состояний и когнитивных расстройств. Неврологические состояния включают, но не ограничиваясь этим, такие состояния, как эпилепсия (включая простые парциальные эпилептические припадки, эпилептические припадки автоматизма, вторичные большие эпилептические припадки, далее, включая миоклонические эпилептические припадки, клонические эпилептические припадки, тонические эпилептические припадки, тонически-клонические эпилептические припадки и атонические эпилептические припадки), дегенеративная деменция (включая старческое слабоумие, болезнь Альцгеймера, болезнь Пика, болезнь Паркинсона) и сосудистая деменция (включая мультиинфарктную деменцию, инсульт и церебральную ишемию), а также деменция, связанная с повреждениями в интракраниальном пространстве, травмой, инфекциями и родственными состояниями (включая ВИЧ-инфекцию), метаболизмом, токсинами, аноксией и авитаминозом; и легкое когнитивное ухудшение, связанное со старением, особенно, с возрастом, ассоциированным с ухудшением памяти, нарушениями движений (постэнцефалитический паркинсонизм, прогрессирующий супрануклеарный паралич, кортикобазальная дегенерация), нарколепсией, связанными с дефицитом и гиперактивностью нарушениями (ADHD), боковым амиотрофическим склерозом, синдромом Дауна.
Соединения согласно данному изобретению также пригодны для лечения психиатрических расстройств. Психиатрические расстройства включают, но не ограничиваясь этим, маниакальную депрессию, также известную как маниакально-депрессивный психоз (такой как маниакально-депрессивные психозы I и II типа), циклотимическое расстройство, быстрый цикл развития болезни, ультрадианный цикл развития болезни, биполярную депрессию, сильную, простую и смешанную манию к чему-либо, олигоманию или униполярную депрессию, шизофрению, расстройство шизофренического типа, шизоаффективные расстройства, расстройства, сопровождающиеся бредом, кратковременные психотические расстройства, общие психотические расстройства, психотические расстройства вследствие общего состояния здоровья, психотические расстройства, вызванные веществами, или психотическое расстройство, не определенное иным образом, расстройства, сопровождающиеся страхом, и, кроме того, курение и наркоманию.
Соединения согласно данному изобретению также пригодны для лечения таких периферических заболеваний, как шум в ушах, мышечный спазм, мышечный склероз, и других заболеваний, включая, но не ограничиваясь этим, сердечно-сосудистых заболеваний (таких как сердечная аритмия, инфаркт миокарда или стенокардия, повышенное кровяное давление, гипоксия, сердечная ишемия), эндокринных расстройств (таких как акромегалия или несахарный диабет), заболеваний, в случае которых патофизиология расстройства включает чрезмерную или гиперсекреторную или иную несоответствующую клеточную секрецию эндогенного вещества (такого как катехоламин, гормон или фактор роста).
Соединения согласно данному изобретению также пригодны для лечения такого заболевания печени, как воспалительное заболевание печени, например хронический вирусный гепатит В, хронический вирусный гепатит С, повреждение печени вследствие алкоголизма, первичный билиарный цирроз печени, аутоиммунный гепатит, неалкогольный стеатогепатит и отторжение трансплантата печени.
Соединения согласно данному изобретению ингибируют воспалительные процессы, поражающие все системы организма. Следовательно, они пригодны для лечения воспалительных процессов мышечно-скелетной системы, которые перечислены ниже в перечне примеров, но не охватывают все целевые расстройства: артритные состояния, такие как алкилозирующий спондилит, шейный артрит, фибромиалгия, кишечное расстройство, ювенильный ревматоидный артрит, пояснично-крестцовый артрит, остеоартрит, остеопороз, псориатический артрит, ревматическое заболевание; расстройства, поражающие кожу и родственные ткани: экзема, псориаз, дерматит и воспалительные состояния, такие как солнечный ожог; расстройства дыхательной системы: астма, аллергический ринит и респираторный дистресс-синдром, заболевания легких, опосредуемые воспалением, как, например, астма и бронхит; хроническое обструктивное заболевание легких; расстройства иммунной и эндокринологической систем: нодозный периартериит, тиреоидит, апластическая анемия, склеродома, тяжелая псевдопаралитическая миастения, рассеянный склероз, саркоидоз, почечный синдром, синдром Бехчета, полимиозит, гингивит.
Соединения согласно данному изобретению также пригодны для лечения таких расстройств желудочно-кишечного тракта (GI), как воспалительные расстройства кишечника, включая, но не ограничиваясь этим, язвенный колит, болезнь Крона, илеит, проктит, глютеновую болезнь, энтеропатии, микроскопический или коллагенозный колит, эозинофильный гастроэнтерит или резервуарный илеит, возникающий после проктоколэктомии и постилеонатального анастомоза, и синдром раздраженной толстой кишки, включающий любые расстройства, связанные с абдоминальной болью и/или абдоминальным дискомфортом, как, например, пилороспазм, нервная диспепсия, синдром раздраженной толстой кишки, слизистый колит, спастический кишечник, интестинальный невроз, функциональный колит, слабительный колит и функциональная диспепсия; а также для лечения атрофического гастрита, различных форм гастрита, язвенного колита, пептической язвы, изжоги и другого повреждения GI-тракта, например, бактерией Helicobacter pylori, желудочно-пищеводным рефлюксом, гастропарезом, как, например, диабетический гастропарез; и других функциональных расстройств кишечника, таких как неязвенная диспепсия (NUD); рвота, диарея и висцеральное воспаление.
Соединения согласно данному изобретению также пригодны для лечения таких расстройств мочеполового тракта, как сверхактивность мочевого пузыря, простатит (хронический бактериальный и хронический небактериальный простатит), простадиния, интерстициальный цистит, недержание мочи и доброкачественная гиперплазия предстательной железы, аннексития, пельвиоперитонит, бартолинит и вагинит.
Соединения согласно данному изобретению также пригодны для лечения таких глазных заболеваний, как ретинит, ретинопатия, увеит и сильное повреждение глазной сетчатки, дегенерация желтого пятна или глаукома, конъюнктивит.
Соединения согласно данному изобретению также пригодны для лечения ожирения.
Соединения согласно данному изобретению также пригодны для лечения всех других состояний, опосредуемых ингибированием потенциалзависимых мембранных натриевых каналов и/или потенциалзависимых мембранных кальциевых каналов.
Нужно принимать во внимание, что соединения согласно данному изобретению можно преимущественно применять в сочетании с одним или более другими терапевтическими агентами. Примеры подходящих агентов для дополнительной терапии включают 5НТ1B/1D-агонист, такой как триптан (например, суматриптан или наратриптан); агонист аденозина А1; ЕР-лиганд; NMDA-модулятор, такой как антагонист глицина; антагонист вещества Р (например, NK1-антагонист); каннабиноид; ацетаминофен или фенацетин; ингибитор 5-липоксигеназы; антагонист рецептора лейкотриена; DMARD (например, метотрексат); габапентин и родственные соединения; трициклический антидепрессант (например, амитриптилин); нейронстабилизирующее антиэпилептическое лекарственное средство; моноаминергический ингибитор поглощения (например, венлафаксин); матриксный металлопротеиназный ингибитор; ингибитор синтеза оксида азота (NOS), такой как iNOS- или nNOS-ингибитор; ингибитор высвобождения или действия фактора некроза опухоли альфа; терапия с использованием антител, например, моноклональных антител; противовирусный агент, такой как нуклеозидный ингибитор (например, ламивудин) или модулятор иммунной системы (например, интерферон); анальгетик, такой как ингибитор циклооксигеназы-2; местное анестезирующее средство; стимулятор, включая кофеин; Н2-антагонист (например, ранитидин); ингибитор протонового насоса (например, омепразол); антацид (например, гидроксид алюминия или магния); ветрогонное средство (например, симетикон); противоотечное средство (например, фенилэфрин, фенилпропаноламин, псевдоэфедрин, оксиметазолин, эпинефрин, нафазолин, ксилометазолин, пропилгекседрин или лево-дезоксиэфедрин, ксилометазолин); средство от кашля (например, кодеин, гидрокодон, кармифен, карбетапентан или декстраметорфан); мочегонное средство; или седативное и не седативное антигистаминное средство. Следует подразумевать, что настоящее изобретение относится к применению соединения формулы I или его фармацевтически приемлемой соли в сочетании с одним или более терапевтическими агентами.
Соединения согласно настоящему изобретению пригодны для применения в медицине и ветеринарии. Рекомендация для лечения включает как лечение установленных симптомов, так и профилактическое лечение, за исключением точно назначенного другим образом.
Циклопентильные производные общей формулы I, как описано выше, можно вводить в качестве «активного ингредиента» фармацевтически приемлемой композиции, которую можно получать с помощью стандартных методик, например, путем смешивания активного ингредиента с фармацевтически приемлемыми, терапевтически инертными органическими и/или неорганическими носителями.
Композиции, содержащие вышеописанные циклопентильные производные, можно вводить в различных формах, например, перорально, в форме таблеток, пилюль, капсул, таблеток с сахарным или пленочным покрытием, жидких растворов, эмульсий или суспензий; ректально, в форме суппозиториев; парентерально, например, путем внутримышечной или внутривенной инъекции или инфузии; и трансдермально.
Подходящие фармацевтически приемлемые, терапевтически инертные органические и/или неорганические носители, пригодные для получения такой композиции, включают, например, воду, желатин, гуммиарабик, лактозу, крахмал, целлюлозу, стеарат магния, тальк, растительные масла, полиалкиленгликоли и тому подобное. Композиции, содержащие циклопентильные производные формулы I, как описано выше, можно стерилизовать и они могут, далее, содержать хорошо известные компоненты, такие как, например, консерванты, стабилизаторы, смачивающие или эмульгирующие агенты, например, парафиновое масло, маннид-моноолеат, соли для регулирования осмотического давления, буферы и тому подобное.
Например, твердые пероральные формы могут содержать, наряду с активным ингредиентом, разбавители, например лактозу, декстрозу, сахарозу, целлюлозу, кукурузный крахмал или картофельный крахмал; смазки, например диоксид кремния, тальк, стеариновую кислоту, стеарат магния или кальция, и/или полиэтиленгликоли; связующие агенты, например крахмалы, гуммиарабик, желатин, метилцеллюлозу, карбоксиметилцеллюлозу или поливинилпирролидон; дезагрегирующие агенты, например крахмал, альгиновую кислоту, альгинаты или модифицированный гликолятом натрия крахмал; шипучие смеси; красители; подсластители; смачивающие агенты, такие как лецитин, полисорбаты, лаурилсульфаты; и, в общем, нетоксичные и фармакологически неактивные вещества, применяемые в фармацевтических готовых лекарственных формах. Вышеописанные фармацевтические лекарственные средства можно получать известным образом, например способами смешивания, гранулирования, таблетирования, нанесения сахарного или пленочного покрытия.
Готовые пероральные лекарственные формы включают готовые лекарственные формы пролонгированного действия, которые можно получать обычным образом, например путем нанесения энтеросолюбильной оболочки на таблетки и гранулы.
Жидкой дисперсией для перорального введения могут быть, например, сиропы, эмульсии и суспензии.
Сиропы могут содержать в качестве носителя, например, сахарозу или сахарозу с глицерином, и/или маннитом, и/или сорбитом.
Суспензии и эмульсии могут содержать в качестве носителя, например, природную смолу, агар, альгинат натрия, пектин, метилцеллюлозу, карбоксиметилцеллюлозу или поливиниловый спирт. Суспензии или растворы для внутримышечных инъекций могут содержать, наряду с активным соединением, фармацевтически приемлемый носитель, например стерильную воду, оливковое масло, этилолеат, гликоли, например пропиленгликоль, и, если желательно, подходящее количество гидрохлорида лидокаина. Растворы для внутривенных инъекций или инфузии могут содержать в качестве носителя, например, стерильную воду или, предпочтительно, они могут быть в форме стерильных, водных, изотонических солевых растворов.
Суппозитории могут содержать, наряду с активным ингредиентом, фармацевтически приемлемый носитель, например масло какао, полиэтиленгликоль, поверхностно-активные вещества на основе полиоксиэтиленсорбитановых эфиров жирных кислот или лецитин.
Подходящее лечение проводят 1, 2 или 3 раза в сутки, в зависимости от скорости выведения из организма. Соответственно, желательная доза может представлять собой разовую дозу или быть в виде разделенных доз, вводимых через соответствующие интервалы времени, например, от двух до четырех или более субдоз в сутки.
Фармацевтические композиции, содержащие циклопентильные производные формулы I, как описано выше, включают, на унифицированную дозу, например капсулу, таблетку, порошок для инъекции, полную чайную ложку лекарственного препарата, суппозиторий и тому подобное, в количестве от примерно 0,1 до примерно 500 мг активного ингредиента, более предпочтительно, от 1 мг до 10 мг.
Вводимые оптимальные терапевтически эффективные дозы могут быть легко определены специалистом в данной области и изменяются, в основном, в зависимости от эффективности лекарственного средства, способа введения и динамики изменения состояния или расстройства. Кроме того, факторы, связанные с конкретным субъектом, включающие возраст субъекта, массу тела, режим питания и время введения, определяют необходимость регулирования дозы для достижения соответствующего терапевтического эффекта.
Далее данное изобретение проиллюстрировано следующими примерами.
Пример 1
Амид цис-2-[3-(2-Фторбензилокси)бензиламино]циклопентан-карбоновой кислоты
2 М Раствор амида 2-аминоциклопентанкарбоновой кислоты (0,75 г, 6,5 ммоль) в безводном ТГФ добавляют к 1 М раствору в безводном ТГФ 3-(2-фторбензилокси)бензальдегида (1,64 г, 7,15 ммоль), получаемого как описано в примере 3. К этой смеси по каплям добавляют 2 М раствор Ti(O-iPr)4 (2,77 г, 9,75 ммоль) в безводном ТГФ и реакционную смесь перемешивают в течение 12 часов при комнатной температуре в атмосфере азота.
Добавляют 0,75 М раствор боргидрида натрия (0,69 г, 18,2 ммоль) в абсолютном этаноле и реакционную смесь нагревают при 70оС в течение 6 часов. После охлаждения для гашения реакции добавляют 8 мл воды и полученный осадок белого цвета удаляют фильтрацией. Сырое соединение очищают, используя SCX-картридж (сильная катионо-обменная смола). Чистый продукт выделяют элюированием 3%-ным раствором аммиака в метаноле. После выпаривания растворителя в вакууме получают указанное в заголовке соединение (2,08 г) с выходом 94%.
MS (ESI (ионизация электронным распылением) Pos Spray, 3,5 кВ; Skimmer 20 В; образец при 250оС): 343 [МН+].
1H-ЯМР (ДМСО-d6) δ: 7,55 (м, 1H), 7,45 (м, 2H), 7,25 (м, 3H), 7,0 (с, 1H), 6,88 (м, 2H), 6,78 (с, 1H), 5,1 (с, 2H), 3,7 (дд, 2H), 3,10 (м, 1H), 2,65 (м, 1H), 1,90-1,4 (м, 6H).
Пример 2
Амид цис-2-[4-(2-Фторбензилокси)-3,5-диметилбензиламино]циклопентанкарбоновой кислоты
2 М Раствор амида 2-аминоциклопентанкарбоновой кислоты (0,75 г, 6,5 ммоль) в безводном ТГФ добавляют к 1 М раствору в безводном ТГФ 4-(2-фторбензилокси)-3,5-диметилбензальдегида (1,84 г, 7,15 ммоль), получаемого как описано в примере 4. К этой смеси по каплям добавляют 2 М раствор Ti(O-iPr)4 (2,77 г, 9,75 ммоль) в безводном ТГФ и реакционную смесь перемешивают в течение 12 часов при комнатной температуре в атмосфере азота.
Добавляют 0,75 М раствор боргидрида натрия (0,69 г, 18,2 ммоль) в абсолютном этаноле и реакционную смесь нагревают при 70оС в течение 6 часов. После охлаждения добавляют 8 мл воды и полученный осадок белого цвета удаляют фильтрацией. Сырое соединение очищают, используя SCX-картридж (сильная катионообменная смола). Чистый продукт выделяют элюированием 3%-ным раствором аммиака в метаноле. После выпаривания растворителя в вакууме получают указанное в заголовке соединение (2,14 г) с выходом 89%.
MS (ESI Pos Spray, 3,5 кВ; Skimmer 20 В; образец при 250оС): 371 [МН+].
1H-ЯМР (ДМСО-d6) δ: 7,60 (м, 1H), 7,48 (м, 2H), 7,28 (м, 2H), 6,95 (с, 2H), 6,78 (с, 1H), 4,80 (с, 2H), 3,6 (дд, 2H), 3,15 (м, 1H), 2,68 (м, 1H), 2,2 (с, 6H), 1,85-1,51 (м,6H).
Пример 3
3-(2-Фторбензилокси)бензальдегид
0,5 М Раствор 1-бромметил-2-фторбензола (1,50 г, 8,0 ммоль) в ДМФА по каплям добавляют к суспензии 3-гидроксибензальдегида (0,89 г, 7,3 ммоль), К2СО3 (1,51 г, 11 ммоль) и KI (0,12 г, 0,73 ммоль) в 100 мл ДМФА. Реакционную смесь перемешивают при 90оС в течение ночи. После охлаждения до комнатной температуры твердый остаток отфильтровывают и растворитель выпаривают в вакууме. Остаток растворяют в этилацетате, органический слой дважды промывают 1 М раствором NaOH, сушат над Na2SO4 и выпаривают досуха. Остаток очищают на силикагеле, получая 167 мг указанного в заголовке соединения (количественный выход).
Пример 4
4-(2-Фторбензилокси)-3,5-диметилбензальдегид
0,5 М Раствор 1-бромметил-2-фторбензола (1,50 г, 8,0 ммоль) в ДМФА по каплям добавляют к суспензии, содержащей 1,09 г 4-гидрокси-3,5-диметилбензальдегида (7,3 ммоль), 1,51 г К2СО3 (11 ммоль) и 120 мг KI (0,73 ммоль) в 100 мл ДМФА. Реакцию осуществляют по той же самой методике, описанной в примере 3. Остаток очищают на силикагеле, получая количественный выход указанного в заголовке соединения (1,88 г).
Пример 5
In vitro связывание 3Н-батрахотоксина в мембранах головного мозга крысы
Мембранные препараты (Р2-фракция). Самцов крыс Wistar (Harlan, Италия, массой 175-200 г) умерщвляли под легкой анестезией, быстро извлекали головной мозг и препарировали кору головного мозга, гомогенизировали в 10 объемах 0,25 М ледяного буфера на основе сахарозы (50 мМ Tris·HCl, рН 7,4). Сырой гомогенат центрифугировали при 3250 об/мин в течение 10 мин и супернатант рекуперировали. Осадок после центрифугирования снова гомогенизировали и центрифугировали и два супернатанта объединяли и центрифугировали при 14750 об/мин в течение 10 мин при +4оС. Полученный осадок после центрифугирования сохраняли при -20оС до использования.
Анализ на связывание. Осадок после центрифугирования повторно суспендировали в 50 мМ Hepes-буфере с рН 7,4, содержащем 0,8 мМ MgSO4, 5,4 мМ KCl, 5,5 мМ глюкозы и 130 мМ холина, используя устройство Polytron PT10. Анализ на связывание осуществляли в конечном объеме 0,25 мл, содержащем 50 мкл мембранного препарата (примерно 200 мкг белка), 50 мкл лиганда 3Н-батрахотоксина (10 нМ), 50 мкл ТТХ (1 мкМ), 50 мкл яда скорпиона (37,5 мкг/мл) и 50 мкл тестируемого соединения или буфера или 300 мкМ вератридина для определения неспецифического связывания. Анализ на связывание проводили при 37оС в течение 30 мин и прекращали быстрой фильтрацией в вакууме через фильтры из стекловолокна марки Whatman GF/B. Фильтры (предварительно пропитанные 0,1%-ным раствором полиэтиленимина) промывали ледяным буфером 3 раза по 5 мл и помещали в микропробирки, содержащие сцинтилляционный коктейль (Filter Count, Packard). Связанную радиоактивность измеряли с помощью жидкостного сцинтилляционного спектрометра с эффективностью 45%.
Анализ полученных данных. IC50 рассчитывали из кривых замещения с помощью компьютерной программы LIGAND (McPherson, J. Pharmacol. Methods, 14, 213, 1985). Кривые замещения получали, используя, по меньшей мере, девять концентраций, каждая из которых была дублирована, в 100000-кратном диапазоне.
Пример 6
In vitro связывание 3Н-нитрендипина в мембранах головного мозга крысы
Мембранные препараты. Самцов крыс Wistar (Harlan, Италия, массой 175-200 г) умерщвляли под легкой анестезией, быстро извлекали головной мозг и препарировали кору головного мозга, гомогенизировали в 10 объемах ледяного 50 мМ Tris·HCl, рН 7,7, используя устройство Polytron PT10. Сырой гомогенат центрифугировали с ускорением 50000 g в течение 10 мин. Осадок после центрифугирования дважды гомогенизировали и центрифугировали в свежем буфере с ускорением 50000 g в течение 10 мин при +4оС. Полученный осадок после центрифугирования сохраняли при -20оС до использования.
Анализ на связывание. Осадок после центрифугирования повторно суспендировали в 50 мМ Tris·HCl, рН 7,7, используя устройство Polytron PT10. Анализ на связывание осуществляли в конечном объеме 1 мл, содержащем 900 мкл мембранного препарата (примерно 700 мкг белка), 50 мкл 3Н-нитрендипина (0,15 нМ) и 50 мкл тестируемого соединения или буфера или 1 мкМ нифедипина для определения неспецифического связывания. Анализ на связывание проводили при 25оС в течение 45 мин и прекращали быстрой фильтрацией в вакууме через фильтры из стекловолокна марки Whatman GF/B. Фильтры промывали ледяным буфером 3 раза по 5 мл и помещали в микропробирки, содержащие сцинтилляционный коктейль (Filter Count, Packard). Связанную радиоактивность измеряли с помощью жидкостного сцинтилляционного спектрометра с эффективностью 45%.
Анализ полученных данных. IC50 рассчитывали из кривых замещения с помощью компьютерной программы LIGAND (McPherson, J. Pharmacol. Methods, 14, 213, 1985). Кривые замещения получали, используя, по меньшей мере, девять концентраций, каждая из которых была дублирована, в 100000-кратном диапазоне.
Пример 7
Анализ на приток кальция
Клетки человеческой нейробластомы IMR32, конструктивно, имеют каналы как L-, так и N-типа. В условиях дифференцировки IMR32 предпочтительно экспрессируют на мембранной поверхности кальциевые каналы N-типа. Оставшиеся кальциевые каналы L-типа блокировали, используя селективный блокатор L-типа, нифедипин. В этих экспериментальных условиях можно детектировать только каналы N-типа.
IMR32-клетки подвергали дифференцировке, используя 1 мМ дибутирил-сАМР и 2,5 мкМ бромдезоксиуридин, в течение 8 суток (4 раза) в колбе емкостью 225 см2, затем отделяли, высевали в количестве 200000 клеток на лунку на 96-луночные планшеты, покрытые полилизином, и далее инкубировали в течение 18-24 часов в присутствии ранее используемого буфера для дифференцировки.
Использовали набор для анализа на Са2+ (Molecular Devices), основанный на флуоресцентном кальциевом индикаторе, с длиной волны 485-535 нм.
Дифференцированные клетки инкубировали с красителем в течение 30 мин при 37оС, затем в течение следующих 15 мин добавляли только нифедипин (1 мкМ) или в присутствии ω-конотоксина или тестируемых соединений.
Флуоресценцию (485-535 нм) измеряли до и после (30-40 сек) автоматизированно вводимой инъекции 100 мМ деполяризующего раствора KCl, используя планшет-ридер Victor (Perkin Elmer).
Кривые ингибирования рассчитывали из пяти концентраций, каждую из которых повторяли три раза, и IC50 определяли, используя линейный регрессионный анализ.
Предпочтительные соединения общей формулы I ингибируют кальциевые каналы N-типа при значении IC50 меньше, чем 10 мкМ.
Пример 8
Электрофизиологический анализ
Эксперименты по определению тонической блокировки осуществляли на изолированных овоцитах Xenopus, экспрессирующих натриевый канал Nav 1.3. Токи регистрировали, используя двухэлектродный способ фиксации потенциала (TEVC).
Получение овоцитов:
Лягушку (Xenopus Laevis) анестезировали раствором этилового эфира 3-аминобензойной кислоты (1 г/л) и, спустя 25 мин, ее помещали спиной на «ледяную подстилку». Разрезали кожу и другие ткани, удаляли овариальные доли и сохраняли в растворе ND96ØCa2+ (96 мМ NaCl, 2 мМ KCl, 1 мМ MgCl2, 10 мМ Hepes, с pH 7,85, установленным с помощью NaOH).
После удаления овоцитов мышцы и кожу сшивали по отдельности.
Овариальные доли объединяли в кластеры по 10/20 овоцитов, помещали в пробирки с раствором коллагеназы (1 мг/мл) и выдерживали в состоянии движения в течение примерно 1 часа в инкубаторе.
По окончании этой стадии, когда овоциты хорошо отделялись одни от других, их промывали три раза раствором ND96ØCa2+ и три раза раствором NDЕ (ND96ØCa2++0,9 мМ СаCl2, 0,9 мМ MgCl2, 2,5 мМ пирувата, 50 мг/л гентамицина).
Полученные овоциты находятся на разных стадиях развития. Только клетки на стадиях V или VI выбирали для последующих экспериментов с инъекцией РНК.
Через сутки после получения овоциты инъецировали (Drummond Nanoject) с 20 нг Nav 1,3 кРНК и сохраняли в растворе NDЕ.
Начиная с 48 часов после мРНК-инъекции, регистрировали все клеточные токи, используя двухмикроэлектродный автоматизированный модуль фиксации потенциала.
Типичные микроэлектроды имеют сопротивление от 0,5 до 1 МОм и заполнены 3 М раствором KCl.
Контрольный раствор электролита содержит (мМ): 98 NaCl, 1 MgCl2, 1,8 СаCl2, 5 HEPES (рН 7,6).
Соединения получали в исходных растворах (20 мМ) и разводили до конечных концентраций с помощью «внешнего» раствора электролита.
Регистрация токов
Зависимость ток/потенциал (I/V) для токов Nav 1.3, экспрессируемых в овоцитах, впервые была изучена для определения мембранного потенциала, индуцирующего максимальную активацию. Nav 1.3 показывает максимальную активацию при 0 мВ, которую авторы настоящего изобретения использовали как тест-потенциал (V-тест) для исследований тонической блокировки.
Свойства устойчивость - состояние инактивации токов Nav 1.3 затем изучали для определения мембранных потенциалов в состоянии покоя (Vrest), при котором доступность канала является максимальной (Imax), и мембранного потенциала для полумаксимальной инактивации (½V), продуцирующего половину максимальной доступности тока (½I), соответственно. Эти два состояния потенциала затем использовали для определения зависимости от потенциала тонической блокировки.
В заключение двухстадийный протокол использовали для определения зависимости от потенциала блокировки Nav 1.3: овоциты фиксировали при -80 мВ, токи активировали путем импульс-шага 100 мс до 0 мВ (V-тест) от предварительного стандартного потенциала 3000 мс при -80 мВ (состояние покоя, Imax) и при -40 мВ (деполяризованное состояние, ½I), соответственно.
Амплитуды тока в двух состояниях регистрировали в отсутствие и в присутствии различных концентраций соединения (с промежуточной промывкой) для получения кривых концентрация - ингибирование и значений IC50 для тонической блокировки в деполяризованных (полумаксимальная доступность тока) состояниях.
Предпочтительные соединения общей формулы I ингибируют натриевые каналы Nav 1.3 при значении IC50 ниже, чем стандартный блокатор натриевого канала ралфинамид.
Пример 9
Тест на максимальный электрошок у крыс и мышей
Крыс Wistar подвергали электрошоку (160 мА в течение 0,2 сек с последовательностью импульсов 60 Гц, имеющих длительность импульса 0,4 мсек; ЕСТ-установка, модель 7801, Ugo Basile, Comerio, Италия) через внутриушно клипированные электроды, достаточному для получения тонического экстензорного ответа задней конечности, по меньшей мере, у 97% контрольных животных.
Мышей подвергали электрошоку 28 мА в течение 0,7 сек с последовательностью импульсов 80 Гц, имеющих длительность импульса 0,4 мсек. Отдельные дозы тестируемого соединения и стандартные AEDs вводили группам из 10-20 мышей или крыс на дозу объемом 5 мл/кг в течение 60 мин перорально или 30 мин внутрибрюшинно перед индукцией максимального электрошока (MES), для расчета значений ED50. Полную супрессию тонического экстензорного компонента судорог задней конечности получали как доказательство противосудорожной активности.
Пример 10
Формалиновый тест на мышах
В соответствии с измененным протоколом Rosland и др. (1990), мышам инъецировали подкожно 20 мкл 2,7%-ного раствора формалина в подошвенную поверхность левой задней лапы и сразу помещали в прозрачные камеры из поливинилхлорида для наблюдения (размером 23×12×13 см). Болевое поведение оценивали путем вычисления совокупного времени зализывания (сек) инъецированной лапы. Измерения проводили в течение ранней фазы (0-5 мин) и поздней фазы (30-40 мин) после инъекции формалина (Tjolsen и др., 1992).
Тестируемое соединение вводили перорально за 15 мин до инъекции формалина в объеме 10 мл/кг массы тела группам из 10 мышей на дозу. Контрольную группу обрабатывали эксципиентом.
Пример 11
Каррагенановая модель воспаления
Использовали самцов крыс Wistar массой 175-200 г.
В левую заднюю лапу инъецировали 100 мкл каррагенана (2% масс./объем в физиологическом растворе). Соединения согласно данному изобретению (30 мг/кг), индометацин (5 мг/кг) или контрольный эксципиент (такой как дистиллированная вода) перорально вводили за 1 час перед инъекцией каррагенана. Объем лапы измеряли с помощью плетизмометра (Ugo Basile) непосредственно перед (основной) и спустя 1, 2, 3, 4 и 5 часов после инъекции каррагенана.
| название | год | авторы | номер документа |
|---|---|---|---|
| ПРИМЕНЕНИЕ (ГАЛОБЕНЗИЛОКСИ)БЕНЗИЛАМИНО-ПРОПАНАМИДОВ ДЛЯ ПРОИЗВОДСТВА ЛЕКАРСТВЕННЫХ СРЕДСТВ, ДЕЙСТВУЮЩИХ КАК СЕЛЕКТИВНЫЕ МОДУЛЯТОРЫ НАТРИЕВЫХ И/ИЛИ КАЛЬЦИЕВЫХ КАНАЛОВ | 2005 |
|
RU2391973C2 |
| N-АЦИЛ-N`-БЕНЗИЛАЛКИЛЕНДИАМИНОПРОИЗВОДНЫЕ | 2004 |
|
RU2387636C2 |
| 2-ФЕНИЛЭТИЛАМИНОПРОИЗВОДНЫЕ В КАЧЕСТВЕ МОДУЛЯТОРОВ КАЛЬЦИЕВЫХ И/ИЛИ НАТРИЕВЫХ КАНАЛОВ | 2006 |
|
RU2397160C9 |
| ПРОИЗВОДНЫЕ 3-АМИНОПИРРОЛИДОНА | 2004 |
|
RU2395495C2 |
| ЗАМЕЩЕННЫЕ ТРИАЗОЛЫ В КАЧЕСТВЕ БЛОКАТОРОВ НАТРИЕВЫХ КАНАЛОВ | 2004 |
|
RU2372339C2 |
| АРИЛ-ЗАМЕЩЕННЫЕ КАРБОКСАМИДНЫЕ ПРОИЗВОДНЫЕ В КАЧЕСТВЕ БЛОКАТОРОВ КАЛЬЦИЕВЫХ ИЛИ НАТРИЕВЫХ КАНАЛОВ | 2010 |
|
RU2575168C2 |
| КОМПОЗИЦИИ, ПОЛЕЗНЫЕ В КАЧЕСТВЕ ИНГИБИТОРОВ ПОТЕНЦИАЛЗАВИСИМЫХ НАТРИЕВЫХ КАНАЛОВ | 2007 |
|
RU2470012C2 |
| ПРОИЗВОДНЫЕ ПИРИДИНАМИДОВ И ЛЕКАРСТВЕННОЕ СРЕДСТВО НА ИХ ОСНОВЕ | 2003 |
|
RU2309950C2 |
| ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ СПИРО-ОКСИНДОЛЬНОГО СОЕДИНЕНИЯ ДЛЯ МЕСТНОГО ВВЕДЕНИЯ И ИХ ПРИМЕНЕНИЕ В КАЧЕСТВЕ ТЕРАПЕВТИЧЕСКИХ АГЕНТОВ | 2011 |
|
RU2596488C2 |
| ПРОИЗВОДНЫЕ АМИДА КОРИЧНОЙ КИСЛОТЫ | 2003 |
|
RU2318802C2 |
Описывается соединение формулы I, где Х означает кислород; R1 означает линейную или разветвленную C1-C8-алкильную цепь, замещенную фенилом, необязательно замещенным атомами галогенов; R2, R3 независимо означают водород, C1-С3-алкильную цепь, галоген, метокси; R4, R5, R6, R7 независимо означают водород, а также способ его получения, фармацевтическая композиция, применение соединения для получения лекарственного средства, которое эффективно в качестве модулятора натриевого и/или кальциевого канала и, следовательно, пригодно для предотвращения, облегчения и лечения широкого спектра патологий, включая неврологические, психиатрические, сердечно-сосудистые, воспалительные, глазные, урологические, метаболические и желудочно-кишечные заболевания, где вышеуказанные механизмы описываются как играющие патологическую роль. 5 н. и 1 з.п. ф-лы.

1. Соединение формулы I:

где Х означает кислород;
R1 означает линейную или разветвленную С1-С8-алкильную цепь, замещенную фенилом, необязательно замещенным атомами галогенов;
R2, R3 независимо означают водород, C1-С3-алкильную цепь, галоген, метокси;
R4, R5, R6, R7 независимо означают водород;
и его фармацевтически приемлемые соли.
2. Соединения формулы I по п.1, где Х означает кислород, R1 означает C1-C8-алкильную цепь, замещенную фенилом, где ароматическое кольцо в R1 необязательно замещено одним или двумя атомами галогена, R2 и R3 означают водород, метил, метокси, фтор, хлор или бром, R4, R5 и R6 означают водород.
3. Соединение, выбираемое из группы, состоящей из:
амида цис-2-[3-(2-фторбензилокси)бензиламино]циклопентанкарбоновой кислоты;
амида цис-2-[4-(2-фторбензилокси)-3,5-диметилбензиламино]циклопентанкарбоновой кислоты;
и всех их фармацевтически приемлемых солей.
4. Способ получения соединения формулы I по п.1, или его фармацевтически приемлемой соли, включающий:
а) взаимодействие соединений формулы II:

где R1, R2, R3 и Х имеют значения, как указано выше, с соединениями формулы III, в присутствии восстановителя:

где R4, R5 и R6 такие, как определено выше, таким образом получая соединение формулы I;
и, если желательно, превращение соединения в другое соединение и/или, если желательно, превращение соединения в фармацевтически приемлемую соль и/или, если желательно, превращение соли в свободное соединение и/или, если желательно, разделение смеси изомеров соединений.
5. Фармацевтическая композиция, обладающая модулирующей кальциевый и/или натриевый канал активностью, содержащая соединение формулы I по п.1 или его фармацевтически приемлемую соль в смеси с подходящим носителем и/или разбавителем.
6. Применение соединения формулы I по п.1 или его фармацевтически приемлемой соли для получения лекарственного средства, обладающего модулирующей натриевый и/или кальциевый канал активностью, для предотвращения, облегчения и лечения неврологических, психиатрических, сердечно-сосудистых, воспалительных, глазных, урологических, метаболических и желудочно-кишечных заболеваний, где натриевые и/или кальциевые каналы вовлечены в патологический процесс.
| ИЗМЕЛЬЧАЮЩИЙ ВАЛОК С ЗАЩИТОЙ КРАЕВ | 2013 |
|
RU2624290C2 |
| Прибор, замыкающий сигнальную цепь при повышении температуры | 1918 |
|
SU99A1 |
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| N-ФЕНИЛАЛКИЛАЗАМЕЩЕННЫЕ ПРОИЗВОДНЫЕ α -АМИНОКАРБОКСАМИДА, СПОСОБ ИХ ПОЛУЧЕНИЯ, ФАРМАКОЛОГИЧЕСКИ АКТИВНАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ И СПОСОБ ПРЕДУПРЕЖДЕНИЯ РАЗВИТИЯ БОЛЕЗНИ | 1992 |
|
RU2097371C1 |
Авторы
Даты
2009-11-10—Публикация
2004-11-12—Подача