Изобретение относится к медицинской иммунологии, а именно к способам определения функциональной активности факторов комплемента в сыворотке крови человека при диагностике ряда заболеваний и в биологических препаратах.
Наиболее перспективным из современных методов определения белков сыворотки крови является метод иммуноферментного анализа благодаря своей чувствительности, избирательности и возможности автоматизации аналитического процесса. Известен способ определения функциональной активности фактора В альтернативного пути комплемента человека [1], который предусматривает сорбцию в лунках микропанели активатора альтернативного пути комплемента, выбранного из ряда: иммуноглобулин А, иммуноглобулин G, компонент С3, липополисахарид, затем внесение в лунки микропанели раствора, содержащего реагент RB (сыворотки крови человека, лишенной активности фактора В), и анализируемой пробы, содержащей фактор В комплемента человека с неизвестной активностью, проведение инкубации в присутствии ионов Mg2+ и в отсутствие ионов Ca2+ (в ходе которой происходит формирование С3-конвертазы (С3bВb) на сорбированном активаторе альтернативного пути в количествах, зависящих от концентрации функционально активного определяемого фактора В, участвующего в образовании С3-конвертазы, в результате чего происходит активация этой конвертазой С3 и ковалентное связывание последнего на сорбированном активаторе), выливание содержимого лунок, а затем внесение конъюгата фермента с антителами против компонента С3 человека и субстрата этого фермента и проведение расчета активности фактора В по количеству образовавшегося продукта ферментативной реакции.
Единственным недостатком этого способа является относительно трудная доступность и плохая длительная сохраняемость активирующей способности индивидуальных, высокоочищенных препаратов активаторов альтернативного пути, сорбируемых на микропанели, а в случае липополисахаридов, кроме того, трудности в их сорбции на полистироловых микропанелях, обычно используемых в иммуноферментном анализе.
Задачей заявленного изобретения является разработка способа и набора на основе иммуноферментного метода, позволяющего определять функциональную активность фактора В альтернативного пути системы комплемента человека с использованием доступного и хорошо сохраняемого в обычных условиях коммерческого препарата для использования в качестве активатора альтернативного пути комплемента.
Поставленная задача достигается путем разработки способа определения и набора. Способ определения предусматривает сорбцию в лунках микропанели аптечного препарата лизоцима, хорошо сохраняемого в обычных условиях, затем внесение в лунки микропанели раствора, содержащего реагент RB (сыворотки крови человека, лишенной активности фактора В), и анализируемой пробы, содержащей фактор В комплемента человека с неизвестной активностью, проведение инкубации в присутствии ионов Mg2+ и в отсутствие ионов Са2+ (в ходе которой происходит формирование С3-конвертазы (С3bВb) на сорбированном активаторе альтернативного пути в количествах, зависящих от концентрации функционально активного определяемого фактора В, осуществляющего активацию фактора В в ходе образования С3-конвертазы, в результате чего происходит активация этой конвертазой С3 и ковалентное связывание последнего на сорбированном активаторе), выливание содержимого лунок, а затем внесение конъюгата фермента с антителами против компонента С3 человека и субстрата этого фермента и проведение расчета активности фактора В по количеству образовавшегося продукта ферментативной реакции.
Набор содержит плоскодонную микропанель с сорбированным лизо-цимом, реагент RB (сыворотку крови человека, лишенную активности фактора В), конъюгат фермента с антителами к компоненту С3 комплемента человека, субстратный буфер и стандарт с известной активностью фактора В.
Техническим результатом заявленного изобретения является разработка способа и набора для определения функциональной активности фактора В комплемента человека, обладающего хорошей воспроизводимостью результатов и отсутствием необходимости использования труднодоступных высокоочищенных препаратов активаторов альтернативного пути, плохо сохраняющих свою активирующую способность, какими являются иммуноглобулины G и А, компонент С3 и липополисахарид.
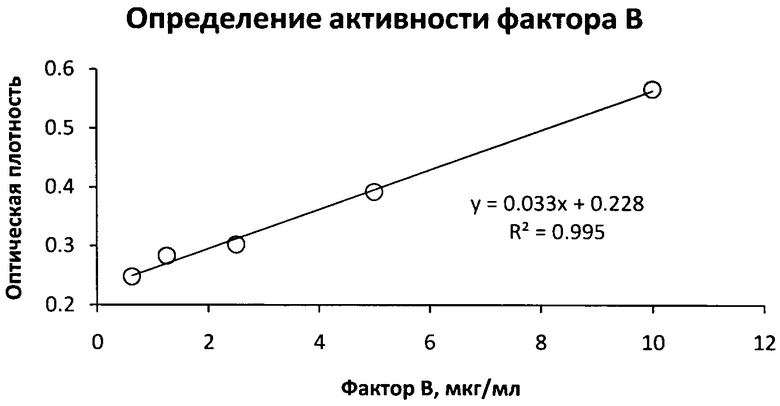
Пример 1. Определение функциональной активности препарата фактора В. Растворяют активатор альтернативного пути комплемента - аптечный препарат лизоцима в 0,05 М натрий-карбонатном буфере, pH 9,5, в концентрациях 10-100 мкг/мл и вносят по 100 мкл раствора в каждую лунку плоскодонной полистироловой 96-луночной микропанели. Закрывают крышкой и оставляют на ночь при 4°С. Три раза отмывают микропанель вероналовым буферным раствором, pH 7,4, содержащим 0,15 М NaCl, 10 мМ этиленгликоль-бис(β-аминоэтиловый эфир)-N,N,N',N'-тетрауксусную кислоту и 5 мМ MgCl2 (Mg-EGTA), заливая по 150 мкл в каждую лунку, затем микропанель осушают путем вытряхивания остатка жидкости. В лунки микропанели ряда вносят по 100 мкл раствора Mg-EGTA, содержащего 10 мкл реагента RB (RB - сыворотка человека, лишенная фактора В с сохранением активностей остальных компонентов и факторов комплемента, получаемая, например, прогреванием ее в течение 30 мин при 50°С [2]) и анализируемую пробу, содержащую фактор В с неизвестной активностью. После инкубации в термостате в течение 1 ч при 37°С, двукратной отмывки фосфатным буфером, pH 7,4, содержащим 0,15 М NaCl и 0,05% твин-20 и осушения планшета в каждую лунку вносят по 100 мкл конъюгата пероксидазы с антителами против компонента С3 человека в том же буфере в подобранном разведении. После инкубации в термостате в течение 1 ч при 37°С двукратной отмывки с детергентом и осушения планшета в каждую лунку вносят по 100 мкл субстратного буфера (3,3',5,5'-тетраметилбензидин в 15 мл цитратно-фосфатного буфера, pH 5,0, и 50 мкл 3% перекиси водорода). После 15-30 мин инкубации в темноте реакцию останавливают внесением в каждую лунку 50 мкл 14% серной кислоты. Результаты реакции учитывают с помощью спектрофотомегра с вертикальным лучом измерением светопоглощения при 450 нм. Функциональную активность препарата фактора В рассчитывают по стандартной кривой (фиг.1).
Пример 2. Набор для определения функциональной активности фактора В. Набор содержит плоскодонную микропанель с сорбированным лизоцимом, реагент RB (сыворотку крови человека, лишенную активности фактора В), конъюгат пероксидазы с антителами к компоненту С3 комплемента человека, субстратный буфер и донорскую сыворотку крови в качестве стандарта. Данный набор используется в соответствии с примером 1.
Из приведенных результатов следует, что измеряемая оптическая плотность линейно зависит от концентрации активного фактора В с коэффициентом корреляции
R2=0,995, что позволяет достоверно определять функциональную активность фактора В от 0,6 мкг/мл описанным способом с использованием описанного набора. Достоверное определение функциональной активности фактора В по способу прототипу начиналось от 2 мкг/мл.
ЛИТЕРАТУРА
1. Козлов Л.В., Романов С. В., Дьяков В.Л., Лахтин В.М. Способ определения функциональной активности фактора В комплемента человека. Патент РФ №2232993. 20.07.2004.
2. Козлов Л.В., Соляков Л.С. Возможность участия зимогенных форм факторов В и D в активации альтернативного пути системы комплемента. Биоорганическая химия. 1982. Т.8. №3. С.342-348.
Изобретение относится к медицинской иммунологии, а именно к способам определения функциональной активности факторов комплемента в сыворотке крови человека при диагностике ряда заболеваний и в биологических препаратах. Сущность изобретения состоит в том, что в лунках микропанели сорбируют лизоцим как активатор альтернативного пути комплемента, затем вносят раствор, содержащий реагент RB, и анализируемую пробу, содержащую фактор В комплемента человека с неизвестной активностью. Проводят инкубацию в присутствии ионов Mg2+ и в отсутствие ионов Са2+, а затем вносят конъюгат фермента с антителами против компонента С3 человека и субстрат этого фермента, расчет активности фактора В проводят по количеству образовавшегося продукта ферментативной реакции. Набор для определения функциональной активности фактора В комплемента человека содержит плоскодонную микропанель с сорбированным лизоцимом, реагент RB (сыворотку крови человека, лишенную активности фактора В), конъюгат пероксидазы с антителами к компоненту СЗ комплемента человека, субстратный буфер и донорскую сыворотку крови в качестве стандарта. Способ обладает хорошей воспроизводимостью результатов и отсутствием необходимости использования труднодоступных высокоочищенных препаратов активаторов альтернативного пути, плохо сохраняющих свою активирующую способность. 2 с.п. ф-лы, 1 ил.
1. Способ определения функциональной активности фактора В комплемента человека, предусматривающий сорбцию в лунках микропанели активатора альтернативного пути комплемента, внесение раствора, содержащего реагент RB, и анализируемой пробы, содержащей фактор В комплемента человека с неизвестной активностью, инкубирование в присутствии ионов Mg2+ и в отсутствие ионов Са2+ выливание содержимого лунок, а затем последовательное внесение конъюгата фермента с антителами против компонента СЗ человека и субстрата этого фермента и проведение расчета активности фактора В по количеству образовавшегося продукта ферментативной реакции, отличающийся тем, что в качестве активатора альтернативного пути комплемента используют лизоцим.
2. Набор для определения функциональной активности фактора В комплемента человека, характеризующийся тем, что он содержит плоскодонную микропанель с сорбированным лизоцимом, реагент RB, конъюгат фермента с антителами к компоненту СЗ комплемента человека, субстратный буфер и стандарт с известной активностью фактора В.
| СПОСОБ ОПРЕДЕЛЕНИЯ ФУНКЦИОНАЛЬНОЙ АКТИВНОСТИ ФАКТОРА B КОМПЛЕМЕНТА ЧЕЛОВЕКА | 2003 |
|
RU2232993C1 |
| J GREENBLATT et al Activation of the alternate complement pathway by peptidoglycan from streptococcal cell wall., Infect Immun | |||
| Чугунный экономайзер с вертикально-расположенными трубами с поперечными ребрами | 1911 |
|
SU1978A1 |
| М.О.OGUNDELE A novel anti-inflammatory activity of lysozyme: modulation of serum complement activation, Mediators of Inflammation, 7, 363-365 (1998) | |||
| JS SUNDSMO, LM | |||
Авторы
Даты
2009-11-27—Публикация
2008-09-30—Подача