Изобретение относится к медицинской иммунологии, а именно к способам определения функциональной активности факторов комплемента в сыворотке крови человека при диагностике ряда заболеваний и в биологических препаратах.
Наиболее перспективным из современных методов определения белков сыворотки крови является метод иммуноферментного анализа благодаря своей чувствительности, избирательности и возможности автоматизации аналитического процесса. Однако имеющиеся на сегодня методы иммуноферментного анализа белков комплемента позволяют определять лишь их содержание как антигена. Тем не менее, наиболее информативным является оценка функциональной активности этих белков, которая и характеризует развитие патологического процесса. Что касается определения функциональной активности фактора В комплемента, то практически единственным является гемолитический метод [1] определения активности В, проявляющейся в активации системы по альтернативному пути, не отличающийся высокой степенью воспроизводимости и неохотно используемый клиницистами из-за трудностей, связанных с приготовлением гемолитической системы на основе эритроцитов кролика.
Задачей заявленного изобретения является разработка способа, позволяющего определять функциональную активность фактора В альтернативного пути системы комплемента человека на основе иммуноферментного метода.
Поставленная задача достигается путем разработки способа определения, который предусматривает сорбцию в лунках микропланшета активатора альтернативного пути комплемента, выбранного из ряда: иммуноглобулин А, иммуноглобулин G, компонент С3, липополисахарид, затем внесение в лунки микропланшета раствора, содержащего реагент RB (сыворотки крови человека, лишенной активности фактора В), и анализируемой пробы, содержащей фактор В комплемента человека с неизвестной активностью, проведение инкубации в присутствии ионов Mg2+ и в отсутствие ионов Са2+ (в ходе которой происходит формирование С3-конвертазы (С3bВb) на сорбированном активаторе альтернативного пути в количествах, зависящих от концентрации функционально активного определяемого фактора В, а также активация этой конвертазой компонента С3 и ковалентное связывание последнего на сорбированном активаторе. Таким образом, количество связавшегося С3 зависит от количества С3-конвертазы, т.е. количества определяемого фактора В. Количество ковалентно связавшегося в результате активации компонента С3 определяют по продукту ферментативной реакции с помощью антител к С3-фракции иммуноглобулинов G, конъюгированных с ферментом. Тем самым достигается определение функциональной активности фактора В иммуноферментным методом, пригодным для стандартизации.
Техническим результатом заявленного изобретения является разработка упрощенного способа определения функциональной активности фактора В комплемента человека, обладающего хорошей воспроизводимостью результатов и отсутствием необходимости использования таких плохо сохраняемых и трудно стандартизуемых компонентов, какими являются эритроциты.
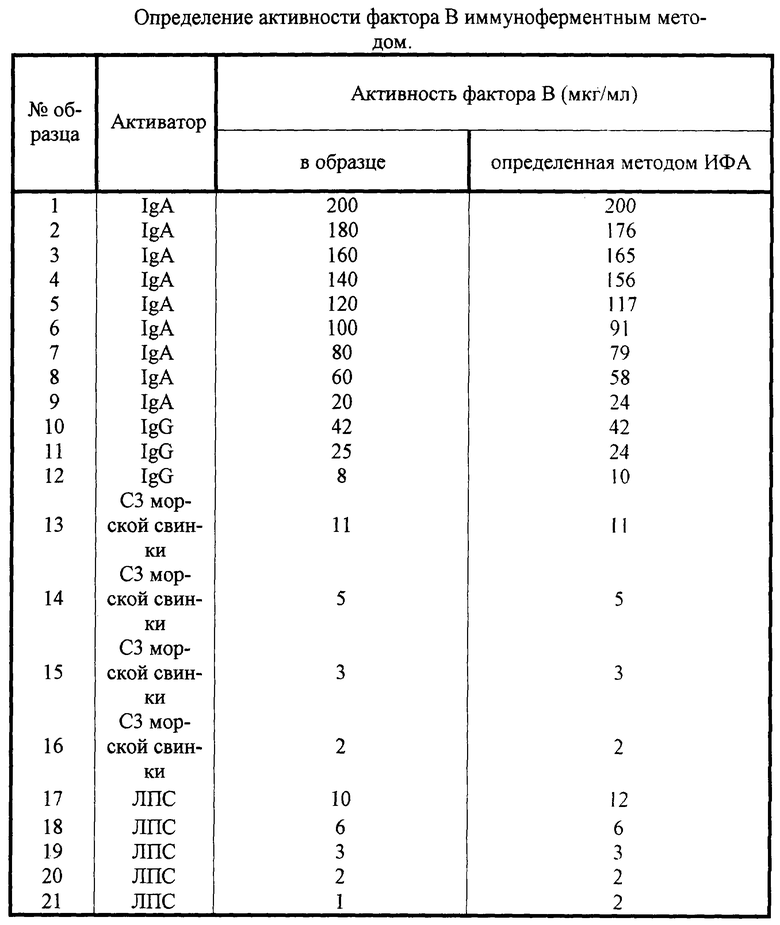
Пример 1. Определение функциональной активности препарата фактора В. Растворяют активатор альтернативного пути комплемента - иммунохимически чистый IgA в 0,05 М натрий-карбонатном буфере, рН 9,5, в концентрациях 10-100 мкг/мл и вносят по 100 мкл раствора в каждую лунку плоскодонного полистиролового 96-луночного планшета. Закрывают крышкой и оставляют на ночь при 4°С. Три раза отмывают планшет вероналовым буферным раствором, рН 7,4, содержащим 0,15 М NaCl, 10 мМ этиленгликоль-бис(β-аминоэтиловый эфир)-N,N,N’,N’- тетрауксусную кислоту и 5 мМ MgCl2 (Mg-EGTA), заливая по 150 мкл в каждую лунку, затем планшет осушают путем вытряхивания остатка жидкости. В лунки планшета ряда вносят по 100 мкл раствора Mg-EGTA, содержащего 10 мкл реагента RB (RB - сыворотка человека, лишенная фактора В с сохранением активностей остальных компонентов и факторов комплемента, получаемая, например, прогреванием ее в течение 30 мин при 50°С) и анализируемую пробу, содержащую фактор В с неизвестной активностью. После инкубации в термостате в течение 1 ч при 37°С, двукратной отмывки фосфатным буфером, рН 7,4, содержащим 0,15 М NaCl и 0,05% твин-20, и осушения планшета в каждую лунку вносят по 100 мкл конъюгата пероксидазы с антителами против компонента С3 человека в том же буфере в подобранном разведении. После инкубации в термостате в течение 1 ч при 37°С, двукратной отмывки с детергентом и осушения планшета в каждую лунку вносят по 100 мкл субстратного буфера (10 мг ортофенилендиамина в 25 мл цитратно-фосфатного буфера, рН 5,0, и 50 мкл 3% перекиси водорода). После 30 мин инкубации в темноте реакцию останавливают внесением в каждую лунку 50 мкл 14% серной кислоты. Результаты реакции учитывают с помощью спектрофотомегра с вертикальным лучом измерением светопоглощения при 492 нм. Функциональную активность препарата фактора В рассчитывают по стандартной кривой. Этим методом проведено определение активности фактора В в образцах с известным содержанием фактора В. Полученные результаты приведены в таблице.
Пример 2. Определение функциональной активности препарата фактора В проводят аналогично примеру 1, но в качестве активатора альтернативного пути используют иммуноглобулин G. Полученные результаты приведены в таблице.
Пример 3. Определение функциональной активности препарата фактора В проводят аналогично примеру 1, но в качестве активатора альтернативного пути используют препарат компонента С3 морской свинки. Полученные результаты приведены в таблице.
Пример 4. Определение функциональной активности препарата фактора В проводят аналогично примеру 1, но в качестве активатора альтернативного пути используют липополисахарид (ЛПС - препарат клеточной стенки бактерий, пирогенал). Полученные результаты приведены в таблице.
Литература
1. Козлов Л.В., Соляков Л.С. Возможность участия зимогенных форм факторов В и D в активации альтернативного пути системы комплемента./Биоорганическая химия, 1982, т. 8, №3, с.342-348.
Изобретение относится к области медицинской иммунологии, а именно к способам определения функциональной активности факторов комплемента в сыворотке крови человека и может быть использовано при диагностике ряда заболеваний и в биологических препаратах. Сущность изобретения состоит в том, что в лунках микропланшета сорбируют активатор альтернативного пути комплемента, вносят раствор, содержащий реагент RB, и анализируемую пробу, содержащую фактор В комплемента человека с неизвестной активностью, проводят инкубацию в присутствии ионов Mg2+ и в отсутствие ионов Са2+, вносят конъюгат фермента с антителами против компонента С3 человека и субстрат этого фермента, расчет активности фактора В проводят по количеству образовавшегося продукта ферментативной реакции. Техническим результатом является разработка способа, позволяющего определять функциональную активность фактора В альтернативного пути системы комплемента человека. 1 табл.
Способ определения функциональной активности фактора В комплемента человека, отличающийся тем, что сорбируют в лунках микропланшета активатор альтернативного пути комплемента, выбранный из ряда иммуноглобулин А, иммуноглобулин G, компонент С3, липополисахарид, затем в лунки микропланшета вносят раствор, содержащий реагент RB, и анализируемую пробу, содержащую фактор В комплемента человека с неизвестной активностью, проводят инкубацию в присутствии ионов Mg2+ и в отсутствие ионов Са2+, выливают содержимое лунок, а затем вносят конъюгат фермента с антителами против компонента С3 человека и субстрат этого фермента, после чего проводят расчет активности фактора В по количеству образовавшегося продукта ферментативной реакции.
| КОЗЛОВ Л.В | |||
| и др | |||
| Возможность участия зимогенных форм факторов В и D в активации альтернативного пути системы комплемента | |||
| Биоорганическая химия | |||
| Устройство для видения на расстоянии | 1915 |
|
SU1982A1 |
| US 6087120, 11.07.2000 | |||
| WO 00/21559, 20.04.2000 | |||
| NIEMANN M.A | |||
| et al | |||
| The principal site of glycation of human complement factor B, Biochem J | |||
| Циркуль-угломер | 1920 |
|
SU1991A1 |
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
Авторы
Даты
2004-07-20—Публикация
2003-04-09—Подача