Изобретение относится к медицине и предназначено для использования в сердечнососудистой хирургии при стентировании артерий.
Известно гибридное покрытие, состоящее из двух слоев, первый - из трех компонентов полимерной основы, сшивающего вещества и паклитакселя (таксола), и второго слоя - гепарина. (Патент США №6231600, М.кл. A61F 2/06, 1999 г.).
Недостатком известного покрытия является сложная структура, которая имеет два слоя, первый слой покрытия состоит из трех компонентов: полимера, активного вещества и сшивающего агента, т.е. тип полимера не позволяет включить препарат прямо в полимерную матрицу без использования дополнительного сшивающего агента.
Наиболее близким техническим решением является двухслойное полимерное покрытие с активным веществом паклитакселем. Первый слой покрытия состоит из смеси двух полимеров: полилактида полиэтиленоксида (PLA-PEO) - это быстро разрушающийся гидрофильный материал. Второй слой - медленно разрушающийся гидрофобный материал, состоящий из смеси полилактида и поликапролактона (PLA-PCL), а в качестве активного вещества применяют таксол (паклитаксел), подавляющий развитие рестеноза после пластических операций на сосудах. (Патент США №6258121 В1, М. кл. A61F 2/06, 1999 г.)
Недостатками известного покрытия являются использование в качестве биосовместимого покрытия полимера молочной кислоты (полилактида), у которого при гидролизе полимерной цепи in vivo происходит высвобождение мономеров молочной кислоты, сопровождающееся существенным закислением тканей (сдвиг рН 3,2-3,4). Полилактид уступает многим синтетическим полимерам по теплостойкости, при нагревании свыше 50°С изделия из полилактида деформируются, и, как следствие этого, они не могут быть подвергнуты стерилизации с применеием тепловых методов. Полиактид подвергается гидролизу в жидких средах, поэтому время его резорции in vivo исчисляется небольшим периодом 10-12 суток. Для повышения прочностных, температурных и биосовместимых свойств полилактид подвергают модификации с добавлением полигликолиевой кислоты и других технологических добавок. Это приводит к тому, что покрытие является сложным.
Применение цитостатического препарата паклитаксель (таксола) является дорогостоящим из-за получения его из экзотического сырья.
Задачей предлагаемого изобретения является создание более простого покрытия стента, обладающего биосовместимостью и гемосовместимостью, оптимальными физико-механическими свойствами, а также способностью медленно биорезорбироваться in vivo без образования токсичных продуктов и негативных реакций со стороны стенки сосуда в процессе использования.
Поставленная задача достигается тем, что в покрытии стента, включающем полимерный материал с активным антипролиферативным веществом, новым является то, что в качестве полимерного материала используют сополимер гидроксибутирата и гидоксивалериата кислот, а в качестве активного антипролиферативного вещества - рубомицин, количество сополимера гидроксибутирата и гидроксивалериата на один стент равно 2-15 мг/стент, и рубомицин включают в слой полимера в количестве 0,002-0,025 мг/стент.
В предлагаемом покрытии стента использован представитель нового класса термопластичных, биоразрушаемых и биосовместимых полимеров - полимеры гидроксипроизводных алкановых кислот (полигидроксиалкаонаты), а именно сополимер гидроксибутирата и гидроксивалериата и в качестве антипролиферативного вещества (цитостатического препарата) применен рубомицин - антибиотик антрациклинового ряда.
Сополимер гидроксибутирата и гидроксивалериата обладает следующими преимуществами:
- высокой биосовместимостью, включая гемосовместимость, так как не активирует ферментные системы крови и не вызывает агрегации тромбоцитов на поверхности;
- способностью не гидролизоваться в жидких средах, так как деградация данного сополимера является истинно биологической и происходит клеточным и гуморальными путями, образующиеся при этом мономеры гидроксибутирата и гидроксивалериата не вызывают резкого закисления тканей и, следовательно, выраженной воспалительной реакции;
- скорости биорезорбции сополимера значительно ниже, чем у полилактида, и поэтому покрытие стента in vivo может функционировать до 120 суток и более. Описание используемого сополимера гидроксибутирата и гидроксивалериата и примеры его получения следующие. Сополимер гидроксибутирата и гидроксивалериата (или другое название- гидроксимасляной и гидроксивалериановой кислот) - перспективный представитель семейства полигидроксиалканаотов (ПГА) - синтезируется микроорганизмами. Это химическое соединение (не два вещества!), образованные внутриклеточно в результате сополимеризации двух мономеров (гидрокси-бутирата и гидрокси-валериата); химическая формула:
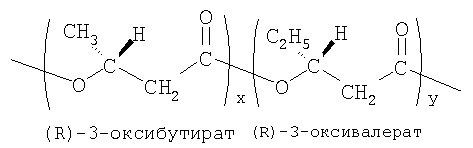
Способ синтеза сополимеров защищен патентом РФ 2051968 «Способ получения гетерополимера β-оксимасляной и β-оксивалериановой кислот». 1996. Волова Т.Г., Калачева Г.С., Константинова В.М., и опубликован в статье «Синтез сополимеров полигидроксибутирата и полигидроксивалерата поли(3ГБ/3ГВ) бактериями Ralstonia eutropha» в журнале «Микробиология», 2005. Т.74, №1, С.63-69. / Волова Т.Г., Калачева Г.С.
Получение сополимеров гидоксибутирата и гидроксивалериата [поли(3ГБ/3ГВ)] осуществляется микробиологическим способом. Для этого бактерии Ralstonia eutropha B5786 культивировали на минеральной солевой среде с использованием в качестве источника углерода и энергии при автотрофном режиме СO2 и Н2, при гетеротрофном - фруктозу. Бактерии культивировали в периодическом режиме в лабораторном аппарате объемом до 10 литров при коэффициенте заполнения 0.3, оснащенном турбинной мешалкой открытого типа с частотой 1000 об/мин. Исходное соотношение компонентов в газовой смеси в контроле составляло для СО2, О2 и Н2 соответственно как 1:2:6 по объему. При гетеротрофных условиях подачу фруктозы осуществляли перистальтическим насосом-дозатором (при текущей концентрации фруктозы в культуре не выше 10 г/л). Для максимальной аккумуляции ПГА применяли разработанный режим культивирования бактерий с лимитированием роста по азоту на первом этапе и в без азотной среде - на втором, при рН 7.0 и температуре 30°С [Волова Т.Г., Калачева Г.С. Способ получения полимера β-оксимасляной кислоты. Патент РФ №2051967, 1996]. Для включения в ПГА в качестве сополимера гидрокси-валериата в среду вносили добавки валерата. Содержание полимера в биомассе и химический состав мономеров определяли хроматографией метиловых эфиров жирных кислот после метанолиза проб сухой биомассы на хроматомасс-спектрометре GSD plus (Hewlett Packard, USA). Вследствие токсичности валерата для культуры повышение фракции 3ГВ в сополимере увеличением дозы валерата оказалось невозможным. Выявлено, что при увеличение разовой подачи валерата в культуру в концентрации свыше 2.0 г/л наблюдается выраженное ингибирование роста бактерий и синтеза ПГА в целом. Для повышения включения фракции 3ГВ в поли(3ГБ/3ГВ) с учетом токсичности для культуры R.eutropha B5786 валерата в концентрации, свыше 2 г/л, разработаны режимы культивирования бактерий с дробной подачей валерата. Сочетанием количества добавок валерата в культуру (1, 2, 3 и более) и последующего времени культивирования найдены условия, при которых возможен синтез ПГА с варьированием соотношения мономеров 3ГБ/3ГВ в широких пределах, от 9:1 до 1:9 (мол%). Реализован процесс выращивания бактерий, обеспечивающий высокий общий выход сополимера (свыше 80-85%) с варьированием соотношения мономеров в нем.
Результаты потенциальных областей применения сополимеров гидроксибутирата и гидроксивалериата для получения специальных изделий опубликованы нами в следующих работах.
Волова Т.Г., Некрасов Ю.П., Шишацкая Е.И., Пузырь А.П., Гордеев С.А. Характеристика изделий на основе полиоксиалканоатов - разрушаемых природных полиэфиров // Пластические массы. 2003, №3. С.6-8.
Шишацкая Е.И., Гордеев С.А., Волова Т.Г. Исследование свойств полигидроксиалканоатов, перспективных для получения пористых матриц // Перспективные материалы. 2004. №5. С.40-44.
Гордеев С.А., Шишацкая Е.И., Волова Т.Г. Получение и исследование ориентированных волокон из сополимеров поли(гидроксибутирата/гидроксивалерата) // Перспективные материалы. - 2005. - №.3. - С.50-55.
Шишацкая Е.И., Жемчугова А.В., Волова Т.Г. Исследование биоразрушающихся полигидроксиалканоатов в качестве носителя противоопухолевых препаратов // Антибиотики и химиотерапия. - 2005. - №2-3. - С.3-14.
Волова Т.Г., Шишацкая Е.И., Гордеев С.А. Характеристика ультратонких волокон, полученных электростатическим формованием термопластичного полиэфира [поли(гидроксибутирата/гидроксивалерата)] // Перспективные материалы. - 2006. - №3. - С.25-29.
Шишацкая Е.И., Горева А. Микрочастицы из биорарушаемого полиоксибутирата в качестве матрикса для депонирования рубомицина // Перспективные материалы, - 2006. - №.4 - С.65-70.
Шишацкая Е.И. Клеточные матриксы из резорбируемых полигидроксиалканоатов // Клеточная трансплантология и тканевая инженерия. - 2007. - T.II, №2. - С.68-76.
Свойства семейства ПГА, в том числе сополимеров гидроксибутирата и гидроксивалериата, изучены в различных аспектах и широко опубликованы в следующих работах.
На отсутствие цитотоксичности.
Шишацкая Е.И., Еремеев А.В., Гительзон И.И., Сетков Н.А., Волова Т.Г. Исследование цитотоксичности полиоксиалканоатов в культуре животных клеток // ДАН. 2000. Т.374, №4. С.561-564.
Шишацкая Е.И., Есимбекова Е.Н., Волова Т.Г., Калачева Г.С., Кратасюк В.А. Гигиеническая оценка полиоксиалканоатов - природных полиэфиров нового поколения // Гигиена и санитария. 2002, №4. С.59-63.
Шишацкая Е.И., Еремеев А.В. Гительзон И.И. Исследование свойств биодеградируемых полимеров (полиоксиалканоатов) в культуре животных клеток // Перспективные материалы. 2001. №3. С.40-47.
Токсикологические исследования.
Шишацкая Е.И., Волова Т.Г., Гительзон И.И. Токсикологические исследования полиоксиалканоатов в эксперименте in vivo II ДАН. 2002. Т.383, №4. С.565-567
Шишацкая Е.И., Волова Т.Г., Попова Т.Г. Исследование биологических свойств полиоксиалканоатов в хроническом эксперименте in vivo // Медицинская техника. 2002, №4. С.29-32.
Благоприятная тканевая реакция на сополимеры гидроксибутирата и гидроксивалериата.
Шишацкая Е.И., Волова Т.Г., Ефремов С.Н., Пузырь А.П., Могильная О.А. Реакция тканей на биодеградируемые шовные нити из полиоксиалканоатов // Медицинская техника. 2002, №4. С.23-26.
Шишацкая Е.И., Горева А.Ю., Воинова О.Н., Волова Т.Г. Реакция тканей на имплантацию микрочастиц из резорбируемых полимеров при внутримышечном введении // Бюллетень экспериментальной биологии и медицины. - 2007. - №12. - С.635-639.
Результаты исследования биосовместимости.
Севастьянов В.И., Перова Н.В., Довжик И.А., Титушкин И.А., Немец Е.А., Беломестная З.М., Шишацкая Е.И., Волова Т.Г. Медико-биологические свойства полиоксиалканоатов - биодеградируемых бактериальных полимеров // Перспективные материалы. 2001. №5. С.46-55.
Пригодность для контакта с кровью.
Sevastianov V.I., Perova N.V., Shishatskaya E.I., Kalacheva G.S., Volova T.G. Production of purified polyhydroxyalkanoates (PHAs) for applications in contact with blood // J. Biomater. Sci. Polymer Edn. 2003. V.14, №10. Р.1029-1042.
Исследование разрушаемости сополимеров гидроксибутирата и гидроксивалериата в биологических средах, подтверждающие отсутствие гидролиза и закономерности медленного биоразрушения.
Волова Т.Г., Беляева О.Г., Плотников В.Ф., Пузырь А.П. Исследование биодеградации микробных полиоксиалканоатов // Прикладная биохимия и микробиология. 1998. Т.34, №5. С.539-543.
Шишацкая Е.И., Волова Т.Г., Гордеев С.А., Пузырь А.П. Биодеградация шовных нитей на основе полиоксиалканоатов в биологических средах // Перспективные материалы. 2002, №2. С.56-62.
Физические свойства.
Волова Т.Г., Плотников В.Ф., Шишацкая Е.И., Миронов П.В., Васильев А.Д. «Физико-химические свойства двухкомпонентных -[поли(3ГБ/3ГВ)] полигидроксиалканоатов» в журнале «Биофизика». 2004. Т.49., №6, С.1038-1046.
Примеры осуществления изобретения при указании количества используемых сополимеров гидроксибутирата и гидроксивалериата в интервале от 2 до 15 мг и количества рубомицина в интервале от 0,002 до 0,025 мг/стент следующие.
Пример 1.
Раствор сополимера гидроксибутирата и гидроксивалериата в дихлорметане (или хлороформе), содержащий рубомицин, наносят на поверхности стента, далее изделие высушивают в беспылевом боксе-ламинаре. Масса полимерного покрытия составляет 2 мг/стент, содержание рубомицина в покрытие - 0,002 мг/стент.
Пример 2.
Раствор сополимера гидроксибутирата и гидроксивалериата в дихлорметане (или хлороформе), содержащий рубомицин, наносят на поверхности стента, далее изделие высушивают в беспылевом боксе-ламинаре. Масса полимерного покрытия составляет 8 мг/стент, содержание рубомицина в покрытие - 0,012 мг/стент.
Пример 3.
Раствор сополимера гидроксибутирата и гидроксивалериата в дихлорметане (или хлороформе), содержащий рубомицин, наносят на поверхности стента, далее изделие высушивают в беспылевом боксе-ламинаре. Масса полимерного покрытия составляет 10 мг/стент, содержание рубомицина в покрытие - 0,018 мг/стент.
Пример 4.
Раствор сополимера гидроксибутирата и гидроксивалериата в дихлорметане (или хлороформе), содержащий рубомицин, наносят на поверхности стента, далее изделие высушивают в беспылевом боксе-ламинаре. Масса полимерного покрытия составляет 12 мг/стент, содержание рубомицина в покрытие - 0,020 мг/стент.
Пример 5.
Раствор сополимера гидроксибутирата и гидроксивалериата в дихлорметане (или хлороформе), содержащий рубомицин, наносят на поверхности стента, далее изделие высушивают в беспылевом боксе-ламинаре. Масса полимерного покрытия составляет 15 мг/стент, содержание рубомицина в покрытие - 0,025 мг/стент; вариант осуществления изобретения примера 5 является оптимальным.
При включении рубомицина в слой полимера в количестве меньше 0,002 мг/стент не обеспечивает подавление развития неоинтимы, а в количестве больше 0,025 мг/стент может иметь побочный токсический эффект.
В качестве полимерной основы (полимера) для получения покрытия стента используют одно вещество - сополимер гидроксибутирата и гидроксивалериата, который растворяют в дихлорметане или хлороформе, а затем вводят раствор рубомицина. Полученный гомогенный прозрачный раствор наносят на поверхность стента. Стент помещают в беспылевой бокс-ламинар при комнатной температуре. После испарения растворителя на поверхности стента образуется покрытие в виде пленки. Покрытие состоит из одногослоя из двух компонентов: один полимер и одно активное вещество.
В таблице приведены характеристики покрытий.
Предлагаемое изобретение поясняется фотографиями и графиком.
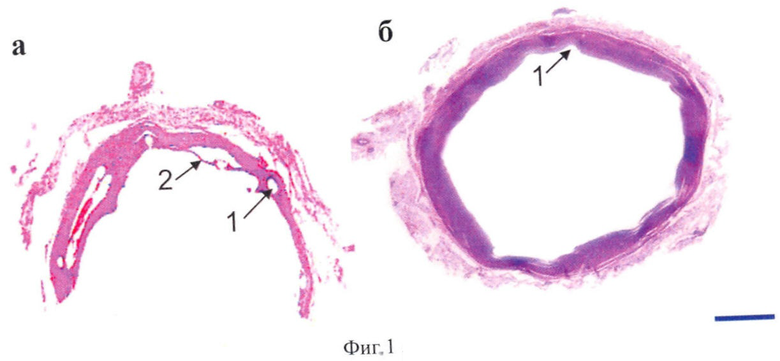
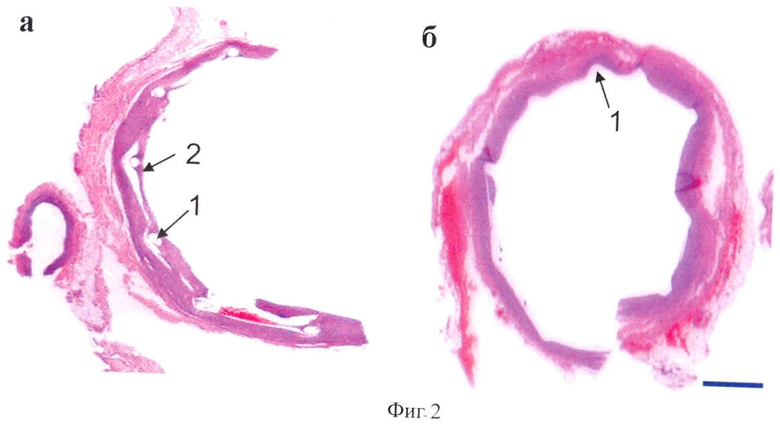
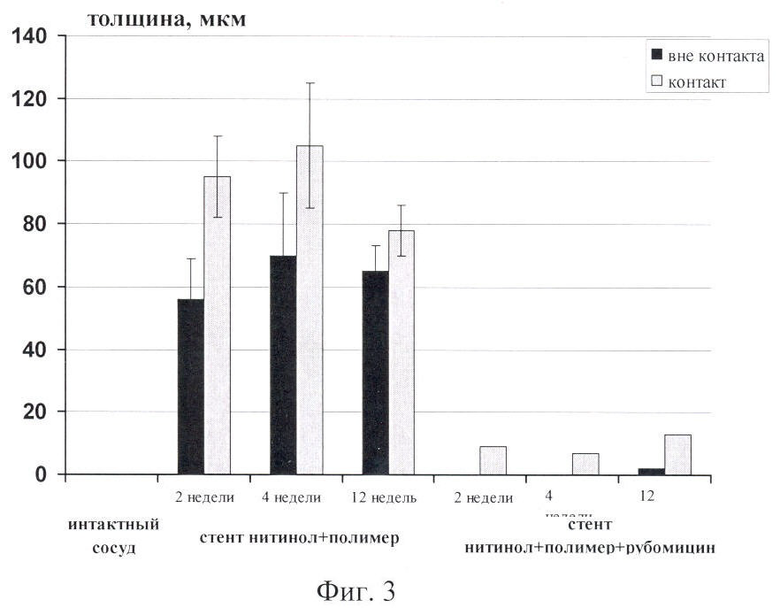
На фиг.1 изображена морфология фрагмента стенки сосуда через две недели после стентирования в месте контакта сосуда с полимерным покрытием (а) и стентом с полимерным покрытием, содержащем рубомицин (б): где 1 - отверстие от элемента стента, 2- неоинтима. Окраска - гематоксилин-эозин. Маркер - 1 мм; Фиг.2 - морфология фрагмента стенки сосуда через двенадцать недель после стентирования вместе контакта стенки сосуда со стентом с полимерным покрытием (а) и стентом с полимерным покрытием, содержащем рубомицин (б): где 1 - отверстие от элемента стента, 2-неоинтима. Окраска - гематоксилин-эозин. Маркер - 1 мм. Фиг.3 - динамика образования и толщина неоинтимы вокруг стента с полимерным покрытием и стентом с полимерным покрытием, содержащем рубомицин.
Техническим результатом является создание более простого покрытия стента, обладающего биосовместимостью и гемосовместимостью, с оптимальными физико-механическими свойствами, а также способностью медленно биорезорбироваться in vivo без образования токсичных продуктов и негативных реакций со стороны стенки сосуда в процессе использования.
Авторами получены высокоочищенные образцы полимеров для покрытия стентов, пригодные для биомедицинских применений, включая контакт с кровью.
| название | год | авторы | номер документа |
|---|---|---|---|
| ХИРУРГИЧЕСКОЕ ВОЛОКНО, СПОСОБ ЕГО ПОЛУЧЕНИЯ И ИЗДЕЛИЯ ИЗ НЕГО | 2010 |
|
RU2436595C1 |
| ХИРУРГИЧЕСКИЙ МАТЕРИАЛ (ВАРИАНТЫ) | 2010 |
|
RU2433836C1 |
| СПОСОБ ПОЛУЧЕНИЯ СОПОЛИМЕРА 3-ГИДРОКСИБУТИРАТА, 3-ГИДРОКСИВАЛЕРАТА И 4-ГИДРОКСИБУТИРАТА | 2014 |
|
RU2565815C1 |
| СПОСОБ ПОЛУЧЕНИЯ СОПОЛИМЕРА 3-ГИДРОКСИБУТИРАТА И 3-ГИДРОКСИГЕКСАНОАТА | 2014 |
|
RU2565819C1 |
| БИОЛОГИЧЕСКИ АКТИВНАЯ ПОЛИМЕРНАЯ МЕДИЦИНСКАЯ КОМПОЗИЦИЯ (ВАРИАНТЫ) | 2010 |
|
RU2447902C2 |
| ГЕРБИЦИДНОЕ СРЕДСТВО ДЛИТЕЛЬНОГО ДЕЙСТВИЯ ДЛЯ ГРУНТОВОГО ПРИМЕНЕНИЯ | 2012 |
|
RU2494621C1 |
| СПОСОБ ПОЛУЧЕНИЯ СОПОЛИМЕРОВ МИКРОБНОГО ПРОИСХОЖДЕНИЯ, ОБРАЗОВАННЫХ МОНОМЕРАМИ 3-ГИДРОКСИМАСЛЯНОЙ И 4-ГИДРОКСИМАСЛЯНОЙ КИСЛОТ | 2015 |
|
RU2582255C1 |
| ШТАММ БАКТЕРИЙ Cupriavidus eutrophus ВКПМ В-10646 - ПРОДУЦЕНТ ПОЛИГИДРОКСИАЛКАНОАТОВ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2010 |
|
RU2439143C1 |
| БИОЛОГИЧЕСКИ АКТИВНАЯ ПОЛИМЕРНАЯ МЕДИЦИНСКАЯ КОМПОЗИЦИЯ | 2023 |
|
RU2815508C1 |
| СПОСОБ МОДИФИКАЦИИ ПОВЕРХНОСТИ ЭНДОКАРДИАЛЬНЫХ ЭЛЕКТРОДОВ | 2010 |
|
RU2452516C1 |
Изобретение относится к медицине и предназначено для использования в сердечно-сосудистой хирургии при стентировании артерий. В покрытии стента, включающем полимерный материал с активным антипролиферативным веществом, в качестве полимерного материала используют сополимер масляной и валериановой кислот, а в качестве активного антипролиферативного вещества - рубомицин, количество сополимера масляной и валериановой кислот на один стент равно 2-15 мг/стент, рубомицин включают в слой полимера в количестве 0,002-0,025 мг/стент. Техническим результатом является создание более простого покрытия стента, обладающего биосовместимостью и гемосовместимостью, с оптимальными физико-механическими свойствами, а также способностью медленно биорезорбироваться in vivo без образования токсичных продуктов и негативных реакций со стороны стенки сосуда в процессе использования. 2 з.п. ф-лы, 3 ил., 1 табл.
1. Покрытие стента, включающее полимерный материал с активным антипролиферативным веществом, отличающееся тем, что в качестве полимерного материала используют сополимер гидрокси-бутирата и гидрокси-валериата, а в качестве активного антипролиферативного вещества - рубомицин.
2. Покрытие стента по п.1, отличающееся тем, что количество сополимера гидрокси-бутирата и гидрокси-валериата на один стент равно 2-15 мг.
3. Покрытие стента по п.1, отличающееся тем, что рубомицин включают в слой полимера в количестве 0,002-0,025 мг/стент.
| US 6258121 B1, 10.07.2001 | |||
| US 6702850 B1, 09.03.2004 | |||
| RU 2004124387 А, 10.06.2005. |
Авторы
Даты
2010-01-27—Публикация
2008-08-19—Подача