Изобретение относится к медицине, а именно к медицинской композиции, предназначенной для депонирования и доставки лекарственных средств.
Известно парабульбарное введение этамзилата 12,5% 0,5 мл №5, дексаметазона 0,4% 0,5 мл с гепарином 750-1000 ЕД [RU №2416402, A61K 31/205, A61K 31/341, A61K 31/433, A61K 31/573, A61K 31/616, A61K 31/727, A61K 38/43, А61Р 27/02, опубл. 21.01.2010 г.] для комбинированной терапии острых тромбозов вен сетчатки.
Недостатком данного изобретения является отсутствие пролонгированного действия.
Известно применение этамзилата в качестве лекарственного агента при лечении отита и ринита [ЕР 3167881, A61K 31/185, A61K 31/205, А61Р 19/00, А61Р 19/04, А61Р 19/02 А61Р 21/00, А61Р 27/16, опубл. 28.08.2019 г.].
Недостатком данного изобретения является отсутствие пролонгированного и/или комбинированного действия.
Известно локальное введение этамзилата [ЕР 3 572 079, A61K 31/185, А61Р 31/22, опубл. 27.11.2019 г.] с использованием гепарансульфата для проникновения в клетки для лечения вируса герпеса, возникающего на слизистых/эпителиальных поверхностях, таких как генитальный и герпетический стромальный кератит, особенно при лечении состояния, вызванного лабиальным герпесом.
Недостатком данного изобретения является отсутствие пролонгированного действия.
Известна пористая биологически активная полимерная композиция 3-полигидроксибутирата с поликапролактоном или полиэтиленгликолем в смеси с протеолитическим ферментом и антимикробным веществом [RU №2318535, А61K 38/43, опубл. 10.03.2008 г.], используемая в качестве раневых покрытий, покрытий шовных волокон, полимерных пленок.
Недостатком данной композиции является использование 3-полигидроксибутирата высококристалличного - полимера с низкими технологическими свойствами, для него характерны низкая ударная прочность, жесткость и повышенная хрупкость изделий.
Известна композиция для получения микрочастиц, получаемая из полимера группы альфа-гидроксикислот (типа полигидроксимасляной, поликапролактона) и сложного детергента, одна часть которого связана с полимером, а также адсорбированного на поверхности микрочастиц комплекса, состоящего из биологически активной молекулы и этого же детергента или другого детергента [RU №2257198, F61K 9/16, опубл. 27.08.2004 г.]. Микрочастицы предназначены для депонирования и доставки биологически активных соединений, антител, лекарственных средств. Микрочастицы характеризуются улучшенной адсорбцией на их поверхности биологически активных молекул.
Недостатком композиции является сложная структура микрочастиц, использование высококристалличного поли-3-гидроксибутирата для их получения.
Известна композиция из гомополимера поли-3-гидроксибутирата и полиамида для получения пленок с депонированным антисептиком фурацилином. [А.А. Ольхов, Ю.Н. Панкова, Р.Ю. Косенко. Матрицы контролируемого высвобождения лекарственных веществ на основе композиций полиамид - полигидроксибутират. Химико-фармацевтический журнал. - 2018. - Т. 52, №1, стр. 47-53].
Недостаток данной композиции заключается в узкой области действия, т.к. композиция содержит только одно биологически активное вещество и предназначена только для нанесения пленочных покрытий.
Известна композиция из сополимера поли-3-гидроксибутирата и поли-3-гидроксивалерата (включение гидроксивалерата 5 мол.%) для получения плавлением различных предметов (нитей, трубочек, пленок, прутков и палочек), обладающих желтым цветом и запахом, полученная в результате добавления к сополимеру термостабильных соединений солей сульфитов в виде растворов или кристаллов [US №5525658, С08К 3/30, опубл. 11.06.1996 г.].
Недостаток композиции - остаточное присутствие в изделиях солей сульфитов, которые снижают биоразрушаемость сополимера.
Известна композиция для покрытия стента [RU №2380059, Е61А 2/06, опубл. 27.01.2010 г.], включающая полимерный материал с активным антипролиферативным веществом, где в качестве полимерного материала используют сополимер поли-3-гидроксибутирата и поли-3-гидроксивалериата, а в качестве активного антипролиферативного вещества - антибиотик рубомицин гидрохлорид.
Недостаток композиции - узкая область действия, т.к. композиция содержит только одно биологически активное вещество и предназначена только для нанесения пленочных покрытий.
Известна композиция для получения микрочастиц с биологически активным веществом [Муруева А.В., Шершнева A.M., Немцев И.В. и др. Конъюгация коллагена с модифицированными карбоксилом микрочастицами из поли-3-гидроксибутирата: подготовка, характеристика и оценка in vitro. Journal of Polymer Research. - 2022. - T. 29, №324], где в качестве полимерного материала используют гомополимер поли-3-гидроксибутират, а в качестве активного вещества - коллаген 1-го типа.
Недостаток композиции - узкая область действия, т.к. композиция содержит только одно биологически активное вещество, ковалентно пришитое на поверхности микрочастиц.
Наиболее близким техническим решением является композиция для получения микрочастиц [Владимирова А.В. Функциональные характеристики микросферических носителей биологически активных веществ для реконструктивных технологий мягких тканей [Электронный ресурс]: магистерская диссертация: 06.04.01 / А.В. Владимирова. - Красноярск: СФУ, 2018.] содержащая, по меньшей мере, один полимер, в частности гомополимер поли-3-гидроксибутират и, по меньшей мере, одно биологически активное вещество, выбранное из группы антисептиков, состоящей из бриллиантового зеленого, фурацилина и мирамистина, причем полимер и, по меньшей мере, одно биологически активное вещество растворено, по меньшей мере, в одном растворителе.
Недостаток данного технического решения - композиция узкого действия и применения, так как композиция содержит только одно антисептическое вещество из трех возможных.
Техническим результатом является разработка биологически активной полимерной медицинской композиции широкого спектра действия и применения, обладающей биосовместимостью, оптимальными физико-химическими свойствами, а также способностью медленно биорезорбироваться in vivo без образования токсичных продуктов и негативных реакций в процессе использования.
Технический результат достигается тем, что в биологически активной полимерной медицинской композиции в виде микрочастиц, включающей полимер поли-3-гидроксибутират, и, по меньшей мере, одно биологически активное вещество, новым является то, что композиция содержит биологически активное вещество, выбранное из группы антисептиков или гемостатиков, состоящей из бриллиантового зеленого или этамзилата, и дополнительно содержит желатин, наполненный наночастицами серебра, при следующем соотношении компонентов, мас. %: полимер поли-3-гидроксибутират 20-40; биологически активное вещество антисептик или гемостатик 10-20; желатин, наполненный наночастицами серебра 5-10; растворитель - остальное.
А также тем, что выполнена в виде микрочастиц.
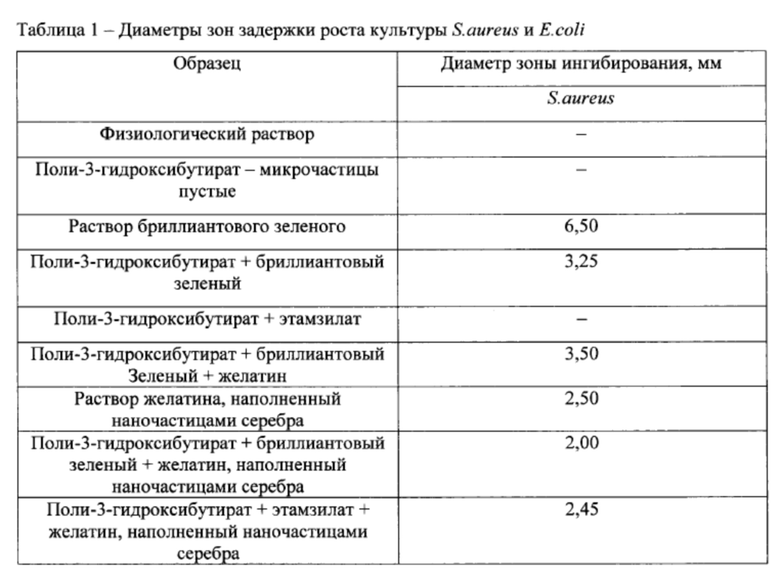
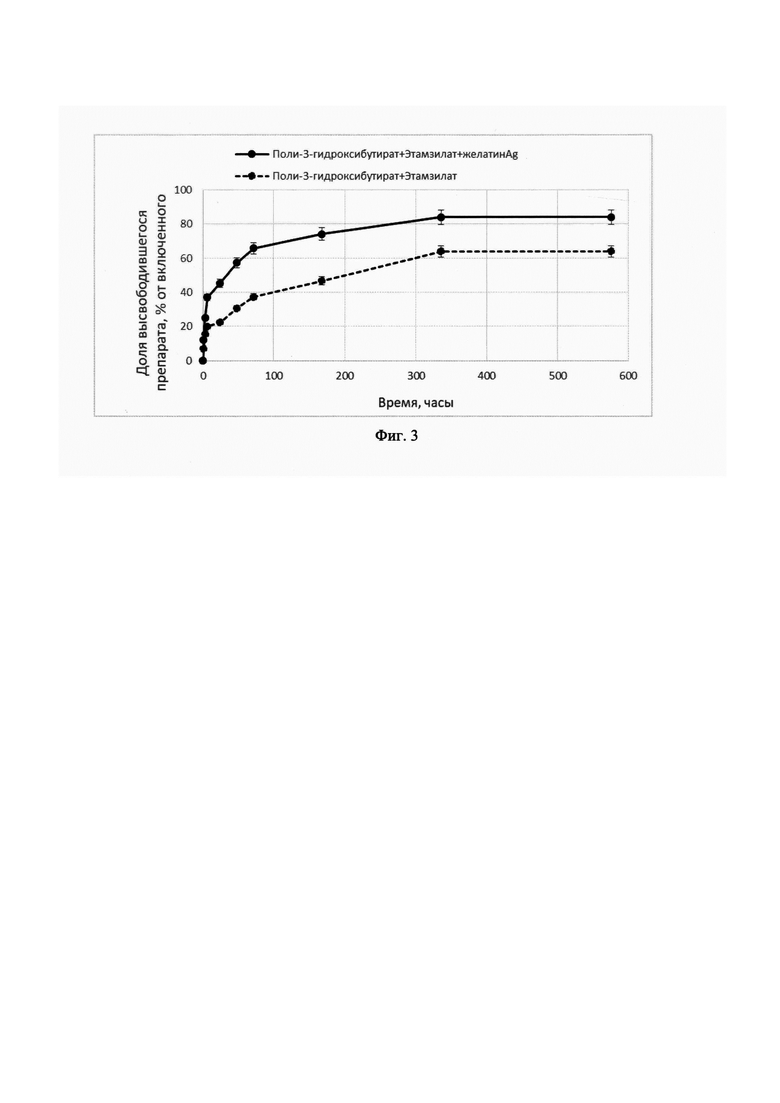
Сущность изобретения поясняется чертежами. На фиг. 1 представлены снимки сканирующего электронного микроскопа (СЭМ) микрочастиц, полученных механическим перемешиванием эмульсии из композиции, содержащей полимер поли-3-гидроксибутират, нагруженных антисептиком в концентрации 10 мас. %: без поверхностной модификации (1); после реакции карбоксилирования (2); после присоединения желатина (3); после присоединения желатина, наполненного наночастицами серебра (4) (Маркер - 40 и 50 мкм). На фиг. 2 представлены профили высвобождения антисептика из микрочастиц, полученных из композиции, содержащей полимер поли-3-гидроксибутират и 10% антисептика, а также поли-3-гидроксибутират, 10% антисептика и желатин; или поли-3-гидроксибутират, 10% антисептика и желатина, наполненного наночастицами серебра, в разные сроки наблюдения. На фиг. 3 представлены профили высвобождения гемостатика этамзилата из микрочастиц, полученных из композиции, содержащей полимер поли-3-гидроксибутират и 10% гемостатика, а также поли-3-гидроксибутират, 10% гемостатика и желатин, наполненный наночастицами серебра, в разные сроки наблюдения. В таблице 1 даны результаты, свидетельствующие о наличие бактериостатической эффективности действия разработанной биологически активной полимерной медицинской композиции в виде микрочастиц: значения диаметров зон ингибирования бактерий в ответ на внесение микрочастиц из композиции, содержащей полимер поли-3-гидроксибутират и 10% антисептика, а также 3-полигидроксибутират, 10% антисептика и желатин; или 3-полигидроксибутират, 10% антисептика и желатин, наполненный наночастицами серебра.
Получение и применение заявляемой биологически активной полимерной медицинской композиции иллюстрируется следующими вариантами примеров.
Для приготовления биологически активной полимерной медицинской композиции используют сополимер, полученный микробиологическим способом согласно Техническим условиям на сополимер (ТУ №2200-001-03533441-2004, рег. 14.12.2005, №068/003058) на опытном производстве Сибирского федерального университета, согласно техническим условиям на полимер поли-3-гидроксибутират (ТУ №2200-003-03533441- 2005 рег. 27.04.2004 №068/003057). Полимер синтезирован штаммом Cupriavidus eutropha ВКПМ В-10646 на сахарах [RU №2439143, C12N 1/20, С12Р 7/62, опубл. 10.01.2012]. Выделение и очистку сополимера из бактериальной биомассы осуществляют смесью дихлорметана или хлороформа с этанолом в соотношении 2:1 по объему. Полимер выделяют из экстракта, после его концентрирования на роторном испарителе Rotavapor R-210 (Швейцария) осаждением в изопропаноле. Для получения высокоочищенных образцов полимера проводят процедуру многократного перерастворения полимера и последующего осаждения. Полученный полимер высушивают при 40°С в бокселаминаре. Определение степени кристалличности сополимера осуществляют на рентгеноспектрометре D8 ADVANCE фирмы «Bruker» (Германия) (графитовый монохроматор на отраженном пучке), степень кристалличности (Сх) составляет 60%. Химический состав сополимера определяют на хроматомасс-спектрометре Agilent 5975Inert фирмы Agilent (США) после предварительного метанолиза пробы полимера. Температуру плавления образца определяют на дериватографе СТА - STA 449 Jupiter фирмы NETZSCH (Германия).
Характеристики полимера: средневесовая молекулярная масса Мв 570 кДа, полидисперсность D=2,6; степень кристалличности 76%, температура плавления и термической деградации, соответственно, 168,5 и 280°С.
Для приготовления биологически активной полимерной медицинской композиции используют полимер, синтезируемый, как описано выше. Раствор полимера в дихлорметане или хлороформе с концентрацией 2% готовят при температуре 38-40°С, после его охлаждения до комнатной температуры вносят 10% раствор биологически активного вещества из группы антисептиков или гемостатиков, состоящей из бриллиантового зеленого или этамзилата. Полученную полимерную композитную систему подвергают эмульгированию в растворе 1% поливинилового спирта (ПВС) и оставляют на сутки при постоянном механическом перемешивании на 750 об/мин на магнитной мешалке до полного испарения растворителя. Сформированные микрочастицы собирают центрифугированием, со скоростью 5000 об/мин, в течение 5 мин, промывают многократно дистиллированной водой и высушивают в сушильном шкафу при 37°С в течение 72 часов. Морфологию микрочастиц анализируют с применением сканирующей электронной микроскопии (СЭМ) на микроскопе ТМ-4000 (Hitachi, Япония). Напыление образцов платиной осуществляют в установке «Balzers CPD-030» (Германия). Величину включения препарата в полимерном матриксе определяют спектрофотометрически его исходных и остаточных концентраций в эмульсии на регистрирующем спектрофотометре Genesys 10S UV-Vis (Thermo Scientific, США). В зависимости от состава композиции, депонированного биологически активного вещества и типа поверхностно-активного вещества получают частицы со средним размером частиц от 50 мкм до 60 мкм с гладкой, пористой и слоистой поверхностью (фиг. 1), с различной скоростью оттока из полимерного матрикса в среду (фиг. 2, 3).
Полученные микрочастицы (МЧ) из поли-3-гидроксибутирата имели четко очерченную сферическую форму независимо от модификаций (фиг. 1). Было обнаружено, что проведение реакции карбоксилирования сильно влияет на поверхность микрочастиц. Микрочастицы без поверхностных модификаций имели гладкую поверхность, в то время как поверхность карбоксилированных микрочастиц была шероховатой с крупными порами. Это можно объяснить тем, что при проведении карбоксилирования происходит частичное разрушение полимерных цепей и увеличивается количество СООН-групп. Ковалентное присоединение желатина также изменяет микрочастицы - они становятся гладкими с четко заметными слоями. Следует отметить, что на поверхности некоторых микрочастиц видны отдельные кристаллы желатина.
На фиг. 2 видно, что высвобождение бриллиантового зеленого (БЗ) в модельную среду было активным во всех случаях и постепенно возрастало в течение месяца до 30% (масс.) для МЧ-БЗ и до 35 % (масс.) для МЧ-БЗ-желатин и МЧ-БЗ-желатин Ag. Следует отметить отсутствие «взрывного эффекта» выхода в системах с депонированным антисептиком без модифицированной поверхности, что является важным показателем качества полученной системы доставки. МЧ-БЗ имели относительно низкий показатель общего высвобождения лекарства, что можно объяснить гидрофобностью поли-3-гидроксибутирата и плотной упаковкой полимерных цепей в процессе затвердевания микрочастиц, в результате чего большая часть бриллиантового зеленого находится внутри частиц.
Характер профиля высвобождения антисептика in vitro (фиг. 2) показал, что в первой фазе высвобождения препарата из микрочастиц, поверхностно желатином и желатином, наполненным наночастицами серебра, наблюдается более активный выход, в отличие от частиц без белка. Так, в первые сутки было высвобождено около 15% лекарства для МЧ-БЗ, в то время как почти 30% было высвобождено за тот же период из МЧ-БЗ-желатин и МЧ-БЗ-желатинAg. Очевидно, что скорость высвобождения лекарства увеличилась вследствие изменения поверхностной структуры микрочастиц и возможным выходом бриллиантового зеленого ближе к поверхности частиц. То есть молекулы лекарства, расположенные близко к поверхности, очень легко покидают матрицу. Следующая фаза высвобождения бриллиантового зеленого (48-600 ч) определялась диффузионными механизмами, связанными с высвобождением лекарства из поверхностных структур микрочастиц.
Более активное высвобождение бриллиантового зеленого в системах с поверхностными модификациями ожидаемо и необходимо для реализации местного антисептического эффекта бриллиантового зеленого, так как инициация процесса заживления должна происходить только на уже обеззараженной раневой поверхности.
На фиг. 3 видно, что высвобождение этамзилата в модельную среду было активным во всех случаях и постепенно возрастало в течение месяца до 60% (масс.) для МЧ-этамзилат и до 80 % (масс.) для МЧ-этамзилат-желатинAg. Следует отметить отсутствие «взрывного эффекта» выхода в системах с депонированным гемостатиком без модифицированной поверхности, что является важным показателем качества полученной системы доставки.
Антимикробную активность микрочастиц из заявляемой композиции тестируют в культуре гемолитического стафилококка (Staphylococcus aureus), посевом в чашки Петри на плотную агаризованную среду (таб. 1). На поверхности среды после засева микроорганизмов размещают микрочастицы из заявляемой биологически активной полимерной медицинской композиции, содержащую антисептик. Антимикробная активность материала оценивается по величине зоны отсутствия роста тест-организмов на плотной среде вокруг микрочастиц диаметром 0,5 см. Данные представлены в таблице 1.
При оценке эффективности систем на основе состава поли-3-гидроксибутират-бриллиантовый зеленый в агаре, с использованием культуры Staphylococcus aureus было выявлено низкое антибактериальное действие с контролем по исходной форме антисептика, так как исходная форма препарата представлена 1% спиртовым раствором.
В целом, использование инкапсулированного препарата обеспечило нерезкий, но длительный ингибирующий эффект в зависимости от состава поли-3-гидроксибутират-микрочастиц с бриллиантовым зеленым. Рост анализируемых культур подавлен в пределах допустимых значений.
В результате проведенной работы:
1. Изучено влияние включения антисептиков на характеристики микросферических частиц. Отмечено, что инкапсулирование антисептиков увеличивает электрокинетический потенциал и, соответственно, повышает стабильность микрочастиц. Высвобождение антисептиков из полимерных микросфер составило от 26% для «Фурацилина» до 35% для «Бриллиантового зеленого».
2. Максимальный выход этамзилата составил: 83,9% для частиц из поли-3-гидроксибутирата с модификацией желатином, наполненным наночастицами серебра, и 63,8% для частиц без поверхностной модификации желатином, наполненным наночастицами серебра.
3. Проведена первичная оценка цитотоксичности по отношению к культуре клеток NIH 3Т3, а также оценка антибактериальной активности в культурах патогенных и условно патогенных микроорганизмов. Антибактериальный эффект подтвержден подавлением роста культур Staphylococcus aureus и Escherichia coli.
Заявляемая биологически активная полимерная медицинская композиция предназначена для закрытия дефектов кожных покровов, а также в качестве барьерных средств, для направленной тканевой регенерации, матрикса для депонирования и доставки лекарственных средств и биологически активных препаратов.
| название | год | авторы | номер документа |
|---|---|---|---|
| БИОЛОГИЧЕСКИ АКТИВНАЯ ПОЛИМЕРНАЯ МЕДИЦИНСКАЯ КОМПОЗИЦИЯ (ВАРИАНТЫ) | 2010 |
|
RU2447902C2 |
| БИОРЕЗОРБИРУЕМАЯ ГИДРОГЕЛЕВАЯ ПОЛИМЕРНАЯ КОМПОЗИЦИЯ С БИОЛОГИЧЕСКИ АКТИВНЫМИ ВЕЩЕСТВАМИ (ВАРИАНТЫ) | 2012 |
|
RU2519103C2 |
| Способ получения гибридной двухфазной системы доставки малорастворимых и нерастворимых в воде биологически активных веществ с контролируемой кинетикой выделения | 2015 |
|
RU2607598C1 |
| БИОИНТЕГРИРУЕМЫЙ КОМПОЗИТНЫЙ МАТЕРИАЛ И СПОСОБ ФОРМИРОВАНИЯ ПОКРЫТИЯ НА ИЗДЕЛИЯХ МЕДИЦИНСКОГО НАЗНАЧЕНИЯ С ИСПОЛЬЗОВАНИЕМ БИОИНТЕГРИРУЕМОГО КОМПОЗИТНОГО МАТЕРИАЛА | 2013 |
|
RU2535067C1 |
| ИНТРАНАЗАЛЬНАЯ КОМПОЗИЦИЯ ДЛЯ ПРОФИЛАКТИКИ И/ИЛИ ЛЕЧЕНИЯ ИНФЕКЦИЙ ВИРУСНОЙ И БАКТЕРИАЛЬНОЙ ЭТИОЛОГИИ | 2023 |
|
RU2825642C1 |
| Ультраволокнистый биополимерный материал с бактерицидным эффектом | 2017 |
|
RU2681319C1 |
| ПОЛИМЕРНЫЕ БЕЛКОВЫЕ МИКРОЧАСТИЦЫ | 2012 |
|
RU2768492C2 |
| ПОЛИМЕРНЫЕ БЕЛКОВЫЕ МИКРОЧАСТИЦЫ | 2012 |
|
RU2642664C2 |
| БИОЛОГИЧЕСКИ АКТИВНАЯ ПОЛИМЕРНАЯ КОМПОЗИЦИЯ | 2006 |
|
RU2318535C1 |
| ИМПЛАНТИРУЕМЫЕ ПРОДУКТЫ, СОДЕРЖАЩИЕ НАНОЧАСТИЦЫ | 2009 |
|
RU2524644C2 |

Настоящее изобретение относится к биологически активной полимерной медицинской композиции в виде микрочастиц, включающей полимер поли-3-гидроксибутират и по меньшей мере одно биологически активное вещество и растворитель, отличающейся тем, что содержит биологически активное вещество, выбранное из группы антисептиков или гемостатиков, состоящей из бриллиантового зеленого и этамзилата, и дополнительно содержит желатин, наполненный наночастицами серебра, при следующем соотношении компонентов, мас. %: полимер поли-3-гидроксибутират 20-40; биологически активное вещество 10-20; желатин, наполненный наночастицами серебра 5-10; растворитель - остальное. Настоящее изобретение обеспечивает разработку биологически активной полимерной медицинской композиции широкого спектра действия и применения, обладающей биосовместимостью, оптимальными физико-химическими свойствами, а также способностью медленно биорезорбироваться in vivo без образования токсичных продуктов и негативных реакций в процессе использования. 1 табл., 3 ил.
Биологически активная полимерная медицинская композиция в виде микрочастиц, включающая полимер поли-3-гидроксибутират и по меньшей мере одно биологически активное вещество и растворитель, отличающаяся тем, что содержит биологически активное вещество, выбранное из группы антисептиков или гемостатиков, состоящей из бриллиантового зеленого и этамзилата, и дополнительно содержит желатин, наполненный наночастицами серебра, при следующем соотношении компонентов, мас. %:
| Владимирова А.В | |||
| Приспособление для точного наложения листов бумаги при снятии оттисков | 1922 |
|
SU6A1 |
| Владимирова | |||
| — Красноярск : СФУ, 2018 | |||
| Г.А | |||
| Рыльцева и др | |||
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
Авторы
Даты
2024-03-18—Публикация
2023-01-12—Подача