Настоящее изобретение относится к ранее неизвестной кристаллической форме В (3-циано-1Н-индол-7-ил)-[4-(4-фторфенэтил)пиперазин-1-ил]метанона, гидрохлорида (указанного ниже как EMD281014), к способу его получения и к его применению для получения лекарственного средства.
Предпосылки создания изобретения
Соединение EMD281014 известно из Европейского Патента ЕР 1198453 В1 и имеет следующую структуру:
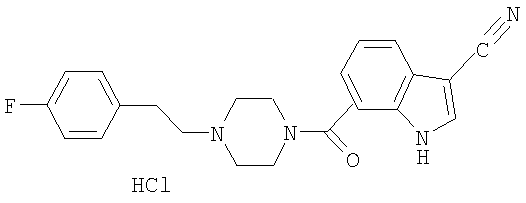
EMD281014 проявляет, из числа других, воздействия на центральную нервную систему, являясь при этом хорошо переносимым, а также имеет ценные фармакологические свойства. Таким образом, это вещество имеет сильную аффинность к 5-НТ2А рецепторам, при этом проявляя 5-НТ2А рецептор-антагонистические свойства.
Большое количество медицинских применений EMD281014, например, таких как лечение шизофрении и расстройств сна, описано в ЕР 1198453 B1. Дополнительные медицинские применения являются предметом WO 03/45392 и WO 04/32932.
Способы получения EMD281014 раскрыты в Европейских Патентах 1198453 B1 и 1353906 B1.
В качестве конечной стадии процесса в каждом случае гидрохлорид осаждают из раствора свободного основания путем добавления водного раствора HCl и отделяют от реакционной смеси.
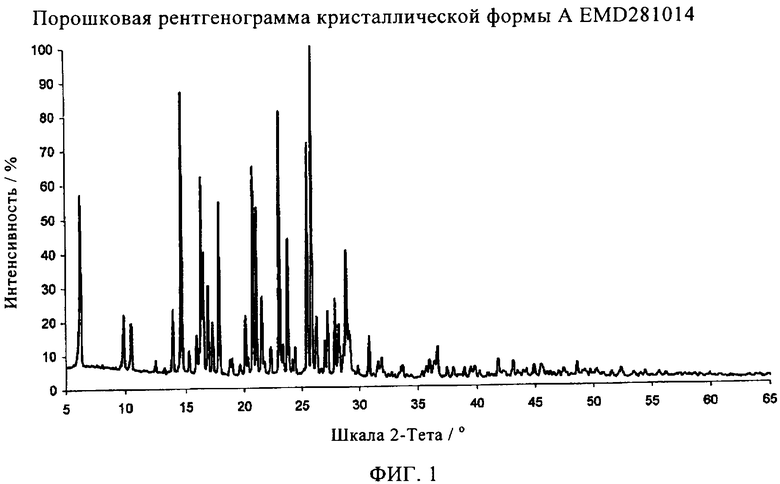
Указанная известная процедура всегда приводит к получению кристаллической формы А, которая характеризуется параметрами кристаллической решетки, показанными в таблице 1, определяемыми с помощью дифракции рентгеновских лучей на порошке.
Неожиданно изобретатели настоящей патентной заявки обнаружили, что вторая кристаллическая форма В образуется при прессовании соединения EMD281014 с получением таблеток в условиях механического давления и присутствует в значительных количествах наряду с формой А в полученных таблетках. Количество образовавшейся формы В зависит от используемого давления прессования.
Для таблетки лекарственного средства считается чрезвычайно неблагоприятным содержать множество кристаллических форм активного ингредиента наряду одна с другой, если эти кристаллические формы имеют различные биодоступности, например, если они растворяются с разными скоростями в физиологических условиях. Даже легкие изменения в условиях производства подвергали бы сомнению воспроизводимость биодоступности.
Таким образом, цель настоящего изобретения заключается в обеспечении EMD281014 в форме, которая не меняет своих свойств в условиях таблетирования и поэтому является подходящей для производства таблеток определенного и постоянного качества.
Описание изобретения
Неожиданно было обнаружено, что EMD281014 как твердое вещество может существовать в различных кристаллических модификациях. Более того, было найдено, что процесс кристаллизации и, таким образом, предпочтительное образование одной из двух форм А или В может контролироваться путем подходящего выбора параметров процесса. Также существует возможность превратить форму А в форму В и форму В в форму А без необходимости переведения EMD281014 в раствор для этой цели.
Форму В следует рассматривать как стабильную в условиях производства таблеток. Невозможно однозначно идентифицировать фракции формы А или других полиморфных форм EMD281014 в рентгенограммах образцов таблеток, полученных из формы В.
Обе кристаллические формы содержат только EMD281014, т.е. не содержат ни воды, ни других молекул растворителя.
Как уже было указано выше, форму А получают способами, известными из предыдущего уровня техники. Форма А характеризуется данными рентгеноструктурного анализа, как показано в таблице 1.
Условия измерения: режим передачи, мощность генератора 40 кВ/30 мА, Cu-Kα1 излучение (λ=1,54056 Å), позиционно-чувтствительный детектор (3,3 кВ), диапазон измерений: 3-65°2θ, размер шага: 0,05°2θ, время/шаг: 1,4 с.
Оценка: рентгенограммы были скомпенсированы с поправкой на фон по всему диапазону записи 3-65°2θ, и интенсивности отражения определяли для 20 наиболее сильных отраженных сигналов в каждом случае. Допустимое отклонение положения наклона составляет ±0,1°2θ для используемого Cu-Kα1 излучения.
Для того чтобы получить форму В с высоким выходом и в основном в чистой форме, следуют указанной ниже процедуре.
Сначала свободное основание EMD281014 получают способом, известным per se, и далее сушат термически для того, чтобы удалить оставшиеся растворители.
Вместо того чтобы потом осадить гидрохлорид путем добавления водного HCl раствора, газообразный HCl пропускают через раствор свободного основания. Это также приводит к получению осадка, который, однако, неожиданно состоит не из формы А, а из формы В.
Термин "форма В, в основном чистая" или "в основном состоящее из формы В" в этом описании означает, что форма В включает меньше чем 5%, предпочтительно меньше чем 2% и особенно предпочтительно меньше чем 1% формы А.
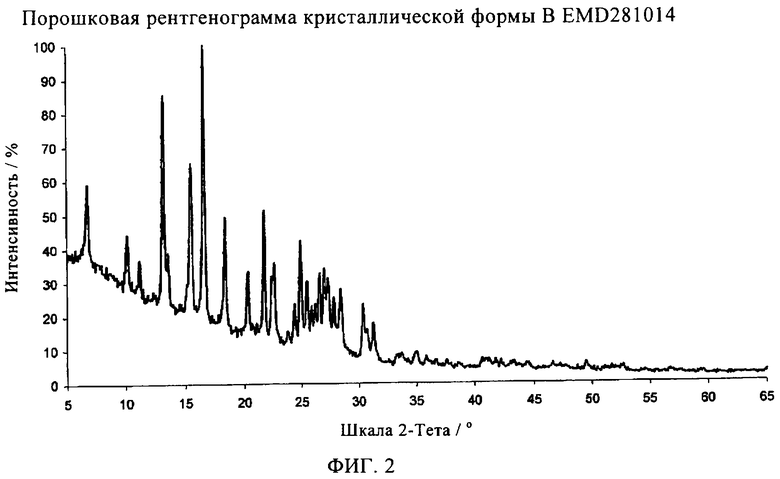
Форма В характеризуется данными рентгеноструктурного анализа, как показано в таблице 2.
Условия измерения и оценку выполняли, как описано для таблицы 1.
В предпочтительном воплощении форма В характеризуется с помощью рентгеновских данных, как показано в таблице 2a. Данные, показанные в таблице 2a, содержат отражения из таблицы 2 и, кроме того, 10 дополнительных отражений более низкой интенсивности.
Условия измерения и оценку выполняли, как описано для таблицы 1.
Настоящее изобретение соответственно относится к полиморфной кристаллической форме В соединения EMD281014, которая характеризуется характеристическими расстояниями между плоскостями решетки, показанными в таблице 2.
В частности, настоящее изобретение относится к полиморфной кристаллической форме В соединения EMD281014, которая характеризуется характеристическими расстояниями между плоскостями решетки, показанными в таблице 2a.
Кроме того, настоящее изобретение относится к способу получения кристаллической формы В соединения EMD281014 из раствора свободного основания EMD281014, который характеризуется тем, что газ HCl пропускают через этот раствор и осадок, который образуется, отделяют.
В основном при этом используют молярный избыток растворителя к растворенному веществу от 50:1 до 200:1, но предпочтительно от 100:1 до 150:1. Предпочтительным растворителем является тетрагидрофуран (THF).
Кроме того, было найдено, что форма В также может быть получена путем перемешивания суспензии кристаллов формы А в трет-бутил-метиловом эфире (МТВЕ).
Поэтому настоящее изобретение также относится к соответствующему способу получения.
Если этот способ выполняют при комнатной температуре в течение 14 дней, приблизительно 30% формы В получают вдобавок к форме А, где соотношение В к А оценивают путем сравнения образца дифракции рентгеновских лучей на порошке смеси с образцами дифракции чистых веществ. Выбор более короткого или более продолжительного времени реакции позволяет осуществить получение смесей В и А в любых желаемых композициях. Поэтому настоящее изобретение относится к EMD281014, содержащему форму В.
Смеси, которые являются предпочтительными в соответствии с настоящим изобретением, включают в каждом случае более чем 10%, 20%, 30%, 40%, 50%, 60%, 70%, 80% или 90% формы В. Кроме того, данное изобретение относится к EMD281014, которое в основном состоит из формы В.
Также можно получить форму А путем перемешивания суспензии кристаллов формы В. В этом случае используют полярные растворители, такие как, например, ацетон, вода или смеси этих двух растворителей. В этом описании предпочтительная смесь представляет собой смесь ацетон/вода в соотношении 55:45% по массе. Если воду используют как единственный растворитель, процесс предпочтительно проводят при кислом pH (в частности pH 1). Поэтому настоящее изобретение также относится к соответствующему способу получения.
Как указано выше, форма В образуется из формы А под действием давления. Поэтому настоящее изобретение, кроме того, также относится к способу получения кристаллической формы В EMD281014, который характеризуется тем, что механическое давление прилагают к кристаллам формы А.
В этом описании давления предпочтительно представляют собой те, которые обычно преобладают в процессе производства таблеток, если усилия плунжера от приблизительно 2 до 16 кН, в частности от 6 до 16 кН, используют как максимальные усилия прессования. Согласно наблюдениям содержание формы В повышается с увеличением давления. При таблетировании в кулачковом прессе с продолжительностью (время контактирования) 310 мс и максимальными усилиями прессования 16 кН получают смесь приблизительно 25% формы В и 75% формы А. При таблетировании в кулачковом прессе с временем контактирования 250 мс и максимальными усилиями прессования 6 кН часть формы В составляет приблизительно 20%.
Более того, был найден очень простой способ получения формы А из формы В. Для этого форму В необходимо просто сохранять при повышенных температурах от приблизительно 75 до приблизительно 225°С, предпочтительно от 90 до 160°С и особенно предпочтительно от 110 до 140°С. В зависимости от температуры и продолжительности сохранения могут быть достигнуты разные степени превращения. В зависимости от целевой степени превращения продолжительность сохранения при данной температуре может составлять от нескольких минут до нескольких дней. Для того чтобы достигнуть высоких степеней превращения, форму А предпочтительно сохраняют в течение от нескольких часов до дней. Приемлемое время сохранения составляет, например, 4, 8, 12, 16, 20, 24, 36 или 48 часов. При 105°С может быть достигнуто полное превращение формы В в форму А, например, путем хранения в течение 24 часов.
Настоящее изобретение также относится к соответствующему способу получения формы А из формы В.
Наконец, настоящее изобретение относится к применению формы В в качестве лекарственного средства или для получения фармацевтических композиций и лекарственных средств, а также к этим композициям и лекарственным средствам как таковым.
Указанное применение происходит аналогично известной форме А, как описано в ЕР 1198453 B1, WO 03/45392 и WO 04/32932.
Примеры
1. Получение формы В соединения EMD281014 из раствора свободного основания
50 г основания (3-циано-1Н-индол-7-ил)-[4-(4-фторфенэтил)пиперазин-1-ил]метанона, на котором основано EMD281014, растворяют в 1400 мл THF в 2-литровой круглодонной колбе. Затем смесь охлаждают до 5°С. Далее 20 г HCl газообразного (в соответствии с молярным избытком 4,1 в пересчете на используемое основание) пропускают в течение 4 минут при охлаждении с помощью бани лед/этанол. Образуется белый осадок. После завершения реакции смесь перемешивают при температуре от 25 до 27°С в течение дополнительных 60 минут. Потом осадок отфильтровывают при этой температуре через воронку Бюхнера и сушат в течение 18 часов при 23°С в вакуумном сушильном шкафу с получением 53,3 г белых твердых кристаллов (выход 97% от теоретического), что соответствует кристаллической форме В (определение с помощью дифракции рентгеновских лучей на порошке).
Кристаллы, полученные этим способом, имеют характеристические расстояния между плоскостями решетки, как показано в таблице 2 и/или 2а. Для дополнительной характеристики записывают рамановский спектр, который показывает типичные полосы, представленные в таблице 3.
Условия измерения: FT рамановская спектроскопия, Bruker RFS 100, 1064 нм возбуждение, 750 мВт, 1 см-1 спектральное разрешение, 250 сканирований.
Оценка: полученный рамановский спектр вектор-стандартизируют в спектральном интервале 3600-250 см-1. Полосы классифицируют на основе их интенсивности следующим образом, S = сильная, М = средняя и W = слабая:
S I>0,075
М 0,01<I<0,075
W I<0,01
2. Сравнительный пример. Получение формы A EMD281014 из раствора свободного основания, как описано в ЕР 1353906 B1
2,1 г свободного основания EMD281014 нагревают в 50 мл ацетона и добавляют воду до образования прозрачного раствора. Далее примешивают смесь 0,6 мл соляной кислоты (мас.=37%) и 1,2 мл ацетона. Потом смесь выпаривают до половины объема в роторном испарителе. Осажденный гидрохлорид отфильтровывают с вакуумным насосом, промывают ацетоном и диэтиловым эфиром и сушат, что приводит к получению 1,6 г 7-{4-[2-(4-фторфенил)этил]пиперазин-1-карбонил}-1Н-индол-3-карбонитрила, гидрохлорида (69% от теоретического), температурный интервал разложения 314-319°С.
Кристаллы, полученные этим способом, имеют характеристические расстояния между плоскостями решетки, как показано в таблице 2 и/или 2a. Для дополнительной характеристики записывают рамановский спектр, который показывает типичные полосы, представленные в таблице 4.
Условия измерения и оценку выполняли, как описано в таблице 3.
3. Получение формы В EMD281014 из формы А путем перемешивания суспензии А в МТВЕ
250 мг EMD281014 формы А диспергируют в 5 мл МТВЕ (трет-бутил-метиловый эфир) и перемешивают в течение 14 дней при комнатной температуре в герметично закрытом сосуде из коричневого стекла. Осадок отфильтровывают через круглый бумажный фильтр и сушат в условиях комнатной атмосферы. Результат исследования дифракции рентгеновских лучей: присутствует смесь EMD281014 формы А и формы В. Часть формы В оценивают как приблизительно 30% по массе в сравнении с моделями дифракции рентгеновских лучей на порошке чистых форм.
4. Получение формы В из формы А путем применения давления
На ЕК0 кулачковом прессе от Korsch (Berlin, Germany), год выпуска 2002, таблетки производят со скоростью 50 единиц в минуту, используя 7 мм круглый плоский пресс-шток с фаской.
Таблетки содержат 50 мг EMD281014 в кристаллической форме А, 93,2 мг моногидрата лактозы, 4,5 мг кроскармеллозы и 2,3 мг стеарата магния. Эти ингредиенты смешивают в сухом виде и непосредственно прессуют.
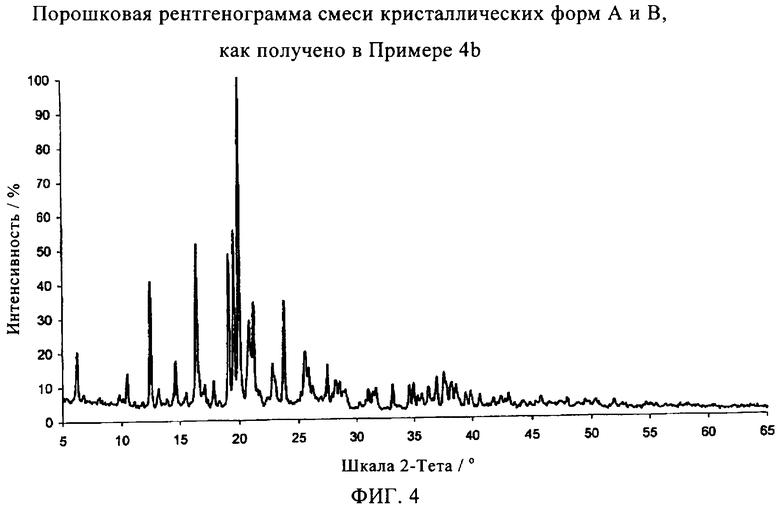
Часть формы В оценивают путем сравнения рентгенограмм смесей (фиг.3 и 4) с рентгенограммами чистых форм (фиг.1 и 2).
Получают следующие результаты.
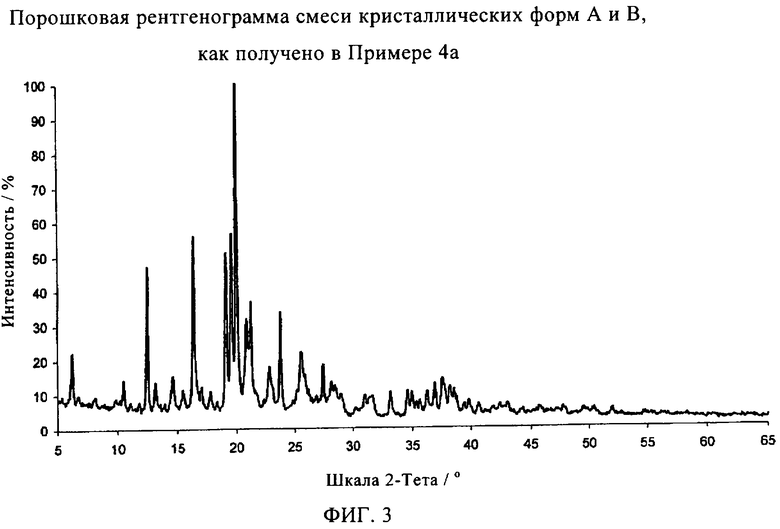
Настоящее изобретение относится к кристаллической форме В (3-циано-1 Н-индол-7-ил)-[4-(4-фторфенэтил)пиперазин-1-ил]метанона гидрохлорида, а также к способу его получения путем пропускания газа HCl через раствор (3-циано-1Н-индол-7-ил)-[4-(4-фторфенэтил)пиперазин-1-ил]метанона, отделения образующегося осадка от реакционной смеси и сушки. Технический результат - получена новая кристаллическая форма (3-циано-1Н-индол-7-ил)-[4-(4-фторфенэтил)пиперазин-1-ил]метанона гидрохлорида, который может найти применение в медицине в качестве лекарственного средства, оказывающего антагонистическое действие на рецептор 5-НТ2А. 3 н. и 1 з.п. ф-лы, 4 ил., 6 табл.
1. Кристаллическая форма В (3-циано-1Н-индол-7-ил)-[4-(4-фторфенэтил)пиперазин-1-ил]метанона гидрохлорида, характеризующаяся следующими характеристическими расстояниями между плоскостями решетки в 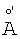 : 13,083±0,20, 6,688±0,10, 5,669±0,05, 5,292±0,05, 4,786±0,05, 4,040±0,02, 3,881±0,02, 3,514±0,02, 3,239±0,02, 3,200±0,02.
: 13,083±0,20, 6,688±0,10, 5,669±0,05, 5,292±0,05, 4,786±0,05, 4,040±0,02, 3,881±0,02, 3,514±0,02, 3,239±0,02, 3,200±0,02.
2. Кристаллическая форма В (3-циано-1Н-индол-7-ил)-[4-(4-фторфенэтил)пиперазин-1-ил]метанона гидрохлорида, по п.1, характеризующаяся следующими характеристическими расстояниями между плоскостями решетки в 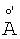 : 13,083±0,20, 8,706±0,10, 6,688±0,10, 6,499±0,05, 5,669±0,05, 5,292±0,05, 4,786±0,05, 4,322±0,05, 4,040±0,02, 3,881±0,02, 3,595±0,02, 3,514±0,02, 3,435±0,02, 3,337±0,02, 3,289±0,02, 3,239±0,02, 3,200±0,02, 3,143±0,02, 3,073±0,02, 2,867±0,01.
: 13,083±0,20, 8,706±0,10, 6,688±0,10, 6,499±0,05, 5,669±0,05, 5,292±0,05, 4,786±0,05, 4,322±0,05, 4,040±0,02, 3,881±0,02, 3,595±0,02, 3,514±0,02, 3,435±0,02, 3,337±0,02, 3,289±0,02, 3,239±0,02, 3,200±0,02, 3,143±0,02, 3,073±0,02, 2,867±0,01.
3. Способ получения кристаллической формы В по п.1 или 2, отличающийся тем, что газ HCl пропускают через раствор (3-циано-1Н-индол-7-ил)-[4-(4-фторфенэтил)пиперазин-1-ил]метанона, и образующийся осадок отделяют от реакционной смеси и сушат.
4. Кристаллическая форма по п.1 и 2, в качестве лекарственного средства, оказывающего антагонистическое действие на рецептор 5-НТ2А.
| Анализатор спектра низких частот | 1956 |
|
SU107435A1 |
| WO 02059092 A, 01.08.2002 | |||
| WO 03045392 A, 05.06.2003 | |||
| WO 2004032932 A, 22.04.2004 | |||
| 4-ПИРИМИДИН- ИЛИ ПИРИДИНИЛЬНЫЕ ПРОИЗВОДНЫЕ ИНДОЛ-3-ИЛ-АЛКИЛПИПЕРАЗИНОВ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 1992 |
|
RU2114111C1 |
Авторы
Даты
2010-03-10—Публикация
2005-09-08—Подача