ПЕРЕКРЕСТНАЯ ССЫЛКА НА РОДСТВЕННЫЕ ЗАЯВКИ
Настоящая заявка претендует на приоритет по предварительной заявке на патент США № 60/462070, поданной 13 апреля 2003 г., содержание которой включено здесь в качестве ссылки.
ОБЛАСТЬ ТЕХНИКИ
Настоящее изобретение относится к полимерным нуклеотидным пролекарствам, пригодным в качестве терапевтических агентов. Также предложены композиции и способы применения таких пролекарств.
УРОВЕНЬ ТЕХНИКИ
Хорошо известно, что на большую часть соматических состояний многоклеточных организмов, включая большинство болезненных состояний, оказывают влияние белки. Такие белки путем непосредственного воздействия или за счет своих ферментативных или других функций в большой степени вносят вклад во многие заболевания и регуляторные функции у животных и человека. В случае болезненных состояний классическая терапия обычно была сфокусирована на взаимодействии с такими белками в попытке ослабить их функции, вызывающие заболевания или усиливающие заболевания. В новейших терапевтических подходах желательно регулировать существующую продукцию таких белков. Оказывая влияние на продукцию белков, можно достичь максимального терапевтического эффекта при минимальных побочных эффектах. Таким образом, общая цель таких терапевтических подходов состоит во влиянии или модификации иным способом экспрессии генов, которые приводят к образованию нежелательного белка.
Один из способов такого ингибирования экспрессии специфического гена состоит в использовании олигонуклеотидов, в особенности олигонуклеотидов, которые комплементарны специфической последовательности информационной РНК (мРНК) мишени. Обычно последовательности нуклеиновых кислот, комлементарные продуктам генной транскрипции (например, мРНК) обозначают как «антисмысловые», а последовательности нуклеиновых кислот, содержащие ту же самую последовательность, что и транскрипт, или получаемые в качестве транскрипта обозначают здесь как «смысловые». См., например, Crooke, 1992, Annu. Rev. Pharmacol. Toxicol., 32: 329-376. Антисмысловой олигонуклеотид может быть выбран для гибридизации со всем геном или его частью, таким образом, чтобы модифицировать экспрессию этого гена. Транскрипционные факторы взаимодействуют с двухцепочечной ДНК в ходе регуляции транскрипции. Олигонуклеотиды могут служить в качестве конкурентных ингибиторов транскрипционных факторов для модификации их действия. Несколько недавних сообщений описывают такие взаимодействия (см. Bielinska, A., et al., 1990, Science, 250: 997-1000; и Wu, H., et al., 1990, Gene 89: 203-209).
Развиваются молекулярные стратегии понижающей регуляции экспрессии нежелательного гена. В последнее время использование модифицированных олигонуклеотидных соединений развилось в многообещающий способ терапии, направленный против таких заболеваний, как вирусные инфекции, воспалительные и генетические заболевания и, в значительной степени, рак. Антисмысловые ДНК были впервые предложены как алкилирующие комплементарные олигодезоксинуклеотиды, направленные против природных нуклеиновых кислот (Belikova, et al., Tetraxedron Lett. 37: 3557-3562, 1967). Zamecnik и Stephenson были первыми, кто предложил использовать синтетические антисмысловые олигонуклеотиды в терапевтических целях. (Zamecnik & Stephenson, 1978, Proc. Natl. Acad. Sci. U.S.A., 75: 285-289; Zamecnik & Stephenson, 1978, Proc. Natl. Acad. Sci. U.S.A., 75: 280-284). Они сообщили о применении 13-мера олигонуклеотида, комплементарного РНК вируса саркомы Рауса для ингибирования роста вируса в культуре клеток. С этого времени было опубликовано множество других исследований, показывающих эффективность in vitro антисмысловых олигонуклеотидов в ингибировании роста вирусов, например, вирусов везикулярного стоматита (Leonetti et al., 1988, Gene, 72: 323), вирусов простого герпеса (Smith et al., 1987, Proc. Natl. Acad. Sci. U.S.A., 83: 2787) и вируса гриппа (Seroa, et al., 1987, Nucleic Acids Res., 15: 9909).
Олигонуклеотиды также нашли использование, помимо прочих, в диагностических исследованиях, реактивах для исследований, например праймеры в технологии ПЦР (PCR) и других лабораторных операциях. Олигонуклеотиды можно синтезировать специально, чтобы они включали функции, которые приспособлены, чтобы подходить для желаемого применения. Таким образом, в олигомерные соединения были внедрены многочисленные химические модификации для усиления пригодности при диагностике, в качестве реагентов для исследований и в качестве элементов терапии.
Хотя олигонуклеотиды, в особенности антисмысловые олигонуклеотиды, подают надежды в качестве терапевтических агентов, они чрезвычайно подвержены действию нуклеаз и могут быть быстро разрушены перед тем и после того, как они попадают в клетки-мишени, что делает немодифицированные антисмысловые олигонуклеотиды непригодными для использования в in vivo системах. Поскольку ферменты, ответственные за их разрушение, присутствуют в большинстве тканей, были проведены модификации олигонуклеотидов в попытках стабилизировать соединения и исправить эту проблему. Наиболее широко изученные модификации относятся к остову олигонуклеотидных соединений. В общих чертах см. Uhlmann и Peymann, 1990, Chemical Reviews, 90 на страницах 545-561 и цитированные там ссылки. Среди многочисленных полученных остовов, только фосфоротиоат показал значительную антисмысловую активность. См., например, Padmapriya и Agrawal, 1993, Bioorg. & Med. Chem. Lett. 3, 761. Хотя введение атомов серы в остов замедляет скорость ферментативного разрушения, в то же время оно увеличивает токсичность. Другой недостаток введения атомов серы состоит в том, что это делает ахиральный остов хиральным, что приводит к 2n диастереомерам. Это может вызывать дополнительное побочное действие. Другие недостатки существующих антисмысловых олигонуклеотидов состоят в том, что они могут иметь отрицательный заряд на фосфатной группе, что ингибирует их способность проходить через преимущественно липофильную клеточную мембрану. Чем дольше соединение остается вне клетки, тем более оно разрушается и тем меньше активного соединения поступает к мишени. Дополнительный недостаток существующих антисмысловых соединений состоит в том, что олигонуклеотиды склонны к образованию в растворах вторичной структуры и структур более высокого порядка. Как только эти структуры образуются, они становятся мишенями для связывания с различными ферментами, белками, РНК и ДНК. Это приводит к неспецифическим побочным действиям и уменьшает количество активного соединения, связывающегося с мРНК. Другие попытки улучшения нуклеотидной терапии включили добавление линкерного фрагмента и полиэтиленгликоля. См., например, Kawaguchi et al., Stability, Specific Binding Activity, and Plasma Concentration in Mice of Oligonucleotide Modified at 5'-Terminal with Poly(ethylene glycol), Biol. Pharm. Bull., 18(3) 474-476 (1995), и патент США № 4904582. В обоих этих примерах модификации касаются использования линкерных фрагментов на постоянной основе с целью стабилизации олигонуклеотида от разрушения и увеличения клеточной проницаемости. Однако обе этих попытки оказались неэффективными.
Из-за неадекватности настоящих способов существует необходимость улучшить стабильность и устойчивость к разрушению нуклеазами, а также понизить токсичность и увеличить связывающее сродство по отношению к мРНК олигонуклеотидных соединений. Используемая олигонуклеотидная терапия является чрезвычайно дорогостоящей. Главным образом, это связано с проблемой разрушения. Таким образом, существует реальная необходимость в защите антисмысловых олигонуклеотидных соединений от разрушения, предотвращении образования структур высокого порядка и, в то же самое время, в доставке достаточных количеств активных антисмысловых олигонуклеотидных соединений к мишени. В настоящем изобретении предлагаются такие усовершенствования.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
В одном аспекте настоящего изобретения предлагаются олигонуклеотидные пролекарства формулы (I):
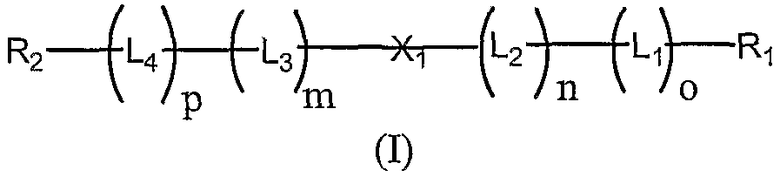
в которой
R1 и R2 независимо представляют собой Н или полимерный остаток;
L1 и L4 независимо представляют собой высвобождаемые линкерные фрагменты;
L2 и L3 независимо представляют собой спейсерные группы;
Х1 представляет собой нуклеотидный остаток или олигонуклеотидный остаток;
m, n, o и р независимо представляют собой ноль или положительное целое число, при условии, что или (o+n), или (p+m)≥2.
Другой аспект настоящего изобретения включает бифункциональные соединения, которые образуются когда R1 и/или R2 представляют собой полимерные остатки, которые одновременно включают альфа- и омега- терминальную линкерную группу, как здесь описано, так что два олигонуклеотида связаны с предусмотренными полимерными системами доставки. Примеры этого варианта осуществления включают олигонуклеотиды, связанные с полимерными системами через их соответствующие 3'-, 5'-терминальные группы, например 3'-бис-олигонуклеотидные конъюгаты или 5'-бис-олигонуклеотидные конъюгаты, или конъюгаты, образованные связыванием первого олигонуклеотида через 3'-конец к 5'-концу второго олигонуклеотида. Примеры таких полимерных конъюгатов проиллюстрированы ниже как формулы (i), (ii), (iii) и (iv):
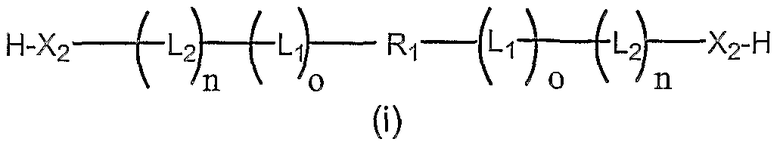
бис-3'-олигонуклеотид,
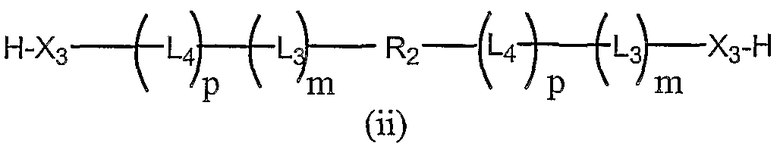
бис-5'-олигонуклеотид,
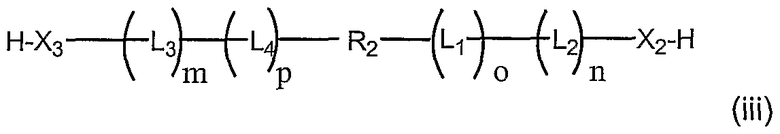
бис-5',3'-олигонуклеотид и
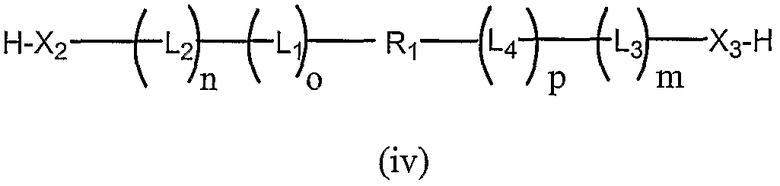
бис-3',5'-олигонуклеотид,
где все переменные такие же, как описано выше.
В целях настоящего изобретения термин «остаток» следует понимать для обозначения того фрагмента биологически активного соединения, т.е. олигонуклеотида, более конкретно антисмыслового олигонуклеотида, который остается после того, как он вступил в реакцию замещения, в которой был присоединен носитель пролекарства.
В целях настоящего изобретения термин «остаток полимера» или «остаток PEG» следует понимать для обозначения той части полимера или полиэтиленгликоля (PEG), который остается после того, как он вступил в реакцию с модифицированным олигонуклеотидным соединением.
В целях настоящего изобретения термин «алкил» следует понимать, как включающий неразветвленные, разветвленные, замещенные, например, галоген-, алкокси-, нитро-, С1-12 алкилы, С3-8 циклоалкилы или замещенные циклоалкилы и т.д.
В целях настоящего изобретения термин «замещенный» следует понимать, как включающий добавление или замещение одного или нескольких атомов, содержащихся в функциональной группе или соединении с одним или несколькими различными атомами.
В целях настоящего изобретения замещенные алкилы включают карбоксиалкилы, аминоалкилы, диалкиламино, гидроксиалкилы и меркаптоалкилы; замещенные алкенилы включают карбоксиалкенилы, аминоалкенилы, диалкениламины, гидроксиалкенилы и меркаптоалкенилы; замещенные алкинилы включают карбоксиалкинилы, аминоалкинилы, диалкиниламины, гидроксиалкинилы и меркаптоалкинилы; замещенные циклоалкилы включают фрагменты, такие как 4-хлорциклогексил; арилы включают фрагменты, такие как нафтил; замещенные арилы включают фрагменты, такие как 3-бромфенил; арилалкилы включают фрагменты, такие как толуил; гетероалкилы включают фрагменты, такие как этилтиофен; замещенные гетероалкилы включают фрагменты, такие как 3-метокситиофен; алкокси включают фрагменты, такие как метокси; и фенокси включают фрагменты, такие как 3-нитрофенокси. Галоген следует понимать как включающий фтор, хлор, йод и бром.
Термин «достаточные количества» или «эффективные количества» в целях настоящего изобретения должен обозначать количество, которое приводит к терапевтическому эффекту, такому как эффект, подразумеваемый специалистами в данной области техники.
Некоторые из главных преимуществ настоящего изобретения включают новые полимерные олигонуклеотидные пролекарства, которые демонстрируют повышенную стабильность и устойчивость к разрушению нуклеазами, повышенную растворимость, повышенную клеточную проницаемость и пониженную токсичность.
Другое преимущество соединений по настоящему изобретению состоит в том, что к модифицированным олигонуклеотидным соединениям присоединяют с возможностью высвобождения разнообразные полимерные пролекарственные платформы. Это преимущество позволяет специалисту разрабатывать конъюгат лекарства, которым можно манипулировать, для включения различных фрагментов между полимерным остатком и присоединенным олигонуклеотидом, таким образом, чтобы влиять на скорость гидролиза пролекарства. Специалист, таким образом, обладает возможностью включать заместители, которые позволяют изменять скорость гидролиза пролекарства.
Представлены способы получения и применения этих соединений, такие как способы лечения рака или злокачественных образований, а также описанные здесь конъюгаты. Также предполагается, чтобы полимерные олигонуклеотидные пролекарства по изобретению назначали вместе с (одновременно и/или последовательно) любым другим подходящим антираковым агентом.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
Фиг.1 схематически показывает способы получения полиэтиленгликолированных олигонуклеотидов соединений 3 и 5.
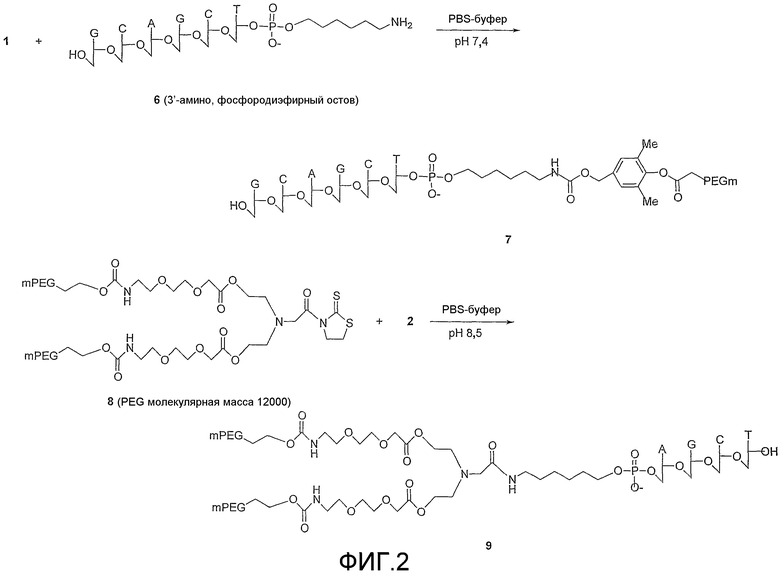
Фиг.2 схематически показывает способы получения полиэтиленгликолированных олигонуклеотидов соединений 7 и 9.
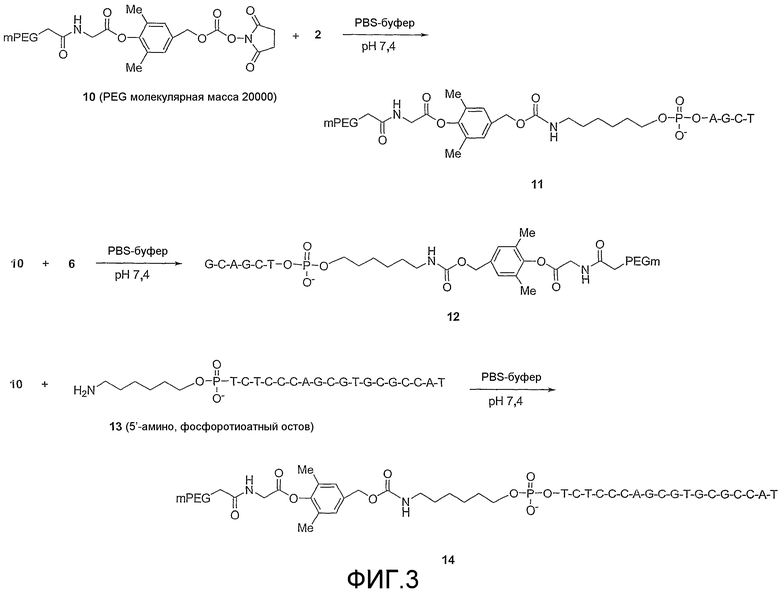
Фиг.3 схематически показывает способы получения полиэтиленгликолированных олигонуклеотидов соединений 11, 12 (SEQ ID NO: 1) и 14 (SEQ ID NO: 1).
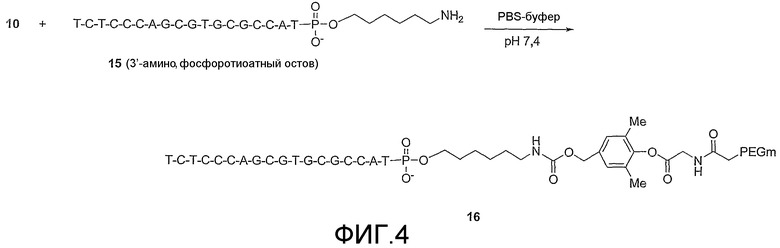
Фиг.4 схематически показывает способ получения полиэтиленгликолированного олигонуклеотида соединения 16 (SEQ ID NO: 1).
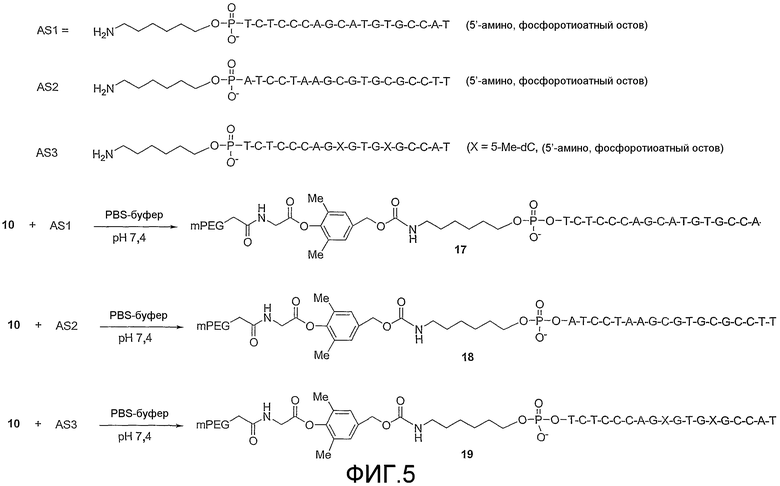
Фиг.5 схематически показывает способы получения полиэтиленгликолированных олигонуклеотидов соединений 17 (SEQ ID NO: 2), 18 (SEQ ID NO: 3) и 19 (SEQ ID NO: 4) из AS1 (SEQ ID NO: 2), AS2 (SEQ ID NO: 3) и AS3 (SEQ ID NO: 4).
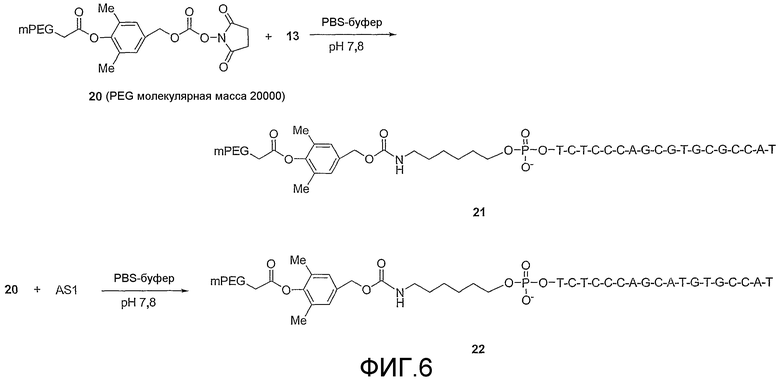
Фиг.6 схематически показывает способы получения полиэтиленгликолированных олигонуклеотидов соединений 21 (SEQ ID NO: 1) и 22 (SEQ ID NO: 2).
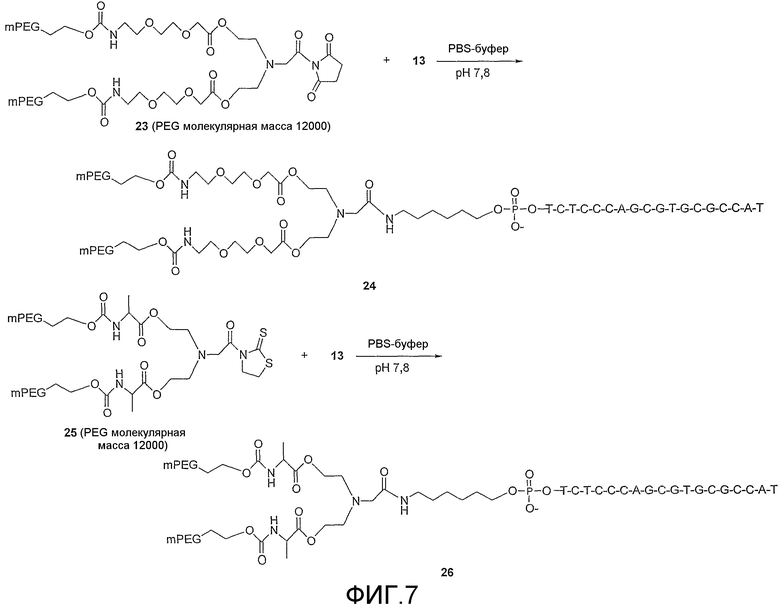
Фиг.7 схематически показывает способы получения полиэтиленгликолированных олигонуклеотидов соединений 24 (SEQ ID NO: 1) и 26 (SEQ ID NO: 1).
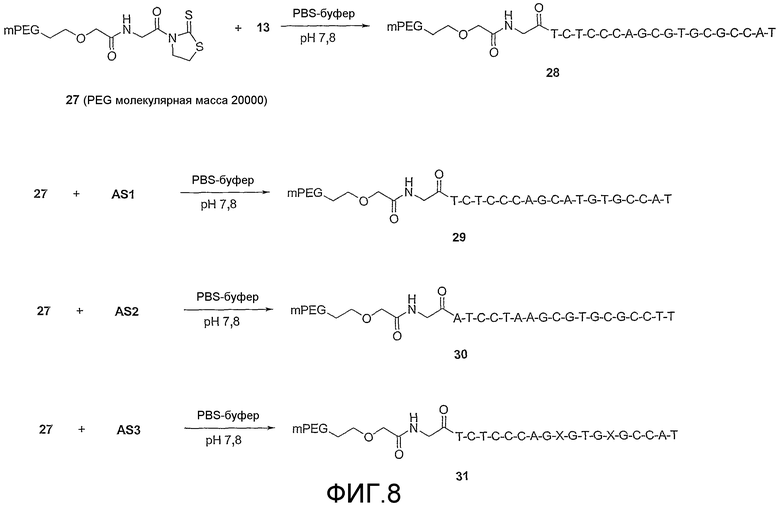
Фиг.8 схематически показывает способы получения полиэтиленгликолированных олигонуклеотидов соединений 28 (SEQ ID NO: 1), 29 (SEQ ID NO: 2), 30 (SEQ ID NO: 3) и 31 (SEQ ID NO: 4) из AS1 (SEQ ID NO: 2), AS2 (SEQ ID NO: 3) и AS3 (SEQ ID NO: 4).
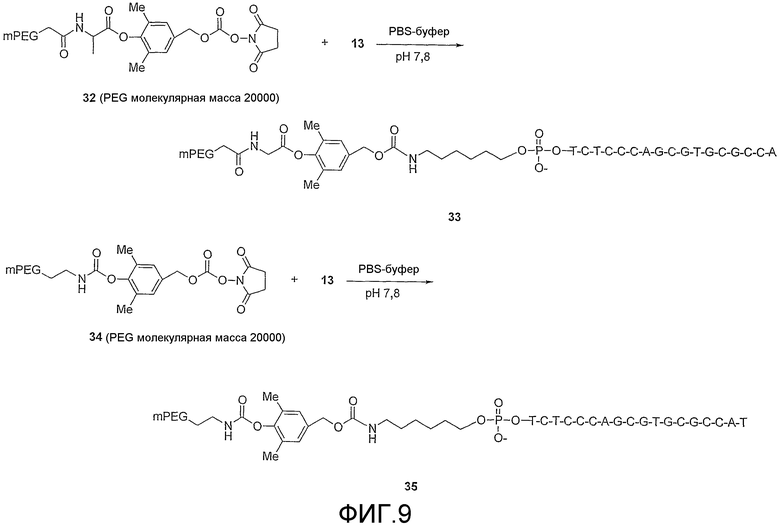
Фиг.9 схематически показывает способы получения полиэтиленгликолированных олигонуклеотидов соединений 33 (SEQ ID NO: 1) и 35 (SEQ ID NO: 1).
Фиг.10 показывает ингибирующий эффект соединения 14 и соединения 28 на рост РС3 клеток. 0,4×104 клеток высевали в 96-луночные планшеты, обрабатывали комплексами соединения 14 или соединения 28 (400 нМ) и липофектина (15 мкг/мл) в течение 24 часов в Opti-MEM и затем полной средой без комплексов. Жизнеспособность клеток определяли ежедневно и поглощение определяли при 570 нм. Данные представлены как среднее ± стандартное отклонение; n=4. Кривые представляют собой следующие:
контроль обозначен ♦ и точечной линией;
соединение 28 при 400 нМ обозначено  и сплошной линией;
и сплошной линией;
соединение 14 при 400 нМ обозначено ▲ и пунктирной линией;
соединение 28 при 200 нМ обозначено  и пунктирной линией;
и пунктирной линией;
соединение 14 при 200 нМ обозначено ■ и точечной линией.
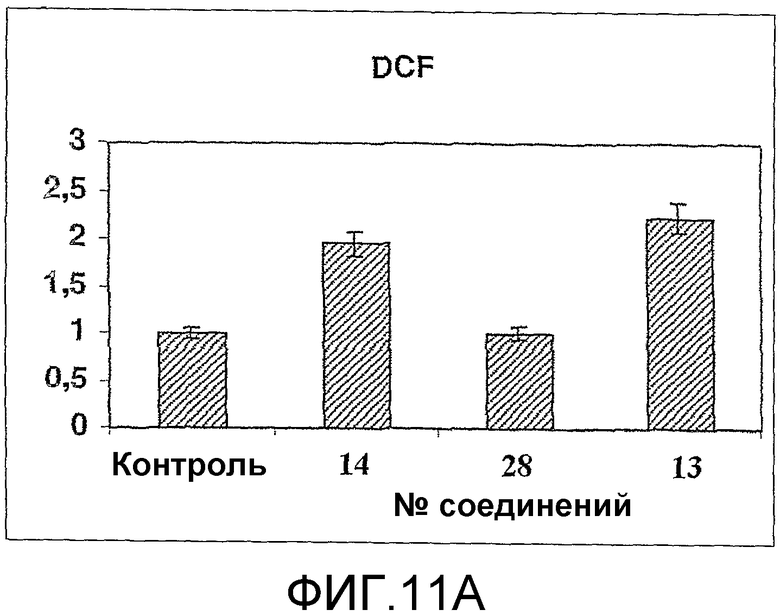
Фиг.11 А представляет анализ продукции ROS (из проточного цитометрического анализа) с помощью олигонуклеотидов соединения 14 и соединения 28, определением окисления проникающего в клетку 2',7'-дигидродихлорфлуоресцеин диацетата до флюоресцентного 2',7'-дихлорфлуоресцеина (DCF). РС3-клетки обрабатывали комплексами олигонуклеотид (400 нМ)/липофектин (15 мкг/мл) в течение 24 часов и анализировали через 3 дня, как описано. Кратные увеличения в среднем канале флуоресценции были нормализованы по сравнению с необработанными клетками. Эксперименты проводили трижды, и данные представлены как среднее ± стандартное отклонение (n=3).
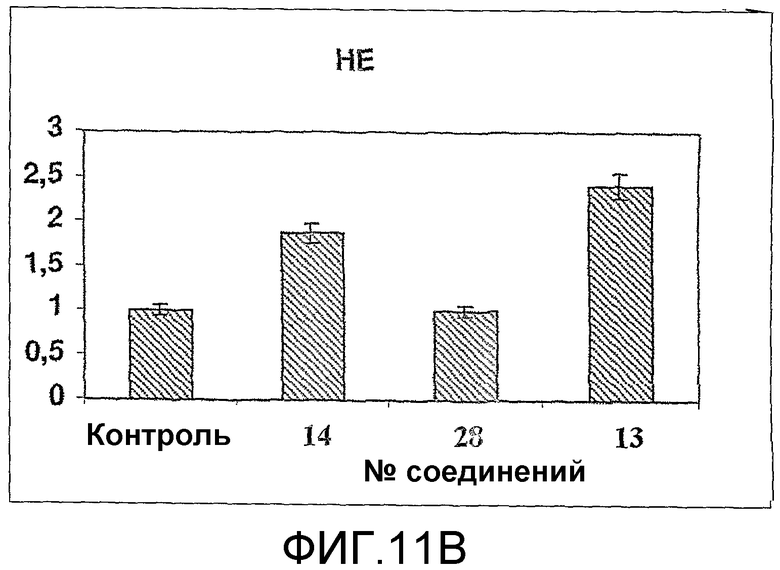
Фиг.11В представляет анализ продукции ROS (из проточного цитометрического анализа) с помощью олигонуклеотидов соединения 14 и соединения 28, определением окисления гидроэтидия (НЕ) до этидия (Е), который затем включается в ДНK, флуоресцентно определяемого поточной цитометрией. РС3-клетки обрабатывали комплексами олигонуклеотид (400 нМ)/липофектин (15 мкг/мл) в течение 24 часов и анализировали через 3 дня, как описано. Кратные увеличения в среднем канале флуоресценции были нормализованы по сравнению с необработанными клетками. Эксперименты проводили трижды, и данные представлены как среднее ± стандартное отклонение (n=3).
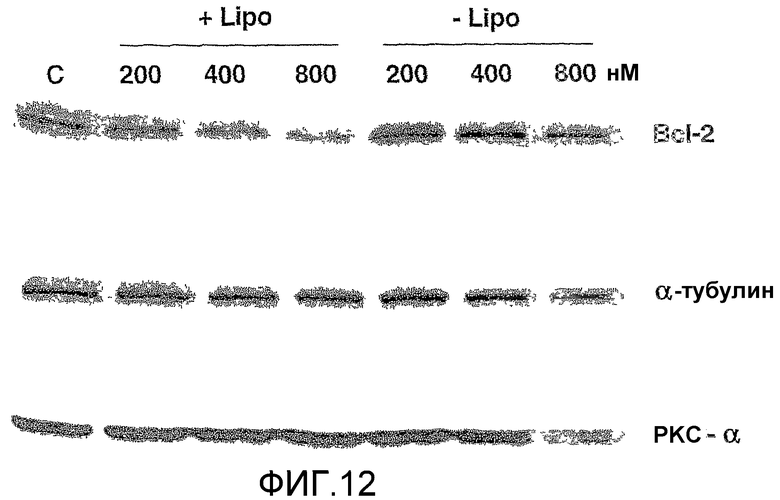
Фиг.12 представляет собой результаты Вестерн-Блота, подтверждающие ингибирование экспрессии белка bcl-2 соединением 14 в присутствии липофектина. РС3-клетки обрабатывали олигонуклеотидным соединением 14 (200, 400 и 800 нМ) в присутствии (+Lipo) и в отсутствие (-Lipo) липофектина в течение 24 часов в Opti-MEM и затем в течение дополнительных 67 часов в полной среде. Образцы белков (30-40 мкг белка/полоса) анализировали вестерн-блоттингом, как описано в "Материалах и методах", с тубулином, используемым в качестве контроля протеиновых образцов. «С» обозначает контроль.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Таким образом, настоящее изобретение предусматривает полимерно-связанные олигонуклеотидные пролекарства, имеющие большое число практических применений, включая использование в качестве диагностических и аналитических реагентов, в качестве инструментов для исследований и научных изысканий как in vitro, так и in vivo и в качестве терапевтических агентов. Для того чтобы более полно оценить область применения настоящего изобретения, определены следующие термины. Специалисту будет понятно, что термины «нуклеиновая кислота» или «нуклеотид» относятся к дезоксирибонуклеиновой кислоте (ДНК), рибонуклеиновой кислоте (РНК), одноцепочечной или двухцепочечной, если не оговорено специально, и к любым их химическим модификациям. «Олигонуклеотид» в общем представляет собой относительно короткий полинуклеотид, например, с размером в диапазоне от примерно 2 до примерно 200 нуклеотидов, или, более предпочтительно, от примерно 10 до примерно 30 нуклеотидов в длину. Олигонуклеотиды согласно изобретению в общем представляют собой синтетические нуклеиновые кислоты и являются одноцепочечными, если не оговорено специально. В качестве синонимов могут также использоваться термины «полинуклеотид» и «полинуклеиновая кислота».
Модификации олигонуклеотидов по изобретению необязательно включают, например, добавление к или замещение выбранных нуклеотидов функциональными группами или фрагментами, что делает возможным ковалентное связывание олигонуклеотида с заданным полимером, и/или добавление или замещение функциональными фрагментами, которые сообщают олигонуклеотиду дополнительный заряд, поляризуемость, водородные связи, электростатическое взаимодействие и функциональность. Такие модификации включают, но не ограничиваются перечисленным, модификации 2'-положения сахара, модификации 5-положения пиримидина, модификации 8-положения пурина, модификации экзоциклических аминов, замещение 4-тиоуридина, замещение 5-бром- или 5-йодурацила, модификации боковой цепи, метилирование, комбинации комплементарного спаривания оснований нуклеиновых кислот, такие как изооснования изоцитидин и изогуанидин и аналогичные комбинации. Олигонуклеотидные модификации также могут включать 3'- и 5'- модификации, такие как кэппирование.
Термин «антисмысловой» используется здесь по отношению к нуклеотидным последовательностям, которые комплементарны к определенной ДНК или РНК последовательности, кодирующей генный продукт или кодирующей контрольную последовательность. Термин «антисмысловая цепь» используется по отношению к цепи нуклеиновой кислоты, которая комплементарна «смысловой» цепи. При нормальном функционировании клеточного метаболизма смысловая цепь молекулы ДНК представляет собой цепь, которая кодирует полипептиды и/или другие генные продукты. Смысловая цепь служит в качестве матрицы для синтеза транскрипта информационной РНК («мРНК») (антисмысловая цепь), которая, в свою очередь, направляет синтез любого кодируемого генного продукта. Антисмысловые молекулы нуклеиновых кислот могут быть получены любым из способов, известных в данной области техники, включая синтез путем лигирования гена(ов), представляющего(их) интерес, в обратной ориентации к вирусному промотору, что делает возможным синтез комплементарной цепи. После введения в клетку эта транскрибированная цепь объединяется с природными последовательностями, синтезированными клеткой, с образованием дуплексов. Эти дуплексы затем блокируют дальнейшую транскрипцию или трансляцию. Таким образом могут быть генерированы мутантные фенотипы. Обозначения «отрицательная» или «-» также известны в данной области техники и относятся к антисмысловой цепи и «положительная» или «+» также известны в данной области техники и относятся к смысловой цепи.
Например, если необходима понижающая регуляция экспрессии мРНК транскрипта в клетке или клетках, в клетку вводят антисмысловой олигонуклеотид. После введения в клетку антисмысловой нуклеотид гибридизуется с соответствующей мРНК последовательностью за счет связывания Уотсона-Крика, образуя гетеродуплекс. Как только образуется дуплекс, ингибируется трансляция белка связанной мРНК, кодируемого последовательностью. Таким образом, антисмысловые олигонуклеотиды также используются в данной области техники в качестве зондов, например зондов гибридизации, обычно связанные с идентификатором или меткой, как и используются для обеспечения высокоточной понижающей регуляции экспрессии определенных клеточных продуктов или генетических регулирующих элементов, как для исследовательских, так и для терапевтических целей.
В целях настоящего изобретения использование единственного или множественного числа не означает ограничения до определенного численного значения в указываемом пункте или объекте. Таким образом, использование единственного числа по отношению к клетке, полимеру или лекарству не означает, что обрабатывают только одну клетку, только одну молекулу, получают или используют и/или применяют только одно лекарство, и использование множественного числа не исключает применение только к одному указываемому объекту, если не указано непосредственно.
В целях настоящего изобретения термин «остаток» следует понимать как часть биологически-активного соединения, такого как олигонуклеотид, которая сохраняется после того, как оно вступило в реакцию, в которой часть носителя пролекарства присоединили путем модификации, например, доступной гидроксильной или аминогруппы с образованием, например, сложноэфирной или амидной группы соответственно.
А. ОПИСАНИЕ ОЛИГОНУКЛЕОТИДОВ
Один из признаков изобретения состоит в способности обеспечить усовершенствованные нуклеотидные или олигонуклеотидные полимерные конъюгаты. Описанные здесь полимерные системы транспорта не ограничиваются одним типом олигонуклеотида, но, напротив, предназначены для работы с широким разнообразием подобных фрагментов, подразумевая, что полимерные системы транспорта могут быть присоединены к одному или нескольким 3'- или 5'-концам, обычно РО4 или SO4 группам нуклеотида. Последовательности нуклеотидов изображены здесь при использовании принятой номенклатуры, в которой последовательности считывают слева направо, от 5'-конца к 3'-концу (5'- → 3'-).
Х1-3 представляют собой одинаковые или различные нуклеотидные или олигонуклеотидные остатки, которые в целях настоящего изобретения включают олигодезоксинуклеотидные остатки. Более предпочтительно Х1-3 представляют собой независимо выбранные антисмысловые олигонуклеотидные остатки или олигодезоксинуклеотидные остатки.
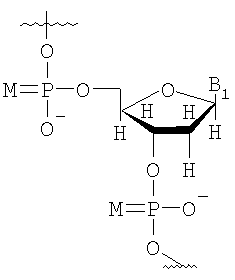
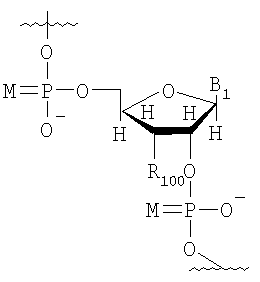
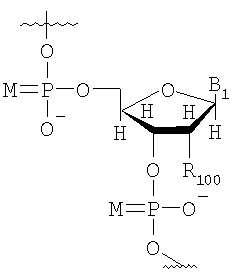
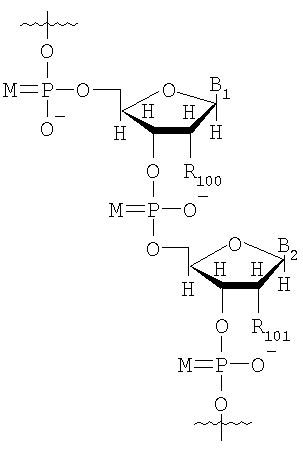
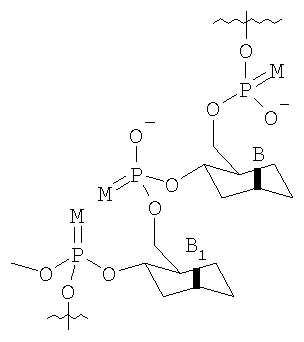
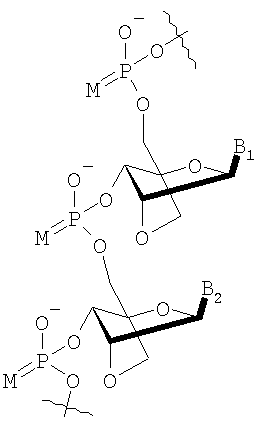
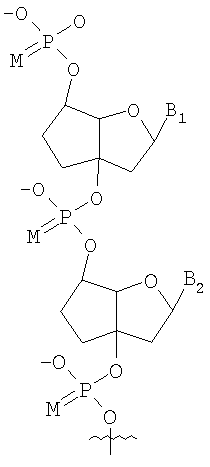
Неограничивающий список потенциальных нуклеотидов, которые могут быть использованы исключительно или в качестве части олигонуклеотида (10-1000 нуклеотидов) включают
 ,
,  ,
, 
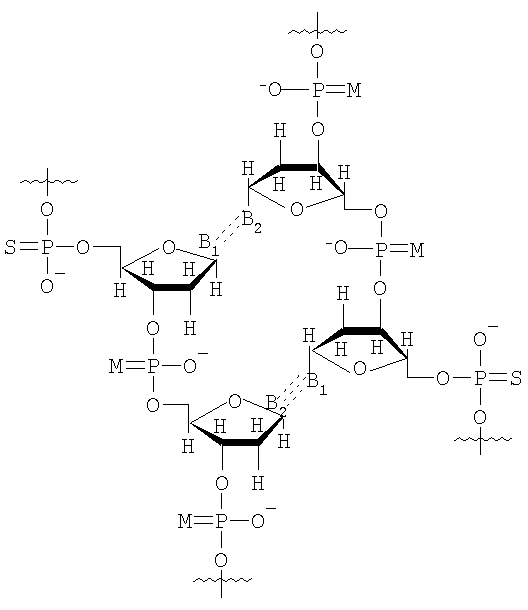
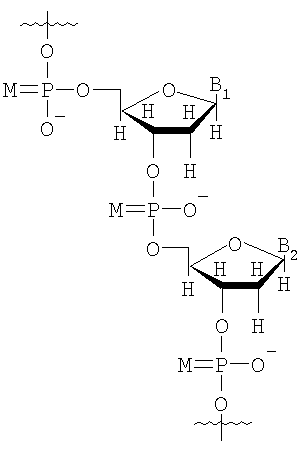 ,
, 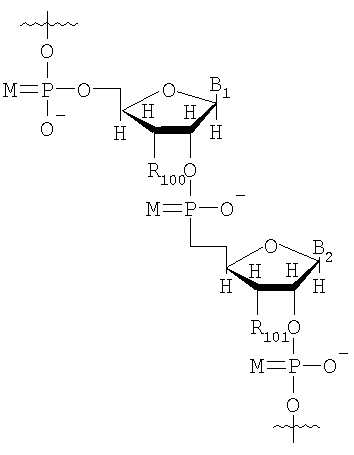 ,
,  ,
,
 ,
, 
 ,
, 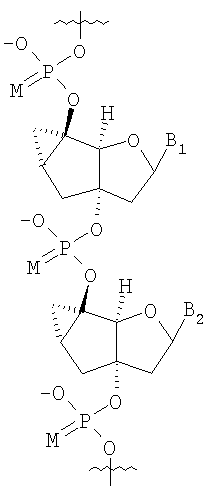 и
и 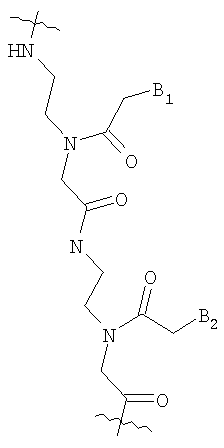
в которых
М представляет собой О или S;
B1 и В2 независимо выбирают из группы, состоящей из А (аденин), G (гуанин), С (цитозин), Т (тимин), U (урацил) и модифицированных оснований;
R100 и R101 независимо выбирают из группы, состоящей из Н, OR', в которой R' представляет собой Н, C1-6 алкил, замещенный алкил, нитро, галоген и арил.
Некоторые из данных олигонуклеотидов и олигодезоксинуклеотидов, используемых в способах по изобретению, включают, но не ограничиваются перечисленным, следующие:
олигонуклеотиды и олигодезоксинуклеотиды с природным фосфородиэфирным остовом или фосфоротиоатным остовом, или любыми другими модифицированными аналогами остова;
ЗНК (замкнутая нуклеиновая кислота);
ПНК (пептидная нуклеиновая кислота);
трицикло-ДНК;
ложный ОДН (двухцепочечный олигонуклеотид);
РНК (каталитическая последовательность РНК);
рибозимы;
зеркально-ориентированные олигонуклеотиды (spiegelmers) (олигонуклеотиды с L-конформацией);
CpG олигомеры и т.п., такие как олигомеры, описанные в:
Tides 2002, Oligonucleotide and Peptide Technology Conferences, 6-8 мая 2002 г., Las Vegas, NV, и
Oligonucleotide and Peptide Technology, 18 и 19 ноября 2003 г., Hamburg, Germany, содержание которых включено здесь в качестве ссылки.
Олигонуклеотиды по изобретению могут также необязательно включать любые пригодные известные в данной области техники нуклеотидные аналоги и производные, включая нуклеотидные аналоги и производные, приведенные в табл.1 ниже.
Представители нуклеотидных аналогов и производных
Предпочтительно антисмысловой олигонуклеотид представляет собой олигонуклеотид, который понижает экспрессию белка, обуславливающего устойчивость опухолевых клеток к противораковой терапии. Например, белок BCL-2 ингибирует высвобождение цитохрома С и фактора, вызывающего апоптоз, из митохондрий и, таким образом, препятствует осуществлению апоптоза.
Раковые клетки, которые имеют высокие уровни BCL-2, таким образом, очень устойчивы как к химиотерапии, так и к радиотерапии. Патент США № 6414134, включенный здесь в качестве ссылки, описывает антисмысловые олигонуклеотиды, понижающие экспрессию белка Bcl-2, который связан с устойчивостью к противораковой терапии в большом числе раковых клеток, например, включая клетки рака предстательной железы, клетки миеломы и другие опухолевые клетки. Согласно упомянутому выше патенту США полагают, что ген bcl-2 способствует патогенезу рака, в первую очередь повышая коэффициент выживаемости опухолевых клеток, а не ускоряя клеточное деление. Патент США № 6414134 в общем виде описывает антисмысловые олигонуклеотиды длиной от 17 до 35 оснований, которые комплементарны мРНК bcl-2 и которые включают молекулу нуклеиновой кислоты, имеющую последовательность TACCGCGТGCGACCCTC (SEQ ID NO: 5). Они предпочтительно включают по крайней мере одну фосфоротиоатную связь.
Другие известные в данной области техники клеточные белки, которые рассматриваются различными компаниями в качестве мишеней для понижения их экспрессии антисмысловыми олигонуклеотидами, для противораковой терапии, приведены в следующей табл.2.
Антисмысловые олигонуклеотиды, пригодные для использования для понижающей регуляции экспрессии белков, связанных с выживаемостью раковых клеток, такой как экспрессия bcl-2, включают олигонуклеотиды, которые имеют от примерно двух до двухсот нуклеотидных кодонов, более предпочтительно от десяти до сорока кодонов и наиболее предпочтительно примерно от 17 до 20 кодонов. Эти олигонуклеотиды предпочтительно выбраны из олигонуклеотидов, комплементарных стратегическим сайтам в цепи предшественника мРНК bcl-2, таких как сайты инициации трансляции, донорные или сплайсинговые сайты, или сайты переноса или разрушения.
Блокировка трансляции в этих стратегических сайтах предотвращает образование функционального bcl-2 генного продукта. Следует понимать, однако, что любая комбинация или субкомбинация антикодирующих олигомеров, включая олигонуклеотиды, комплементарные или в значительной степени комплементарные по отношению к bcl-2 предшественнику мРНК или мРНК, которые ингибируют пролиферацию клеток, пригодна для использования в изобретении. Например, олигодезоксинуклеотиды, комплементарные частям последовальности на смежных или несмежных фрагментах bcl-2 РНК, могут ингибировать пролиферацию клеток и будут, таким образом, пригодны для использования в способах по изобретению.
Олигонуклеотиды, пригодные для понижающей регуляции экспрессии bcl-2, также включают олигонуклеотиды, комплементарные или в значительной степени комплементарные частям последовательности фланкирующей стратегические и другие сайты вдоль bcl-2 мРНК. Части фланкирующей последовательности предпочтительно находятся в диапазоне от примерно двух до примерно ста оснований до и после ранее указанных сайтов вдоль bcl-2 мРНК. Длина этих сайтов предпочтительно находится в диапазоне от примерно пяти до примерно двадцати кодонов. Также предпочтительно, чтобы олигонуклеотиды были комплементарны части последовательности предшественника мРНК или мРНК, которые обычно не содержатся в предшественнике мРНК или мРНК других генов, для того чтобы минимизировать гомологию олигонуклеотидов предшественника мРНК или мРНК кодирующих цепочек других генов.
Ряд предпочтительных антисмысловых или комплиментарных олигонуклеотидов для понижающей регуляции bcl-2 приведен в табл.3.
Будет понятно, что могут использоваться антисмысловые олигонуклеотиды, которые включают больше или меньше замещенных нуклеотидов и/или которые имеют большее протяжение вдоль bcl-2 мРНК цепи или в 3'- или в 5'-направлении, по отношению к олигонуклеотидам, перечисленным в табл.3 выше.
Предпочтительно, антисмысловые олигонуклеотиды, применяемые в пролекарствах по изобретению, имеют одну и ту же, или в значительной степени сходную нуклеотидную последовательность как имеет Genasense (a/k/a облимерсен натрия, производимый Genta Inc, Berkeley Heights, NJ). Genasense представляет собой 18-мерный фосфоротиоатный антисмысловой олигонуклеотид, TCTCCCAGCGTGCGCCAT (SEQ ID NO: 1), который комплементарен первым шести кодонам инициирующей последовательности bcl-2 мРНК человека (человеческая bcl-2 мРНК хорошо известна в данной области техники и описана, например, как SEQ ID NO: 19 в патенте США № 6414134, включенном здесь в качестве ссылки). Управление по контролю за продуктами и лекарствами США (FDA) придало Genasense статус «Orphan» в августе 2000 г. и приняло Заявку на новый препарат (NDA) для Genasense для лечения рака. NDA предлагает введение Genasense в комбинации с дакарбозином для лечения пациентов с генерализованной меланомой, которую ранее не лечили химиотерапией. Дополнительно FDA придала данной заявке статус приоритетной экспертизы (priority review), что имеет целью деятельность не позднее 8 июня 2004 г. См. также публикацию Chi et al., 2001, Clinical Cancer Research, vol. 7, 3920-3927, включенную здесь в качестве ссылки, подтверждающую активность Genasense в комбинированной терапии рака предстательной железы в ранних клинических испытаниях. Пролекарства по настоящему изобретению имеют такое же применение, как и идентифицированное для нативного (немодифицированного) 18-мера.
Было показано, что Genasense характеризуется понижением продукции белка Bcl-2 и улучшает чувствительность опухолевых клеток к терапии и в конечном счете вызывает смерть клеток. Ряд исследований показал многообещающие результаты при лечении нескольких видов рака Genasense в сочетании с противораковыми агентами. Фаза I/II испытания Genasense в комбинации с дакарбозином у пациентов с меланомой показал многообещающую активность и фаза III мультицентрового испытания проводится в настоящее время. Дополнительно, Genasense, используемый в комбинации с митоксантроном у пациентов с гормонорефрактерным раком предстательной железы, показал многообещающие результаты. Kim et al., 2001, там же.
Сочетание антисмысловых олигонуклетидов, таких как Genasense, с полимерами представляет собой пример одного предпочтительного варианта исполнения изобретения.
В альтернативных вариантах осуществления дополнительные пригодные антисмысловые олигонуклеотиды включают:
T-C-T-C-C-C-A-G-C-G-T-G-C-G-C-C-A-T (соединение 13, SEQ ID NO: 1);
T-C-T-C-C-C-A-G-C-A-T-G-Т-G-C-C-A-T (соединение 36, SEQ ID NO: 2);
A-T-C-C-T-A-A-G-C-G-T-G-C-G-C-C-T-T (соединение 37, SEQ ID NO: 3); и
T-C-T-C-C-C-A-G-X-G-T-G-X-G-C-C-A-T (соединение 38, SEQ ID NO: 4),
а также олигонуклеотиды, представленные в других примерах.
В. ФОРМУЛА (I)
В одном предпочтительном исполнении изобретения обеспечиваются олигонуклеотидные пролекарства формулы (I):
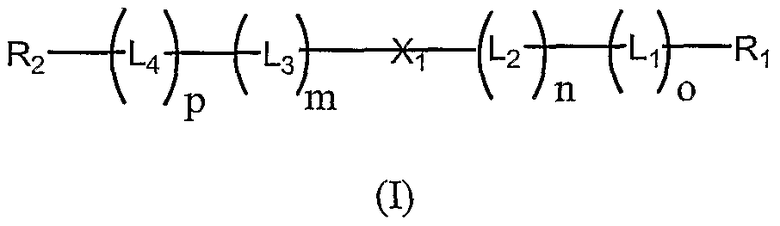
в которой
R1 и R2 независимо представляют собой Н или полимерный остаток;
L1 и L4 представляют собой независимо выбираемые высвобождаемые линкерные фрагменты;
L2 и L3 представляют собой независимо выбираемые спейсерные группы;
X1 представляет собой нуклеотидный остаток или олигонуклеотидный остаток;
m, n, o и p независимо выбирают из нуля или положительного целого числа, при условии, что (о+n) или (р+m)≥2.
Полимерная система транспорта по настоящему изобретению базируется, по крайней мере частично, на одном R1 и R2, предпочтительно представляющем собой полимерный остаток, необязательно имеющий кэппирующую группу, обозначаемую здесь как А. Пригодные кэппирующие группы включают, например, ОН, NH2, SH, CO2H, C1-6 алкилы, а также олигонуклеотидсодержащие группы, такие как
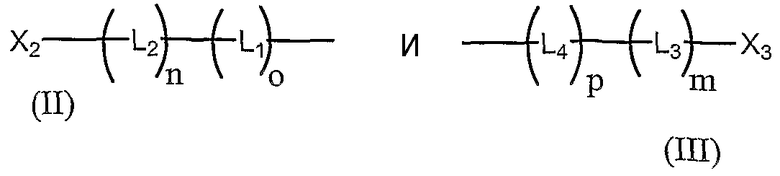
в которых Х2 и Х3 или такие же, как Х1, или представляют собой другой нуклеотидный или олигонуклеотидный остаток.
Предпочтительные кэппирующие группы (II) или (III) позволяют образовывать композиции с формулами (i), (ii), (iii) и (iv), показанные ниже.
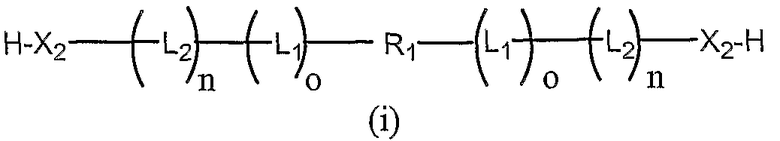
бис-3'-олигонуклеотид,
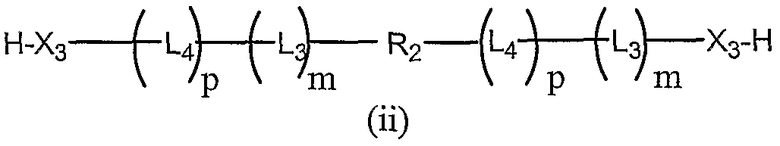
бис-5'-олигонуклеотид,

бис-5',3'-олигонуклеотид и
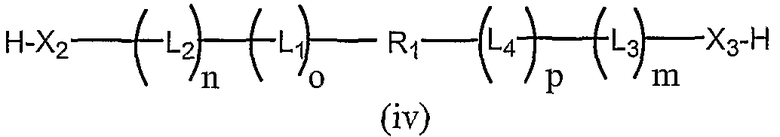
бис-3',5'-олигонуклеотид,
в которых все переменные такие же, как описано ранее.
В другом предпочтительном варианте исполнения изобретения L4 представляет собой высвобождаемый линкерный фрагмент, выбранный из формул
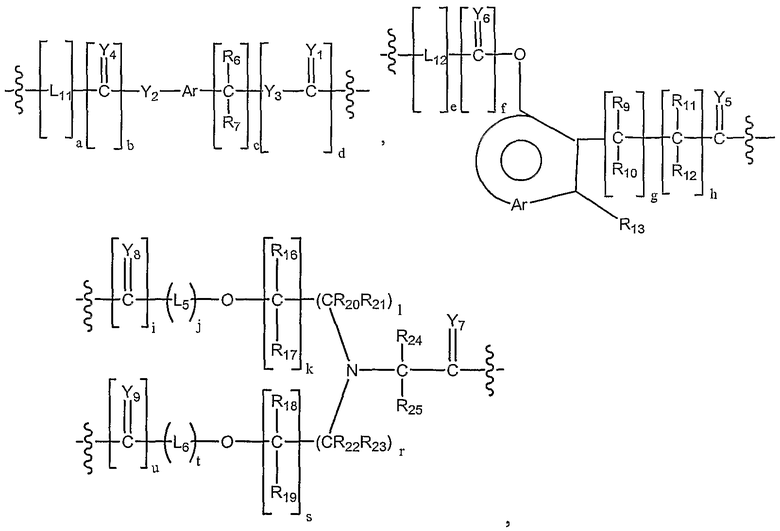
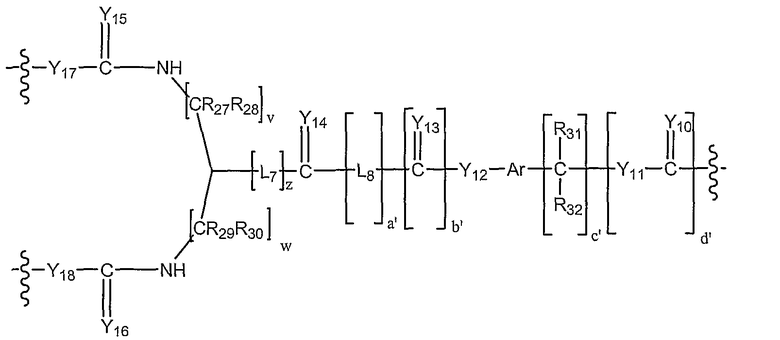
и
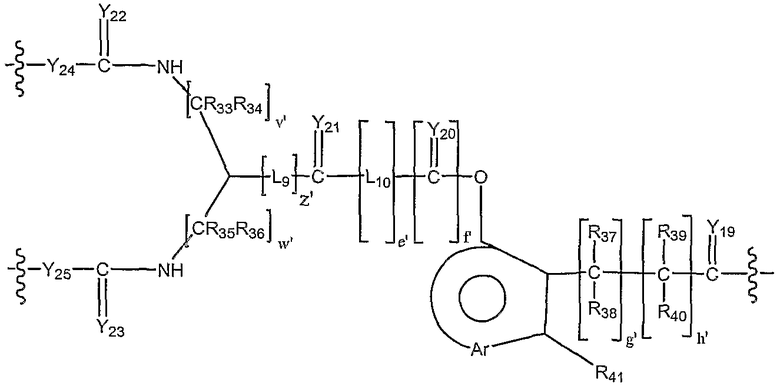
в которых
Y1-25 независимо выбирают из группы, состоящей из О, S или NR9;
R6-7, R9-13, R16-25 и R27-41 представляют собой независимо выбранные из группы, состоящей из водорода, С1-6 алкилов, С3-12 разветвленных алкилов, С3-8 циклоалкилов, С1-6 замещенных алкилов, С3-8 замещенных циклоалкилов, арилов, замещенных арилов, арилалкилов, С1-6 гетероалкилов, замещенных С1-6 гетероалкилов, С1-6 алкокси, фенокси и С1-6 гетероалкокси;
Ar представляет собой фрагмент, который образует мультизамещенный ароматический углеводород или мультизамещенную гетероциклическую группу;
L5-12 независимо представляют собой бифункциональные спейсеры;
Z выбирают из фрагментов, активно траспортируемых в клетку-мишень, гидрофобных фрагментов, бифункциональных линкерных фрагментов и их комбинаций;
c, h, k, l, r, s, v, w, v', w', c' и h' представляют собой независимо выбранные положительные целые числа;
а, e, g, j, t, z, a', z', e' и g' независимо представляют собой или ноль, или положительное целое число; и
b, d, f, i, u, q, b', d' и f' независимо представляют собой ноль или единицу.
В другом предпочтительном варианте осуществления L1 представляет собой высвобождаемый линкерный фрагмент, выбранный из формул:
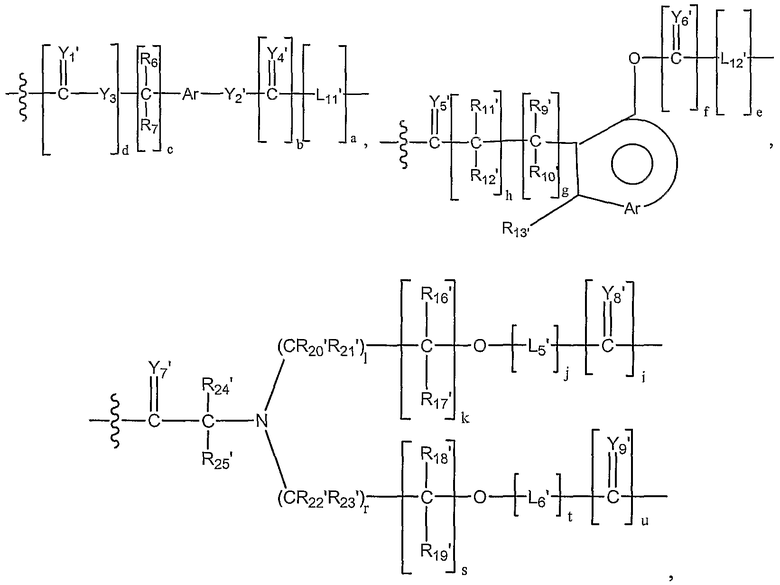
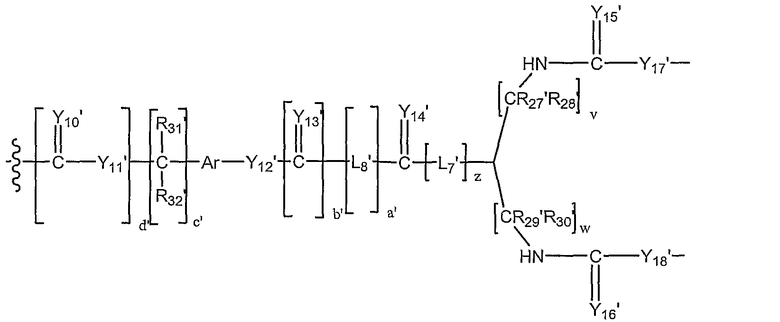
и
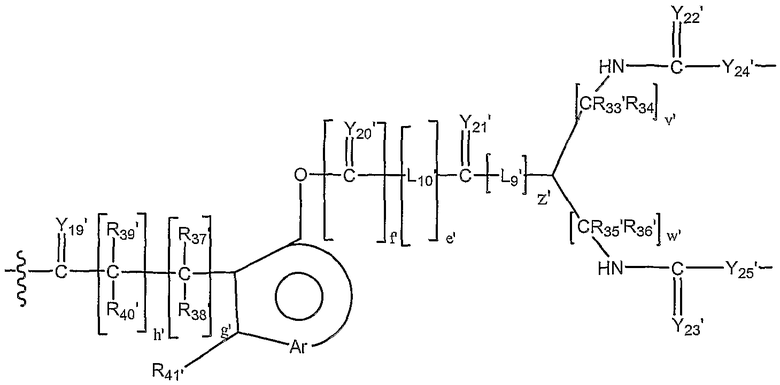
в которых
Y1'-25' представляют собой независимо выбранные из группы, состоящей из О, S или NR9;
R6'-7', R9'-13', R16'-25' и R27'-41' представляют собой независимо выбранные из группы, состоящей из водорода, С1-6 алкилов, С3-12 разветвленных алкилов, С3-8 циклоалкилов, С1-6 замещенных алкилов, С3-8 замещенных циклоалкилов, арилов, замещенных арилов, арилалкилов, С1-6 гетероалкилов, замещенных С1-6 гетероалкилов, С1-6 алкокси, фенокси и С1-6 гетероалкокси; и
L5'-12' представляют собой независимо выбранные бифункциональные спейсеры.
В некоторых предпочтительных вариантах осуществления изобретения L5-12 независимо представляют собой бифункциональные спейсеры, выбранные из
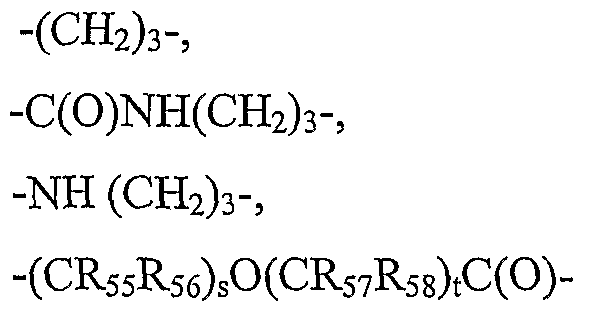
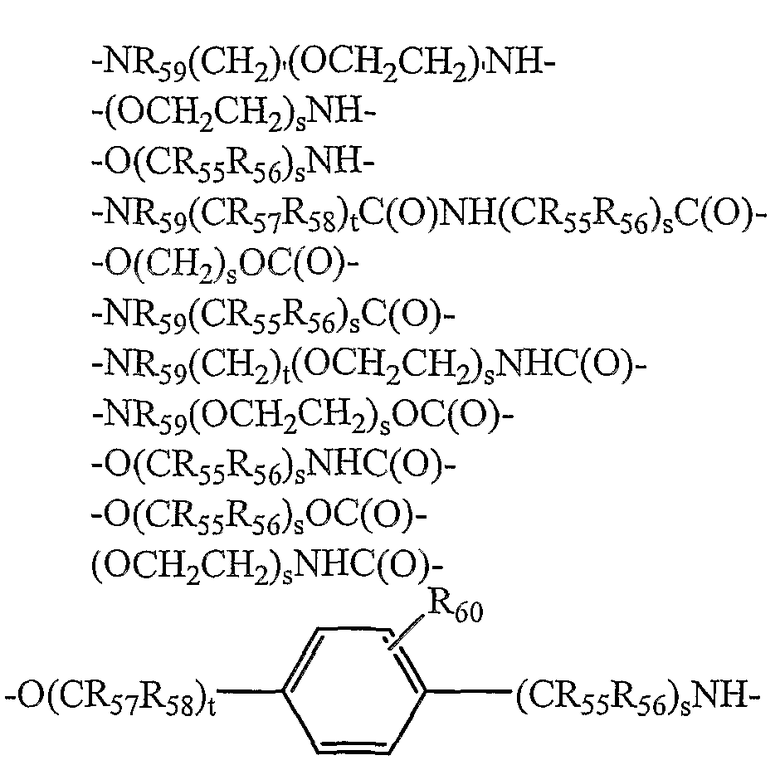
и
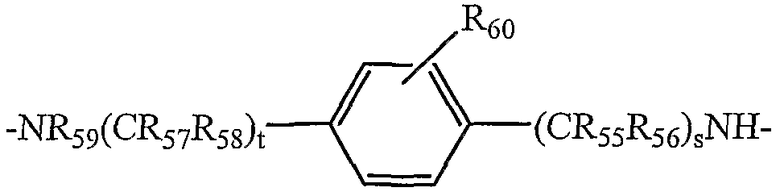
и L5'-12' независимо представляют собой бифункциональные спейсеры, выбранные из
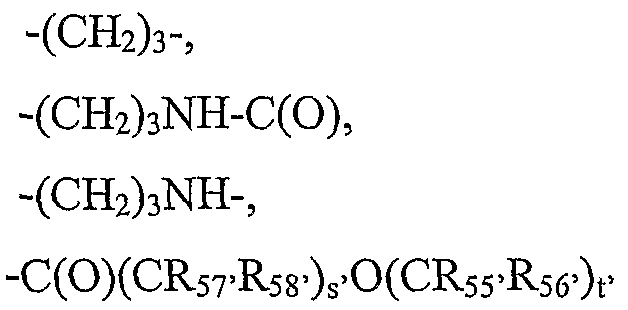
и
в которых:
R55-R59 и R55'-59' независимо выбраны из группы, состоящей из водорода, С1-6 алкилов, С3-12 разветвленных алкилов, С3-8 циклоалкилов, С1-6 замещенных алкилов, С3-8 замещенных циклоалкилов, арилов, замещенных арилов, арилалкилов, С1-6 гетероалкилов, замещенных С1-6 гетероалкилов, С1-6 алкокси, фенокси и С1-6 гетероалкокси, и
R60 и R60' выбраны из группы, состоящей из водорода, С1-6 алкилов, С3-12 разветвленных алкилов, С3-8 циклоалкилов, С1-6 замещенных алкилов, С3-8 замещенных циклоалкилов, арилов, замещенных арилов, арилалкилов, С1-6 гетероалкилов, замещенных С1-6 гетероалкилов, С1-6 алкокси, фенокси, С1-6 гетероалкокси, NO2, галогеналкила и галогена; и
s' и t', каждый, представляет собой положительное целое число.
В другом предпочтительном варианте осуществления изобретения L2 и L3 независимо представляют собой спейсерные группы, имеющие от примерно 1 до примерно 60 атомов углерода и от примерно 1 до 10 гетероатомов. Предпочтительно L2 и L3 независимо представляют собой спейсерные группы, имеющие от примерно 2 до примерно 10 атомов углерода и от примерно 1 до примерно 6 гетероатомов. Наиболее предпочтительно L3 выбирают из
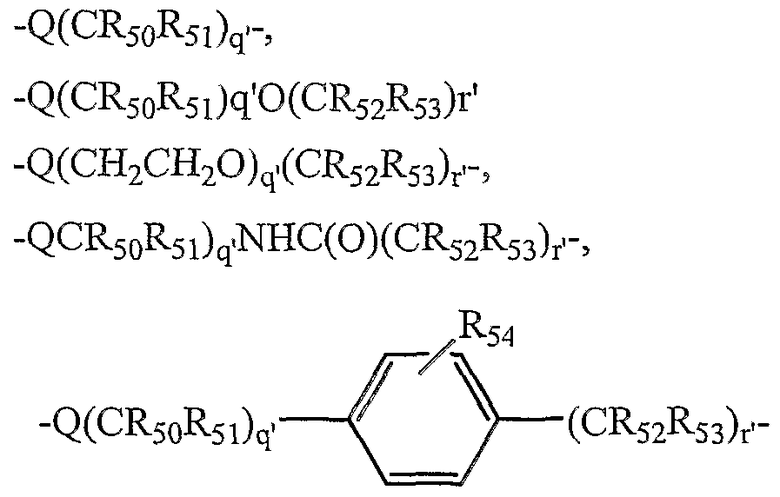
и
 и
и
наиболее предпочтительно L2 выбирают из
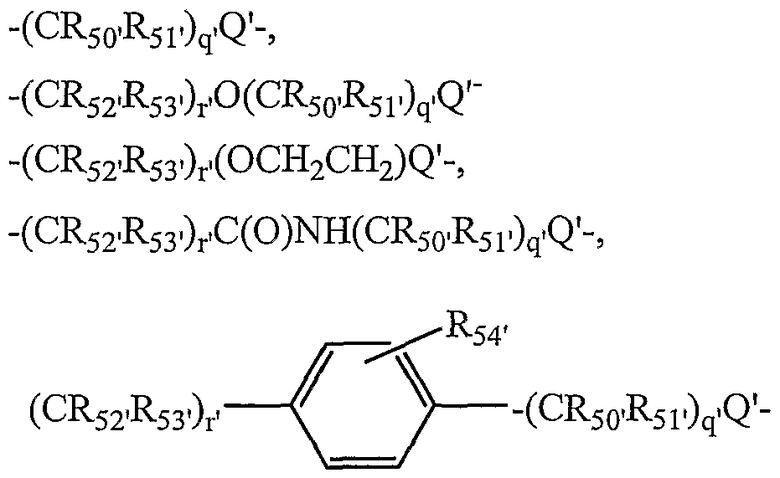
и

в которых
Q и Q' независимо выбирают из О, S и NH;
R50-53 и R50'-53' независимо выбраны из группы, состоящей из водорода, С1-6 алкилов, С3-12 разветвленных алкилов, С3-8 циклоалкилов, С1-6 замещенных алкилов, С3-8 замещенных циклоалкилов, арилов, замещенных арилов, арилалкилов, С1-6 гетероалкилов, замещенных С1-6 гетероалкилов, С1-6 алкокси, фенокси, С1-6 гетероалкокси;
R54 и R54' независимо выбраны из группы, состоящей из водорода, С1-6 алкилов, С3-12 разветвленных алкилов, С3-8 циклоалкилов, С1-6 замещенных алкилов, С3-8 замещенных циклоалкилов, арилов, замещенных арилов, арилалкилов, С1-6 гетероалкилов, замещенных С1-6 гетероалкилов, С1-6 алкокси, фенокси, С1-6 гетероалкокси, NO2, галогеналкила и галогена; и
q' и r', каждый, представляет собой положительное целое число.
C точки зрения других переменных, которые содержатся в формулах по настоящему изобретению, предпочтительны следующие:
Y1-25 и Y1'-25' представляют собой независимо выбранные из группы, состоящей из О, S или NR9;
R6-7, R9-13, R16-25, R27-41 и R6'-7', R9'-13', R16'-25' и R27'-41' представляют собой независимо выбранные из группы, состоящей из водорода, С1-6 алкилов, С3-8 циклоалкилов, арилов, арилалкилов и С1-6 гетероалкилов;
c, h, k, l, r, s, v, w, v', w', c' и h' представляют собой единицу;
а, e, g, j, t, z, a', z', e' и g' независимо представляют собой или ноль, или единицу; и
b, d, f, i, u, q, b', d' и f' независимо представляют собой ноль или единицу.
В еще одном предпочтительном варианте осуществления изобретения обеспечиваются соединения формулы (Ia):
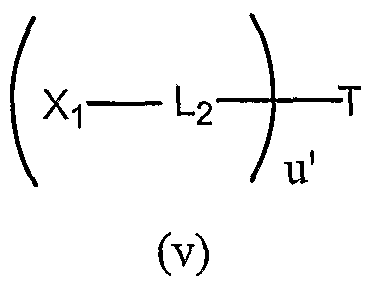
в которой
L2 представляет собой спейсерную группу;
X1 представляет собой нуклеотидный или олигонуклеотидный остаток;
u' представляет собой положительное целое число;
T представляет собой разветвленный полимер, который предпочтительно выбран из соединений, описанных в поданных обычным образом РСТ публикациях номер WO 02/065988 и WO 02/066066, описание каждой из которых включено здесь в качестве ссылки. В пределах этой общей формулы следующие являются предпочтительными:
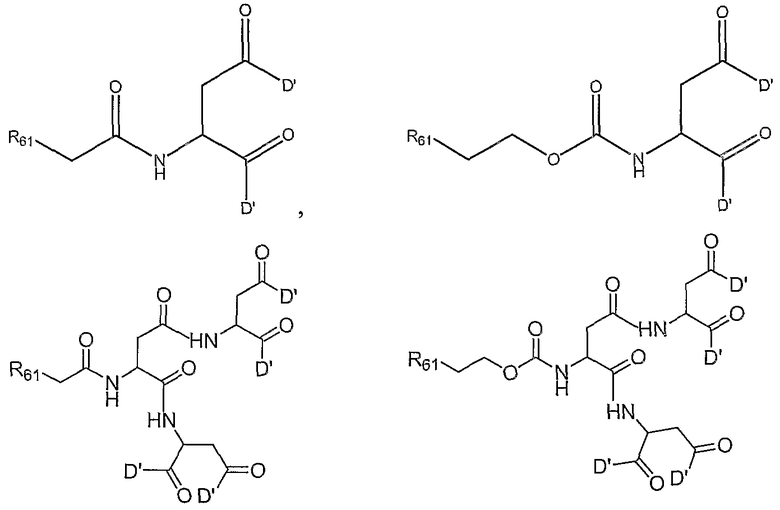
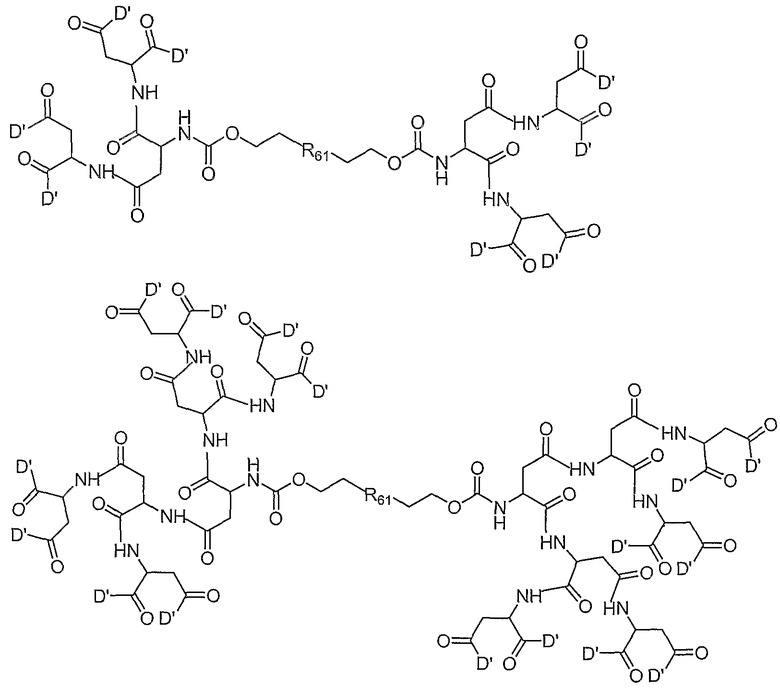
и
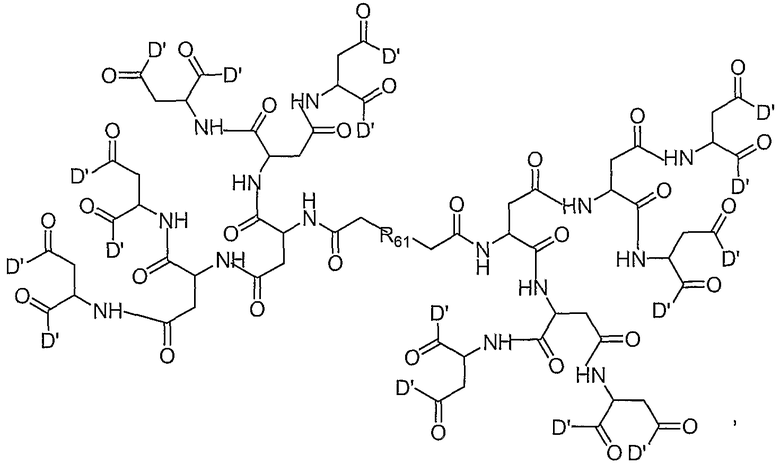
в которых D' является одним из
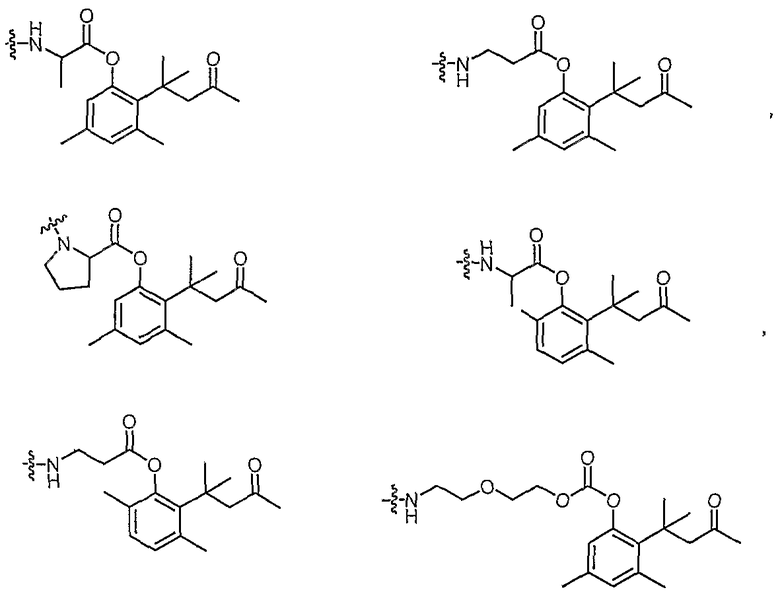
и
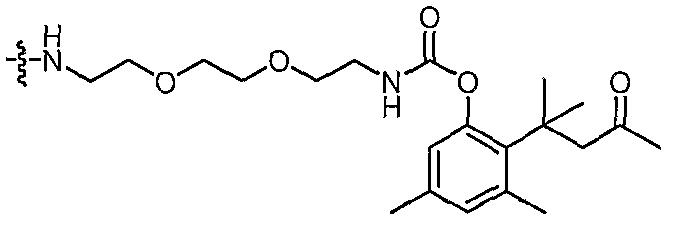
в которых R61 представляет собой полимерный остаток, такой как определен для R1, понимая, что полимер может быть бифункциональным, если R61 показан с заместителями на обоих концах; и все прочие переменные являются такими же, как описано выше.
В целях иллюстрации неограничивающим соединением формулы (Ia) является:
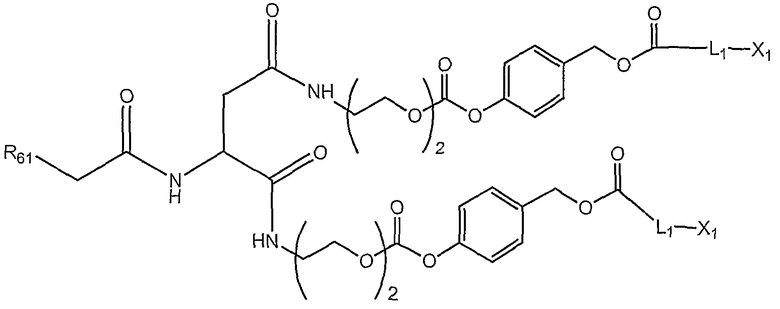
в котором все переменные представляют собой такие же, как описано выше.
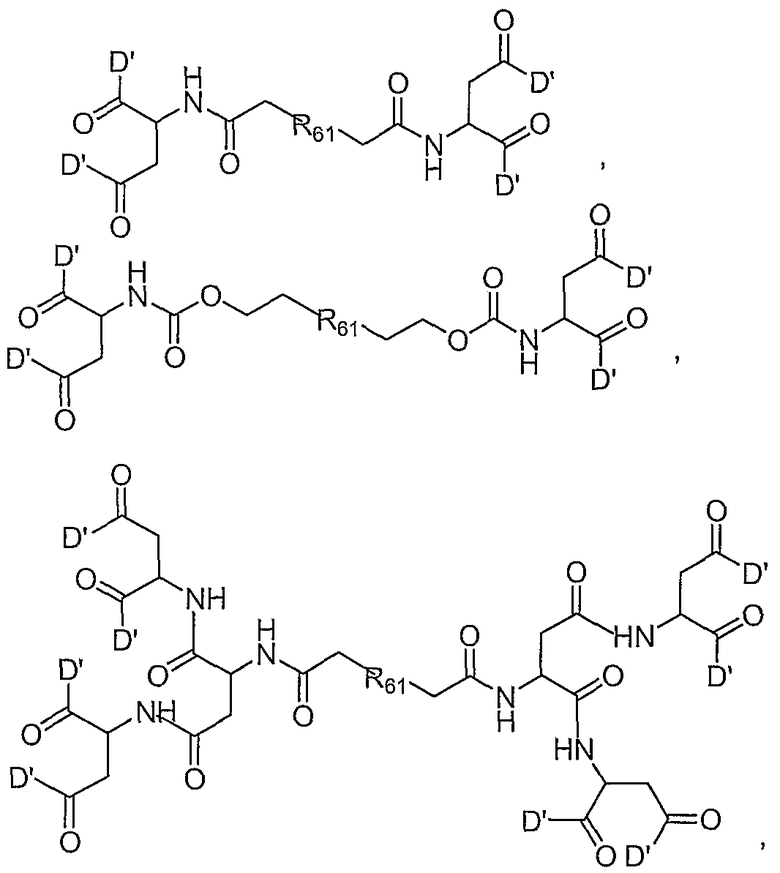
Другой аспект формулы (Ia) включает бифункциональные соединения, которые образованы в том случае, если полимерный остаток (R61) включает обе альфа- и омега-терминальные линкерные группы, так что доставляются по крайней мере четыре олигонуклеотида. Примеры таких полимерных конъюгатов проиллюстрированы ниже как формулы (vi) и (vii)
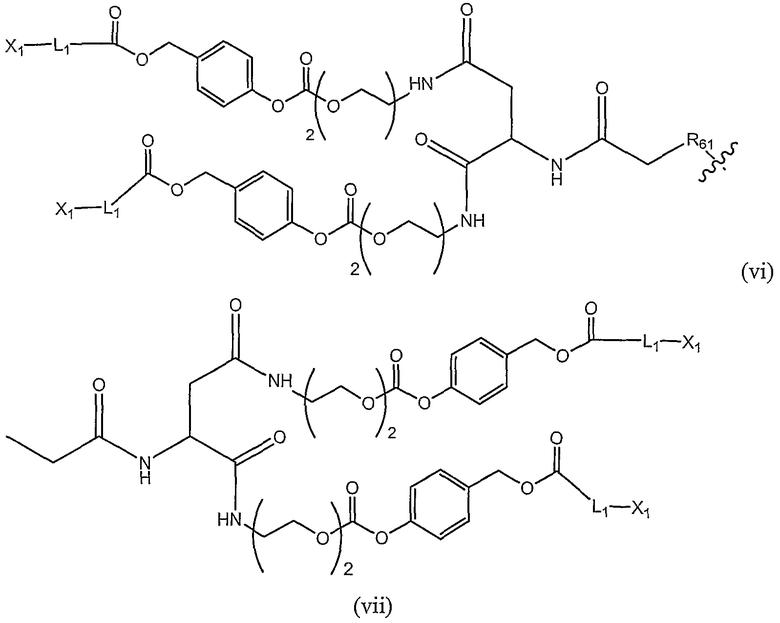
в которых все переменные представляют собой такие же, как описано выше.
В другом предпочтительном варианте осуществления изобретения L2 и L3 независимо представляют собой спейсерные группы, имеющие от примерно 1 до примерно 60 атомов углерода и от примерно 1 до примерно 10 гетероатомов. Предпочтительно L2 и L3 независимо представляют собой спейсерные группы, имеющие от примерно 2 до примерно 10 атомов углерода и от примерно 1 до примерно 6 гетероатомов. Наиболее предпочтительно L3 выбирают из
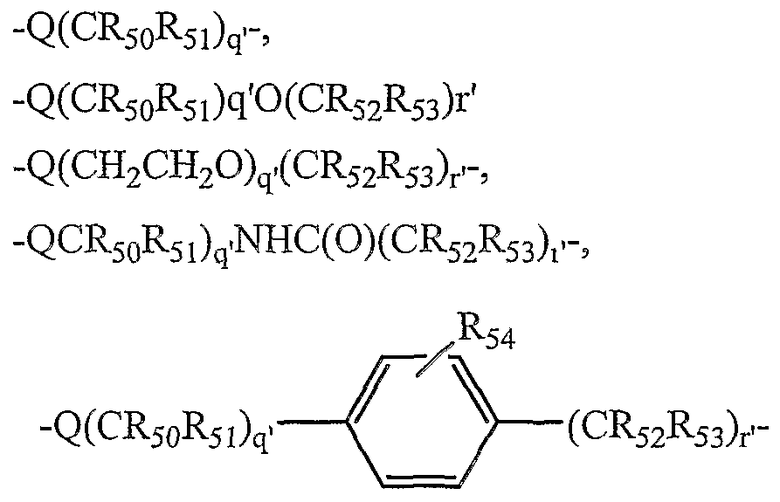
и
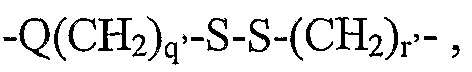 и
и
наиболее предпочтительно L2 выбирают из
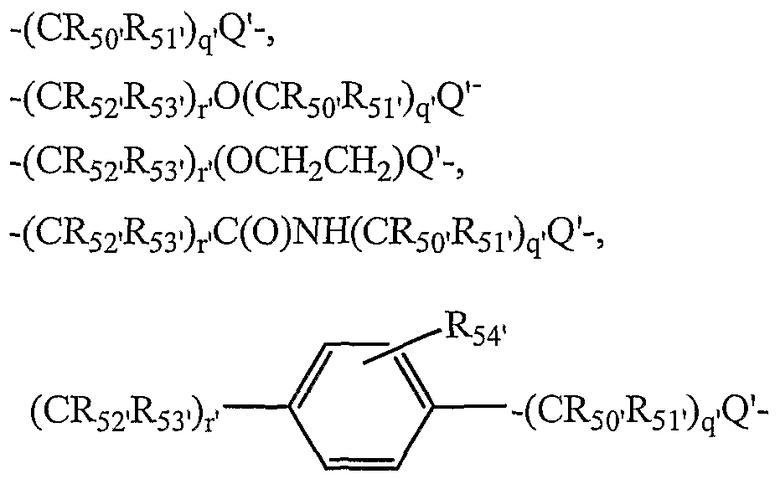
и
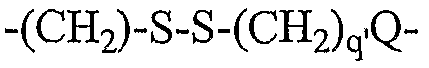 ,
,
в которых
Q и Q' независимо выбирают из О, S или NH;
R50-53 и R50'-53' независимо выбраны из группы, состоящей из водорода, С1-6 алкилов, С3-12 разветвленных алкилов, С3-8 циклоалкилов, С1-6 замещенных алкилов, С3-8 замещенных циклоалкилов, арилов, замещенных арилов, арилалкилов, С1-6 гетероалкилов, замещенных С1-6 гетероалкилов, С1-6 алкокси, фенокси, С1-6 гетероалкокси;
R54 и R54' независимо выбраны из группы, состоящей из водорода, С1-6 алкилов, С3-12 разветвленных алкилов, С3-8 циклоалкилов, С1-6 замещенных алкилов, С3-8 замещенных циклоалкилов, арилов, замещенных арилов, арилалкилов, С1-6 гетероалкилов, замещенных С1-6 гетероалкилов, С1-6 алкокси, фенокси, С1-6 гетероалкокси, NO2, галогеналкила и галогена; и
q' и r', каждый, представляют собой положительное целое число.
C точки зрения других переменных, которые содержатся в формулах по настоящему изобретению, предпочтительны следующие:
Y1-25 и Y1'-25' представляют собой независимо выбранные из группы, состоящей из О, S или NR9;
R6-7, R9-13, R16-25, R27-41 и R6'-7', R9'-13', R16'-25' и R27'-41' представляют собой независимо выбранные из группы, состоящей из водорода, С1-6 алкилов, С3-8 циклоалкилов, арилов, арилалкилов и С1-6 гетероалкилов;
c, h, k, l, r, s, v, w, v', w', c' и h' представляют собой единицу;
а, e, g, j, t, z, a', z', e' и g' независимо представляют собой или ноль, или единицу; и
b, d, f, i, u, q, b', d' и f' независимо представляют собой ноль или единицу.
С. ОПИСАНИЕ Ar ФРАГМЕНТА
В определенных аспектах изобретения можно видеть, что Ar фрагмент представляет собой фрагмент, который при включении в формулу (I) образует полизамещенный ароматический углеводород или мультизамещенную гетероциклическую группу. Основная характеристика состоит в том, что Ar фрагмент является по своей природе ароматическим. Обычно, чтобы быть ароматическим, пи электроны должны распределяться в «облаке» над и под плоскостью циклической молекулы. Более того, число пи электронов должно удовлетворять правилу Хюккеля (4n+2). Средние специалисты в данной области поймут, что существует бесчисленное число фрагментов, которые будут удовлетворять требованиям для ароматичности фрагмента в формуле (I) и, таким образом, будут пригодны для использования здесь.
Некоторые в особенности предпочтительные ароматические группы включают:
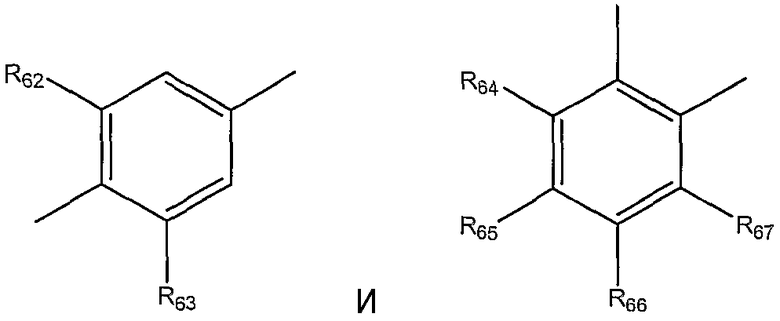
в которых R62-67 независимо выбраны из той же группы, которая определяет R6.
Другие предпочтительные ароматические углеводородные фрагменты включают, но не ограничиваются
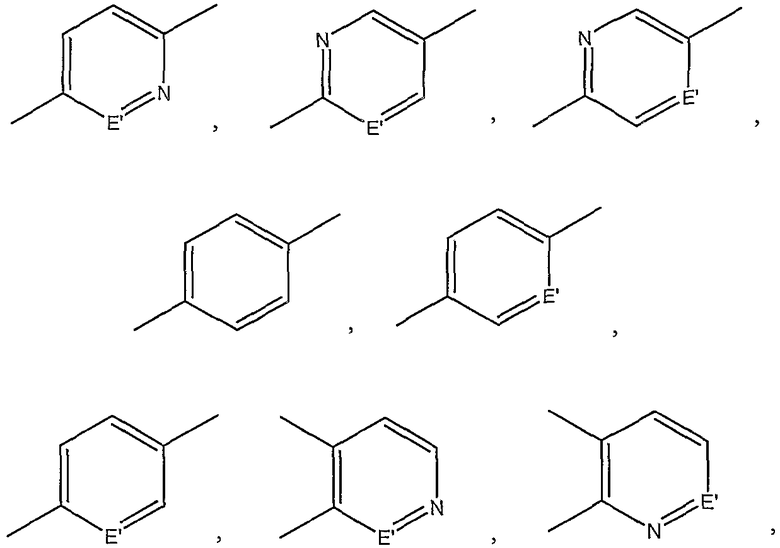
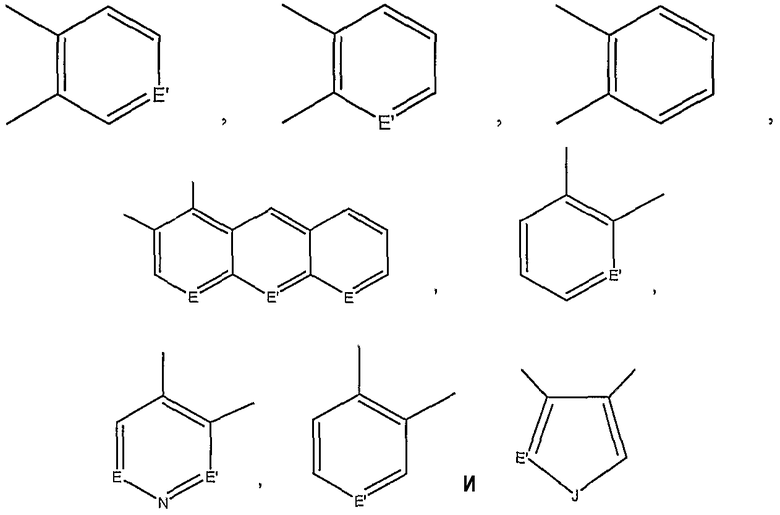
в которых E и Е' независимо представляют собой СR68 или NR69; и J представляет собой О, S или NR70, в которых R68-70 выбирают из той же группы, что и определено для R6, или циано, нитро, карбоксила, ацила, замещенного ацила или карбоксиалкила. Также охватываются изомеры пяти и шестичленных циклов, как и бензо-, и дибензо-системы и имеющие к ним отношение родственные соединения. Специалисту без особых навыков в данной области также будет понятно, что ароматические кольца также могут необязательно быть замещены гетероатомами, такими как О, S, NR9 и т.д., при условии, что правило Хюккеля все еще соблюдается. Более того, ароматические или гетероциклические структуры могут также необязательно быть замещены галогеном(ами) и/или боковыми цепями, как эти термины обычно понимают в данной области техники.
D. ПОЛИАЛКИЛЕНОКСИДЫ
Обращаясь к формуле (I), можно видеть, что R1 и R2 представляют собой полимерные фрагменты, такие как полиалкиленоксид. Пригодные примеры таких полимеров включают полиэтиленгликоли, которые, по существу, не являются антигенными. Также пригодны полипропиленгликоли, такие как те, которые описаны в поданных обычным образом патентах США №№ 5643575, 5919455 и 6113906. Другие PEG, пригодные в способах по изобретению, описаны в Shearwater Polymers, Inc. каталоге «Polyethylene Glycol and Derivates 2001». Описание каждого из перечисленных включено здесь в качестве ссылки. R1 и R2 предпочтительно представляют собой PEG производные, например -О-(СН2СН2О)х-. В этом аспекте R1-2 представляют собой независимо выбранные из
J-O-(CH2CH2O)n'-
J-O-(CH2CH2O)n'-СН2С(O)-O-,
J-O-(CH2CH2O)n'-CH2CH2NR48-,
J-O-(CH2CH2O)n'-CH2CH2S-,
-O-C(O)CH2-O-(CH2CH2O)n'-CH2C(O)-О-,
-NR48CH2CH2-O-(CH2CH2O)n'-CH2CH2NR48-,
-SCH2CH2-O-(CH2СН2O)n'-CH2CH2S-,
в которых
n' представляет собой степень полимеризации, выбранную таким образом, что средневесовая молекулярная масса составляет по крайней мере от 2000 Да до примерно 136000 Да;
R48 выбран из группы, состоящей из водорода, C1-6 алкилов, С3-12 разветвленных алкилов, С3-8 циклоалкилов, C1-6 замещенных алкилов, С3-8 замещенных циклоалкилов, арилов, замещенных арилов, арилалкилов, C1-6 гетероалкилов, замещенных C1-6 гетероалкилов, C1-6 алкокси, фенокси и C1-6 гетероалкокси, и
J представляет собой кэппирующую группу, такую как метил или дополнительную линкерную группу, которая позволяет получить бифункциональный полимер.
Хотя РАО и PEG могут в значительной степени отличаться по молекулярному весу, предпочтительно R1 и R2 независимо имеют средневесовую молекулярную массу от примерно 2000 Да до примерно 136000 Да в большинстве аспектов изобретения. Более предпочтительно R1 и R2 независимо имеют средневесовую молекулярную массу от примерно 3000 Да до примерно 100000 Да, с наиболее предпочтительной средневесовой молекулярной массой от примерно 5000 Да до примерно 40000 Да.
Полимерные вещества, включенные здесь, предпочтительно являются водорастворимыми при комнатной температуре.
Неограничивающий список таких полимеров включает гомополимеры полиалкиленоксида, такие как полиэтиленгликоль (PEG) или полипропиленгликоли, полиоксиэтиленированные полиспирты, их сополимеры и их блок-сополимеры, обеспечивая, чтобы поддерживалась растворимость блок-сополимера в воде.
Е. СИНТЕЗ КОНЪЮГАТОВ ОЛИГОНУКЛЕОТИДОВ С ПОЛИМЕРАМИ
Обычно пролекарства получают
а) взаимодействием соединения формулы:
R2-L4-уходящая группа
с соединением формулы
Н-L3-Х1
при условиях, достаточных для образования пролекарства формулы
R2-L4-L3-Х1,
в которой
R2 представляет собой полимерный остаток;
L4 представляет собой высвобождаемый линкерный фрагмент;
L3 представляет собой спейсерную группу;
Х1 представляет собой нуклеотидный или олигонуклеотидный остаток.
В этом аспекте изобретения предпочтительно использовать активированные полимеры, которые уже включают присоединенные к ним высвобождаемые линкеры. Неограничивающий список пригодных комбинаций включает высвобождаемые транспортные системы на основе PEG, описанные в поданных обычным образом патентах США №№ 6624142, 6303569, 5965119, 6566506, 5965119, 6303569, 6624142 и 6180095, содержание каждого из которых включено здесь в качестве ссылки.
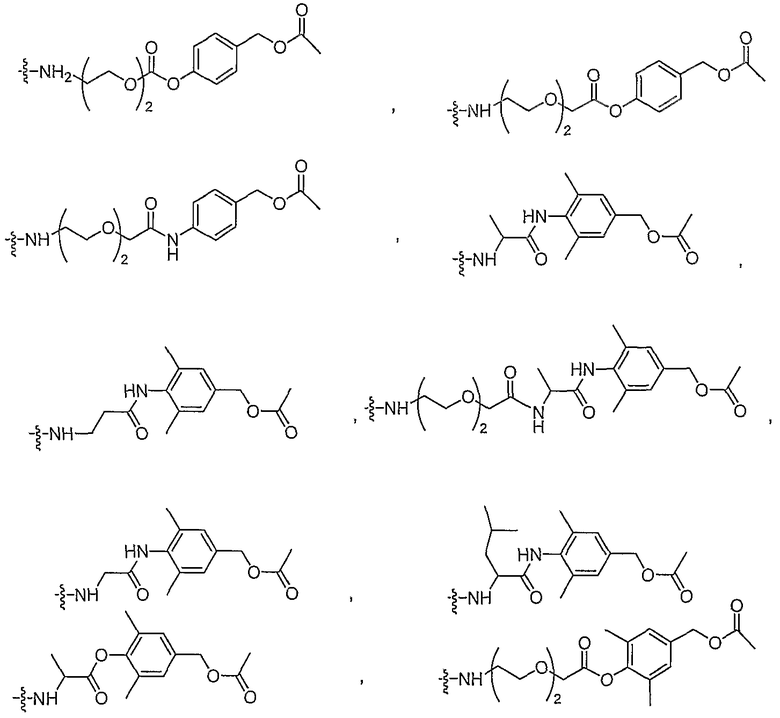
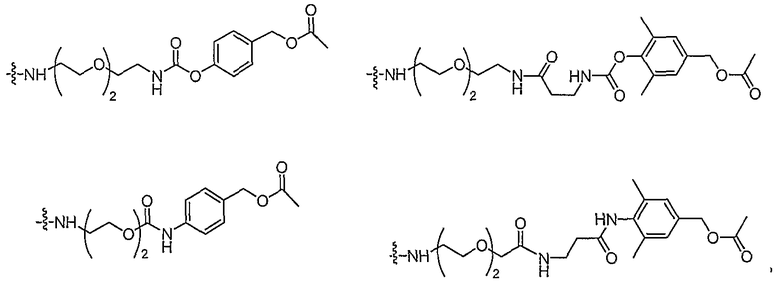
Конкретные примеры включают, но не ограничиваются
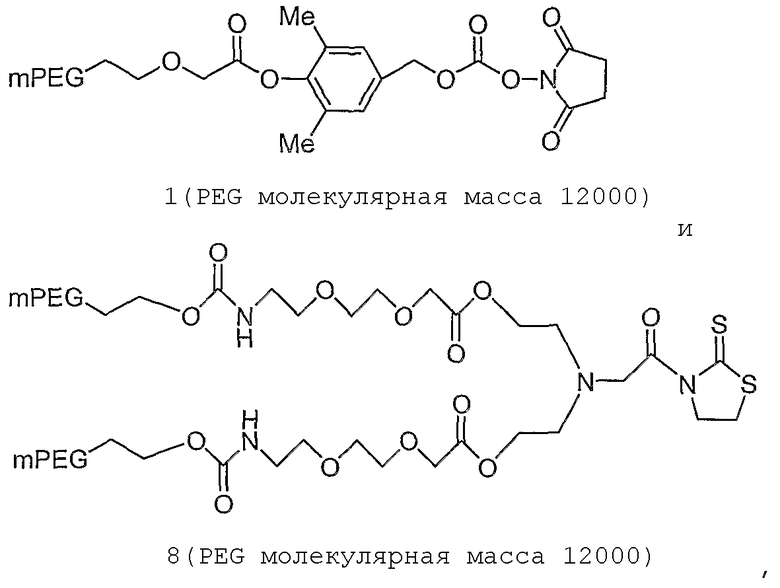
конечно, подразумевается, что молекулярная масса полимерной части может изменяться согласно потребностям изготовителя.
Затем высвобождающий полимер линкер, показанный выше, вводят в реакцию с модифицированным олигомером при условиях, делающих возможным образование конъюгата.
Любой из нуклеотидов или олигонуклеотидов, описанных выше, может быть функционализирован по одному из 5'- или 3'-терминальному фосфату или фосфоротиоату при использовании стандартных способов, таких как фосфорамидатные способы, для присоединения заданного алкиламина или другой группы к терминальному фосфату. Например, присоединяют блокированный (Fmoc) аминоалкил, полученное соединение окисляют, снимают защиту и очищают.
Синтез определенных конъюгатов олигонуклеотидов с полимерами или пролекарств излагается в примерах. В качестве альтернативы пролекарства могут быть получены:
1) введением в реакцию активированного PEG полимера с защищенной бифункциональной высвобождающейся линкерной группой при подходящих условиях сочетания для образования первого промежуточного продукта,
2) снятием защиты и активацией промежуточного продукта из стадии 1) подходящей активирующей группой, такой как NHS сложный эфир, и
3) введением активированного промежуточного продукта из стадии 2) в реакцию с модифицированным олигонуклеотидом в PBS буферной системе для получения заданного олигонуклеотид-полимерного пролекарства.
Неограничивающий список активированных полимеров включает бис-сукцинимидил-карбонат-активированный PEG (SC-PEG), бис-тиазолидин-2-тион-активированный PEG (T-PEG), N-гидроксифталамидил-карбонат-активированный PEG (BSC-PEG) (см. поданные обычным образом USSN 09/823296, описание которых включено здесь в качестве ссылки), сукцинимидил-сукцинат-активированный PEG (SS-PEG) и моноактивированные PEG, такие как указанные в, например, в вышеупомянутом 2001 Shearwater Catalog.
Конъюгация активированного PEG полимера с защищенной бифункциональной высвобождающейся линкерной группой может проводиться в присутствии конденсирующего агента. Неограничивающий список пригодных конденсирующих агентов включает 1,3-диизопропилкарбодиимид (DIPC), любой пригодный диалкилкарбодиимид, галогениды 2-галоген-1-алкилпиридиния (реагенты Мукайямы), 1-(3-диметиламинопропил)-3-этилкарбодиимид (EDC), циклический ангидрид пропанфосфоновой кислоты (PPACA) и фенилдихлорфосфаты и т.д., которые доступны, например, из коммерческих источников, таких как Sigma-Aldrich Chemical, или могут быть синтезированы при использовании известных способов.
Предпочтительно заместители вводят в реакцию в инертном растворителе, таком как тетрагидрофуран (ТГФ), ацетонитрил (CH3CN), метиленхлорид (DCM), хлороформ (CHCl3), диметилформамид (ДМФА) или в их смесях и при температуре от 0°С до примерно 22°С (комнатная температура).
Конъюгацию модифицированного олигонуклеотида с PEG-высвобождающим линкером можно проводить в PBS-буферной системе при рН в диапазоне примерно 7,4-8,5. Специалист в данной области безусловно поймет, что описанный здесь синтез пролекарств также включает использование типичных лабораторных условий, таких как растворители, температура, связывающие агенты и т.д., таких как описано в примерах.
Вне зависимости от выбранного синтеза некоторые предпочтительные соединения, которые получают при использовании синтетических способов, описанных здесь, включают
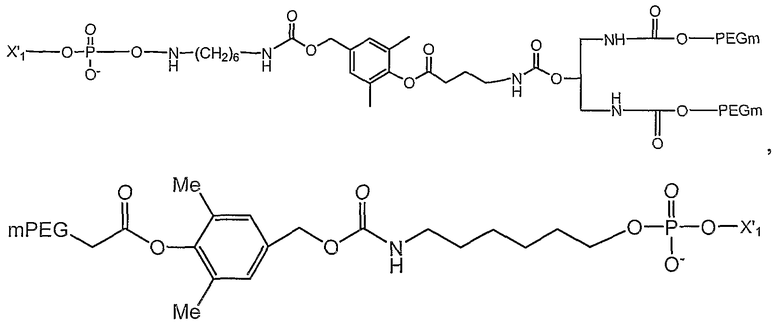
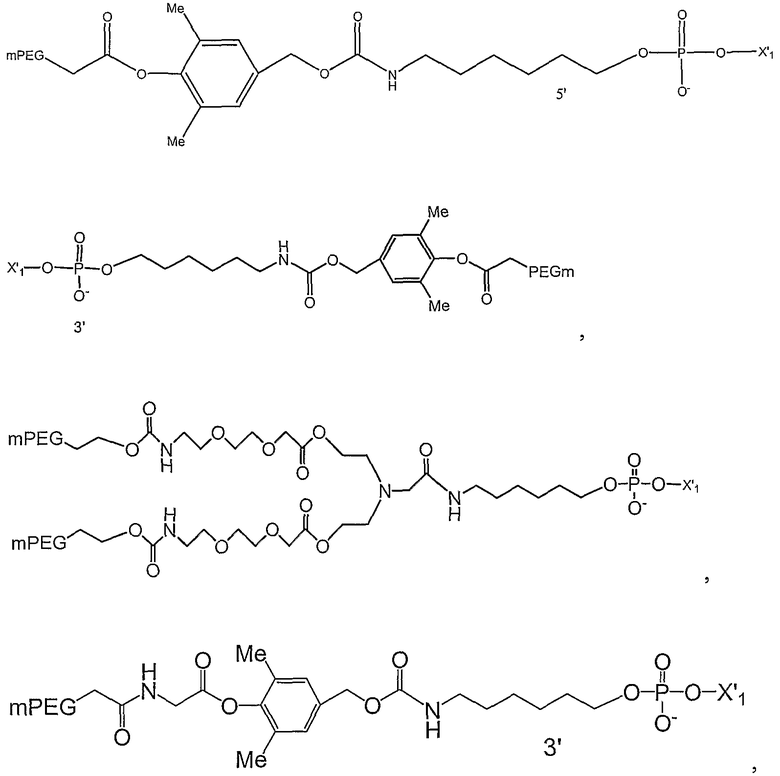
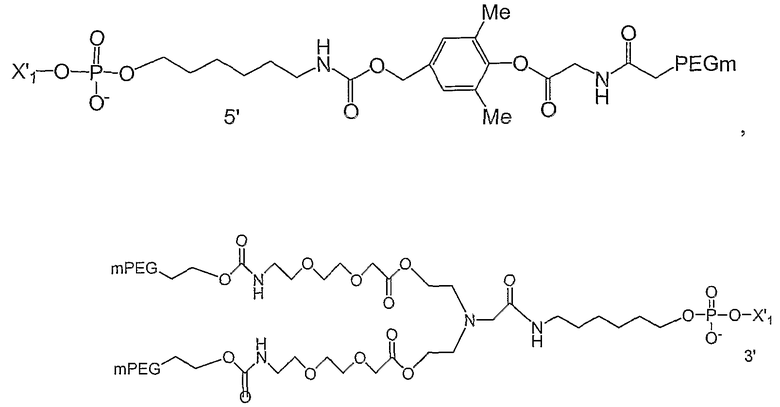
и
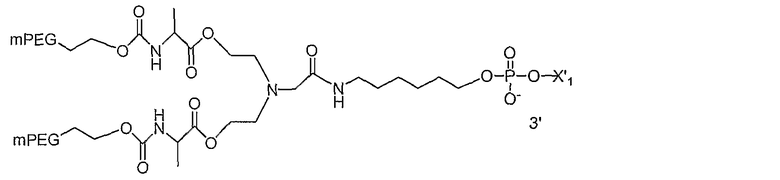
в которых

представляют собой олигонуклеотид и место модификации терминального фосфата, и mPEG представляет собой CH3-O-(CH2-CH2-O)X-, в котором х представляет собой положительное целое число, выбираемое из от примерно 10 до примерно 2300.
Более предпочтительные соединения по изобретению включают:
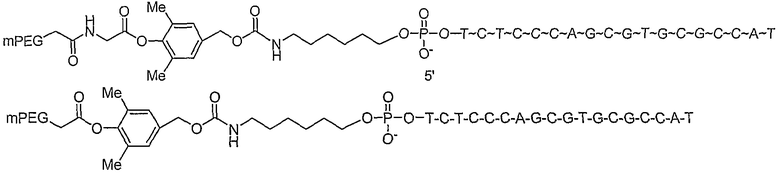
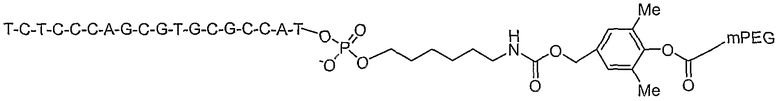
и
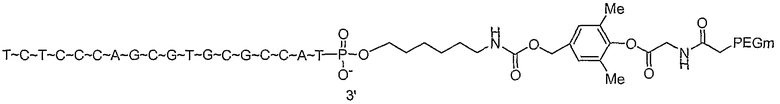
G. СПОСОБЫ ЛЕЧЕНИЯ
Другой аспект настоящего изобретения обеспечивает способы лечения различных заболеваний у млекопитающих. Способы включают введение млекопитающему, нуждающемуся в таком лечении, эффективного количества олигонуклеотидного пролекарства, которое было получено, как описано здесь. Композиции используют для лечения среди прочих заболеваний, новообразований, уменьшения тяжести опухоли, предотвращения метастаз новообразований и предотвращения рецидивов роста опухоли/новообразования, заболеваний печени, вирусных заболеваний, таких как ВИЧ, у млекопитающих. Пролекарства по настоящему изобретению можно использовать при любых показаниях, при которых используют нативный олигонуклеод и антисмысловые олигонуклеотиды, т.е. при терапии рака и т.д. Исключительно в качестве примера пролекарства по изобретению предполагаются для использования при лечении множественной миеломы, хронической лимфоцитарной лейкемии, немелкоклеточного рака легкого, мелкоклеточного рака легкого, рака предстательной железы и других опухолей или видов рака, которых слишком много, чтобы перечислять.
Количество вводимого пролекарства будет зависеть от исходной входящей в него молекулы и заболевания, подвергаемого лечению. Обычно количество пролекарства, используемого в способах лечения, представляет собой такое количество, которое эффективно достигает заданного терапевтического результата у млекопитающих. Естественно, дозы различных пролекарственных веществ будут несколько различаться в зависимости от исходного соединения, скорости гидролиза в живом организме (in vivo), молекулярной массы полимера и т.д. Диапазон, указанный выше, приведен для иллюстративных целей, и специалисты в данной области определят оптимальные дозы выбранного пролекарства, основываясь на клиническом опыте и показаниях лечения. Реальные дозы будут понятны специалисту без избыточного экспериментирования.
Пролекарства по настоящему изобретению могут быть включены в одну или несколько пригодных фармацевтических композиций для введения млекопитающим. Фармацевтические композиции могут быть в форме раствора, суспензии, таблетки, капсулы и т.п., полученных согласно способам, хорошо известным в данной области техники. Также предполагается, что введение таких композиций можно осуществлять пероральным или парентеральным путями, в зависимости от необходимости специалиста. Раствор и/или суспензию композиции можно применять в качестве основы носителя для инъекций или введения композиции любыми известными в данной области техники способами, например внутривенно, внутримышечно, подкожно, инъекцией и т.п.
Такое введение также может проводиться путем инфузии в отделы или полости тела, а также ингаляцией и/или интерназально. Однако в предпочтительных аспектах изобретения пролекарства вводят млекопитающим, в них нуждающимся, парентерально.
Также предполагается, что пролекарства по изобретению можно вводить в сочетании (например, одновременно и/или последовательно) с другими известными в данной области противораковыми агентами. Пригодные противораковые агенты включают, исключительно в качестве примера, чтобы перечислить несколько таких агентов: (Паклитаксел; Briston Myers Squibb); Camptosar® (Иринотекан; Pfizer); Gleevec® (Иматииниба мезилат; Novartis); Rituxan® (Ритуксимаб; Genentech/IDEC); Fludara® (Флударабин; Berlex Labs); Сytoxan® (циклофосфамид; Bristol Myers Squibb); Taxotere® (Доцетаксел; Aventis Pharmaceuticals); Mylotarg® (Гемтузумаб озогамицин; Wyeth-Ayerst); Цитозина арабинозид и/или дексаметазон.
ПРИМЕРЫ
Следующие примеры служат для обеспечения дальнейшего понимания изобретения, но ни в какой мере не ограничивают эффективный объем применения изобретения. Подчеркнутые и полужирные номера, перечисленные в примерах, соответствуют номерам, показанным на чертежах. В каждом из чертежей сахарный фрагмент и фосфатный остов представлены в виде
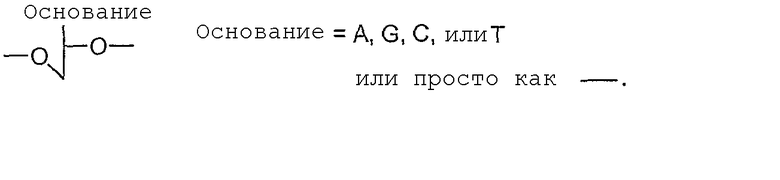
Обозначение mPEG следует понимать, как представляющее собой 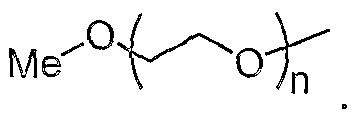
Общие процедуры. Все реакции конъюгации между PEG линкерами и олигонуклеотидами проводили в PBS буферной системе при комнатной температуре. Экстракцией органическим растворителем обычно удаляли непрореагировавшие олигонуклеотиды, последующей анионообменной хроматографией отделяли PEG-олигоконъюгаты от непрореагировавшего избытка PEG линкеров с получением чистых продуктов.
Способы ВЭЖХ. Реакционные смеси и чистоту промежуточных продуктов и конечных продуктов анализировали на приборе ВЭЖХ Beckman Counter System Gold® при использовании ZORBAX® 300 SB C-8 колонки с обращенной фазой (150×4,6 мм) или Phenomenex Jupiter® 300А C18 колонки с обращенной фазой (150×4,6 мм) с мультиволновым УФ детектором, при использовании градиента 30-90% ацетонитрила в 0,5% трифторуксусной кислоте (TFA) и 25-35% ацетонитрила в 50 мМ ТЕАА буфере с 4 мМ TBACl при скорости потока 1 мл/мин. Анионообменную хроматографию проводили на Bio-Cad 700E Perfusion Chromatography Workstation от Applied Biosystems при использовании или Poros 50HQ сильной анионообменной смолы от Applied Biosystems или DEAE Sepharose Fast flow слабой анионообменной смолы от Amersham Biosciences, упакованной в AP-пустую стеклянную колонку от Waters. Высаливание проводили с использованием HiPrep 26/10 или PD-10 высаливающих колонок от Amersham Biosciences.
Пример 1
Соединение 3. Раствор соединения 1 (440 мг, 0,036 ммоль) и 2 (5 мг, 3,6 мкмоль) в PBS буфере (10 мл, рН 7,4) перемешивали при комнатной температуре в течение 12 часов. Реакционный раствор экстрагировали метиленхлоридом (DCM, 3×10 мл) и объединенные органические слои сушили (MgSO4), фильтровали и выпаривали растворитель при пониженном давлении. Остаток растворяли в дважды дистиллированной воде (1,5 мл на 100 мг) и загружали в HQ/10 Poros сильно анионообменную колонку (10 мм × 60 мм, объем слоя ~6 мл). Непрореагировавшие PEG линкеры элюировали водой (3~4 объема колонки) и затем продукт элюировали 0,2 М раствором NH4HCO3 (~2 объема колонки). Фракции, содержащие чистый продукт, объединяли и лиофилизировали с получением чистого 3 (19 мг, 1,44 ммоль, 40%).
Примеры 2-6
Соединения 5, 7, 9, 11 и 12 получали и очищали таким же образом, как 3 с выходами в диапазоне от 30% до 50%.
Пример 7
Соединение 14. К раствору соединения 13 (10 мг, 1,7 мкмоль) в PBS буфере (5 мл, рН 7,4) добавляли 10 (175 мг, 85 мкмоль) в пяти эквивалентных частях каждый час и перемешивали при комнатной температуре в течение 12 часов. Реакционный раствор экстрагировали DCM (3×10 мл) и насыщенным солевым раствором (10 мл) и объединенные органические слои сушили (MgSO4), фильтровали и выпаривали растворитель при пониженном давлении. Остаток растворяли в дважды дистиллированной воде (1,5 мл) и загружали в DEAE Fast flow, слабую анионообменную колонку (10 мм × 60 мм, объем слоя ~6 мл), которую предварительно калибровали 20 мМ Tris-HCl буфером, рН 7,4. Непрореагировавшие PEG линкеры элюировали водой (от 3 до 4 объемов колонки) и затем продукт элюировали с градиентом от 0 до 100% 1 М NaCl в 20 мМ Tris-HCl буфере 7,4 в течение 10 минут, с последующим 100% 1 М NaCl в течение 10 минут со скоростью потока 3 мл/мин. Фракции, содержащие чистый продукт, объединяли и высаливали на PD-10 высаливающей колонке 0,2 М раствором NH4HCO3 (~2 объема колонки) и полученный раствор лиофилизировали с получением чистого 14 (25 мг, 0,95 мкмоль, 57%).
Пример 8
Соединение 16 получали и очищали таким же образом, как 14 с выходом 60%.
Пример 9
Соединение 17. К раствору AS1 (5 мг, 0,85 мкмоль) в фосфатном буфере (2 мл, рН 7,8) добавляли 10 (175 мг, 0,085 ммоль), который разделяли на пять эквивалентных частей, в течение 2 часов и полученный раствор перемешивали при комнатной температуре в течение дополнительных 2 часов. Реакционный раствор экстрагировали DCM (3×6 мл) и насыщенным солевым раствором (5 мл) и объединенные органические слои сушили (MgSO4), фильтровали и выпаривали растворитель при пониженном давлении. Остаток растворяли в дважды дистиллированной воде (5 мл) и загружали в DEAE fast flow, слабую анионообменную колонку (10 мм × 60 мм, объем слоя ~6 мл), которую предварительно калибровали 20 мМ Tris-HCl буфером, рН 7,4. Непрореагировавшие PEG линкеры элюировали водой (от 3 до 4 объемов колонки) и затем продукт элюировали с градиентом от 0 до 100% 1 М NaCl в 20 мМ Tris-HCl буфере, рН 7,4 в течение 10 минут, с последующим 100% 1 М NaCl в со скоростью потока 3 мл/мин в течение 10 минут. Фракции, содержащие чистый продукт, объединяли и высаливали на PD-10 высаливающей колонке и полученный раствор лиофилизировали с получением чистого 17 (15 мг, 0,57 мкмоль, 67%).
Примеры 10-11
Соединения 18 и 19 получали и очищали таким же образом, как 17 с выходами конечных продуктов 67%, при использовании AS2 и AS3 вместо AS1.
Примеры 12-15
Соединение 21 получали и очищали таким же образом, как 14, путем замены 12 на 20 с выходом, равным 90%.
Соединение 22 получали и очищали таким же образом, как 14, путем замены 12 на 20 с выходом 65%.
Соединение 24 получали и очищали таким же образом, как 14, путем замены 12 на 23 и для высаливания использовали воду (~2 объема колонки) для элюирования продукта вместо 0,2 М раствора NH4HCO3. Конечный выход составлял 30%.
Соединение 26 получали и очищали таким же образом, как 24, путем замены 23 на 25. Выход составлял 30%.
Пример 16
Соединение 27. К раствору 13 (10 мг, 1,7 мкмоль) в фосфатном буфере (5 мл, рН 8,5) добавляли 27 (180 мг, 0,084 ммоль), который разделяли на десять эквивалентных частей и полученный раствор перемешивали при комнатной температуре в течение 4 дней. Реакционный раствор экстрагировали DCM (3×10 мл) и насыщенным солевым раствором (10 мл) и объединенные органические слои сушили (MgSO4), фильтровали и выпаривали растворитель при пониженном давлении. Остаток растворяли в дважды дистиллированной воде (1,5 мл) и загружали в DEAE fast flow, слабую анионообменную колонку (10 мм × 60 мм, объем слоя ~6 мл), которую предварительно калибровали 20 мМ Tris-HCl буфером, рН 7,4. Непрореагировавшие PEG линкеры элюировали водой (от 3 до 4 объемов колонки) и затем продукт элюировали с градиентом от 0 до 100% 1 М NaCl в 20 мМ Tris-HCl буфере, рН 7,4 в течение 10 минут, с последующим 100% 1 М NaCl со скоростью потока 3 мл/мин в течение 10 минут. Фракции, содержащие чистый продукт, объединяли и высаливали на PD-10 высаливающей колонке и полученный раствор лиофилизировали с получением 14 (105 мг, 0,0102 ммоль, 60%). Чистоту продукта определяли ВЭЖХ.
Примеры 17-21
Соединения 29, 30 и 31 получали и очищали таким же образом, как 28, за исключением того, что 13 заменяли на AS1, AS2 и AS3, соответственно. Для каждого из конечных продуктов был получен выход 65%.
Соединение 33 получали и очищали таким же образом, как 14, путем замены 12 на 32, что приводило к выходу 76%.
Соединение 35 получали и очищали таким же образом, как 14, за исключением того, что вместо 10 использовали активированный PEG 34. Конечный выход составил 30%.
БИОЛОГИЧЕСКИЕ ДАННЫЕ
Некоторые in vitro свойства PEG-олигоконъюгатов, представлены ниже:
In vitro свойства PEG-олигоконъюгатов
PE I = фосфодиэcтераза I, 5'-экзонуклеаза, кинетику исследовали при рН 8,8 ТЕАА буфер при 37°С; PE II = фосфодиэcтераза II, 3'-экзонуклеаза, кинетику исследовали при рН 6,5 ТЕАА буфер при 37°С; Нуклеаза Р1 = эндонуклеаза, кинетику исследовали при рН 5,3 ТЕАА буфер при 37°С; для всех ферментов 1 единица высвобождает 1 мкмоль олигонуклеотида.
Фармакокинетика РЕG-олигоконъюгатов у мышей ICR
Общая процедура
1) Содержание животных: мышей помещали по 6 в клетку, в ящики для разведения. Размер клеток выбирали в соответствии с “Guide for the Care and Use of Laboratory Animals of the Institute of Laboratory Animal Resources”, National Research Council.
2) Режим питания: мыши имели доступ к водопроводной воде и их кормили коммерчески доступным кормом для лабораторных животных вдоволь (ad libitum).
3) Подготовка соединений: соединение 13 растворяли в 4,0 мл солевого раствора и соединение 14 растворяли в 4,1 мл солевого раствора.
4) Место введения: соединения 13 и 14 вводили в виде одной дозы (день 1) через хвостовую вену.
План исследования
Шестьдесят (60) мышей выбирали, вводили препарат и обескровливали согласно следующему плану, показанному в табл.5 ниже.
iv = внутривенно
*олигоэквивалент
Трех (3) необработанных мышей обескровливали посредством пункции сердца в пробирки, содержащие ЭДТА, для сбора необработанной контрольной плазмы.
Мышам вводили внутривенно исходное соединение 13 или 14 по 100 мкл каждой мыши. После седации 0,09% Авертина мышей полностью обескровливали ~1000 мкл посредством пункции сердца. Кровь собирали в ампулы, содержащие ЭДТА. Плазму собирали после центрифугирования крови и немедленно замораживали при -80°С на сухом льду.
Клинические исследования
Мышей осматривали визуально раз в день после инфузии исследуемого вещества на смертность и признаки реакции на лечение. Отмечали любую смертность и клинические проявления. Вес тела измеряли только перед днем инъекции.
Фармакокинетические исследования соединений 28 и 33 проводили сходным способом.
Результаты исследований
Фармакокинетические результаты представлены в последующей табл.6 ниже.
In vivo свойства PEG-олигоконъюгатов
Примеры 22-25
Подтверждение in vitro активности антисмысловых PEG конъюгатов
Как было показано, белок bcl-2 имеет значительную антиапоптозную активность в клетках рака предстательной железы. Понижающая регуляция экспрессии белка bcl-2 в раковых клетках предстательной железы подтверждена смертью клеток, а индукцию смерти клеток bcl-2 антисмысловыми PEG конъюгатами использовали для подтверждения успешной внутриклеточной доставки антисмысловых олигонуклеотидов.
Материалы и методы для примеров 22-25.
Исследуемые соединения представлены в табл.7 ниже
Были получены, как описано выше.
Культура клеток
Не содержащие микоплазмы РС3 клетки, полученные от American Type Culture Collection (Rockville, MD), выращивали в Roswell Park Memorial Institute среде (“RPMI”) (Invitrogen, Grand Island, NY) с добавлением 10% околоплодной телячьей сыворотки (“FBS”), содержащей 10% (об./об.) инактивированной нагреванием (56°С) FBS с добавлением 1% заменимых аминокислот, 1% пирувата, 25 мМ HEPES (N-2-гидроксиэтилпиперазин-N'-2-этансульфоновая кислота) буфера, 100 Е/мл пенициллина G натрия и 100 мкг/мл стрептомицин сульфата. Маточные культуры поддерживали при 37°С в инкубаторе с увлажненной 5% атмосферой СО2.
Реагенты
FBS и липофектин (липосомный состав катионного липида N-[1-(2,3-диолеилокси)пропил]-n,n,n-триметиламмоний хлорид) приобретали у Invitrogen (Grand Island, NY). Анти-bcl-2 моноклональное антитело было от Dako (Carpinteria, CA). Анти-α-тубулин моноклональное антитело и 3-(4,5-диметилтиазол-2-ил)-2,5-дифенилтетразолий бромид (“MTT”) приобретали от Sigma-Aldrich (St. Louis, MO). Фосфоротиоатные олигонуклеотиды синтезировали и очищали при использовании стандартных способов.
Трансфекция олинуклеотидов
Клетки высевали за день до эксперимента в 6-луночные планшеты с плотностью 25×104 клеток на лунку, с 60-70% слиянием в день эксперимента. Все трансфекции проводили в Opti-MEM среде в отсутствие FBS и антибиотиков, как изложено в инструкции производителей. Пригодные количества реагентов разбавляли 100 мкл Opti-MEM среды с получением конечной концентрации липофектина и олигонуклеотида. Растворы осторожно перемешивали и предварительно инкубировали при комнатной температуре в течение 30 минут, делая возможным образование комплексов. Затем добавляли 800 мкл Opti-MEM, раствор перемешивали и наносили на клетки, которые предварительно промывали Opti-MEM. Время инкубации для комплексов олигонуклеотид/липофектин в Opti-MEM составляло 24 часа, с последующей инкубацией в полной среде, содержащей 10% FBS. Общее время инкубации до лизиса клеток и изоляции белка составляло обычно 72 часа при 37°С.
Вестерн-блот анализ
Клетки, обработанные комплексами олигонуклеотид-липид, промывали в PBS затем экстрагировали в лизирующем буфере [50 мМ Tris-HCl pH 7,4, 1% NP-40, 0,25% дезоксихолата натрия, 150 мМ NaCl, 1 мM EGTA, 50 мкг/мл Pefabloc SC, 15 мкг/мл апротинина, лейпептина, химостатина, пепстатина А, 1 мМ Na3VO4, 1 мМ NaF] при 4°С в течение 1 часа. Клеточные фрагменты удаляли центрифугированием при 14000 g в течение 20 минут при 4°С. Концентрации белка определяли при использовании Bio-Rad системы анализа белка (Bio-Rad Laboratories, Richmond, CA). Аликвоты клеточных экстрактов, содержащие 25-40 мкг белка, разделяли SDS-PAGE и переносили на Hybond ECL фильтровальную бумагу (Amersham, Arlington Heights, IL) и фильтры инкубировали при комнатной температуре в течение 1-2 часов в 5% BSA в PBS, содержащем 0,5% Tween-20. Фильтры затем исследовали 1:500 разбавленным анти bcl-2 антителом в 5% BSA в PBS, содержащем 0,5% Tween-20, при 4°С в течение ночи. После промывания в PBS, содержащем 0,5% Tween-20, фильтры инкубировали в течение 1 часа при комнатной температуре в 5% молоке в PBS, содержащем 0,5% Tween, с разбавленным 1:3000 пероксидаза конъюгированным вторичным антителом (Amersham). После промывания (3Ч10 минут) проводили электрохимическую люминесценцию (“ECL”) согласно инструкциям производителя.
Определение скорости пролиферации клеток
Влияние PEG конъюгатов на жизнеспособность клеток определяли анализом МТТ. Кратко, 15-20×104 клеток высевали в 6-луночные планшеты и позволяли закрепляться в течение ночи. Затем клетки обрабатывали подходящими концентрациями комплексов олигонуклеотидов с липофектином в течение 24 часов при 37°С, с последующей инкубацией в полной среде (100 мкл), содержащей 10% FBS. Жизнеспособность клеток определяли ежедневно. 10 мкл 5 мг/мл МТТ в PBS добавляли в каждую лунку с последующей инкубацией в течение 4 часов при 37°С. Затем в каждую лунку добавляли 100 мкл 10% SDS в 0,04 М HCl, с последующей инкубацией в течение ночи при 37°С для растворения кристаллов формазана. Поглощение определяли при 570 нм при использовании Benchmark plus Microplate спектрофотометра (Bio Rad, Hercules, CA). Эксперименты проводили 6 раз и данные приводили, как среднее значение +/- S.D. (среднеквадратическое отклонение).
Количественный анализ внутриклеточных уровней ROS
2',7'-дихлордигидрофлуоресцеина диацетат (H2DCF-DA) и дигидроэтидиний (НЕ) использовали для определения содержания реакционно-активных форм кислорода (“ROS”) и супероксида. Оба красителя представляют собой нефлуоресцентные и могут свободно диффундировать в клетки. Когда НЕ окисляется до этидиния (Е), он внедряется в клеточную ДНК и флуоресцирует. Окисление H2DCF-DA приводит к образованию 2',7'-дихлорфлуоресцеина (DCF), который также флуоресцирует, и тот, и другой могут быть определены проточной цитометрией. Клетки собирали при помощи обработки трипсином, промывали PBS и окрашивали 50 мкМ H2DCF-DA или 50 мкМ НЕ в феноле, не содержащем красного DMEM, в течение 2 часов при 37°С. Средние числа флуоресцентных каналов DCF и Е анализировали при использовании проточной цитометрии в FL-1 и FL-2 каналах соответственно. Для каждого образца было необходимо минимально 10000 клеток и данные анализировали при использовании CELLQuest программного обеспечения (Becton Dickinson). Гистограммы строили в логарифмической шкале.
Пример 22
Ингибирование экспрессии белка bcl-2
Три PEG олигонуклеотида (соединения 14, 28 и 33), объектом которых являлась экспрессия bcl-2, трансфектировали в РС3 клетки и их способность ингибировать белок bcl-2 анализировали вестерн-блоттингом.
Влияние липофектина
В начале степень ингибирования экспрессии белка bcl-2 в РС3 клетках, вызванного соединением 14, определяли в присутствии и в отсутствие липофектина. РС3 клетки обрабатывали соединением 14 (при 200, 400 и 800 нМ) в присутствии или в отсутствие липофектина в течение 24 часов в Opti-MEM и затем дополнительно 67 часов в полной среде. Образцы белка (30-40 мкг белка/полоса) анализировали вестерн-блоттингом, как описано в "Материалах и способах", при использовании тубулина в качестве контрольных образцов белка. Процент ингибирования по сравнению с контролем необработанных клеток определяли при помощи лазер-сканирующей денситометрии. Результаты вестерн-блоттинга показаны на фиг.12.
Экспрессия α-тубулина и РКС-α не изменялась, подтверждая, что липофектин полезен для достижения проникновения соединения 14 в РС-3 клетки, и подтверждая, что понижающая регуляция экспрессии белка bcl-2 была вызвана исключительно соединением 14.
Дополнительные исследования показали, что соединения 14 и 28 были наиболее активными при 400 нМ. РС3 клетки обрабатывали комплексами соединения 14, соединения 28 и соединения 23 при 400, 800 и 1000 нМ и липофектина в течение 24 часов в Opti-MEM и затем дополнительно 67 часов в полной среде. Образцы белка (30-40 мкг белка/полоса) анализировали вестерн-блоттингом, как описано в "Материалах и способах", при использовании тубулина в качестве контрольных образцов белка. Процент ингибирования по сравнению с контролем необработанных клеток определяли при помощи лазер-сканирующей денситометрии.
Соединение 14 приводило к 86% понижающей регуляции и соединение 28 приводило к 78% понижающей регуляции.
Пример 23
Анализ экспрессии белка bcl-2 в зависимости от дозы PEG олигонуклеотидов
Для того чтобы дополнительно подтвердить ингибирующий эффект соединений 14 и 28 на экспрессию белка bcl-2, РС3 клетки обрабатывали увеличивающимися концентрациями (25, 50, 100, 200 и 400 нМ) соединения 14, соединения 28 и соединения 13 в качестве положительного контроля в комплексе с липофектином в течение 24 часов в Opti-MEM и затем дополнительно 67 часов в полной среде. Образцы белка (30-40 мкг белка/полоса) анализировали вестерн-блоттингом, как описано выше в разделе "Материалы и способы".
Ингибирование экспрессии белка bcl-2 в зависимости от концентрации наблюдали при помощи вестерн-блоттинга для соединений 14 и 28 по отношению к контролю. Примерно 1-2% ингибирование наблюдали при 50 нМ, увеличивающееся до 99% и 75% при концентрации 400 нМ. Для соединения 24 при 50 нМ не наблюдалось какого-либо ингибирования, но при концентрации 400 нМ ингибирование увеличивалось до 77%. Трансфекцию соединением 13 использовали в качестве положительного контроля. Ни один из олигонуклеотидов не ингибировал экспрессию α-тубулина.
Вышеописанный эксперимент в качестве контроля повторяли для соединения 24. РС3 клетки обрабатывали увеличивающимися концентрациями соединения 35 и 24 (25, 50, 100, 200 и 400 нМ) в комплексе с липофектином в течение 24 часов в Opti-MEM и затем дополнительно 67 часов в полной среде. Образцы белка (30-40 мкг белка/полоса) анализировали вестерн-блоттингом, как описано выше в разделе "Материалы и способы", при использовании α-тубулина в качестве контрольных образцов белка. Процент ингибирования по сравнению с контролем необработанных клеток определяли при помощи лазер-сканирующей денситометрии.
Пример 24
Влияние PEG олигонуклеотидов на рост РС3 клеток
Также исследовали влияние соединения 14 и соединения 28 на рост раковых клеток предстательной железы РС3, in vitro. РС3 клетки обрабатывали комплексами олигонуклеотид/липофектин. Как показано на фиг.10 трансфекция антисмыслового олигонуклеотидного соединения 14 при 400 и 200 нМ сильно ингибировала рост клеток, тогда как соединение 28 лишь незначительно влияло на скорость пролиферации.
Пример 25
Влияние PEG олигонуклеотидов на продукцию реакционно-активных форм кислорода в РС3 клетках
Продукцию реакционно-активных форм кислорода или ROS в РС3 клетках оценивали проточной цитометрией двумя способами. Первый основывался на окислении гидроэтидиния (НЕ) до этидиния (Е), который затем встраивается в ДНК с флуоресценцией, определяемой проточной цитометрией. Второй способ использовал окисление проникающего в клетки 2',7'-дигидродихлорфлуоресцин диацетата до флуоресцирующего 2',7'-дихлорфлуоресцина (DCF). В РС3 клетках обработка комплексами соединение 14/липофектин (14 нМ/15 мкг/мл) в течение 24 часов в Opti-MEM приводила к ROS через три дня после определения проточной цитометрией как Е (1,9 кратное увеличение по сравнению с контролем необработанных клеток), так и DCF (2-кратное увеличение по сравнению с контролем необработанных клеток) флуоресценцией. Как подтверждается данными, представленными на фиг.11, соединение 28 не приводит к какому-либо увеличению продукции ROS по сравнению с контролем необработанных клеток. Более того, продукция ROS чрезвычайно тесно связана со скоростью пролиферации клеток; клетки перестают расти после обработки 400 нМ соединения 14 и этот олигонуклеотид также вызывает увеличение в продукции ROS (DCF и НЕ).

Настоящее изобретение относится к полимерным конъюгатам формулы (I), включающим нуклеотидный или олигонуклеотидный остаток, которые могут применяться для лечения рака, и способу их получения.
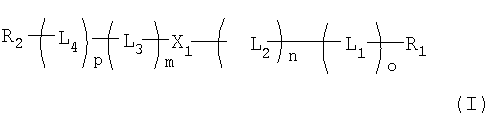
где R1 и R2 независимо представляют собой Н или полиалкиленоксид, необязательно имеющий кэппирующую группу, выбранную из ОН, NH2, SH, СО2Н, С1-6 алкилов, соединений формулы (II) и формулы (III)
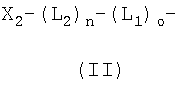 и
и 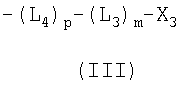 ,
,
и когда (o+n)≥2, n и o каждый является положительным целым числом, p и m каждый равен нулю и R2 представляет Н, и когда (p+m)≥2, p и m каждый является положительным целым числом, n и o каждый равен нулю и R1 представляет Н; X1, X2, X3 независимо выбраны из одноцепочечного или двухцепочечного олигонуклеотидного остатка; L1 и L4 независимо представляют собой высвобождаемые линкерные фрагменты; L2 и L3 независимо выбраны из бифункциональных спейсерных групп. Технический результат - разработка новых конъюгатов нуклеотидов с противоопухолевой активностью. 4 н. и 17 з.п. ф-лы, 7 табл., 12 ил.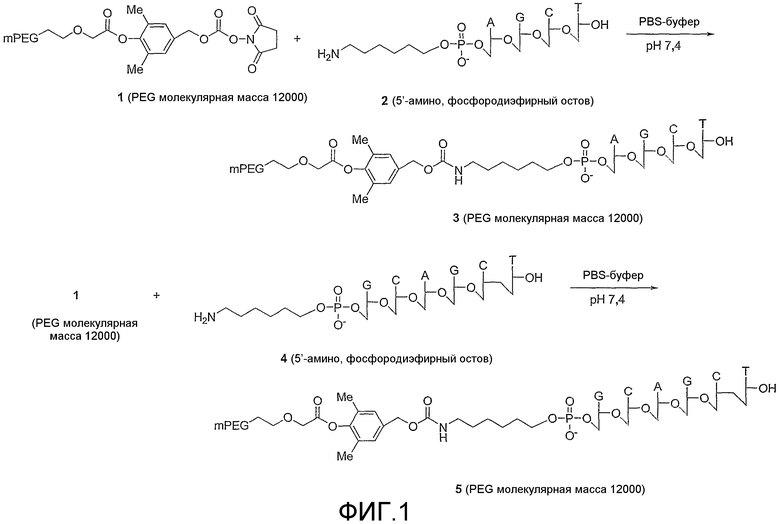
1. Олигонуклеотидное пролекарство формулы (I):
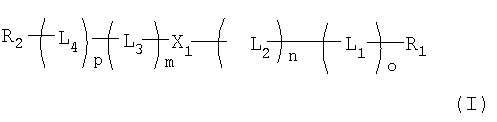
в которой R1 и R2 независимо представляют собой Н или полиалкиленоксид с молекулярной массой от 2000 до 136000 Да, необязательно имеющий кэппирующую группу, выбранную из группы, состоящей из ОН, NH2, SH, CO2H, C1-6 алкилов, формулы (II) и формулы (III)
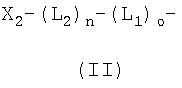 и
и 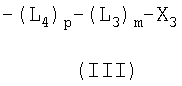 ,
,
при условии, что когда (o+n)≥2, n и o каждый является положительным целым числом, p и m каждый равен нулю, и R2 представляет Н, и когда (p+m)≥2, p и m каждый является положительным целым числом, n и o каждый равен нулю, и R1 представляет Н;
X1, X2, X3 независимо представляют одноцепочечный или двухцепочечный олигонуклеотидный остаток длиной от 10 до 1000 нуклеотидов;
L1 и L4 независимо представляют собой высвобождаемые линкерные фрагменты,
где L1 выбирают из группы, состоящей из
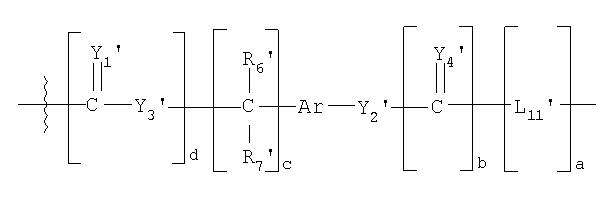 ,
,
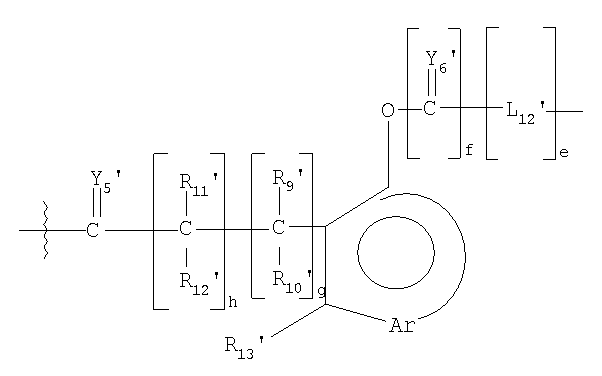
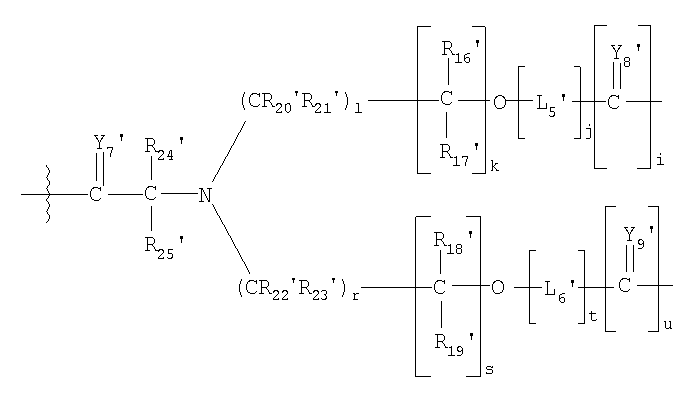
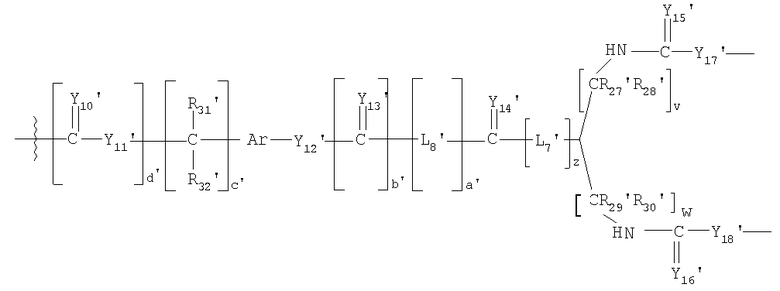 и
и
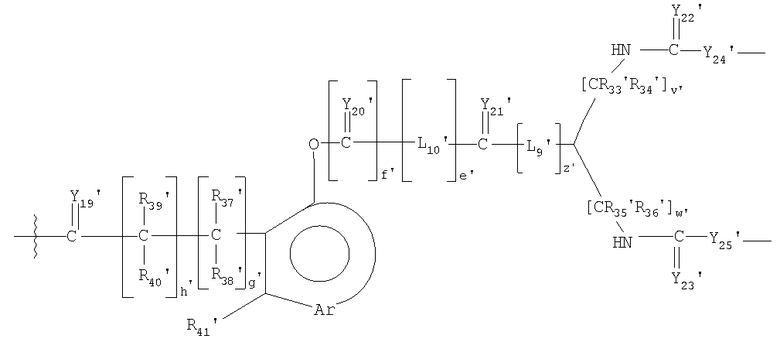
L4 выбирают из группы, состоящей из
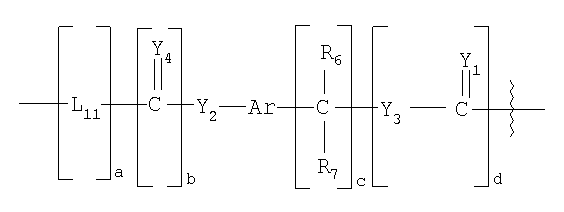 ,
,
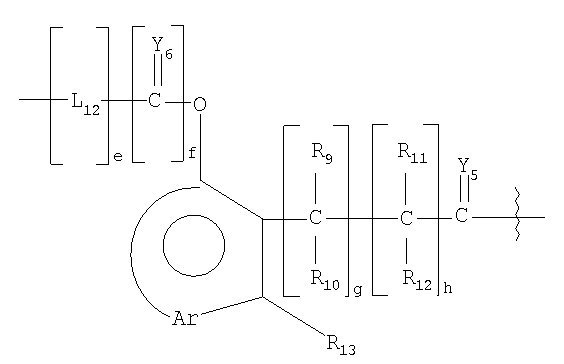
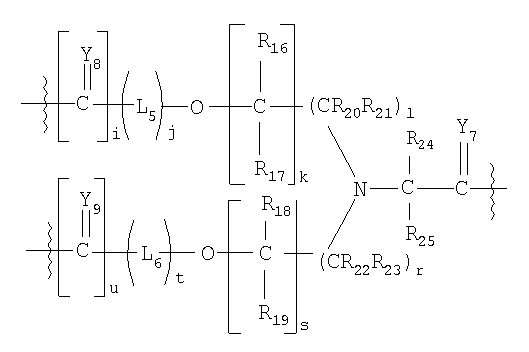 ,
,
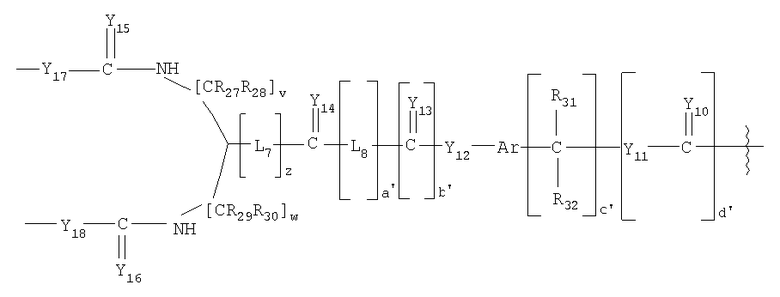
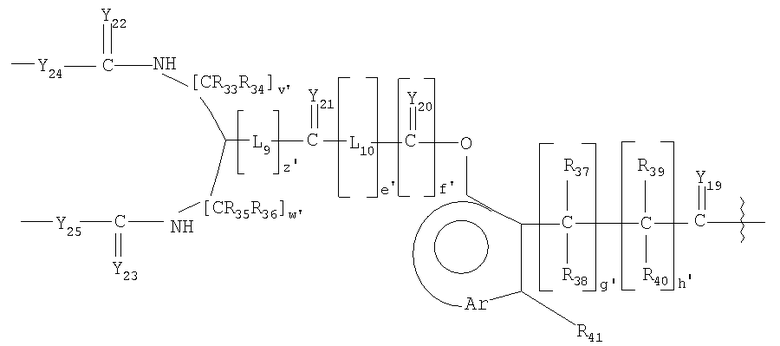
где Y1'-25' и Y1-25 представляют независимо О, S или NR109;
Ar представляет
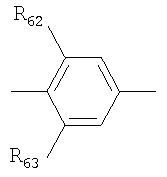 или
или 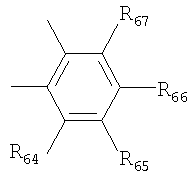 ;
;
R6'-7', R9'-13', R16'-25', R27'-41', R6-7, R9-13, R16-25, R27-41, R62-67 и R109 независимо выбирают из группы, состоящей из водорода, С1-6алкилов, разветвленных С3-12алкилов и С1-6алкокси;
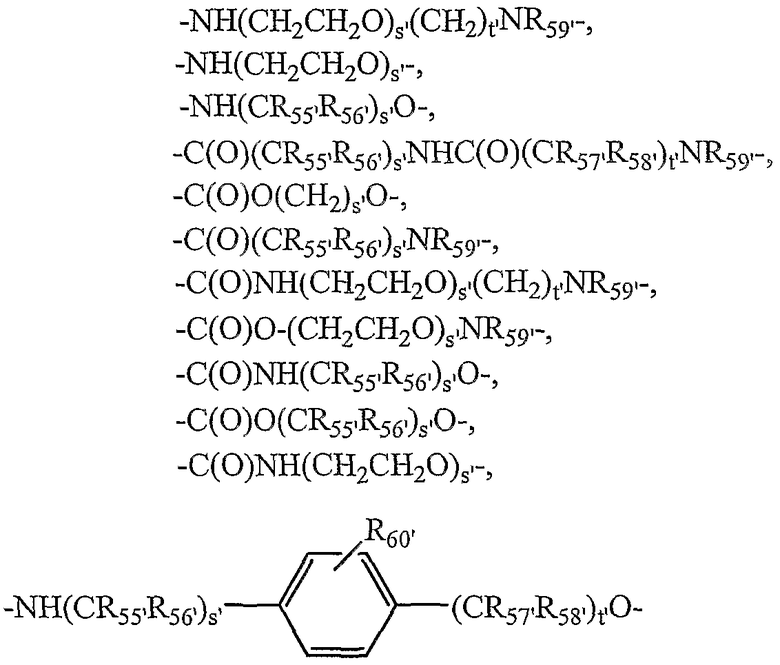
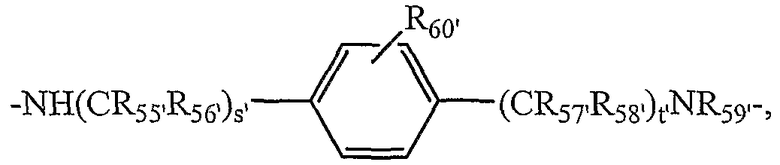
L5'-12' независимо выбраны из группы, состоящей из
-(СН2)3-,
-(СН2)3NHC(O)-,
-(СН2)3NH-,
-C(O)(CR57'R58')s'O(CR55'R56')t'-,
-NH(CH2CH2O)s'(CH2)t'NR59'-,
-NH(CH2CH2O)s'-,
-NH(CR55'R56')s'O-,
-C(O)(CR55'R56')s'NHC(O)(CR57'R58')t'NR59'-,
-C(O)O(CH2)s'O-,
-C(O)(CR55'R56')s'NR59'-
-C(O)NH(CH2CH2O)s'(CH2)t'NR59'-,
-C(O)O(CH2CH2O)s'NR59'-,
-C(O)NH(CR55'R56')s'-O-,
-C(O)O(CR55'R56')s'O-,
-C(O)NH(CH2CH2O)s'-,
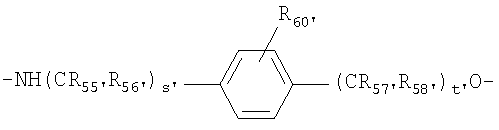 и
и
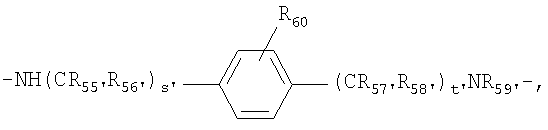 ;
;
или L5'-6' выбраны из -С(O)СН2(ОСН2СН2)2NH-;
L5-12 независимо выбраны из группы, состоящей из
-(СН2)3-,
-С(O)NH(СН2)3-,
-NH(СН2)3-,
-(CR55R56)sO(CR57R58)tC(O)-
-NR59(CH2)(OCH2CH2)NH-,
-(OCH2CH2)sNH-,
-O(CR55R56)sNH-,
-NR59(CR57R58)tC(O)NH(CR55R56)sC(O)-,
-O(CH2)sOC(O)-,
-NR59(CR55R56)sC(O)-
-NR59(CH2)t(OCH2CH2)sNHC(O)-,
-NR59(OCH2CH2)sOC(O)-,
-O(CR55R56)sNHC(O)-,
-O(CR55R56)sOC(O)-,
-(OCH2CH2)sNHC(O)-,
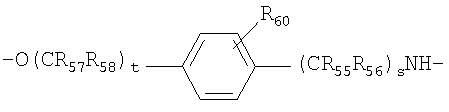 и
и
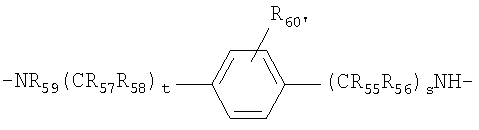 ;
;
или L5-6 выбраны из -NH(CH2CH2O)2CH2C(O)-;
где R55'-59' и R55-59 независимо выбирают из группы, состоящей из водорода, C1-6алкилов, разветвленных С3-12алкилов и С1-6алкокси;
R60 и R60' независимо выбирают из группы, состоящей из водорода, C1-6алкилов, разветвленных С3-12алкилов и C1-6алкокси;
s' и t' каждый равен 1;
с, h, k, l, r, s, v, w, v', w', с' и h' каждый равен 1;
а, е, g, j, t, z, a', z', e' и g' каждый независимо равен или 0 или 1;
b, d, f, i, u, q, b', d' и f' каждый независимо равен или 0 или 1;
L2 и L3 независимо выбраны из бифункциональных спейсерных групп, каждый из которых включает от 2 до 10 атомов углерода,
где L2 выбран из группы, состоящей из
-(CR50'R51')q'Q'-,
-(CR52'R53')r'O(CR50'R51')q'Q'-,
-(CR52'R53')r'(OCH2CH2)Q'-,
-(CR52'R53')r'C(O)NH(CR50'R51')q'Q'-,
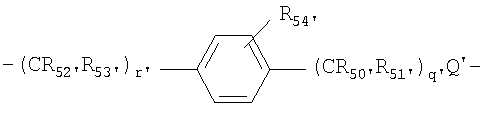 и
и
-(CH2)-S-S-(CH2)q'Q'-;
L3 выбран из группы, состоящей из
-Q(CR50R51)q'-,
-Q(CR50R51)q'O(CR52R53)r',
-Q(CH2CH2O)q'(CR52R53)r'-,
-Q(CR50R51)q'NHC(O)(CR52R53)r'-,
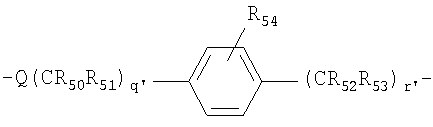 и
и
-Q(CH2)q'-S-S-(CH2)r'-;
и
где Q и Q' независимо выбраны из О, S или NH, где Q и Q' присоединены к L4 и L1, соответственно;
R50'-54' и R50-54 независимо выбирают из группы, состоящей из водорода, C1-6алкилов, разветвленных С3-12алкилов, замещенных С1-6алкилов и С1-6алкокси, где замещенные алкилы включают карбоксиалкилы, аминоалкилы, диалкиламино, гидроксиалкилы и меркаптоалкилы; и
q' и r' каждый независимо равны от 1 до 9.
2. Пролекарство по п.1, в котором указанный нуклеотид выбирают из группы, состоящей из
 ,
,  ,
, 

 ,
, 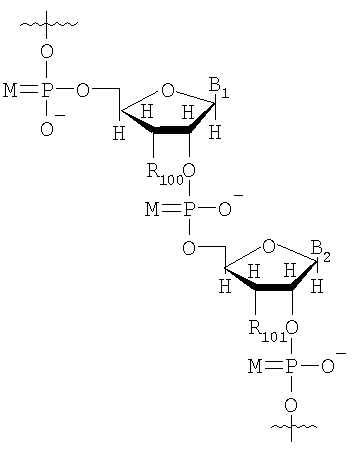 ,
,  ,
,

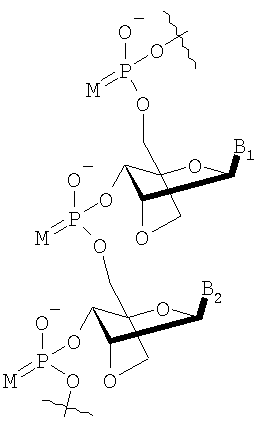
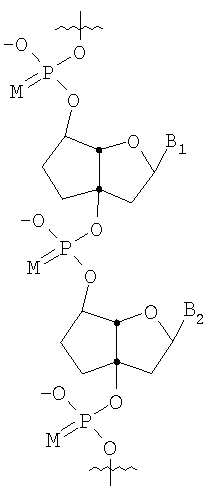 ,
, 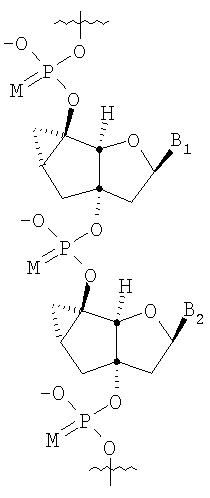 и
и 
в которых М представляет собой О или S;
B1 и В2 независимо выбирают из группы, состоящей из А (аденин), G (гуанин), С (цитозин), Т (тимин), U (урацил) и модифицированных оснований;
R100 и R101 независимо выбирают из группы, состоящей из Н, OR', в которой R' представляет собой Н, C1-6 алкил, замещенные алкилы, нитро, галоген и арил.
3. Пролекарство по п.2, в котором М представляет S.
4. Пролекарство по п.1, в котором олигонуклеотидный остаток представляет собой олигонуклеотидный остаток с фосфодиэфирным остовом или фосфоротиоатным остовом.
5. Пролекарство по п.1, в котором олигонуклеотидный остаток представляет собой антисмысловой олигонуклеотидный остаток или олигодезоксинуклеотидный остаток.
6. Пролекарство по п.5, в котором указанный антисмысловой олигонуклеотидный остаток или олигодезоксинуклеотидный остаток выбирают из группы, состоящей из олигонуклеотидов и олигодезоксинуклеотидов с фосфордиэфирными остовами или фосфоротиоатными остовами, замкнутых нуклеиновых кислот, пептидных нуклеиновых кислот, трицикло-ДНК, ложных олигодезоксинуклеотидов, РНК, зеркально-ориентированных олигонуклеотидов и CpG олигомеров.
7. Пролекарство по п.5, в котором указанный антисмысловой олигонуклеотид имеет последовательность, выбираемую из группы, состоящей из SEQ ID NO:
1, SEQ ID NO:2, SEQ ID NO:3 и SEQ ID NO:4.
8. Пролекарство по п.1, имеющее формулу (I)
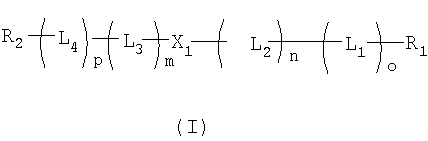
где R2 представляет собой водород,
p и m равны 0, и
R1 представляет собой полиалкиленоксид с кэппирующей группой формулы (II):
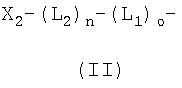
где X1 и Х2 независимо представляют собой 3'-олигонуклеотид или 5'-олигонуклеотид.
9. Пролекарство по п.1, в котором R1 представляет собой полиэтиленгликоль.
10. Пролекарство по п.1, в котором R1 выбирают из группы, состоящей из:
J-O-(CH2CH2O)n'-
J-O-(CH2CH2O)n'-CH2C(O)-O-,
J-O-(CH2CH2O)n'-CH2CH2NR48-,
J-O-(CH2CH2O)n'-CH2CH2S-,
-O-С(O)СН2-O-(СН2СН2О)n'-СН2С(O)-O-,
-NR48CH2CH2-O-(CH2CH2O)n'-CH2CH2NR48-,
-SCH2CH2-O-(CH2CH2O)n'-CH2CH2S-,
в которых n' является целым положительным числом таким, чтобы средневесовая молекулярная масса полимерной части пролекарства по п.1 составляла от 2000 до 136000 Да;
R48 выбирают из группы, состоящей из водорода, C1-6 алкилов,
С3-12 разветвленных алкилов, С3-8 циклоалкилов, C1-6 замещенных алкилов,
С3-8 замещенных циклоалкилов, арилов, замещенных арилов, арилалкилов,
C1-6гетероалкилов, замещенных С1-6гетероалкилов, C1-6алкокси, фенокси и
С1-6гетероалкокси; и
J представляет собой кэппирующую группу, выбранную из группы, состоящей из ОН, NH2, SH, CO2H, C1-6 алкилов, формулы (II) и формулы (III)
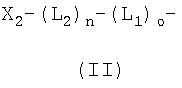 и
и 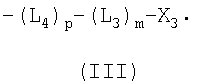
11. Пролекарство по п.1, в котором R1 включает
-O-(CH2CH2O)x-,
где x представляет собой положительное целое число, выбираемое таким образом, чтобы средневесовая молекулярная масса составляла от 2000 до 136000 Да.
12. Пролекарство по п.1, в котором R1 имеет средневесовую молекулярную массу, составляющую от 3000 до 100000 Да.
13. Пролекарство по п.1, в котором R1 имеет средневесовую молекулярную массу, составляющую от 5000 до 40000 Да.
14. Пролекарство по п.6, в котором указанный антисмысловой олигонуклеотид имеет последовательность SEQ ID NO:1.
15. Олигонуклеотидное пролекарство формулы:
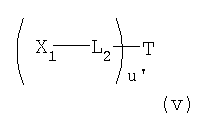
в которой L2 представляет собой бифункциональную спейсерную группу, содержащую от 2 до 10 атомов углерода;
X1 представляет собой одноцепочечный или двухцепочечный олигонуклеотидный остаток, где длина олигонуклеотида составляет примерно от 10 до 1000 нуклеотидов;
u' представляет собой положительное целое число; и
Т представляет собой:
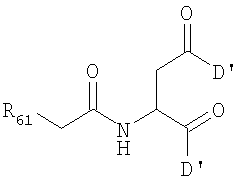 или
или 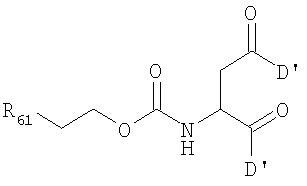
в которых D' является одним из
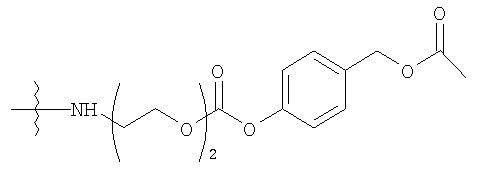 ,
, 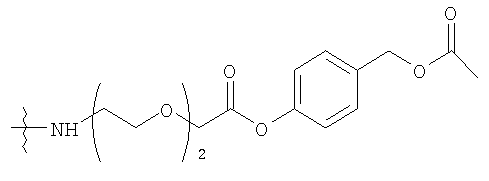
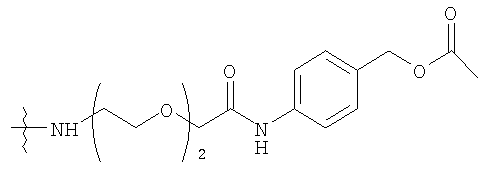 ,
, 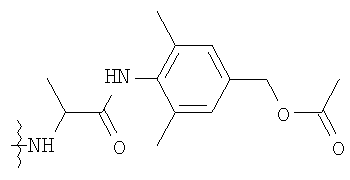 ,
,
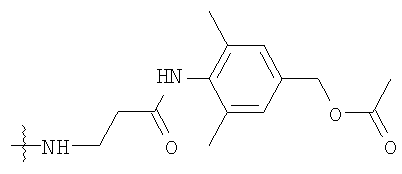 ,
, 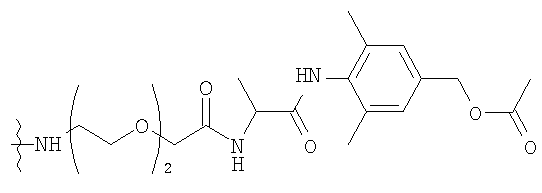
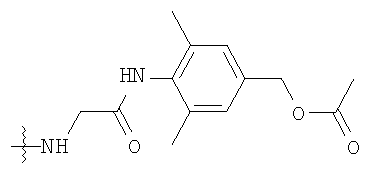 ,
, 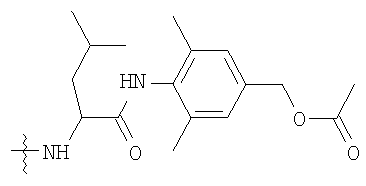 ,
,
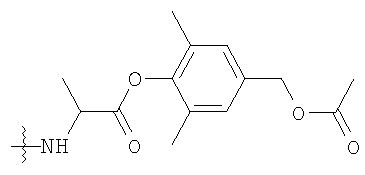 ,
, 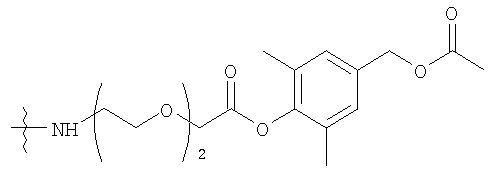
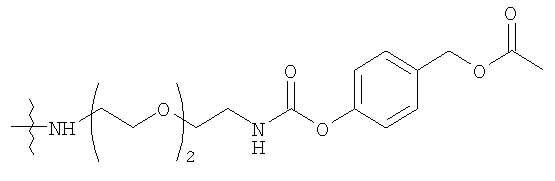 ,
, 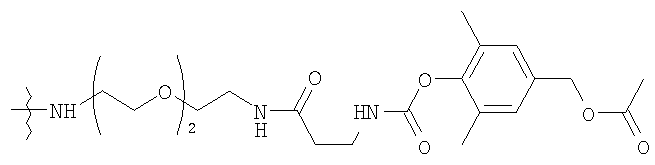
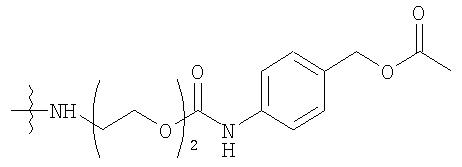 ,
, 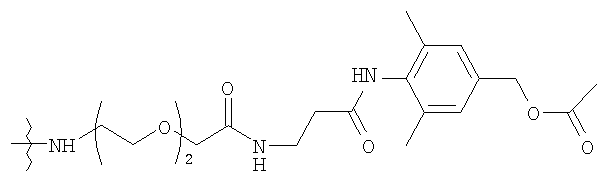
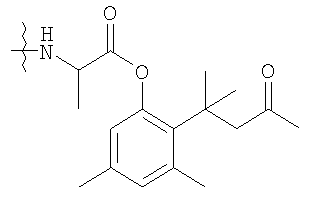 ,
, 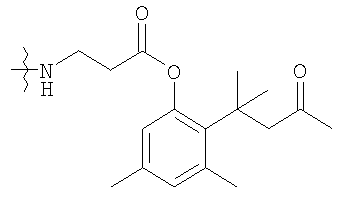
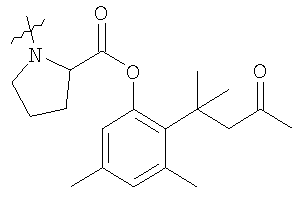 ,
, 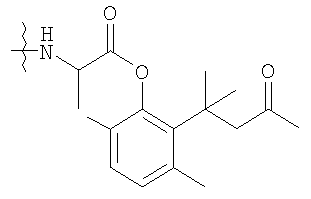 ,
,
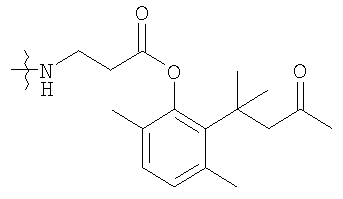 ,
, 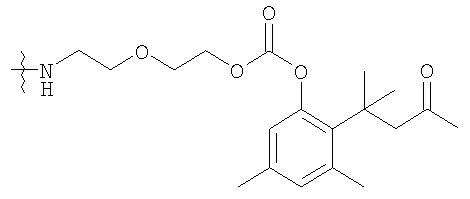
и
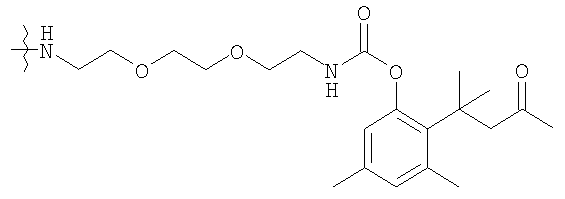 ,
,
где R61 представляет собой полиалкиленоксид;
L2 выбирают из группы, состоящей из
-(CR50'R51')q'Q'-,
-(CR52'R53')r'O(CR50'R51')q'Q'-,
-(CR52'R53')r'(OCH2CH2)Q'-,
-(CR52'R53')r'C(O)NH(CR50'R51')q'Q'-,
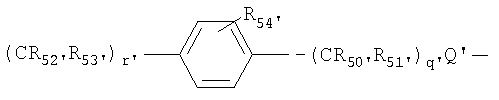 и
и
-(CH2)-S-S-(CH2)q'Q'-;
где Q' независимо выбирают из О, S и NH;
R50'-54' независимо выбирают из группы, состоящей из водорода, C1-6алкилов, разветвленных С3-12алкилов, замещенных C1-6алкилов и С1-6алкокси, где
замещенные алкилы включают карбоксиалкилы, аминоалкилы, диалкиламино, гидроксиалкилы и меркаптоалкилы; и
q' и r' каждый независимо является целым числом от 1 до 9.
16. Пролекарство по п.1, выбираемое из группы, состоящей из:
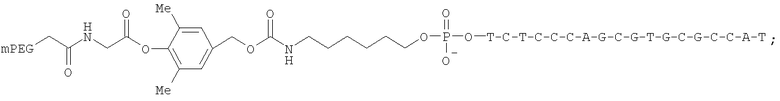
и
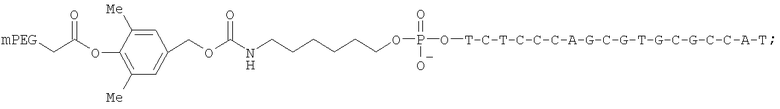
причем все из них включают олигонуклеотид SEQ ID NO:1.
17. Способ получения пролекарства, включающий:
взаимодействие соединения формулы:
R2-L4-уходящая группа
с соединением формулы
H-L3-X1
при условиях, достаточных для образования пролекарства формулы
R2-L4-L3-X1,
в которой R2 представляют собой полиалкиленоксид с молекулярной массой от 2000 до 136000 Да;
L4 представляет собой высвобождаемый линкерный фрагмент, выбираемый из группы, состоящей из:
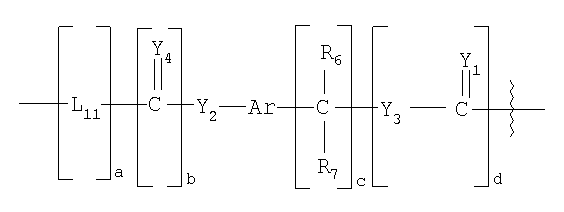 ,
,

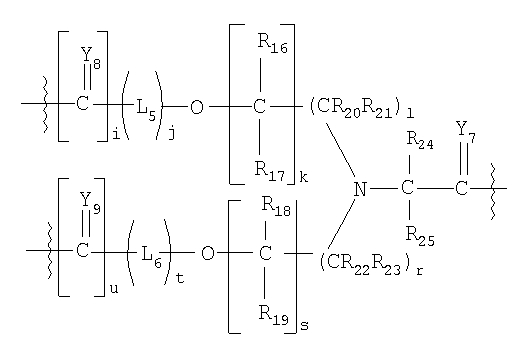 ,
,
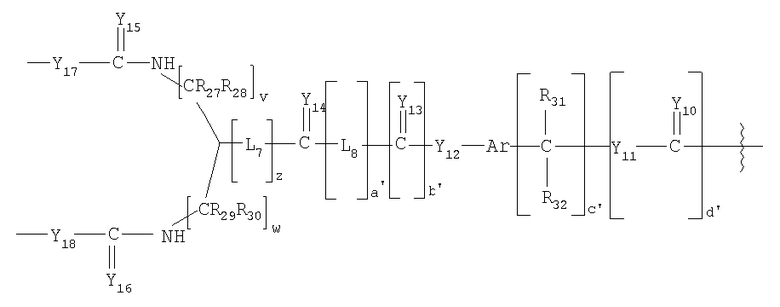
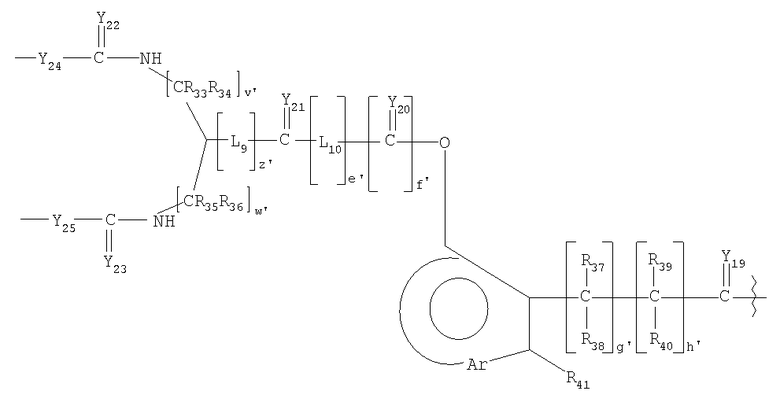
где Y1-25 представляет независимо О, S и NR109;
Ar представляет
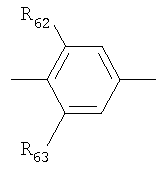 или
или 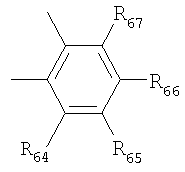 ;
;
R6-7, R9-13, R16-25, R27-41, R62-67 и R109 независимо выбирают из группы, состоящей из водорода, C1-6алкилов, разветвленных С3-12алкилов и С1-6алкокси;
L5-12 независимо выбраны из группы, состоящей из
-(СН2)3-,
-С(O)NH(СН2)3-,
-NH(СН2)3-,
-(CR55R56)sO(CR57R58)tC(O)-,
-NR59(CH2)(OCH2CH2)NH-,
-(OCH2CH2)sNH-,
-O(CR55R56)sNH-,
-NR59(CR57R58)tC(O)NH(CR55R56)sC(O)-,
-O(CH2)sOC(O)-,
-NR59(CR55R56)sC(O)-
-NR59(CH2)t(OCH2CH2)sNHC(O)-,
-NR59(OCH2CH2)sOC(O)-,
-O(CR55R56)sNHC(O)-,
-O(CR55R56)sOC(O)-,
-(OCH2CH2)sNHC(O)-,
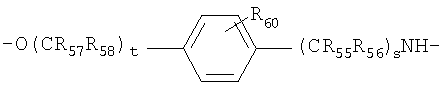 и
и
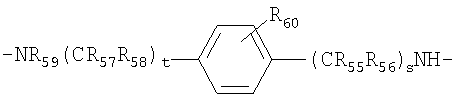
или L5-6 выбраны из -NH(CH2CH2O)2CH2C(O)-;
где R55-59 независимо выбирают из группы, состоящей из водорода, C1-6алкилов, разветвленных С3-12алкилов и С1-6алкокси;
R60 выбирают из группы, состоящей из водорода, С1-6алкилов, разветвленных С3-12алкилов и С1-6алкокси;
s' и t' каждый равен 1;
с, h, k, l, r, s, v, w, v', w', с' и h' каждый равен 1;
а, е, g, j, t, z, a', z', e' и g' каждый независимо равен или 0 или 1;
b, d, f, i, u, q, b', d' и f' каждый независимо равен или 0 или 1;
L3 представляет собой бифункциональную спейсерную группу, содержащую от 2 до 10 атомов углерода;
причем L3 выбирают из группы, состоящей из
-Q(CR50R51)q'-,
-Q(CR50R5l)q'O(CR52R53)r'-,
-Q(CH2CH2O)q'(CR52R53)r'-,
-Q(CR50R51)q'NHC(O)(CR52R53)r'-,
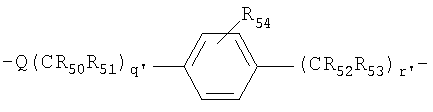 и
и
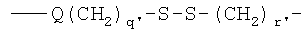 ;
;
где Q независимо выбирают из O, S и NH, где Q присоединен к L4;
R50-54 независимо выбирают из группы, состоящей из водорода, C1-6алкилов, разветвленных С3-12алкилов, замещенных С1-6алкилов и С1-6алкокси, где замещенные алкилы включают карбоксиалкилы, аминоалкилы, диалкиламино, гидроксиалкилы и меркаптоалкилы; и
q' и r' каждый независимо является целым числом от 1 до 9;
X1 представляет собой одноцепочечный или двухцепочечный олигонуклеотидный остаток, где длина олигонуклеотида составляет примерно от 10 до 1000 нуклеотидов.
18. Способ доставки олигонуклеотида в органы, ткани и клетки, включающий введение млекопитающему, нуждающемуся в такой доставке, эффективного количества олигонуклеотидного пролекарства по п.1.
19. Способ по п.18, в котором доставку осуществляют с целью лечения рака.
20. Способ по п.18, в котором указанный антисмысловой олигонуклеотид имеет последовательность, выбираемую из группы, состоящей из SEQ ID NO:1, SEQ ID NO:2, SEQ ID NO:3 и SEQ ID NO:4.
21. Пролекарство по п.1 формулы (I)

где R1 представляет собой водород,
n и o равны 0, и
R2 представляет собой полиалкиленоксид с кэппирующей группой формулы (III):
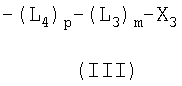
где X1 и Х3 независимо представляют собой 3'-олигонуклеотид или 5'-олигонуклеотид.
| US 2002183259, 05.12.2002 | |||
| ПОЛИНУКЛЕОТИДНЫЕ КОМПОЗИЦИИ | 1995 |
|
RU2175337C2 |
| US 6040181, 21.03.2000 | |||
| US 6303569, 16.10.2001 | |||
| US 5707813, 13.01.1998. | |||
Авторы
Даты
2010-07-10—Публикация
2004-04-09—Подача