Изобретение относится к медицине, а именно к гематологии, и может быть использовано для прогноза развития и течения хронического лимфолейкоза, а также ответа на проводимую терапию.
Согласно современным представлениям хронический лимфолейкоз (ХЛЛ) - опухоль кроветворной системы, характеризующаяся пролиферацией и аккумуляцией морфологически зрелых лимфоцитов, в большинстве случаев В-лимфоцитов. Известно, что ряд ангиогенных ростовых факторов, таких как bFGF и VEGF, играют важную роль в патогенезе ХЛЛ, множественной миеломы, некоторых солидных опухолей. Они включены во множество патологических и физиологических процессов, включая ангиогенез, васкулогенез, неопластическую трансформацию, рост и метастазирование опухоли и процессы апоптоза. По новой переработанной и дополненной классификации гемобластозов лимфатической природы А.И.Воробьева и М.Д.Бриллиант (1999) хронический В-клеточный лейкоз относится к зрелоклеточным опухолям лимфатической системы. Согласно этой классификации больные были разделены на 2 группы - с агрессивным и доброкачественным течением заболевания [Воробьев А.И., Кременецкая A.M. // гематол. и трансфизиол. - 2000, - Т.45, N3. - С.4-14].
Все формы с агрессивным течением требуют назначения полихимиотерапии. При данном течении прогноз неблагоприятный и наблюдается лекарственная резистентность.
Таким образом, раннее определение прогноза позволило бы:
- оптимизировать терапию данного заболевания;
- повлиять на качество жизни этих пациентов;
- снизить количество затрачиваемых государством средств на лечение данных больных.
Известны следующие традиционные способы прогнозирования развития ХЛЛ:
Критерии прогнозирования ХЛЛ [nelson К., Bruce D., Cheson / the oncologist 1999; 4: 352-369]:
- Удвоение времени лимфоцитов (<12 месяцев - прогноз хуже);
- Диффузная инфильтрация лимфоцитами костного мозга в биопсийном материале (плохой прогноз);
- Сывороточный бета-2 микроглобулин (повышенный уровень - прогноз хуже);
- Растворимый CD23 в сыворотке и ЛДГ (повышенный уровень - прогноз хуже).
Аналогом предлагаемого изобретения является способ прогнозирования течения ХЛЛ путем определения сывороточного уровня интерлейкина-6 (ИЛ-6), который является индикатором активности течения ХЛЛ [Robak Т., Wierzbowska A., Blasinska-Morawiec М. Et al: Mediators inflamm. - 1999. - Vol.8 (6). - Р.277-86]. Так в работе [Fayad L., Keating M.J. at al: Blood. - 2001. - Vol.97 (1). - P.256-63] показано, что уровень ИЛ-6 и ИЛ-10 был выше у пациентов с ХЛЛ по сравнению с контролем. Пациенты с повышенным уровнем ИЛ-6 и/или ИЛ-10 имели худшую медиану или 3-летнюю выживаемость и неблагоприятные характеристики (предшествующая температура, увеличение уровня бета-2 микроглобулина или лактатдегидрогеназы, или стадию заболевания по Rai III или IV). Результаты [Hulkkolen J., Vilpo J., et al: Br. J. Haemato. - 1998. - Vol.100 (3). - P.478-83] свидетельствуют, что различная способность продуцировать ИЛ-6 и фактор некроза опухоли-альфа может играть роль при В-ХЛЛ прогрессии и клинической манифестации этого заболевания.
Вместе с тем к недостаткам способа можно отнести следующее:
1. относительно высокую вариабельность сывороточного уровня (СУ) ИЛ-6 даже в течение суток у одного и того же пациента (например, в утреннее и послеобеденное время);
2. наличие сопутствующих заболеваний у пациентов может существенно влиять на регистрируемый СУ ИЛ-6. Главным недостатком способа является невозможность выделить группы благоприятного (неблагоприятного) течения заболевания на начальной стадии и тем самым осуществить своевременные профилактические мероприятия (проведение адекватной химиотерапии).
Вторым аналогом изобретения является способ прогнозирования ХЛЛ путем определения зависимости течения заболевания от мутационного статуса и длины теломеры (определяемой как в случаях с мутацией, так и в случаях без нее). Так, в работе [Pawel Grabowski, Magnus Hultdin, Karin Karlsson, Gerard Tobin, at al: Blood. - 2005. - Vol.105: 4807-4812] показано, что ХЛЛ состоит из 2 прогностических видов, где в случае с мутированными генами VH иммуноглобулина прогноз благоприятнее, чем в случае с немутированными. Пациенты с диагнозом ХЛЛ с VH-мутацией показывают более длинные теломеры по сравнению с немутированными случаями, и длина теломер является индикатором клинического исхода. Длина теломеры оценивалась методом ПЦР, показывая очень хорошую корреляцию длины теломеры, опредедляемую при помощи метода Саусблотинга (Р<0,001). Результаты свидетельствовали, что прогностическое значение мутационного статуса (n=282) и длина теломеры (n=246) была значительной (Р<0,001 соответственно) и длина теломеры является прогоностическим фактором у пациентов со стадией А (Р=0,021) и стадией В/С (Р=0,018), где мутацонный статус был показателем клинического исхода только стадии А (Р<0,0001). Кроме того, случаи ХЛЛ с наличием мутации были подразделены при помощи определения длины теломеры на 2 группы с различными прогнозами (Р=0,003), в подразделении пациентов показавших не мутировавшие случаи (Р=0,232). У группы с VH-мутацией с короткими теломерами выживаемость оказалась близка с немутированными случаями ХЛЛ. Таким образом, комбинируя определение статуса VH-мутации и длины теломеры, можно достичь улучшения субклассификации ХЛЛ, определяя ранее нераспознаваемых пациентов с различными клиническими исходами.
К недостаткам этого способа можно отнести следующее:
1. трудоемкость процесса;
2. дороговизна проводимых диагностических манипуляций.
Прототипом данного изобретения является метод оценки течения ХЛЛ путем определения уровня цитокинов, участвующих в ангиогенезе [Appl Immunohistochem Mol Morphol. 2006 Jun; 14 (2): 154-60]. Авторы исследовали экспрессию CD34, VEGF, bFGF и TGF-бета и их рецепторов при различных стадиях В-ХЛЛ, анализируя образцы костного мозга от 23 пациентов (11 со стадиями Rai 0-II; 12 со стадиями III или IV). TGF-beta2 был более выражен на стадиях 0-II, чем при стадиях III или IV (Р=0.03). Не было никакого существенного различия в интенсивности содержания уровня CD34, TGF-betal, VEGF и bFGF и их рецепторов между стадиями 0-II и стадиями III или IV. Окрашивание показало, что экспрессия bFGF более выражена, чем экспрессия VEGF (Р=0.001). Результаты не подтвердили взаимосвязь между интенсивностью ангиогенеза и стадиями и течением В-ХЛЛ. Экспрессия TGF-beta2 было более выражена на ранних стадиях болезни и может способствовать замедлению течения заболевания.
Недостатками данного метода являются:
1. отсутствие данных о сывороточном уровне цитокинов;
2. отсутствие данных о корреляции экспрессии и ответа на проводимую терапию.
Технический результат при использовании изобретения - повышение точности оценки развития и течения заболевания, прогноз плохого ответа на проводимую терапию у больных ХЛЛ.
Указанный технический результат достигается тем, что в способе прогнозирования развития и течения хронического лимфолейкоза, включающем определение количественного содержания фактора роста сосудистого эндотелия человека (VEGF) и основного фактора роста фибробластов (bFGF), согласно изобретению определяют их содержание в сыворотке крови и при значениях VEGF 185,66±33,5 и более пг/мл, bFGF 35,84±2,02 и более пг/мл прогнозируют быстрое развитие и агрессивное течение заболевания, плохой ответ на проводимую терапию, при значениях VEGF 72,67±12,3 пг/мл, bFGF 34,06±2,59 пг/мл прогнозируют медленное развитие и доброкачественное течение заболевания.
Предлагаемый способ осуществляется следующим образом. У больного осуществляют забор крови натощак в объеме 5 мл. Проводят количественное определение in vitro основного фактора роста фибробластов (bFGF) и фактора роста сосудистого эндотелия человека (VEGF) методом ИФА (ELISA) в сыворотке крови человека. При значениях VEGF 185,66±33,5 и более пг/мл, bFGF 35,84±2,02 и более пг/мл прогнозируют быстрое развитие и агрессивное течение заболевания, плохой ответ на проводимую терапию. При значениях VEGF 72,67±12,3 пг/мл, bFGF 34,06±2,59 пг/мл прогнозируют медленное развитие и доброкачественное течение заболевания.
Материалом для исследования служили образцы сыворотки крови человека, замороженные при -70°C. Кровь набирали в пробирки (5 мл), центрифугировали при 1000 об/мин, отделяли сыворотку, которую замораживали при -70°C. До проведения ИФА образцы хранились при данной температуре. Количественное определение bFGF и VEGF в сыворотке проводилось с методом ИФА (ELISA), данный тест основан на методе твердофазного иммуноферментного анализа. Микропланшет покрывается антителами против bFGF и VEGF. В ходе реакции в лунки планшета добавляются стандарты, контроли и неизвестные образцы. Во время первой инкубации bFGF и VEGF связываются произвольно с иммобилизованными в лунках антителами одним сайтом связывания. После промывки добавляются биотинилированные антитела против bFGF и VEGF, которые во второй инкубации связываются с иммобилизованными bFGF и VEGF, связавшимися в первой инкубации. После удаления избытка вторых антител добавляется стрептавидин-пероксидаза, которая связывается с биотинилированными антителами с формированием сандвич-комплекса из 4-х реагентов. После третьей инкубации и промывки удаляется несвязавшийся фермент, после чего добавляется субстратный раствор, который взаимодействует с ферментом с образованием цветного комплекса. Интенсивность окраски раствора прямо пропорциональна концентрации bFGF и VEGF, присутствующих в образце.
Для подсчета результатов рассчитывали среднее значение поглощения для каждого стандарта, контроля и образца. Для корректировки разведения, сделанного в процессе анализа, необходимо умножить значения, полученные для образцов на 2.
В качестве контроля обследовали группу практически здоровых индивидов, проживающих на территории Республики Башкортостан (29 человек), у которых отсутствовали какие-либо злокачественные заболевания.
В группу с доброкачественным течением ХЛЛ вошли больные с медленным нарастанием лейкоцитоза, очаговым типом роста в костном мозге, незначительным увеличением периферических лимфоузлов и селезенки. В начальной стадии заболевания лечение таким больным не назначается либо назначается терапия хлорбутином или флударабином в виде монотерапии.
В группу с неблагоприятным агрессивным течением вошли больные с прогрессирующей формой (быстрое увеличение лимфоузлов, селезенки, диффузный рост опухоли в костном мозге, наличие больших конгломератов лимфоузлов, плохим ответом на проводимую терапию, небольшим сроком выживаемости), данным пациентам необходимо назначение полихимиотерапии с применением нескольких цитостатических препаратов (флударабин + циклофосфан + ритуксимаб, ритуксимаб + СНОР, CHOP, СОР).
Группа больных с доброкачественным течением составила 44 человека, а группа с агрессивным течением - 34 человека. В качестве контроля обследована группа практически здоровых доноров, подобранных в соответствии с возрастом и полом исследуемых больных.
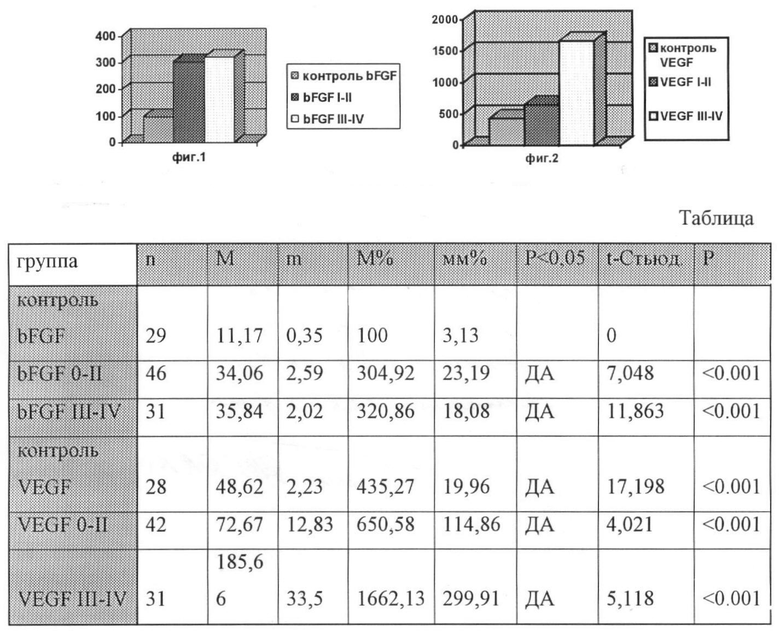
В результате изучения содержания уровня VEGF в сыворотке больных ХЛЛ в зависимости от течения заболевания было обнаружено следующее. Наиболее высокие уровни VEGF в сыворотке соответствуют группе больных с агрессивным течением заболевания, быстрым развитием болезни, плохим ответом на проводимую терапию 185,66±33,5 и более пг/мл (Р<0,001) по сравнению с группой с доброкачественным течением заболевания 72,67±12,3 пг/мл (р<0,001) и контрольной группой 48,62±2,23 пг/мл (р<0,001), т.е разница в количественном уровне содержания в сыворотке VEGF является статистически значимой. Можно судить о том, что высокий уровень VEGF напрямую коррелирует с высоким риском агрессивного течения заболевания, быстрым развитием болезни, худшим ответом на терапию (таблица).
Немного отличные значения были получены при изучении содержания уровня bFGF в сыворотке. Наиболее высокий уровень был обнаружен в группе больных со злокачественным течением заболевания 35,84±2,02 и более пг/мл (р<0,001), в группе больных с доброкачественным течением заболевания показатели содержания bFGF в сыворотке составляют 34,06±2,59 пг/мл (Р<0,001). Но в контрольной группе обследуемых показатели bFGF значительно ниже - 11,17±0,35 пг/мл (р<0,001) и являются статистически значимыми (таблица).
Таким образом, определение уровня bFGF и VEGF, характеризующееся повышенным уровнем этих показателей в группах больных с быстрым и агрессивным течением заболевания, плохим ответом на проводимую терапию, позволяет использовать bFGF и VEGF в качестве прогностических факторов развития заболевания (фиг.1-2).
Предлагаемый способ иллюстрируется следующими клиническими примерами.
Пример 1. Больной А., 1964 года рождения, г.Кумертау, РБ. Диагноз ХЛЛ выставлен в 2001 году, подтвержден стернальной пункцией (костный мозг богат клеточными элементами, представлен зрелыми лимфоцитами - 89%). С 2005 года регулярно получает полихимиотерапию с включением циклофосфана, преднизолона, моноклональных антител, пуриновых аналогов. Смерть наступила в июле 2008 года на фоне прогрессирования лимфоцитоза до 132×109/л, тромбоцитопении, увеличения всех групп лимфоузлов (периферических + внутрибрюшных до образования больших конгломератов), присоединения инфекционных осложнений. При определении уровня bFGF и VEGF в сыворотке крови у больного: кровь набирали в пробирки (5 мл), центрифугируя, отделяли сыворотку, которую замораживали при -70°C. До проведения ИФА образцы хранились при данной температуре. Количественное определение bFGF и VEGF в сыворотке проводилось с методом ИФА (ELISA), данный тест основан на методе твердофазного иммуноферментного анализа. Микропланшет покрывали антителами против bFGF и VEGF. В ходе реакции в лунки планшета добавляли стандарты, контроли и неизвестные образцы. Во время первой инкубации bFGF и VEGF связывались произвольно с иммобилизованными в лунках антителами одним сайтом связывания. После промывки добавляли биотинилированные антитела против bFGF и VEGF, которые во второй инкубации связывались с иммобилизованными bFGF и VEGF, связавшимися в первой инкубации. После удаления избытка вторых антител добавили стрептавидин-пероксидазу, которая связывается с биотинилированными антителами с формированием сандвич-комплекса из 4-х реагентов. После третьей инкубации и промывки удалили несвязавшийся фермент, после чего добавили субстратный раствор, который взаимодействует с ферментом с образованием цветного комплекса. Интенсивность окраски раствора прямо пропорциональна концентрации bFGF и VEGF, присутствующих в образце. Для подсчета результатов рассчитывали среднее значение поглощения для каждого стандарта, контроля и образца. Получили содержание bFGF - 39,667 пг/мл и VEGF - 331,730 пг/мл, что позволило прогнозировать злокачественное течение заболевания.
Пример 2. Больная М., 1931 года рождения, г.Салават, РБ. Диагноз ХЛЛ выставлен в апреле 2004 года, подтвержден стернальной пункцией (костный мозг богат клеточными элементами, представлен зрелыми лимфоцитами - 63%). Специфическую терапию не получает. В настоящее время диагноз ХЛЛ II стадия по K.Rai. При определении уровня bFGF и VEGF в сыворотке крови у больной: кровь набирали в пробирки (5 мл), центрифугируя отделяли сыворотку, которую замораживали при -70°C. До проведения ИФА образцы хранились при данной температуре. Количественное определение bFGF и VEGF в сыворотке проводилось с методом ИФА (ELISA), данный тест основан на методе твердофазного иммуноферментного анализа. Микропланшет покрывали антителами против bFGF и VEGF. В ходе реакции в лунки планшета добавляли стандарты, контроли и неизвестные образцы. Во время первой инкубации bFGF и VEGF связывались произвольно с иммобилизованными в лунках антителами одним сайтом связывания. После промывки добавляли биотинилированные антитела против bFGF и VEGF, которые во второй инкубации связывались с иммобилизованными bFGF и VEGF, связавшимися в первой инкубации. После удаления избытка вторых антител добавили стрептавидин-пероксидазу, которая связывается с биотинилированными антителами с формированием сандвич-комплекса из 4-х реагентов. После третьей инкубации и промывки удалили несвязавшийся фермент, после чего добавили субстратный раствор, который взаимодействует с ферментом с образованием цветного комплекса. Интенсивность окраски раствора прямо пропорциональна концентрации bFGF и VEGF, присутствующих в образце. Для подсчета результатов рассчитывали среднее значение поглощения для каждого стандарта, контроля и образца. Получили содержание bFGF - 32,1 пг/мл и VEGF - 66,711 пг/мл, что позволило прогнозировать доброкачественное течение заболевания.
Пример 3. Пациент П., 1935 года рождения, г.Уфа, РБ. Диагноз выставлен в 2001 году, подтвержден стернальной пункцией (костный мозг гиперклеточный, представлен зрелыми лимфоцитами 90%). Неоднократно получал курсы химиотерапии с преднизолоном, циклофосфаном. В настоящее время диагноз ХЛЛ, IV стадия по K.Rai, продолжает принимать лечение, наблюдается увеличение всех групп лимфоузлов до 1,0 см в диаметре, умеренная гепато-спленомегалия, лейкоцитоз до 130×109/л, тромбоцитопенией 70×109/л, Hb 85 г/л. При определении уровня bFGF и VEGF в сыворотке крови у больного: кровь набирали в пробирки (5 мл), центрифугируя, отделяли сыворотку, которую замораживали при -70°C. До проведения ИФА образцы хранились при данной температуре. Количественное определение bFGF и VEGF в сыворотке проводилось с методом ИФА (ELISA), данный тест основан на методе твердофазного иммуноферментного анализа. Микропланшет покрывали антителами против bFGF и VEGF. В ходе реакции в лунки планшета добавляли стандарты, контроли и неизвестные образцы. Во время первой инкубации bFGF и VEGF связывались произвольно с иммобилизованными в лунках антителами одним сайтом связывания. После промывки добавляли биотинилированные антитела против bFGF и VEGF, которые во второй инкубации связывались с иммобилизованными bFGF и VEGF, связавшимися в первой инкубации. После удаления избытка вторых антител добавили стрептавидин-пероксидазу, которая связывается с биотинилированными антителами с формированием сандвич-комплекса из 4-х реагентов. После третьей инкубации и промывки удалили несвязавшийся фермент, после чего добавили субстратный раствор, который взаимодействует с ферментом с образованием цветного комплекса. Интенсивность окраски раствора прямо пропорциональна концентрации bFGF и VEGF, присутствующих в образце. Для подсчета результатов рассчитывали среднее значение поглощения для каждого стандарта, контроля и образца. Получили содержание bFGF - 53,163 пг/мл и VEGF - 796,730 пг/мл, что позволило прогнозировать агрессивное течение заболевания и планировать соответствующее лечение.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПРОГНОЗИРОВАНИЯ КЛИНИЧЕСКОЙ ФОРМЫ ХРОНИЧЕСКОГО ЛИМФОЛЕЙКОЗА | 2012 |
|
RU2490642C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ РАЗВИТИЯ И ТЕЧЕНИЯ ХРОНИЧЕСКОГО ЛИМФОЛЕЙКОЗА | 2003 |
|
RU2248574C1 |
| Способ прогнозирования течения хронического лимфолейкоза | 2022 |
|
RU2788816C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ ТЕЧЕНИЯ ХРОНИЧЕСКОГО ЛИМФОЛЕЙКОЗА | 2004 |
|
RU2256921C1 |
| СПОСОБ ДИФФЕРЕНЦИАЛЬНОЙ ДИАГНОСТИКИ ДОБРОКАЧЕСТВЕННОЙ И ПРОГРЕССИРУЮЩЕЙ ФОРМ ХРОНИЧЕСКОГО ЛИМФОЛЕЙКОЗА | 2003 |
|
RU2242004C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ ОТВЕТА НА ХИМИОТЕРАПИЮ ПРИ ХРОНИЧЕСКОМ ЛИМФОЛЕЙКОЗЕ | 2012 |
|
RU2495427C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ "ТЛЕЮЩЕЙ" ФОРМЫ ХРОНИЧЕСКОГО ЛИМФОЛЕЙКОЗА | 2012 |
|
RU2496110C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ ТЕЧЕНИЯ МНОЖЕСТВЕННОЙ МИЕЛОМЫ | 2002 |
|
RU2225612C2 |
| Способ прогнозирования развития жизнеопасных предсердных аритмий у пациентов с гипертонической болезнью | 2016 |
|
RU2634246C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ ЧАСТО РЕЦИДИВИРУЮЩЕГО ТЕЧЕНИЯ ХРОНИЧЕСКОГО ПАНКРЕАТИТА У ЖЕНЩИН С ОТЯГОЩЕННЫМ АНАМНЕЗОМ | 2013 |
|
RU2547582C1 |
Изобретение относится к медицине и касается способа прогнозирования течения хронического лимфолейкоза. Сущность способа заключается в том, что проводят количественное определение in vitro основного фактора роста фибробластов (bFGF) и фактора роста сосудистого эндотелия человека (VEGF) методом ИФА (ELISA) в сыворотке крови человека. При значениях VEGF 185,66±33,5 и более пг/мл, bFGF 35,84±2,02 и более пг/мл прогнозируют быстрое развитие и агрессивное течение заболевания, плохой ответ на проводимую терапию. При значениях VEGF 72,67±12,3 пг/мл, bFGF 34,06±2,59 пг/мл прогнозируют медленное развитие и доброкачественное течение заболевания. Использование изобретения повышает точность оценки развития и течения заболевания, осуществляет прогноз плохого ответа на проводимую терапию у больных хроническим лимфолейкозом. 2 ил., 1 табл.
Способ прогнозирования течения хронического лимфолейкоза, включающий определение у больных количественного содержания фактора роста сосудистого эндотелия человека (VEGF) и основного фактора роста фибробластов (bFGF), отличающийся тем, что их определяют в сыворотке крови и при значениях VEGF 185,66±33,5 и более пг/мл, bFGF 35,84±2,02 и более пг/мл прогнозируют быстрое развитие и агрессивное течение заболевания, плохой ответ на проводимую терапию, при значениях VEGF 72,67±12,3 пг/мл, bFGF 34,06±2,59 пг/мл прогнозируют медленное развитие и доброкачественное течение заболевания.
| НО C.L | |||
| et al | |||
| B-cell chronic lymphocytic leukemia: correlation of clinical stages with angiogenic cytokine expression // Appl | |||
| Immunohistochem | |||
| Mol | |||
| Morphol., 2006, Jun, 14 (2): 154-60 | |||
| SMOLEJ L | |||
| et al | |||
| Basic fibroblast growth factor (bFGF) and vascular endothelial growth factor (VEGF) are elevated in peripheral blood plasma of patients with |
Авторы
Даты
2010-09-27—Публикация
2009-04-21—Подача