Изобретение относится к медицине, а именно к гематологии, может быть использовано для прогнозирования развития множественной миеломы.
Множественная миелома (MM) - одно из наиболее распространенных злокачественных заболеваний системы крови, отличающееся вариабельностью клинических форм, трудностью прогнозирования исходов, сопровождающееся утратой трудоспособности, инвалидизацией и высокой смертностью.
Вместе с тем своевременное назначение адекватной терапии позволяет значительно увеличить продолжительность жизни, выживаемость, а также качество жизни пациентов с ММ. Вышеизложенное определяет необходимость разработки новых способов прогнозирования клинических вариантов течения ММ на самых ранних стадиях развития заболевания.
Согласно литературным данным, к факторам неблагоприятного прогноза ММ относятся: содержание плазматических клеток более 10%, наличие костных повреждений, увеличение концентрации сывороточного β2-микроглобулина более 6 мг/мл, морфологические признаки дисгемопоэза в гранулоцитарном ростке костного мозга (Подольцева Э.И. Классификация множественной миеломы. Гематология и трансфузиология. - 1997. - Т.42, 3, С.8-11).
Известен способ прогнозирования развития ММ по стадии заболевания, сывороточным уровням β-микроглобулина, С-реактивного белка (Anderson K.C., Kyle R.A., Dalton W.S. et al. Multiple Myeloma: New Insights and Therapeutic Approaches. // Hematology. - 2000. - P.147-165). Однако установлено, что изменения этих показателей не всегда выявляются в начале развития патологического процесса, тогда как вероятность благоприятного течения ММ повышается при назначении адекватной терапии с самого начала заболевания.
Известен цитогенетический способ прогнозирования развития и исходов MM (Worel N. et al. Deletion of chromosome 13ql4 detected by fluorescence in situ hybridization has prognostic impact on survival after high-dose therapy in patients with multiple myeloma. // Ann. Hemat. - 2001. - V.80. - P.345-348). Так, например, пациенты с ММ с выявленной делецией хромосомы 13ql4 имели более короткую продолжительность заболевания и более низкую выживаемость. Существенными недостатками этого метода являются его трудоемкость и необходимость дорогостоящего оборудования и реактивов.
Прототипом изобретения является способ прогнозирования развития ММ путем определения уровня интерлейкина-6 (ИЛ-6) в сыворотке крови у больных в различной степенью агрессивности ММ (Зарайский М.И. Роль маркеров главного комплекса гистосовместимости в прогнозировании активности течения множественной миеломы. // Автореф. дисс. канд. мед. наук. - 1998. - 23 с.). Было выявлено, что в группе с агрессивным течением ММ отмечается существенно повышенный уровень сывороточного ИЛ-6, средние значения уровня ИЛ-6 у больных активной и индолентной формами (неагрессивная ММ) достоверно выше, чем в группе здоровых доноров. Указанный способ позволяет достоверно прогнозировать характер течения заболевания у больных ММ на четко выраженной клинической стадии. Вместе с тем к недостаткам способа следует отнести следующие: 1) относительно высокую вариабельность сывороточного уровня (СУ) ИЛ-6 даже в течение суток у одного и того же пациента (например, утреннее или послеобеденное время); 2) широкая вариабельность СУ ИЛ-6 в пределах одной клинической группы (например, агрессивная форма ММ); 3) применение химиотерапии может существенно влиять на регистрируемый СУ ИЛ-6 (Emile С., Fermand J.P. Danon F. Interleukine-6 serum levels in patients with multiple myeloma. // Br. J. Haematol. - 1994.- V.86. - P.439-440; Fishman D., Faulds G., Jeffery R. et al. The effect of novel polymorphisms in the interleukin-6 on IL-6 transcription and plasma levels, and an association with systemic-onset juvenile chronic arthritis. // J. Clin. Invest. - 1998. - V. 102. Р. 1369-1376). Главным недостатком способа является невозможность выделить группы благоприятного (неблагоприятного) течения заболевания на начальной стадии и тем самым осуществить своевременные профилактические мероприятия (адекватная химиотерапия).
Техническим результатом изобретения является повышение точности прогнозирования вариантов клинического течения ММ на самых ранних стадиях развития заболевания.
Указанный технический результат достигается тем, что в выделенной методом фенольно-хлороформной экстракции ДНК из лимфоцитов периферической венозной крови проводят генотипирование полиморфизма промоторной области гена ИЛ-6 в сайте 174 G/C методом полимеразной цепной реакции синтеза ДНК (ПЦР) с последующей рестрикцией. После амплификации и рестрикции фрагменты ДНК разделяют электрофоретически в 7%-ном полиакриламидном неденатурированном геле и анализируют при ультрафиолетовом освещении на трансиллюминаторе: наличие ДНК-фрагментов 31+122+45 нуклеотидных пар (н.п.) интерпретируют как аллель цитозин-С, размером 31+167 н.п. - как гуанин-G. При выявлении у обследуемого пациента с ММ в самом начале заболевания генотипа С/С прогнозируют, что заболевание у больного будет развиваться только по медленно прогрессирующему типу.
Способ осуществляется следующим образом.
ДНК выделяют из лимфоцитов периферической крови. В качестве консерванта используют раствор следующего состава: 0,48% лимонной кислоты, 1,32% цитрата натрия, 1,47% глюкозы. При заборе крови к 1 мл консерванта добавляют 6 мл крови и хорошо перемешивают.
Для получения ДНК необходимой степени чистоты и достаточного молекулярного веса используется метод выделения ДНК из крови фенольно-хлороформной экстракцией, описанный Мэтью (Mathew C.C. The isolation of high molecular weight eucariotic DNA. // Methods in Molecular Biology. / Ed. Walker J.M., N.Y. L.: Human Press. - 1984. - V.2. - P.31-34).
1. Кровь в пробирке с консервантом тщательно перемешивается и переливается в центрифужный стакан на 100 мл, туда же добавляли 50 мл охлажденного лизирующего буфера, содержащего 320 мМ сахарозы, 1% раствор тритона Х-100, 5мМ MgCl2, 10 мМ трисНСl (рН 7,6).
2. Смесь центрифугируется 20 мин при 4000 об/мин.
3. Надосадочную жидкость сливают, к получившемуся осадку приливают 8 мл 25 мМ ЭДТА, рН 8,0, суспендируют.
4. К суспензии добавляют 0,8 мл 10% SDS и протеиназу К (концентрация 10 мг/мл). Смесь для лизиса оставляют на ночь в термостате при температуре 38oС.
Экстракцию ДНК осуществляют в следующем порядке.
1. Для депротеинизации к лизату добавляют 0,5 мл 5 М перхлората натрия и 8 мл фенола, насыщенного 1 М трисНСl до рН 7,8.
2. Смесь центрифугируют при 3000 об/мин в течение 10 мин.
3. Отбирают водную фазу, содержащую ДНК, РНК и неденатурированные белки.
4. Отобранную фазу обрабатывают смесью фенол-хлороформа (1:1), а затем - хлороформом.
5. Препараты осаждают двумя объемами 96% этанола.
6. Образовавшийся осадок ДНК растворяют в 1,5 мл деионизированной Н2О; раствор хранят при -20oС.
В дальнейшем полученную ДНК используют в качестве матрицы для полимеразной цепной реакции (ПЦР) для амплификации нужного фрагмента промоторной области гена ИЛ-6. Специфические последовательности олигонуклеотидных праймеров приведены в работе Fishman и сотр. (Fishman D., Faulds G., Jeffery R. et al. The effect of novel polymorphisms in the interleukin-6 on IL-6 transcription and plasma levels, and an association with systemic-onset juvenile chronic arthritis. // J. Clin. Invest. - 1998. - V. 102. P.1369-1376). Нуклеотидную замену G-->C в положении 174 гена выявляют рестрикцией полученного ПЦР-продукта (198 н.п.) ферментом Hsp92II. Состав реакционной смеси для ПЦР следующий: 0,1-1 мкг геномной ДНК, 0,25 мкМ каждого олигопраймера, 250 мкМ каждого дезоксинуклеозидтрифосфата (Promega, USA) помещали в 25 мкл однократного буфера для ПЦР следующего состава: 67 mM Tris-HCl, рН 8,8, 6,7 mМ MgCl2, 16,6 mM (NH4)2SO4, 0,01% Tween-20. Полученную смесь прогревают 2 минуты при 94oС, добавляют 5 единиц термофильной ДНК-пoлимеразы, 20-30 мкл минерального масла. Режим амплификации: 30 циклов со следующими параметрами: 94oС - 45 секунд, 55oС - 45 секунд, 72oС - 45 секунд.
После 30-го цикла проводили инкубацию при 72oС в течение 7 минут. ПЦР-продукты подвергают рестрикции с помощью фермента Hsp92II при 37oС в течениe ночи и электрофорезу в вертикальном 7% полиакриламидном геле. Для этого 7 мкл ПЦР-продукта смешивают c 5 ед. фермента, смесь выдерживают при 37oС в течение 10 часов. В качестве электролита для электрофореза применяют 1X боратный буфер (0,089 М трис НСl рН 7,8; 0,089 М борная кислота, 0,002 М ЭДТА с рН 8,0).
Перед нанесением на вертикальный электрофорез пробы смешивают в соотношении 1: 5 с краской, содержащей 0,25% бромфенолового синего, 0,25% ксиленцианола, 15% фикола. Электрофорез проводят при постоянном напряжении 10 вольт/см после 15-минутного преэлектрофореза. Детекцию результатов проводят путем окрашивания полиакриламидного геля бромистым этидием в течение 10 минут с последующей визуализацией в ультрафиолетовом свете на трансиллюминаторе. Идентифицированные генотипы типируются по критерию присутствия или отсутствия сайта рестрикции, так что Hsp92II - генотипы GG - это гомозиготы по отсутствию вариабельного сайта (31+167 н.п.), GC - гетерозиготы по отсутствию и наличию сайта (31+167+122+45 н.п.) и СС - гомозиготы по наличию сайта (31+122+45 н.п.).
В качестве контроля обследовали группу здоровых индивидов, проживающих на территории республики Башкортостан (101 человек), у которых отсутствовали какие-либо злокачественные заболевания.
В качестве конкретных примеров обследовано в целом 47 больных ММ, находившихся на лечении в гематологическом отделении РКБ, в возрасте от 32 до 75 лет.
С учетом клинико-лабораторных показателей, характеризующих течение заболевания (лабораторные, рентгенологические, длительность заболевания), с учетом рекомендаций Н. Е. Андреевой (Андреева Н.Е. Диагностика и лечение множественной миеломы. - М. : Ньюдиамед-АО, 1998. - 29 с.) в общей группе больных ММ мы выделили 2 подгруппы:
1) медленно прогрессирующее течение - это отсутствие миелодепрессии, мягкотканых метастазов, сдвига в лейкоформуле, длительность заболевания (20 человек);
2) быстро прогрессирующее течение - в том числе острый плазмобластный лейкоз и ММ-саркома (15 человек).
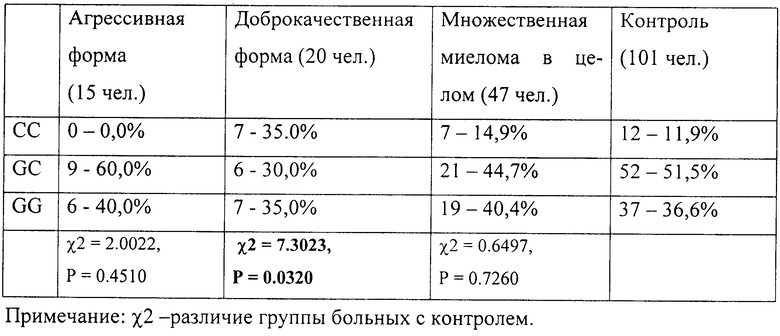
Результаты молекулярно-генетического анализа полиморфного локуса -174 G/C в промоторной области гена ИЛ-6 у больных ММ представлены в таблице (см. в конце описания).
Как видно из приведенных данных, при сопоставлении группы больных ММ в целом и контролe по распределению частот генотипов рассматриваемого локуса достоверных отличий не выявлено. Однако анализ ассоциации данного полиморфизма со степенью агрессивности ММ позволил установить, что генотип СС был обнаружен только у больных ММ с доброкачественной формой, в группе с агрессивным течением индивидов с генотипом СС не выявлено (предположительный протективный эффект генотипа СС). Применение критерия χ2 показало, что существуют достоверные отличия между группой больных с доброкачественной формой ММ и контролем (см. таблицу).
Наши данные согласуются с результатами исследований, полученными другими авторами относительно роли ИЛ-6 как фактора, ингибирующего апоптоз при ММ. По всей видимости, более низкий конститутивный и индуцибельный уровень транскрипции гена ИЛ-6 у индивидов с генотипом СС может иметь выраженное протективное действие при клинической манифестации ММ. В свою очередь, немедленное генотипирование больных ММ при постановке диагноза позволило бы выделить тех пациентов, которые генетически более устойчивы относительно скорости прогрессирования заболевания. Индивидам, обладающим генотипом СС, мы могли бы рекомендовать назначение более мягкого курса химиотерапии, что позволило бы существенно повысить качество их жизни.
Пример 1. Б-ой Ю. А. 1930 года рождения, город Сибай, Республика Башкортостан. Диагноз ММ установлен в апреле 1996 года, подтвержден стернальной пункцией, где обнаружено 31,5% плазматических клеток. Регулярно получает полихимиотерапию с включением циклофосфана, винкристина, алкерана, белюстина, преднизолона. В настоящее время продолжает принимать лечение, наблюдается стабилизация в течении заболевания. При молекулярно-генетическом тестировании у больного было взято 8 мл венозной крови с последующим выделением ДНК и амплификацией полиморфного участка гена ИЛ-6 в реакционной смеси, содержащей примерно 0,1-1 мкг геномной ДНК, 1 ед. Taq-полимеразы, 0,25 мкМ каждого олигопраймера, 250 мкМ каждого дезоксинуклеозидтрифосфата в 25 мкл однократного буфера для ПЦР. После рестрикции амплифицированных ПЦР-продуктов эндонуклеазой Hsp92II провели электрофорез фрагментов при постоянном напряжении 250-300 вольт после 15-минутного преэлектрофореза. После окончания электрофореза гель окрасили раствором бромистого этидия в течение 10 минут и анализировали при ультрафиолетовом освещении на трансиллюминаторе. Исследование полиморфного локуса гена ИЛ-6 больного выявило генотип СС. Выявление данного генотипа позволило прогнозировать медленно прогрессирующее течение заболевания.
Пример 2. Пациент А-ев Я.С. 1931 года рождения, г. Янаул, Республика Башкортостан. Диагноз ММ установлен в сентябре 2000 года, подтвержден миелограммой - 40% плазматических клеток. Заболевание было диагностировано во 2 стадии, осложнено очагами деструкций в плоских костях, позвоночнике. Проводилось лечение по схеме М-2 с включением циклофосфана, белостина с соблюдением доз и интервалов лечения. Увеличивалась площадь остеодеструкций, гиперазотемия, гиперкальцемия. При молекулярно-генетическом тестировании у больного было взято 8 мл венозной крови с последующим выделением ДНК и амплификацией полиморфного участка гена ИЛ-6 в реакционной смеси, содержащей примерно 0,1-1 мкг геномной ДНК, 1 ед. Taq-полимеразы, 0,25 мкМ каждого олигопраймера, 250 мкМ каждого дезоксинуклеозидтрифосфата в 25 мкл однократного буфера для ПЦР. После рестрикции амплифицированных ПЦР-продуктов эндонуклеазой Hsp92II провели электрофорез фрагментов при постоянном напряжении 250-300 вольт после 15-минутного преэлектрофореза. После окончания электрофореза гель окрасили раствором бромистого этидия в течение 10 минут и анализировали при ультрафиолетовом освещении на трансиллюминаторе. При исследовании установлен G/С генотип, что не позволило нам прогнозировать медленно прогрессирующее течение болезни. Смерть наступила в декабре 2000 г.
Таким образом, нами проведено молекулярно-генетическое изучение полиморфного локуса -174 G/C в промоторной области гена ИЛ-6 у 47 больных ММ и в контрольной группе. Установлено, что больные с генотипом СС встречаются только в группе с медленно прогрессирующим течением заболевания. Полученные данные позволяют прогнозировать благоприятные варианты течения ММ у больных с генотипом СС на самых ранних стадиях развития заболевания.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПРОГНОЗИРОВАНИЯ ТЕЧЕНИЯ МНОЖЕСТВЕННОЙ МИЕЛОМЫ | 2005 |
|
RU2282852C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ РАЗВИТИЯ И ТЕЧЕНИЯ ХРОНИЧЕСКОГО ЛИМФОЛЕЙКОЗА | 2003 |
|
RU2248574C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ РАЗВИТИЯ ТОКСИЧЕСКОГО ГЕПАТИТА ПРИ ХИМИОТЕРАПИИ МНОЖЕСТВЕННОЙ МИЕЛОМЫ | 2005 |
|
RU2283494C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ КЛИНИЧЕСКОЙ ФОРМЫ ХРОНИЧЕСКОГО ЛИМФОЛЕЙКОЗА | 2012 |
|
RU2490642C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ ТЕЧЕНИЯ НЕХОДЖКИНСКИХ ЛИМФОМ | 2012 |
|
RU2490641C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ РАЗВИТИЯ В-КЛЕТОЧНЫХ И Т-КЛЕТОЧНЫХ НЕХОДЖКИНСКИХ ЛИМФОМ | 2012 |
|
RU2490638C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ "ТЛЕЮЩЕЙ" ФОРМЫ ХРОНИЧЕСКОГО ЛИМФОЛЕЙКОЗА | 2012 |
|
RU2496110C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ ОТВЕТА НА ХИМИОТЕРАПИЮ ПРИ ХРОНИЧЕСКОМ ЛИМФОЛЕЙКОЗЕ | 2012 |
|
RU2495427C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ ПЕРВИЧНОЙ АДЕНТИИ | 2009 |
|
RU2394242C1 |
| Способ прогнозирования развития детского ожирения в Республике Башкортостан | 2022 |
|
RU2794991C1 |
Изобретение относится к медицине, а именно к гематологии. Сущность изобретения заключается в выделении ДНК из лимфоцитов периферической венозной крови методом фенольно-хлороформной экстракции, генотипировании полиморфизма промоторной области гена ИЛ-6 в сайте 174 G/С методом полимеразной цепной реакции синтеза ДHК с последующей рестрикцией. После амплификации и рестрикции фрагменты ДНК разделяют электрофоретически в 7%-ном полиакриламидном неденатурирующем геле и анализируют при ультрафиолетовом освещении на трансиллюминаторе. Наличие ДНК-фрагментов 31+122+45 нуклеотидных пар интерпретируют как аллель цитозин-С, а размером 31+167 нуклеотидных пар - как гуанин-G. При выявлении у больного с множественной миеломой в начале заболевания генотипа СС прогнозируют его медленно-прогрессирующее течение. Преимущество заключается в повышении точности прогнозирования. 1 табл.
Способ прогнозирования течения множественной миеломы, включающий выделение ДНК из лимфоцитов периферической венозной крови больного, генотипирование полиморфизма промоторной области IL-6 в сайте 174 G/C методом полимеразной цепной реакции синтеза ДНК и при выявлении генотипа СС прогнозируют медленно-прогрессирующее течение множественной миеломы у больного.
| Зарайский М.И | |||
| Роль маркеров главного комплекса гистосовместимости в прогнозировании активности течения множественной миеломы | |||
| Автореферат дисс | |||
| канд | |||
| мед | |||
| наук, 1998, с | |||
| Прибор для равномерного смешения зерна и одновременного отбирания нескольких одинаковых по объему проб | 1921 |
|
SU23A1 |
| СПОСОБ ДИАГНОСТИКИ МНОЖЕСТВЕННОЙ МИЕЛОМЫ | 2000 |
|
RU2172489C1 |
| ПРИМЕНЕНИЕ ЦИКЛОДЕКСТРИНА В КАЧЕСТВЕ МУКОАДГЕЗИВА, КОМПОЗИЦИЯ НА ОСНОВЕ ИНТРАКОНАЗОЛА И ЦИКЛОДЕКСТРИНА И СПОСОБ ЕЕ ПОЛУЧЕНИЯ | 1995 |
|
RU2164418C2 |
| Дорожная спиртовая кухня | 1918 |
|
SU98A1 |
| US 5753464 А, 19.05.1998 | |||
| US 6245562 A1, 12.06.2001. | |||
Авторы
Даты
2004-03-10—Публикация
2002-04-30—Подача