Изобретение относится к области органической химии, конкретно к способу получения хлоридов 2,3-дигидро[1,3]теллуразолия, который может найти применение в тонком органическом синтезе, в производстве лекарственных препаратов, биологически активных веществ. Известен способ получения солей N-метил-2-фенил-1,3-бензотеллуразолия алкилированием йодистым метилом 2-фенил-1,3-бензотеллуразола [Садеков И.Д., Абакаров Г.М., Шнейдер А.А., Минкин В.И. Азот-теллурсодержащие гетероциклы. 3. Реакция 2-фенилбензотеллуразола по гетероатомам // Химия гетероциклических соединений. 1989. №7. С.989-993]. 2-Фенил-1,3-бензотеллуразол синтезирован по реакции циклизации о-метилтеллуро-N-бензоиланилина под действием POCl3 [Абакаров Г.М., Шабсон А.А., Садеков И.Д., Гарновский А.Д., Минкин В.И. Азот-теллур содержащие гетероциклы. 1. Синтез бензотеллуразолов и их производных // Химия гетероциклических соединений. 1988. №2. С.276-278].
Известный способ не позволяет получать соли 2,3-дигидро[1,3]теллуразолия.
Предлагается новый способ синтеза солей 2,3-дигидро[1,3]теллуразолия общей формулы

где R1 - алкил или фенил,
R2 - алкил, фенил или водород,
R1+R2 - циклоалкил.
Технический результат - получение новых солей 2,3-дигидро[1,3]тиазолия.
Этот технический результат достигается тем, что в способе получения хлоридов 2,3-дигидро[1,3]теллуразолия общей формулы

где R1 - алкил или фенил,
R2 - алкил, фенил или водород,
R1+R2 - циклоалкил;
подвергают взаимодействию олефин с 2-пиридинтеллуренилхлоридом в эквимольном соотношении в среде хлористого метилена.
Сущность способа заключается во взаимодействии олефинов с 2-пиридинтеллуренилхлоридом, содержащим в гетарильном фрагменте нуклеофильный атом азота, в среде хлористого метилена при 20-25°С в течение 18-24 ч. Реакции проводятся при эквимольных соотношениях реагентов. По окончании из реакционной массы растворитель удаляют вакуумированием, а остаток кристаллизуют из хлористого метилена. Общий выход хлоридов 2,3-дигидро[1,3]теллуразолия составляет 93-97%.
Реакции протекают по схеме

Способ поясняется следующим примерами.
Пример 1. К суспензии 1.21 г (5 ммоль) 2-пиридинтеллуренилхлорида в 10 мл хлористого метилена при 25°С прибавляют при перемешивании раствор 0.52 г (5 ммоль) стирола в 10 мл хлористого метилена. Через 18 ч после полного растворения реагента растворитель упаривают в вакууме. После перекристаллизации остатка из хлористого метилена получают 1.68 г (97%) хлорида 3-фенил-2,3-дигидро[1,3]теллуразоло[3,2-а]пиридиния-4. Т.пл. 172-174°С. ИК-спектр (KBr), ν, см-1: 2360, 1608, 1552, 1481, 1438, 1292, 765. Спектр ЯМР 1Н (ДМСО-d6), δ, м. д. (J, Гц): 8.52 (1Н, д, 3J=5.9, Het); 8.42 (1Н, д, 3J=7.1, Het); 8.34 (1Н, t, 3J=7.1, Het); 7.75 (1H, т, 3J=5.9, Het); 7.48 (3Н, уш. c, Ph); 7.40 (2H, уш. с, Ph); 6.60 (1H, т, 3J=7.3, CHN+); 4.27 (1Н, д. д, 3J=7.3, 2J=10.3, CH2S); 3.80 (1H, д. д, 3J=7.3, 2J=10.3, CH2Te). Найдено, %: С 45.07; H 3.43; N 4.02. C13H12ClNTe. Вычислено, %: С 45.22; Н 3.50; N 4.06.
Пример 2. К суспензии 1.21 г (5 ммоль) 2-пиридинтеллуренилхлорида в 10 мл хлористого метилена при 20°С прибавляют при перемешивании раствор 0.42 г (5 ммоль) 3,3-диметил-1-бутена в 10 мл хлористого метилена. Через 24 ч после полного растворения реагента растворитель упаривают в вакууме. После перекристаллизации остатка из хлористого метилена получают 1.55 г (95%) хлорида 2-трет-бутил-2,3-дигидро[1,3]теллуразоло-[3,2-а]пиридиния-4. Т. пл. 197-198°С. ИК-спектр (KBr), ν, см-1: 2358, 1606, 1558, 1465, 1440, 1284, 1134, 765. Спектр ЯМР 1Н (ДМСО-d6), δ, м. д. (J, Гц): 9.09 (1Н, д, 3J=6.0, Het); 8.35 (1Н, д, 3J=8.7, Het); 8.26 (1H, т, 3J=8.7, Het); 7.72 (1H, t, 3J=6.0, Het); 5.45 (1H, д. д, 3J=5.9,2J=14.7, CH2N+); 5.16 (1H, д. д, 3J=7.5, 2J=14.7, CH2N+); 4.44 (1H, д. д, 3J=5.9, 3J=7.5, CHTe); 0.98 (9H, c, 3 CH3). Найдено, %: С 40.25; H 4.88; N 4.27. C11H16ClTe. Вычислено, %: С 40.61; H 4.96; N 4.31.
Анализ показывает, что предлагаемое решение соответствует критериям «новизна», «изобретательский уровень» и «промышленная применимость» - способ испытан в лабораторных условиях.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ХЛОРИДОВ [1,4]СЕЛЕНАЗИНО [2,3,4-i,j] ХИНОЛИНИЯ | 2010 |
|
RU2446155C1 |
| СПОСОБ ПОЛУЧЕНИЯ ГЕКСАХЛОРАНТИМОНАТОВ 2,3-ДИГИДРО[1,3]ТИАЗОЛИЯ | 2008 |
|
RU2363701C1 |
| СПОСОБ ПОЛУЧЕНИЯ ХЛОРИДОВ 2,3-ДИГИДРО [1,3] ТЕЛЛУРАЗОЛО [3,2-α] ПИРИМИДИНИЯ | 2013 |
|
RU2529196C1 |
| СПОСОБ ПОЛУЧЕНИЯ ХЛОРИДОВ 2,3-ДИГИДРО[1,3] СЕЛЕНАЗОЛО[3,2-α]ПИРИМИДИНИЯ | 2011 |
|
RU2471779C1 |
| ПРОИЗВОДНЫЕ ИМИДАЗОЛА, СПОСОБ ИХ ПОЛУЧЕНИЯ, ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ НА ИХ ОСНОВЕ И СПОСОБ ЛЕЧЕНИЯ С ИХ ИСПОЛЬЗОВАНИЕМ | 2001 |
|
RU2265598C2 |
| ПИГМЕНТ ДЛЯ ЗАЩИТНЫХ ЭЛЕМЕНТОВ МНОГОСЛОЙНЫХ ИЗДЕЛИЙ НА ОСНОВЕ ЗАМЕЩЕННЫХ ДИТИОЛЕНОВЫХ КОМПЛЕКСОВ НИКЕЛЯ С НЕСИММЕТРИЧНЫМИ ЛИГАНДАМИ | 2019 |
|
RU2703168C1 |
| БИСЧЕТВЕРТИЧНЫЕ СОЛИ АЛКАЛОИДА ХИННОГО ДЕРЕВА В КАЧЕСТВЕ АСИММЕТРИЧЕСКИХ МЕЖФАЗНЫХ КАТАЛИЗАТОРОВ | 2013 |
|
RU2667909C2 |
| 1,3-ДИОКСО -2,3-ДИГИДРО-1H-ПИРРОЛО[3,4-C]ХИНОЛИНЫ (ВАРИАНТЫ), ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ (ВАРИАНТЫ), СПОСОБ ИХ ПОЛУЧЕНИЯ (ВАРИАНТЫ) И СПОСОБЫ ЛЕЧЕНИЯ (ВАРИАНТЫ) | 2003 |
|
RU2257385C2 |
| СПОСОБ ПОЛУЧЕНИЯ N-АРИЛМОРФОЛИНОНОВ, ПРОМЕЖУТОЧНЫЕ СОЕДИНЕНИЯ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2004 |
|
RU2343149C2 |
| НОВЫЕ ФОСФАТНЫЕ СОЕДИНЕНИЯ, СПОСОБ ИХ ПОЛУЧЕНИЯ И ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ, СОДЕРЖАЩИЕ ИХ | 2014 |
|
RU2617682C2 |
Изобретение относится к способу получения новых хлоридов 2,3- дигидро[1,3]теллуразолия общей формулы
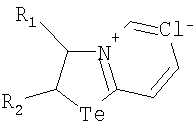
где R1 - алкил или фенил; R2 - алкил, фенил или водород; или R1+R2 - циклоалкил. Способ состоит во взаимодействии олефина с 2-пиридинтеллуренилхлоридом в эквимольном соотношении в среде хлористого метилена. Способ может найти применение в тонком органическом синтезе, в производстве лекарственных препаратов, биологически активных веществ.
Способ получения хлоридов 2,3-дигидро[1,3]теллуразолия общей формулы

где R1 - алкил или фенил;
R2 - алкил, фенил или водород;
R1+R2 - циклоалкил,
отличающийся тем, что подвергают взаимодействию олефин с 2-пиридинтеллуренилхлоридом в эквимольном соотношении в среде хлористого метилена.
| Садеков И.Д | |||
| и др | |||
| Химия гетероциклических соединений, 1989, №7, с.989-993 | |||
| US 4772715 А, 20.09.1988. |
Авторы
Даты
2010-10-27—Публикация
2009-05-12—Подача