ОБЛАСТЬ, К КОТОРОЙ ОТНОСИТСЯ ИЗОБРЕТЕНИЕ
Настоящее изобретение относится к способу получения микросфер с длительным высвобождением, содержащих поддающийся биологическому разложению полимер в качестве носителя и лекарственное средство. Такие микросферы представляют собой инъецируемый состав с длительным высвобождением, который при подкожной или внутримышечной инъекции обеспечивает длительное высвобождение лекарственного средства с постоянной скоростью, поддерживающее его биологическую активность в организме.
УРОВЕНЬ ТЕХНИКИ
Для заключения биоактивных средств в полимерные микросферы, обеспечивающих длительное высвобождение, использовался ряд подходов. Большинство из них основано на разделении фаз (патент США № 4673595, европейский патент № 52510), криопульверизации после экструдирования расплава (патенты США № 5134122, 5192741, 5225205, 5431348, 5439688, 5445832 и 5776885), испарении двойной эмульсии (в/м/в - вода/масло/вода) (патенты США № 4652441, 4711782, 4954298, 5061492, 5330767, 5476663, 5480656, 5611971, 5631020 и 5631021), испарении эмульсии (м/в, масло/вода) (патенты США № 4389330 и 5945126; Shameem М., Lee Hee Yong, DeLuca P.P., AAPS Pharmsci., 1 (3) article 71999; Kostanski J.W., Pharm. Dev. Tech. 5, 585-596, 2000) и распылительной сушке (IE920956).
Инкапсуляция за счет разделения фаз - способ получения микросфер, в котором поддающийся биологическому разложению полимер растворяют в избыточном количестве органического растворителя, например метиленхлорида, и к раствору полимера при перемешивании добавляют лекарственное средство, растворенное в небольшом количестве воды. Затем к смеси лекарственного средства и полимера с постоянной скоростью добавляют силиконовое масло, чтобы образовать зародышевые микросферы, и избыточное количество осадителя, например трихлорфторметана, чтобы извлечь органический растворитель из зародышевых микросфер. Отвержденные микросферы отделяют фильтрацией и сушат под давлением. Однако метод разделения фаз сопряжен со следующими проблемами. Токсичный растворитель, например метиленхлорид, при сушке под давлением не удаляется в достаточном количестве; остаточный растворитель ослабляет стабильность составов, а также может быть вредным для здоровья при введении в организм. Кроме того, добавление для отверждения зародышевых микросфер избытка нерастворителя, такого как фреон, гексан, гептан, циклогексан и трихлорфторметан, при массовом производстве нерентабельно и вызывает серьезное загрязнение окружающей среды.
Криопульверизация после экструдирования расплава, напротив, сопряжена с минимальным использованием токсичных растворителей. Этот метод представляет собой способ получения микросфер, при котором смесь поддающего биологическому разложению полимера с лекарственным средством плавят, экструдируют при высокой температуре и распыляют при низкой температуре. Смесь поддающегося биологическому разложению полимера и лекарственного средства может быть получена путем гомогенного смешивания посредством мешалки полимера и лекарственного средства в растворителе, например метиленхлориде, и удаления органического растворителя с использованием ротационного испарителя или вакуумной сушилки, или путем размалывания при низкой температуре и просеивания каждого порошка и смешивания двух тонких порошков. В последнем случае нет проблемы остаточного токсичного растворителя, потому что во время получения микросфер токсичный растворитель не используется. Однако процедура получения микрочастиц не исключает возможность взаимодействия между полимером и лекарственным средством и денатурации лекарственного средства из-за высокой температуры и высокого давления при экструдировании расплава, а также денатурации лекарственного средства вследствие местного выделениях тепла в процессе криопульверизации. Кроме того, с помощью данного способа трудно получить микросферы одинакового размера, которые легко вводятся с помощью инъекции.
Эти два способа получения микросфер, помимо проблем, связанных с остаточным растворителем, трудностью массового производства и денатурацией лекарственного средства, имеют еще один недостаток, который заключается в том, что поддающийся биологическому разложению полимер, используемый для постоянного высвобождения лекарственного средства, не гидрофилен и, следовательно, плохо диспергируется в водной суспензии для инъекции.
Испарение двойной эмульсии «вода в масле в воде» (в/м/в) широко применялось для заключения гидрофильных лекарственных средств, таких как пептиды или белки, в полимерные микросферы. Данный способ предусматривает получение первичной эмульсии вода в масле, для чего гидрофильное лекарственное средство растворяют в воде, и эту водную фазу диспергируют в органической фазе, содержащей поддающийся биологическому разложению полимер. Первичную эмульсию вновь диспергируют во вторичной водной фазе, содержащей эмульгатор. Для инкапсуляции липофильных лекарственных средств обычно использовалось испарение одинарной эмульсии (масло в воде (м/в)). Согласно этому способу лекарственное средство и поддающийся биологическому разложению полимер вместе растворяют в смеси подходящих органических растворителей (например, метанол и метиленхлорид), и полученный в результате раствор диспергируют в водной фазе. В обоих способах испарения эмульсии по мере того, как органический растворитель удаляется за счет экстракции или испарения во время диспергирования полимера в водной фазе, растворимость полимера снижается, тем самым, он, затвердевая, формирует микросферы. В этих способах технически важным фактором является эффективность инкапсуляции биоактивных лекарственных средств.
Большинство гидрофильных лекарственных средств в большом количестве теряются при диспергировании в водной фазе, что приводит к низкой эффективности инкапсуляции. Чтобы решить эту проблему, Okada и соавторы использовали вещество, например желатин, при получении микросфер способом испарения двойной эмульсии. Это вещество повышало вязкость первичной эмульсии и уменьшало скорость диффузии лекарственного средства (производное LHRH) во вторичную эмульсию, улучшая инкапсуляцию лекарственного средства (Okada, H. and Toguchi, H,, Crit. Rev. Ther. Drug Carrier Syst., 12,1-99, 1995). Аналогично, инкапсуляцию лекарственного средства при испарении одинарной эмульсии тоже можно повысить за счет соответствующего увеличения концентрации поддающегося биологическому разложению полимера (PLGA), растворенного в фазе органического растворителя. Как правило, микросферы, полученные испарением двойной эмульсии, являются более пористыми, чем полученные испарением одинарной эмульсии, и, следовательно, имеют более обширную площадь поверхности, что приводит к относительно высокой начальной скорости высвобождения лекарственного средства.
Однако у способов получения микросфер путем испарения одинарных и двойных эмульсий, таких как метод инкапсуляции за счет разделения фаз, имеются следующие недостатки: трудность удаления органического растворителя, используемого для того, чтобы растворить поддающийся биологическому разложению полимер, затрудненность массового производства из-за изменений в скорости удаления растворителя, аллергические реакции на желатин, используемый для того, чтобы увеличить вязкость первичной эмульсии, возможность денатурации и потери активности лекарственного средства вследствие высоких усилий сдвига, применяемых при получении мелких микросфер во время получения первичной эмульсии, ограниченная инкапсуляция лекарственного средства и тому подобное.
Для получения мелких частиц также использовался способ распылительной сушки. Для этого способа типично следующее: раствор вещества, предназначенного для высушивания, или суспензию, или эмульсию, в которой гомогенно растворены поддающийся биологическому разложению полимер и лекарственное средство, подают в наконечник, распыляют через наконечник и подвергают воздействию горячего воздуха, чтобы испарить используемый растворитель. В частности, в случае получения микросфер с длительным высвобождением, скорость высвобождения лекарственного средства из полученных микросфер сильно зависит от композиции или содержания поддающего биологическому разложению полимера, типа или содержания добавок, состава растворителя и тому подобного. В дополнение к вышеупомянутым параметрам обработки, другие параметры, влияющие на морфологию, размер или свойства микросфер, могут использоваться для контроля скорости высвобождения лекарственных средств. Эти параметры включают тип распылителя, через который распыляют раствор (например, тип, который дробит капельки с использованием сжатого воздуха; тип, который дробит капельки с использованием центробежной силы, когда раствор поступает в диск, вращающийся с высокой скоростью; тип, который дробит капельки, используя ультразвуковые волны, создающиеся при вибрации вибратора, и так далее), скорость подачи и температуру распыляемого раствора, количество подаваемого сухого воздуха и скорость его подачи. Кроме того, способ распылительной сушки, имеет преимущество над другими способами получения микросфер с длительным высвобождения, заключающееся в том, что он обеспечивает непрерывный процесс, который облегчает получение микросфер и, следовательно, переход от небольшого производства к крупномасштабному.
Хотя способ распылительной сушки имеет преимущество крупномасштабного производства микросфер, у него есть и следующие недостатки. Распылительная сушка удаляет используемый растворитель в недостаточной степени. Остаточный растворитель создает угрозу стабильности поддающего биологическому разложению полимера при длительном хранении, что меняет профили высвобождения лекарственного средства из микросфер. Другой недостаток данного способа заключается в том, что поддающие биологическому разложению полимеры, используемые для инкапсуляции лекарственного средства, как правило, негидрофильны, поэтому полученные микросферы плохо поддаются суспендированию, что затрудняет точное дозирование.
Как отмечалось выше, в большинстве традиционных способов получения микросфер с длительным высвобождением используется токсичный растворитель, и эти способы имеют недостатки, включающие присутствие остаточных количеств используемого токсичного растворителя, размер микросфер, не подходящий для инъекции, плохую суспендируемость микросфер и трудности массового производства.
Авторы намереваются предложить способ получения биоактивных, нагруженных лекарственным средством, поддающихся биологическому разложению полимерных микросфер, которые легко получать в крупных масштабах, путем решения вышеупомянутых проблем.
РАСКРЫТИЕ ИЗОБРЕТЕНИЯ
Техническая проблема
Цель настоящего изобретения заключается в том, чтобы предложить способ получения микросфер с длительным высвобождением, содержащих поддающийся биологическому разложению полимер в качестве носителя и биоактивное лекарственное средство, где микросферы можно легко получать в крупных масштабах, они не содержат остаточного токсичного растворителя, который представляет собой проблему для обычных способов получения микросфер с длительным высвобождением, обладают высокой эффективностью при инкапсуляции лекарственного средства и имеют одинаковый размер, подходящий для инъекции.
Техническое решение
Авторы провели интенсивные исследования и обнаружили, что если микросферы, полученные распылительной сушкой раствора, суспензии или эмульсии, содержащих поддающийся биологическому разложению полимер, лекарственное средство и растворитель, суспендировать в водном растворе, содержащем поливиниловый спирт для удаления остаточного растворителя, у микросфер улучшается суспендируемость и проходимость через иглу шприца, они демонстрируют высокую эффективность инкапсуляции лекарственного средства без остаточного токсичного растворителя, что привело к созданию настоящего изобретения.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
Вышеупомянутые и другие объекты, особенности и другие преимущества настоящего изобретения станут более понятны из следующего подробного описания, вместе с сопровождающими рисунками, где:
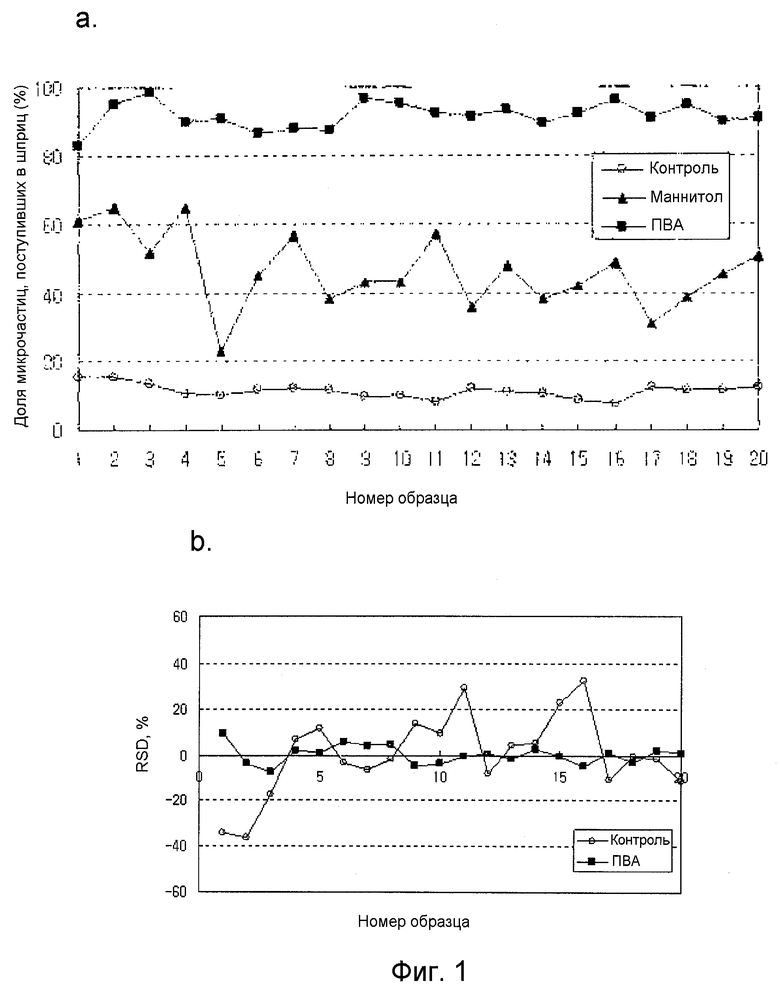
на фиг.1 показана доля диспергированных/поступивших из шприца и прошедших через иглу микросфер, полученных в водном растворе в примере получения 1 по настоящему изобретению, где после выполнения теста по методу, описанному в тестовом примере 1, были измерены доля микросфер, поступивших в каждую пробирку (график а), и отклонение для каждой пробирки от средней доли поступления (график b);
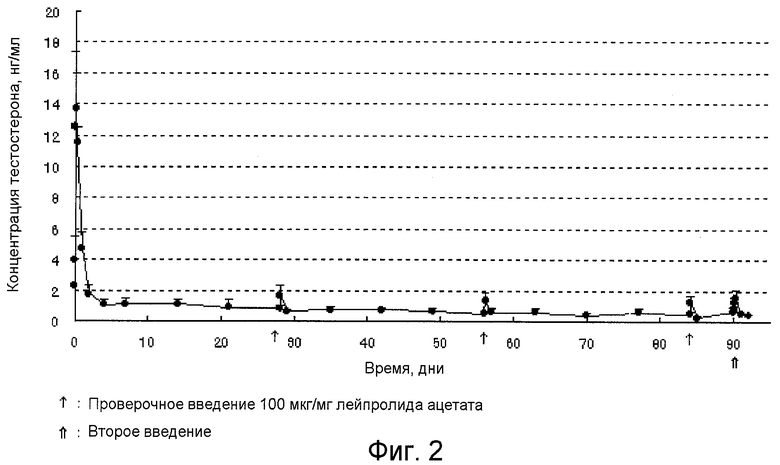
на фиг.2 изображена сывороточная концентрация тестостерона у самцов крыс SD (n=5), которым подкожно ввели, как описано в тестовом примере 5, одну дозу нагруженных лейпрорелином микросфер, полученных в примере получения 8; и
на фиг.3 изображена сывороточная концентрация октреотида у самцов крыс SD (n=6), которым подкожно ввели, как описано в тестовом примере 6, одну дозу нагруженных октреотидом микросфер, полученных в примере получения 9.
ЛУЧШИЙ СПОСОБ ОСУЩЕСТВЛЕНИЯ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к способу получения микросфер с длительным высвобождением, в котором раствор, суспензия или эмульсия, содержащие поддающийся биологическому разложению полимер, лекарственное средство и растворитель, подвергаются распылительной сушке, и таким образом полученные микросферы диспергируются в водном растворе, содержащем поливиниловый спирт, за счет чего лучше удаляется остаточный растворитель и улучшается проходимость микросфер через иглу при введении.
Конкретно настоящее изобретение относится к способу получения микросфер с длительным высвобождением, который отличается высокой эффективностью инкапсуляции лекарственного средства, почти полным отсутствием остаточного растворителя и улучшенной суспендируемостью микросфер, где способ предусматривает растворение и распылительную сушку поддающегося биологическому разложению полимера и лекарственного средства, суспендирование полученных таким образом микросфер в водном растворе, в котором растворен поливиниловый спирт, и выделение, промывку и лиофилизацию микросфер.
Один аспект настоящего изобретения относится к способу получения микросфер с длительным высвобождением, предусматривающему распыление раствора, суспензии или эмульсии, содержащих поддающийся биологическому разложению полимер, лекарственное средство и растворитель в сушильную камеру, и их высушивание с использованием сухого воздуха, чтобы удалить растворитель; и диспергирование микросфер, полученных распылительной сушкой, в водном растворе, содержащем поливиниловый спирт, чтобы удалить остаточный растворитель и улучшить дисперсность микросфер.
Термин «поддающийся биологическому разложению полимер», который используется в данном документе, относится к полимеру, который медленно разрушается после введения в организм и, таким образом, не вреден для организма. Примеры таких полимеров включают полилактид (PLA), полигликозид (PGA) и их сополимер, поли-(лактид-ко-гликозида) (PLGA), полиортоэфир, полиангидрид, полигидроксимасляную кислоту, поликапролактон, полиалкилкарбонат и их производные.
Термин «лекарственное средство», который используется в данном документе, включает пептиды с биологической активностью, такие как противоопухолевые средства, антибиотики, жаропонижающие средства, анальгетики, противовоспалительные средства, противокашлевые отхаркивающие средства, седативные средства, противоязвенные средства, антидепрессанты, антиаллергические средства, антидиабетические средства, гиполипидемические средства, противотуберкулезные средства, гормональные средства, средства, влияющие на метаболизм костей, ингибиторы иммунных реакций, ингибиторы ангиогенеза, противозачаточные средства и средства, подобные витаминам. В частности предпочтительны биологически активный пептид или белковые лекарственные средства. Примеры олигопептидов с биологической активностью включают инсулин, соматостатин и их производные, гормон роста, пролактин, адренокортикотропный гормон, меланоцитстимулирующий гормон, тиреотропин рилизинг-гормон и их соли и производные, тиреотропный гормон, лютеинизирующий гормон, фолликулостимулирующий гормон, вазопрессин и их производные, окситоцин, кальцитонин, паратгормон, глюкагон, гастрин, секретин, панкреозимин, холецистокинин, ангиотензин, плацентарный лактоген человека, хориальный гонадотропин человека и энкефалин, и их производные. Примеры полипептидов включают эндорфин, интерферон (типа α, типа β, типа γ), интерлейкин, тафтсин, тимопоэтин, тимозин, тимостимулин, тимусный гуморальный фактор (THF), сывороточный тимусный фактор и их производные, фактор некроза опухолей, колониестимулирующий фактор (CSF), мотилин, динорфин, бомбезин, нейтротензин, брадикинин, церулеин, урокиназу, аспарагиназу, калликреин, вещество P, фактор роста нервов, факторы свертывания крови VIII и IX, лизозим, полимиксин B, колистин, грамицидин, бацитрацин, пептид, стимулирующий белковый синтез, вазоактивный кишечный полипептид, тромбоцитарный фактор роста, рилизинг-фактор гормона роста, морфогенетический белок костей, эпидермальный фактор роста и эритропоэтин.
В настоящем изобретении водный раствор, содержащий поливиниловый спирт, используют для того, чтобы более эффективно удалить остаточный растворитель из микросфер сразу после распылительной сушки и хорошо диспергировать микросферы в растворе для инъекции при введении. Этот водный раствор удаляется в ходе дополнительной стадии промывки, и его окончательное количество в микросферах составляет менее 1%. Кроме того, если микросферы суспендируют в водном растворе поливинилового спирта, чтобы удалить остаточный растворитель, скорость удаления остаточного растворителя можно контролировать путем изменения температуры суспензии. За счет использования этой особенности при небольших объемах производства остаточный растворитель можно удалить за короткое время при комнатной температуре. В случае производства в больших объемах суспензию выдерживают при низкой температуре, чтобы удалять остаточный растворитель с медленной скоростью, тем самым предотвращая разрушение продуктов из-за увеличенного времени обработки больших количеств продуктов.
На дополнительной стадии диспергирования содержание поливинилового спирта в водном растворе предпочтительно составляет 0,01-20% (мас./об.) и более предпочтительно, 0,05-10% (мас./об.). Поливиниловый спирт имеет молекулярную массу 3000-300000, предпочтительно 5000-100000 и скорость гидратации - 75-95%. Количество поливинилового спирта, остающегося на поверхности микросфер, предпочтительно составляет 0,02-1% (мас./об.) и более предпочтительно 0,05-0,5% (мас./об.).
Термин «растворитель», который используется в данном документе, относится к веществу, которое в состоянии растворить поддающийся биологическому разложению полимер и/или лекарственное средство. Средние специалисты в данной области техники могут выбрать подходящий растворитель в зависимости от типа поддающего биологическому разложению полимера. Предпочтительно использовать ледяную уксусную кислоту.
Настоящее изобретение включает стадию диспергирования микросфер в водном растворе поливинилового спирта, чтобы улучшить дисперсность микросфер. Стадия диспергирования длится приблизительно 1 минуту или дольше, чтобы достичь максимального эффекта. Предпочтительное время диспергирования составляет 5 минут и более.
В заявке на патент, поданной ранее настоящего изобретения (корейская заявка на патент № 10-2003-0023130), Авторы улучшили эффективность инкапсуляции лекарственного средства и профили высвобождения микросфер за счет гомогенного растворения поддающегося биологическому разложению полимера и лекарственного средства в нетоксичном растворителе и распылительной сушки полученного в результате раствора и предложили способ распылительной сушки, облегчающий массовое производство микросфер. Этот способ распылительной сушки имеет такие преимущества, как легкое массовое производство, низкое содержание остаточного растворителя, высокая эффективность инкапсуляции лекарственного средства и идеальные профили высвобождения лекарственного средства, но имеет и недостатки, которые включают затрудненное диспергирование и суспендирование микросфер с длительным высвобождением, полученных распылительной сушкой, в растворе для инъекций из-за отсутствия гидрофильности у полимера, который содержится в микросферах, и требует дополнительной стадии для удаления остаточного растворителя с тем, чтобы гарантировать стабильность микросфер при длительном хранении. Таким образом, Авторы намеревались устранить эти недостатки в настоящем изобретении.
Обычный способ получения микросфер с помощью сушки распылением, при которой используется два наконечника, раскрыт в патенте США № 5622657. Чтобы улучшить дисперсность полимерных микросфер, которые склонны липнуть друг к другу или образовывать агрегаты в ходе распылительной сушки, процитированное изобретение предлагает способ покрытия нагруженных лекарственным средством полимерных микросфер, предотвращающим агрегацию средством с применением двух наконечников и более, в которых раствор полимера, содержащий биологически активное вещество, и водный раствор средства, предотвращающего агрегацию микрочастиц, распыляют по отдельности различными наконечниками в одно и то же время. Подобный способ раскрыт в корейском патенте № 0177309, где способ отличается распылением дисперсии, в которой растворен водорастворимый диспергатор, в направлении, противоположном направлению распыления поддающего биологическому разложению раствора полимера, содержащего активный ингредиент, и направлению потока сухого воздуха, чтобы покрыть водорастворимым диспергатором часть или все микрочастицы с длительным высвобождением. Процитированные изобретения направлены на то, чтобы предотвратить агрегацию микросферы за счет распыления водного раствора, предотвращающего агрегацию микросфер, немедленно после образования микросфер при распылительной сушке, но эти изобретения имеют следующие недостатки. Поскольку микросферы покрыты предотвращающим агрегацию средством сразу после распылительной сушки, токсичный растворитель, используемый, чтобы растворить полимер для получения микросфер, остается в микросферах в больших количествах. Кроме того, если микросферы суспендированы в растворе для инъекции, используется лишнее количество диспергатора. Кроме того, предотвращающие агрегацию средства, использованные в процитированных изобретениях, такие как гидроксипропилцеллюлоза, карбоксиметилцеллюлоза, глицин, аланин, желатин и коллаген, не улучшает суспендируемость в растворе для инъекции или прохождение через иглу шприца, что приводит к неодинаковым дозам.
С другой стороны, чтобы увеличить текучесть гранул для получения таблеток или лекарственных частиц и улучшить растворимость лекарственных средств, вместе с лекарственным средством можно подвергнуть распылительной сушке водорастворимый диспергатор, например гидроксипропилметилцеллюлозу, гидроксипропилцеллюлозу и поливиниловый спирт, которые будут содержаться в полученном в результате препарате в количестве приблизительно 4-19 мас.% (D. Ermis, A. Yuksel, Preparation of spray-dried microspheres of indomethacin and examination of the effects of coating on dissolution rates, J. Microencapsulation, vol. 16, No. 3, 3315-324(1999)). В литературе водорастворимые диспергаторы используются, чтобы увеличить растворимость плохо растворимых в воде лекарственных средств, тем самым растворяя лекарственные средства за несколько часов, и увеличить текучесть частиц лекарственного средства, тем самым, облегчая такую обработку, как таблетирование. Поливиниловый спирт зарегистрирован как вещество, способное вызвать рак при парентеральном введении животным, поэтому остаточное количество этого вещества должно контролироваться (Carcinogenic Studies on Water-Soluble and Insoluble Macromolecules, Archives of Pathology, 67, 589-617 (1959)). Авторы обнаружили, что если поливиниловый спирт, суспендированный в растворе полимера, распыляется, как описано в вышеупомянутой литературе, содержание поливинилового спирта, который с трудом разрушается в организме, повышается, и начальное высвобождение лекарственного средства значительно увеличивается. Такое высокое начальное высвобождение лекарственного средства может вызвать побочные эффекты и может уменьшить продолжительность высвобождения лекарственного средства, тем самым не гарантируя подходящие терапевтические эффекты.
Авторы получали микросферы с дополнительно удаленным остаточным растворителем, которые обладали улучшенным поступлением через иглу шприца, посредством способа, предусматривающего получение микросфер способом распылительной сушки, разработанным авторами до создания настоящего изобретения, суспендирование микросфер в водном растворе, содержащем поливиниловый спирт, промывку и выделение микросфер.
Способ получения поддающих биологическому разложению полимерных микросфер, содержащих лекарственное средство с биологической активностью по настоящему изобретению, предусматривает получение микросферы распылительной сушкой, суспендирование таким образом полученных микросфер в водном растворе, содержащем поливиниловый спирт, и выделение, промывку и сушку микросфер, которые обеспечивают дополнительно удаление остаточного растворителя и улучшают суспендируемость микросфер после введения, тем самым приводя к точному дозированию лекарственных средств и эффективному лечению заболеваний.
Лучшего понимания настоящего изобретения можно достичь с помощью следующих примеров, которые предназначены для иллюстрации и не должны рассматриваться как ограничивающие настоящее изобретение.
ПРИМЕРЫ ОСУЩЕСТВЛЕНИЯ ИЗОБРЕТЕНИЯ
ПРИМЕР ПОЛУЧЕНИЯ 1: Получение микросфер и последующая обработка с использованием различных диспергаторов
Микросферы PLGA получали, используя распылительную сушилку (SODEVA, Франция), оборудованную ультразвуковым наконечником (Sono-Tek, 120 кГц). Использовали поддающийся биологическому разложению полимер, RG503H (Boehringer-Ingelheim, Германия), и лекарственное средство, лейпрорелина ацетат (Polypeptide Laboratories, Дания). 50 г RG503H и 2,5 г лейпрорелина ацетата гомогенно растворили в 500 мл ледяной уксусной кислоты (Yakuri Pure Chemicals, Япония). Раствор перемещали при скорости потока 3 мл/мин, используя поршневой насос. Перемещенный раствор распылили в распылительной сушилке через ультразвуковой наконечник, установленный в верхней части распылителя, и высушивали сухим воздухом при 200°C. Затем микросферы, полученные из циклона, взятые в определенном объеме, точно взвешивали, добавляли при концентрации 50 мг/мл к водному раствору, содержащему дистиллированную воду и 1% (мас./об.) диспергатора и суспендировали в нем в течение одного часа при комнатной температуре, используя магнитную мешалку. Использованные диспергаторы включали поливиниловый спирт (Sigma, P-8136), поливинилпирролидон (Sigma, PVP-360), сывороточный альбумин человека (Sigma, A-1654), полиэтиленгликоль (Yakuri Pure Chemicals, 28123), Твин-80 (Sigma, P-0343), полоксамер (Sigma, P-1300), натрийкарбоксиметилцеллюлозу (Sigma, C-5678), желатин (Sigma, Г 6650), глицин (Sigma, Г 7126) и маннит (Sigma, М. 8429). Суспензию пропускали через вакуумный фильтр. Микросферы, собранные таким образом, промывали дистиллированной водой 2 раза и высушивали сублимацией.
ТЕСТОВЫЙ ПРИМЕР 1: Оценка доли микросфер, поступивших в шприц, и прохождения их через иглу шприца
Микросферы, полученные в примере приготовления 1, диспергированы в водном растворе и оценены по доле микросфер, поступивших в шприц, и прохождения через иглу. Каждый состав микросфер помещали в лабораторный стакан и смешивали с трижды дистиллированной водой в концентрации 50 мг/мл. Когда микросферы были гомогенно диспергированы при помощи магнитной мешалки, 1 мл дисперсии набирали в шприц объемом 1 мл, снабженный иглой 21G (n=20). 1 мл суспензии микросфер в шприце переносили в пробирку Эппендорфа объемом 1,5 мл и сушили сублимацией. У микросфер, поступивших в пробирку Эппендорфа, определяли сухую массу; результаты приведены в таблице 1.
диспергатора
Из таблицы 1 ясно, что у микросфер, взятых немедленно после распылительной сушки, которые не подвергались процессу диспергирования, и у микросфер, которые подвергались процессу диспергирования в дистиллированной воде, не содержащей диспергатор, снижается доля обратного поступления и гомогенности при набирании в шприц и выведении из шприца. Среди нескольких диспергаторов, упомянутых в литературных исследованиях, поливиниловый спирт показал самую высокую долю поступления, за ним идут желатин, сывороточный альбумин человека и Твин-80. На фиг.1 (график a) показаны доли поступления и однородности микросфер, которые не подвергались процессу диспергирования или подвергались этому процессу при использовании маннита и поливинилового спирта в качестве диспергаторов, если суспензию микросфер набирали в шприц и вводили из шприца в пробирку. На фиг.1 (график b) показано отклонение в каждой пробирке от средней доли выведения из шприца для микросфер, которые не подвергались процессу диспергирования или подвергались этому процессу при использовании поливинилового спирта в качестве диспергатора. Как показано на фиг.1, самая высокая скорость выведения и наилучшая однородность отмечены у микросфер, которые подверглись диспергированию с использованием поливинилового спирта.
ПРИМЕР ПОЛУЧЕНИЯ 2: влияние времени диспергирования на дисперсию микросфер
Микросферы PLGA получали, используя распылительную сушилку (SODEVA, Франция), оборудованную ультразвуковым наконечником (Sono-Tek, 120 кГц). Использовали поддающийся биологическому разложению полимер, RG503H (Boehringer-Ingelheim, Германия), и лекарственное средство, лейпрорелина ацетат (Polypeptide Laboratories, Дания). 40 г RG503H и 4 г лейпрорелина ацетата гомогенно растворили в 400 мл ледяной уксусной кислоты (Yakuri Pure Chemicals, Япония). Раствор распыляли в распылительной сушилке через ультразвуковой наконечник при скорости подачи 3 мл/мин и высушили сухим воздухом при 200°C. Затем микросферы, полученные из циклона, взятые в определенном количестве, добавляли при концентрации 50 мг/мл к водному раствору, содержащему дистиллированную воду и 1% (мас./об.) диспергатора и суспендировали в нем в течение 1 мин, 3 мин, 5 мин, 10 мин, 1 ч, 3 ч и 6 ч при 25°C, используя магнитную мешалку. Суспензию пропускали через вакуумный фильтр. Микросферы, собранные таким образом, промывали дистиллированной водой 2 раза и высушивали сублимацией.
ТЕСТОВЫЙ ПРИМЕР 2: Оценка доли выведения и поступления микросфер через иглу шприца
Микросферы, полученные в примере получения 2, диспергировали в водном растворе; затем оценивали долю микросфер, поступивших в шприц, и их прохождение через иглу. Этот тест выполняли по той же методике, что и в тестовом примере 1; результаты приведены в таблице 2, ниже.
диспергирования
Как очевидно из таблицы 2, высокая доля поступления микросфер наблюдалась сразу после того, как микросферы были суспендированы в растворе поливинилового спирта. По мере того как время диспергирования увеличивалось, росли доля поступивших в шприц микросфер и однородность при набирании в шприц и введении из шприца. Однако через определенное время суспендирования доля и однородность микросфер, поступивших в шприц, становились постоянными.
ТЕСТОВЫЙ ПРИМЕР 3: Измерение остаточного содержания поливинилового спирта
Микросферы, полученные в примере приготовления 2, оценивали на остаточное содержание поливинилового спирта. Этот анализ выполнили по модифицированной методике, описанной в Journal of Controlled Release, 82 (2002), 105-114, следующим образом: 2 мг состава, который был точно взвешен, поместили в стеклянный флакон, смешали с 400 мл 0,5 н. NaOH и позволили прореагировать в термостате при 60°С в течение 2-3 ч до полного растворения (n=3). Раствор, в котором были полностью растворены микросферы, нейтрализовали 180 мл 1 н. НСl с добавкой 600 мл 0,65 М борной кислоты и раствора 100 мл I/KI (0,05 М/0,15 М), и позволили реагировать в течение 20 мин. Затем измерили спектральную поглотительную способность при 690 нм (УФ). Результаты приведены в таблице 3.
Как показано в таблице 3, остаточное количество поливинилового спирта увеличивалось по мере того, как возрастало время суспендирования в растворе поливинилового спирта.
Если результаты, приведенные в таблицах 2 и 3, взять вместе, дисперсность и доля микросфер, поступающих в шприц, сразу повышались после того, как микросферы были суспендированы и диспергированы в водном растворе поливинилового спирта, но для оптимального эффекта необходимо время диспергирования приблизительно 5 мин или дольше. В этом случае количество поливинилового спирта, остающегося на поверхности микросфер, превышало 0,05 мас.%. Это критический фактор, определяющий долю микросфер, поступивших в шприц.
СРАВНИТЕЛЬНЫЙ ПРИМЕР ПОЛУЧЕНИЯ 1: получение микросфер совместным распылением с поливиниловым спиртом
Микросферы PLGA получали, используя распылительную сушилку (SODEVA, Франция), оборудованную ультразвуковым наконечником (Sono-Tek, 120 кГц). Использовали поддающийся биологическому разложению полимер, RG503H (Boehringer-Ingelheim, Германия), и лекарственное средство, лейпрорелина ацетат (Polypeptide Laboratories, Дания). Для приготовления контрольного состава микросфер 1,8 г RG503H и 0,2 г лейпрорелина ацетата гомогенно растворяли в 90 мл ледяной уксусной кислоты. Раствор перекачивали со скоростью 3 мл/мин, используя поршневой насос. Перемещенный раствор распыляли в распылительной сушилке через ультразвуковой наконечник, установленный в верхней части распылителя, и высушивали сухим воздухом при 200°C. Затем микросферы, полученные из циклона, взятые в определенном объеме, точно взвесили, добавили при концентрации 50 мг/мл к водному раствору, содержащему дистиллированную воду и 1% (мас./об.) поливинилового спирта в качестве диспергатора и суспендировали в нем в течение 1 ч при комнатной температуре, используя магнитную мешалку. Суспензию пропустили через вакуумный фильтр. Микросферы, собранные таким образом, промывали дистиллированной водой 2 раза и высушили сублимацией.
Сравнительный состав микросфер получили с помощью одновременной распылительной сушки микросфер и поливинилового спирта, чтобы сравнить диспергирующий эффект поливинилового спирта, подвергнутого одновременной распылительной сушке, с контрольным составом. 1,8 г RG503H и 0,2 г лейпрорелина ацетата гомогенно растворили в 90 мл ледяной уксусной кислоты. Раствор перекачивали со скоростью 1,5 мл/мин, используя поршневой насос. Перекачанный раствор распылили в распылительной сушилке через ультразвуковой наконечник, установленный в верхней части распылителя, и высушили сухим воздухом при 200°C, что дало сравнительный состав.
Контрольный и сравнительный составы микросфер, полученные как указано выше, по отдельности диспергировали в водном растворе и оценивали по доле микросфер, поступивших в шприц, и по поступлению через иглу. Этот анализ выполнили по тому же методу, что и в тестовом примере 1, и измерили окончательную сухую массу микросфер в пробирках. Результаты указаны в таблице 4. Остаточное количество поливинилового спирта в каждом составе микросфер определили тем же методом, что и в тестовом примере 3.
In vitro тест на высвобождение выполнили следующим образом. 10 мг каждого состава микросфер поместили в пробирку объемом 1,5 мл, смешали с 1 мл физиологического раствора с фосфатным буфером (PBS) и инкубировали в течение 1 час в термостате при 37 °C и перемешивании со скоростью 5 об./мин, используя ротационный аппарат для встряхивания (SLRM-2M, Seoulin Bioscience). Каждый реакционный раствор центрифугировали и супернатант оценивали на количество лекарственного средства-пептида, высвобожденного из микросфер, используя датчик флюоресценции (Varian, Cary Eclipse; Ex: 280 нм, Em: 350 нм).
и начальное высвобождение лекарственного средства
для контрольного и сравнительного составов микросфер
Как показано в таблице 4, по сравнению с контрольным составом микросфер, подвергшихся диспергированию с поливиниловым спиртом, сравнительный состав микросфер, не подвергавшийся диспергированию, имел высокую остаточную концентрацию поливинилового спирта, но продемонстрировал уменьшенное поступление и однородность при набирании в шприц и выведении из него, а также высокую начальную скорость высвобождения лекарственного средства.
ТЕСТОВЫЙ ПРИМЕР 4: Оценка доли удаленного остаточного растворителя в зависимости от времени диспергирования с поливиниловым спиртом
Микросферы получали и выделяли из циклона тем же самым методом, что и в примере приготовления 2, и суспендировали в 1% водном растворе поливинилового спирта с концентрацией 50 мг/мл.
Когда водный раствор находился при 25°С, скорости удаления остаточной уксусной кислоты измеряли в заданные моменты времени. Концентрацию остаточной уксусной кислоты в микросферах определяли следующим образом. Микросферы растворяли в метиленхлориде (Junsei, 34355-0350), с добавлением 0,07% водного раствора фосфорной кислоты (Sigma, P-6560) и энергично перемешивали. Смесь центрифугировали, чтобы отделить слой водного раствора фосфорной кислоты. Этот слой выделяли и исследовали на количество уксусной кислоты, используя ВЭЖХ. ВЭЖХ выполняли, используя колонку CI 8 (5 мм, 4,6×250 мм, 120Е). В качестве подвижной фазы использовали линейный градиент смеси 5-50% метанола (J.T.Baker, AH230-4) и 0,07% фосфатного буфера (рН 3,0) со скорость потока 1,2 мл/мин. Уксусную кислоту обнаруживали при 210 нм; результаты перечислены в таблице 5. Остаточное содержание уксусной кислоты сразу после получения микросфер составило 0,8 мас.%.
Как показано в таблице 5, доля удаленного растворителя постепенно возрастали с увеличением времени суспендирования микросфер в водном растворе поливинилового спирта. Окончательное количество остаточного растворителя поддерживалось на уровне менее 0,1 мас.%.
ПРИМЕР ПОЛУЧЕНИЯ 3: Получение нагруженных бычьим сывороточным альбумином микросфер распылительной сушкой эмульсии типа в/м, содержащей бычий сывороточный альбумин
0,5 г бычьего сывороточного альбумина (БСА) (Sigma, A-7638) растворяли в дистиллированной воде и гомогенно смешивали с раствором, приготовленным путем растворении 9,5 г RG502H в 95 мл метиленхлорида, что давало эмульсию типа в/м. Пока эмульсия поддерживалась в состоянии эмульсии с помощью мешалки, ее подавали в распылительную сушилку (Buchi-191) со скоростью 3 мл/мин. Сжатый воздух подавали в наконечник с двумя жидкостями со скоростью 450 NL/ч, чтобы высушить распыленные капли, используя сухой воздух с температурой 80°С. Выделенные микросферы суспендировали в течение 3 ч в 1% водном растворе поливинилового спирта при концентрации 50 мг/мл с перемешиванием, используя магнитную мешалку, промывали дистиллированной водой и сушили сублимацией. Микросферы, полученные таким образом, имели средний размер частиц 5,2 мм и количество поливинилового спирта, остающегося на поверхности микросфер, составляло 0,93% (мас./мас.).
ПРИМЕР ПОЛУЧЕНИЯ 4: Получение нагруженных бычьим сывороточным альбумином микросфер с помощью распылительной сушки эмульсии типа S/O, содержащей бычий сывороточный альбумин
1 г БСА тонко измельчали в ступке и гомогенно смешивали с раствором, приготовленным путем растворения 9 г RG502H в 90 мл метиленхлорида, с образованием эмульсии типа 3/0. Пока эмульсия поддерживалась в состоянии эмульсии с помощью мешалки, ее подавали в распылительную сушилку (Buchi-191) со скоростью 3 мл/мин. Сжатый воздух подавали в наконечник с двумя жидкостями со скоростью 450 NL/ч для того, чтобы высушить распыленные капли, используя сухой воздух с температурой 80°С. Выделенные микросферы суспендировали в течение 3 ч в 1% водном растворе поливинилового спирта при концентрации 50 мг/мл с перемешиванием, используя магнитную мешалку, промывали дистиллированной водой и сушили сублимацией. Микросферы, полученные таким образом, имели средний размер частиц 5,8 мм, и количество поливинилового спирта, остающегося на поверхности микросфер, составляло 0,85% (мас./мас.).
ПРИМЕР ПОЛУЧЕНИЯ 5: Получение нагруженных лейпрорелином микросфер
1 г лейпрорелина ацетата и 9 г RG502H растворили в 90 мл ледяной уксусной кислоты. Пока эмульсия поддерживалась в состоянии эмульсии с помощью мешалки, ее подавали в распылительную сушилку (Buchi-191) со скоростью 3 мл/мин. Сжатый воздух подавали в наконечник с двумя жидкостями со скоростью 500 NL/ч, чтобы высушить распыленные капли, используя сухой воздух с температурой 120°С. Выделенные микросферы суспендировали в течение 3 ч в 1% водном растворе поливинилового спирта при концентрации 50 мг/мл с перемешиванием, используя магнитную мешалку, промывали дистиллированной водой и сушили сублимацией. Микросферы, полученные таким образом, имели средний размер частиц 5,1 мм, и количество поливинилового спирта, остающегося на поверхности микросфер, составляло 0,98% (мас./мас.).
ПРИМЕР ПОЛУЧЕНИЯ 6: Получение нагруженных лейпрорелином микросфер
0,4 г лейпрорелина ацетата и 9,6 г RG502H растворили в 96 мл ледяной уксусной кислоты. Раствор подавали в распылительную сушилку (SODEVA, Франция) со скоростью 3 мл/мин, распыляли в сухой камере, используя ультразвуковой распылитель (Sono-Tek, 120 кГц), и сушили сухим воздухом с температурой 200°С. Выделенные микросферы суспендировали в течение 3 ч в 1% водном растворе поливинилового спирта при концентрации 50 мг/мл с перемешиванием, используя магнитную мешалку, промывали дистиллированной водой и сушили сублимацией. Микросферы, полученные таким образом, имели средний размер частиц 23,4 мм, и количество поливинилового спирта, остающегося на поверхности микросфер, составляло 0,16% (мае./мае.).
ПРИМЕР ПОЛУЧЕНИЯ 7: Получение нагруженных лейпрорелином микросфер
0,5 г лейпрорелина ацетата и 9,5 г RG502H растворили в 95 мл ледяной уксусной кислоты. Раствор подавали в распылительную сушилку (SODEVA, Франция) со скоростью 3 мл/мин, распыляли в сухой камере, используя ультразвуковой распылитель (Sono-Tek, 60 кГц), и сушили сухим воздухом с температурой 200°С. Выделенные микросферы суспендировали в течение 3 ч в 1% водном растворе поливинилового спирта при концентрации 50 мг/мл с перемешиванием, используя магнитную мешалку, промывали дистиллированной водой и сушили сублимацией. Микросферы, полученные таким образом, имели средний размер частиц 32,6 мм, и количество поливинилового спирта, остающегося на поверхности микросфер, составляло 0,11% (мас./мас.).
ПРИМЕР ПОЛУЧЕНИЯ 8: Получение нагруженных лейпрорелином микросфер
1,4 г лейпрорелина ацетата и 0,86 г RG502H и 7,74 г R202H растворили в 86 мл ледяной уксусной кислоты. Раствор подавали в распылительную сушилку (SODEVA, Франция) со скоростью 3 мл/мин, распыляли в сухой камере, используя ультразвуковой распылитель (Sono-Tek, 120 кГц), и сушили сухим воздухом с температурой 200°С. Выделенные микросферы суспендировали в течение 90 мин в 1% водном растворе поливинилового спирта при концентрации 50 мг/мл с перемешиванием, используя магнитную мешалку, промывали дистиллированной водой и сушили сублимацией.
ПРИМЕР ПОЛУЧЕНИЯ 9: Получение нагруженных октреотидом микросфер
0,7 г октреотида ацетата и 9,3 г RG502H растворили в 186 мл ледяной уксусной кислоты. Раствор подавали в распылительную сушилку (SODEVA, Франция) со скоростью 3 мл/мин, распыляли в сухой камере, используя ультразвуковой распылитель (Sono-Tek, 120 кГц), и сушили сухим воздухом с температурой 200°С. Выделенные микросферы суспендировали в течение 1 ч в 1% водном растворе поливинилового спирта при концентрации 50 мг/мл с перемешиванием, используя магнитную мешалку, промывали дистиллированной водой и сушили сублимацией.
ТЕСТОВЫЙ ПРИМЕР 5
Нагруженные лейпрорелином микросферы, полученные в примере получения 8, суспендировали в суспензии (0,5% (мас./мас.) натрийкарбоксиметилцеллюлозы, 5% (мас./мас.) маннита, 0,1% Твина-80) и подкожно однократно вводили в дозе 9 мг/кг (лейпрорелина ацетат) самцам крыс линии 3D (n=5, 195±20 г). Пробы крови брали из вен хвоста перед введением лекарственного средства через 30 мин, 1 ч, 3 ч, 6 ч и 1, 2, 4 и 7 дней после введения лекарственного средства, а также каждые 7 дней в течение периода с 8 го по 90-й день. Крысам вводили проверочные дозы микросфер, 100 мг/кг (лейпрорелина ацетата), через 28, 56 и 84 дня после введения лекарственного средства, чтобы оценить длительное высвобождение лекарственного средства из микросфер. Пробы крови собирали перед введением лекарственного средства 3 и 24 ч после введения. Вторичное введение лекарственного средства было выполнено через 90 дней после первичного, и пробы крови брали так, как описано для первичного введения препарата. Собранные пробы крови помещали в пробирки Эппендорфа объемом 1,5 мл и центрифугировали в течение 10 минут при 4°С и 12000 об./мин. Полученную сыворотку хранили при -20°С. Уровень тестостерона в сыворотке измеряли с помощью набора для радиоиммуноанализа (RIA) (DSL-10-4000, Diagnostic System Laboratories, Inc, Вебстер, Техас, США). Результат представлены на фиг.2. Эти три проверочных введения, повторяемые каждые 28 дней после введения препарата, и повторное введение препарата спустя 90 дней после первого введения лекарственного средства привели к ингибированию повышения уровней тестостерона сыворотки. Данные результаты указывают, что лейпрорелин непрерывно высвобождался на протяжении тестового периода 90 дней.
ТЕСТОВЫЙ ПРИМЕР 6
Нагруженные октреотидом микросферы, полученные в примере получения 9, взвешенные в суспензии (0,5% (мас./мас.) натрийкарбоксиметилцеллюлоза, 0,6% (мас./мас.) маннит), подкожно однократно вводили в дозе 5 мг/кг (октреотида) крысам-самцам линии SD (n=6, 195±20 г). Пробы крови брали из вен хвоста перед введением лекарственного средства через 6 ч и 1, 4, 7, 13, 21 и 31 день после введения лекарственного средства. Собранные пробы крови помещали в пробирки Эппендорфа объемом 1,5 мл и центрифугировали в течение 10 мин при 4°C и 12000 об./мин. Полученную сыворотку хранили при -20°C. Концентрацию октреотида в сыворотке измеряли с помощью набора для иммуноферментного анализа (EIA) (Bachem, S-1275, Peninsula Laboratories Inc, США). Результаты изображены на фиг.3. Как показано на фиг.3, октреотид непрерывно высвобождался более 2 недель.
Промышленная применимость
Как описано выше, способ получения микросфер по настоящему изобретению позволяет получать микросферы с длительным высвобождением, лишенные проблем микросферы с длительным высвобождением, полученные обычными способами, в том числе токсичности, обусловленной остаточным растворителем, и плохой проходимости через иглу шприца. При введении в организм микросферы, полученные по настоящему изобретению, высвобождают эффективную концентрацию лекарственного средства постоянно в течение заданного периода, предотвращая быстрое начальное высвобождение лекарственного средства и снижая необходимую частоту введений лекарственного средства. Таким образом, настоящие микросферы применимы в лечении заболеваний.

Изобретение относится к способу получения микросфер с длительным высвобождением, содержащих поддающийся биологическому разложению полимер в качестве носителя и лекарственное средство, и к нагруженным лекарственным средством микросферам, полученным указанным способом. Способ предусматривает распыление в сухую камеру раствора, суспензии или эмульсии, содержащих поддающийся биологическому разложению полимер, лекарственное средство и растворитель, и сушку растворителя воздухом с получением высушенных распылением микросфер. Полученные микросферы диспергируют в водном растворе, содержащем поливиниловый спирт, чтобы удалить остаточный растворитель и улучшить дисперсность микросфер, и извлекают высушенные микросферы из водного раствора. Способ позволяет получать микросферы с высокой эффективностью инкапсуляции лекарственного средства без остаточного токсичного растворителя и улучшенной проходимостью через иглу шприца. 2 н. и 9 з.п. ф-лы, 3 ил, 5 табл.
1. Способ получения микросфер с длительным высвобождением, включающий распыление в сухую камеру раствора, суспензии или эмульсии, содержащих поддающийся биологическому разложению полимер, лекарственное средство и растворитель, и сушку растворителя с использованием сухого воздуха для того, чтобы получить высушенные распылением микросферы;
диспергирование указанных подвергнутых распылительной сушке микросфер в водном растворе, содержащем поливиниловый спирт, чтобы удалить остаточный растворитель и улучшить дисперсность микросфер; и
извлечение указанных высушенных распылением микросфер из водного раствора.
2. Способ получения микросфер с длительным высвобождением по п.1, где поддающийся биологическому разложению полимер представляет собой один и более, выбранный из группы, состоящей из полилактида, полигликолида, поли-(лактидкогликолида), полиортоэфира, полиангидрида, полигидроксимасляной кислоты, поликапролактона, полиалкилкарбоната и их производных.
3. Способ получения микросфер с длительным высвобождением по п.1, где лекарственное средство выбрано из пептида и белка.
4. Способ получения микросфер с длительным высвобождением по п.3, где лекарственное средство выбрано из производных рилизинг-гормона лютеинизирующего гормона (LHRH), производных соматостатина и их солей.
5. Способ получения микросфер с длительным высвобождением по п.4, где лекарственное средство выбрано из лейпрорелина, гозерелина, трипторелина, октреотида и их солей.
6. Способ получения микросфер с длительным высвобождением по п.1, где при диспергировании в водном растворе, содержащем поливиниловый спирт, поливиниловый спирт покрывает микросферы с длительным высвобождением в количестве от 0,02 до 1,0 мас.%.
7. Способ получения микросфер с длительным высвобождением по п.1, где при диспергировании в водном растворе, содержащем поливиниловый спирт, из микросфер с длительным высвобождением дополнительно удаляется более 20% остаточного растворителя.
8. Нагруженные лекарственным средством микросферы с длительным высвобождением, которые получены путем дробления на капли раствора, суспензии или эмульсии, содержащих поддающийся биологическому разложению полимер, лекарственное средство и растворитель; сушки распыленных капель для удаления растворителя и получения высушенных микросфер; диспергирования высушенных микросфер, содержащих поливиниловый спирт в водном растворе для нанесения поливинилового спирта, на микросферы в количестве от 0,02 до 1,0 мас.%.
9. Нагруженные лекарственным средством микросферы с длительным высвобождением по п.8, где лекарственное средство выбрано из пептида и белка.
10. Нагруженные лекарственным средством микросферы с длительным высвобождением по п.9, где лекарственное средство выбрано из производных рилизинг-гормона, лютеинизирующего гормона (LHRH), производных соматостатина и их солей.
11. Нагруженные лекарственным средством микросферы с длительным высвобождением по п.10, где лекарственное средство выбрано из лейпрорелина, гозерелина, трипторелина, октреотида и их солей.
| Прибор для очистки паром от сажи дымогарных трубок в паровозных котлах | 1913 |
|
SU95A1 |
| KR 20030081179 A, 17.10.2003 | |||
| WO 9503036 A1, 02.02.1995 | |||
| ERMIS D | |||
| Preparation of spray-dried microspheres of indomethacin and examination of the effects of coating on dissolution rates | |||
| Journal of Microencapsulation, vol.16, issue 3, 1999, реферат. | |||
Авторы
Даты
2010-11-10—Публикация
2007-05-11—Подача