ОБЛАСТЬ ТЕХНИКИ, К КОТОРОЙ ОТНОСИТСЯ ИЗОБРЕТЕНИЕ
Настоящее изобретение относится к области медицинской химии, особенно к новым производным камптотецина, которые обладают противоопухолевой активностью и являются растворимыми в воде, их применению и содержащим их фармацевтическим композициям.
УРОВЕНЬ ТЕХНИКИ
Камптотецин (далее здесь сокращенно обозначаемый СТР, J. Am. Chem. Soc, 1966, 88, 3888), который был экстрагирован и выделен впервые из camptotheca acuminata Wall et al., является алкалоидом пирроло[3,4-b]хинолином со структурой
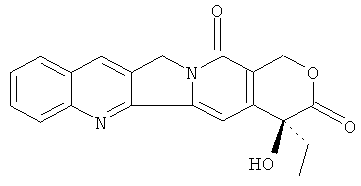
Он имеет пентациклическую структуру с хиральным центром S-типа в 20-положении кольца E и лактоновой структурой около хирального центра. Хотя камптотецин обладает некоторым терапевтическим действием на рак желудка, рак прямой кишки и тому подобное, его клиническое изучение ограничивается вследствие его низкой растворимости в воде и токсического побочного действия.
Интенсивное исследование было проведено по модификациям молекулярной структуры СРТ для получения производных СРТ с более высокой активностью и более низкой токсичностью. Согласно этому, было синтезировано большое число производных СРТ с хорошими результатами. Между тем, обнаружено, что противоопухолевую активность можно повысить введением подходящей группы в 9-положение 10-гидроксикамптотецина. Например, коммерчески доступный в настоящее время топотекан является таким соединением.
В отличие от обычных неорганических оснований и органических оснований, хотя производные СРТ являются алкалоидами, их соли имеют низкую растворимость в воде. В общем, имеется две применяемые схемы для разрешения проблемы растворимости. Одной схемой является введение водорастворимой группы, которую можно превратить в соль, такой как аминогруппа, в производные СРТ, и топотекан является таким примером. Другой схемой является введение предварительной водорастворимой группы, которая может диссоциировать in vivo с образованием производных СРТ, и иринотекан (соединение 4, СРТ-11), водорастворимое лекарственное производное СРТ, является таким примером.
Во время скрининга противоопухолевых лекарственных средств авторы настоящего изобретения неожиданно обнаружили, что соединения, полученные введением низшего алкила в 9-положение 10-гидроксикамптотецина (представляемого нижеследующей формулой II, где R1 представляет собой H, C1-C4алкил, разветвленный С1-C4алкил или С1-C4алкил, замещенный гидрокси и/или аминогруппой), обладают превосходной противоопухолевой активностью. Среди этих соединений некоторые обладают превосходным терапевтическим действием на ксенотрансплантаты солидных опухолей у имеющих опухоли голых мышей и более высокими терапевтическими индексами, что, таким образом, указывает на перспективу применения указанных соединений для дальнейшей разработки противоопухолевых лекарственных средств.
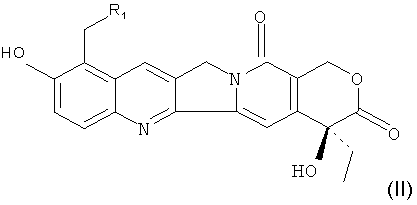
Однако соединения, представленные формулой II, имеют проблему низкой растворимости в воде.
ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Поэтому задачей настоящего изобретения является обеспечение новыми производными камптотецина с высокой противоопухолевой активностью и хорошей растворимостью в воде на основе соединений, представленных формулой II.
Другой задачей настоящего изобретения является обеспечение фармацевтическими композициями, содержащими указанные выше производные камптотецина.
Еще одной задачей настоящего изобретения является обеспечение применений указанных выше производных камптотецина для получения лекарственного средства для лечения опухоли.
Еще одной задачей настоящего изобретения является обеспечение применения указанных выше фармацевтических композиций для получения лекарственного средства для лечения опухоли.
Настоящее изобретение относится к соединениям со структурой, представленной нижеследующей формулой I, их изомерам, энантиомерам или фармацевтически приемлемым солям.
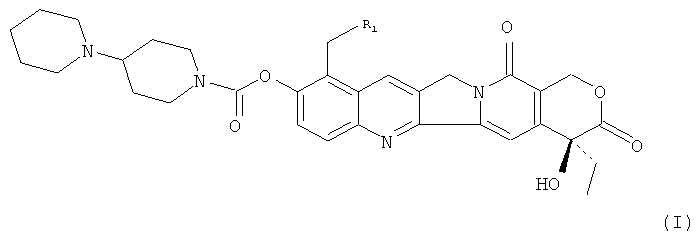
где R1 представляет собой H, C1-C4алкил, разветвленный C1-C4алкил, C1-C4алкил, замещенный гидрокси- и/или аминогруппой, или аллил. В частности, R1 может быть атомом водорода; метилом, этилом, пропилом, аллилом, бутилом и их возможными изомерами, например изопропилом, изобутилом; и гидроксиметилом, гидроксиэтилом, гидроксипропилом, аминометилом, аминоэтилом, аминопропилом и тому подобное.
Примерами указанных фармацевтически приемлемых солей являются соли, которые образованы основной аминогруппой пиперидильной группы, введенной у 10-гидроксигруппы, и фармацевтически приемлемой неорганической кислотой или органической кислотой, и эти соли могут придать лекарственным средствам растворимость в воде. В качестве примера неорганических или органических кислот могут быть хлористоводородная кислота, серная кислота, фосфорная кислота, уксусная кислота, трифторуксусная кислота или трифторметансульфоновая кислота.
Предпочтительными соединениями настоящего изобретения являются нижеследующие соединения:
10-((4'-Пиперидилпиперидин)карбонилокси)-9-метилкамптотецин;
10-((4'-пиперидилпиперидин)карбонилокси)-9-этилкамптотецин;
10-((4'-пиперидилпиперидин)карбонилокси)-9-пропилкамптотецин;
10-((4'-пиперидилпиперидин)карбонилокси)-9-аллилкамптотецин;
10-((4'-пиперидилпиперидин)карбонилокси)-9-изопропилкамптотецин;
10-((4'-пиперидилпиперидин)карбонилокси)-9-н-бутилкамптотецин;
10-((4'-пиперидилпиперидин)карбонилокси)-9-изобутилкамптотецин;
10-((4'-пиперидилпиперидин)карбонилокси)-9-гидроксиметилкамптотецин;
10-((4'-пиперидилпиперидин)карбонилокси)-9-гидроксиэтилкамптотецин или
10-((4'-пиперидилпиперидин)карбонилокси)-9-аминометилкамптотецин.
Соединения настоящего изобретения можно синтезировать таким же способом, как способ синтеза иринотекана, как описано в предшествующем уровне техники. Эти способы описаны во многих ссылках (например, Chem. Pharm. Bull, 1991, 39, 2574).
В нижеследующих двух схемах иллюстрируются определенные синтетические способы. На схеме 1 алкалоид пирроло[3,4-b]хинолин формулы 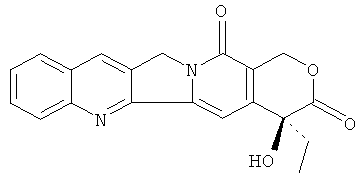
подвергают взаимодействию с фосгеном или твердым фосгеном с получением сначала ацилхлоридного соединения 6 и затем полученное ацилхлоридное соединение 6 подвергают взаимодействию с пиперидилпиперидином (соединение 7), получая при этом требуемый продукт.
Схема 1
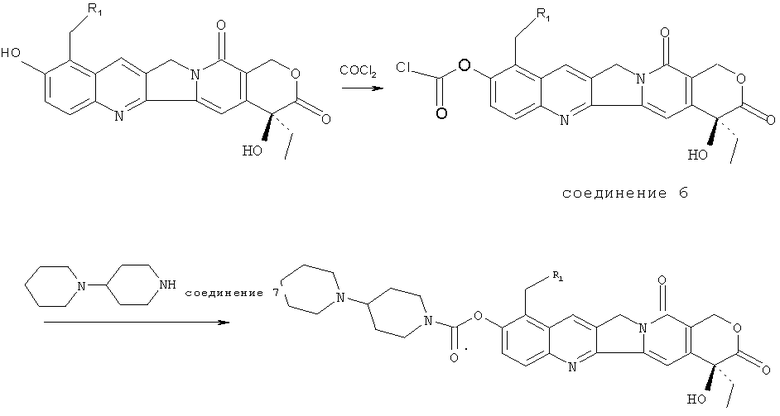
На схеме 2 пиперидилпиперидин подвергают взаимодействию с фосгеном или твердым фосгеном с получением сначала производного амида хлормуравьиной кислоты 8 и затем полученное производное амида хлормуравьиной кислоты 8 подвергают взаимодействию с алкалоидом пирроло[3,4-b]хинолином, указанным на схеме 7, получая при этом требуемый продукт.
Схема 2
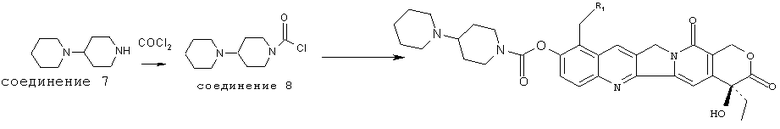
В обеих из указанных выше схем применяют обычные органические синтетические реакции. Что касается родственных документов по синтетической реакции, средний специалист может проводить эти реакции. Для краткости изложения подробное описание здесь не включено.
Фармацевтически приемлемые соли соединений настоящего изобретения можно получить общепринятыми способами. Для краткости изложения подробное описание здесь не включено. Можно получать водорастворимые соли согласно химическим свойствам соединений настоящего изобретения.
Настоящее изобретение относится также к фармацевтической композиции, включающей в себя терапевтически эффективное количество указанного выше соединения и общепринятый фармацевтический адъювант. «Эффективным количеством» является количество соединения, которое достаточно для улучшения патологического состояния и не вызывает тяжелые побочные действия. Безопасное и эффективное количество соединения зависит от определенных критериев, таких как возраст, масса тела, терапевтическое показание, путь введения, курс лечения, любая другая родственная терапия и тому подобное. Указанный фармацевтический адъювант включает в себя фармацевтически приемлемые носители, и термин «фармацевтически приемлемый носитель» означают одно или несколько совместимых твердых или жидких наполнителей или эксципиентов, которые являются подходящими для людей и должны быть достаточно чистыми и иметь достаточно низкую токсичность. «Совместимость» здесь означает, что каждый компонент композиции можно смешать с другим, при том что фармакодинамическое действие соединения несомненно не должно снизиться. Некоторыми примерами фармацевтически приемлемых носителей являются сахарид (такой как глюкоза, сахароза, лактоза и т.д.), крахмал (такой как кукурузный крахмал, картофельный крахмал и т.д.), целлюлоза и ее производные (такие как натриевая соль карбоксиметилцеллюлозы, натрийэтилцеллюлоза, ацетат целлюлозы, микрокристаллическая целлюлоза и т.д.), акриловые смолы, полиакрилат натрия, поливидон, полиэтиленгликоль, полиоксиэтиленмоностеарат, желатин, силикагель, тальк, стеариновая кислота, стеарат магния, сульфат кальция, растительное масло (такое как соевое масло, кунжутное масло, арахисовое масло, оливковое масло и т.д.). Может присутствовать также эмульгатор (такой как твин (Tween®)), смачивающий агент (такой как додецилсульфат натрия), пластификатор (такой как дибутилсебацинат), красящий агент, корригент (ароматизатор), стабилизатор, консервант, непирогенная вода и тому подобное. Выбор носителя, применяемого в композиции настоящего изобретения, зависит от способа введения соединения, и специалист в данной области может выбрать носитель, который является подходящим для определенного способа введения согласно известному уровню техники.
Настоящее изобретение относится также к лекарственным формам указанной выше фармацевтической композиции. Лекарственная форма может быть подходящей для перорального введения, внутривенной инъекции, внутримышечной инъекции и тому подобное, такой как порошок, таблетка, капсула и т.д.
Соединения настоящего изобретения обладают противоопухолевой активностью, поэтому соединения настоящего изобретения и содержащую такие соединения фармацевтическую композицию можно применять для получения лекарственных средств для лечения опухолей и дополнительного лечения опухолей и можно также применять в качестве интервенциональной терапии опухолей.
Соединения настоящего изобретения обладают высокой противоопухолевой активностью и хорошей растворимостью в воде. Эти соединения имеют превосходную перспективу в разработке лекарственного средства.
ОПИСАНИЕ ГРАФИЧЕСКИХ МАТЕРИАЛОВ
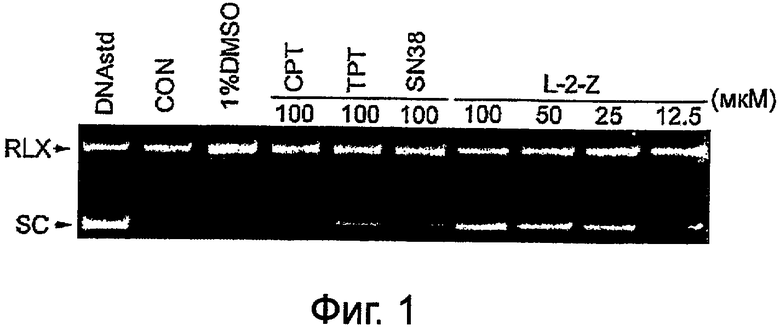
На фиг.1 показано, что активный метаболит СРТ-4 ингибирует TOPO I-опосредуемую релаксацию сильнозакрученной pBR322.
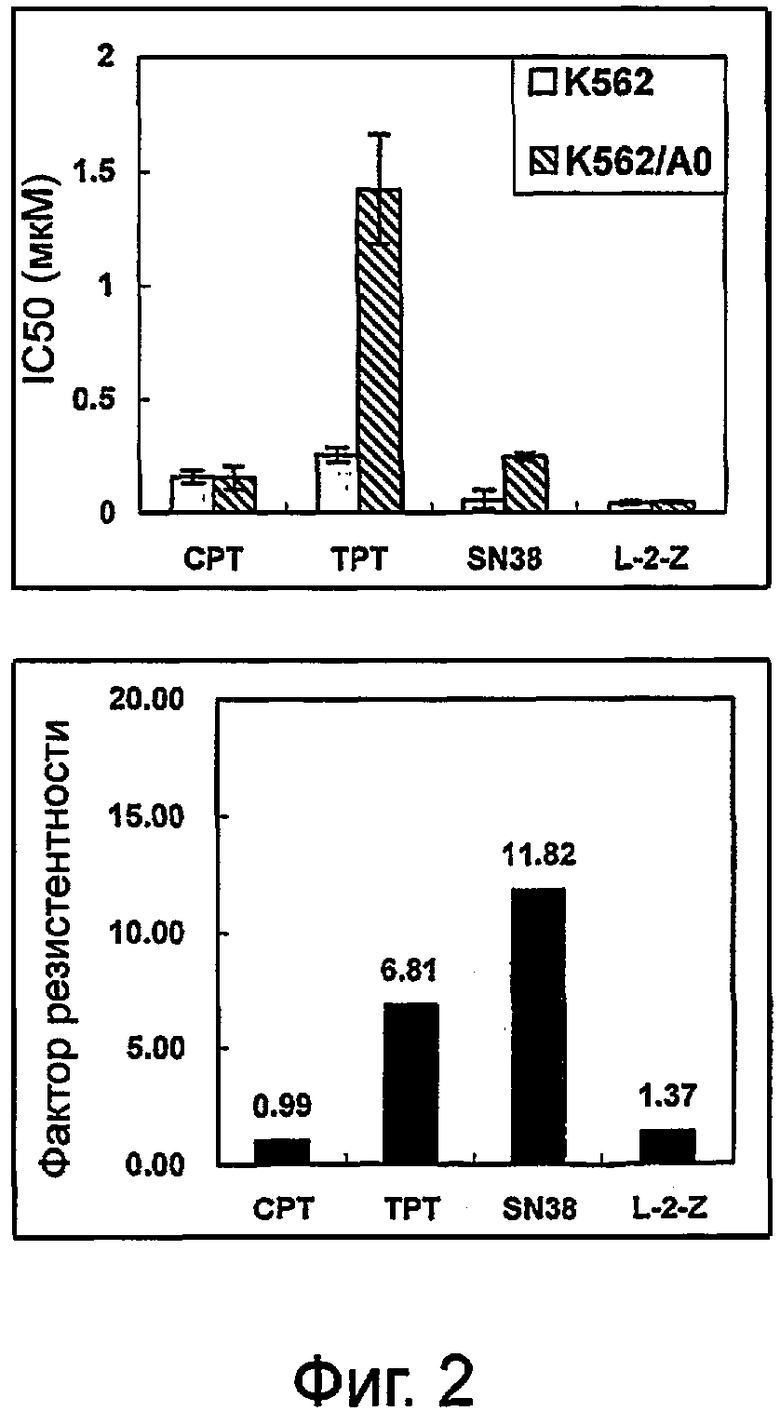
На фиг.2 показана антирезистентность (anti-multidrug resistance) активного метаболита СРТ-4.
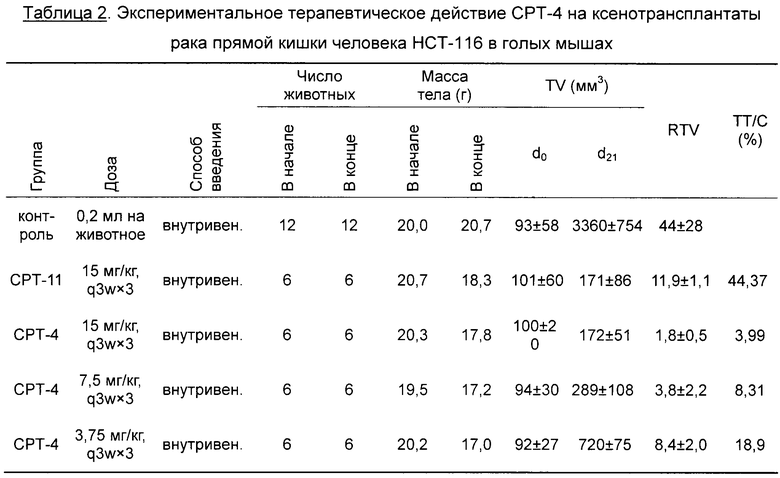
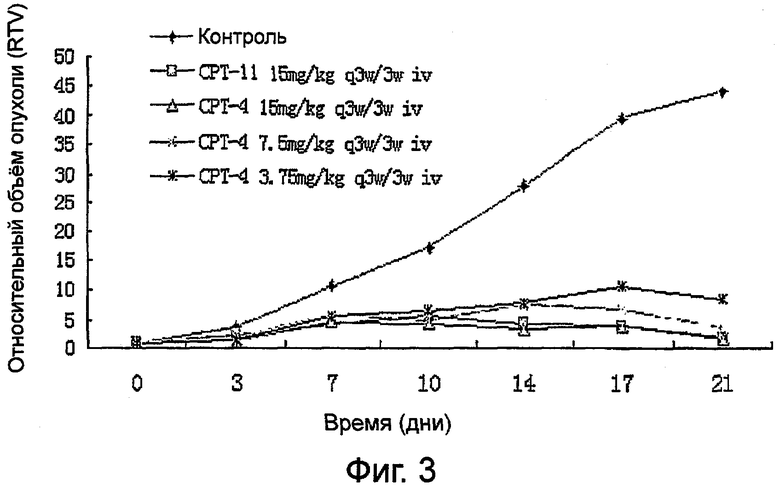
На фиг.3 показано экспериментальное терапевтическое действие СРТ-4 на ксенотрансплантаты рака прямой кишки человека НСТ-116 у голых мышей.
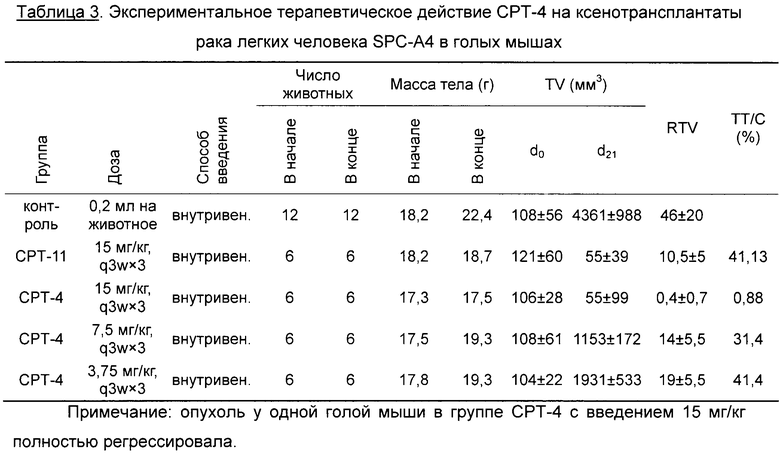
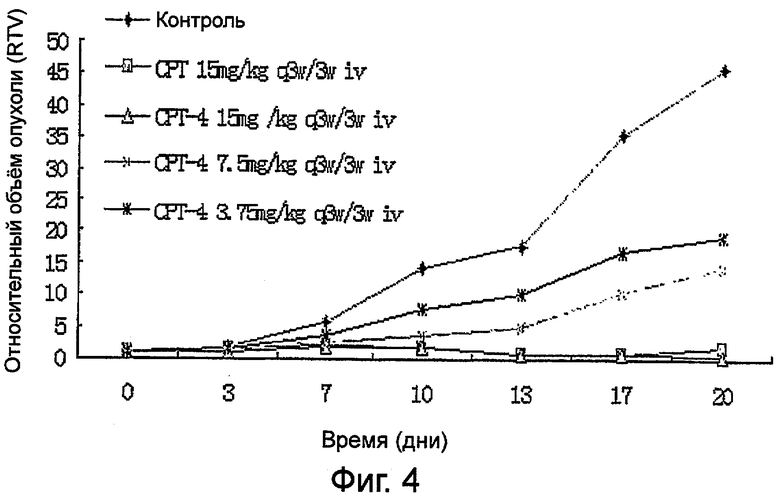
На фиг.4 показано экспериментальное терапевтическое действие СРТ-4 на ксенотрансплантаты рака легких человека SPC-A4 у голых мышей.
ВАРИАНТ ОСУЩЕСТВЛЕНИЯ ИЗОБРЕТЕНИЯ
ПРИМЕРЫ ПОЛУЧЕНИЙ
Пример получения 1
Получение 10-((4'-пиперидилпиперидин)карбонилокси)-9-аллилкамптотецина (СРТ-4)
Один грамм (1,25 массового эквивалента) амида
пиперидилпиперидинхлормуравьиной кислоты (соединение 8) растворяют в 70 мл дихлорметана, 10-гидрокси-9-аллилкамптотецин (1 г, 1 массовый эквивалент) растворяют в 70 мл безводного пиридина и затем указанный выше раствор в дихлорметане добавляют в раствор в безводном пиридине в условиях охлаждения. После завершения реакции растворитель выпаривают при пониженном давлении. Остаток подвергают колоночной хроматографии на силикагеле и получают 1,25 г СРТ-4 в виде желтого твердого вещества. 1H ЯМР (ДМСО-d6) (м.д.): 1,01 (3Н, т), 1,58~1,90 (10Н, м), 1,80~1,99 (2Н, м), 2,89 (4Н, ушир.), 3,09 (1Н, ушир.), 3,71 (2Н, д), 4,45 (2Н, дд), 4,94 (1Н, дд), 5,11 (1Н, дд), 5,14 (2Н, с), 5,15 (1Н, д), 5,66 (1Н, д), 6,00 (1Н, м), 7,47 (1Н, д), 7,65 (1Н, с), 8,11 (1Н, д), 8,51 (1Н, с).
Пример получения 2
Получение 10-((4'-пиперидилпиперидин)карбонилокси)-9-этилкамптотецина (СРТ-2)
В нулевой точке пять граммов (1,25 массового эквивалента) амида пиперидилпиперидинхлормуравьиной кислоты (соединение 8) растворяют в 70 мл дихлорметана, 10-гидрокси-9-этилкамптотецин (1 г, 1 массовый эквивалент) растворяют в 70 мл безводного пиридина и указанный выше раствор в дихлорметане добавляют в раствор в безводном пиридине в условиях охлаждения. После завершения реакции растворитель выпаривают при пониженном давлении. Остаток подвергают колоночной хроматографии на силикагеле и получают 1,24 г СРТ-2 в виде желтого твердого вещества. 1Н ЯМР (ДМСО-d6) (м.д.): 1,01 (3Н, т), 1,20 (3Н, т), 1,58~1,90 (2Н, м), 1,80~1,99 (2Н, м), 2,89 (4Н, ушир.), 3,09 (1Н, ушир.), 3,21 (2Н, кв), 4,45 (2Н, дд), 5,14 (2Н, с), 5,15 (1Н, д), 5,66 (1Н, д), 6,00 (1Н, м), 7,47 (1Н, д), 7,65 (1Н, с), 8,11 (1Н, д), 8,67 (1Н, с).
Пример получения 3
Получение 10-((4'-пиперидилпиперидин)карбонилокси)-9-пропилкамптотецина (СРТ-3)
Один грамм (1,25 массового эквивалента) амида пиперидилпиперидинхлормуравьиной кислоты (соединение 8) растворяют в 70 мл дихлорметана, 10-гидрокси-9-пропилкамптотецин (1 г, 1 массовый эквивалент) растворяют в 70 мл безводного пиридина и указанный выше раствор в дихлорметане добавляют в раствор в безводном пиридине в условиях охлаждения. После завершения реакции растворитель выпаривают при пониженном давлении. Остаток подвергают колоночной хроматографии на силикагеле и получают 1,17 г СРТ-3 в виде желтого твердого вещества. 1Н ЯМР (ДМСО-d6) (м.д.): 1,01 (3Н, т), 1,12 (3Н, т), 1,59 (2Н, м), 1,82~1,90 (2Н, м), 1,80~1,99 (2Н, м), 2,89 (4Н, ушир.), 3,09, 3,22 (2Н, т), (1Н, ушир.), 4,45 (2Н, дд), 5,14 (2Н, с), 5,15 (1Н, д), 5,66 (1Н, д), 6,00 (1Н, м), 7,47 (1Н, д), 7,65 (1Н, с), 8,11 (1Н, д), 8,51 (1Н, с).
ЭКСПЕРИМЕНТАЛЬНЫЕ ПРИМЕРЫ
Нижеследующие фармакологические испытания проводили с применением полученного выше соединения СРТ-4 настоящего изобретения.
Экспериментальный пример 1
Ингибирование иона ТОРО I в системе без клеток
Анализы релаксации TOPO I-опосредуемой сильнозакрученной pBR322 применяли для испытания влияния активного метаболита СРТ-4 на ферментативную активность ТОРО I. В такой системе без клеток (фиг.1, в которой RLX означает релаксированную ДНК; SC означает сильнозакрученную ДНК), активный метаболит СРТ-4 может ингибировать TOPO I-опосредуемую релаксацию сильнозакрученной ДНК. Ингибирующее действие активного метаболита СРТ-4 было сильнее, чем СРТ. ТРТ (топотекан) и SN38 (активный метаболит иринотекана) присутствуют в одинаковых концентрациях.
Экспериментальный пример 2
Противоопухолевая активность in vitro
1. Анализы с крашением белка сульфонилродамином В (SRB) применяли для обнаружения ингибирования пролиферации опухолевых клеток соединением. Результаты показали, что активный метаболит СРТ-4 может эффективно ингибировать пролиферацию опухолевых клеток при низких концентрациях (таблица 1). Его средняя величина IC50 (115,2 нМ) для тринадцати опухолевых клеточных линий была ниже, чем такие величины контрольных соединений ТРТ (378,6 нМ), SN38 (218,5 нМ) и 9-нитрокамптотецина (9-NC) (167,0 нМ). Между тем соединение проявляет селективность для опухолевых клеточных линий, происходящих из разных тканей. Клеточные линии рака легких, рака прямой кишки и рака молочной железы были чувствительными к активному метаболиту СРТ-4, и клеточные линии рака печени, рака желудка и рака яичников были менее чувствительными (результаты показаны в таблице 1).
2. Резистентную ко многим лекарственным средствам клеточную линию К562/А02 и ее родительскую клеточную линию К562 применяли для оценки антирезистентности активного метаболита СРТ-4. IC50 адриамицина в отношении клеток К562 и К562/А01 были 0,493 и 69,141 мкМ, соответственно, и фактор резистентности (RF) был 140,24. Результаты показали, что активный метаболит СРТ-4 обладает эквивалентными токсичностями для обеих клеточных линий, и показали очевидный эффект антирезистентности в отношении резистентных ко многим лекарственным средствам клеточных линий, и такой эффект был сильнее, чем эффект ТРТ и SN38 (результаты показаны на фигуре 2, где (А) означает IC50 для MDR клеточной линии К62/А01 и ее родительской клеточной линии К562; (В) означает фактор резистентности).
Экспериментальный пример 3
Противоопухолевая активность in vivo
Клетки рака прямой кишки человека НСТ-116 или клетки рака легких человека SPC-A4 инокулировали в подмышечные ямки голых мышей. Когда объем опухолей достигал 100~200 мм3, голых мышей произвольным образом расселяли по отдельным клеткам и три раза в неделю им внутривенно вводили СРТ-4 при различных концентрациях или нормальный физиологический раствор. Результаты показали, что соединение может значительно ингибировать рост ксенотрансплантатов опухолей и действие было эквивалентно действию СРТ-11 (водорастворимое лекарственное средство СРТ, иринотекан). Результаты показаны в таблице 2 и таблице 3.
| название | год | авторы | номер документа |
|---|---|---|---|
| КАРБОЦИКЛИЧЕСКИЕ АНАЛОГИ 20(S)-КАМПТОТЕЦИНА, СПОСОБЫ ИХ ПОЛУЧЕНИЯ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, СПОСОБ ЛЕЧЕНИЯ | 1997 |
|
RU2200163C2 |
| ЗАМЕЩЕННЫЕ БЕНЗ/А/АКРИДИНЫ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, ТЕРАПЕВТИЧЕСКИЙ СПОСОБ ИНГИБИРОВАНИЯ РОСТА РАКОВЫХ КЛЕТОК | 1997 |
|
RU2174116C2 |
| ПРОИЗВОДНЫЕ КАМПТОТЕЦИНА, ОБЛАДАЮЩИЕ ПРОТИВООПУХОЛЕВОЙ АКТИВНОСТЬЮ | 2012 |
|
RU2561118C2 |
| ПРОИЗВОДНЫЕ КАМПТОТЕЦИНА С ПРОТИВООПУХОЛЕВОЙ АКТИВНОСТЬЮ | 2007 |
|
RU2441009C2 |
| СОЕДИНЕНИЯ ДЛЯ ЛЕЧЕНИЯ РАКА | 2010 |
|
RU2581367C2 |
| МАКРОЦИКЛИЧЕСКОЕ СОЕДИНЕНИЕ И ЕГО ПРИМЕНЕНИЯ | 2018 |
|
RU2783238C2 |
| РАСТВОРИМЫЕ В ВОДЕ ФОСФОНООКСИМЕТИЛОВЫЕ ЭФИРЫ ЗАТРУДНЕННЫХ СПИРТОВ ИЛИ ФЕНОЛОВ, ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ НА ИХ ОСНОВЕ, СПОСОБ АНЕСТЕЗИИ И СПОСОБ ЛЕЧЕНИЯ ОПУХОЛЕВЫХ ЗАБОЛЕВАНИЙ | 1999 |
|
RU2235727C2 |
| ПРИМЕНЕНИЕ ПРОИЗВОДНЫХ ФТАЛИДА | 2005 |
|
RU2394569C2 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ОСНОВЕ ПРОИЗВОДНОГО ТРИИНДОЛИЛМЕТАНА В КАЧЕСТВЕ ПРОТИВООПУХОЛЕВОГО СРЕДСТВА | 2012 |
|
RU2549430C2 |
| КОМБИНИРОВАННАЯ КОМПОЗИЦИЯ ДЛЯ ПРЕДУПРЕЖДЕНИЯ ИЛИ ЛЕЧЕНИЯ РАКА, СОДЕРЖАЩАЯ ПРОИЗВОДНЫЕ БЕНЗОФЕНОНТИАЗОЛА В КАЧЕСТВЕ VDA И ИНГИБИТОР ТОПОИЗОМЕРАЗЫ | 2017 |
|
RU2724341C1 |
Изобретение относится к новым производным капмтотецина с нижеследующей структурой формулы (I)
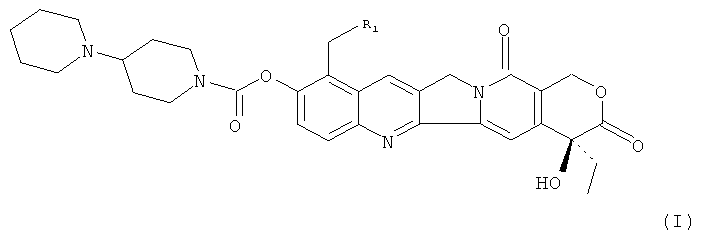 где R1 представляет собой Н, С1-С4алкил, разветвленный С1-С4алкил или винил, а также к фармацевтической композиции, обладающей противоопухолевой активностью, на основе данных соединений и к их применению для получения лекарственного средства для лечения опухолевых заболеваний. Технический результат: получены и описаны новые соединения, которые обладают высокими противоопухолевыми активностями и имеют хорошую растворимость в воде, их можно применять для разработки лекарственных средств. 4 н. и 3 з.п. ф-лы, 3 табл., 4 ил.
где R1 представляет собой Н, С1-С4алкил, разветвленный С1-С4алкил или винил, а также к фармацевтической композиции, обладающей противоопухолевой активностью, на основе данных соединений и к их применению для получения лекарственного средства для лечения опухолевых заболеваний. Технический результат: получены и описаны новые соединения, которые обладают высокими противоопухолевыми активностями и имеют хорошую растворимость в воде, их можно применять для разработки лекарственных средств. 4 н. и 3 з.п. ф-лы, 3 табл., 4 ил.
1. Соединение, представленное нижеследующей общей формулой I, или его фармацевтически приемлемая соль:

где R1 представляет собой Н, С1-С4алкил, разветвленный С1-С4алкил или винил.
2. Соединение или его фармацевтически приемлемая соль по п.1, где указанное соединение выбрано из группы, состоящей из следующих соединений:
10-((4'-пиперидилпиперидин)карбонилокси)-9-метилкамптотецина;
10-((4'-пиперидилпиперидин)карбонилокси)-9-этилкамптотецина;
10-((4'-пиперидилпиперидин)карбонилокси)-9-пропилкамптотецина;
10-((4'-пиперидилпиперидин)карбонилокси)-9-аллилкамптотецина;
10-((4'-пиперидилпиперидин)карбонилокси)-9-изопропилкамптотецина;
10-((4'-пиперидилпиперидин)карбонилокси)-9-н-бутилкамптотецина;
10-((4'-пиперидилпиперидин)карбонилокси)-9-изобутилкамптотецина.
3. Соединение или его фармацевтически приемлемая соль по п.1 или 2, где указанной фармацевтически приемлемой солью является соль, которую получают взаимодействием указанного соединения с соляной кислотой, серной кислотой, фосфорной кислотой, уксусной кислотой, трифторуксусной кислотой или трифторметансульфоновой кислотой.
4. Фармацевтическая композиция, обладающая противоопухолевой активностью, содержащая терапевтически эффективное количество соединения или его фармацевтически приемлемой соли по п.1 и общепринятый фармацевтический адъювант.
5. Фармацевтическая композиция по п.4, где указанную фармацевтическую композицию получают в лекарственной форме для перорального или инъекционного введения.
6. Применение соединения или его фармацевтически приемлемой соли по п.1 для получения лекарственного средства для лечения опухолевых заболеваний.
7. Применение фармацевтических композиций по п.4 для получения лекарственного средства для лечения опухолевых заболеваний.
| US 4604463 А, 05.08.1986 | |||
| CN 1616460 А, 18.05.2005 | |||
| CN 1083817 А, 16.03.1994 | |||
| US 5674872 А, 07.10.1997 | |||
| CN 1704416 А, 07.12.2005 | |||
| RU 98117449 A, 10.09.2000. |
Авторы
Даты
2011-02-10—Публикация
2007-01-17—Подача