ОБЛАСТЬ ТЕХНИКИ, К КОТОРОЙ ОТНОСИТСЯ ИЗОБРЕТЕНИЕ
Настоящее изобретение относится к композиции, содержащей Arthrospira, и применению композиции в качестве биоцида и/или терапевтического средства.
УРОВЕНЬ ТЕХНИКИ
Arthrospira (известная ранее как Spirulina) представляет собой цианобактерию, которая выращивается преимущественно для использования в качестве пищи и/или источника белка. Кроме того, описаны терапевтические применения Arthrospira, включая использование в качестве противовирусного средства, противоракового средства, средства, понижающего холестерин, антидиабетического средства, антигипертензивного средства и иммуномодулятора. Смотри, например, ссылки, помещенные на интернет-сайте Spirulina Source.com, http://www.spirulinasource.com/library.html.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Целью настоящего изобретения является композиция Arthrospira для применения в качестве биоцида и/или терапевтического средства.
Подвергнутая физиологическому стрессу Arthrospira обладает биоцидной активностью
Авторы настоящего изобретения обнаружили, что при физиологическом стрессе Arthrospira вырабатывает по меньшей мере один тип биоактивного вещества, которое активно в отношении грибков, бактерий и, предположительно, вирусов. Arthrospira можно подвергать физиологическому стрессу, например, лишая организм питательных веществ или света, или посредством обезвоживания/высушивания организма. Признаком того, что филамент Arthrospira (трихом) находится в состоянии «физиологического стресса», является его вхождение в состояние анабиоза, в этом состоянии филамент скручивается, и образуется толстая слизистая оболочка. Филамент и/или толстая слизистая оболочка, как предполагают авторы настоящего изобретения, содержит одно или более биоактивных веществ, защищающих организм от хищников. Одно или несколько биоактивных веществ могут разрушать клеточную стенку или внешний скелет организма хищника. Одно или несколько биоактивных веществ могут представлять собой, например, расщепляющие и модифицирующие вещества, такие как хитиназа, хитозаназа и хитин-дезацетилаза, которые расщепляют хитин, производное хитина (такое как хитозан) или другие полимеры клеточной стенки, содержащие, например, N-ацетилглюкозамин или D-глюкозамин в качестве субъединиц полимера. Одним из таких полимеров является пептидогликан грамположительных бактерий, состоящий из N-ацетилглюкозамина и N-ацетилмурамовой кислоты.
Согласно первому аспекту, настоящее изобретение относится к композиции для расщепления или модификации хитина, производного хитина или полимера, содержащего N-ацетил-D-глюкозамин в качестве субъединицы полимера, где указанная композиция содержит подвергнутую физиологическому стрессу Arthrospira.
Согласно второму аспекту, настоящее изобретение относится к способу расщепления или модификации хитина, производного хитина или полимера, содержащего N-ацетил-D-глюкозамин в качестве субъединицы полимера, где указанный способ включает стадию контактирования хитина, производного хитина или полимера, содержащего N-ацетил-D-глюкозамин в качестве субъединицы полимера, с композицией, содержащей подвергнутую физиологическому стрессу Arthrospira.
Хитин, производное хитина или полимер могут находиться в любой подходящей форме. Хитин, производное хитина или полимер могут находиться в по существу очищенном виде или могут быть частями организма, такими как клеточная стенка грибка или грамположительных бактерий, или частью внешнего скелета насекомого.
Согласно третьему аспекту, настоящее изобретение относится к способу идентификации биоактивного вещества из Arthrospira, где указанный способ включает стадии:
(I) объединения композиции, содержащей подвергнутую физиологическому стрессу Arthrospira, с по меньшей мере одним тестируемым субстратом, модифицируемым биоактивным веществом из Arthrospira; и
(II) анализ модификации тестируемого субстрата.
Может быть использован любой подходящий тип тестируемого субстрата. Анализ модификации тестируемого субстрата может проводиться любым подходящим способом. Тем не менее, предпочтителен крупномасштабный скрининг.
Предпочтительно, биоактивным веществом является хитинaза, хитозаназа или хитин-дезацетилаза, а тестируемым субстратом является хитин, производное хитина или полимер, содержащий N-ацетил-D-глюкозамин в качестве субъединицы полимера. Предпочтительно, для анализа модификации (то есть деградации) хитина, производного хитина или другого полимера применяется респирометрия.
Способ может дополнительно включать стадию очистки биоактивного вещества. Очистка может проводиться любым подходящим способом. Способ может также включать стадии клонирования и экспрессии гена/генов биоактивного вещества. Эти стадии могут проводиться любым подходящим способом. Например, стадии могут представлять собой стадии, описанные в Maniatis et al., Molecular Cloning: A Laboratory Manual, Cold Spring Harbor Laboratory, 1982, приведенной здесь в качестве перекрестной ссылки в полном объеме.
Применение подвергнутой физиологическому стрессу Arthrospira в качестве биоцида и/или терапевтического средства
Хитин, производное хитина и полимеры, содержащие глюкозамин, обнаруживаются повсеместно в природе, обычно в виде компонента клеточной стенки или внешнего скелета, например, водорослей, грибов, простейших, инфузорий, кишечнополостных, мшанок, моллюсков, кольчатых червей, членистоногих, жаброногих, форонид, погонофор и бактерий (грамположительных бактерий и Rhizobia).
Поэтому подвергнутая физиологическому стрессу Arthrospira, обладающая расщепляющей или модифицирующей активностями по отношению к хитину, производным хитина и полимерам, содержащим глюкозамин, потенциально может быть использована в качестве биоцида против широкого круга организмов. Используемый здесь термин «биоцид» относится либо к уничтожению организма, либо к ингибированию роста или репликации организма (то есть в действительности организм может не быть убитым). Следует принять во внимание, что некоторые применения биоцида будут иметь терапевтическое назначение.
Согласно четвертому аспекту, настоящее изобретение относится к композиции для применения в качестве биоцида и/или терапевтического средства, где указанная композиция содержит эффективное количество подвергнутой физиологическому стрессу Arthrospira.
Согласно пятому аспекту, настоящее изобретение относится к способу профилактики или лечения инфекции или заражения субъекта организмом, где указанный способ включает стадии введения субъекту эффективного количества композиции, содержащей подвергнутую физиологическому стрессу Arthrospira.
Предпочтительно, способ включает стадию выявления субъекта, нуждающегося в таком лечении или нуждающегося в такой профилактике.
Предусмотрено также использование подвергнутой физиологическому стрессу Arthrospira при изготовлении лекарственного средства для профилактики или лечения инфекции или заражения субъекта организмом.
Неожиданно авторами настоящего изобретения было обнаружено, что изъятие Arthrospira из ее среды роста может быть достаточным для наступления физиологического стресса и для индукции экспрессии одного или более биоактивных веществ, обладающих биоцидной активностью. То есть для наличия у Arthrospira биоцидной активности нет необходимости ни в проведении стадий вызывания у нее физиологического стресса, как указано в описаниях к патентам Новой Зеландии № 336620 и № 336619, ни в дальнейшей ее обработке (разрушением, взрывной декомпрессией, потенциированием, измельчением, повторным замачиванием в бикарбонате натрия или высушиванием замораживанием).
Более того, было обнаружено, что все коммерчески доступные препараты (таблетки, капсулы и порошки) Arthrospira, которые до сих пор были тестированы авторами настоящего изобретения, обладали активностью по отношению к субстрату, и что такая активность, по мнению авторов, свидетельствует о биоцидной активности. Такие препараты изготавливают, как правило, путем сбора Arthrospira, промывания и высушивания Arthrospira, минуя стадию специфического стрессового воздействия на организм. Фактически, коммерческие производители Arthrospira стремятся максимально уменьшить стрессовое воздействие на организм, поскольку толстая слизистая оболочка имеет свойство засорять оборудование по переработке организма.
Для любой одной или нескольких из описанных в данной работе композиций Arthrospira может быть любого подходящего вида, или смесью видов или вариантов Arthrospira, включая, но без ограничения, A. maxima. Следует отметить, что Arthrospira и Spirulina являются двумя различными родами. Различия между этими двумя родами неоднократно подтверждались на основании многих признаков, таких как спиральность и размер трихома, структура клеточной стенки и строение поры, содержание вакуолей, структура тилакоидов, подвижность и фрагментация трихомов, GC-состав, олигонуклеотидный каталог 16S рРНК и мутации в локусе cpcB-cpcA. Смотри, например, J.F. Manen and J. Falquet (2002) «The cpcB-cpcA locus as a tool for the genetic characterization of the genus Arthrospira (Cyanobacteria): evidence for horizontal transfer». International Journal of Systematic and Evolutionary Microbiology, Vol. 52, 861-867; и Chapter 1: Morphology, Ultrastructure and Taxonomy of Arthrospira (Spirulina) Maxima and Arthrospira (Spirulina) Platensis by Luisa Tomaselli, of Spirulina platensis (Arthrospira): Physiology, Cell-biology and Biotechnology. Taylor and Francis. Avigad Vonshak (Ed) 1997. Композиции, представленные в этих описаниях, не включают виды рода Spirulina.
Композиция может содержать неповрежденные филаменты Arthrospira, сегменты филаментов, разорванные/разрушенные сегменты или их экстракты/фракции. Композиция может включать как живую, так и неживую Arthrospira. Предпочтительно, чтобы композиция включала разрушенные филаменты и сегменты Arthrospira.
Композиция на основе Arthrospira может быть изготовлена любым подходящим способом, при котором сохраняется биоцидная активность. В норме, он мог бы включать стадии: (I) выращивания Arthrospira любым подходящим способом; (II) сбора выращенной Arthrospira любым подходящим способом; и (III) высушивания Arthrospira любым подходящим способом. Дополнительные стадии включают подвергание Arthrospira физиологическому стрессу любым подходящим способом, разрушение филаментов и сегментов любым подходящим способом, стерилизация организма любым подходящим способом, обесцвечивание Arthrospira любым подходящим способом, удаление или разрушение хлорофилла любым подходящим способом и измельчение высушенной Arthrospira.
Некоторые из вышеприведенных стадий описаны, например, в описаниях патентов Новой Зеландии № 336620 и 336619, полные содержания которых приведены здесь в качестве перекрестной ссылки. Например, стресс может вызываться во время сбора биомассы либо лишая Arthrospira необходимых питательных веществ (уменьшая количество питательных веществ) или света на время, достаточное для стресса, но не гибели, либо создавая условия роста. Вызвать стресс можно также при частичном высушивании или при сборе Arthrospira и выдерживании ее во влажных условиях живой до вызывания стресса, но не гибели. Например, для образования мелкодисперсного порошка разрушенных клеток Arthrospira может быть высушена распылением. Высушивание распылением может проводиться, например, при 50-190°С в течение нескольких секунд. Например, высушивание может проводится любым подходящим способом, включая вихревое высушивание, высушивание при помощи теплового насоса, высушивание в нагретых трубах, рефракторное высушивание или высушивание при температуре около 67°С в течение короткого промежутка времени. Например, филаменты могут быть разрушены измельчением или взрывной декомпрессией, как описано в патентах Новой Зеландии № 328013 и № 328740, полное содержание которых приведено здесь в качестве перекрестной ссылки.
Концентрация Arthrospira в композиции может меняться в зависимости от задач, то есть быть любой в интервале от 0,01% до 100%. Композиция может включать любой подходящий растворитель, носитель, основу, формообразующее, наполнитель, связующее вещество, пластификатор, эмульгатор, стабилизатор, смазку, буферный агент, смягчитель, вещество, усиливающее растворимость, суспендирующее вещество, загуститель, отдушку, краситель и консервант.
В зависимости от предназначения, композиция может быть дополнена одним или несколькими активными веществами, полученными не из Arthrospira, такими как противомикробные средства (например, бактерицид или фунгицид), терапевтические средства (например, средства для заживления ран, стероиды) или обычные питательные вещества (например, аминокислоты, витамины). Такие активные вещества хорошо известны в данной области.
Композиция может быть в любой подходящей форме. Композиция может вводиться или применяться любым подходящим способом. Композиция может быть жидкой, гелеобразной или твердой, или смесью таковых. Композиция может быть жидкой культурой Arthrospira, которая применяется в виде аэрозоля. Альтернативно, композиция может быть порошком, который равномерно распределяется по поверхности обрабатываемого участка при помощи приспособления для встряхивания или распыления. Инфицированный или зараженный субъект может быть помещен в ванну, содержащую жидкую форму композиции. Композиция и способ применения или введения могут быть такими, как изложено в описаниях патентов Новой Зеландии № 336620 и № 336619.
Для терапевтических целей композиция может вводиться или применяться, например, перорально, парентерально, в виде спрея для ингаляции, местно, ректально, через нос, трансбуккально или вагинально. Композиция может быть в виде таблетки, раствора, аэрозоля, спрея, крема, мази, примочки, эмульсии, геля или порошка. Композиция может быть в форме наполненного Arthrospira бандажа, одежды, клейкого пластыря, суппозитория, пессария или примочки.
Предпочтительно, биоцид активен в отношении грибов, грамположительных бактерий, простейших, вирусов, ракообразных, клещей и насекомых, некоторые из этих случаев более подробно рассмотрены ниже.
Согласно шестому аспекту, настоящее изобретение относится к способу получения композиции на основе Arthrospira для применения в качестве биоцида и/или терапевтического средства, где указанный способ включает стадии:
(1) подвергания Arthrospira физиологическому стрессу; и
(2) объединения подвергнутой стрессу Arthrospira по п.(1) с подходящими носителем, растворителем, основой или наполнителем.
Согласно седьмому аспекту, настоящее изобретение относится к способу получения композиции на основе Arthrospira для применения в качестве биоцида и/или лекарственного средства, где указанный способ включает в себя стадии:
(1) вызывания физиологического стресса у Arthrospira путем удаления, приблизительно, до 80% жидкости, в которой Arthrospira выращивается;
(2) промывки подвергнутой стрессу Arthrospira в целях удаления загрязнений;
(3) высушивания промытой Arthrospira; и
(4) объединения промытой Arthrospira с подходящими носителем, растворителем, основой или наполнителем.
Любой из вышеизложенных способов может быть использован для приготовления одной или нескольких из описанных здесь композиций.
Предпочтительно, описанные выше способы исключают специфические стадии взрывной декомпрессии и/или высушивания при замораживании подвергнутой физиологическому стрессу Arthrospira перед добавлением носителя, раствора, основы или наполнителя.
Применение подвергнутой физиологическому стрессу Arthrospira в качестве противогрибкового средства
Согласно восьмому аспекту, настоящее изобретение относится к композиции для применения в качестве противогрибкового средства, где указанная композиция содержит эффективное количество подвергнутой физиологическому стрессу Arthrospira.
Согласно девятому аспекту, настоящее изобретение относится к способу профилактики или лечения грибковой инфекции или заражения субъекта, где указанный способ включает стадию введения субъекту эффективного количества композиции, содержащей подвергнутую физиологическому стрессу Arthrospira.
Предпочтительно, способ включает стадию выявления субъекта, нуждающегося в таком лечении или нуждающегося в такой профилактике.
Предусмотрено также использование подвергнутой физиологическому стрессу Arthrospira при изготовлении лекарственного средства для профилактики или лечения грибковой инфекции или заражения субъекта.
Подвергнутая физиологическому стрессу Arthrospira может быть использована для обработки по меньшей мере следующих типов грибов: Zygomycotina; Ascomycotina; Fungi Imperfecti, Malassezia; Microsporum; Trichophyton и Epidermophyton.
В первом варианте осуществления, субъектом является человек или животное, такое как млекопитающее или позвоночное. В случае, когда субъектом является человек, композиция может применяться для лечения:
- дерматомикоза (например, ступни спортсменов, паховая эпидермофития, стригущий лишай, глубокая инфекция ногтевого ложа), который вызывается, главным образом, родами Microsporum, Trichophyton, Candida и Epidermophyton;
- молочницы, вызываемой Candida;
- перхоти, вызываемой Malassezia;
- тропической мицетомы - гранулярное распространяющееся образование в коже, мышечной ткани и лимфатических узлах, вызываемое Madurella;
- споротрихоза - гранулярное распространяющееся образование в коже и лимфатических узлах, вызываемое Sporothrix schenkii; и
- гистоплазмоза - хроническая пневмония с распространенной системной инфекцией, вызываемая Histoplasma capsulatum.
В случае, когда субъектом является животное, композиция может применяться для лечения, например, стригущего лишая, инфекции копыт (Candida, Malassezia), дерматитов и фолликулитов (Microsporum, Trichophyton, Alternaria, Fusarium). Местные грибковые заболевания у животных обычно вызываются теми же грибками, что и у людей.
Во втором варианте осуществления, субъектом является сельскохозяйственный или садоводческий продукт, как например, растение, цветок, фрукт, овощ, злак, зерно, боб, грибной мицеллий, пастбище или газон. Композиция может быть использована для обработки, например, гнилей метелки и корневой шейки (Fusarium), экземы поверхности (Pithomyces Chartarum), серой гнили (Botrytis cineria), пятен на листьях (Septoria, Alteria, Bipolaris), настоящей мучнистой росы (Sphaerotheca macularis, Erysiphe, Sphaerotheca pannosa), бурой гнили (Monilinia fruiticola) и ржавчины листьев и стеблей (Puccinia).
В третьем варианте осуществления, субъектом является почва, лесоматериал, строительный материал или здание. Композиция может применяться, например, для обработки плесени внутри или снаружи зданий и для обработки грибковых пятен на древесине строительных материалов и столбов линий электропередач.
Неожиданно авторы настоящего изобретения обнаружили, что подвергнутая физиологическому стрессу Arthrospira синергетически взаимодействует с известными противогрибковыми веществами (фунгистатическими веществами), что обеспечивает более широкий спектр противогрибковой активности. Авторы обнаружили, что подвергнутая стрессу Arthrospira может ингибировать рост грибков, уничтожать грибки и препятствовать повторному росту грибков.
Согласно десятому аспекту, настоящее изобретение относится к противогрибковой композиции, содержащей синергическую комбинацию подвергнутой физиологическому стрессу Arthrospira с по меньшей мере одним фунгистатическим веществом.
Согласно одиннадцатому аспекту, настоящее изобретение относится к способу профилактики или лечения грибковой инфекции или заражения субъекта, где указанный способ включает стадию введения субъекту эффективного количества композиции, содержащей синергическую комбинацию подвергнутой физиологическому стрессу Arthrospira с по меньшей мере одним фунгистатическим веществом.
Предпочтительно, способ включает стадию выявления субъекта, нуждающегося в таком лечении или нуждающегося в такой профилактике.
Предусмотрено также использование подвергнутой физиологическому стрессу Arthrospira в комбинации с по меньшей мере одним фунгистатическим веществом при изготовлении лекарственного средства для профилактики или лечения грибковой инфекции или заражения субъекта.
Может быть использовано любое подходящее фунгистатическое вещество (известное вещество), такое как тербинафин, бифоназол, клотримазол, миконазол, эконазол, кетоконазол или толнафтат. В зависимости от предполагаемого применения композиции может быть использована любая подходящая концентрация известного вещества.
Применение подвергнутой физиологическому стрессу Arthrospira в качестве антибактериального средства
Авторами настоящего изобретения было обнаружено, что подвергнутая физиологическому стрессу Arthrospira является эффективным антибактериальным средством против грамположительных бактерий. Характер антибактериального действия не вполне понятен. Возможно, клеточные стенки грамположительных бактерии разрушаются или иным образом модифицируются при воздействии одного или более биоактивных веществ Arthrospira. Клеточные стенки содержат пептидогликан (состоящий из N-ацетилглюкозамина и N-ацетилмурамовой кислоты) и пептидогликан, возможно, расщепляется одним или несколькими биоактивными веществами.
Согласно двенадцатому аспекту, настоящее изобретение относится к композиции для применения в качестве антибактериального средства, где указанная композиция содержит эффективное количество подвергнутой физиологическому стрессу Arthrospira.
Согласно тринадцатому аспекту, настоящее изобретение относится к способу профилактики или лечения бактериальной инфекции или заражения субъекта, где указанный способ включает стадию введения субъекту эффективного количества композиции, содержащей подвергнутую физиологическому стрессу Arthrospira.
Предпочтительно, способ включает стадию выявления субъекта, нуждающегося в таком лечении или нуждающегося в такой профилактике.
Предусмотрено также использование подвергнутой физиологическому стрессу Arthrospira при изготовлении лекарственного средства для профилактики или лечения бактериальной инфекции или заражения субъекта.
Предпочтительно, бактерии относятся к грамположительным бактериям и могут представлять собой, например, Bacilli, Clostridia, Staphylococci или Pneumococci. Бактерии, предпочтительно, являются Propionibacterium acne, которые вызывают угри.
В первом варианте осуществления, субъектом является человек или животное, такое как млекопитающее или позвоночное. В случае, когда субъектом является человек, композиция может быть применена для обработки угрей, дерматитов, язв или ран, вызванных или инфицированных грамположительными бактериями. Композиция может быть применена для обработки внутренних инфекций, например, дыхательных путей, полости рта, пищеварительного и мочеполового тракта (например, стрептококковые инфекции глотки, среднего уха).
Во втором варианте осуществления, субъектом является сельскохозяйственный или садоводческий продукт, такой как растение, цветок, фрукт, овощ, злак, зерно, боб или грибной мицеллий.
В третьем варианте осуществления, субъектом является, например, загрязненное искусственное сооружение или водопроток, в котором могут расти бактерии.
Применение подвергнутой физиологическому стрессу Arthrospira в качестве пестицида
Согласно четырнадцатому аспекту, настоящее изобретение относится к композиции для применения в качестве пестицида, где указанная композиция содержит эффективное количество подвергнутой физиологическому стрессу Arthrospira.
Согласно пятнадцатому аспекту, настоящее изобретение относится к способу подавления или устранения вредителей, где указанный способ включает введение или употребление эффективного количества композиции, содержащей подвергнутую физиологическому стрессу Arthrospira.
Пестицид может быть применен против вредителей, таких как ракообразные и клещи. Пестицид может быть применен против насекомых, таких как мухи (напр. Simulidae - черные мухи), осы, москиты и термиты. Пестицид может быть применен для прекращения распространения паразитов, например тех, которые вызывают малярию и другие заболевания, переносимые насекомыми.
В первом варианте осуществления, композиция может быть определена как средство, отпугивающее насекомых, или приманка.
Во втором варианте осуществления, композиция может применяться для сельскохозяйственного или садоводческого продукта, такого как растение, цветок, фрукт, овощ, злак, зерно, боб или грибной мицеллий.
В третьем варианте осуществления, композиция может применяться, например, для загрязненного искусственного сооружения, здания, строительного материала, реки, озера или заболоченного участка.
Применение Arthrospira в качестве терапевтического средства
Авторы настоящего изобретения обнаружили, что при использовании подвергнутой физиологическому стрессу Arthrospira в качестве биоцида и/или лекарственного средства для обработки кожи один или несколько других заменителей Arthrospira синергически взаимодействуют с одним или несколькими биоактивными веществами, что способствует излечиванию кожи. Данные другие заменители, как предполагают, включают бета-каротин, который обеспечивает питание кожи; фикоцианин, который оказывает противовоспалительное действие; другие белки; и другие питательные вещества, включая витамины, минералы, микроэлементы, антиоксиданты, незаменимые масла и углеводороды.
Сначала подвергнутая стрессу Arthrospira ингибирует или уничтожает микробы будь то грибы, бактерии или вирусы, а затем другие заменители Arthrospira восстанавливают повреждение, вызванное микробом.
Авторы настоящего изобретения обнаружили, что даже не подвергнутая физиологическому стрессу Arthrospira обладает терапевтическими свойствами, например, при лечении заболеваний кожи и при восстановлении кожи.
Согласно шестнадцатому аспекту, настоящее изобретение относится к композиции для восстановления или профилактики дефектов кожи млекопитающего, где указанная композиция содержит эффективное количество Arthrospira.
Предпочтительно, композиция включает подвергнутую физиологическому стрессу Arthrospira.
Согласно семнадцатому аспекту, настоящее изобретение относится к способу заживления или профилактики повреждения кожи млекопитающего, где указанный способ включает применение эффективного количества композиции, содержащей Arthrospira.
Предпочтительно, композиция содержит подвергнутую физиологическому стрессу Arthrospira.
Предпочтительно, способ включает стадию выявления млекопитающего, нуждающегося в таком лечении или нуждающегося в такой профилактике.
Предусмотрено также использование Arthrospira, предпочтительно подвергнутой физиологическому стрессу, при изготовлении лекарственного средства для заживления или профилактики дефекта кожи у млекопитающего.
Согласно шестнадцатому и семнадцатому аспектам изобретения, композиция может иметь одну или более составных частей или свойств, как описано для композиций согласно другим аспектам изобретения, которые были определены.
Согласно шестнадцатому и семнадцатому аспектам изобретения, композиция предпочтительно получается любым из описанных выше способов.
Дефектом кожи может быть, например, оспина, угревое повреждение, красные угри, покрасневшее пятно, трещина, ожог, волдырь, псориаз, экзема, шелушение, морщина, папула, стоматит, ссадина, пустула, рана, себорейный дерматит, опрелость, язва, герпес, высыпание после бритья, ветряная оспа, дерматит, трещины на пятках и локтях. Композиция может применяться для лечения ожогов, укусов насекомых и животных и для устранения раздражения кожи. Композиция может применяться для ослабления зуда на коже. Композиция может применяться для заживления рубцовой ткани, солнечных ожогов и сухой и шелушащейся кожи, потерявшей свою эластичность.
Другие аспекты и варианты осуществления изобретения станут очевидными из последующего подробного описания.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
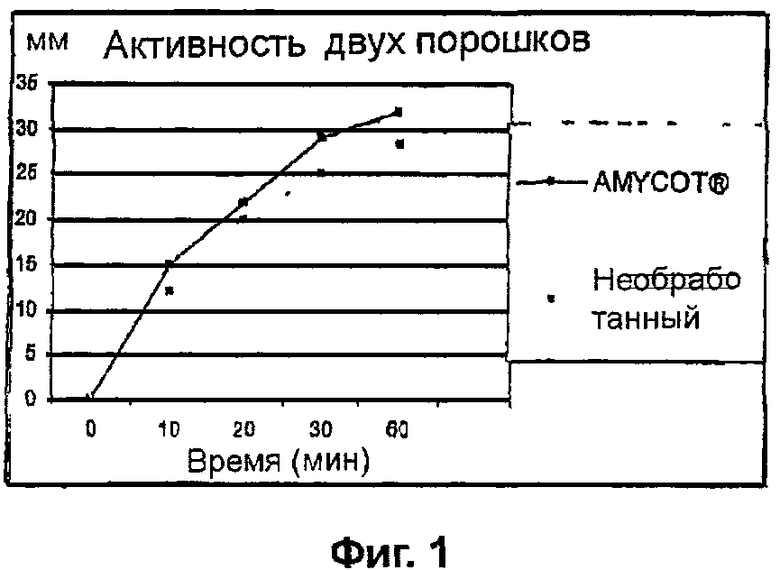
На фиг. 1 показана активность подвергнутой физиологическому стрессу Arthrospira (AMYCOT® и необработанный порошок) по отношению к хитину на основании данных респирометрии;
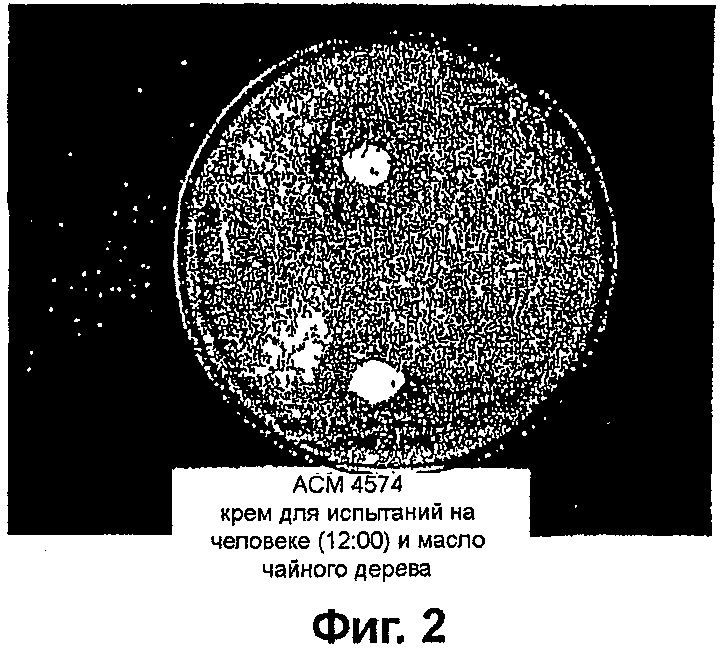
На фиг. 2 показана противогрибковая активность AMYCOT® по отношению к C. albicans;
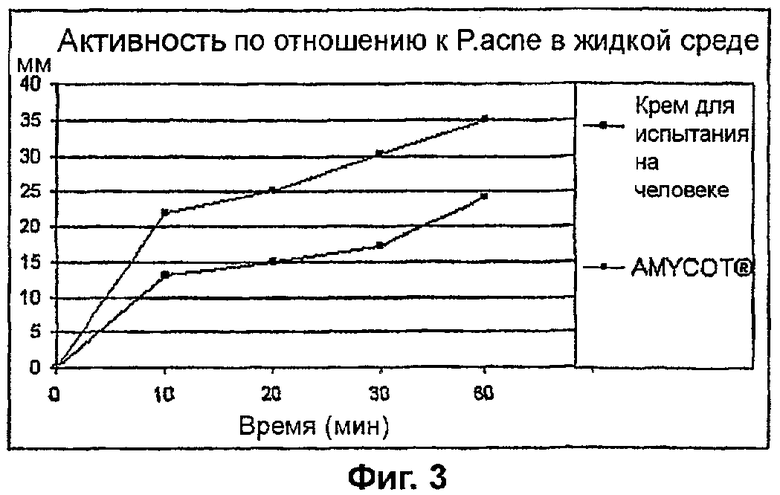
На фиг. 3 показана антибактериальная активность AMYCOT® по отношению к P. acne на основании данных респирометрии;
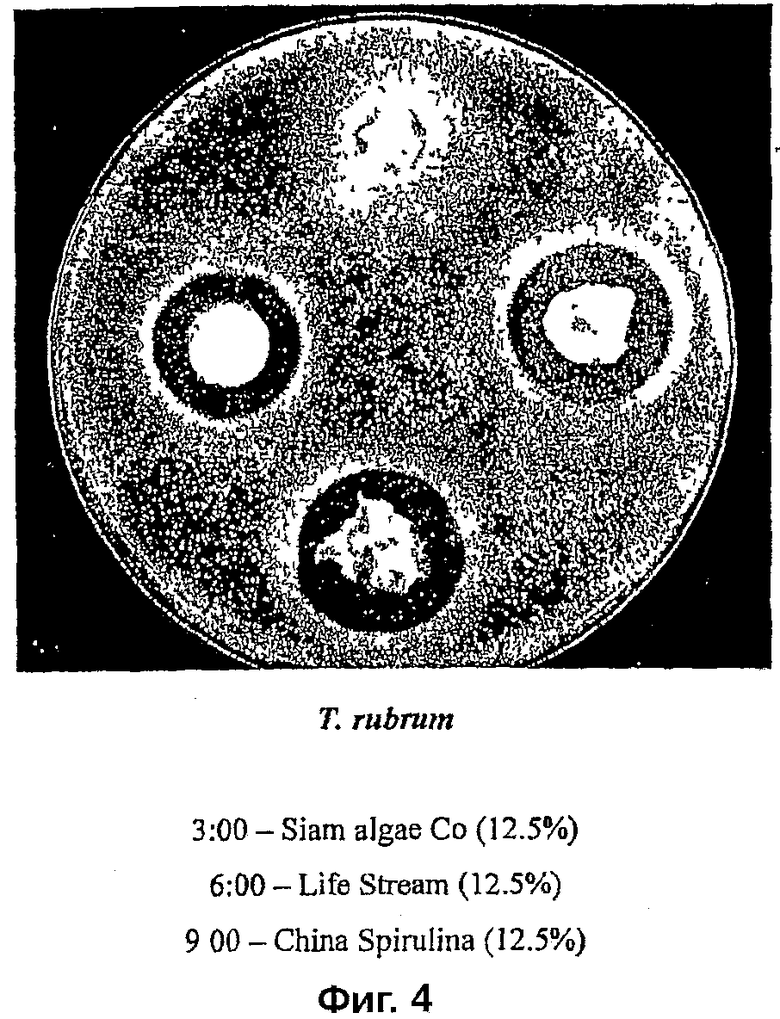
На фиг. 4 показана противогрибковая активность различных коммерческих препаратов Arthrospira (Spirulina) по отношению к T. rubrum;
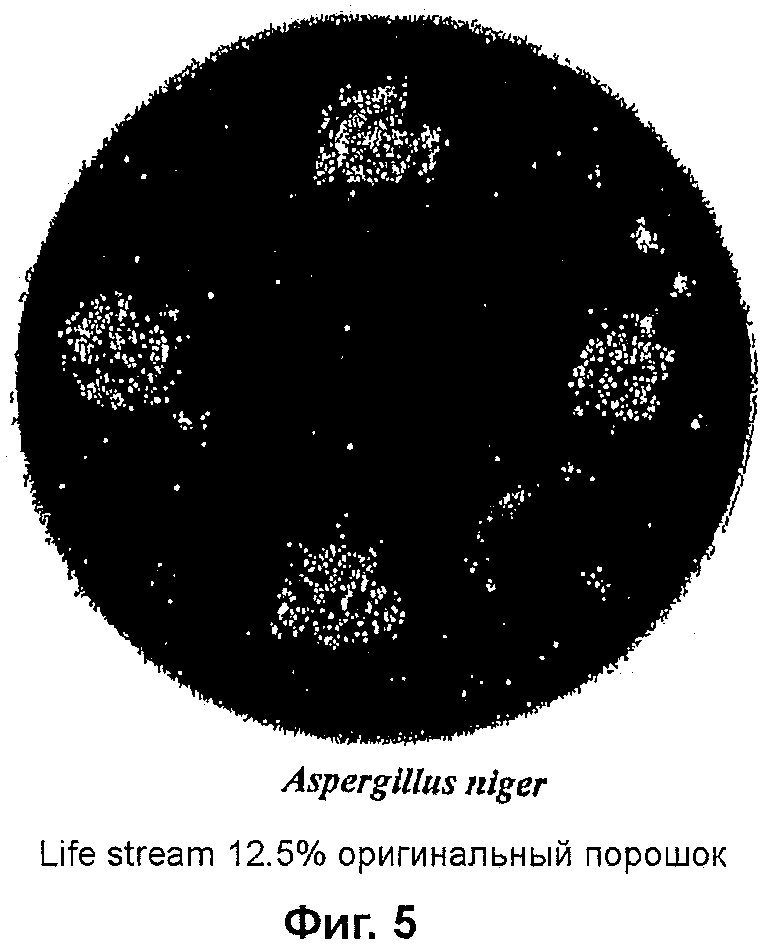
На фиг. 5 показана противогрибковая активность коммерческого препарата (Life Stream) Arthrospira по отношению к A. niger;
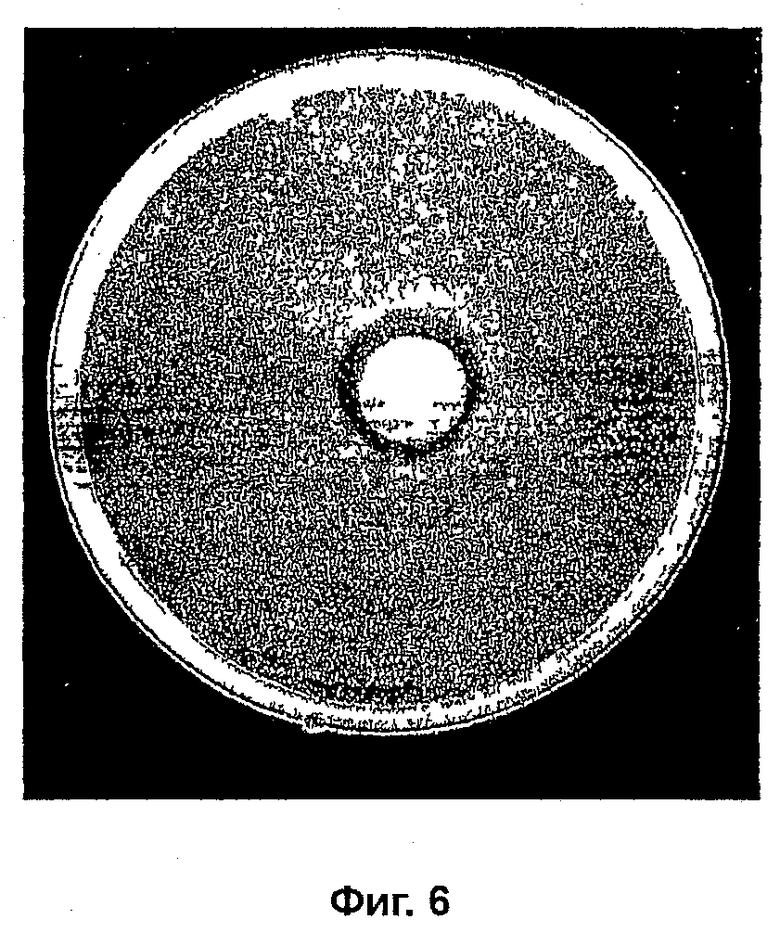
На фиг. 6 показана противогрибковая активность AMYCOT® по отношению к M. canis;
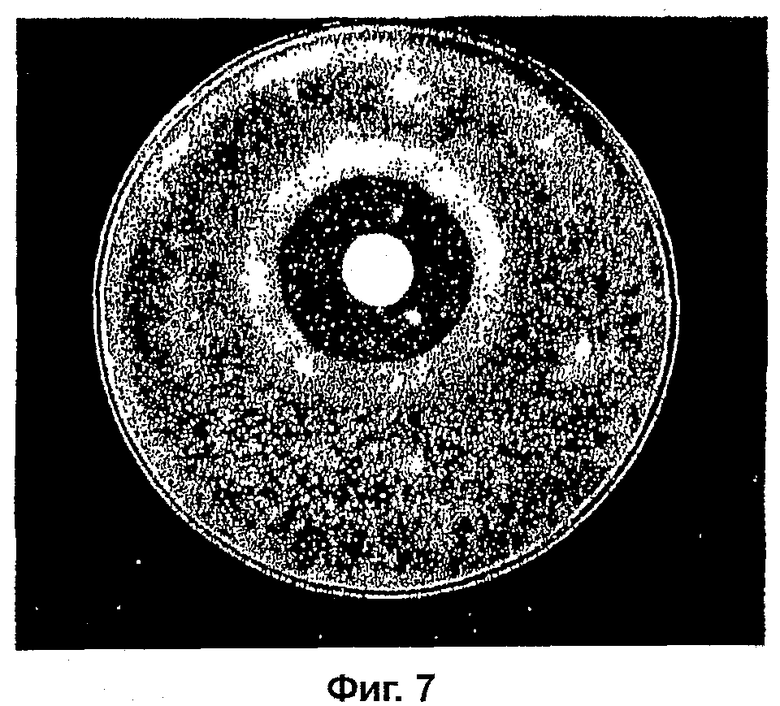
На фиг. 7 показана противогрибковая активность of AMYCOT® по отношению к F. grаminearum;
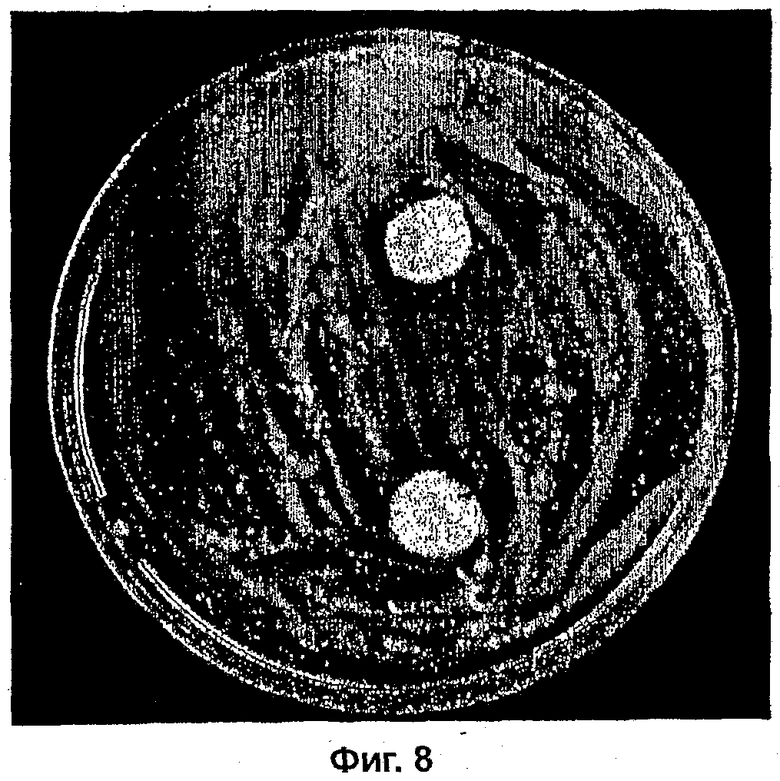
На фиг. 8 показана противогрибковая активность AMYCOT® по отношению к M. furfur;
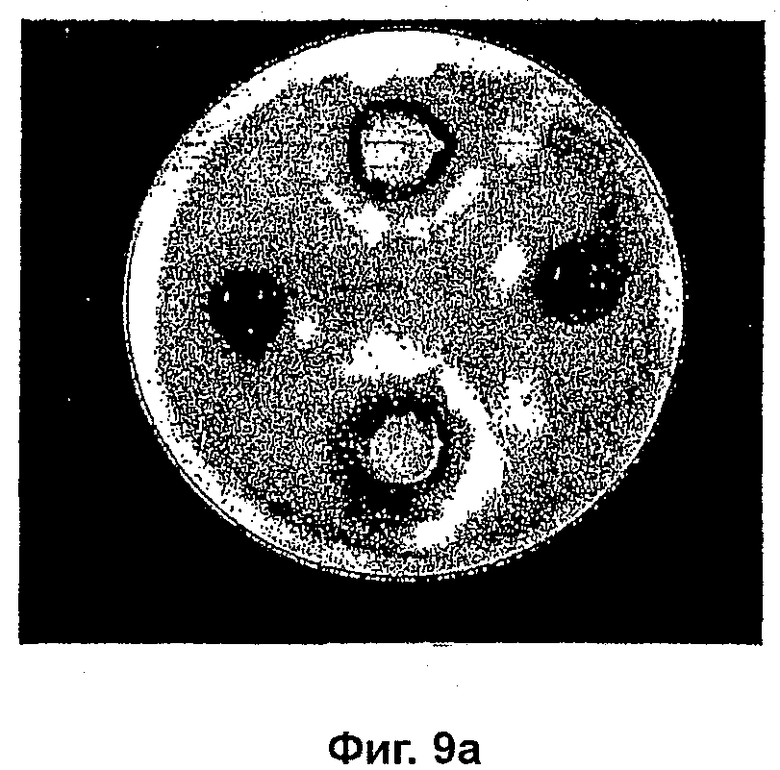
На фиг. 9a показана противогрибковая активность шампуня AMYCOT® по отношению к T. rubrum;
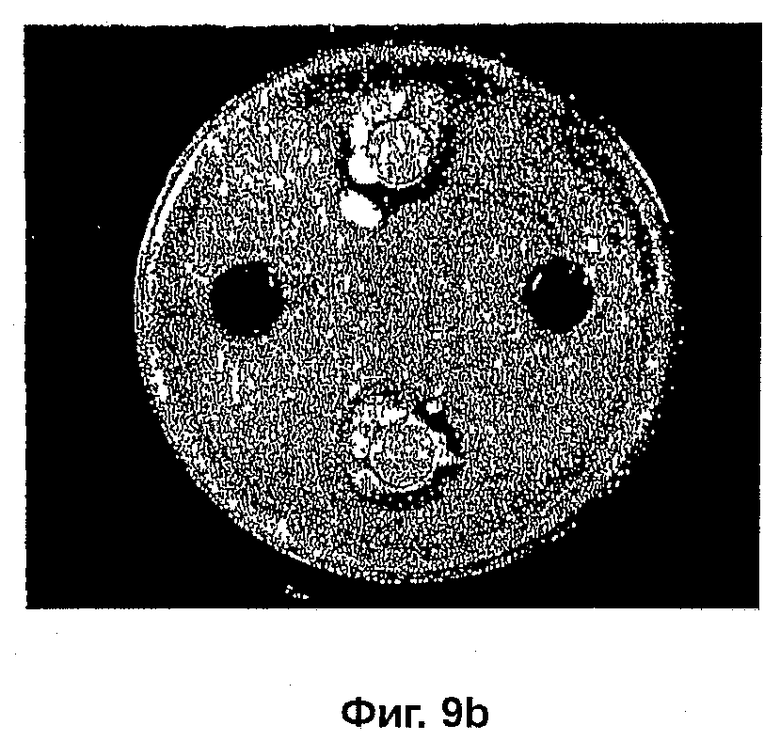
На фиг. 9b показана противогрибковая активность шампуня AMYCOT® по отношению к C. albicans;
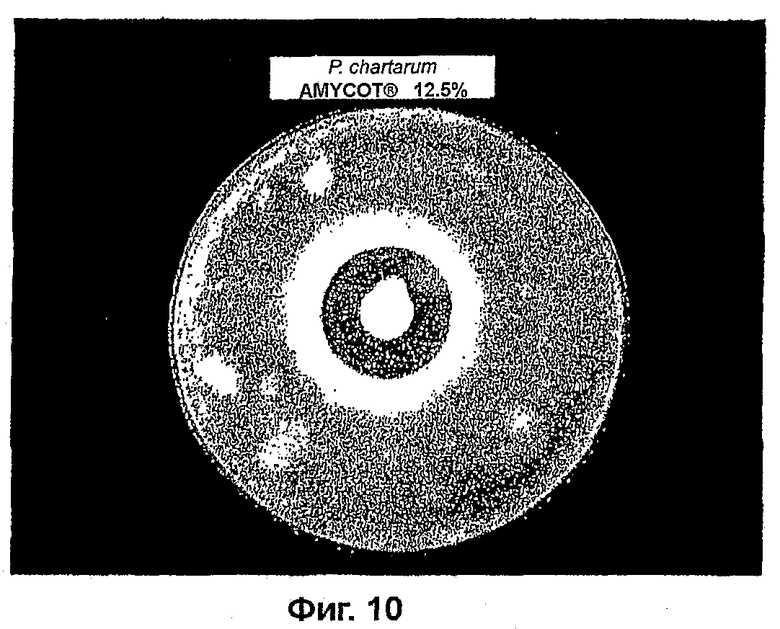
На фиг. 10 показана противогрибковая активность AMYCOT® по отношению к P. chartarum;
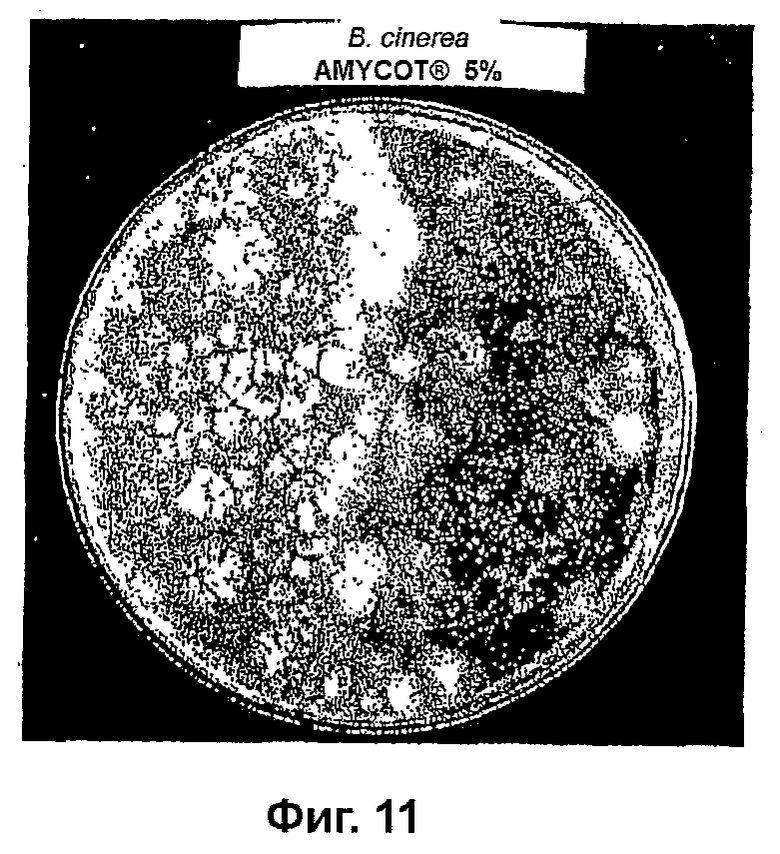
На фиг. 11 показана противогрибковая активность AMYCOT® по отношению к B. cinerea;
На фиг. 12 представлены данные ингибирования T. rubrum при помощи AMYCOT® и различных известных противогрибковых веществ;
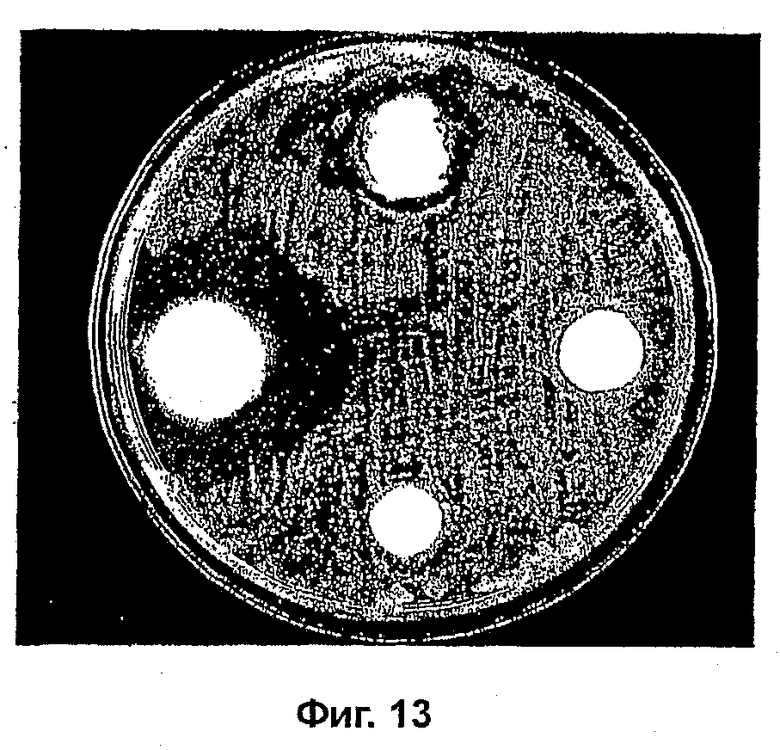
На фиг. 13 представлены данные ингибирования T. mentagrophytes при помощи AMYCOT® и различных известных веществ;
На фиг. 14 представлены данные ингибирования C. albicans при помощи AMYCOT® и различных известных веществ;
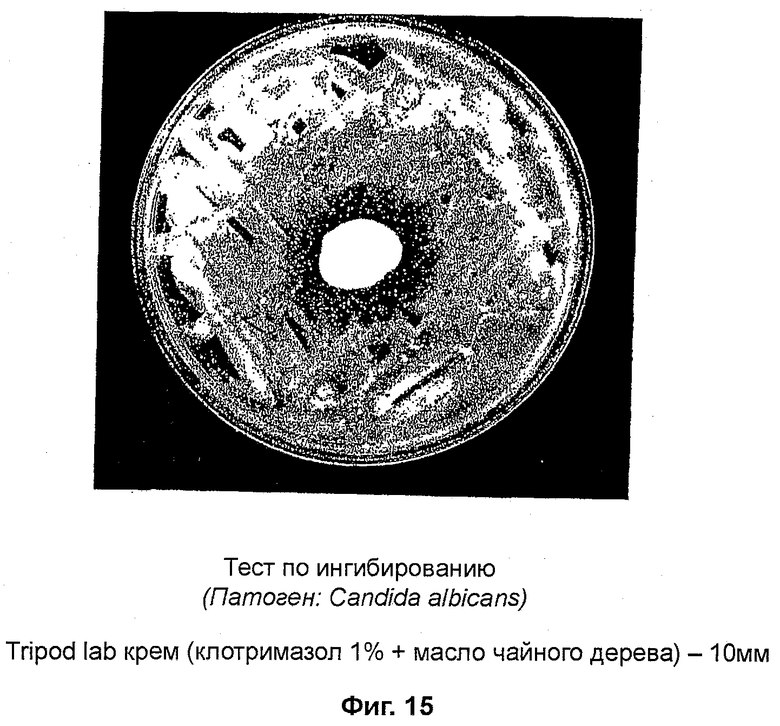
На фиг. 15 представлены данные ингибирования C. albicans при помощи различных известных веществ;
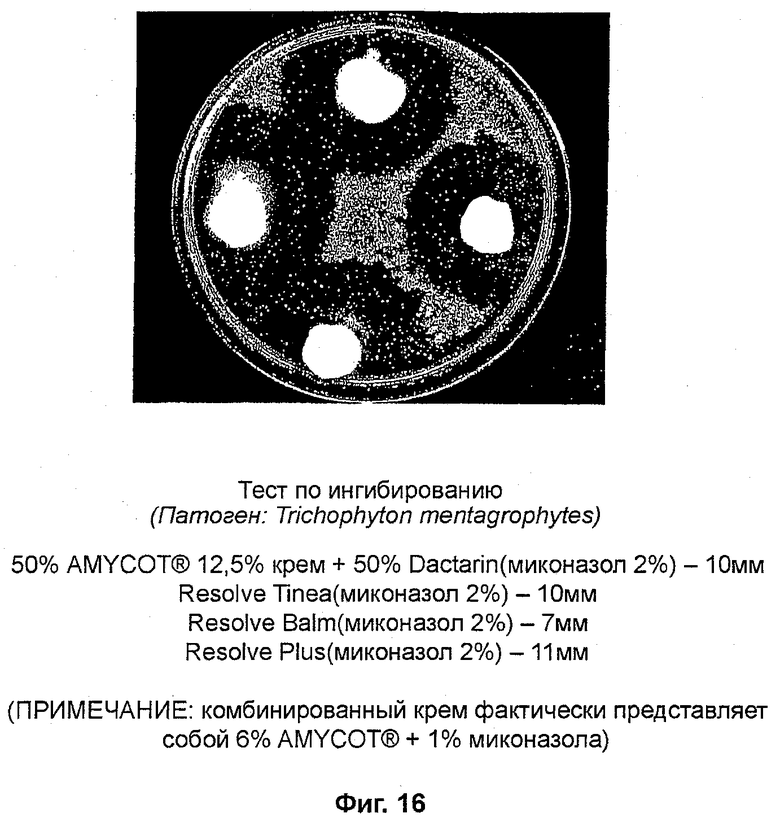
На фиг. 16 представлены данные ингибирования T. mentagrophytes при помощи AMYCOT® в сочетании с известным веществом и различными известными веществами;
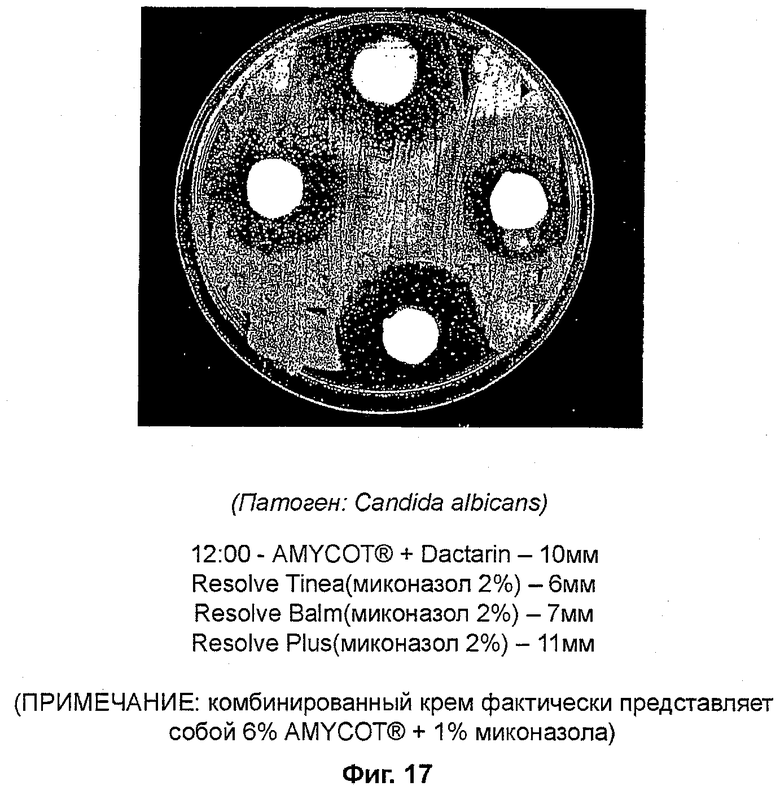
На фиг. 17 представлены данные ингибирования C. albicans при помощи AMYCOT® в сочетании с известным веществом и различными известными веществами;
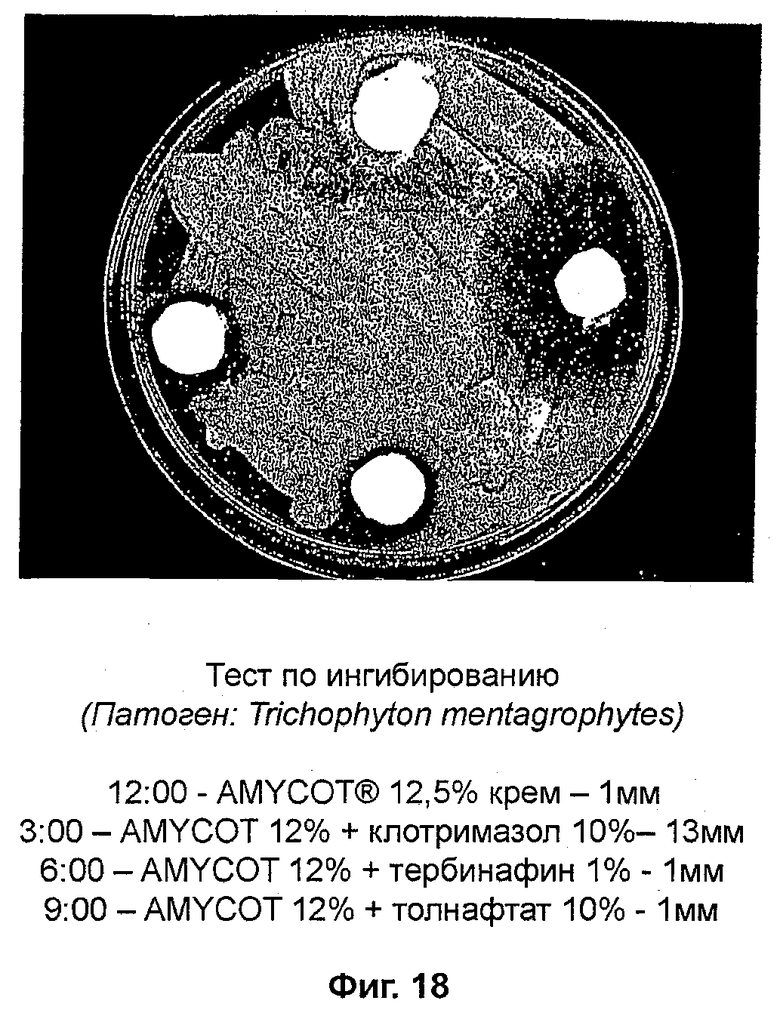
На фиг. 18 представлены данные ингибирования T. mentagrophytes при помощи AMYCOT® в сочетании с известными веществами;
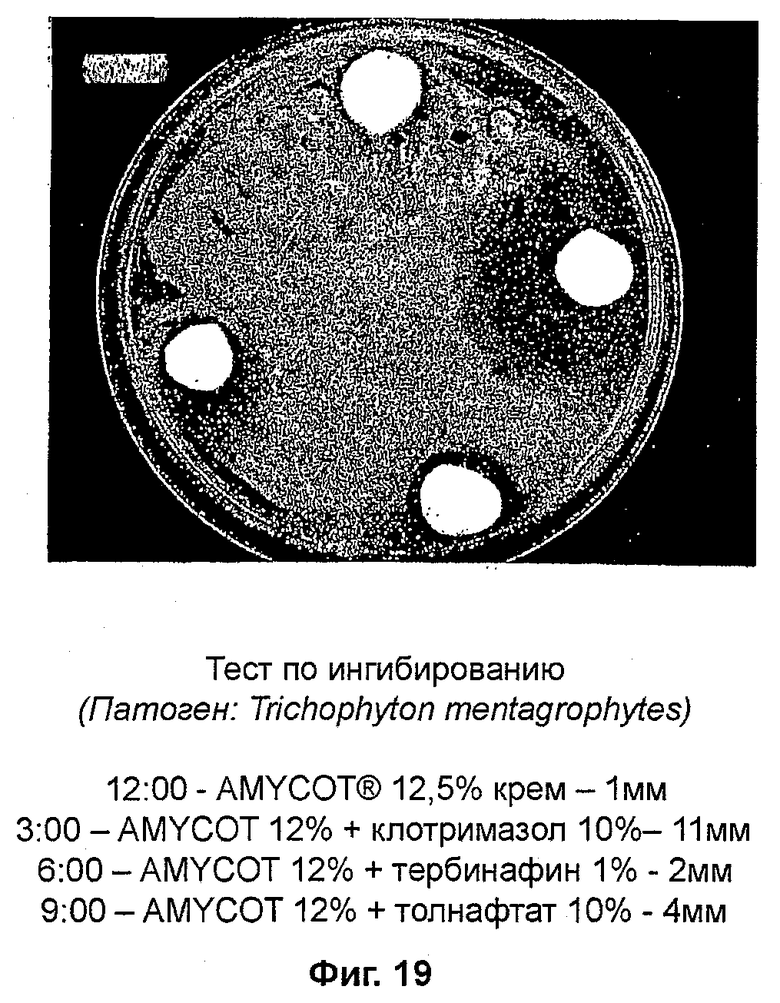
На фиг. 19 представлены данные ингибирования T. mentagrophytes при помощи AMYCOT® в сочетании с известными веществами;
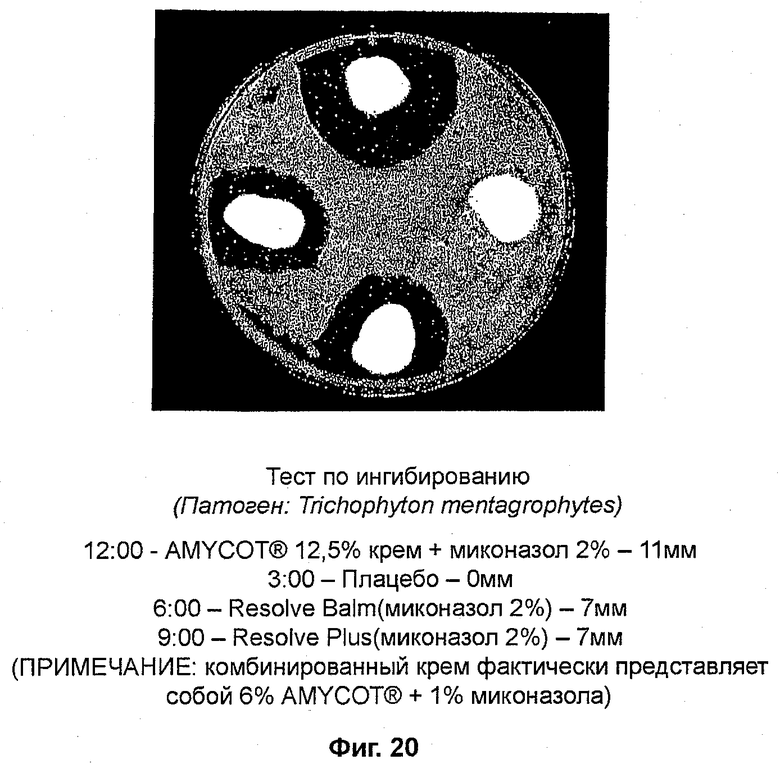
На фиг. 20 представлены данные ингибирования T. mentagrophytes при помощи AMYCOT® в сочетании с известным веществом и различными известными веществами;
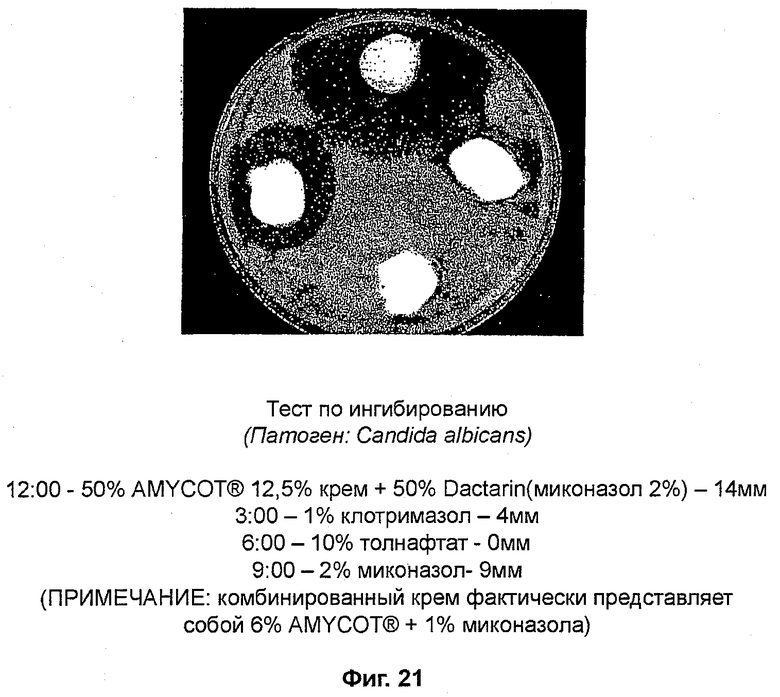
На фиг. 21 представлены данные ингибирования C. albicans при помощи AMYCOT® в сочетании с известным веществом и различными известными веществами;
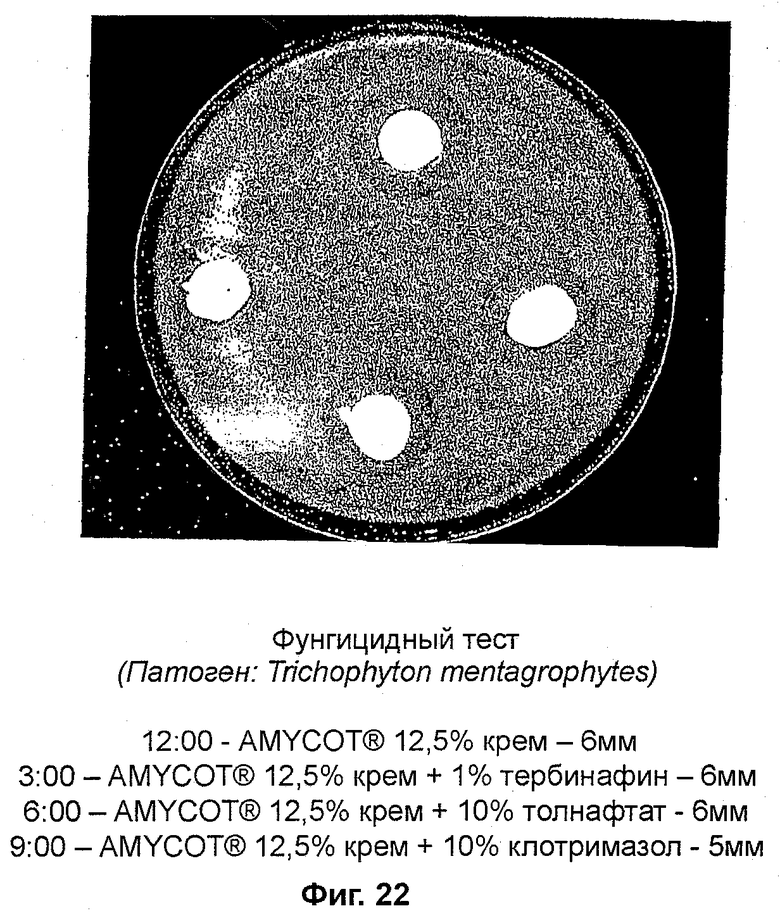
На фиг. 22 представлены данные фунгицидного действия в отношении T. mentagrophytes с использованием AMYCOT® в сочетании с известными веществами;
На фиг. 23 представлены данные фунгицидного действия AMYCOT® в сочетании с известными веществами в отношении T. rubrum с использованием;
На фиг. 24 представлены данные фунгицидного действия AMYCOT® в сочетании с известными веществами в отношении T. mentagrophytes;
На фиг. 25 представлены данные фунгицидного действия AMYCOT® в сочетании с известными веществами в отношении T. mentagrophytes;
На фиг. 26 представлены данные фунгицидного действия AMYCOT® в сочетании с известными веществами в отношении T. mentagrophytes;
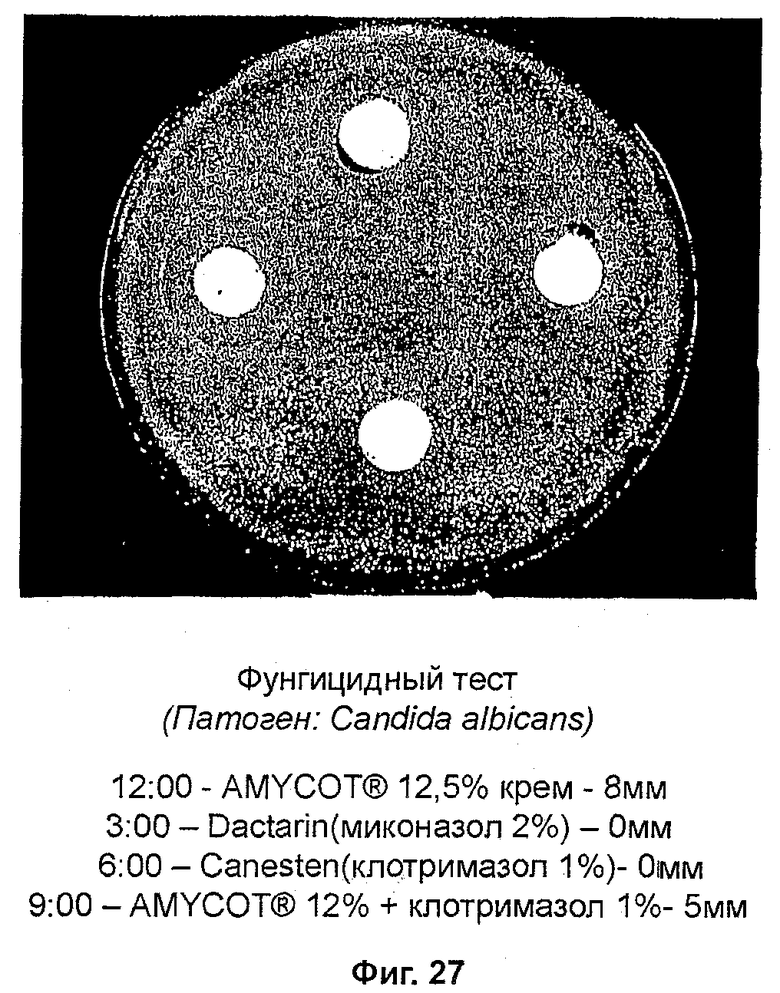
На фиг. 27 представлены данные фунгицидного действия AMYCOT® в сочетании с известным веществом и различными известными веществами в отношении C. albicans с использованием;
На фиг. 28 представлены данные фунгицидного действия в отношении T. rubrum с использованием AMYCOT® и известных веществ;
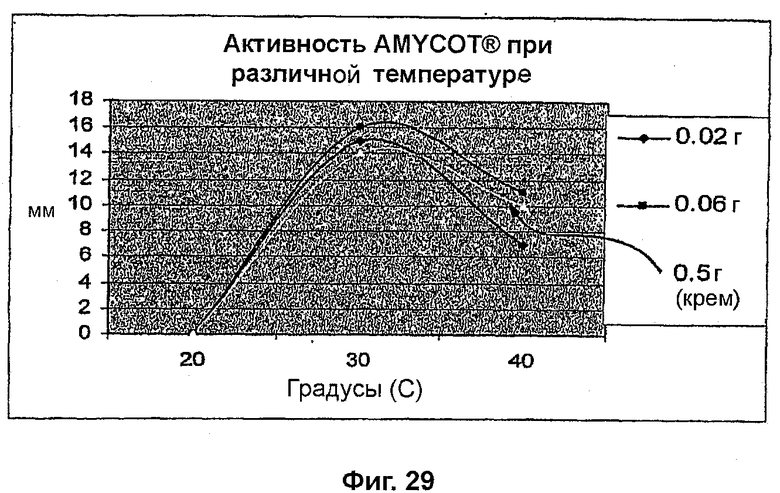
На фиг. 29 показано действие подвергнутой физиологическому стрессу Arthrospira (AMYCOT®) по отношению к хитину при различных температурах на основании данных респирометрии;
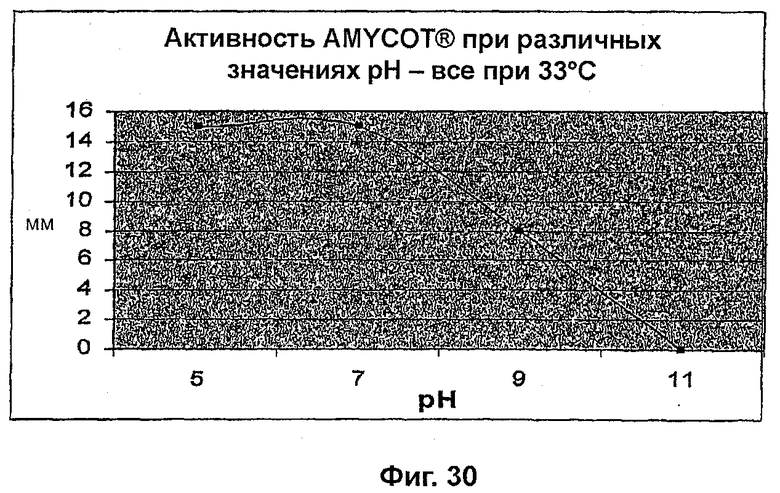
На фиг. 30 показано действие подвергнутой физиологическому стрессу Arthrospira (AMYCOT®) по отношению к хитину при различных значениях pH на основании данных респирометрии;
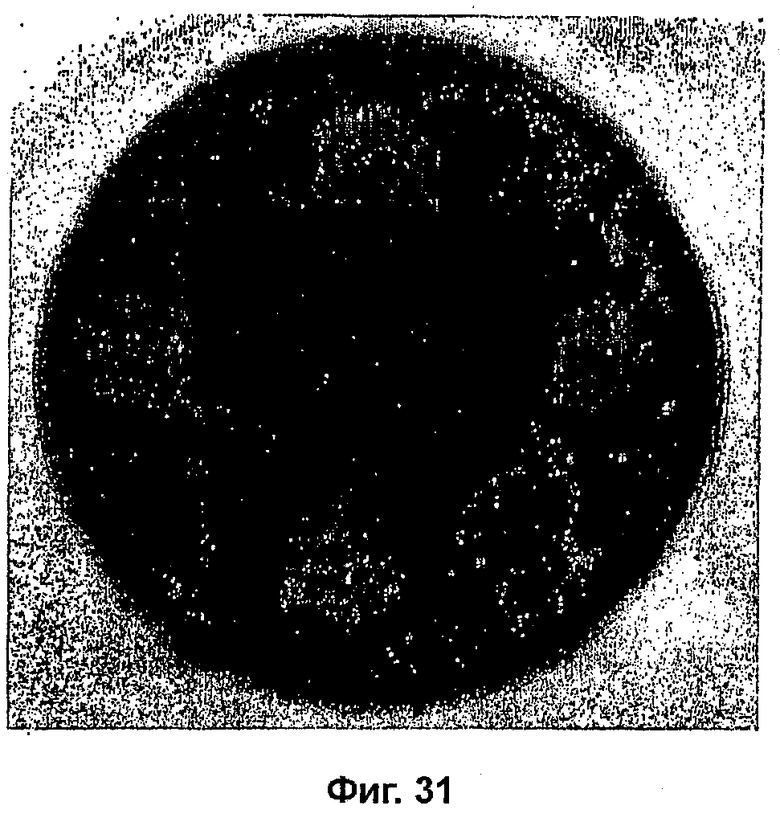
На фиг. 31 показана противогрибковая активность Arthrospira по отношению к T. mentagrophytes;
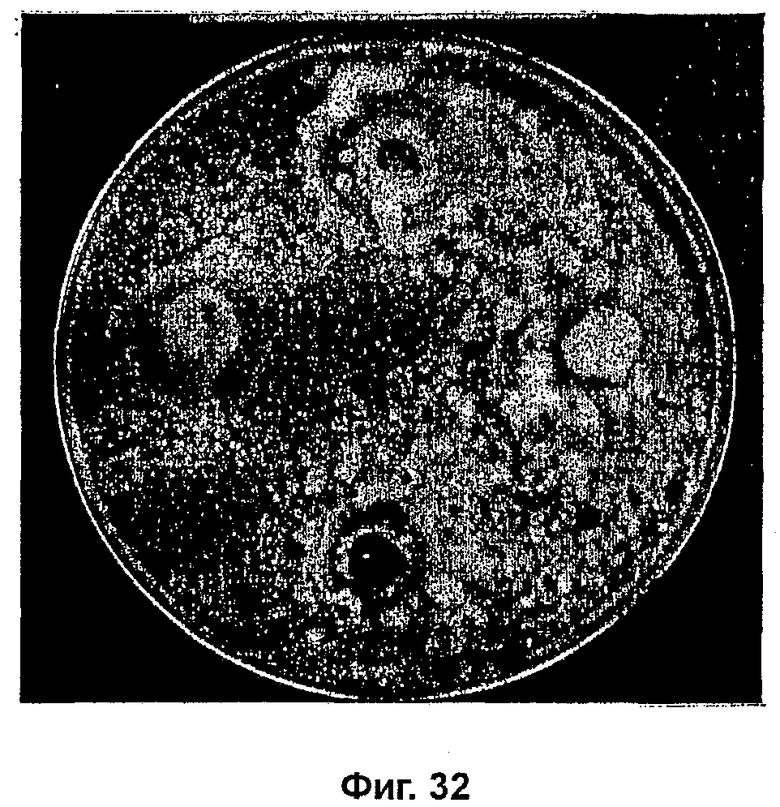
На фиг. 32 показана противогрибковая активность Arthrospira по отношению к T. rubrum;
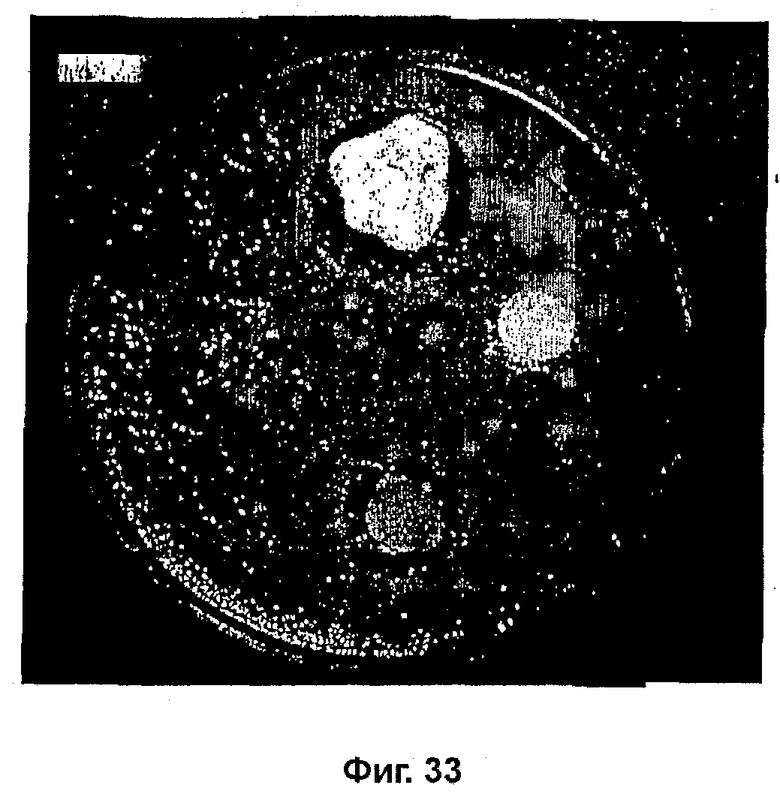
На фиг. 33 показана противогрибковая активность Arthrospira по отношению к M. fructicola;
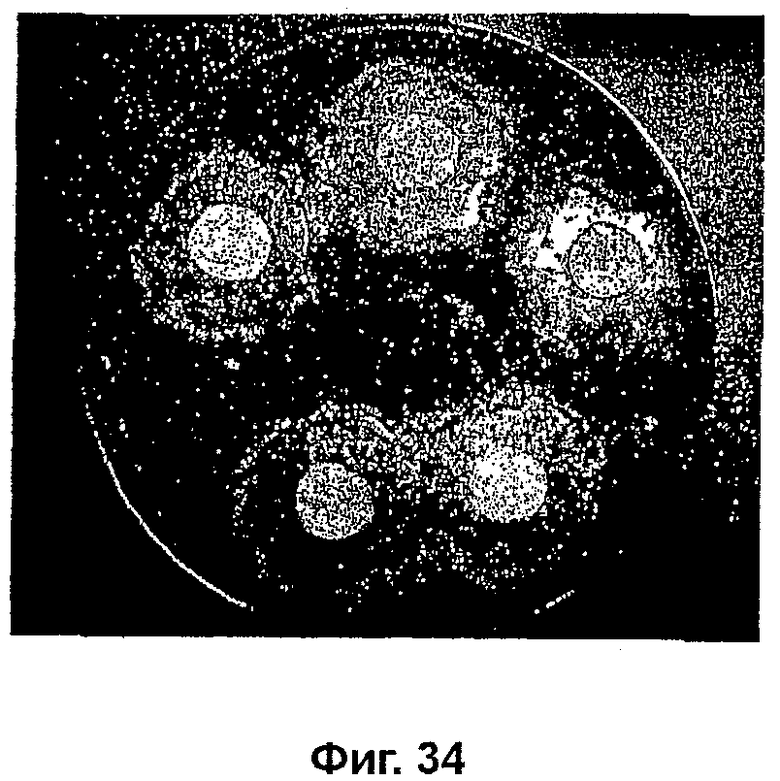
На фиг. 34 показана противогрибковая активность «усиленного AMYCOT®» и «оригинального AMYCOT®» по отношению к Alternaria sp.
НАИЛУЧШИЙ ВАРИАНТ И ДРУГИЕ ВАРИАНТЫ ОСУЩЕСТВЛЕНИЯ ИЗОБРЕТЕНИЯ
Предпочтительные варианты осуществления настоящего изобретения подробно описаны со ссылкой на следующие серии примеров только в качестве иллюстрации.
Пример 1 - Получение подвергнутой физиологическому стрессу Arthrospira
Культура Arthrospira maxima (полученная от Biovite Australia Pty Ltd) была подвергнута стрессу путем уменьшения количества питательных веществ или частичного высушивания. Arthrospira была обезвожена и высушена, в результате был получен «необработанный» порошок. Высушенная Arthrospira затем была подвергнута взрывной декомпрессии (потенциирована) при помощи способа, описанного в патентах Новой Зеландии № 328013 и № 328740. Arthrospira была заново смочена водой, обесцвечена, высушена и измельчена, в результате была получена «предварительная порошковая смесь». Предварительная порошковая смесь затем была растворена в подходящем носителе (например, в коммерчески доступном креме на водной основе производства British Pharmacopoeia или в воде). Предварительная порошковая смесь получила название «предварительная порошковая смесь AMYCOT®».
Пример 2 - Определение активности подвергнутой стрессу Arthrospira
Данные респирометрии позволяют предположить, что подвергнутая физиологическому стрессу Arthrospira обладает способностью модифицировать или разрушать субстраты, содержащие хитин, хитозан и/или N-ацетил-D-глюкозамин.
Хитин в качестве субстрата
Стандартные количества предварительно смешанного порошка AMYCOT® и необработанного порошка отдельно использовали в реакции с полимером хитина BHD из четырех звеньев (Sigma, № в каталоге C7170) в респирометре Варбурга по стандартной методике. Каждая композиция была смешана с хитином, и было измерено количество выделившегося газа. Реакция проводилась в течение часа, затем в течение 30 минут происходило уравновешивание. Та же самая композиция, но предварительно прокипяченная в течение 5 минут в водяной бане, не приводила к образованию какого-либо газа, что позволило предположить, что активность может быть ферментативной и может быть обусловлена одним или несколькими типами подверженных денатурации белков.
Результаты в виде графиков представлены на фиг. 1. Удельная активность (предположительно, ферментативная активность) необработанного порошка составляла 694,9 мл/г клеточной массы/г субстрата/час. Удельная активность предварительно смешанного порошка AMYCOT® составляла 729,65 мл/г клеточной массы/г субстрата/час.
При помощи респирометрии была также определена температура, оптимальная для активности. Предварительная порошковая смесь AMYCOT® (0,02 г и 0,06 г) была инкубирована с хитином (0,02 г) при 20°C, 30°C, 33°C и 40°C. Предварительная порошковая смесь AMYCOT® в основе для крема (0,05 г) была также инкубирована с хитином (0,02 г) при тех же температурах. Результаты графически представлены на фиг. 29. Оптимальная температура для активности в обоих случаях составила 33°С.
При помощи респирометрии было также определено оптимальное для активности значение pH. Предварительная порошковая смесь AMYCOT® (0,02 г) была суспендирована в буферах с различным значением pH (60-70% этанол, 30-40% вода, 0-0,05% фенолфталеин, 0-0,03% бромтимоловый голубой, 0-0,02% метиловый красный, натриевая соль, 0-0,01% гидроксид натрия и 0-0,01% метиловый оранжевый, натриевая соль, с pH 5, 7, 9 и 11) и был инкубирован с хитином (0,02 г) при 33°C. Результаты графически представлены на фиг. 30. Было определено, что для активности оптимальным значением pH является 6.
Эти результаты позволяют предположить, что при местном применении на коже биоактивное вещество или вещества должны обладать активностью, поскольку кожа имеет сходные температуру и pH.
N-ацетил-D-глюкозамин и хитозан в качестве субстратов
Предварительно смешанный порошок AMYCOT® (0,02 г) был по отдельности инкубирован с N-ацетил-D-глюкозамином (0,02 г, № A8625-5G в каталоге Sigma) и хитозаном (0,02 г, № C3646 в каталоге Sigma) в качестве субстратов в респирометре Варбурга при 33°C. Каждая реакция проводилась в течение одного часа, затем в течение 30 минут происходило уравновешивание.
Результаты для AMYCOT® плюс N-ацетил-D-глюкозамин представлены в таблице ниже.
AMYCOT® + N-ацетил-D-глюкозамин
В таблице ниже представлены результаты в случае AMYCOT® плюс хитозан.
AMYCOT® + хитозан
Для сравнения, в таблице ниже представлены результаты в случае AMYCOT® плюс хитин (0,02 г), инкубированных при 33°C.
AMYCOT® + хитин
Эти результаты позволяют предположить, что подвергнутая физиологическому стрессу Arthrospira содержит одно или более биоактивных веществ, которые разрушают или модифицируют хитин, хитозан и/или N-ацетил-D-глюкозамин, или, возможно, другой тип полимера, содержащего N-ацетил-D-глюкозамин в качестве субъединицы полимера. Биоактивным веществом может являться, например, хитинaза, хитозаназа или хитин-дезацетилaза.
Пример 3 - Противогрибковая и антибактериальная активности подвергнутой стрессу Arthrospira
Биоцидная активность предварительной порошковой смеси AMYCOT® была тестирована in vitro на живых грибках и грамположительных бактериях.
Живые культуры выбранных патогенов были получены от American Type Culture Collection (ATCC), Australian Collection of Microorganisms (ACM) и Sullivan Niccolaides. Тестированные культуры представлены в Таблице 4.
Равномерный газон каждого патогена был выращен на чашках, содержащих среду картофельно-декстрозный агар (PDA). После 3-4 дней инкубации в среде PDA при помощи стерильного перфоратора для пробок диаметром 8 мм были вырезаны 4 лунки. В каждую лунку было помещено определенное количество предварительной порошковой смеси AMYCOT® и контрольных кремов/порошков. Чашки культивировались в условиях, предназначенных для соответствующего патогена, и просматривались ежедневно.
Через 2-4 дня вокруг лунок проявлялись две концентрические зоны.
1. Меньшая прозрачная круглая зона «просветления» вокруг лунки. Эта область, в которой грибы погибли, остался лишь остаточный материал цитоплазмы (что было видно на просвет и в электронный микроскоп).
2. Большая полупрозрачная зона «повреждения», распространяющаяся от периметра зоны просветления. Зона повреждения отличается меньшей толщиной газона, меньшей его плотностью и большей прозрачностью по сравнению с нетронутым газоном. Это область, в которой клеточные стенки грибков были сильно разрушены, но какое-то количество все еще присутствовало, в основном, в виде округлых цитоплазматических сфер (что было видно на просвет и в электронный микроскоп).
В каждом случае измерение зон проводилось от внешнего периметра лунки до внешнего периметра зоны. Эта величина обозначена как размер зоны (РЗ). Радиус зоны нелинейным образом отражает эффективность действия биоцидного вещества/веществ по отношению к патогену in vitro.
Результаты проверки in vitro представлены в Таблице 5.
На фиг. 2 показано просветление для Candida albicans (ACM 4574) с использованием AMYCOT®, что свидетельствует об эффективности действия одного или нескольких биоцидных веществ в отношении заболевания молочницы. Предварительная порошковая смесь AMYCOT® находится в положении 6 часов, а «крем для испытаний на человеке», содержащий 12,5% (масс/масс) AMYCOT® в креме на водной основе - в положении 12 часов (РЗ = 9 мм).
В случае анаэробных бактерий Propionibacterium acne, вызывающих угри, при тестировании в анаэробных условиях просветление отсутствовало. Объяснение этому дается в Примере 4.
Пример 4 - Антибактериальная активность подвергнутой стрессу Arthrospira по отношению к Propionibacterium acne
По данным респирометрии, AMYCOT® обладает антибактериальной активностью по отношению к P. acne.
Предварительная порошковая смесь AMYCOT® (0,02 г) и 5г «крема для испытаний на человеке», содержащего 12,5% (масс/масс) AMYCOT®, были по отдельности добавлены к жидкой среде с анаэробным организмом P. acne, вызывающим угри (ACM № 5109), в респирометре Варбурга в присутствии или отсутствие кислорода. Результаты сравнивались с таковыми для контроля, содержащего жидкую среду с P. acne без AMYCOT®. В отсутствие кислорода газ не высвобождался. В присутствии кислорода газ освобождался, и каждая композиция обладала антибактериальной активностью.
Результаты для AMYCOT® и «крема для испытаний на человеке» в присутствии кислорода графически представлены на фиг. 3. (Предположительно ферментативная) удельная активность предварительной порошковой смеси AMYCOT® составляла 626,00 мл/г клеточной массы/г субстрата/час. Удельная активность для крема для испытаний на человеке составляла 12,00 мл/г клеточной массы/г субстрата/час.
Результаты показали, что для того, чтобы композиция могла оказывать антибактериальное действие in vivo по отношению к P. acne, необходимо присутствие кислорода. Следовательно, по меньшей мере одно из биоцидных веществ может являться оксидазой.
Авторы настоящего изобретения полагают, что одно или несколько биоцидных по отношению грибкам веществ могут разрушать или модифицировать клеточные стенки грибков. Такими веществами могут являться хитинaза, хитозаназа или хитин-дезацетилaза.
Хотя P. acne и другие грамположительные бактерии, как полагают, не содержат хитин или хитозан в своих клеточных стенках, предполагается, что одно или несколько биоцидных веществ разрушают или модифицируют N-ацетил-D-глюкозамин/пептидогликаны бактериальной клеточной стенки.
Пример 5 - Различные коммерчески доступные препараты Arthrospira обладают противогрибковой активностью
Коммерческие препараты высушенной Arthrospira (порошки, таблетки и капсулы) были получены от различных производителей, находящихся в разной ведомственной подчиненности, и были тестированы на наличие противогрибковой активности. Как правило, порошки изготавливаются путем сбора Arthrospira, промывки собранной Arthrospira и высушивания Arthrospira. Некоторые поставщики измельчают Arthrospira во влажном состоянии. При изготовлении опускается стадия подвергания Arthrospira специфическому стрессу после сбора биомассы, в результате которого Arthrospira входит в состояние анабиоза. Действительно, как было отмечено выше, коммерческие производители Arthrospira стремятся максимально уменьшить стрессовое воздействие на организм, поскольку толстая слизистая оболочка имеет свойство засорять оборудование для переработки организма.
Порошки Arthrospira (Spirulina) были получены от следующих производителей:
1. China Spirulina - Jiangsu Cibainian Nutrition Food Co., Ltd. Китай;
2. Febico - Far East Biotech Co. Ltd. Тайвань;
3. Life Stream/Earthrise - DIC. Калифорния, США;
4. Pacifica - Cyanotech. Гавайи, США;
5. Siam Algae Co. - DIC. Таиланд;
6. Spirin - Yunnan Spirin Co. Ltd. Китай;
7. Synergy - DIC. Китай.
Каждый порошок был смешан с кремом на водной основе в концентрации 12,5% масс/масс. Затем каждый крем был обесцвечен. Равномерный газон T. rubrum был выращен на чашках со средой PDA. После 3-4 дней инкубации в среде PDA при помощи стерильного перфоратора для пробок были сделаны лунки. Определенные количества каждого крема были помещены в соответствующую лунку, и чашки затем инкубировались в течение 2-4 дней.
На фиг. 4 показаны противогрибковые активности 12,5% (масс/масс) Siam Algae Co. (положение 3 час), 12,5% (масс/масс) Life Stream (положение 6 часов) и 12,5% (масс/масс) China Spirulina (положение 9 часов).
Полученные результаты показывают, что все тестированные коммерческие порошки обладали некоторой противогрибковой активностью. Данные респирометрии подтвердили, что все тестированные коммерческие порошки при инкубации с хитином обладали активностью (предположительно ферментативной) (результаты не приведены).
Один из порошков (Life Stream) был случайным образом выбран для смешивания с продаваемым без рецепта кремом на водной основе в концентрации 12,5% (масс/масс) без дальнейшей обработки и использован для тестирования противогрибковой активности в отношении Aspergillus niger. Крем приводил к образованию просветления в 4 мм, что видно на фиг. 5 в положениях 12, 3, 6 и 9 часов. Это показывало, что, возможно, все коммерческие препараты высушенной Arthrospira, по-видимому, обладали некоторым уровнем противогрибковой активности, что снимает необходимость проведения дополнительной стадии по вызыванию стресса или стадии дальнейшей обработки, например разрушения филаментов.
Пример 6 - Активность подвергнутой стрессу Arthrospira в отношении грибковых заболеваний млекопитающих
Противогрибковая активность AMYCOT® была тестирована in vitro в отношении различных грибковых заболеваний млекопитающих. Следующие патогены были получены из Department of Primary Industries, Department of Agriculture, ACM и детских садов:
- Candida albicans;
- Microsporum canis;
- Trichophyton mentagrophytes;
- Trichophyton rubrum;
- Epidermophyton floccosum;
- Fusarium graminearum;
- Alternaria sp.;
- Malassezia furfur.
Равномерный газон каждого патогена был выращен на среде PDA. После 1-2 дней инкубации в среде PDA были сделаны лунки при помощи стерильного перфоратора для пробок диаметром 8 мм. В каждую лунку было помещено определенное количество AMYCOT®. Чашки инкубировались при подходящей температуре, в зависимости от патогена. Чашки с лунками просматривались ежедневно. Прозрачность была измерена через 2-3 дня. Измерение зоны проводилось от периметра лунки до внешнего периметра зоны.
Указанная зона была свободна от живых клеток грибков, что говорило об эффективности AMYCOT® в отношении выбранных патогенов.
12,5% (масс/масс) крем AMYCOT® приводил к образованию просветления в 8 мм патогена T. rubrum. T. rubrum вызывает инфекции копыт и стригущий лишай.
12,5% (масс/масс) крем AMYCOT® приводил к образованию просветления в 15 мм патогена T. mentagrophytes. T. mentagrophytes вызывает инфекции копыт и стригущий лишай.
На фиг. 6 показана лунка с 12,5% (масс/масс) кремом AMYCOT®, который приводил к образованию просветления в 3 мм патогена M. canis. M. canis вызывает инфекции копыт и стригущий лишай.
12,5% (масс/масс) крем AMYCOT® приводил к образованию просветления в 3 мм патогена E. floccosum. E. floccosum вызывает инфекции копыт и стригущий лишай.
12,5% (масс/масс) крем AMYCOT® приводил к образованию просветления в 4,5 мм патогена C. albicans. C. albicans вызывает стригущий лишай и дерматит.
На фиг. 7 показана лунка с 12,5% (масс/масс) кремом AMYCOT®, который приводил к образованию просветления в 12 мм F. graminearum. F. graminearum вызывает инфекцию копыт.
На фиг. 8 показана лунка с 12,5% (масс/масс) кремом AMYCOT®, который приводил к образованию просветления M. furfur. M. furfur вызывает перхоть.
На фиг. 9a показана лунка с 5% (масс/масс) шампунем AMYCOT®, который приводил к образованию просветления в 3 мм патогена T. rubrum.
На фиг. 9b показана лунка с 5% (масс/масс) шампунем AMYCOT®, который приводил к образованию просветления в 4 мм патогена C. albicans.
Пример 7 - Активность подвергнутой стрессу Arthrospira в отношении грибковых заболеваний растений
Противогрибковая активность AMYCOT® была тестирована in vitro в отношении различных грибковых заболеваний растений. Следующие патогены были получены от Department of Primary Industries, Department of Agriculture, ACM и детских садов:
- Fusarium graminearum;
- Pithomyces Chartarum;
- Botrytis cinerea;
- Alternaria sp.
Равномерный газон каждого патогена был выращен на среде PDA. После 1-2 дней инкубации в среде PDA были сделаны лунки при помощи стерильного перфоратора для пробок диаметром 8 мм. В каждую лунку были внесены определенные количества AMYCOT®. Чашки инкубировались при подходящей температуре в зависимости от патогена. Чашки с лунками просматривались ежедневно.
Прозрачность была измерена через 2-3 дня. Измерение зоны проводили от периметра лунки до внешнего периметра зоны.
Зона была свободна от живых клеток грибков, что говорило об эффективности действия AMYCOT® в отношении выбранных патогенов.
12,5% (масс/масс) крем AMYCOT® приводил к образованию просветления в 13 мм патогена F. graminearum. F. graminearum вызывает увядание колосьев и гниение корневой шейки у малых злаков.
На фиг. 10 показана лунка с 12,5% (масс/масс) кремом AMYCOT®, который приводил к образованию просветления в 10 мм P. chartarum. P. chartarum вызывает экзему морды у овец.
12,5% (масс/масс) крем AMYCOT® приводил к образованию просветления в 8 мм патогена B. cinerea. B. cinerea вызывает образование серой гнили на фруктах.
12,5% (масс/масс) крем AMYCOT® приводил к образованию просветления в 9 мм патогена Alternaria sp., который вызывает пятнистость листьев фруктовых растений.
Пример 8 - Тестирование AMYCOT ® в виде спрея в отношении грибковых патогенов растений
AMYCOT® в форме противогрибкового аэрозоля был тестирован in vitro в отношении распространенного среди растений патогена Botrytis cinerea. 5% (масс/масс) порошок AMYCOT® был смочен водой, но оказался малорастворимым.
Равномерный газон B. cinerea был выращен на чашке со средой PDA. Затем правая сторона чашки была обработана аэрозолем и выдержана в течение 24 часов при комнатной температуре. Левая сторона чашки аэрозолем не обрабатывалась. На фиг. 11 показано, что обработанная аэрозолем сторона чашки содержит погибшие грибы. Аэрозоль был эффективен для уничтожения серой гнили и для подавления дальнейшей споруляции.
Пример 9 - Противомикробные тесты in vitro с подвергнутой стрессу Arthrospira и известными препаратами
В этом и других примерах были тестированы противогрибковые и антибактериальные активности различных продаваемых без рецепта противогрибковых и антибактериальных кремов (включая LamisilTM, Dakta GoldTM, CanestenTM, TinadermTM, DaktarinTM, Tripod LabsTM, Resolve TineaTM, Resolve BalmTM, Resolve PlusTM, ClearasilTM, Benzac WTM) и AMYCOT®.
В данном примере, противогрибковая и антибактериальная активности различных продаваемым без рецепта кремов и AMYCOT® были тестированы в независимой лаборатории (ConMac Laboratory Services) в отношении выбранных патогенов Trichophyton mentagrophytes, Epidermophyton floccosum, Trichophyton rubrum и Propionibacterium acne.
Результаты представлены в Таблице 6.
Результаты показывают, что только AMYCOT® был активен в отношении каждого патогена. Единственным отличным от AMYCOT® кремом, обладающим активностью, оказался крем LamisilTM с активностью в отношении T. rubrum.
Пример 10 - Тесты in vitro c известными веществами и комбинациями с AMYCOT ®
Противогрибковые вещества, такие как миконазол, толнафтат, бифоназол и клотримазол, действуют путем подавления образования специфических белков, препятствуя нормальным функциям, таким как репродукция. Противогрибковое вещество тербинафин препятствует образованию жизненно важных стероидов.
Первой целью этих тестов in vitro было определение эффективностей действия различных отпускаемых без рецепта кремов или входящих в их состав активных компонентов в качестве ингибиторов грибков и сравнение с эффективностью действия AMYCOT®. Второй целью было определение эффективности действия AMYCOT® в сочетании с одним или несколькими продаваемыми без рецепта кремами или входящими в их состав активными веществами в качестве ингибиторов грибков.
Жидкая среда Sabouraud засевалась выбранным патогеном. Затем культура инкубировалась в течение одной недели при 28°С. В среду, содержащую патоген, погружался стерильный тампон, и чашки со средой PDA засевали штрихами под прямыми углами, обеспечивая ровный газон в чашках.
Известные вещества, не входящие в основу для крема, смешивали с соответствующей основой для крема. Выбранный крем помещался на диск фильтровальной бумаги диаметром 10 мм, после чего диск помещался на только что засеянную чашку. На одной чашке располагалось до четырех различных дисков. Чашка затем инкубировалась в течение 24-48 часов при подходящей температуре, зависящей от патогена. По прошествии 24-48 часов делали фотографии.
Результаты тестов по ингибированию приведены на фиг. 12-21 и в таблицах 7-16 ниже.
Тест по ингибированию (фиг. 12)
Патоген: Trichophyton rubrum
Тест по ингибированию (фиг. 13)
Патоген: Trichophyton mentagrophytes
Тест по ингибированию (фиг. 14)
Патоген: Candida albicans
Тест по ингибированию (фиг. 15)
Патоген: Candida albicans
Тест по ингибированию (фиг. 16)
Патоген: Trichophyton mentagrophytes
Тест по ингибированию (фиг. 17)
Патоген: Candida albicans
Тест по ингибированию (фиг. 18)
Патоген: Trichophyton mentagrophytes
Тест по ингибированию (фиг. 19)
Патоген: Trichophyton mentagrophytes
Тест по ингибированию (фиг. 20)
Патоген: Trichophyton mentagrophytes
Тест по ингибированию (фиг. 21)
Патоген: Candida albicans
В случае фиг. 21 известные вещества содержатся в креме на водной основе, в отличие от обычно используемой спиртовой основы.
В тестах in vitro выяснилось, что миконазол и клотримазол являются наиболее эффективными ингибиторами патологических грибков (смотри фиг. 12-21). Фиг. 16 и 17 и таблицы 11 и 12 доказывают, что миконазол является эффективным ингибитором грибков. AMYCOT® также действует в качестве ингибитора, однако его эффективность составляет примерно 40% от эффективности клотримазола и миконазола (смотри фиг. 12-14). Фиг. 18-21 и таблицы 13-16 позволяют предположить, что комбинации AMYCOT® плюс миконазол и AMYCOT® плюс клотримазол являются наиболее эффективными грибковыми ингибиторами in vitro по сравнению с тербинафином и толнафтатом.
Третьей целью указанных тестов in vitro было определение эффективностей действия различных отпускаемых без рецепта кремов или входящих в их состав активных веществ в качестве фунгицидов и сравнение с эффективностью действия AMYCOT®. Четвертой целью было определение эффективности действия AMYCOT® в сочетании с известными веществами.
Фунгицидный тест включал в себя выращивание газона с патогеном на чашках со средой PDA в течение 2-3 дней и затем экспонирование выросшего патогена с противогрибковыми веществами. Это было сделано посредством вырезания лунок в покрытом газоном агаре, удаления агара и заполнения лунок кремом.
Результаты фунгицидного теста приведены на фиг. 22-28 и в таблицах 17-23 ниже.
Фунгицидный тест (фиг. 22)
Патоген: Trichophyton mentagrophytes
Фунгицидный тест (фиг. 23)
Патоген: Trichophyton rubrum
Фунгицидный тест (фиг. 24)
Патоген: Trichophyton mentagrophytes
Фунгицидный тест (фиг. 25)
Патоген: Trichophyton mentagrophytes
Фунгицидный тест (фиг. 26)
Патоген: Trichophyton mentagrophytes
Фунгицидный тест (фиг. 27)
Патоген: Candida albicans
Тест по ингибированию (фиг. 28)
Патоген: Trichophyton rubrum
В случае фиг. 28 известные вещества содержатся в креме на водной основе в отличие от спиртовой основы, которая обычно используется.
Результаты подтверждают, что рассматриваемые продаваемые без рецепта противогрибковые вещества и известные вещества представляют собой фунгистатические вещества и не являются фунгицидами. Фиг. 22-28 и таблицы 17-23 показывают, что AMYCOT® является эффективным фунгицидом даже в сочетании с известными веществами.
Комбинация AMYCOT® с миконазолом или клотримазолом не приводила к значительному уменьшению эффективности каждого. Комбинация усиливала ингибиторный эффект (смотри фиг. 17-21). Это говорит о создании очень эффективного продукта с широким спектром действия.
Комбинация AMYCOT® с клотримазолом слабо ингибировала противогрибковую активность AMYCOT® (смотри фиг. 22-28), однако комбинация AMYCOT® с миконазолом не оказывала значительных вредных эффектов на ингибиторную или противогрибковую активность комбинированного крема (смотри фиг. 17-26).
Комбинированный крем с AMYCOT® и миконазолом был более эффективен в качестве продукта широкого спектра действия по сравнению с другими благодаря ингибиторным свойствам миконазола и как ингибиторной, так и противогрибковой активности AMYCOT®.
Крем, содержащий такую комбинацию, действовал как ингибитор и затем «не сдавал позиции», тогда как просветление, полученное лишь с одним миконазолом, нарушалось в результате повторного роста, как в случае с патогеном T. mentagrophytes (смотри фиг. 20).
Было также обнаружено, что комбинация крема AMYCOT® с 2% миконазолом препятствует повторному росту патогена после просветления, образованного вокруг лунок.
Пример 11 - Испытания Arthrospira при различных заболеваниях кожи
Субъект имел большие атлетические стопы с глубокими повреждениями между пальцами. Субъект сообщил, что вызванный грибком зуд прекратился через 15 минут после первого применения 12,5% (масс/масс) крема AMYCOT®. Раздражение уменьшалось и в некоторых случаях полностью исчезло в течение 12 часов. Повреждение начало затягиваться через 24 часа и полностью зажило через 4-5 дней.
Подобная картина наблюдалась в случае угрей у субъектов, которые отмечали, что сопутствующее раздражение исчезало и что их кожа приобретала нормальный цвет и становилась мягкой и пластичной подобно новой коже. Пустулы также подсыхали.
По мнению авторов настоящего изобретения, один или несколько биоцидных веществ (таких как хитинaза, хитозаназа, хитин-дезацетилаза) синергически взаимодействуют с другими компонентами Arthrospira, что усиливает терапевтический эффект. При грибковых инфекциях зуд является показателем высвобождения из грибов пищеварительных ферментов или метаболитов. Зуд прекращается, как только нарушается нормальный метаболизм грибов, что происходит при разрушении клеточной стенки.
Аналогичные результаты были получены при использовании крема при заболеваниях, не связанных с грибками, в случае сухих и треснувших пяток и локтей, розовых угрей, экземы, солнечных ожогов и псориаза. Субъекты сообщали о почти немедленном прекращении зуда при дерматите.
Пример 12 - Противогрибковая активность подвергнутой стрессу Arthrospira при использовании «необработанного» порошка
Пример 5 подтвердил, что коммерческие препараты высушенной Arthrospira обладали, по-видимому, некоторым уровнем противогрибковой активности, не требующим дополнительной стадии стессового воздействия или стадии обработки собранной биомассы, как например разрушение филаментов. Пример 12 дополнительно подтверждает это наблюдение.
Высушенный препарат Arthrospira maxima был получен от коммерческого производителя. Препарат был смешан с продаваемым без рецепта кремом на водной основе в концентрации 12,5% (масс/масс) без дальнейшей обработки, и его противогрибковая активность была тестирована в отношении T. mentagrophytes, T. rubrum и M. fructicola (как описано в Примере 5).
Как показано на фиг. 31, крем приводил к образованию просветления T. mentagrophytes в положениях 12, 3, 6 и 9 часов.
Как видно на фиг. 32, крем приводил к образованию просветления T. rubrum в положении 6 часов.
Как видно на фиг. 33, крем приводил к образованию просветления M. fructicola в положении 6 часов.
Эти наблюдения подтверждают, что для получения Arthrospira, обладающей фунгицидной активностью, нет необходимости в проведении стадий, следующих за сбором биомассы, таких как взрывная декомпрессия, высушивание замораживанием, обесцвечивание и измельчение.
Пример 13 - Противогрибковая активность Arthrospira, не подвегнутой взрывной декомпрессии
Этот пример дополнительно подтверждает, что для получения Arthrospira, обладающей противогрибковой активностью, не требуется проведение стадии взрывной декомпрессии (потенциирования), которая следует за стадией сбора биомассы.
Высушенный препарат Arthrospira maxima был получен от коммерческого производителя. В одном случае, высушенная Arthrospira была разрушена при помощи взрывной декомпрессии (потенциирована) с использованием способа, описанного в патентах Новой Зеландии № 328013 и № 328740. Arthrospira была повторно смочена, обесцвечена, высушена и перемолота, в результате была получена сухая «предварительная порошковая смесь». Предварительная порошковая смесь затем была смешана с подходящим носителем (12,5%) и получила название «усиленный AMYCOT®».
В другом случае, при изготовлении был исключен способ взрывной декомпрессии, описанный в патентах Новой Зеландии № 328013 и № 328740, и такой препарат получил название «оригинальный AMYCOT®».
Как видно на фиг. 34, как «оригинальный AMYCOT®», так и «усиленный AMYCOT®» приводили к образованию почти одинакового просветления Alternaria sp. в положениях 12 и 7 часов, соответственно. Таким образом, для получения Arthrospira, обладающей фунгицидной активностью, стадия взрывной декомпрессии, следующая за сбором биомассы, не является существенной.
Следует дополнительно принять во внимание, что могут быть внесены многие изменения в композиции, способы применения и получения, поясняемые вышеприведенными примерами, без выхода за определенные рамки и объем изобретения.
Термин «содержать» и варианты этого термина «содержит» и «содержащий» используются здесь для обозначения включения заявленного числа или заявленных чисел, но не исключает любое другое число или другие числа, если только в контексте или при использовании не требуется особая интерпретация термина.
Любые ссылки на цитируемые здесь публикации не допускаются, так как в Австралии открытия составляют общедоступное знание.







Изобретение относится к биотехнологии, а именно к композиции, содержащей подвергнутую физиологическому стрессу Arthrospira maxima, для применения в качестве биоцида и/или терапевтического средства. Изобретение также относится к способу профилактики или лечения инфекции или заражения субъекта организмом, где способ включает стадию введения субъекту эффективного количества композиции, содержащей подвергнутую физиологическому стрессу Arthrospira. Изобретение позволяет повысить эффективность биоцидных композиций и терапевтических средств. 18 н. и 12 з.п. ф-лы, 23 табл., 34 ил.
1. Способ получения композиции на основе Arthrospira для местного применения у индивида в качестве биоцида или средства для восстановления или профилактики дефектов кожи у млекопитающего, который включает стадии
(1) проведения физиологического стресса Arthrospira, но не высушивания замораживанием Arthrospira; и
(2) объединения количества, эффективного в качестве биоцида или средства для восстановления или профилактики дефектов кожи, Arthrospira, подвергнутой стрессу, по (1) с носителем, растворителем, основой или наполнителем, подходящим для местного применения у индивида, причем эффективное в качестве биоцида количество является эффективным против грибков, грамположительных бактерий или вирусов.
2. Способ по п.1, в котором Arthrospira представляет собой A.maxima.
3. Композиция на основе Arthrospira для местного применения у индивида в качестве биоцида или средства для восстановления или профилактики дефектов кожи у млекопитающего, полученная способом по п.1.
4. Способ получения композиции на основе Arthrospira для местного применения у индивида в качестве биоцида против грибков, грамположительных бактерий или вирусов, или средства для восстановления или профилактики дефектов кожи у млекопитающего, который включает стадии
(1) проведения физиологического стресса у Arthrospira путем удаления приблизительно до 80% жидкости, в которой выращивают Arthrospira;
(2) промывки подвергнутой стрессу Arthrospira для удаления загрязнений;
(3) высушивания промытой Arthrospira; и
(4) объединения количества, эффективного в качестве биоцида или средства для восстановления или профилактики дефектов кожи, Arthrospira, полученной на стадии (3), с носителем, растворителем, основой или наполнителем, подходящим для местного применения у индивида или млекопитающего, причем Arthrospira не высушивали замораживанием.
5. Композиция на основе Arthrospira для местного применения у индивида в качестве биоцида или средства для восстановления или профилактики дефектов кожи у млекопитающего, полученная способом по п.4.
6. Фунгицидная композиция для профилактики или лечения местной грибковой инфекции или заражения у индивида, содержащая количество, эффективное в качестве фунгицида, подвергнутой физиологическому стрессу Arthrospira и носитель, растворитель, основу или наполнитель, подходящие для местного применения у индивида, причем Arthrospira не высушивали замораживанием.
7. Способ профилактики или лечения местной грибковой инфекции или заражения у индивида, который включает стадию местного применения у индивида композиции по п.6.
8. Способ по п.7, дополнительно включающий стадию первоначального выявления индивида, нуждающегося в таком лечении или нуждающегося в такой профилактике.
9. Способ по п.7, в котором индивидом является человек, животное, сельскохозяйственный или садоводческий продукт, почва или искусственное сооружение.
10. Способ получения фунгицидной композиции для местного применения по п.6 для профилактики или лечения местной грибковой инфекции у индивида, который включает стадии
(1) проведения физиологического стресса Arthrospira;
(2) объединения количества, эффективного в качестве фунгицида, подвергнутой стрессу Arthrospira по (1) с носителем, растворителем, основой или наполнителем, подходящим для местного применения у указанного индивида, причем Arthrospira не высушивали замораживанием.
11. Фунгицидная композиция для местного применения для профилактики или лечения местной грибковой инфекции или заражения индивида, содержащая синергическую комбинацию количества, эффективного в качестве фунгицида, подвергнутой физиологическому стрессу Arthrospira и по меньшей мере одного фунгистатического средства и носителя, растворителя, основы или наполнителя, подходящих для местного применения у указанного индивида, причем Arthrospira не высушивали замораживанием.
12. Фунгицидная композиция для местного применения по п.11, в которой фунгистатическое средство выбрано из группы, состоящей из тербинафина, бифоназола, клотримазола, миконазола, эконазола, кетоконазола и толнафтата.
13. Способ профилактики или лечения местной грибковой инфекции или заражения у индивида, который включает стадию местного применения у индивида композиции по п.11.
14. Способ по п.13, в котором фунгистатическое средство выбрано из группы, состоящей из тербинафина, бифоназола, клотримазола, миконазола, эконазола, кетоконазола и толнафтата.
15. Способ получения фунгицидной композиции для местного применения по п.11 для профилактики или лечения местной грибковой инфекции или заражения индивида, который включает стадии
(1) проведения физиологического стресса Arthrospira;
(2) объединения композиции, эффективной в качестве фунгицида, подвергнутой стрессу Arthrospira по (1) по меньшей мере с одним фунгистатическим средством и носителем, растворителем, основой или наполнителем, подходящими для местного применения у индивида, причем Arthrospira не высушивали замораживанием.
16. Бактерицидная композиция для местного применения для профилактики или лечения местной инфекции, вызванной грамположительными бактериями, у индивида, содержащая количество, эффективное в качестве бактерицидного, подвергнутой физиологическому стрессу Arthrospira и носитель, растворитель, основу или наполнитель, подходящие для местного применения у индивида, причем Arthrospira не высушивали замораживанием.
17. Способ профилактики или лечения местной инфекции, вызванной грамположительными бактериями, или заражения у индивида, который включает стадию местного применения у индивида композиции по п.16.
18. Способ по п.17, дополнительно включающий стадию первоначального выявления индивида, нуждающегося в таком лечении или нуждающегося в такой профилактике.
19. Способ по п.17, в котором бактериальная инфекция вызвана грамположительными бактериями Propionibacterium acne.
20. Способ по п.17, в котором индивидом является человек.
21. Способ получения бактерицидной композиции против грамположительных бактерий для местного применения по п.16 для профилактики или лечения местной инфекции, вызванной грамположительными бактериями, который включает стадии
(1) проведения физиологического стресса Arthrospira; и
(2) объединения количества, эффективного в качестве бактерицидного против грамположительных бактерий, подвергнутой стрессу Arthrospira по (1) с носителем, растворителем, основой или наполнителем, подходящими для местного применения у указанного индивида, причем Arthrospira не высушивали замораживанием.
22. Противовирусная композиция для местного применения для профилактики или лечения местной вирусной инфекции у индивида, содержащая количество, эффективное в качестве противовирусного, подвергнутой стрессу Arthrospira и носитель, растворитель, основу или наполнитель, подходящие для местного применения у указанного индивида, причем Arthrospira не высушивали замораживанием.
23. Способ профилактики или лечения местной вирусной инфекции у индивида, который включает стадию местного применения у индивида эффективного количества композиции по п.22.
24. Способ по п.23, дополнительно включающий стадию первоначального выявления индивида, нуждающегося в таком лечении или нуждающегося в такой профилактике.
25. Способ по п.24, в котором индивидом является человек.
26. Способ получения противовирусной композиции для местного применения по п.22 для профилактики или лечения местной вирусной инфекции у индивида, который включает стадии
(1) проведения физиологического стресса Arthrospira; и
(2) объединения количества, эффективного в качестве противовирусного, подвергнутой стрессу Arthrospira по (1) с носителем, растворителем, основой или наполнителем, подходящими для местного применения у указанного индивида, причем Arthrospira не высушивали замораживанием.
27. Композиция для заживления или профилактики дефекта кожи для местного применения у млекопитающего, где указанная композиция содержит количество, эффективного в качестве биоцида, подвергнутой физиологическому стрессу Arthrospira и носитель, растворитель, основу или наполнитель, подходящие для местного применения у млекопитающего, причем количество, эффективное в качестве биоцида, является эффективным против грибков, грамположительных бактерий или вирусов, при этом Arthrospira не высушивали замораживанием.
28. Способ для заживления или профилактики дефекта кожи у млекопитающего, который включает стадию местного введения млекопитающему композиции по п.27.
29. Способ по п.28, дополнительно включающий стадию первоначального выявления млекопитающего, нуждающегося в таком лечении или нуждающегося в такой профилактике.
30. Способ по п.28, в котором дефект кожи выбран из группы, состоящей из оспины, угревого повреждения, розового угря, покрасневшего пятна, трещины, ожога, волдыря, псориаза, экземы, шелушения, морщины, папулы, стоматита, повреждения, пустулы, раны, себорейного дерматита, опрелости, язвы, герпеса, высыпаний после бритья, ветряной оспы, дерматита и трещин на пятках и локтях.
| WO 1998025470 A, 18.06.1998 | |||
| WO 1998025471 A, 18.06.1998 | |||
| AYEHUNIE S | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| J | |||
| Acquir | |||
| Immune Defic | |||
| Syndr | |||
| Hum | |||
| Retrovirol | |||
| Способ и аппарат для получения гидразобензола или его гомологов | 1922 |
|
SU1998A1 |
| СПОСОБ ПОЛУЧЕНИЯ ПРЕПАРАТА СПИРУЛИНЫ, СОДЕРЖАЩЕЙ ХРОМ | 2002 |
|
RU2230560C2 |
Авторы
Даты
2011-02-27—Публикация
2005-11-03—Подача