Настоящее изобретение относится к способу минерализации дентальной поверхности, в частности зубной эмали. Также предлагаются способы минерализации гипоминерализованных повреждений (включая субповерхностные повреждения) в зубной эмали, вызванных дентальным кариесом, дентальной эрозией и флюорозом.
Предшествующий уровень техники
Распространенными причинами гипоминерализованных повреждений являются кариес и флюороз.
Дентальный кариес инициируется путем деминерализации твердой ткани зубов обычно органическими кислотами, продуцированными в результате ферментации пищевого сахара одонтопатогенными бактериями дентальных бляшек. Дентальный кариес представляет собой по-прежнему важную проблему здравоохранения. Более того, восстановленные зубные поверхности могут быть чувствительны к дальнейшему дентальному кариесу вокруг краев восстановления. Несмотря на то что распространенность дентального кариеса сократилась в результате применения фторида в большинстве развитых стран, заболевание остается важной проблемой здравоохранения. Дентальная эрозия или коррозия представляет собой утрату зубного минерала посредством пищевой или отрыгнутой кислот. Дентальная гиперчувствительность происходит в обработанных дентинных канальцах в результате утраты защитного минерализованного слоя, цемента. Дентальный налет представляет собой нежелательное нарастание кальцийфосфатных минералов на зубной поверхности. Все эти состояния, дентальный кариес, дентальная эрозия, дентальная гиперчувствительность и дентальный налет представляют собой, поэтому, дисбалансы уровня кальций фосфатов.
Флюороз эмали (пятнистое поражение) был исследован в течение почти столетия, однако этиологическая роль фторида не была идентифицирована до 1942 (Black и McKay, 1916). Характеристическая картина флюороза может отличаться от других нарушений эмали (Fejerskov с сотр., 1991). Клинические признаки флюорозных повреждений эмали (FLE) представляют континуум, начиная с тонких темных линий, исходящих из перикумата, до меловой, белой эмали (Fejerskov с сотр., 1990; Giambro с сотр., 1995). Наличие сравнительно высокоминерализованной эмалевой наружной поверхности и гипоминерализованной субповерхности во флюорозном повреждении имитирует зарождающееся эмалевое «белое пятно» кариозного повреждения (Fejerskov с сотр., 1990). С увеличением тяжести заболевания глубина эмали, вовлеченной в повреждение, и степень гипоминерализации увеличиваются (Fejerskov с сотр., 1990; Giambro с сотр., 1995). Развитие флюороза сильно зависит от дозы, длительности и времени экспозиции фторида (Fejerskov с сотр., 1990; Fejerskov с сотр., 1996; Aoba и Fejerskov, 2002) и, полагают, имеет отношение к повышению концентраций сывороточного фторида. Повреждения в виде меловых «белых пятен» могут также формироваться на развивающихся зубах у детей, как, например, после лечения антибиотиками или лихорадки. Такие повреждения обозначают области гипоминерализации зубной эмали.
В зависимости от тяжести повреждения с флюорозом справлялись клинически путем восстановительного замещения или микроабразии наружной эмали (Den Besten и Thariani, 1992: Fejerskov с сотр., 1996). Эти курсы лечения являются недостаточными, так как они включают замещение или удаление зубной ткани. Что желательно, так это лечение, которое будет минерализовать гипоминерализованную эмаль с продуцированием природной картины и структуры.
Было показано, что специфические комплексы казеиновых фосфопептидов и аморфного кальция фосфата («CPP-ACP», доступные коммерчески как RecaldentTM) реминерализуют эмалевые субповерхностные повреждения in vitro и in situ (Reynolds, 1998; Shen с сотр., 2001; Reynolds с сотр., 2003).
WO 98/40406 по поручению университета Мельбурна (содержание которого в данном описании включено полностью посредством ссылки) описывает комплексы казеиновый фосфопептид-аморфный кальция фосфат (CPP-ACP) и CPP-стабилизированные комплексы аморфный кальция фторид фосфат (CPP-ACFP), которые будут продуцироваться при щелочном pH. Было показано, что такие комплексы предотвращают деминерализацию эмали и стимулируют реминерализацию эмалевых субповерхностных повреждений на in situ кариесных моделях животных и человека (Reynolds, 1998).
CPP, который активен в формировании комплексов, не зависит от того, являются ли они частью полноразмерного казеинового белка. Примеры активного (CPP), который может быть выделен после триптического переваривания полноразмерного казеина, были описаны в Патенте США № 5015628 и включают пептиды Bos αs1-казеин X-5P (f59-79) [1], Bos β-казеин X-4P (f1-25) [2], Bos αs2-казеин X-4P (f46-70) [3] и Bos αs2-казеин X-4P (f1-21) [4], как указано ниже:


Доступ минерализующих ионов к зубной эмали во многих случаях может быть ограничен слоем слюнных белков, который формируется поверх поверхности эмали, названной кутикула. Белки кутикулы могут также накапливаться в субповерхностных эмалевых повреждениях, тем самым ингибируя минерализацию этих повреждений. Такие скопления белков могут изменять цвет с течением времени, приводя к некрасивым бляшкам на зубе. Соответственно требуется удаление этих белков с удалением областей изменения окраски и предотвращение ограничений доступа к эмали реминерализующих ионов. С этой целью было проведено преодоление этих и других ограничений известных курсов лечения.
Сущность изобретения
В одном аспекте настоящее изобретение предлагает способ минерализации дентальной поверхности или субповерхности, включающий контактирование дентальной поверхности с белок-разрушающим агентом и контактирование дентальной поверхности со стабилизированным аморфным кальция фосфатом (ACP) или аморфным кальция фторид фосфатом (ACFP). Дентальной поверхностью является предпочтительно дентальная эмаль. В одном варианте осуществления дентальная поверхность представляет собой повреждение в эмали, такое как повреждение, вызванное кариесом, дентальной эрозией или флюорозом.
Минерализация дентальных поверхностей может быть значительно усилена путем разрушения кутикулярных белков дентальной поверхности перед аппликацией реминерализующего материала, такого как стабилизированный ACP и/или ACFP. В частности, было обнаружено, что минерализация эмали посредством стабилизированных растворимых форм ACP (CPP-ACP) и ACFP (CPP-ACFP) усиливается путем предварительной обработки эмалевой поверхности белок-разрушающим агентом, таким как щелочной отбеливатель.
Предпочтительно ACP и/или ACFP является фосфопептид(PP)-стабилизированным. Предпочтительно фосфопептидом (как определено ниже) является казеиновый фосфопептид.
В предпочтительном варианте осуществления ACP и/или ACFP находятся в форме казеинового фосфопептида, стабилизированного комплексом ACP и/или ACFP.
Предпочтительно фаза ACP является преимущественно базовой фазой, где ACP включает преимущественно виды Ca2+, PO4 3- и OH-. Базовая фаза ACP может иметь общую формулу [Ca3(PO4)2]x[Ca2(PO4)(OH)], где x≥1. Предпочтительно x=1-5. Более предпочтительно x=1. Предпочтительно два компонента формулы находятся в равных пропорциях. Соответственно в одном варианте осуществления базовая фаза ACP имеет формулу Ca3(PO4)2Ca2(PO4)(OH).
Предпочтительно фаза ACFP является преимущественно базовой фазой, где ACFP включает преимущественно виды Ca2+, PO4 3- и F-. Базовая фаза ACFP может иметь общую формулу [Ca3(PO4)2]x[Ca2(PO4)F]y, где x≥1, когда y=1, или где y≥1, когда x=1. Предпочтительно y=1 и x=1-3. Более предпочтительно y=1 и x=1. Предпочтительно два компонента формулы находятся в равных пропорциях. Соответственно в одном варианте осуществления базовая фаза ACFP имеет формулу Ca3(PO4)2Ca2(PO4)F.
В одном варианте осуществления комплекс ACP состоит в основном из фосфопептидов, кальция, фосфата, гидроксидных ионов и воды.
В одном варианте осуществления комплекс ACFP состоит в основном из фосфопептидов, кальция, фосфата, фторида, гидроксидных ионов и воды.
Подробное описание изобретения
Любой приемлемый белок-разрушающий агент может быть использован в способе по настоящему изобретению. Агент необходим для уменьшения белкового барьера, сформированного над поверхностью, которая должна быть пролечена, такой как кутикула над зубами. Примеры приемлемых агентов включают отбеливатель, детергент, хаотропные агенты, такие как мочевина, высокие фосфатные концентрации, коктейли протеаз (например, эндопептидаз, протеиназ и экзопептидаз) и любой другой белок-солюбилизирующий, разрушающий или гидролизующий агент.
Примеры приемлемых отбеливателей включают натрия гипохлорит (NaOCl) и карбамид пероксидные отбеливатели. В следующем предпочтительном варианте осуществления отбеливателем является щелочной отбеливатель. В следующем предпочтительном варианте осуществления щелочным отбеливателем является NaOCl. Белок-разрушающий агент действует путем солюбилизации и частичного или полного удаления белков с дентальной поверхности, особенно белков кутикулы.
В другом аспекте настоящего изобретения предлагается способ минерализации дентальной поверхности, включающий предоставление белок-разрушающего агента и источника ACP или ACFP. В предпочтительном варианте осуществления дентальной поверхностью является эмаль.
В другом аспекте настоящего изобретения предлагается способ лечения флюороза, включающий контактирование флюоротического повреждения в зубной эмали с белок-разрушающим агентом и стабилизированным ACP и/или ACFP.
В другом аспекте настоящего изобретения предлагается способ лечения дентального кариеса, включающий контактирование кариесного повреждения в зубной эмали с белок-разрушающим агентом и стабилизированным ACP и/или ACFP.
В другом аспекте настоящего изобретения предлагается способ лечения дентальной эрозии, включающий контактирование повреждения в зубной эмали, вызванного эрозией, с белок-разрушающим агентом и стабилизированным ACP и/или ACFP.
В другом аспекте настоящего изобретения предлагается способ уменьшения повреждений в виде белых пятен на зубной эмали, включающий контактирование повреждения в виде белого пятна с белок-разрушающим агентом и стабилизированным ACP и/или ACFP.
В другом аспекте настоящего изобретения предлагается способ реминерализации повреждения в зубной эмали, включающий контактирование повреждения с белок-разрушающим агентом и стабилизированным ACP и/или ACFP.
Предпочтительно ACP и/или ACFP стабилизируют фосфопептидом. В предпочтительном варианте осуществления фосфопептидом является казеиновый фосфопептид. Предпочтительно ACP или ACFP находится в форме казеинового фосфопептида, стабилизированного комплексом ACP или ACFP.
В одном варианте осуществления белок-разрушающим агентом является NaOCl. Может быть использована концентрация NaOCl приблизительно 1-20%. Альтернативно, концентрация NaOCl составляет 1-10%. В предпочтительном варианте осуществления используют приблизительно 5% NaOCl.
Белок-разрушающий агент может контактировать с дентальной поверхностью в течение приблизительно 1-60 минут или в течение приблизительно 1-30 минут. В одном варианте осуществления белок-разрушающий агент контактирует с дентальной поверхностью в течение приблизительно 20 минут.
Предпочтительно стабилизированный ACP и/или ACFP контактирует с дентальной поверхностью в течение периода от приблизительно 1 минуты до 2 часов, или от 5 минут до 60 минут, или приблизительно 10 минут. Стабилизированный ACP и/или ACFP может быть повторно нанесен на дентальную поверхность в течение периода от 1 дня до нескольких месяцев.
В одном варианте осуществления стабилизированный ACP и/или ACFP контактирует с дентальной поверхностью после того, как дентальная поверхность была в контакте с белок-разрушающим агентом.
В предпочтительном варианте осуществления белок-разрушающий агент контактирует с дентальной поверхностью 1-60 минут, или 1-30 минут, или 1-5 минут перед контактированием дентальной поверхности со стабилизированным ACP и/или ACFP.
В другом аспекте настоящего изобретения предлагается способ минерализации зубной поверхности, включающий аппликацию комплекса ACP и/или ACFP на зубную поверхность, которая была предобработана белок-разрушающим агентом. Предпочтительно зубной поверхностью является зубная эмаль. В предпочтительном варианте осуществления зубной поверхностью является зубная эмаль, содержащая повреждение, выбранное из группы, состоящей из: одного или нескольких повреждений в виде белого пятна; флюорозного повреждения; кариесного повреждения или повреждения, вызванного зубной эрозией. В другом предпочтительном варианте осуществления белок-разрушающим агентом является отбеливатель.
В одном варианте осуществления дентальная поверхность нуждается в таком лечении. Изобретение также включает способ лечения субъекта, страдающего флюорозом, дентальным кариесом, дентиновой гиперчувствительностью или дентальным налетом.
Без связи с любой теорией или способом действия понятно, что прекондиционирование зубной эмали с белок-разрушающим агентом приводит к частичному или полному депротеинированию эмали, усиливая диффузию кальция и фосфата в субповерхностную эмаль.
Далее понятно, что лечение зубной эмали стабилизированным ACFP продуцирует фторапатит, который является более резистентным к кислотной нагрузке, чем нормальная зубная эмаль. Это может привести к зубной эмали с исключительно высокими свойствами резистентности к кариесу. Соответственно в предпочтительном варианте осуществления способ по настоящему изобретению включает стабилизированный ACFP.
«Фосфопептид» в контексте описания этого изобретения означает аминокислотную последовательность, в которой по меньшей мере одна аминокислота фосфорилирована. Предпочтительно фосфопептид включает одну или несколько аминокислотных последовательностей -A-B-C-, где A является фосфоаминовым остатком, B является любым аминокислотным остатком, включающим фосфоаминовый остаток, и C выбран из глутамилового, аспартилового или фосфоаминового остатка. Любой из фосфоаминовых остатков может независимо быть фосфосериловым остатком. B представляет желательно остаток боковой цепи, который не является ни относительно большим, ни гидрофобным. Он может быть Gly, Ala, Val, Met, Leu, Ile, Ser, Thr, Cys, Asp, Glu, Asn, Gln или Lys.
В другом варианте осуществления по меньшей мере две фосфоаминокислоты в последовательности являются предпочтительно смежными. Предпочтительно фосфопептид включает последовательность A-B-C-D-E, где A, B, C, D и E являются независимо фосфосерином, фосфотреонином, фосфотирозином, фосфогистидином, глутаминовой кислотой или аспарагиновой кислотой, и по меньшей мере две, предпочтительно три, A, B, C, D и E являются фосфоаминокислотой. В предпочтительном варианте осуществления фосфоаминокислотными остатками является фосфосерин, более предпочтительно три смежных фосфосериновых остатка. Также предпочтительно, что D и E являются независимо глутаминовой или аспарагиновой кислотой.
Также будет понятно, что термин «включает» (или его грамматические варианты), как использовано в этом описании, эквивалентен термину «содержит» и может быть использован взаимозаменяемо и не должен приниматься как исключающий присутствие других элементов или признаков.
В одном варианте осуществления ACP или ACFP стабилизируют посредством казеинового фосфопептида (CPP), который находится в форме интактного казеина или фрагмента казеина, и сформированный комплекс предпочтительно имеет формулу [CPP(ACP)8]n или [(CPP)(ACFP)8]n, где n равно или больше чем 1, например 6. Сформированный комплекс может быть коллоидным комплексом, где коровые частицы агрегируют с формированием больших (нап., 100нм) коллоидных частиц, суспендированнных в воде. Таким образом, PP может быть казеиновым белком или полифосфопептидом.
PP может быть получен из любого источника; он может быть представлен в контексте большего полипептида, включая полноразмерный казеиновый полипептид, или он может быть выделен путем триптического или другого ферментативного или химического переваривания казеина или других обогащенных фосфоаминокислотой белков, таких как фосфитин, или путем химического или рекомбинантного синтеза, при условии, что он включает последовательность -A-B-C- или A-B-C-D-E, как описано выше. Последовательность, фланкирующая эту коровую последовательность, может быть любой последовательностью. Однако те фланкирующие последовательности в αs1(59-79) [1], β(1-25) [2], αs2(46-70) [3] и αs2(1-21) [4] являются предпочтительными. Фланкирующие последовательности могут быть необязательно модифицированы путем делеции, добавления или консервативного замещения одного или нескольких остатков. Аминокислотная композиция и последовательность фланкирующей области не являются критическими.
Примеры консервативных замещений показаны в Таблице 1 ниже.
Таблица 1


Фланкирующие последовательности могут также включать не встречающиеся в природе аминокислотные остатки. Обычно встречающиеся аминокислоты, которые не кодируются генетическим кодом, включают:
2-аминоадипиновую кислоту (Aad) для Glu и Asp;
2-аминопимелиновую кислоту (Apm) для Glu и Asp;
2-аминомасляную кислоту (Abu) для Met, Leu и других алифатических аминокислот;
2-аминогептановую кислоту (Ahe) для Met, Leu и других алифатических аминокислот;
2-аминоизомасляную кислоту (Aib) для Gly;
циклогексилаланин (Cha) для Val, Leu и Ile;
гомоаргинин (Har) для Arg и Lys;
2,3-диаминопропионовую кислоту (Dpr) для Lys, Arg и His;
N-этилглицин (EtGly) для Gly, Pro и Ala;
N-этиласпарагин (EtAsn) для Asn и Gln;
гидроксилизин (Hyl) для Lys;
аллогидроксилизин (AHyl) для Lys;
3-(и 4)гидроксипролин (3Hyp, 4Hyp) для Pro, Ser и Thr;
аллоизолейцин (Alle) для Ile, Leu и Val;
п-амидинофенилаланин для Ala;
N-метилглицин (MeGly, саркозин) для Gly, Pro, Ala;
N-метилизолейцин (Melle) для Ile;
норвалин (Nva) для Met и других алифатических аминокислот;
норлейцин (Nle) для Met и других алифатических аминокислот;
орнитин (Orn) для Lys, Arg и His;
цитруллин (Cit) и метионин сульфоксид (MSO) для Thr, Asn и Gln;
N-метилфенилаланин (MePhe), триметилфенилаланин, галогено (F, Cl, Br и I) фенилаланин, трифторфенилаланин для Phe.
В одном варианте осуществления PP представляет собой один или несколько фосфопептидов, выбранных из группы, состоящей из αs1(59-79) [1], β(1-25) [2], αs2(46-70) [3] и αs2(1-21) [4].
В другом варианте осуществления по изобретению стабилизированный комплекс ACFP или ACP включают в оральные композиции, такие как зубная паста, жидкости для полоскания рта или составы для рта для обеспечения профилактики и/или лечения дентального кариеса, разрушения зуба, дентальной эрозии или флюороза. Комплекс ACFP или ACP может включать 0,01-50% по весу композиции, предпочтительно 1,0-50%. Для оральных композиций предпочтительно, что количество введенного CPP-ACP и/или CPP-ACFP составляет 0,01-50% по весу, предпочтительно 1,0%-50% по весу композиции. В особенно предпочтительном варианте осуществления оральная композиция по настоящему изобретению содержит приблизительно 2% CPP-ACP, CPP-ACFP или смеси и того и другого. Оральная композиция по этому изобретению, которая содержит вышеупомянутые агенты, может быть получена и использована в различных формах, применимых для полости рта, таких как средство для ухода за зубами, включая зубные пасты, зубные порошки и жидкие средства для ухода за зубами, жидкости для полоскания рта, пастилки, жевательные резинки, дентальные пасты, десневые массажные кремы, таблетки для полоскания, молочные продукты и другие продукты питания. Оральная композиция в соответствии с изобретением может далее включать дополнительные хорошо известные ингредиенты в зависимости от типа и формы определенной оральной композиции.
В некоторых предпочтительных формах по изобретению оральная композиция может быть в значительной степени жидкой по своему характеру, такой как жидкость для полоскания рта или жидкость для промывания. В таком препарате наполнитель обычно представляет водно-спиртовую смесь, желательно включающую увлажнитель, как описано ниже. Обычно весовое отношение воды к спирту находится в диапазоне от приблизительно 1:1 до приблизительно 20:1. Общее количество водно-спиртовой смеси в этом типе препарата находится обычно в диапазоне от приблизительно 70 до приблизительно 99,9% по весу препарата. Спиртом является обычно этанол или изопропанол. Этанол является предпочтительным.
pH такой жидкости и других препаратов по изобретению находится обычно в диапазоне от приблизительно 5 до приблизительно 9 и типично от приблизительно 5,0 до 7,0. pH может контролироваться кислотой (нап., фосфорной кислотой, лимонной кислотой или бензойной кислотой), или основанием (нап., натрия гидроксид), или буферным веществом (как в случае натрия цитрата, бензоата, карбоната или бикарбоната, гидрофосфат натрия, натрия дигидрофосфата и т.п.).
В другой желательной форме по этому изобретению стабилизированные композиции ACP или ACFP могут быть в основном твердыми или пастообразными по своему характеру, такими как зубной порошок, дентальная таблетка, зубная паста (дентальный крем) или гелевое средство для ухода за зубами. Наполнитель таких твердых или пастообразных оральных препаратов обычно содержит дентально приемлемый полирующий материал. Примерами полирующих материалов являются водонерастворимый натрия метафосфат, калия метафосфат, трикальция фосфат, двуводный кальция фосфат, безводный дикальция фосфат, кальция пирофосфат, магния ортофосфат, тримагния фосфат, кальция карбонат, гидратированный алюминий, кальцинированный алюминий, алюминия силикат, циркония силикат, кремнезем, бентонит и их смеси. Другой приемлемый полирующий материал включает измельченные термоотверждающиеся смолы, такие как меламино-, фенольные и мочевино-формальдегиды и поперечно сшитые полиэпоксиды и сложные полиэфиры. Предпочтительные полирующие материалы включают кристаллический кремнезем, имеющий размер частиц вплоть до приблизительно 5 микрон, средний размер частиц вплоть до приблизительно 1,1 микрон и площадь поверхности вплоть до приблизительно 50000 см2/г, силикагель или коллоидный кремнезем и комплекс аморфного алюминосиликата щелочного металла.
Когда используют визуально прозрачный гель, полирующий агент коллоидного кремнезема, такой как те, которые продают под торговой маркой SYLOID как Syloid 72 и Syloid 74 или под торговой маркой SANTOCEL как Santocel 100, комплексы алюминосиликата щелочного металла особенно полезны, так как они имеют коэффициенты отражения, близкие к коэффициентам отражения систем гелеобразующий агент-жидкость (включая воду и/или увлажнитель), обычно используемых в средствах для ухода за зубами.
Многие так называемые «водонерастворимые» полирующие материалы являются анионными по характеру и также включают небольшое количество растворимого материала. Так, нерастворимый натрия метафосфат может быть образован любым приемлемым способом, например, как иллюстрировано в Thorpe's Dictionary of Applied Chemistry, Volume 9, 4th Edition, p. 510-511. Формы нерастворимого натрия метафосфата, известные как соль Мадрелла и соль Карола, являются далее примерами приемлемых материалов. Эти соли метафосфата показывают только небольшую растворимость в воде и поэтому обычно относятся к нерастворимым метафосфатам (IMP). Там присутствует небольшое количество растворимого фосфатного материала в качестве примеси, обычно несколько процентов, как, например, вплоть до 4% по весу. Количество растворимого фосфатного материала, которое, как считают, включает растворимый натрия триметафосфат в случае нерастворимого метафосфата, может быть уменьшено или исключено путем промывания водой по желанию. Нерастворимый метафосфат щелочного металла обычно применяют в форме порошка с размером частиц таким, что не более чем 1% материала составляет более чем 37 микрон.
Полирующий материал обычно представлен в твердых или пастообразных композициях в весовых концентрациях от приблизительно 10% до приблизительно 99%. Предпочтительно он представлен в количестве от приблизительно 10% до приблизительно 75% в зубной пасте и от приблизительно 70% до приблизительно 99% в зубном порошке. В зубных пастах, когда полирующий материал является силикатным по природе, он обычно представлен в количестве от приблизительно 10 до 30% по весу. Другие полирующие материалы обычно представлены в количестве от приблизительно 30 до 75% по весу.
В зубной пасте жидкий наполнитель может включать воду и увлажнитель обычно в количестве в диапазоне от приблизительно 10% до приблизительно 80% по весу препарата. Глицерин, пропиленгликоль, сорбит и полипропиленгликоль являются примерами приемлемых увлажнителей/носителей. Также эффективными являются жидкие смеси воды, глицерина и сорбита. В прозрачных гелях, где коэффициент отражения является важным фактором, предпочтительно использовать приблизительно 2,5-30% в весовом отношении воды, от 0 до приблизительно 70% в весовом отношении глицерина и приблизительно 20-80% в весовом отношении сорбита.
Зубная паста, кремы и гели обычно содержат природный или синтетический загуститель или гелеобразующий агент в пропорциях от приблизительно 0,1 до приблизительно 10, предпочтительно от приблизительно 0,5 до приблизительно 5% в весовом отношении. Приемлемым загустителем является синтетический гекторит, синтетическая комбинированная глина из коллоидного магния и силиката щелочного металла, приемлемый, например, как Laponite (нап., CP, SP 2002, D), предлагаемый Laporte Industries Limited. Laponite D состоит из приблизительно по весу 58,00% SiO2, 25,40% MgO, 3,05% Na2O, 0,98% Li2O и небольшого количества воды и следов металла. Его истинное значение удельной массы составляет 2,53, и он имеет кажущуюся объемную плотность 1,0 г/мл при 8% влажности.
Другие приемлемые загустители включают ирландский мох, йота каррагенан, трагакантовую камедь, крахмал, поливинилпирролидон, гидроксиэтилпропилцеллюлозу, гидроксибутил метил целлюлозу гидроксипропил метил целлюлозу, гидроксиэтил целлюлозу (нап., доступную как Natrosol), натрия карбоксиметил целлюлозу и коллоидный кремнезем, такой как тонкоизмельченный Syloid (нап., 244). Также могут быть включены солюбилизирующие агенты, такие как увлажняющие полиолы, такие как пропиленгликоль, дипропиленгликоль и гексиленгликоль, целлозольвы, такие как метилцеллозольв и этилцеллозольв, растительные масла и воски, содержащие по меньшей мере приблизительно 12 углеродов в прямой цепи, такие как оливковое масло, касторовое масло и петролатум, и сложные эфиры, такие как амил ацетат, этил ацетат и бензил бензоат.
Понятно, что, как общепринято, оральные препараты, как правило, будут твердыми или в противоположном случае распределены в приемлемые маркированные упаковки. Так, баночка зубного эликсира будет иметь этикетку, описывающую его по существу как зубной эликсир или жидкость для полоскания рта и содержащую инструкции по его применению; и зубная паста, крем или гель должны находится, как правило, в легкосжимаемой тубе, обычно алюминиевой, освинцованной или пластиковой, или с другим устройством для сжимания, распыления или выдавливания для дозирования содержимого, содержать этикетку, описывающую его по существу как зубную пасту, гель или дентальный крем.
Органические поверхностно-активные агенты могут быть использованы в композициях по настоящему изобретению с достижением усиленного профилактического действия, содействующего достижению глубокой и полной дисперсии активного агента через ротовую полость, и представлением необходимых композиций, косметически более приемлемых. Органический поверхностно-активный материал является предпочтительно анионным, неионным или амфолитическим по природе и предпочтительно не взаимодействует с активным агентом. Его предпочтительно применяют как поверхностно-активный агент моющего материала, который придает композиции моющие и пенящие свойства. Приемлемыми примерами анионных сурфактантов являются водорастворимые соли моноглицерида моносульфатов высших жирных кислот, такие как натриевая соль моносульфатированного моноглицерида гидрогенизированных жирных кислот масла кокосового ореха, высшие алкил сульфаты, такие как натрия лаурил сульфат, алкил арил сульфонаты, такие как натрия додецил бензол сульфонат, высшие алкил сульфо-ацетаты, высшие сложные эфиры жирной кислоты и 1,2-дигидрокси пропан сульфоната и существенно насыщенные высшие алифатические ацил амиды низших алифатических соединений аминокарбоновой кислоты, такие как те, которые имеют 12-16 углеродов в жирной кислоте, алкиловые или ациловые радикалы и тому подобное. Примерами последних упомянутых амидов являются N-лауроил саркозин и натриевая, калиевая и этаноламиновая соли N-лауроил, N-миристоил или N-пальмитоил саркозина, который должен быть существенно свободен от мыльного материала или материала аналогичной высшей жирной кислоты. Применение этих сарконитных соединений в оральных композициях по настоящему изобретению является особенно выгодным, так как эти материалы проявляют пролонгированный выраженный эффект на ингибирование формирования кислоты в ротовой полости вследствие разложения углеводородов в дополнение к влиянию на некоторое снижение растворимости зубной эмали в кислых растворах. Примерами водорастворимых неионных сурфактантов, приемлемых для использования, являются продукты конденсации этилен оксида с различными реакционноспособными водород-содержащими соединениями, реагирующие, при этом имея длинные гидрофобные цепи (нап., алифатические цепи от приблизительно 12 до 20 углеродных атомов), продукты конденсации которых («этоксамеры») содержат гидрофильные полиоксиэтиленовые части, такие как продукты конденсации поли(этилен оксида) с жирными кислотами, жирными спиртами, жирными амидами, многоатомными спиртами (нап., сорбитан моностеарат) и полипропиленоксидом (нап., Плюрониловые материалы).
Поверхностно-активный агент обычно представлен в количестве от приблизительно 0,1-5% по весу. Стоит отметить, что поверхностно-активный агент может принимать участие в растворении активного агента по изобретению и тем самым уменьшать количество требуемого солюбилизирующего увлажнителя.
Различные другие материалы могут быть включены в оральные препараты по этому изобретению, такие как отбеливающие агенты, консерванты, силиконы, соединения хлорофилла и/или аммонизированный материал, такой как мочевина, диаммония фосфат и их смеси. Эти адъюванты в случае их присутствия включаются в препараты в количестве, которое не оказывает заметного вредного влияния на желательные свойства и характеристики.
Может использоваться любой приемлемый ароматизирующий или подслащивающий материал. Примерами приемлемых ароматизирующих компонентов являются ароматические масла, например масло мяты кудрявой, мяты перечной, винтергрена, сассафраса, гвоздичного дерева, шалфея, эвкалипта, майорана, коричного дерева, лимона и апельсина и метил салицилат. Приемлемые подслащивающие агенты включают сахарозу, лактозу, мальтозу, сорбит, ксилит, натрия цикламат, периллартин, AMP (аспартил фенил аланин, метиловый эфир), сахарин и тому подобное. Приемлемые ароматизирующие или подслащивающие агенты могут каждый или совместно включать от приблизительно 0,1% до 5% и более препарата.
Изобретение также предлагает композицию ACP или ACFP, как описано выше, далее включающую белок-разрушающий агент. В одном варианте осуществления белок-разрушающим агентом является отбеливатель. В предпочтительном варианте осуществления отбеливателем является NaOCl.
Композиции по этому изобретению также могут быть включены в пастилки, в жевательную резинку или другие продукты, например, путем размешивания в теплой гуммиоснове или покрытия наружной поверхности гуммиосновы, иллюстрацией которых являются джелутонг, каучуковый латекс, винилитовый полимер и т.п., желательно с соответствующими пластификаторами или умягчителями, сахаром или другими подсластителями, такими как глюкоза, сорбит и тому подобное.
В дальнейшем аспекте изобретение предлагает композиции, включающие фармацевтические композиции, включающие любой из комплексов ACFP и/или ACP, как описано выше, вместе с белок-разрушающим агентом и фармацевтически приемлемым носителем. Такие композиции могут быть выбраны из группы, состоящей из дентальных, антикариогенных композиций и терапевтических композиций. Дентальные композиции или терапевтические композиции могут быть в форме геля, жидкости, твердой фазы, порошка, крема или пастилки. Терапевтические композиции могут быть также в форме таблеток или капсул. В одном варианте осуществления комплексы ACP и/или ACFP представляют собой, в основном, только реминерализующие активные компоненты такой композиции. Например, состав крема, который может быть применен, содержит: воду; глицерин; CPP-ACP; D-сорбит; кремния диоксид; натрия карбоксиметилцеллюлозу (CMC-Na); пропиленгликоль; титана диоксид; ксилит; фосфорную кислоту; гуаровую камедь; цинка оксид; натрия сахарин; этил п-гидроксибензоат; магния оксид; бутил п-гидроксибензоат и пропил п-гидроксибензоат.
Изобретение далее включает состав, описанный выше, предлагаемый вместе с инструкциями по его применению для лечения или профилактики любого одного или нескольких дентального кариеса или разрушения зуба, дентальной эрозии и флюороза.
В одном варианте осуществления активные компоненты композиции состоят в основном из белок-разрушающего агента и стабилизированного ACP и/или ACFP. Без связи с любой теорией или способом действия понятно, что стабилизированный ACP и/или ACFP и белок-разрушающий агент являются центральными в терапевтическом или профилактическом действии вышеупомянутых вариантов осуществления по изобретению, и, таким образом, варианты осуществления, состоящие в основном из тех компонентов (с носителями, эксципиентами и тому подобное, как указано), включены в объем изобретения.
Изобретение также относится к набору для лечения или профилактики одного или нескольких дентального кариеса, флюороза и дентальной эрозии, включающему: а) белок-разрушающий агент; и б) комплекс CPP-ACP или CPP-ACFP в фармацевтически приемлемом носителе. Желательно, что набор далее включает инструкции по их использованию для минерализации дентальной поверхности у пациента, нуждающегося в таком лечении. В одном варианте осуществления агент и комплекс имеются в приемлемом количестве для лечения пациента.
В дальнейшем аспекте предлагается способ лечения или профилактики одного или нескольких, выбранных из дентального кариеса, разрушения зуба, дентальной эрозии и флюороза, включающий стадии введения белок-разрушающего агента в зубы субъекта, с последующим введением комплекса ACP или ACFP, или композиции. Топическое введение комплекса является предпочтительным. Способ предпочтительно включает введение комплекса в состав, как описано выше.
В другом аспекте предлагается использование белок-разрушающего агента для изготовления первой композиции и использование стабилизированного аморфного кальция фосфата (ACP) или аморфного кальция фторид фосфата (ACFP) для изготовления второй композиции, первая и вторая композиции использованы для лечения и/или профилактики одного или нескольких дентального кариеса, разрушения зуба, дентальной эрозии и флюороза, где первую композицию наносят на дентальную поверхность перед второй композицией.
В другом аспекте предлагается первая композиция, включающая белок-разрушающий агент, и вторая композиция, включающая стабилизированный аморфный кальция фосфат (ACP) или аморфный кальция фторид фосфат (ACFP), для лечения и/или профилактики одного или нескольких дентального кариеса, разрушения зуба, дентальной эрозии и флюороза, где первую композицию наносят на дентальную поверхность перед второй композицией.
Легко понять, что хотя это описание относится специфически к применению на людях, изобретение также полезно для ветеринарных целей. Так, во всех аспектах изобретение полезно для домашних животных, таких как крупный рогатый скот, овцы, лошади и домашняя птица; для животных-компаньонов, таких как кошки и собаки; и для животных зоопарков.
Изобретение описано далее со ссылками на следующие неограниченные примеры.
Одним примером минерализующей композиции является композиция, включающая следующее (в порядке снижения пропорции):
воду,
глицерин,
CPP-ACP,
D-сорбит,
кремния диоксид,
натрия карбоксиметилцеллюлозу (CMC-Na),
пропиленгликоль,
титана диоксид,
ксилит,
фосфорную кислоту,
гуаровую камедь,
цинка оксид,
натрия сахарин,
этил п-гидроксибензоат,
магния оксид,
бутил п-гидроксибензоат,
пропил п-гидроксибензоат.
Такая композиция доступна от GC корпорации под названием Tooth MousseTM. Она приемлема для использования после белок-разрушающего агента и находится в форме пасты или крема для облегчения ее задержки на зубах в течение приемлемого периода. Альтернативно, эта минерализующая композиция может содержать белок-разрушающий агент, такой как натрия гипохлорит.
Эффективность изобретения может быть продемонстрирована следующим образом.
Семь премолярных зубов с FLE (Thylstrup Fejerskov Индекс, TF=3) выбрали из зубов, удаленных по ортодонтическим причинам у здоровых пациентов в возрасте 10-28 лет из Королевской стоматологической больницы Мельбурна, Австралия. Для удаленных зубов получили информированное согласие пациента, и протокол исследования утвердил Комитет по этике исследований на человеке Университета Мельбурна. Все образцы очищали от приросшей мягкой ткани и хранили в 18% вес/объем растворе формалин ацетата при комнатной температуре.
Зубы очищали вращающейся резиновой чашечкой и шлифовали пемзой, промывали в двукратно деионизированной воде (DDW) (Fejerskov с сотр., 1988). Анатомические коронки отделяли от корней с использованием водоохлаждаемого диска с алмазной режущей коронкой. Каждую коронку разделяли с обеспечением пары эмалевых блоков, каждый из которых содержал FLE. Над каждым повреждением создавали окно 4х4 мм2 путем помещения прямоугольного кусочка Parafilm® (American National Can, Чикаго, III, США) над повреждением и покрывали соответствующей эмалью лака для ногтей (RevlonTM, Нью-Йорк, США). Парафильм затем осторожно удаляли с раскрытием окна эмалевого повреждения, которое разделили пополам как контрольное и тестируемое окна. Контрольное окно покрывали лаком для ногтей. Два повреждения каждого образца рандомизированно определяли в одну из двух реминерализованных групп; Группа I - обработка 5% CPP-ACFP и Группа II - обработка 5% CPP-ACFP с немедленным последующим прекондиционированием с 5,25% NaOCl.
CPP-ACFP был получен от Recaldent Pty Ltd (Мельбурн, Австралия) и содержал 47,6% в весовом отношении CPP, 15,7% в весовом отношении Ca2+, 22,9% в весовом отношении PO4 3- и 1,2% в весовом отношении F-. CPP-ACFP растворяли в дистиллированной и деионизированной воде в 5% вес/объем и регулировали до pH 7,0 с помощью HCl. Для первой группы каждый образец помещали в 2 мл 5% вес/объем CPP-ACFP в пластиковую пробирку на 5 мл при 37°C. Раствор CPP-ACFP меняли ежедневно в течение 10 дней. Для второй группы каждый образец помещали в 5,25% раствор NaOCl в течение 20 мин, промывали и затем помещали в 2 мл 5% вес/объем CPP-ACFP в пластиковую пробирку на 5 мл при 37°C. Раствор CPP-ACFP меняли ежедневно в течение 10 дней.
Chroma Meter (Minolta ChromaMeter CR241, Минолта, Япония) использовали для регистрации поверхностного отражения. Измерение поверхностного отражения было определено в L*a*b* цветовом пространстве Comission de L'Eclairage в 1978 и измерено относительно человеческого цветовосприятия в трех цветовых измерениях (Comission Internationale de L'Eclaige, 1978). L* значения представляют цветовые градиенты от белого до черного, a* значения представляют цветовые градиенты от зеленого до красного, и b* значения представляют цветовые градиенты от голубого до желтого (Comission Internationale de L'Eclaige, 1978). Только измерения L* значений использовали в этом исследовании с белыми цветами, имеющими более высокое показание, и темными цветами, имеющими более низкое показание. Для обеспечения воспроизводимого положения образцов в Chroma Meter для каждого образца получили и хранили восковую матрицу. Все образцы сушили на воздухе дентальным шприцем из трех частей в течение 60 сек перед каждой обработкой. Индивидуальные образцы перемещали десять раз до и после обработки и регистрировали L* значения цветовой отражающей способности.
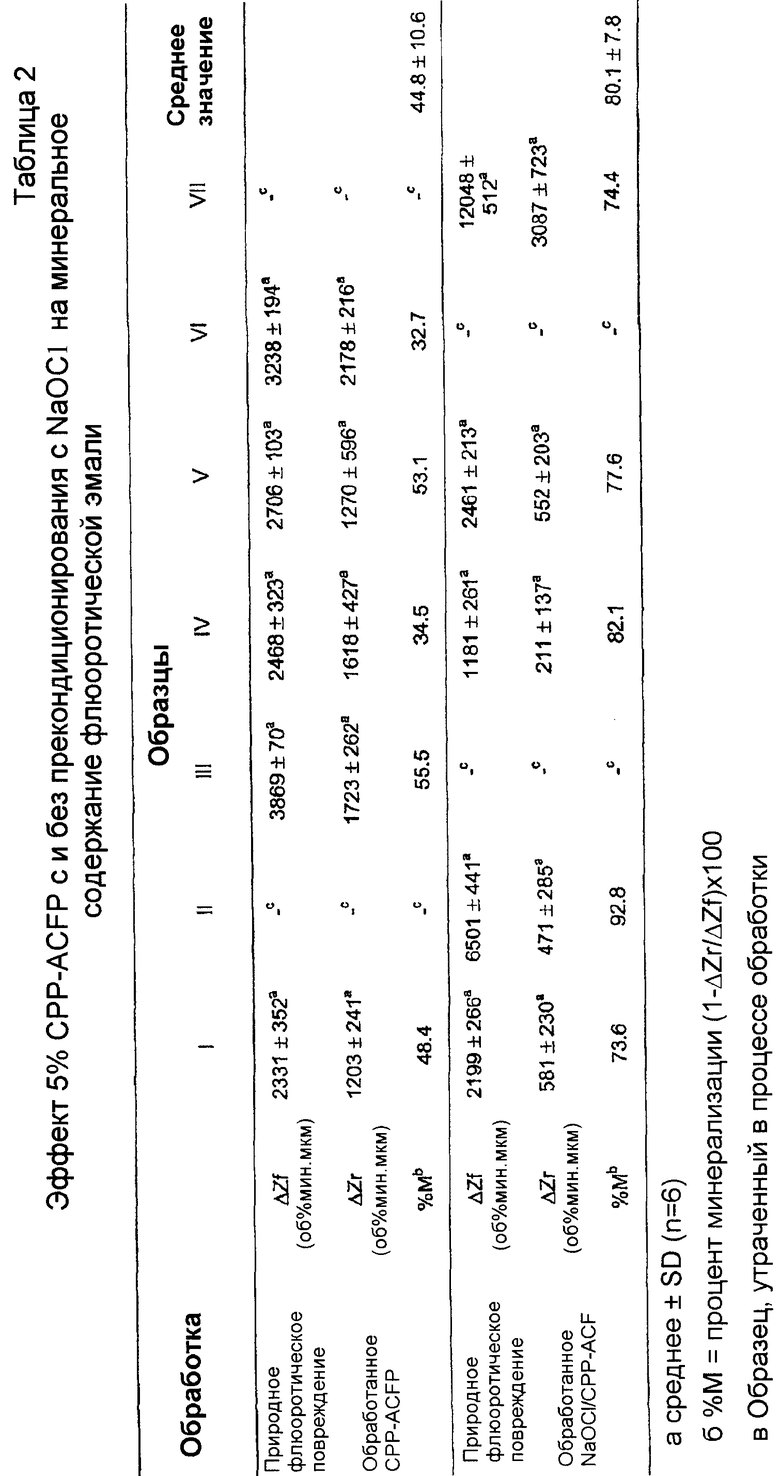
Каждый образец удаляли из минерализующего раствора и промывали в DDW в течение 60 сек, пятна сушили фильтровальной бумагой. Лак для ногтей с контрольного окна осторожно удаляли ацетоном. Контрольное и тестируемое окна затем разделяли путем разрезания через среднюю линию между окнами. Два полублока с поврежденными окнами затем помещали параллельно и заливали на холоде отверждающейся метакрилатной смолой (Paladur, Heraus Kulzer, Германия). Два спаренных эмалевых полублока затем разрезали на срезы и подвергали микрорадиографии и микроденситометрическому анализу изображения с определением минерального содержания, именно так, как описано Shen с сотр. (2001).
Область, свободную от дефектов, рядом со средней линией каждого микрорадиографического изображения каждого повреждения (контрольного и тестируемого) выбирали и сканировали шесть раз (Shen с сотр., 2001). Каждое сканирование включало 200 показаний, снятых с эмалевой поверхности в середине эмалевой области с включением общего флюоротического повреждения. Тестируемое (CPP-ACFP-обработанное) повреждение сканировали точно на такую же глубину, что и контрольное (необработанное) повреждение. Уровни яркости, полученные от каждого сканирования, конвертировали в эквивалентную толщину алюминия (tA) с использованием изображения алюминиевого ступенчатого клина, включенного в каждый срез (Shen с сотр., 2001). С использованием формулы Ангмара с сотр. (1963) процентный объем минерала получали для каждого показания следующим образом: V=(52,77(tA)-4,54)/tS, где: V = объем минерала как процента; tA = относительная толщина алюминия, полученная от сканирования уровня яркости; и tS = толщина среза (80 мкм).
Из денситометрического профиля [(об.% мин против глубины повреждения (мм)] для каждого повреждения значения DZ рассчитали с использованием интегрирования методом трапеций (Reynolds, 1997). Различие между площадью под профилем необработанной флюоротической эмали в контрольном окне и соседней нормальной эмалью обозначили DZf и различие между площадью под CPP-ACFP-обработанной флюоротической эмалью в тестируемом окне и соседней нормальной эмалью обозначили DZr. Процент минерализации (%M) флюоротического повреждения составил соответственно (1-DZr/(DZf) 100 (Reynolds, 1997).
После микрорадиографии срезы, содержащие контрольные и минерализованные FLE, подвергли энергодисперсионному рентгено-спектральному анализу (EDAX), как описано ранее (Reynolds, 1997).
Средние L* значения сравнивали с использованием анализа односторонней классификации дисперсии (ANOVA) с множественным сравнением Шеффе. Средние %M значения также сравнивали с использованием односторонней классификации ANOVA. Общие средние L* и %M значения анализировали с использованием двустороннего критерия Стьюдента.
L* значения необработанных флюоротических эмалевых повреждений колебались от 79,1 до 87,8 со средним значением 83,6±3,6 (Таблица 1). Обработка 5% CPP-ACFP достоверно снижала L* значение до 74,6±4,1, которое недостоверно отличалось от такового нормальной эмали (Таблица 1). Прекондиционирование с NaOCl с последующей обработкой 5% CPP-ACFP достоверно снижало L* значение до 72,6 ± 5,6, которое также недостоверно отличалось от такового нормальной эмали (Таблица 1). Отсутствовали достоверные различия в L* значениях для двух групп с постобработкой (CPP-ACFP и NaOCl/CPP-ACFP). Внешний вид поверхности эмали обеих обработанных групп существенно улучшился с проявлением у обеих внешнего вида нормальной полупрозрачной эмали.
Различие между минеральным содержанием интактной эмали и таковой с предобработкой повреждений (DZf) варьировало от 426 до 12,048 об.% мин мм (Таблица 2). Не выявлено корреляции между поверхностным отражением (L*) и DZf необработанного FLE. Обработка 5% CPP-ACFP индивидуально существенно увеличивала минеральное содержание флюоротических повреждений с восстановлением от 32,7% до 55,5% недостающего минерала со средним значением 44,8±10,6% (Таблица 2). Восстановление 100% недостающего минерала конвертировало бы полное повреждение в интактную эмаль по отношению к минеральному содержанию. Прекондиционирование эмали с NaOCl перед обработкой CPP-ACFP увеличивало минеральное поглощение от 73,6% до 92,8% недостающего минерала со средним значением 80,1±7,8 (Таблица 2). Энергодисперсионный рентгено-спектральный анализ минерализованного повреждения поперечных срезов подтвердил, что минерал, сформированный обработкой CPP-ACFP, представлял собой фторидсодержащий апатит.

В клинике в качестве примера пациента, нуждающегося в лечении реминерализацией зубной эмали, лечили с использованием стадий:
1. Предобработка эмалевой области, нуждающейся в лечении, выделенной с использованием резиновой чашечки, 5% раствором в течение 5 минут.
2. Удаление раствора NaOCl с области влажной ватной палочкой.
3. Нанесение CPP-ACFP-содержащего топического крема Tooth MousseTM (GC Корпорация) на эмалевую поверхность немедленно в течение 5 минут, и затем пациент в дальнейшем наносит Tooth MousseTM на ночь без ополаскивания в течение четырех недель.
Понятно, что изобретение, раскрытое и определенное в этом описании, распространяется на все альтернативные комбинации двух или нескольких индивидуальных особенностей, упомянутых или очевидно вытекающих из текста или чертежей. Все эти различные комбинации являются различными альтернативными аспектами изобретения.
ССЫЛКИ



Группа изобретений относится к области медицины, а именно к стоматологии. Предлагается способ минерализации эмали зубов, включающий контактирование зубной эмали или повреждения в зубной эмали с белок-солюбилизирующим, белок-разрушающим или белок-гидролизующим агентом перед контактированием зубной эмали с фосфопептид-стабилизированным аморфным кальция фосфатом (АСР) или аморфным кальция фторид фосфатом (ACFP). Фосфопептидом предпочтительно является казеиновый фосфопептид (СРР). Белок-солюбилизирующий, белок-разрушающий или белок-гидролизующий агент выбирают из одного или нескольких веществ группы, состоящей из отбеливателя, детергента, хаотропного агента, протеазы или смеси протеаз. Предпочтительно используют отбеливатель, такой как натрия гипохлорит или пероксид карбамида. Также предлагаются способы минерализации гипоминерализованных повреждений в зубной эмали, вызванных кариесом зубов, флюорозом, дентальной эрозией, и набор для лечения и профилактики указанных состояний, включающий: а) белок-солюбилизирующий, белок-разрушающий или белок-гидролизующий агент и б) комплекс СРР-АСР или CPP-ACFP в фармацевтически приемлемом носителе. При осуществлении способов достигается эффективное восстановление содержания недостающего минерала в зубной эмали, имеющей гипоминерализованные повреждения. 7 н. и 3 з.п. ф-лы, 3 табл.
1. Способ минерализации дентальной эмали, включающий контактирование дентальной эмали или повреждения в дентальной эмали с белок-солюбилизирующим, белок-разрушающим или белок-гидролизующим агентом перед контактированием дентальной эмали с фосфопептид-стабилизированным аморфным кальция фосфатом (АСР) или аморфным кальция фторид фосфатом (ACFP), причем указанный агент выбран из одного или нескольких веществ группы, состоящей из отбеливателя, детергента, хаотропного агента, протеазы или смеси протеаз.
2. Способ по п.1, где повреждение вызвано дентальным кариесом, дентальной эрозией или флюорозом.
3. Способ по п.1, где фосфопептидом является казеиновый фосфопептид.
4. Способ по п.1, где отбеливателем является натрия гипохлорит или карбамид пероксидный отбеливатель.
5. Способ реминерализации повреждения в зубной эмали, включающий контактирование повреждения с белок-солюбилизирующим, белок-разрушающим или белок-гидролизующим агентом перед контактированием дентальной эмали с фосфопептид-стабилизированным АСР и/или ACFP, причем указанный агент выбран из одного или нескольких веществ группы, состоящей из отбеливателя, детергента, хаотропного агента, протеазы или смеси протеаз.
6. Способ лечения флюороза, включающий контактирование повреждения с белок-солюбилизирующим, белок-разрушающим или белок-гидролизующим агентом перед контактированием дентальной эмали с фосфопептид-стабилизированным АСР и/или ACFP, причем указанный агент выбран из одного или нескольких веществ группы, состоящей из отбеливателя, детергента, хаотропного агента, протеазы или смеси протеаз.
7. Способ лечения дентального кариеса, включающий контактирование повреждения с белок-солюбилизирующим, белок-разрушающим или белок-гидролизующим агентом перед контактированием дентальной эмали с фосфопептид-стабилизированным АСР и/или ACFP, причем указанный агент выбран из одного или нескольких веществ группы, состоящей из отбеливателя, детергента, хаотропного агента, протеазы или смеси протеаз.
8. Способ лечения дентальной эрозии, включающий контактирование повреждения с белок-солюбилизирующим, белок-разрушающим или белок-гидролизующим агентом перед контактированием дентальной эмали с фосфопептид-стабилизированным АСР и/или ACFP, причем указанный агент выбран из одного или нескольких веществ группы, состоящей из отбеливателя, детергента, хаотропного агента, протеазы или смеси протеаз.
9. Способ уменьшения повреждений в виде белых пятен на зубной эмали, включающий контактирование повреждения с белок-солюбилизирующим, белок-разрушающим или белок-гидролизующим агентом перед контактированием дентальной эмали с фосфопептид-стабилизированным АСР и/или ACFP, причем указанный агент выбран из одного или нескольких веществ группы, состоящей из отбеливателя, детергента, хаотропного агента, протеазы или смеси протеаз.
10. Набор для лечения или профилактики одного или нескольких из дентального кариеса, флюороза и дентальной эрозии, включающий: а) белок-солюбилизирующий, белок-разрушающий или белок-гидролизующий агент; и б) фосфопептид-стабилизированный комплекс АСР или ACFP в фармацевтически приемлемом носителе, где белок-солюбилизирующий, белок-разрушающий или белок-гидролизующий агент наносится перед контактированием дентальной эмали с фосфопептид-стабилизированным АСР и/или ACFP, причем указанный агент выбран из одного или нескольких веществ группы, состоящей из отбеливателя, детергента, хаотропного агента, протеазы или смеси протеаз.
| US 20020028251 A1, 07.03.2002 | |||
| WO 9840406 A1, 17.09.1998 | |||
| D.INABA et al | |||
| Effect of Sodium Hypochlorite Treatment on Remineralization of Human Root Dentine in vitro, Caries Research, 1996, 30 (3), p.218-224 | |||
| СПОСОБ ИЗМЕРЕНИЯ ПЛОЩАДЕЙ ДЕТАЛЕЙ, ВЫПОЛНЕННЫХ ИЗ ЭЛЕКТРОПРОВОДНОГО МАТЕРИАЛА, В ЧАСТНОСТИ, ЭКВИВАЛЕНТНЫХ ПЛОЩАДЕЙ ПОКРЫТИЯ ДЕТАЛЕЙ ПРИ ГАЛЬВАНОТЕХНИЧЕСКИХ ПРОЦЕССАХ | 1954 |
|
SU100558A1 |
| US 4522805 A, 11.06.1985 | |||
| GINIGER M | |||
| et al | |||
| The clinical performance of professionally dispensed bleaching gel with | |||
Авторы
Даты
2011-03-10—Публикация
2006-06-07—Подача