Перекрестные ссылки
Настоящая заявка испрашивает приоритет по заявке на патент №60/572,650, поданной в США 18 мая 2004 г.
Область техники, к которой относится изобретение
Настоящее изобретение относится в общем к медицинским устройствам постоянной установки, например стентам, катетерам, трубкам и другим вспомогательным инструментам, которые остаются в теле пациента продолжительные периоды времени и вызывают проблемы бактериального загрязнения и биосовместимости. В частности, изобретение относится к системам для защиты поверхностей от нежелательных микроорганизмов и остатков органических веществ. Устройство «постоянной установки» представляет собой устройство, которое устанавливают и оставляют на месте в течение продолжительных периодов, например на пятнадцать минут или на большее время. Термин «бактерия» в настоящем описании охватывает бактерии, вирусы, грибы и другие биоактивные материалы.
Изобретение применимо к уринальным катетерам, трахеальным, сердечным, центральным и другим венозным катетерам, имплантатам и другим медицинским вспомогательным инструментам. Изобретение пригодно также для применения для трубок, которые орошают или дренируют полости тела, например (без исключения) плевральную, брюшинную и интратрахеальную полости.
Обзор состояния техники
Настоящее изобретение в первую очередь предназначено для решения проблем, которые обусловлены накоплением засоряющих осадков и контаминирующих бактерий на постоянном катетере или других имплантатах. В частности, настоящее изобретение касается проблем образования, роста и миграции микроорганизмов и загрязнителей на устройствах постоянной установки, и в частности на поверхностях катетеров.
Известно, что образование бактериальной биопленки на медицинских устройствах (катетерах, питающих трубках, эндотрахеальных трубках, системах внутривенного вливания и т.д.) является главным источником внутрибольничной инфекции. Образование биопленки на имплантированных устройствах, например уринальных катетерах, эндотрахеальных трубках, гастростомических питательных трубках и системах внутривенного вливания, указывает на присутствие бактерий, которые являются главной причиной внутрибольничных инфекций. Данные инфекции часто вызывают серьезные осложнения и приводят к увеличению смертности, продолжительности пребывания в больницах и расходов на лечение. По консервативной оценке исследователей медицинского колледжа шт. Виргиния, приведенной в Emerging Infectious Diseases, vol.7, no.2, March-April 2001, от 875000 до 3,5 миллионов человек получают внутрибольничные инфекции ежегодно в больницах США.
В последние несколько лет стало очевидным, что около 80% всех бактериальных инфекций обусловлены образованием бактериальных сообществ, организованных в созданную ими матрицу. Матрица придает атибиотикорезистентность и препятствует очищению иммунной системой. Для создания таких сообществ бактерии сообщаются между собой химическими сигналами. Первый этап образования биопленки на поверхностях медицинских устройств начинается с прикрепления бактерий к поверхности. Затем следует общение между членами сообщества, называемое определением кворума. Поскольку данный процесс зависит от прикрепления, то очевидно, что предотвращением прикрепления можно предотвратить последовательное образование биопленки.
Резистентность биопленок очень сильно влияет на стоимость медицинского ухода и лечения. Предлагались различные решения, например покрытие устройств ионами серебра или антибиотиками. Данные решения являются недолговечными; вымывание антибиотика или ионов серебра блокируется секретами слизистых оболочек и коагулированием остатков органических веществ. В некоторых публикациях сообщается, что ультразвуковая обработка биопленок повышает эффективность антибиотиков.
Предотвращение или снятие отложения прикреплением традиционных ультразвуковых излучателей к медицинскому устройству описано в работе Qian, Sagers and Pitt, The Role of Insonation Intensity in Acoustic Enhanced Antibiotic Treatment of Bacterial Biofilms, Colloids Surfaces B: Bacferiol, 1994; 176; 2773-2780. Рыночные излучатели по определению обеспечивают только одну форму колебаний в данный момент времени: продольные или торсионные, или изгибные. Традиционные излучатели являются крупными, дорогими и лимитирующими. Их присоединение к медицинским устройствам является очень сложным. Данные излучатели предназначены для создания объемных колебаний (в дополнение к поверхностным колебаниям), которые требуют больших количеств энергии. Энергия теряется в форме тепла в массе устройства. К настоящему времени способы противодействия данному источнику медицинских осложнений с их слишком высокими экономическими последствиями оказались далеко не удовлетворительными. Главным препятствием более широкого применения устройств постоянной установки является неотъемлемый риск инфекций, связанных с их применением. Ожидается, что снижение риска откроет целый новый ряд возможностей и применение технологии практически во всех устройствах постоянной установки.
Сущность изобретения
Образование бактериальных сообществ на поверхностях, например, медицинских устройств зависит от общения между членами сообщества. Данное общение осуществляется посредством химических молекул, вырабатываемых микроорганизмами. Вышеописанное следует рассматривать как активный биологический процесс.
Нановибрации, передаваемые и распространяющиеся по поверхностям медицинских устройств и вблизи них, препятствуют биологическому процессу. В результате образующаяся характеристика внеклеточной матрицы данных сообществ, известной как биопленка, менее выражена. Внеклеточная матрица состоит в основном из полисахаридов, которые делают бактерии резистентными к иммунной системе, и антибиотикам, и дезинфектантам.
Принцип нашей технологии основан на поверхностных акустических волнах (SAW). Развернутые эксперименты в лабораториях фирмы авторов показывают, что с помощью поверхностных акустических волн (SAW), в частности нановибраций, можно добиться предотвращения прикрепления бактерий, так как микроорганизмы не находят поверхности пленки для прикрепления к ней.
Поверхностные акустические волны (как Релея, так и псевдо-SAW) можно возбуждать на свободной поверхности упругого твердого тела (медицинского устройства). Рассмотрим распространение волны Релея по упругой поверхности, что можно соотнести механически с зависимым от времени эллиптическим движением поверхностной структуры. Одна составляющая данного физического движения параллельна оси распространения SAW, а другая является нормальной к поверхности. Расстояние x связано с осью распространения SAW, а y является нормальной осью в системе координат. Амплитуда движения поверхности по оси y больше, чем по оси x распространения SAW. Амплитуды обеих данных составляющих движения SAW становятся ничтожно малыми при глубине проникновения вглубь твердого тела свыше нескольких длин акустических волн. Давление (наполнение газом или жидкостью) способствует затуханию акустической волны и изменению скорости. Затухание обусловлено формированием волн сжатия в газе или жидкости в месте контакта с поверхностью, подводящей SAW. Другими словами, сдвиговая вертикальная составляющая волны вызывает периодические сжатие и разрежение газа или жидкости и в результате ввод акустической энергии из устройств в газ или жидкость. Ослабление линейно зависит от акустического давления. В случае уринального катетера, в котором биопленка образуется как на внешней, так и на внутренней поверхностях, желательно обеспечить равномерное распределение SAW на обеих поверхностях. Предлагаемое изобретение использует тонкий пьезоэлемент в качестве резонатора для генерации и распределения SAW. Данный резонатор обеспечивает следующие преимущества:
1. Небольшая потребность в энергии, допускающая широкое применение облегченных аккумуляторных батарей;
2. Меньшие масса и габариты пьезоэлемента облегчают сопряжение с существующими медицинскими устройствами без потребности в дополнительном пространстве, и поэтому не требуется существенных модификаций стандартных медицинских устройств;
3. Данные элементы являются экономичными и допускают удаление в отходы в конце их использования;
4. Благодаря миниатюрному размеру, предлагаемый пьезоэлемент не сказывается на гибкости медицинских устройств;
5. Миниатюрный размер предлагаемого пьезоэлемента позволяет применять, по меньшей мере, один элемент в одном устройстве и способствует их массовому производству.
Развернутые эксперименты в лабораториях фирмы авторов показывают, что с помощью поверхностных нановибраций можно воспрепятствовать развитию бактерий. Микроорганизмы не находят поверхности пленки для прикрепления в вышеописанном цикле, поэтому не могут распространяться, и данный цикл обрывается. Эффект распространяется на окружающие области протяженностью до нескольких сантиметров, и биопленка не допускается не только на устройстве, но также на соседних тканях. Длина волны вибраций и акустическая энергия являются решающими факторами при получении антимикробного действия. На поверхности наросшего материала, а также на чистой поверхности создается виртуальное нановибрационное покрытие. Иногда отложение происходит в присутствии высоких концентраций твердых частиц (что дает в результате высоковязкое липкое вещество). Устройство оказывается покрытым слоями твердых частиц. В данном случае создание отложений не препятствует образованию виртуального нановибрационного покрытия на поверхности материала отложения.
Кроме того, предлагаемое изобретение относится к биоматериалам и биосовместимости. Биоматериал определяют как естественное или синтетическое вещество, применяемое при лечении пациента, которое контактирует с тканью на некоторой стадии и связано с осложнениями. Исследователи считают, что необходимо оптимизировать биосовместимость и ослабить вызываемые биоматериалами осложнения, например инфицирование и образование корки в мочевыводящем пути, сосудистой системе и других органах, связанных с имплантатами. Процесс осаждения и образования кристаллов кинетически ускоряется в присутствии неровных поверхностей, отверстий под катетеры и кромок. В соответствии с предлагаемым изобретением посредством генерации поверхностных акустических волн возбуждается вибрация структуры материала, что приводит к уменьшению трения по биоматериалу. Данное явление улучшает биосовместимость благодаря ослаблению вызванного трением раздражения и прилипания клеток на границе между биоматериалом и тканью.
Кроме того, установлено, что ультразвук влияет на антибиотическую активность и требуется меньше антибиотика для получения искомого результата. Именно поэтому возбуждение SAW на поверхностях имплантата или медицинского устройства постоянной установки будет активировать антибиотическое действие. В соответствии с предложенным изобретением подача SAW в медицинские устройства открывает возможность ослабить трение, сократить применение антибиотиков и повысить эффективность лекарственных средств, применяемых с медицинскими устройствами постоянной установки. Данные эффекты важны для биосовместимости материалов и ослабляют вызываемые биоматериалами осложнения, например инфицирование и образование корки.
Краткое описание чертежей
Принципы и действие системы, устройства и способа в соответствии с настоящим изобретением становятся понятнее из чертежей и нижеследующего описания, однако следует помнить, что данные чертежи предназначены только для иллюстрации и не предполагают ограничений, при этом:
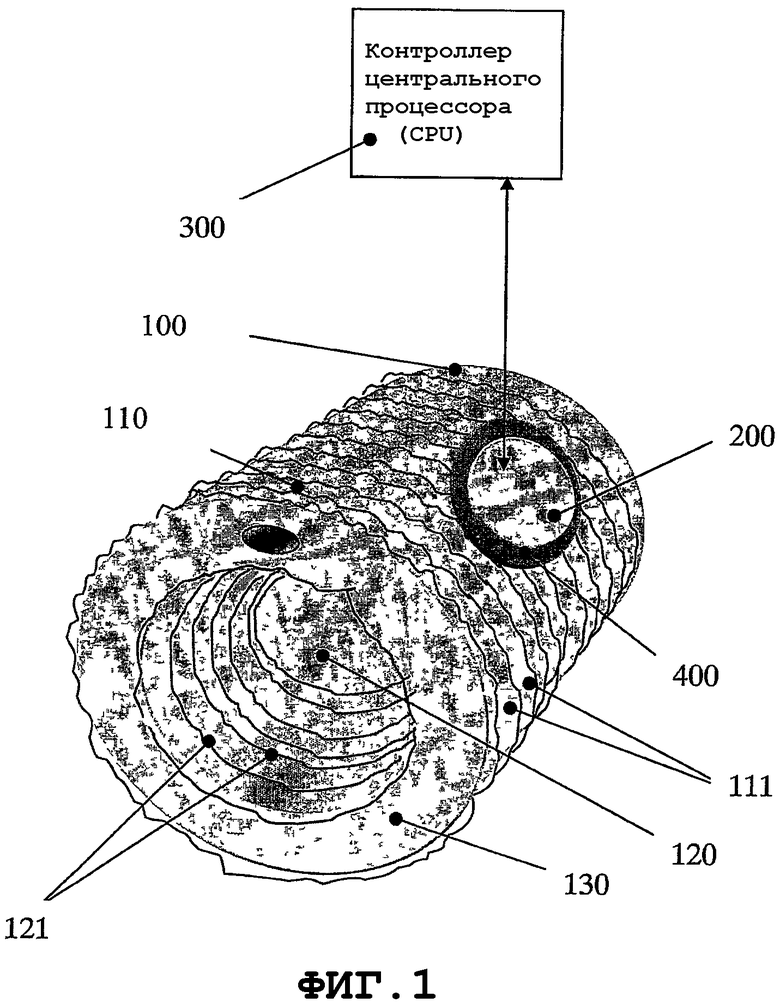
на фиг.1 схематично показаны тонкий механический вибрационный элемент и коммутирующее устройство для распространения упругих акустических продольных волн в системе медицинского устройства при покрытии нановибрациями внешней и внутренней поверхностей для предотвращения образования биопленки и/или уничтожения биопленочных образований, где тонкая пьезоэлектрическая керамика содержит электроды, по меньшей мере, одной формы на внутренней и внешней поверхностях, в соответствии с некоторыми вариантами осуществления настоящего изобретения;
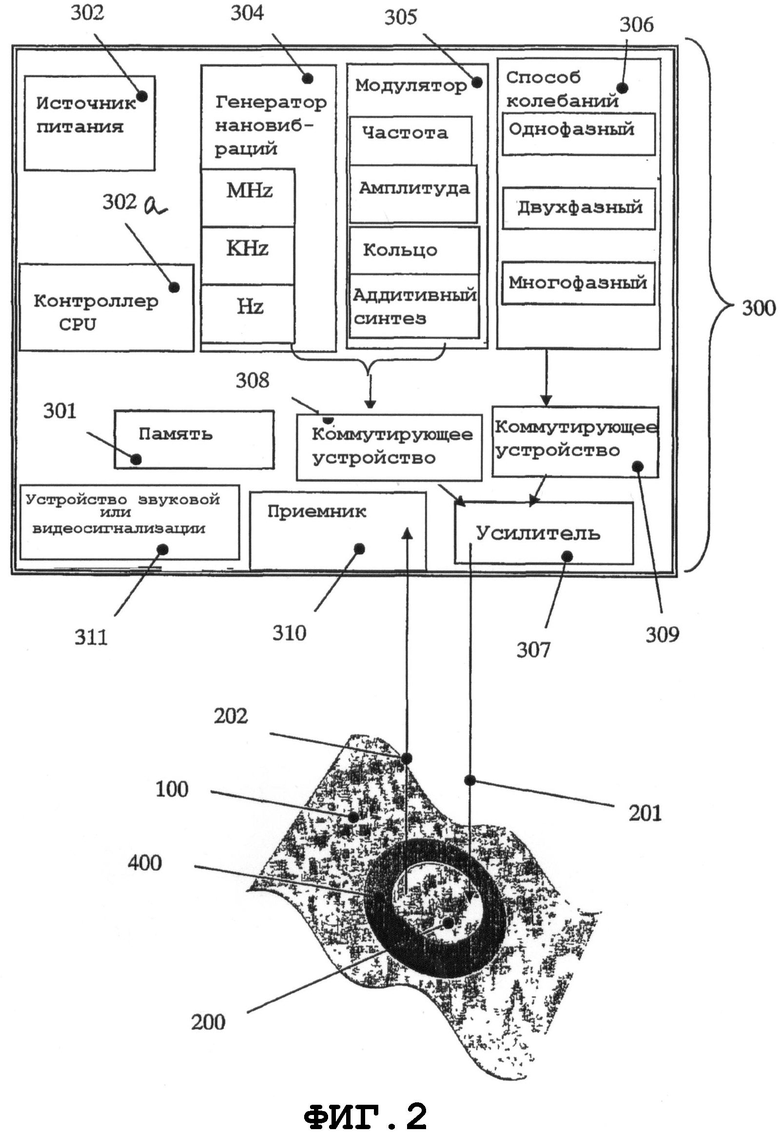
на фиг.2 схематично показаны тонкий механический вибрационный элемент и коммутирующее устройство для распространения упругих акустических продольных волн в системе медицинского устройства при покрытии нановибрациями внешней и внутренней поверхностей для предотвращения образования биопленки и/или уничтожения биопленочных образований, где тонкая пьезоэлектрическая керамика содержит электроды, по меньшей мере, одной формы на внутренней и внешней поверхностях, в соответствии с некоторыми вариантами осуществления настоящего изобретения;
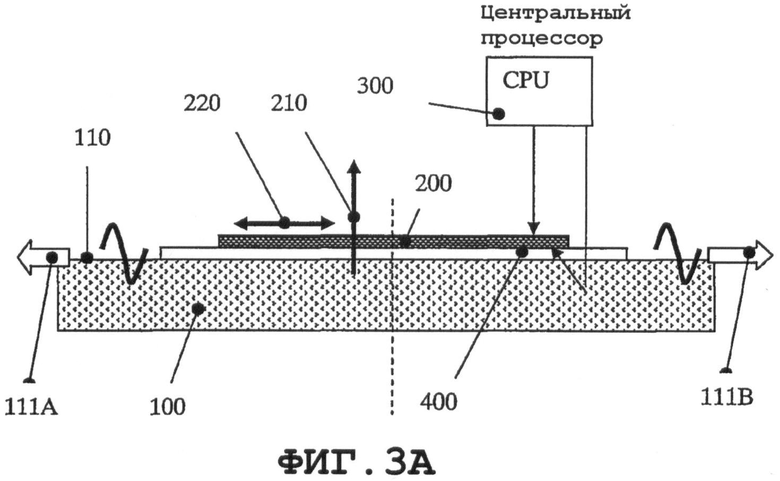
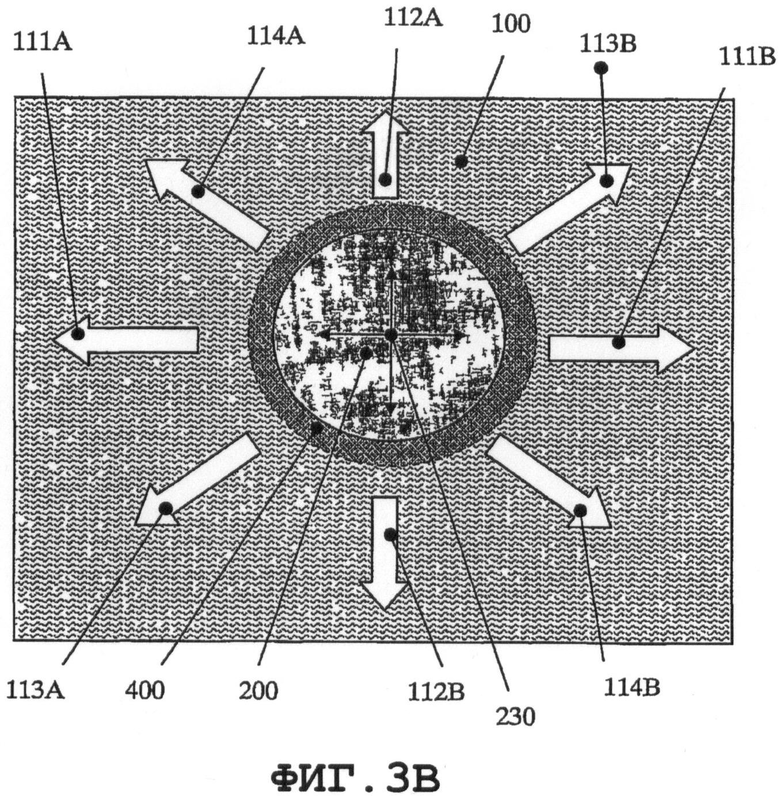
на фиг.3А-3В схематично показано направление поверхностных акустических волн на внешней поверхности медицинского устройства, когда применяют продольные колебания тонкого пьезоэлемента;
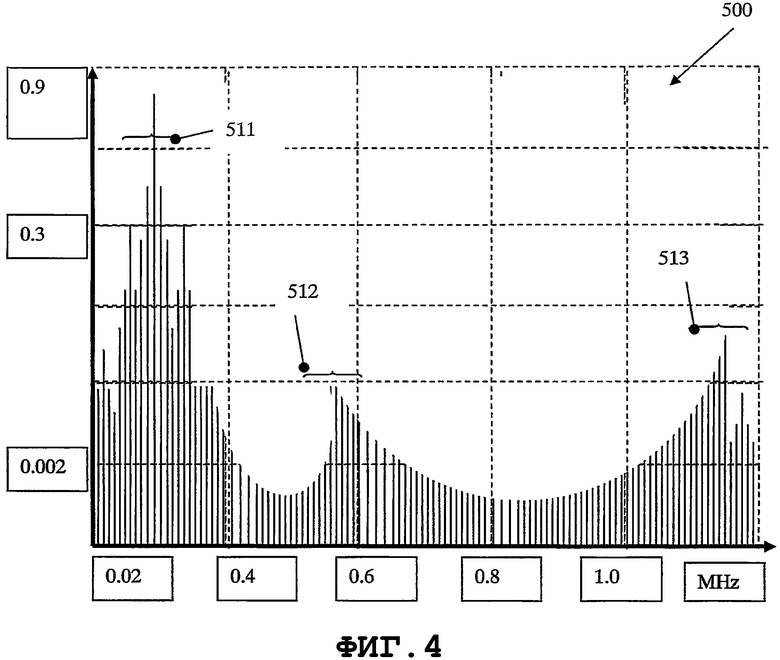
на фиг.4 схематично показана спектральная диаграмма SAW в медицинском устройстве, когда используют моду продольных автоколебаний тонкого пьезоэлемента для предотвращения образования биопленки и/или уничтожения биопленочных образований, в соответствии с некоторыми вариантами осуществления настоящего изобретения;
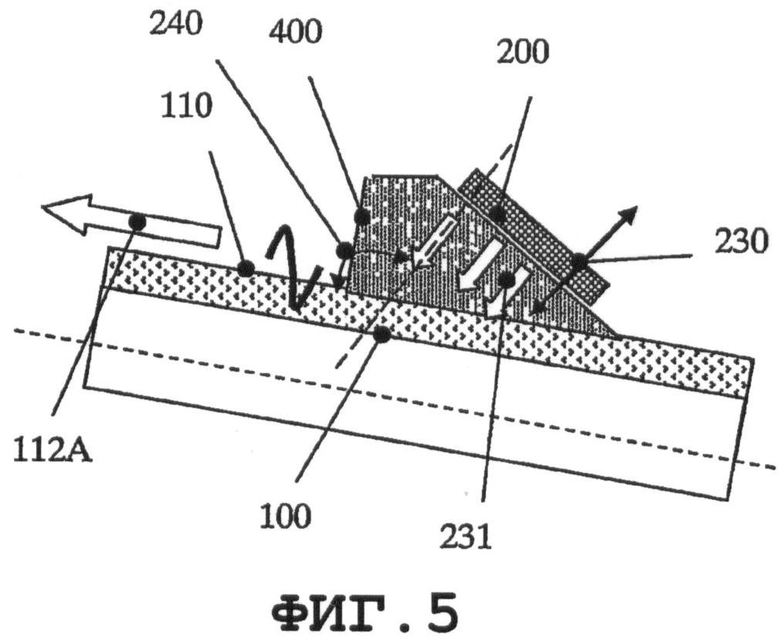
на фиг.5 схематично показаны направления SAW при применении колебаний по толщине тонкого пьезоэлемента;
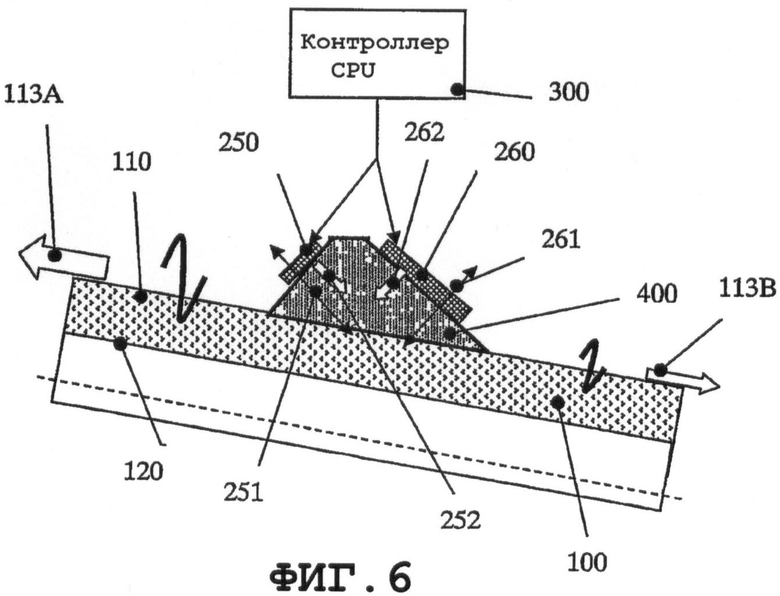
на фиг.6 схематично показан SAW-процесс, когда относительно резонатора данный процесс сильнее в положительном направлении, чем в противоположном направлении (два резонатора на тонком пьезоэлементе присоединены к системе связи, и резонатор совершает колебания по толщине);
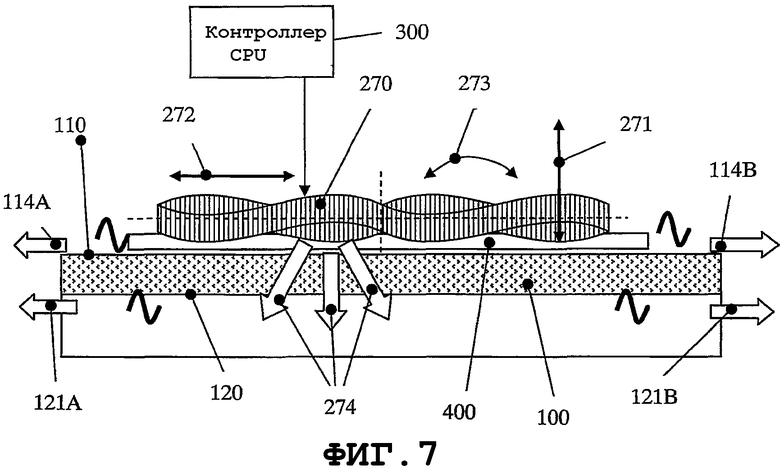
на фиг.7 схематично показан способ, в котором резонатор присоединяют на внешней, или внутренней, или торцевой поверхности медицинского устройства для проведения управляемых SAW-процессов на данных поверхностях (тонкий пьезорезонатор возбуждают для колебания одновременно на трех модах колебаний: изгибных, продольных и по толщине);
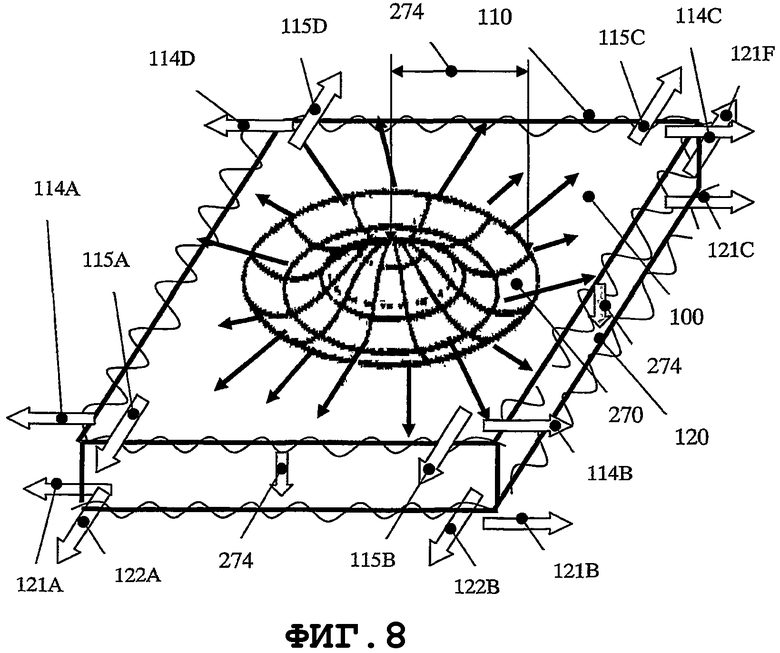
на фиг.8 изображена круглая тонкая пьезоэлектрическая мембрана, совершающая колебания изгибной (собственной) моды;
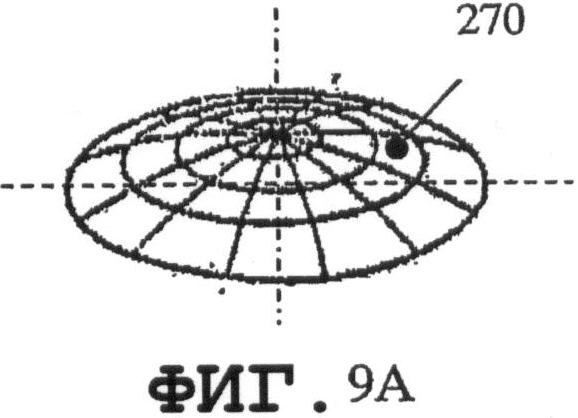
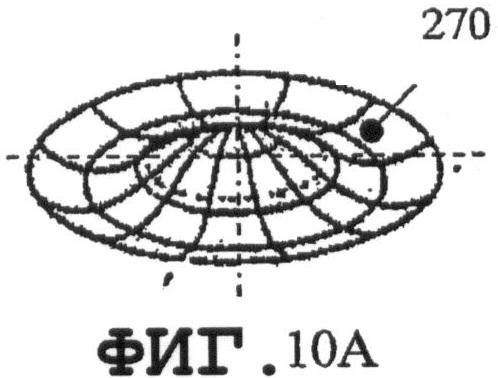
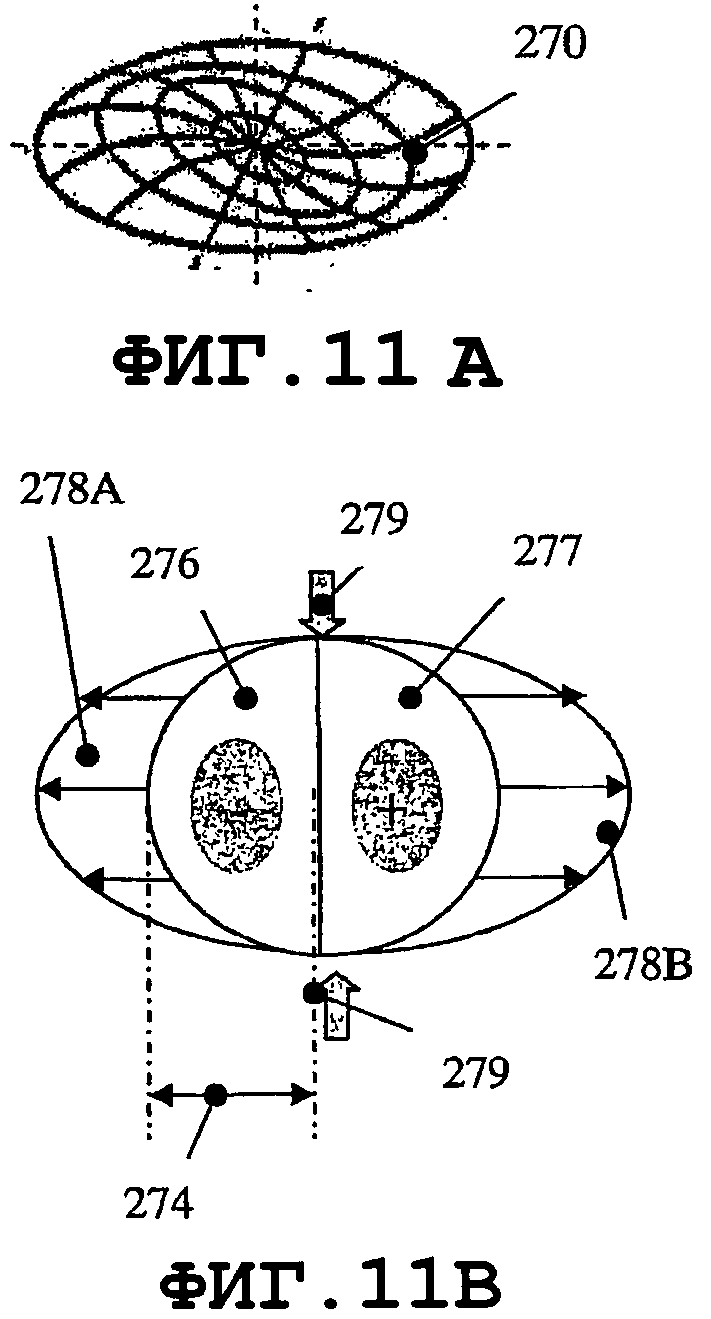
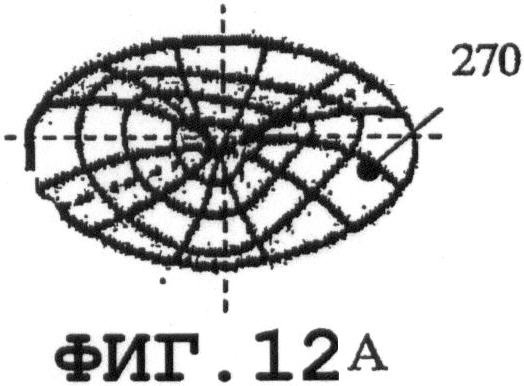
на фиг.9А, 10А, 11А и 12А графически представлены моды нормальных колебаний мембран круглой формы для разных n и m;
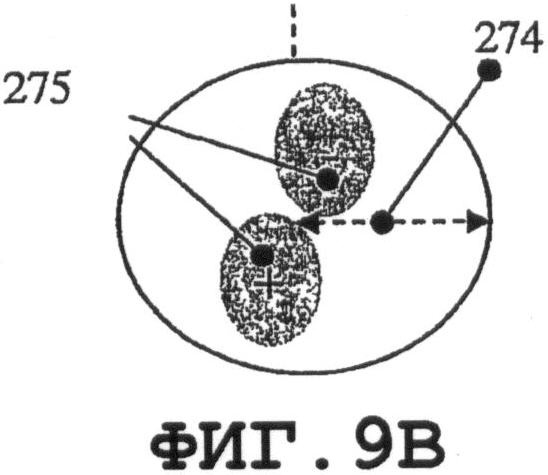
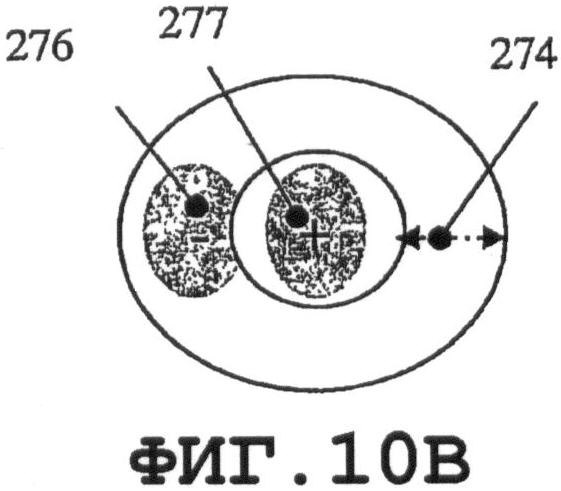
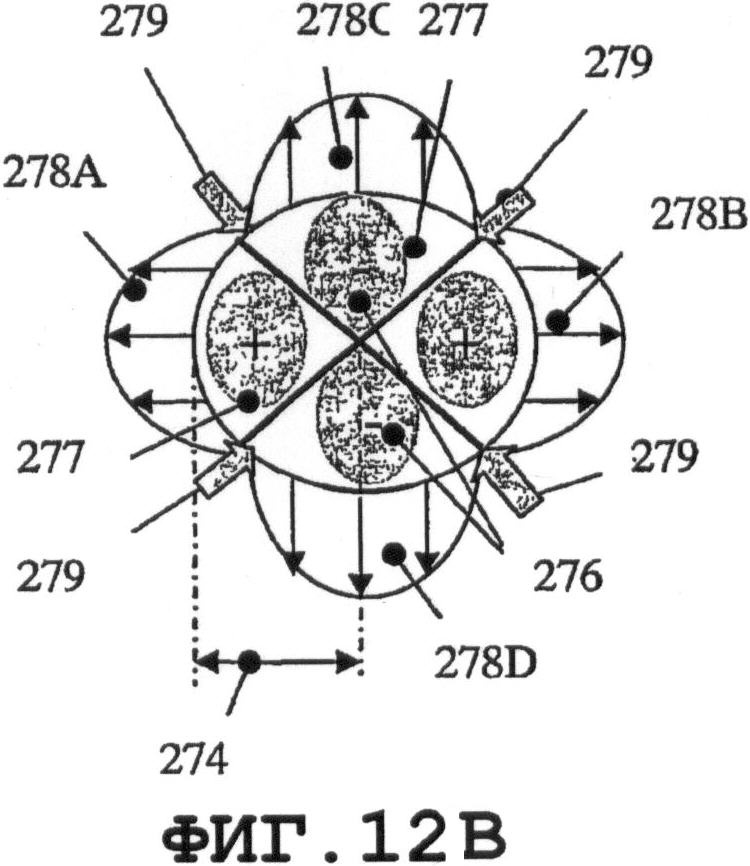
на фиг.9В, 10В, 11В и 12В схематично показаны те же самые моды;
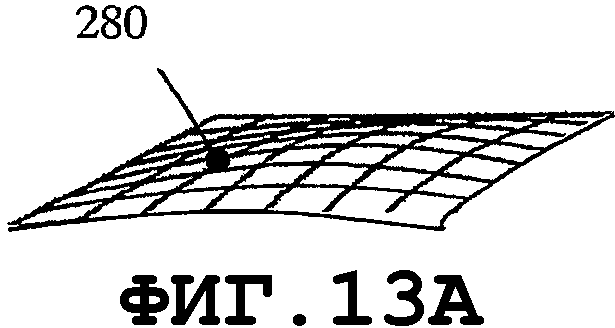
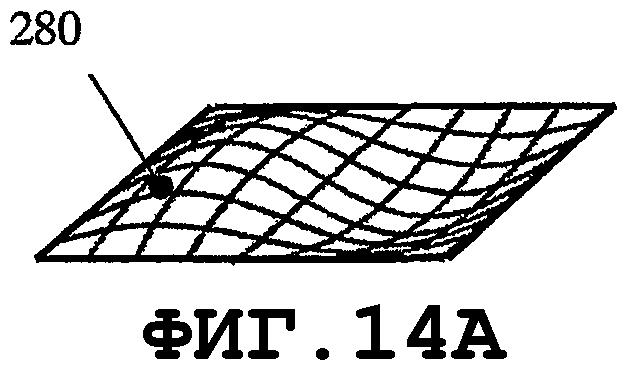
на фиг.13А, 14А, 15А и 16А графически представлены нормальные моды прямоугольной пластины;
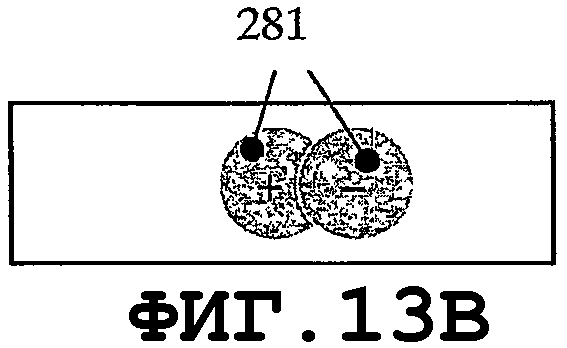
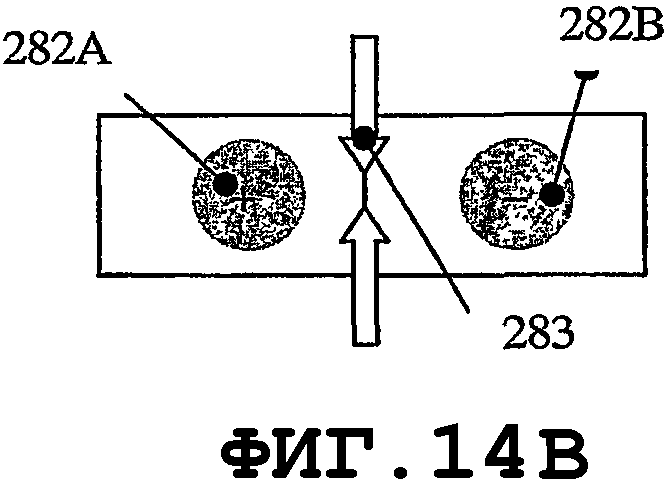
на фиг.13В, 14В, 15В и 16В схематично показаны те же самые моды для разных гармоник n и m;
на фиг.17-24 схематично показаны несколько предлагаемых резонаторов круглой формы для защиты поверхности медицинского устройства от биопленки;
на фиг.25-34 схематично показано несколько предлагаемых конструкций тонкого пьезоэлемента, когда геометрия медицинского устройства требует применения пьезопластин;
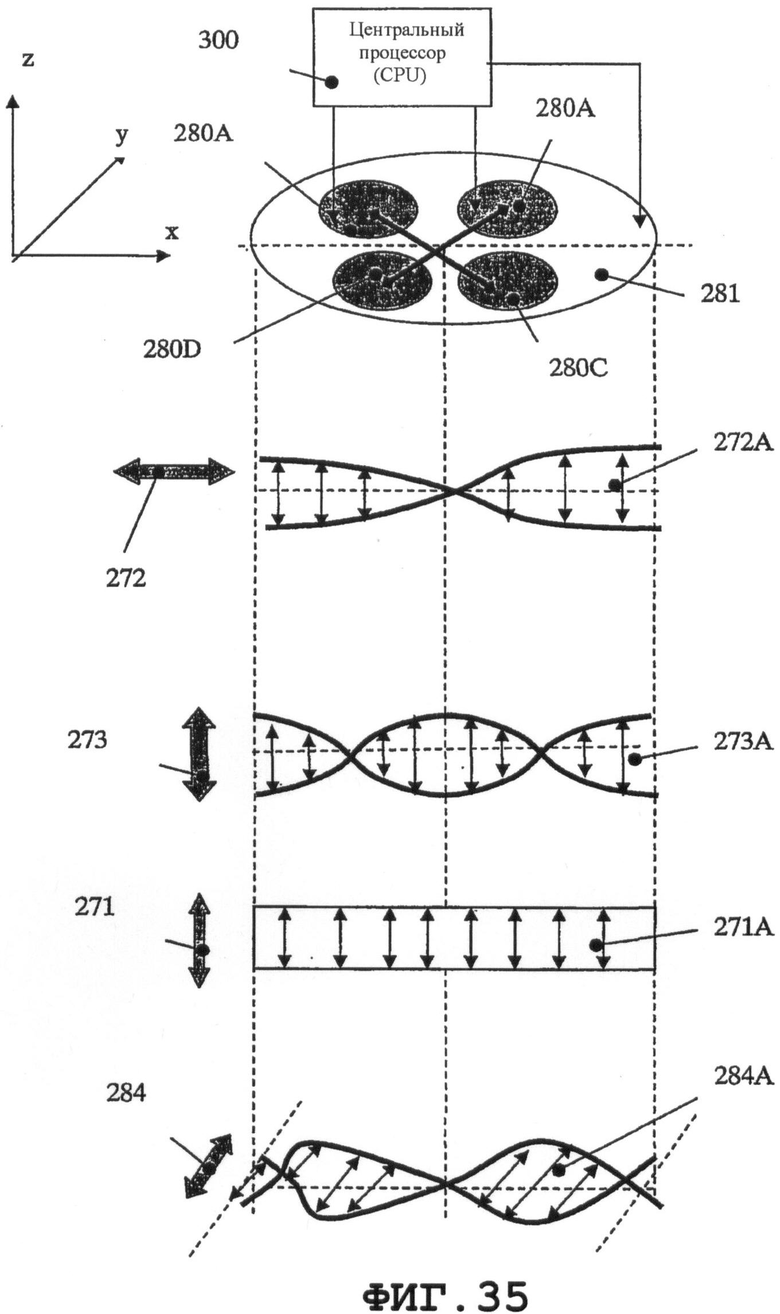
на фиг.35 схематично показано предлагаемое применение с раздельными пьезоэлементами на одном резонаторе;
на фиг.36-44 схематично показаны предлагаемые присоединения резонаторов к медицинскому устройству или его частям (предлагаемые примеры применимы при объединении пьезорезонатора с новыми медицинскими устройствами. По меньшей мере, один резонатор SAW-процесса можно присоединять к одному медицинскому устройству);
на фиг.45 (А, В, С) представлены результаты электронно-микроскопического исследования в ходе экспериментов in vitro для оценки безопасности возбуждаемых SAW применительно к биологическому действию (воздействие на присоединенный монослой клеток в культурах тканей);
на фиг.46 показано предлагаемое применение технологии со стандартной периферической внутривенной катетерной системой;
на фиг.47 и 48 графически представлены варианты осуществления, в которых тонкий пьезоэлемент имеет форму сегмента тонкого кольца, который механически присоединяют к соединителю катетера или встраивают в него;
на фиг.49 показано другое применение, в котором пьезорезонатор (по меньшей мере, один) объединен с клейкой лентой;
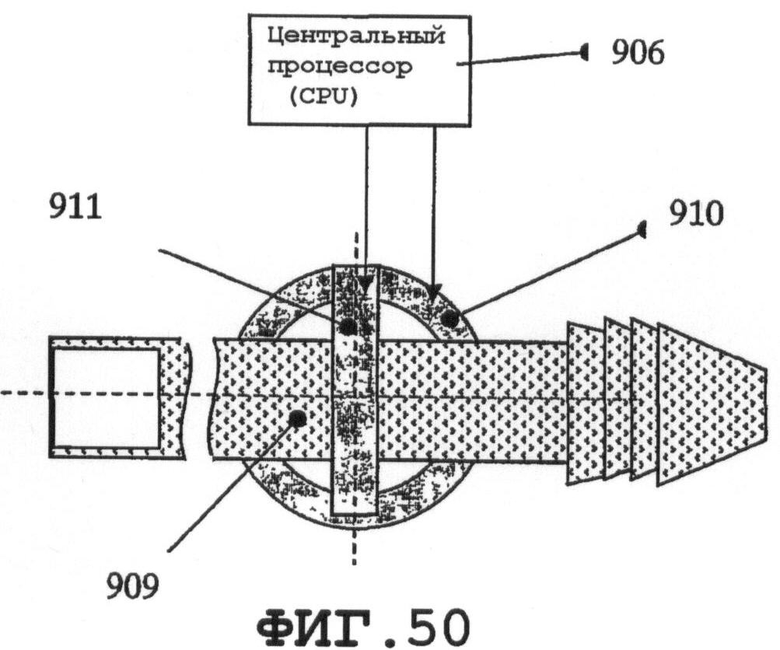
на фиг.50 показан тонкий пьезодиск специальной формы - кольцевой элемент, присоединенный к соединителю внутривенного катетера;
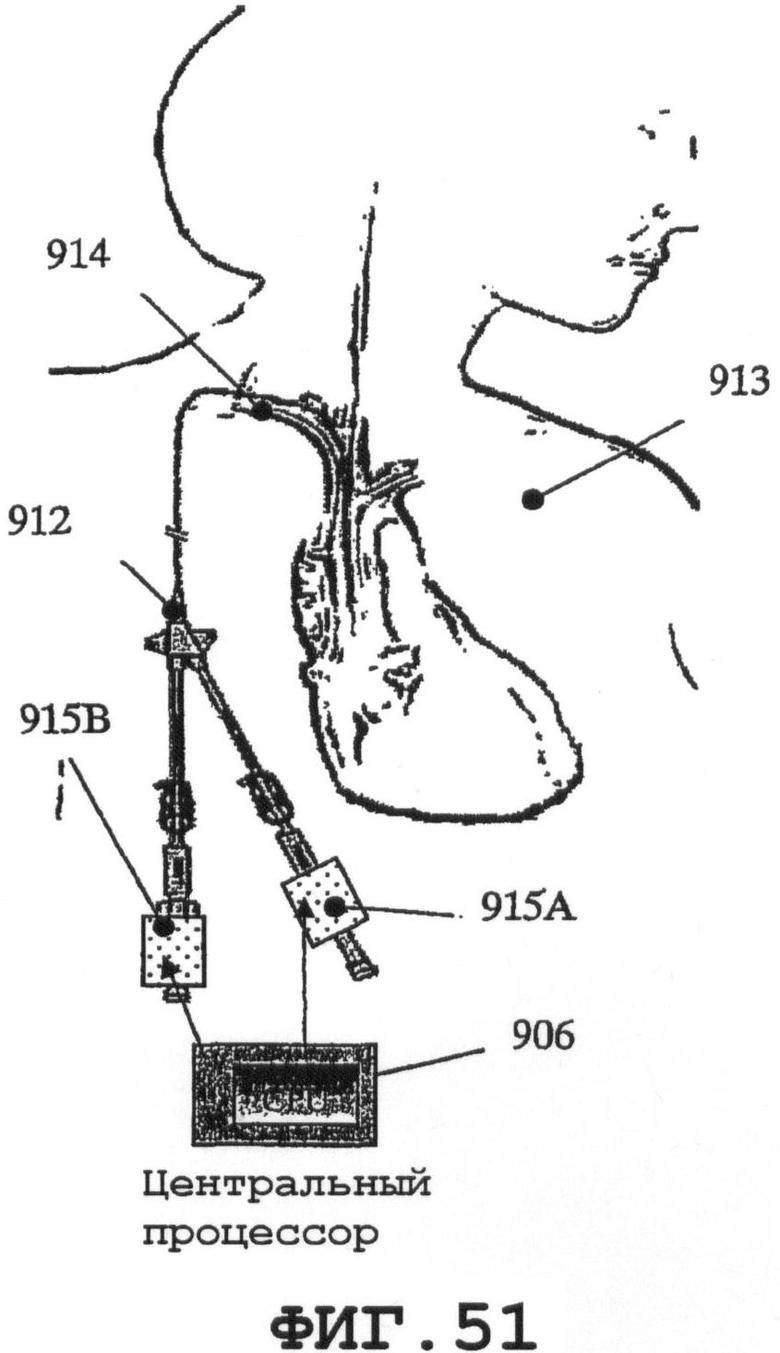
на фиг.51 показаны два тонких пьезоэлемента, присоединенные к отдельным просветам центрального венного катетера;
на фиг.52 показано другое применение предлагаемого изобретения, в котором клейкую ленту с тонкими пьезоэлементами применяют в системе центрального венного катетера;
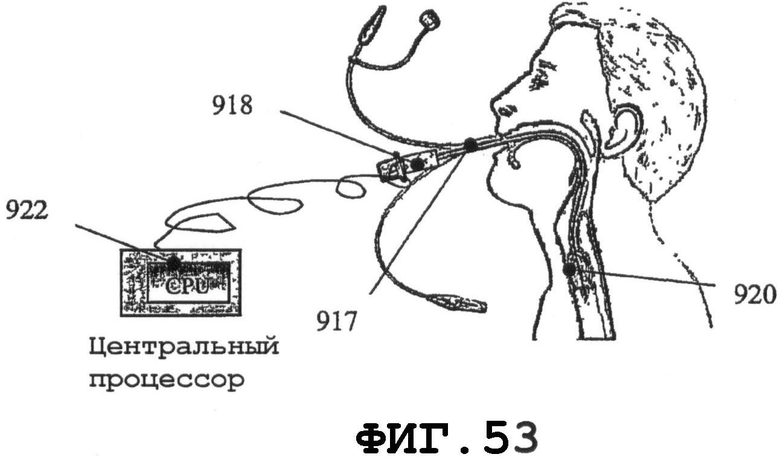
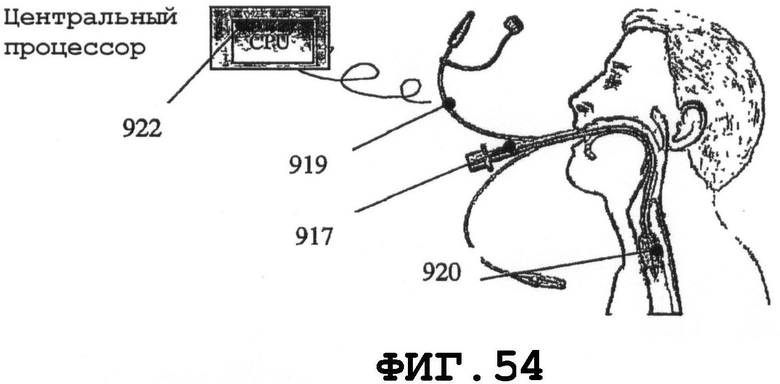
на фиг.53-55 графически представлены другие варианты осуществления изобретения, в которых резонаторы SAW разного типа присоединяют к системам эндотрахеальных трубок для вентиляции легких;
на фиг.56 представлен принцип другого применения предлагаемого изобретения - устройство «Uroshield» (типа 010);
на фиг.57 показано другое решение сопряжения для устройства Uroshield, при этом несколько пьезоэлементов присоединяют в точках перехода на катетере;
на фиг.58-61 представлены результаты исследований in vivo (посредством SEM (сканирующего электронного микроскопа));
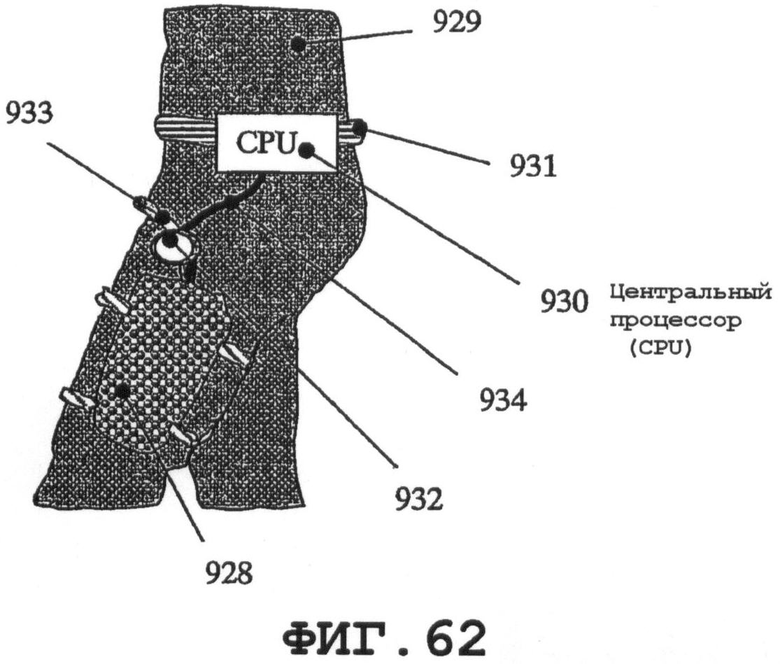
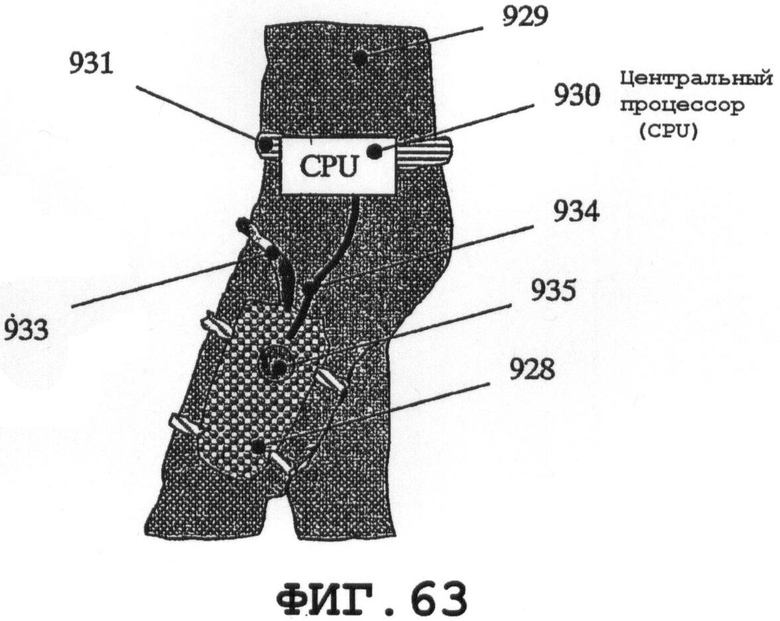
на фиг.62 и 63 схематично показаны возможные варианты, в которых мочеприемник можно закреплять на ноге пациента;
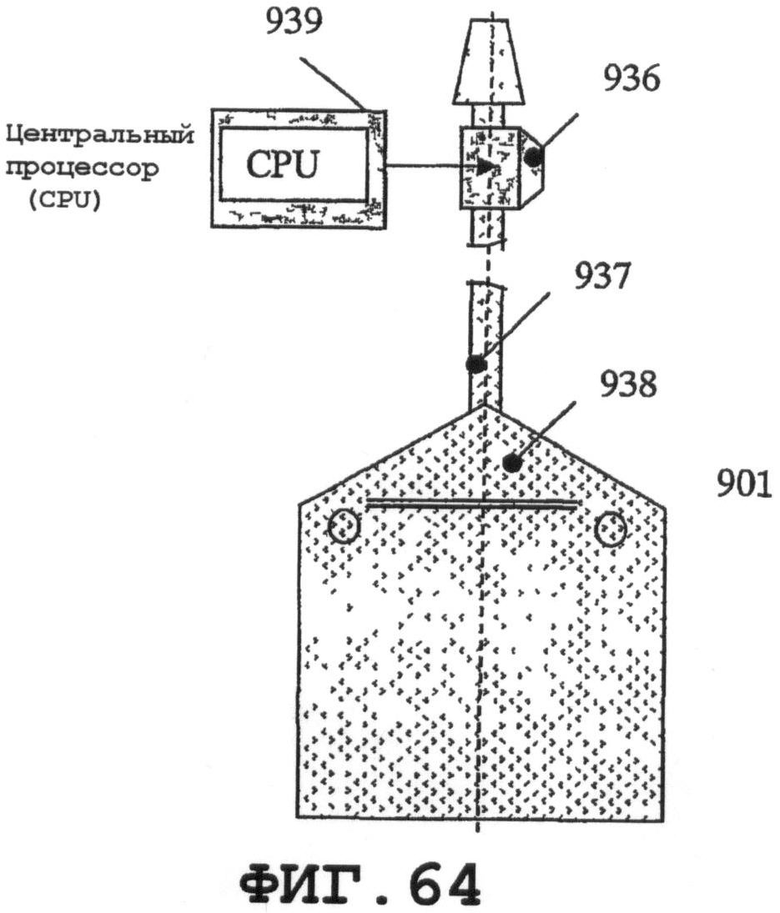
на фиг.64 показаны дополнительные возможные варианты присоединения резонатора SAW к сборной трубке мочеприемника;
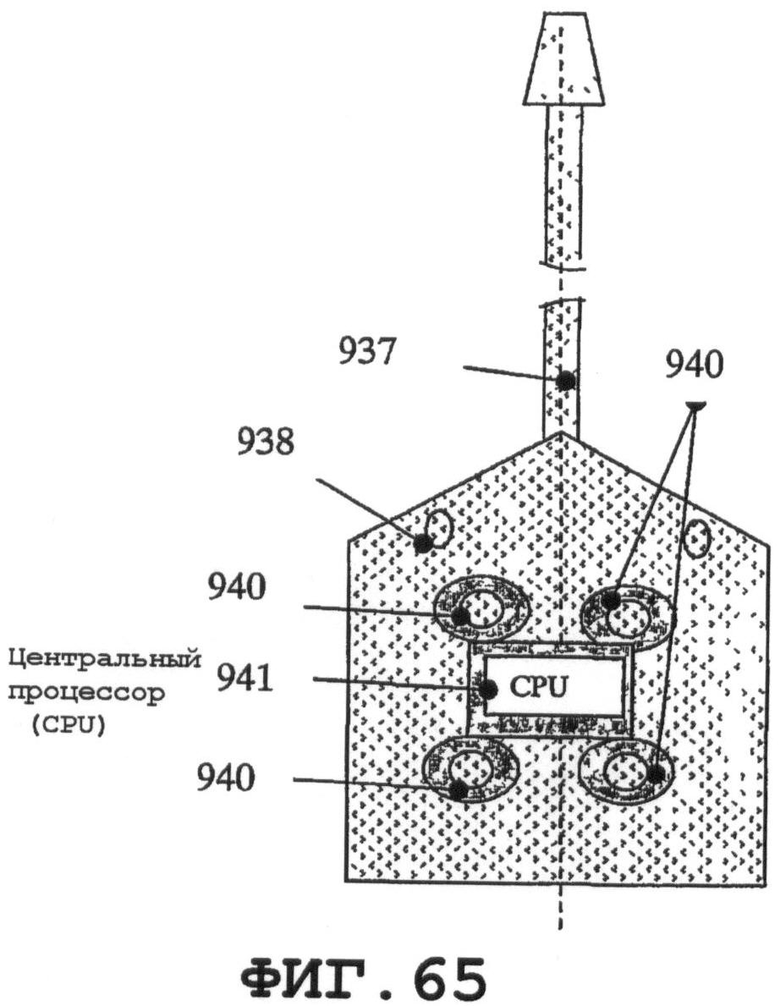
на фиг.65 схематично показано другое применение, в котором, по меньшей мере, один пьезорезонатор с CPU (центральным процессором) присоединены к мочеприемнику;
на фиг.66 показаны экспериментальные результаты с мочеприемником.
Подробное описание чертежей
На фиг.1 изображен вариант осуществления изобретения, содержащий медицинское устройство 100 постоянной установки, которое содержит проход для текучих сред, жидкостей или газов или того и другого. Жидкости могут протекать внутрь тела пациента или из него. Медицинское устройство постоянной установки может обладать стандартной или специально разработанной конфигурацией.
Целью изобретения является предотвращение образования биопленки на внешней 110, внутренней 120 и торцевых 130 поверхностях медицинского устройства 100. Данную цель достигают возбуждением акустических волн в нанометрическом диапазоне на поверхностях медицинского устройства (SAW). Процесс можно считать процессом создания виртуального нановибрационного покрытия. Главная особенность данного процесса состоит в том, что перемещается каждая материальная точка поверхности и нет точки, которая не перемещается, по меньшей мере, в одном месте. Процесс содержит возможность формирования SAW на внешней, внутренней, торсионных поверхностях и соединительных линиях между ними, одновременно или по отдельности.
Кроме того, упомянутая небольшая энергия механических колебаний, передаваемая поверхности механического устройства, препятствует прикреплению бактерий и предотвращает попадание микроорганизмов от внешних и внутренних источников.
Для формирования процесса создания нановибрационного покрытия на внутренних и наружных поверхностях медицинского устройства к медицинскому устройству следует присоединить возбудитель - резонатор механических колебаний. Резонатор 200 должен быть прицеплен на медицинское устройство снаружи тела пациента.
Ряд экспериментов показал, что резонаторы на основе принципов обратного пьезоэлектрического эффекта являются наиболее подходящими и показывают наилучшие результаты. Пьезорезонатор 200 способен возбуждать высокочастотные механические колебания в килогерцовом (кГц) - мегагерцовом (МГц) диапазоне. Данные высокочастотные механические колебания резонатора 200 создают поверхностные акустические волны (SAW) с длинами волн менее чем 100 микрометров. Амплитуды данных колебаний составляют несколько нанометров.
Вид SAW, возбуждаемых на внутренней 111 и внешней 121 поверхностях медицинского устройства 100, имеет характер бегущей волны. Волны передаются в двух противоположных направлениях от резонатора 200. Управляемый процесс SAW (процесс создания нановибрационного покрытия) обеспечивает эффект толкания или тяги материалов на упомянутых поверхностях, в том числе подвешенных на них текучих сред и частиц. В случае биопленки, образующейся независимо или зависимо от медицинского устройства, введение нановибрационных волн: (а) убавит существующую биопленку; (b) усилит и ускорит действие антибиотиков на биопленку (ускорит резистентность биопленки к антибиотикам) с получением антимикробных и антитромбогенных поверхностей.
Когда резонатор 200 использует тонкий пластинчатый элемент PZT (пьезоэлектрического преобразователя), периодический прямоугольный электрический импульс подается из генератора, и тонкий пластинчатый элемент PZT совершает механические колебания нормальных мод колебаний. Следует подчеркнуть, что для возбуждения данных колебаний требуется незначительное энергопотребление (по сравнению с другими способами) и процесс можно продолжать длительный период времени. Эксперименты доказали возможность предотвращения образования биопленки на поверхности медицинских устройств в течение периода времени до 28 суток.
Пьезорезонатор 200 типа тонкой пластины может нуждаться в разных геометрических формах в зависимости от типа медицинского устройства и режима работы. Основными формами тонких пластинчатых пьезорезонаторов являются формы, выбираемые из пластины, диска, мембран (пластин и дисков), тонких безмоментных оболочек и их комбинаций.
Как показано на фиг.1, тонкий пьезорезонатор 200 электрически связан с контроллером 300 CPU (на базе центрального процессора). Частота электрического генератора непосредственно связана с частотой возбужденных механических колебаний в резонаторе 200. Применяемый источник энергии может быть периодического или непериодического характера и может быть электромеханического или электромагнитного происхождения.
Кроме того, для повышения эффективности передачи механических колебаний от резонатора 200 к поверхности медицинского устройства 100 следует применить специальную систему 400 связи. Система 400 состоит из согласующих слоев с разными толщинами и зависит от материалов и композитов. Система 400 связи функционально предназначена для сведения к минимуму саморазогревания в резонаторе. Для оптимизации процесса резонатор настроен на работу в резонанс с SAW-процессом на внутренних, внешних и торцевых поверхностях медицинского устройства.
На фиг.2 представлена акустическая система медицинского устройства, которая содержит центральный процессор (CPU) и тонкий пластинчатый пьезорезонатор 200 в качестве электромеханического преобразователя. Пластина 200 непосредственно или посредством системы 400 связи присоединена к обычному специально разработанному медицинскому устройству 100 или его части. CPU 300 передает и управляет электрическими сигналами, подаваемыми в тонкий электромеханический пьезорезонатор 200. Резонатор 200 преобразует электрические сигналы CPU 300 в механическую энергию пропорционально по времени и диапазону. В результате возбуждаются механические колебания тонкого резонатора 200, и пространственные векторы его механических колебаний обладают переменным характером. По меньшей мере, один такой резонатор (возбудитель) 200 может возбуждать поверхностные механические колебания на медицинском устройстве 100. Возникновение SAW на медицинском устройстве зависит от конкретной области, к которой присоединен резонатор 200. SAW можно рассматривать как виртуальное нановибрационное покрытие на всех поверхностях реального медицинского устройства 100. Тонкий пьезорезонатор 200 передает энергию возбуждаемых механических колебаний механическому устройству 100. С другой стороны, резонатор способен управлять данным процессом посредством передачи в CPU электрических сигналов, пропорциональных максимальному диапазону механической энергии на медицинском устройстве (для обеспечения требований к безопасности). По указанным причинам предлагаемый электронный блок CPU 300 должен содержать информационный вход, соответствующий типу геометрических размеров медицинского устройства. Данная информация записана в блоке 301 памяти.
Электронный блок CPU 300 содержит блок 302 питания (аккумуляторную батарею или источник переменного тока), память 301, контроллер 303, генератор 304 нановибраций, модулятор 305, контроллер 306 моды колебаний, усилитель 307 устройства для применения моды колебаний, коммутирующие устройства 308 и 309, приемник 310 и устройство 311 звуковой/видеосигнализации. Электрическая связь между CPU 300 и резонатором 200 с механическими колебаниями обеспечивается прямым и обратным соединениями 201 и 202. Процесс нановибраций на поверхности медицинского устройства возникает, когда каждая точка поверхности перемещается в нанометровом диапазоне. Резонатор 200, получающий электрические сигналы из CPU 300, одновременно создает механические колебания разных частот (резонансных и нерезонансных). Способность создавать колебания на нескольких резонансных частотах одновременно характерна для материалов с пьезоэлектрическими свойствами. В последующем подробном описании предполагается, что резонатор 200 с механическими колебаниями изготовлен в форме тонкой пьезопластины и снабжен, по меньшей мере, двумя электродами.
На фиг.3А-3В изображен тонкий пьезорезонатор 200 (дисковидный) такого типа, который связан посредством согласующей системы 400 с внешней поверхностью 110 медицинского устройства 100. Резонатор 200 покрыт электродами (серебром, латунью, золотом и т.п.) с электрическими проводниками для передачи электрического сигнала от CPU 300. Каждый поверхностный электрод тонкого пьезорезонатора 200 может содержать одну или несколько изолирующих зон разной площади. В альтернативном варианте тонкий пьезорезонатор 200 может содержать пьезоэлектрический материал с простой поляризацией или поляризацией по нескольким направлениям.
На фиг.3А и 3В показан также тонкий (дисковидный) пьезорезонатор 200 с поляризацией 210 по толщине. Тонкий пьезорезонатор 200 может быть выполнен для механического колебания по толщине и на других модах, например продольной, радиальной и изгибной, по отдельности или одновременно.
На фиг.4 представлена спектральная диаграмма 500 зависимости амплитуд механических колебаний от частоты. Например, тонкое пьезокерамическое устройство 200 может колебаться на изгибной моде (зона 511 спектра частот) и одновременно колебаться на других модах - радиальной моде колебаний (зона 512 спектра частот) и моде колебаний по толщине (зона 513 спектра частот). С другой стороны, одна колебательная мода (например, радиальная) может наводить другие моды колебаний (по толщине, изгибные). Данная особенность зависит от формы и геометрических размеров тонкого пьезоэлемента, направления поляризации, технических характеристик пьезоэлектрического материала, коэффициентов добротности и т.д. Число колебательных мод зависит от формы электрического сигнала, подаваемого в тонкий пьезоэлемент, который может быть периодическим, импульсным или специальной формы. Подача импульсных электрических сигналов может возбуждать колебания не только основной, но и последующих гармоник. Когда соотношение между толщиной и длиной тонкого пьезоэлемента не меньше чем 1:10, возникают гармоники дополнительных частот. Это может быть обусловлено внутренним трением частиц пьезоэлектрического материала, развивающих большие амплитуды. Колебания с амплитудами в десятые доли микрометра вызывают сильные нелинейные процессы. Подача широкого спектра частот в тонкий пьезоэлемент одновременно возбуждает колебания элемента на нескольких модах колебаний. Широкий спектр колебательных мод пьезорезонатора позволяет генерировать SAW на поверхности различных частей медицинского устройства. Они могут быть изготовлены из разных материалов и характеризоваться разными скоростями распространения в них акустических волн и длинами волн SAW. Значение SAW-процесса состоит в том, что каждая точка поверхности медицинского устройства перемещается в трех измерениях и данный процесс можно рассматривать как виртуальное нановибрационное покрытие поверхности.
Тонкий пьезорезонатор 200 возбуждает механические колебания в широком диапазоне: от нескольких Гц до МГц. На фиг.2 показан CPU 300 для электрического возбуждения, который регулирует форму и время электрического сигнала. Генератор 304 нановибраций может генерировать по отдельности или одновременно электрические сигналы в диапазоне, измеряемом Гц, кГц или МГц. Данные импульсы могут иметь формы синусоидальных, импульсных или специальных сигналов, характеризующих гармонические и негармонические колебания.
Для расширения спектра частот сигналов, как показано на фиг.2, генератор 304 вибраций посредством коммутирующего устройства 309 (которым управляет контроллер 302) подключается к модулятору 305. Модулятор 305 содержит электронный блок, который позволяет производить, по отдельности или одновременно, амплитудную модуляцию (AM), частотную модуляцию (FM), кольцевую модуляцию (RM), аддитивный, субтрактивный, постепенный и табличный синтез. Синтезированный сигнал из модулятора 305 поступает в устройство 306 моды колебаний, которое, по команде контроллера 302, преобразует сигнал в однофазный, двухфазный или многофазный сигнал. Сигнал через усилитель 307 и второе коммутирующее устройство 309 передается в разные области возбуждения механических колебаний на резонаторе 200 механических колебаний (для тонкого пьезоэлемента на фиг.3 такими областями являются разные электроды). Устройство 311 звуковой или видеосигнализации осуществляет управление и сигнализирует, если система действует/не действует (например, если имеет место плохой контакт). Предусмотрена возможность управления и регулирования по состоянию здоровья пациента и соответственно биологическим циклам, изменениям температуры тела или патологическим состояниям. Данная система сигнализации применяется в устройстве «Uroshield», разработанном компанией Nanovibronix, Ltd., и данная система информирует пользователя о низкой мощности аккумуляторной батареи или об отсутствии контакта проводов. В альтернативном варианте система сигнализации может информировать о помехах (например, обусловленных движениями пациента) контроллера и предотвращении ситуации по соответствующей команде. Другими словами, сенсорная функция медицинского устройства может вызывать изменения колебаний системы и продолжение процесса предотвращения биопленки. Возможность контроля позволяет компенсировать помехи части медицинского устройства внутри тела пациента. Если требуется, контроль может представлять информацию о пульсации кровотока. Резонатор 200 механических колебаний характеризуется спектром собственных частот колебаний, который зависит от материала и формы медицинского устройства 100, места присоединения резонатора 200 и системы 400 связи. Частоты резонатора 200 механических колебаний могут изменяться в диапазоне от приблизительно 1,0 Гц до приблизительно 50 МГц. Обратная связь позволяет управлять модами колебаний и их гармониками в процессе автогенерации SAW. SAW обладает характеристикой бегущей волны и регулируется соответственно упругим характеристикам материала, составляющего резонаторное устройство.
На фиг.3А показаны два направления SAW, а именно 111А и 111В, на внешней поверхности 110 медицинского устройства 100. Тонкий пьезоэлемент 200 присоединен посредством системы 400 связи к внешней поверхности 110 медицинского устройства 100. Пластинчатый пьезорезонатор 200 совершает колебания продольной моды 220 (направление поляризации - по толщине 210), возбуждает две SAW, распространяющиеся в противоположных, 111А и 111В, направлениях от пластинчатого пьезорезонатора 200. Эксперименты, выполненные компанией Nanovibronix, Ltd., показали, что максимальная амплитуда SAW формируется, когда отношение толщины к длине пластины составляет 1:8.
На фиг.3В показано устройство пластинчатого пьезорезонатора 200 в форме диска, который совершает колебания радиальной моды 220 колебаний. SAW, возбуждаемые на поверхности медицинского устройства при дисковидной форме, будут иметь следующие направления: 111А-111В, 112А-112В, 113А-113В, 114А-114В. При применении тонкого резонатора 200 на пьезоэлементе в форме диска для возбуждения SAW, можно возбуждать однородные колебания во всех радиальных направлениях распространения SAW (что невозможно при других формах). Описанный способ применим, когда SAW требуется для предотвращения биопленки на внешней поверхности 110 медицинского устройства. На практике часто требуется, чтобы вибрационные процессы применялись к внутренним поверхностям. С другой стороны, внутренние поверхности могут быть труднодоступными и очень малыми или могут иметь другие характеристики, не допускающие присоединения резонатора непосредственно на данные поверхности.
Ниже приведено описание способа возбуждения SAW в одном заданном направлении посредством резонатора, присоединенного или встроенного во внешнюю поверхность медицинского устройства. На фиг.5 показан тонкий пьезорезонатор 200, присоединенный посредством согласующего слоя специальной призматической формы (системы 400 связи) к внешней поверхности 110. Резонатор 200 механически вибрирует на моде 230 по толщине и посредством системы 400 связи направленно передает механическую энергию. Механическая энергия в форме плоской продольной волны 210 передается (под углом 240) в зону между внешней поверхностью и поверхностью системы связи. Угол 240 выбирают соответственно скорости акустической волны в системе связи, которая должна быть выше, чем скорость акустической волны на внешней поверхности 110 медицинского устройства 100. С другой стороны, скорость акустической волны в тонком пьезорезонаторе 200 должна быть выше, чем скорость акустической волны в системе 400 связи. В результате между внешней поверхностью 110 медицинского устройства и системой 400 связи возбуждается SAW-процесс. SAW работают, когда энергия периодических механических колебаний в форме продольной волны 231 имеет пространственную периодичность с длиной волны, равной длине волны SAW на медицинском устройстве. Направление 112А механических колебаний 231 является положительным относительно резонатора 200.
На фиг.6 показана возможность образования SAW (процесса создания виртуального нановибрационного покрытия) на всей внешней поверхности устройства 110. Относительно резонатора SAW-процесс мощнее в положительном направлении 113А, чем в противоположном направлении 113 В. Этого можно добиться с системой 400 связи призматической формы. Два тонких резонатора 250 и 260 на пьезоэлементах присоединяют к системе связи. Резонатор 250 совершает колебания моды 251 по толщине и генерирует энергию механических колебаний, которая, в виде продольной волны 252, через систему 400 связи переносит механическую энергию в зону между системой связи и поверхностью медицинского устройства. Данная энергия создает SAW в отрицательном направлении 113В относительно резонатора. Условия создания SAW описаны выше со ссылкой на фиг.5. Аналогично, в зоне между системой связи и поверхностью 110 медицинского устройства механическая энергия в форме продольной волны может генерироваться через посредство системы 400 связи модой 261 колебаний по толщине тонкого пьезоэлемента 260. CPU 300 управляет параметрами (частотой, амплитудой, формой сигнала, коэффициентом заполнения и т.п.) тонких пьезоэлементов 250 и 260. Данные пьезоэлементы вибрируют на колебательной моде, соответственно по толщине 251 и по толщине 261. Фиг.5 и 6 поясняют способ возбуждения SAW (процесса создания нановибрационного покрытия) на внешней поверхности медицинского устройства. Аналогично, SAW можно возбуждать на внутренней поверхности медицинского устройства тонким резонатором, присоединенным к внутренним поверхностям 120 устройства. Соответствующие SAW следует выбирать с учетом биологической проблемы. Обычно более высокий уровень SAW требуется для внутренних поверхностей устройства, и более низкие уровни требуются для внешних поверхностей медицинского устройства постоянной установки, в соответствии с требованиями FDA (Управления по контролю за продуктами и лекарствами США) к акустической энергии. Кратковременные высокие уровни SAW могут быть желательными в качестве профилактического средства для предотвращения биопленки на имплантатах и тем самым обеспечения антимикробного и антитромбогенного действия.
С другой стороны, большинство медицинских устройств нуждаются в предотвращении биопленок на всех поверхностях устройства. С данной точки зрения, может быть желательно возбуждение процесса создания виртуального нановибрационного покрытия на всех поверхностях посредством одного тонкого пьезоэлемента. Присоединение тонкого пьезоэлемента с осями поляризации, перпендикулярными поверхности медицинского устройства, и применение продольной моды колебаний пьезоэлемента имеют следствием SAW-процесс только на внешней поверхности. Аналогично, при использовании моды колебаний по толщине пьезоэлемента SAW направляются только на внутреннюю поверхность.
Создание нановибрационного покрытия как на внешней, так и на внутренней поверхностях возможно передачей колебаний изгибной моды пьезоэлемента к данным поверхностям. SAW возбуждается, когда период моды изгибных колебаний равен длине поверхностной акустической волны. Посредством возбуждения в разных направлениях (непосредственно или посредством пьезоэлемента) различных управляемых комбинаций колебательных мод, которые можно формировать одновременно и изменять периодически, одним элементом можно обеспечить колебательные моды.
На фиг.7 показан способ, в котором резонатор 270 присоединяют на внешней, или внутренней, или торцевой поверхности медицинского устройства для проведения управляемых SAW-процессов на данных поверхностях. С этой целью тонкий пьезорезонатор 270 возбуждают для колебания одновременно на трех колебательных модах: по толщине 271, продольной 272 и изгибной 273. Минимальную частоту изгибной моды 273 следует выбирать так, чтобы расстояние между двумя фрикционными точками (две точки между максимальными амплитудами) было не меньше, чем длина волны SAW на поверхности; смотри фиг.8. Частоту электрических сигналов, подаваемых в тонкую пьезопластину, подбирают по отношению к частоте 271 моды колебаний по толщине. Данный электрический сигнал в CPU 300 модулируется одновременно еще двумя частотами, соответственно для продольной 272 и изгибной 273 мод. Тонкая пьезопластина 270 посредством системы 400 связи плотно присоединена к внешней поверхности 110 медицинского устройства 100. Тем самым колебания SAW на внешней 110 и внутренней 120 поверхностях возбуждаются одновременно тремя модами механических колебаний. Бегущие волны на внешней поверхности распространяются в положительном 114А и отрицательном 114В направлениях.
Передача механической энергии от резонатора к внутренней поверхности 120 происходит следующим образом. Механическая энергия передается в направлении 274 плоскими продольными волнами через систему 400 связи и заполненное материалом расстояние между внешней 110 и внутренней 120 поверхностями и характеризуется частотой изгибных колебаний. В результате уровень механической энергии модулируется по времени частотами продольной 272 и изгибной 273 мод и SAW с направлениями 121А и 121В на внутренней поверхности.
Разные частотные диапазоны можно обеспечивать сочетанием видов колебаний (по толщине, продольных, изгибных) на разных гармониках (1-й, 2-й, 3-й, 4-й). Эффект можно обеспечить либо присоединением резонаторов изнутри, либо снаружи к поверхности медицинского устройства. Следует понимать, что присоединение элементов снаружи обеспечивает более сильное вибрационное действие на внутренней поверхности.
На фиг.8 изображена круглая тонкая пьезоэлектрическая мембрана 270, совершающая колебания изгибной (собственной) моды. Мембрана 270 характеризуется следующими параметрами собственной моды колебаний: n=0 и m=1. Данная мембрана может совершать симметричные механические колебания относительно ее оси вращения. SAW на внешней поверхности 110 должна распространяться в направлениях 114А, 114В, 114С, 114D и 115А, 115В, 115С 115D. Аналогично, SAW может распространяться по внутренней поверхности 120 в направлениях 121А, 122А, 121В, 122В (другие направления не показаны). На фиг.9 графически показана возможность изменения направления и уровня распространяющейся SAW посредством управления параметрами колебательных мод тонкой круглой пьезоэлектрической мембраны 270. На фиг.9А, 10А, 11А и 12А графически представлены моды нормальных колебаний мембран круглой формы для разных средних значений n и m.
На фиг.9В, 10В, 11В и 12В схематично показаны те же самые моды. Когда тонкий пьезоэлемент 270 в виде мембраны круглой формы имеет n=0 и m=1, как показано на фиг.9А и 9В, он характеризуется только одним пиковым средним значением смещения. Расстояние между пиком и кромкой мембраны должно быть равным, по меньшей мере, j длины волны SAW. Если n=0 и m=2, как показано на фиг.10А и 10В, то пьезоэлемент 270 содержит два максимальных пика амплитуд, отрицательный 276 и положительный 277. В данном случае минимальная j длина волны SAW соответствует расстоянию 274, которое меньше, чем на фиг.9А и 9В.
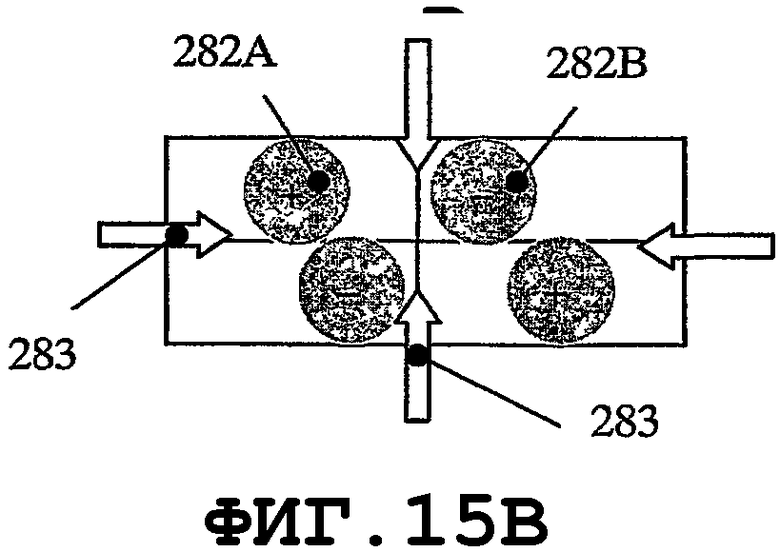
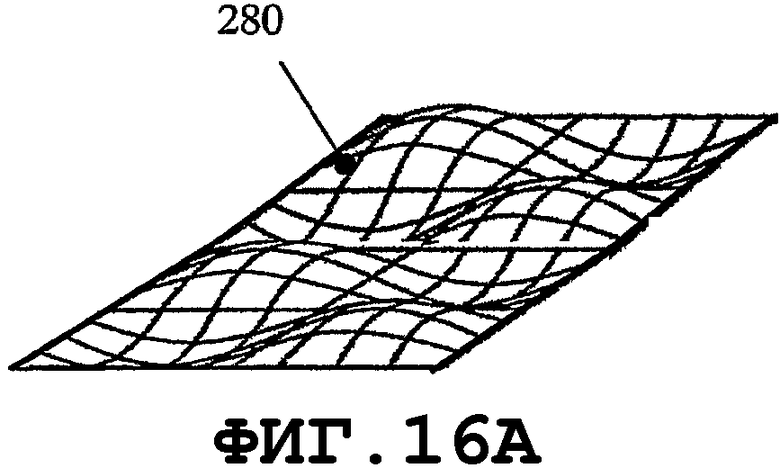
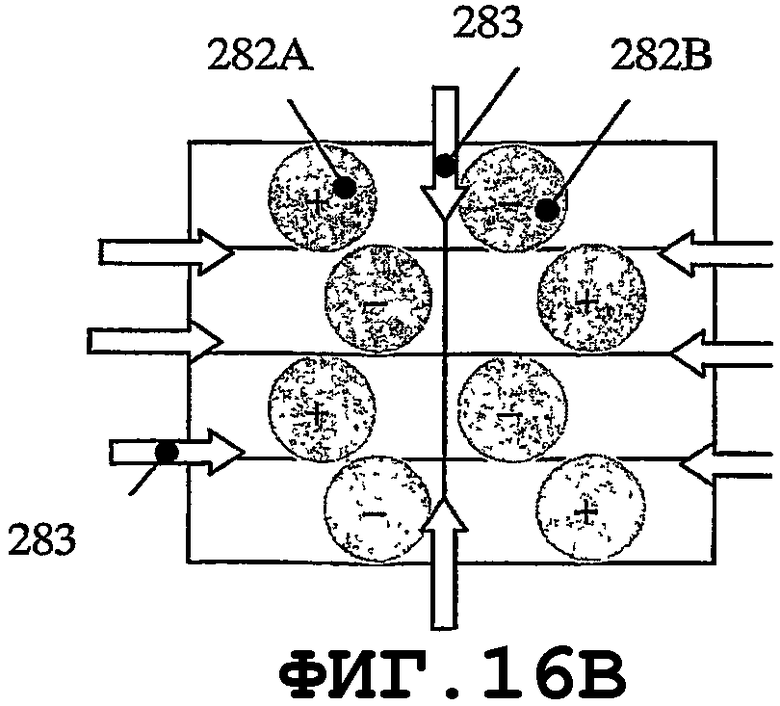
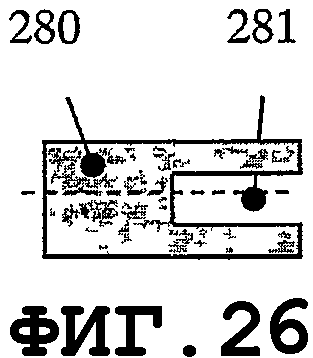
На фиг.9 и 10 показано, что, в случае когда пьезоэлемент 270 имеет форму круглой мембраны, можно организовать процесс распространения однородной SAW по элементу. Кроме того, если возбуждаются колебания с параметрами n=1 и m=1 (смотри фиг.11А и 11В) в тонком пьезоэлементе 270, то будут получены две максимальные амплитуды 276 и 277. Направления распространения SAW 278A и 278В являются взаимно симметричными. SAW-процесс не возбуждается в точках 279, поскольку амплитуды колебаний в данных точках равны 0. Аналогичный процесс возбуждается в мембране 270, когда n=2 и m=1, с четырьмя максимальными пиковыми смещениями, двумя отрицательными 276 и двумя положительными 277. Распространение SAW-процесса характеризуется четырьмя направлениями 278А, 278В, 278С и 278D и зонами 279, в которых SAW-процесс не возбуждается. В заключение следует добавить, что изменением колебательных мод n и m мембраны можно возбуждать разные SAW-процессы одним и тем же тонким пьезоэлементом. Расстояния 274 должны быть пропорциональными длине волны SAW. Аналогичные SAW-процессы можно возбуждать, когда пьезоэлемент имеет форму прямоугольной мембраны. На фиг.13А, 14А, 15А и 16А графически представлены нормальные моды прямоугольной пластины 280. На фиг.13В, 14В, 15В и 16В схематично показаны те же самые моды для разных n и m. Мембрана 280 характеризуется одним амплитудным максимумом смещения 281, если n=1 и m=1, как показано на фиг.13А и 13В. В случае когда n=2 и m=1, SAW-процесс характеризуется двумя максимальными амплитудами 282А и 282В смещения и двумя зонами 283, в которых колебания не возбуждаются, как показано на фиг.14А и 14В. В случае когда n=2 и m=2, SAW-процесс характеризуется четырьмя максимальными амплитудами смещения, двумя положительными 282А и двумя отрицательными 282В, а также четырьмя зонами 283, в которых колебания не возбуждаются. Смотри фиг.15А и 15В. В случае когда n=2 и m=4 (как показано на фиг.16А и 16В), SAW-процесс характеризуется восемью максимальными амплитудами смещения - четырьмя положительными 282А и четырьмя отрицательными 282В. Процесс характеризуется восемью зонами 283, в которых колебания не возбуждаются.
Обеспечение возбуждения SAW на медицинском устройстве требует, чтобы колебательные моды, гармоники, продолжительности периодов, возбуждаемые в пьезоэлементе, соответствовали длине SAW на медицинском устройстве. Прямоугольные пьезоэлементы могут возбуждать распространение разных SAW по направлениям длины и ширины элементов (это может быть важно, когда в конструкции медицинского устройства применяются разные материалы и необходимо возбуждать разные SAW).
На фиг.14В показана мембрана 280 и возбуждаемая мода механических колебаний тонкой пьезопластины в направлении длины с одним соответствующим периодом. На фиг.15В изображен случай, когда возбуждаемая мода механических колебаний тонкой пьезопластины содержит по одному периоду в направлении длины и в направлении ширины. На фиг.16В изображен случай, когда мода механических колебаний тонкой пьезопластины, при возбуждении, содержит один период в направлении длины и два периода в направлении ширины. Устойчивость возбужденного SAW-процесса в медицинском устройстве соответствует числу периодов колебательных мод, возбужденных в пьезопластине (большее число периодов означает более устойчивый SAW-процесс). Круговая и прямоугольная формы являются не единственными формами, подходящими для предотвращения биопленки посредством возбуждения резонаторов SAW. Такие же колебательные моды можно возбуждать резонаторами с другой геометрией.
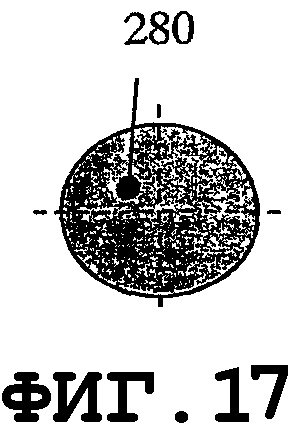
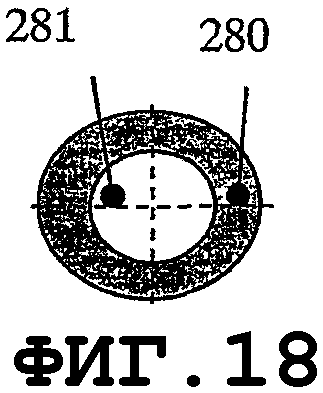
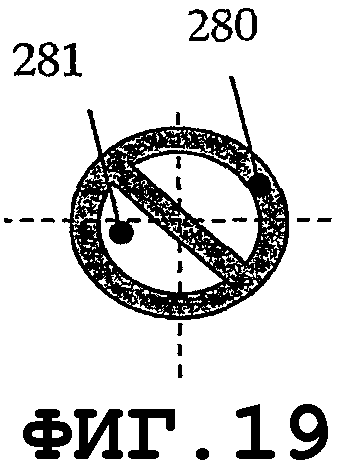
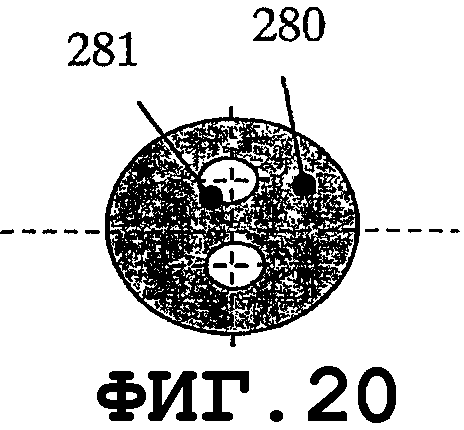
На фиг.17-24 показаны несколько других предлагаемых резонаторов круглой формы для защиты поверхности медицинского устройства от биопленки. На фиг.17 показан тонкий пьезоэлемент 280 дисковидной формы. На фиг.18 показан тонкий пьезоэлемент 280 кольцевой формы с отверстием 281. На фиг.19 показан тонкий пьезоэлемент 280 специальной формы с крепежными отверстиями 281. На фиг.20 показан тонкий пьезоэлемент 280 дисковидной формы с, по меньшей мере, двумя крепежными отверстиями 281. Краевые области, окружающие крепежные отверстия, выполняют функцию дополнительных источников возбуждения колебаний.
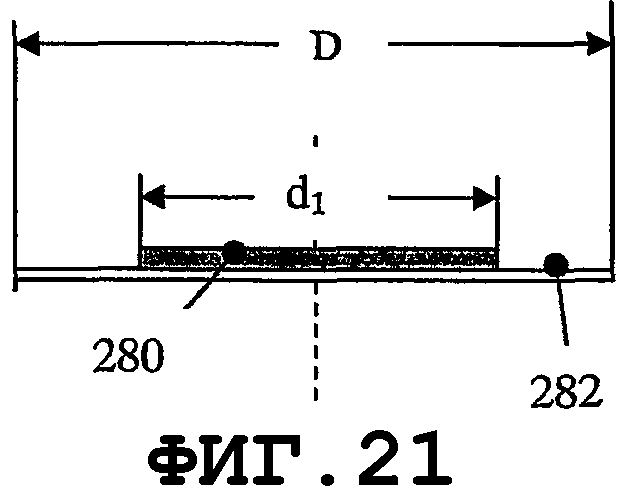
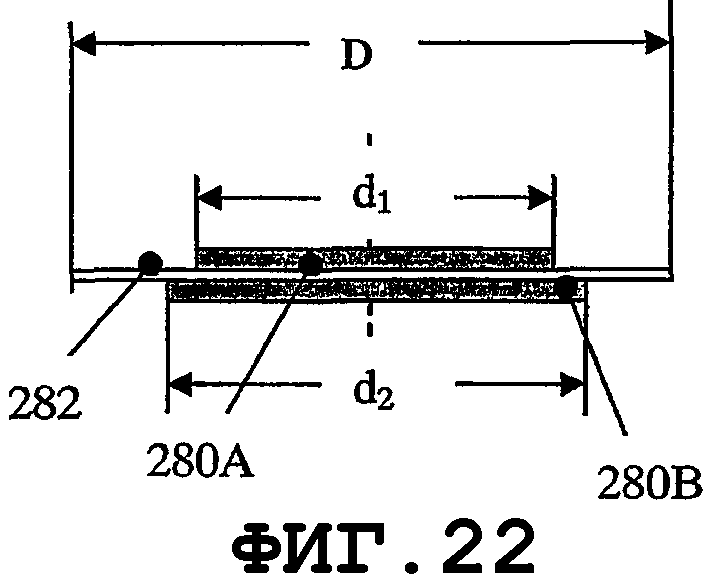
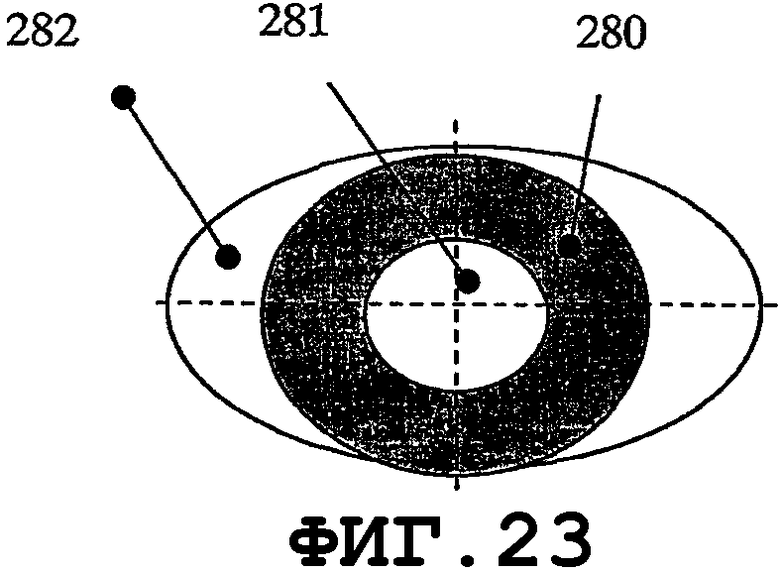
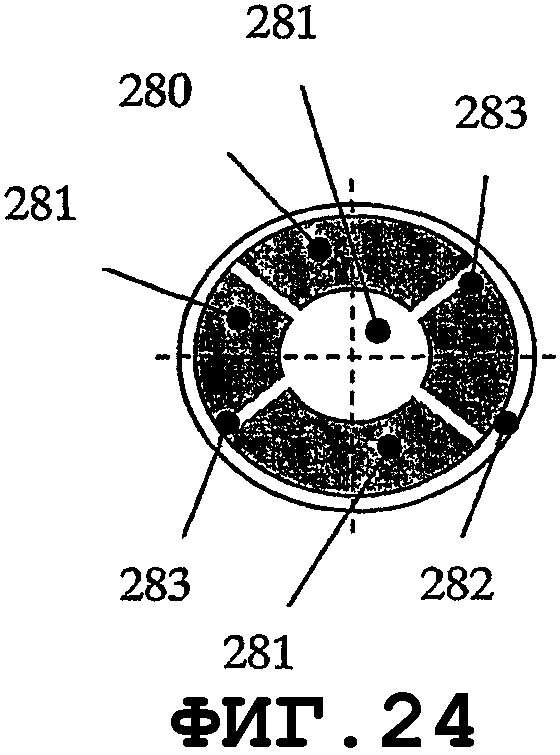
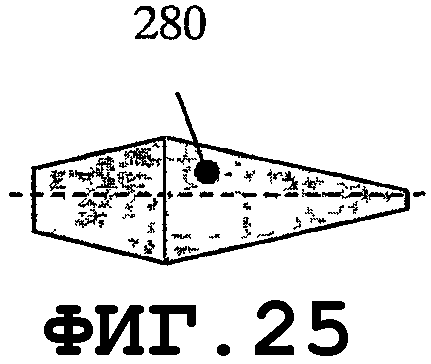
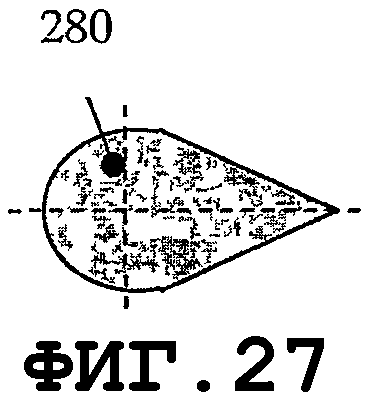
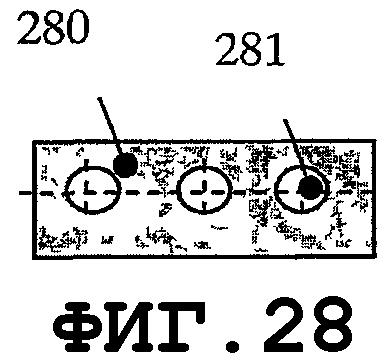
На фиг.21-24 показаны преимущества элемента зуммерного типа для возбуждения SAW на поверхности медицинского устройства. Геометрия зуммера допускает применение очень тонкого слоя пьезоэлектрического материала, механически прикрепленного к тонкому слою дисковидной формы, выполненному из металла или электропроводящего пластика. Тонкие пьезоэлементы такой многослойной конструкции с разными D, d1 и d2 позволяют возбуждать собственные колебательные моды с высокими значениями n и m гармоник. На фиг.21 показан тонкий пьезоэлемент 280 дисковидной формы, прикрепленный к опорной пластине 282 дисковидной формы. Опорная пластина 282 может быть выполнена из металла, пластика или композиционного материала с проводящими свойствами. На фиг.22 показан такой элемент, состоящий из пьезоэлектрических дисков 280А и 280В с соответствующими диаметрами d1 и d2, прикрепленных с обеих сторон к опорной пластине 282 диаметром D. На фиг.23 показан вариант осуществления, в котором пьезоэлемент 280 вместе с опорной пластиной 282 содержит отверстие 281. Один или несколько пьезоэлементов 280, которые электрически изолированы элементами 283, можно прикреплять с одной стороны опорной пластины 282. Посредством подачи сигналов разной частоты в данные пьезоэлементы можно возбуждать виды колебаний разных собственных мод. Экспериментальные результаты показали, что для повышения устойчивости стоячей волны, при использовании второй и высших гармоник тонкого биморфного пьезоэлемента, слой пьезоэлектрического материала должен быть снят в центральной части опорной пластины. Оптимальный (с точки зрения энергетической эффективности) процесс создания нановибрационного покрытия на поверхности медицинского устройства можно обеспечить, когда отношение между слоем пьезоэлетрического материала и металлическим слоем в биморфном пьезоэлементе находится в диапазоне от приблизительно 0,95 до приблизительно 1,35. Тонкие пьезоэлементы обеспечивают преимущество создания более однородного нановибрационного покрытия на поверхности медицинского устройства. Данная особенность желательна, когда один и тот же резонатор SAW присоединяют к медицинским устройствам нескольких типов, которые отличаются одно от другого по материалам, геометрическим параметрам и свойствам образования биопленки. На фиг.25-34 показано несколько предлагаемых конструкций тонкого пьезоэлемента, когда геометрия медицинского устройства требует применения тонких пьезопластин. Пьезоэлементы такой же конструкции можно применять, когда на поверхности медицинского устройства требуются разные SAW-процессы. Геометрия и материал некоторых медицинских устройств могут требовать возбуждения разных SAW-процессов для обеспечения однородной защиты от биопленки. На фиг.25 показан пьезоэлемент типа тонкой пластины, края которого возбуждают разные SAW-процессы. На фиг.26 показана пьезопластина 280 с прямоугольным отверстием 281. Пьезопластины 280 комбинированной формы показаны на фиг.28.
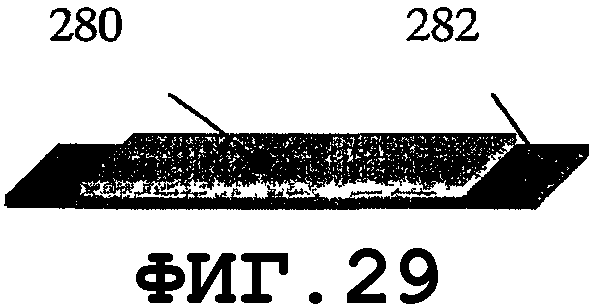
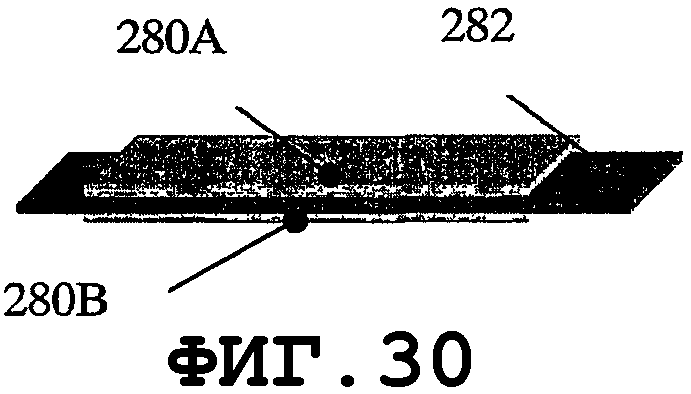
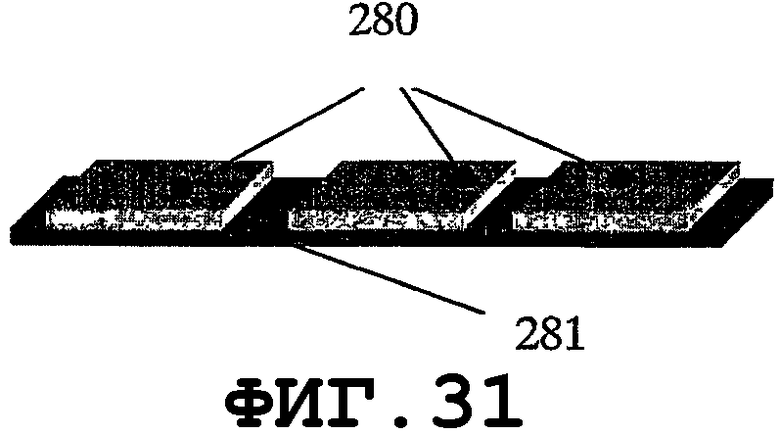
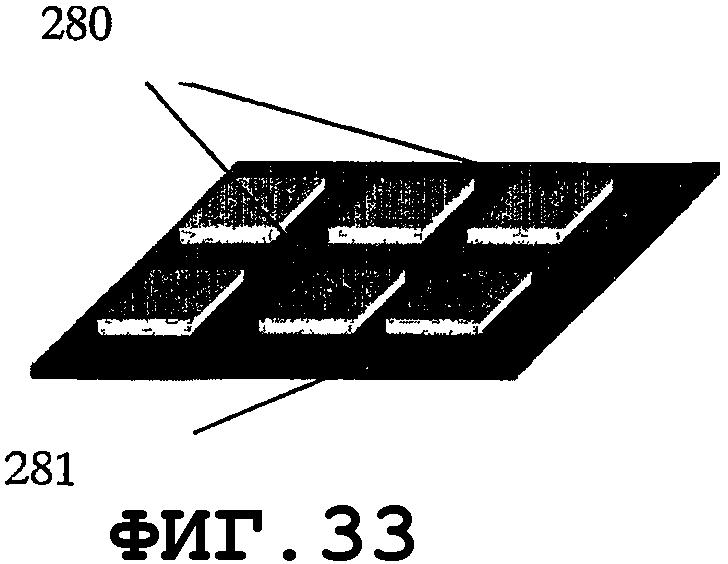
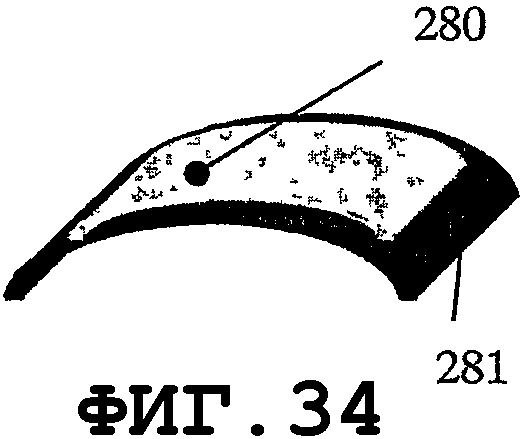
На фиг.29-33 показано применение биморфных пьезоэлементов. На фиг.29 показана простая биморфная пластина, состоящая из одной тонкой пьезопластины 280, прикрепленной к металлической подложке 282. На фиг.30 показаны два пьезоэлемента 280А и 280В, прикрепленные к одной опорной пластине 282. На фиг.31 показаны, по меньшей мере, два пьезоэлемента 280, механически прикрепленных к одной опорной пластине. На фиг.32 и 33 показаны другие предлагаемые варианты крепления пьезоэлементов 280 к металлической опорной пластине 282. На фиг.34 показано применение биморфного пьезоэлемента типа тонкой оболочки. Расположение пьезоэлементов 280 относительно пластины 282 может включать в себя все возможные вышеописанные варианты.
Фиг.35 поясняет предлагаемое применение с раздельными пьезоэлементами на одном резонаторе. Способ допускает возбуждение дополнительной колебательной моды, точнее, изгибной моды по оси симметрии в продольном направлении пьезопластины, показанной на фиг.35. Резонатор SAW может одновременно возбуждать четыре типа колебательных мод, которые представляют колебания по осям x, y, z. Графически изображены мода продольных колебаний 272 в плоскости y-z на графике 272А, мода колебаний 271 по толщине на графике 271А, две моды изгибных колебаний 273 в плоскости z-x на графике 273А и другая изгибная мода колебаний 284 в плоскости y-x на графике 284А. Указанное решение можно обеспечить прикреплением четырех пьезоэлементных частей 280А, 280В, 280С и 280D к одной пластине 281. Данные части электрически соединены следующим образом: 280А с 280С и 280В с 280С. Специальный вариант осуществления может представлять собой одну пьезопластину или один пьезоэлектрический диск, как показано на фиг.24, где электроды подсоединяются к отдельным площадкам на пьезоэлементе. Когда CPU 300 подает электрический сигнал в части 280А и 280С, резонатор на тонком пьезоэлементе начинает колебаться с частотой, соответствующей резонансу изгибной моды 284 пластины в плоскости x-y. При подаче одинакового электрического сигнала в части 280В и 280D, резонатор на тонком пьезоэлементе начинает колебаться противоположным образом благодаря фазовому резонансу моды 284 изгибных колебаний. Если желательно усилить моду 273 изгибных колебаний, поляризации частей 280А и 280В должны быть противоположными поляризации частей 280С и 280D. В результате подачи электрического сигнала, модулированного резонансной частотой вышеупомянутых механических колебаний, из CPU 300 в резонатор на медицинском устройстве можно возбуждать SAW, характеризующиеся разными формами и уровнями. Они также допускают управление в требуемом направлении и передачу на внутреннюю поверхность. При возбуждении второй высшей гармоники стоячей волны в тонком пьезоэлементе эффективность процесса создания нановибрационного покрытия повышается приблизительно на 30% по сравнению со стоячей волной первой гармоники.
Резонаторы колебаний на нескольких частотах можно присоединять к реальному медицинскому устройству или формировать в виде неразъемного блока с устройством. Возможны несколько видов присоединения для возбуждения SAW: приклеивание прочным клеем, механическое присоединение, пружинное присоединение. Предлагаемые жесткие виды присоединения (на клею, механическое) обеспечивают постоянное местоположение резонатора на медицинском устройстве. Пружинное присоединение позволяет смещать резонатор по поверхности медицинского устройства.
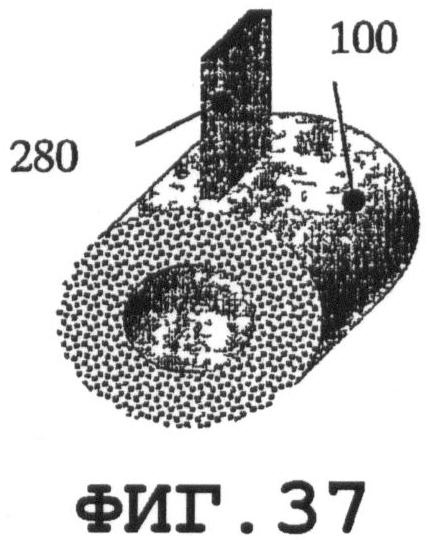
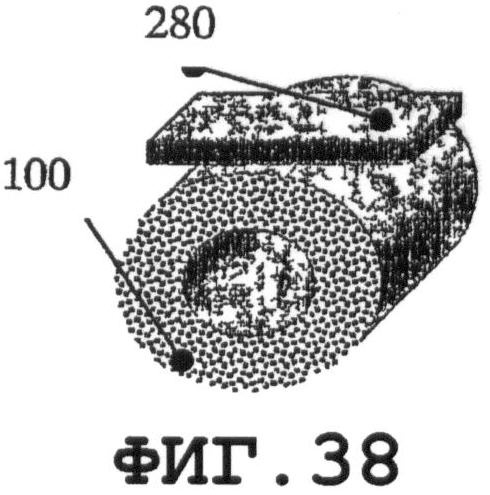
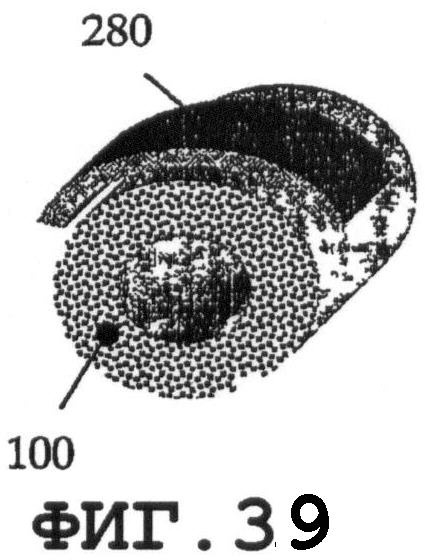
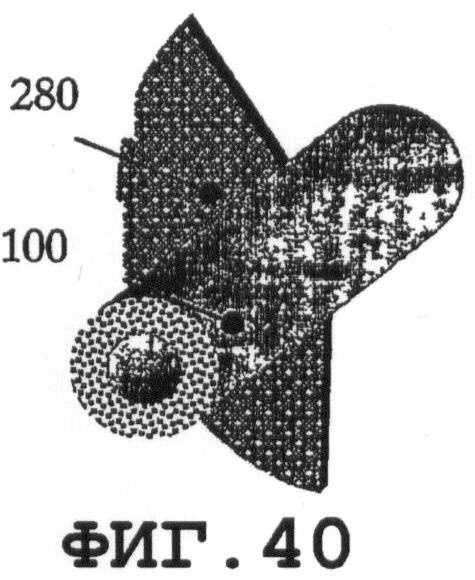
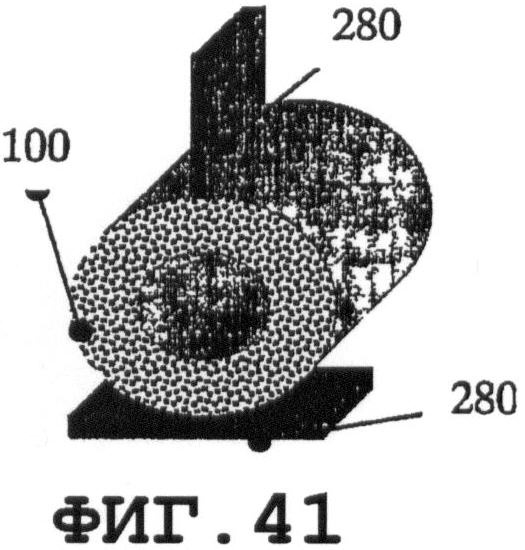
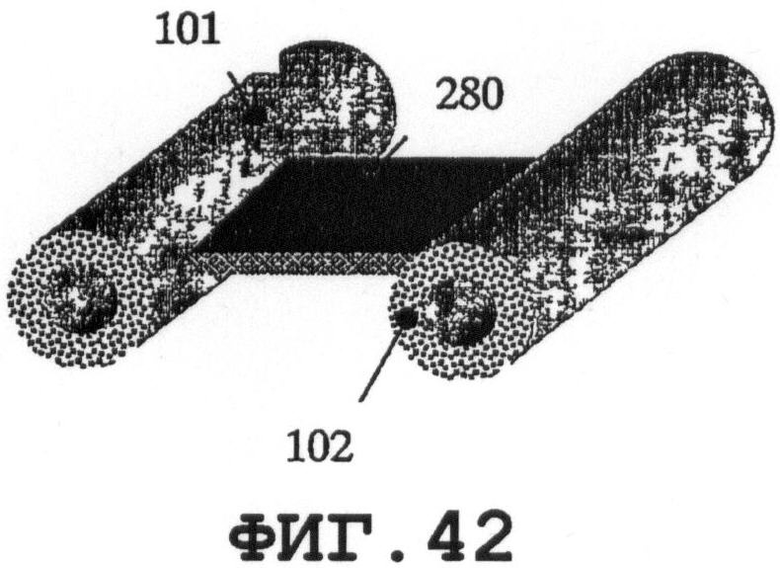
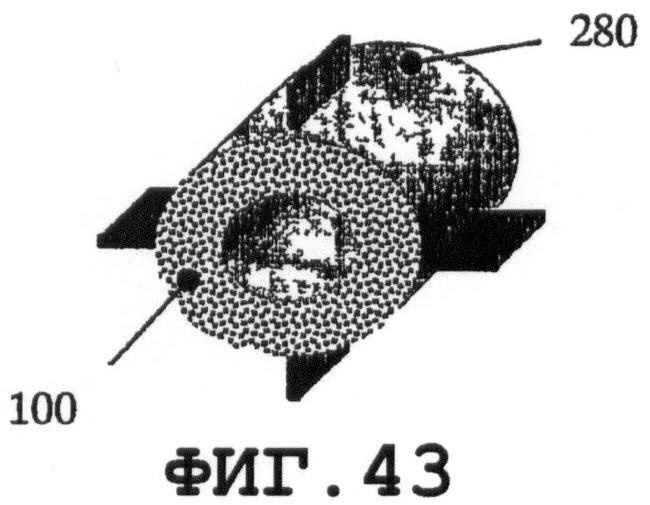
На фиг.36-44 показаны соединения вышеописанных резонаторов 280 с медицинским устройством 100 или разными его частями. Предлагаемые примеры применимы при встраивании пьезорезонаторов в новые медицинские устройства. По меньшей мере, один резонатор SAW-процесса можно присоединять к одному медицинскому устройству.
Фиг.42 поясняет предлагаемое применение одного пьезорезонатора 280 для возбуждения SAW на разных частях медицинского устройства 101 и 102. Фиг.36-38 поясняют предлагаемые варианты присоединения одной и той же пьезопластины 280 к медицинскому устройству 100. Ориентацию пластины относительно медицинского устройства следует выбирать с учетом требуемого SAW-процесса и конструктивных (геометрических) особенностей медицинского устройства. На фиг.39 показано присоединение оболочечной пьезопластины 280. На фиг.40 показана предлагаемая тонкая пьезопластина 280 в форме сегмента кольца. Варианты применения с использованием, по меньшей мере, двух пьезопластин 280 схематично показаны на фиг.41 и 43. На фиг.44 показано предлагаемое изобретение в варианте, когда элемент 280 фиксации медицинского устройства состоит из оболочечных пьезоэлементов 280.
Высокая концентрация вязких липких твердых частиц может приводить к образованию отложений. Устройства могут покрываться слоями отложений данных твердых частиц. В данных обстоятельствах образование отложения не препятствует SAW-процессу или эффективному проведению процесса на поверхности отлагающегося материала.
На фиг.45 (А, В, С) представлены результаты экспериментов, проведенных авторами in vitro для подтверждения безопасности возбуждаемых SAW применительно к биологическому действию (воздействие на присоединенный монослой клеток в культурах тканей). В следующих экспериментах авторы моделировали разные уровни энергии, испускаемой медицинским устройством на внутренней поверхности колбы с тканью.
Целью данных экспериментов было изучение воздействия обработки нановолнами на человеческие клетки в монослое культуры ткани. Исследовали клеточную линию U87MG человеческой глиобластомы и клеточную линию ARPE19 эпителиальных клеток пигмента сетчатки человека (нормальные, неканцерогенные). Клетки высевали в 25-см2 колбы (Corning) для выращивания культуры ткани, при этом резонаторы были приклеены к внешней поверхности колб, чтобы не нарушить их стерильность. Устройства активизировали в инкубаторе для культур тканей, при 37°С и 5% СО2, в продолжение 48 часов. Затем культуры промывали раствором PBS (фосфатно-буферным раствором), фиксировали метанолом, окрашивали красителем Гимза по Мею-Грюнвальду и исследовали под микроскопом. Резонаторы приклеивали к внешней нижней поверхности 25-см2 колбы для выращивания культуры ткани (фирмы Costar). Один набор элементов возбуждал колебания на частоте 220 кГц с амплитудой 0,22 кПа акустического давления. На другой набор колб приклеивали элементы, возбуждающие колебания 285 кГц, 1,2 кПа.
Результаты представлены на фиг.45. Как можно видеть, клетки в активной (45В, 45С) группе сохраняли нормальную морфологию, не замечено признаков или случая апоптоза (утраты клеток), поскольку апоптические тела (содержащих фрагменты ядер) не наблюдались. Отсутствуют также свидетельства разрушения монослоя клеток, остатков мертвых клеток или вызова гибели клеток при некрозе. Авторы не смогли обнаружить каких-либо вредных воздействий обработки ни на одну из культур клеток.
Нижеописанные применения иллюстрируют множество разных случаев, когда имеет значение проблема предотвращения образования биопленки. Медицинские устройства постоянной установки, например периферийные и особенно центральные венные катетеры, все чаще применяют при интенсивной терапии и в общих медицинских палатах для введения внутривенных жидкостей и материалов крови, лекарственных средств, парентерального питания. Образование колоний микроорганизмов на катетере является одним из факторов риска, сопутствующих внутривенным катетерам. Поэтому большое значение имеет возможность формирования поверхностных акустических волн (процесса создания виртуального нановибрационного покрытия) по всем поверхностям медицинского устройства посредством сообщения незначительной энергии механических колебаний медицинскому устройству, что в результате не допускает прикрепления бактерий и попадания микроорганизмов с внешних и внутренних поверхностей. Кроме того, SAW-процесс ослабляет трение и механические напряжения во время введения и извлечения медицинского устройства.
Контролируемый SAW-процесс обеспечивает толкание или натягивание материалов, включая жидкости и подвешенные в них твердые частицы, по поверхности медицинских устройств. В некоторых случаях может принести пользу использование разных энергий колебаний для создания разных условий и стимулирования роста, выбранных в предпочтении перед другими. Это означает возможность выбора бактерий, которые различаются по их способности к прикреплению и образованию сообществ.
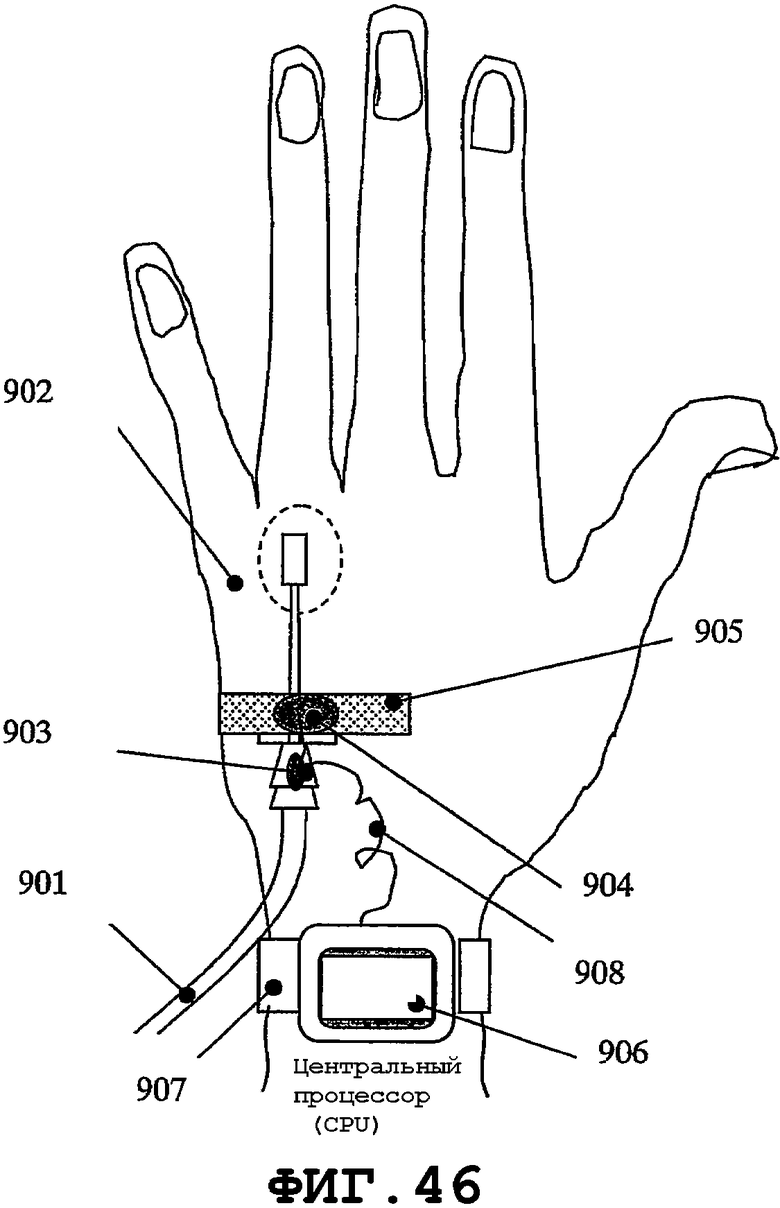
На фиг.46 показано еще одно предлагаемое применение технологии со стандартной периферической внутривенной катетерной системой, состоящей из катетера 901 с трубкой. Данный катетер представляет собой типичную систему «внутривенного вливания в больнице», применяемую на руке 902 или предплечье (не показанном) пациента. По меньшей мере, один тонкий пьезорезонатор 903 присоединен к втулке катетера. Пьезорезонатор 903 может содержать свойства обнаружения и контроля SAW-процессов. Возбуждение пьезорезонатора 903 осуществляется посредством CPU 906. В контактной зоне между тканью и медицинским устройством SAW-процесс фокусирует поперечно распространяющуюся механическую энергию, которая влияет на окружающие ткани и предотвращает образование биопленок. Воздействие распространяется вокруг на расстояние несколько миллиметров. Биопленка предотвращается не только на устройстве, но также на соседних тканях. Данное действие соответствует длине волны колебаний до 5 см. Кроме того, часто предотвращаются тромбы и прилипание материала на наконечнике благодаря ослаблению трения жидкости, протекающей через устройство, независимо от направления течения.
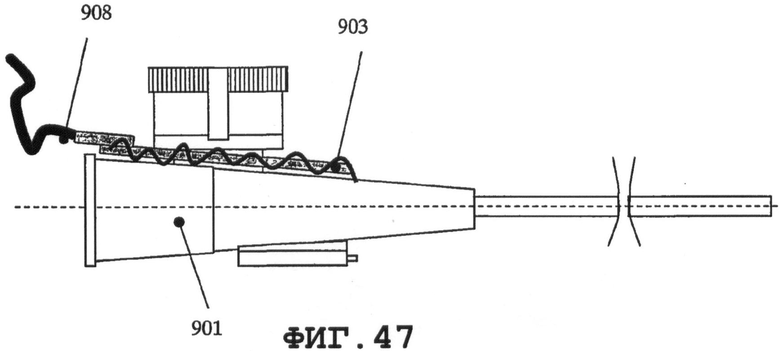
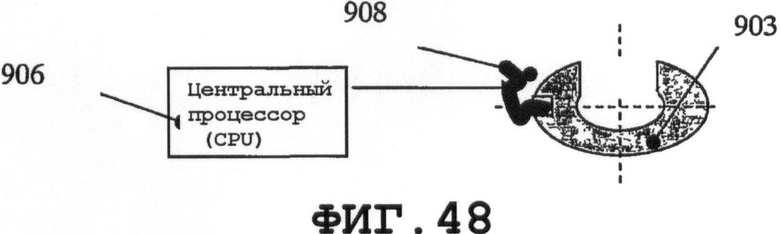
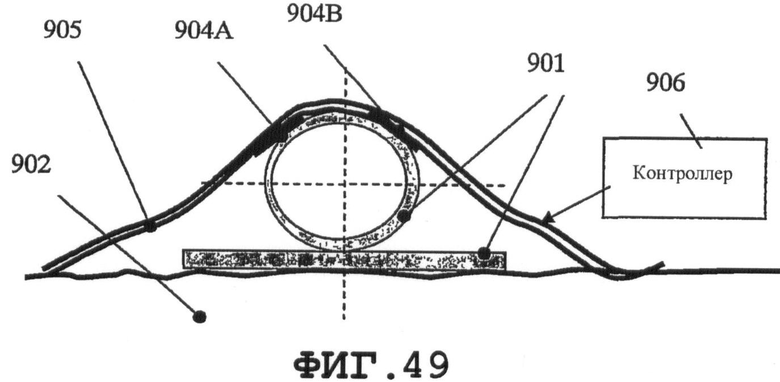
На фиг.46 показаны несколько способов соединения пьезорезонатора с периферической внутривенной катетерной системой, когда последняя присоединена к руке 902 пациента. В первом случае тонкий пьезорезонатор имеет форму тонкого сегмента 903 кольца (в виде, показанном на фиг.47 и 48), механически прикрепленного к соединителю катетера или встроенного в него. Другое применение показано на фиг.46 и 49, где пьезорезонатор 904 (по меньшей мере, один) заделан в клейкую ленту 905.
На фиг.49 показана клейкая лента 905 с двумя тонкими пьезорезонаторами 904А и 904В, которые можно присоединять к катетерной системе 901 с целью возбуждения процесса создания нановибрационного покрытия. Пьезорезонаторы 904А и 904В содержат элементы датчика и возбудителя для возбуждения SAW и контроля данного процесса. Пьезорезонаторы 903 и 904 возбуждаются сигналами от CPU 906, проходящими через несколько управляющих устройств. Смотри фиг.46. CPU 906 может быть прикреплен к руке 902 пациента ремнем 907 или другим средством, например клейкой лентой. CPU 906 соединен с пьезорезонаторами 903 и 904 (совместно или раздельно) посредством провода 908.
На фиг.49 показано другое применение предлагаемого изобретения, когда CPU 906 соединяют с пьезорезонаторами 904А и 904В, при этом резонаторы и их электропровода присоединены к медицинскому устройству клейкой лентой 905. CPU 906 способен возбуждать колебания и принимать электрические сигналы от данных элементов. Работа CPU 906 описана выше, и его схема показана на фиг.2. Кроме того, резонатор 903 или 904 для возбуждения процесса создания нановибрационного покрытия может быть размещен на любой части постоянного сосудистого катетера.
На фиг.50 показана тонкая пьезопластина 910 специальной дисковидно-кольцевой формы, присоединенная к соединителю 909. Внутренняя пластина 911 дисковидно-кольцевой пластины 910 служит средством присоединения к соединителю. Пластины 910 и 911 могут не только возбуждать SAW (виртуальное нановибрационное покрытие), но одновременно могут действовать как датчики распространения SAW по частям медицинского устройства постоянной установки.
На фиг.51 и 52 показана система 912 центрального венного катетера, закрепленного на теле пациента 913. Катетерная система 912 вводится по вене в шее (внешней или внутренней яремной вене) или вене в верхней части груди под ключицей (подключичной вене) в большую центральную вену в груди (полую верхнюю вену) 914. Два общих типа катетерных систем 912, которые постоянно размещаются под кожей 913: без выхода катетера через кожу (внутренний катетер) или с катетером, выходящим через кожу (внешние катетеры). Синтетические вещества, применяемые при лечении пациента катетерной системой, контактируют с тканью на некоторой стадии и имеют отношение к осложнениям. Предлагаемое изобретение оптимизирует биосовместимость и ослабит вызываемые биоматериалом осложнения, например инфицирование и образование корки в мочевых путях, сосудистых системах, и осложнения, связанные с имплантатами. Механизм изобретения использует поверхностные акустические волны, вызывающие вибрацию материала конструкции, что ведет к снижению коэффициента трения биоматериала и тем самым улучшает биосовместимость за счет ослабления раздражения трением и адгезии клеток на поверхности контакта биоматериала с тканью. Процесс осаждения и образования кристаллов (кинетически ускоряемый в присутствии неровных поверхностей, отверстий и кромок катетера) будет замедляться.
На фиг.51 показаны две тонких пьезопластины 915А и 915В, присоединенных к отдельным просветам центрального катетера (внешней части катетера) и электрически соединенных с CPU 906 для возбуждения процесса создания нановибрационного покрытия. Пластины 915А и 915В могут работать в одном или раздельных режимах при возбуждении распространяющейся SAW.
На фиг.52 представлено другое применение предлагаемого изобретения, в котором клейкую ленту с тонкой пьезопластиной 916 применяют в системе центрального венного катетера. Тонкие пьезоэлектрические возбуждающие пластины 903, 905, 915А, 915В и 916 можно устанавливать на любую часть катетерной системы внутривенного вливания, в том числе 901 и 912, без ограничения емкостями для жидкости, насосами или другим вспомогательным оборудованием.
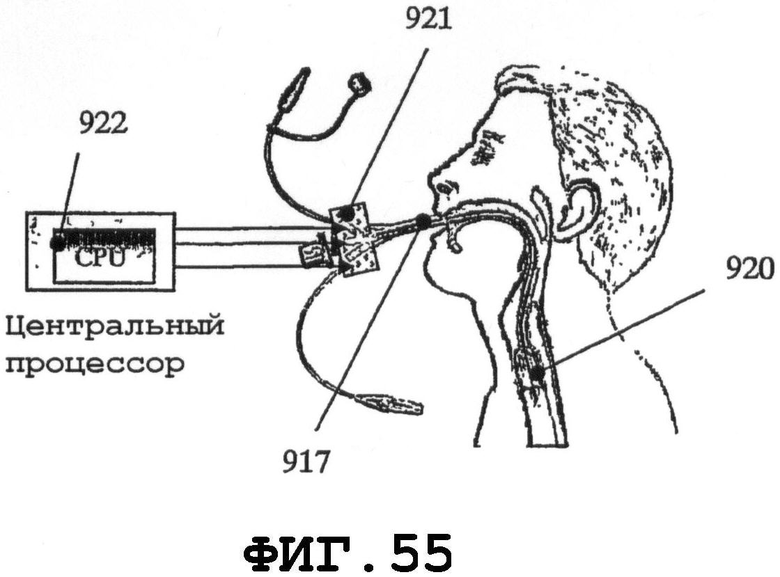
Проблемы биосовместимости связаны с другой категорией устройств постоянной установки - эндотрахеальными трубками для вентиляции легких. Данные проблемы являются главной причиной смертей из-за пневмонии, обусловленной биопленками. На фиг.53-55 представлен другой вариант осуществления изобретения, в котором резонаторы SAW разного типа присоединены к системе 917 эндотрахеальной трубки для вентиляции легких. На фиг.53 представлен вариант осуществления с резонатором SAW на тонком пьезоэлементе 918 в форме оболочки, прикрепленном к центральной трубке катетера или встроенном в него. На фиг.54 представлен вариант осуществления, в котором резонатор SAW имеет форму пьезодиска 919 с крепежным отверстием или объединен с каналом наддува баллона 920. На фиг.55 представлен другой вариант осуществления, в котором резонатор SAW содержит систему 921 из нескольких пьезоэлементов, присоединенных к отдельным просветам катетерной системы 917. CPU 922 позволяет вышеупомянутым резонаторам 918, 919 и 921 SAW возбуждать поверхностные механические колебания на внешних поверхностях баллона 920. Шкала частот механических колебаний имеет протяженность от 10 кГц до МГц. Коэффициент заполнения может изменяться от 1:1 до 1:1000. Амплитуды перемещений измеряются нанометрами. Акустическая мощность меньше чем 1 мВт/см2. Эндотрахеальная трубка для вентиляции легких, например трубка, показанная на фиг.53-55, является оборудованием, сопряженным с высоким риском заражения при стандартном применении на практике аппаратов для вентиляции легких. Благодаря SAW-процессу, поперечно распространяющаяся механическая энергия воздействует на контактные жидкости и тем самым ослабляется трение жидкостей. Вибрация изгоняет жидкость и способствует процессу высушивания в точке контакта с кожей, что обеспечивает сопротивляемость попаданию бактерий.
Проблему создают вызываемые катетером инфекции мочевых путей (CAUTI), так как катетеры являются главным резервуаром резистентных патогенных микроорганизмов. Предлагаемое изобретение по возбуждению SAW на поверхностях медицинского устройства постоянной установки и в результате предотвращения данных инфекций, без сомнения, будет важным шагом в борьбе с резистентностью к антибиотикам.
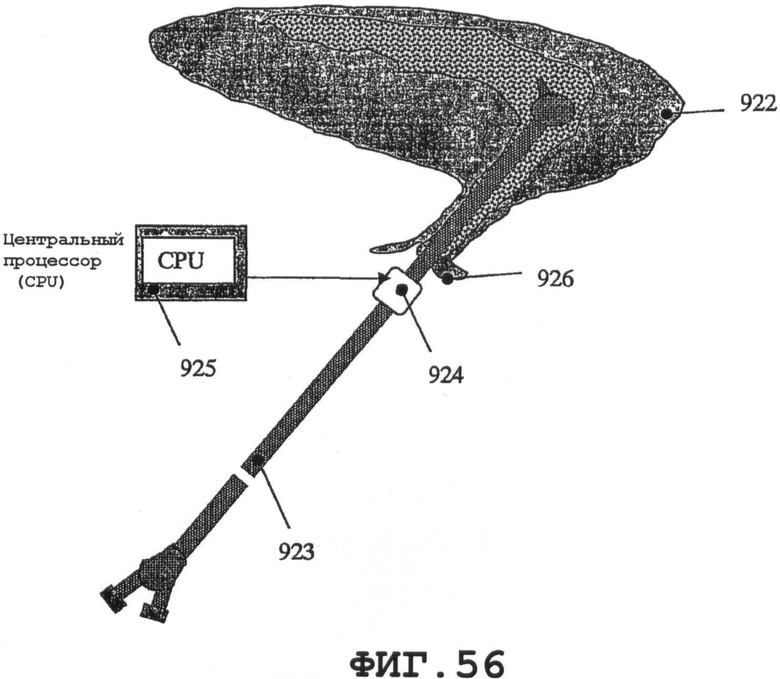
На фиг.56 и 57 схематично показаны дополнительные применения процесса возбуждения SAW для системы 922 мочевых путей. На фиг.56 изображена трубка 923 уринального катетера с присоединенным тонким пьезоэлементом 924, подключенным соответственно к CPU 925. Катетер 923 с баллоном вставлен в мочевой путь 922, и, благодаря возбуждению механических нанометровых колебаний, образование биопленки предотвращается на всех поверхностях катетера 923. Процесс возбуждения SAW характеризуется дополнительным аспектом поперечного распространения. Это означает, что энергия может передаваться в ткани человеческого тела с внешних поверхностей и передаваться в биологическое вещество, контактирующее с внутренней поверхностью устройства.
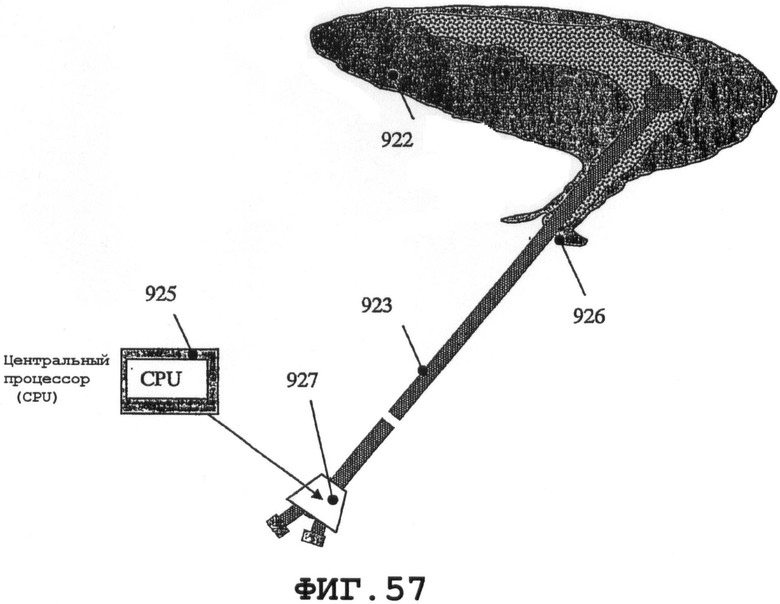
На фиг.56 представлен принцип другого применения предлагаемого изобретения, устройства 924 «Uroshield» (тип 010), которое создано компанией Nanovibronix Inc., для предотвращения образования биопленок на мочеточниковых катетерах. Другое решение сопряжения для того же устройства показано на фиг.57. Несколько пьезоэлементов 927 присоединяют в точках перехода на катетере.
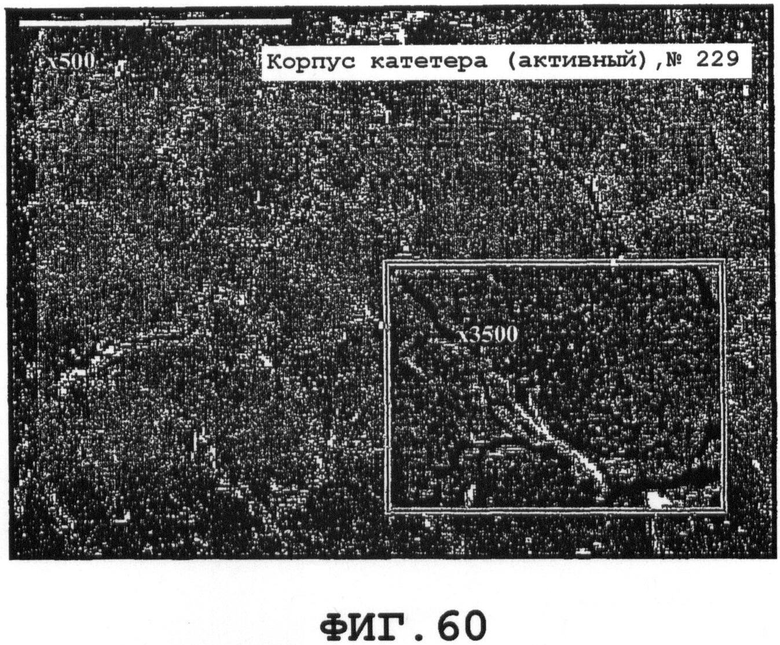
На фиг.58-61 представлены результаты исследований in vivo. Целью исследования была оценка безопасности и эффективности устройства Uroshield (смотри фиг.56) с точки зрения замедления/предотвращения образования биопленки на мочеточниковых катетерах на кроликах. Конечным пунктом исследования была проверка эффективности SAW с точки зрения замедления/предотвращения накопления бактерий, а также подавления или исключения образования биопленки с использованием сканирующего электронного микроскопа (SEM). Кроме того, применительно к такому целевому ориентиру, как безопасность, исследовали воздействие SAW на мочевые пути с оценкой методом гистопатологии. Безопасность изучали сравнением гистопатологических образцов мочевых путей в обеих группах следующим путем.
1. Ежедневная оценка функционирования устройства Uroshield с использованием устройства для проверки на пригодность, измеряющего частоту, амплитуду, соединители, ток и акустические данные в соответствии с заданным набором параметров.
2. В конце экспериментальных животных умертвляли и вскрывали и катетер извлекали изнутри мочевого пузыря и мочеиспускательного канала, вместе с прилегающей слизистой оболочкой. Катетер погружали в 4% буферный формальдегид и отправляли на анализ методом SEM (сканирующей электронной микроскопии). Срезы слизистой оболочки мочевых путей собирали в 4% буферный формальдегид из воронки мочевого пузыря, из среднего пузыря, треугольной области, проксимального мочеиспускательного канала и дистального мочеиспускательного канала для гистологических анализов. Катетер делили на секции по акустической мощности. Амплитуды акустического давления в точках излучения на катетере делили следующим образом: D - корпус; В - баллон; максимальная амплитуда акустического давления в разных точках уринального катетера: корпус - D, Pmax=0,14 (кПа); максимальная амплитуда акустического давления на баллоне мочеточникового катетера - В, Pmax=1,2 (кПа).
Результаты
Результаты показывают, что:
процентная доля активных животных, сохраняющих стерильность на протяжении эксперимента = 50% (2 из 4);
процентная доля контрольных животных, сохраняющих стерильность на протяжении эксперимента = 0%;
среднее время до бактериурии у активных животных, у которых развилась инфекция = 5 суток;
среднее время до бактериурии у контрольных животных = 1,5 суток.
Все части катетера тщательно исследовали: нижеприведенные оценки методом SEM выполняла исследовательская группа из компании авторов.
Кролик 229 (активный, корпус катетера от кролика №229) - при исследовании всех частей катетера (за исключением наконечника, который отсутствовал) не обнаружилось никаких признаков образования биопленки или присутствия бактерий. Материал на катетере оказался клеточными остатками, коагулированными белками, частицами латекса и силикона. Клетки спермия наблюдались на внешней поверхности корпуса, а внутренняя поверхность была в значительной степени покрыта кристаллами.
Кролик 143 (активный, корпус катетера от кролика №143) - немного биопленок обнаружили только на баллоне, тогда как на других частях катетера биопленок не найдено. Многочисленные эритроциты наблюдались на внутренней поверхности катетера.
Кролик 31 (контрольный, корпус катетера от кролика №31) - мощные толстые биопленки наблюдались на всех частях катетера. Некоторые из биопленок отделяли от катетера. Латекс и силикон были отслоены, и присутствовала слизистая ткань, прилипшая к катетеру.
Кролик 150 (контрольный, корпус катетера от кролика №150) - катетер был покрыт биопленками, и скопления бактерий были разбросаны по всей поверхности, в частности, особенно много на баллоне и внутренней поверхности корпуса. Слой силикона был отслоен, и клетки спермия были разбросаны по всей поверхности.
В общих словах: шестьдесят шесть процентов контрольных катетеров было покрыто мощными биопленками и скоплениями бактерий. Образцы катетеров кроликов 31 и 150 были покрыты мощными биопленками, тогда как катетер кролика 28 характеризовался только среднемощными структурами биопленок, разбросанными на разных частях катетера. На поверхности 75% активных катетеров отсутствовали биопленки и скопления бактерий. Образцы катетеров кроликов 163 и 229, которые оставались стерильными (бактериурия равна 0) в течение 7 и 9 суток соответственно, не были покрытыми биопленками или бактериальными скоплениями. Биопленки наблюдались на поверхности катетера кролика 265 (несмотря на то что на катетер активно действовала вибрация). Однако бактериурия развилась у кролика 265 в течение последних 2 суток исследования. Уровень бактериурии в последние сутки составлял 106 CFU/мл, т.е. достаточно высокий уровень для создания возможности образования биопленок. Данные результаты предполагают, что образование биопленок на поверхности катетера коррелируется с уровнем бактериурии.
Независимое слепое исследование фигур с SEM-изображениями образцов катетеров проводилось специалистом по электронной микроскопии.
Экспериментальные результаты подтвердили, что, в случае образования биопленок как независимо, так и в зависимости от медицинского устройства, подведение наноколебательных волн (а) ослабляло существующие биопленки и (b) усиливало и улучшало действие антибиотиков на биопленку (ослабляло резистентность биопленки к антибиотикам). Возможность возбуждения процесса создания направленного нановибрационного покрытия с движением в соответствии с естественным дренажом и поток жидкостей, производимых телом в данном месте (для наружной и трахеальной жидкости, мочи и т.д.), имеют следствием вытеснение или замедление проникания бактерий в полость тела. Все упомянутые факторы значительно замедляют инфицирование.
Экспериментальные результаты подтвердили, что резонаторы 924 и 927 SAW в качестве устройств для предотвращения образования биопленок можно устанавливать на любую предпочтительную часть медицинского устройства: соединитель, приемник или любое вспомогательное оборудование (например, показанное на фиг.56 и 57).
На фиг.62 и 63 схематично показаны дополнительные возможные варианты. Мочеприемник 928 может быть закреплен на ноге пациента 929, тогда как CPU 930 с аккумуляторной батареей закреплен на ремне 931. Пьезорезонатор 932 SAW может быть присоединен к соединительной трубке 933, и электрический сигнал может подаваться по кабелю 934 из CPU 930, как показано на фиг.62. Другой вариант осуществления содержит дополнительный резонатор 935 SAW, присоединенный к мочеприемнику 928 или встроенный в него.
На фиг.64 и 66 показаны дополнительные возможные варианты. На фиг.64 представлен резонатор 936 SAW (допускается вышеописанного типа Uroshield), присоединенный к сборной трубке 937 мочеприемника 938. CPU 939 передает электрические сигналы в пьезоэлемент 936 (может быть, по меньшей мере, один), и пьезоэлементы возбуждают колебания. Это вызывает процесс предотвращения образования биопленки как в системе мочеточникового катетера, так и в емкости мочеприемника.
На фиг.65 схематично показано другое применение, в котором, по меньшей мере, один пьезорезонатор 940 с CPU 941 присоединены к мочеприемнику 938. Несколько тонких пьезоэлементов 940 можно поместить на стенку мочеприемника 938 (при желании, на одну или две противоположные стенки). В данном случае могут быть созданы противоположные наноколебательные волны, и могут происходить два отдельных акустических процесса: возбуждение SAW, когда пьезоэлемент присоединен к одной стенке; и процесс формирования стоячих волн в собранной моче, когда два пьезоэлемента присоединены к противоположным стенкам. Первый процесс позволяет предотвратить образование биопленки; второй процесс позволяет убивать бактерий в моче. Два данных пьезоэлемента размещают противоположно один другому, причем, при небольшой подводимой энергии, они могут формировать стоячие акустические волны, характеризующиеся высоким динамическим давлением (процесс кавитации). Недавно показано, что свободно плавающие бактерии способны каким-то образом согласовывать свое движение в жидкости с координацией массового движения сообщества. Нановибрационная обработка путем пропускания упругих волн в жидкость дезорганизует согласованное движение сообщества. Это приводит к замедлению организованного действия сообществ.
На фиг.66 показаны экспериментальные результаты с мочеприемником. Контейнер для жидкости с минимумом питательной среды и 104/мл бактерий (Pseudomonas Aeuriginosa) культивировали при 37°С в течение 12 суток. Контейнер с присоединенным возбудителем свидетельствует о применении SAW-процесса. Жидкость в данном контейнере с возбудителем была чистой, контрольная жидкость была мутной. Лабораторные результаты показывают сокращение на 2 порядка по сравнению с контрольным образцом (бактериальное загрязнение в активируемом контейнере составляло 106/мл против 108/мл в контрольном контейнере). На фотографиях видна прозрачная жидкость из контейнера 942 с тонкими пьезовозбудителями. Жидкость в контрольном контейнере 943 была непрозрачной вследствие ферментации среды бактериями.
Предлагаемая технология позволяет предотвращать образование биопленок в любой части системы, которая может быть оборудована возбудителями. Ткани тела, которые находятся в контакте с активируемым медицинским устройством, являются защищенными. Таким образом, артерии, вены, слизистые оболочки и другие органы и полости тела защищают от образования колоний бактерий и биопленок. Кроме того, если SAW-процесс возбуждается на медицинском устройстве постоянной установки, данный процесс можно дополнительно распространять на артерии, вены, мочевые пути и другие полости тела, в которые введено устройство.
Дополнительное пропускание SAW может оказывать положительное влияние на проблемные точки в теле пациента.
Никакие из вышеупомянутых описаний и вариантов осуществления не ограничиваются использованием в медицинских устройствах. Специалистам в данной области техники должно быть очевидно, что SAW на устройствах в соответствии с настоящим изобретением можно вводить, или встраивать, или объединять с любым ожидаемым в будущем медицинским устройством или приспособлениями.
| название | год | авторы | номер документа |
|---|---|---|---|
| УЛЬТРАЗВУКОВОЙ ПРЕОБРАЗОВАТЕЛЬ | 1992 |
|
RU2067789C1 |
| Датчик силы | 1980 |
|
SU917007A1 |
| Устройство для генерации ультразвуковых импульсов | 1988 |
|
SU1547084A1 |
| СПОСОБ ГЕНЕРАЦИИ СТАБИЛЬНЫХ КОЛЕБАНИЙ | 2009 |
|
RU2389129C1 |
| УЛЬТРАЗВУКОВОЙ НАКЛОННЫЙ ПРЕОБРАЗОВАТЕЛЬ | 2007 |
|
RU2356044C1 |
| УСТРОЙСТВО ЭЛЕКТРОФИЗИЧЕСКОГО ВОЗДЕЙСТВИЯ НА АЭРОЗОЛИ | 2010 |
|
RU2430509C1 |
| Ультразвуковой низкочастотный преобразователь | 2024 |
|
RU2835372C1 |
| СЕНСОР, СИСТЕМА И МЕТОД ДЛЯ ИЗМЕРЕНИЯ СВОЙСТВ ТЕКУЧЕЙ СРЕДЫ С ИСПОЛЬЗОВАНИЕМ МНОГОМОДОВОГО КВАЗИ - СДВИГОВОГО - ГОРИЗОНТАЛЬНОГО РЕЗОНАТОРА | 2009 |
|
RU2451287C2 |
| Пъезоэлектрический фильтр | 1979 |
|
SU938368A2 |
| ТЕРМОКОМПЕНСИРОВАННЫЙ КВАРЦЕВЫЙ ГЕНЕРАТОР | 2011 |
|
RU2455754C1 |












Группа изобретений относится к медицине, а именно к медицинским устройствам постоянной установки в теле пациента, и предназначена для препятствования образованию биопленки, связанной с данным устройством, и попаданию микроорганизмов в тело пациента. Предлагаются устройство и способ для предотвращения образования биопленки, связанной с медицинским устройством постоянной установки. Способ заключается в формировании поверхностных акустических волн посредством пластинчатого пьезорезонатора, колеблющихся с частотами второй и высших гармоник в диапазоне от 0,02 до 50 МГц по поверхностям медицинского устройства постоянной установки в теле пациента. Данный пластинчатый пьезорезонатор может содержать биморфный элемент, содержащий пьезокерамический слой и металлический слой. Устройство включает пластинчатый пьезорезонатор, выполненный с возможностью генерирования поверхностных акустических волн, колеблющихся с частотами второй и высших гармоник в диапазоне от 0,02 до 50 МГц по поверхностям медицинского устройства постоянной установки в теле пациента. Устройство может включать источник энергии для возбуждения пластинчатого пьезорезонатора, управляемый центральным процессором. Группа изобретений позволяет предотвратить образование бактериальной биопленки на медицинских устройствах постоянной установки в теле пациента. 5 н. и 38 з.п. ф-лы, 66 ил., 2 табл.
1. Способ препятствования образованию биопленки, связанной с медицинским устройством постоянной установки в теле пациента, при этом медицинское устройство постоянной установки в теле пациента содержит пластинчатый пьезорезонатор с поляризацией по толщине, и способ включает формирование посредством пластинчатого пьезорезонатора акустических волн, колеблющихся с частотами второй и высших гармоник в диапазоне частот от 0,02 до 50 МГц по поверхностям медицинского устройства постоянной установки в теле пациента, создавая энергию механических колебаний в указанном медицинском устройстве, таким образом, препятствуя прикреплению бактерий к медицинскому устройству постоянной установки в теле пациента и, следовательно, попаданию микроорганизмов в тело человека.
2. Способ по п.1, в котором поверхностные акустические волны распространяются по всем поверхностям медицинского устройства постоянной установки в теле пациента.
3. Способ по п.1, в котором амплитуда поверхностных акустических волн изменяется в диапазоне от 1 до 50 нм.
4. Способ по п.1, в котором частоты второй и высших гармоник поверхностных акустических волн изменяются в диапазоне от 0,02 до 1,0 МГц.
5. Способ по п.1, в котором пластинчатый пьезорезонатор является пьезокерамическим резонатором.
6. Способ по п.1, в котором пластинчатый пьезорезонатор соединен с источником энергии для возбуждения указанного пластинчатого пьезорезонатора.
7. Способ по п.6, в котором источник энергии является электромеханическим источником энергии.
8. Способ по п.6, в котором источник энергии является электромагнитным источником энергии.
9. Способ по п.1, в котором медицинское устройство постоянной установки в теле пациента представляет собой катетер.
10. Способ по п.1, в котором указанный пластинчатый пьезорезонатор генерирует поверхностные акустические волны в моде продольных колебаний, за счет чего указанные поверхностные акустические волны приложены к внешней поверхности медицинского устройства постоянной установки в теле пациента.
11. Способ по п.1, в котором указанный пластинчатый пьезорезонатор резонирует в моде колебаний по толщине, за счет чего указанные поверхностные акустические волны приложены к внутренней поверхности медицинского устройства постоянной установки в теле пациента.
12. Способ по п.1, в котором указанный пластинчатый пьезорезонатор резонирует в моде изгибных колебаний, за счет чего указанные поверхностные акустические волны приложены к внутренней поверхности медицинского устройства постоянной установки в теле пациента.
13. Способ по п.12, в котором указанные колебания изгибной моды имеют период, соответствующий длине волны поверхностных акустических волн на медицинском устройстве постоянной установки в теле пациента.
14. Способ по п.1, в котором указанный пластинчатый пьезорезонатор резонирует в моде колебаний, выбранной из группы, включающей моду по толщине, продольную моду, изгибную моду и комбинацию указанных мод.
15. Способ по п.1, в котором пластинчатый пьезорезонатор содержит биморфный элемент, содержащий пьезокерамический слой и металлический слой.
16. Способ по п.15, в котором пьезокерамический слой и металлический слой находятся во взаимном соотношении от 0,95 до 1,35.
17. Способ по п.6, в котором указанный источник энергии управляется центральным процессором для генерирования электрических сигналов, которые преобразуются указанным пластинчатым пьезорезонатором в механические колебания, имеющие нмую амплитуду.
18. Способ по п.17, в котором указанный пластинчатый пьезорезонатор выполнен с возможностью определять поверхностные акустические волны на поверхности медицинского устройства постоянной установки в теле пациента.
19. Способ по п.18, в котором указанный пластинчатый пьезорезонатор выпонен с возможностью регулировать энергию механических колебаний, доставляемых к указанному медицинскому устройству постоянной установки в теле пациента в ответ на поверхностные акустические волны, определенные указанным пластинчатым пьезорезонатором.
20. Способ по п.1, в котором медицинское устройство постоянной установки в теле пациента представляет собой катетер, имеющий втулку или соединитель и пластинчатый пьезорезонатор прикреплен к втулке или соединителю.
21. Способ по п.1, в котором пластинчатый пьезорезонатор содержит множество электродов для выборочного изменения мод колебаний, генерируемых пластинчатым пьезорезонатором.
22. Способ по п.15, в котором пластинчатый пьезорезонатор соединен с электродами, расположенными вне центральной области указанного биморфного элемента, таким образом, обеспечивая стабильность частот второй и высших гармоник, создаваемых пластинчатым пьезорезонатором.
23. Способ по п.5, в котором пластинчатый пьезорезонатор соединен с медицинским устройством постоянной установки в теле пациента посредством клейкого слоя.
24. Способ по п.1, в котором медицинское устройство постоянной установки в теле пациента выбрано из группы, включающей внутривенный катетер, уринальный катетер, гастрокатетер, легочный катетер, сердечнососудистый катетер и эндотрахеальную вентилирующую трубку.
25. Устройство для препятствования образованию биопленки на поверхностях медицинского устройства постоянной установки в теле пациента, содержащее пластинчатый пьезорезонатор, выполненный с возможностью генерирования поверхностных акустических волн, колеблющихся с частотами второй и высших гармоник в диапазоне частот от 0,02 до 50 МГЦ по поверхностям медицинского устройства постоянной установки в теле пациента, препятствуя прикреплению бактерий к поверхностям.
26. Устройство по п.25, в котором поверхностные акустические волны имеют амплитуды, которые изменяются в диапазоне от 1 до 50 нм.
27. Устройство по п.26, в котором поверхностные акустические волны имеют частоты, которые изменяются в диапазоне от 1 Гц до 50 МГц.
28. Устройство по п.25, в котором пластинчатый пьезорезонатор содержит биморфный элемент, содержащий пьезокерамический слой и металлический слой.
29. Устройство по п.28, в котором пьезокерамический слой и металлический слой находятся во взаимном соотношении от 0,95 до 1,35.
30. Устройство по п.25, в котором медицинское устройство постоянной установки в теле пациента содержит втулку или соединитель, и пластинчатый пьезорезонатор прикреплен к втулке или соединителю.
31. Устройство по п.25, в котором пластинчатый пьезорезонатор содержит пьезокерамическую пластину.
32. Устройство по п.31, в котором пьезокерамическая пластина имеет форму, выбранную из группы, включающей круглую, прямоугольную, кольцевую и дисковидную формы.
33. Устройство по п.25, дополнительно содержащее средство для определения поверхностных акустических волн на поверхности указанного медицинского устройства постоянной установки в теле пациента.
34. Способ создания поверхностных акустических волн на поверхности медицинского устройства постоянной установки в теле пациента, включающий обеспечение пластинчатого пьезорезонатора, прикрепленного к устройству постоянной установки в теле пациента, генерирование посредством пластинчатого пьезорезонатора колебаний второй и высших гармоник и распространение вибрации с частотой второй и высших гармоник по поверхностям медицинского устройства постоянной установки в теле пациента, препятствуя прикреплению бактерий и результирующему образованию биопленки на поверхностях устройства постоянной установки в теле пациента.
35. Способ по п.34, в котором колебания с частотой второй и высших гармоник находятся в диапазоне от 0,02 до 50 МГц.
36. Способ создания бегущих поверхностных акустических волн: как Релея, так и псевдо-поверхностных акустических волн, на поверхности упругого медицинского устройства, включающий
обеспечение по меньшей мере одного тонкого биморфного пластинчатого пьезорезонатора поверхностных акустических волн, содержащего по меньшей мере один тонкий слой пьезоэлектрического материала с поляризацией по толщине, механически прикрепленный к тонкой опорной пластине,
и выполненный с возможностью формирования в ней колебаний во второй и высших гармониках собственных мод колебаний в диапазоне частот от 0,02 до 50 МГц с возникающими при этом двумя или более максимальными амплитудами колебаний в опорной пластине, при этом опорная пластина механически прикреплена к поверхности упругого медицинского устройства или встроена в нее,
при этом расстояние между двумя максимальными амплитудами собственных колебаний опорной пластины пропорционально длине поверхностной акустической волны на поверхности упругого медицинского устройства, при этом максимальные амплитуды колебаний приводят к процессу распространения поверхностных акустических волн на поверхности упругого медицинского устройства, и длина поверхностных акустических волн составляет не менее 100 мкм, и
каждая точка поверхности упругого медицинского устройства вибрирует с амплитудами, составляющими несколько нм, таким образом, создавая однородное виртуальное нановибрационное покрытие на поверхности упругого медицинского устройства.
37. Устройство для создания бегущих поверхностных акустических волн: как Релея, так и псевдо-поверхностных акустических волн, на поверхности упругого медицинского устройства, содержащее
по меньшей мере один тонкий биморфный пластинчатый пьезорезонатор поверхностных акустических волн, содержащий по меньшей мере один тонкий слой пьезоэлектрического материала с поляризацией по толщине, механически прикрепленный к тонкой опорной пластине,
и выполненный с возможностью формирования в ней колебаний во второй и высших гармониках собственных мод колебаний в диапазоне частот от 0,02 до 50 МГц, с возникающими при этом двумя или более максимальными амплитудами колебаний в опорной пластине, при этом опорная пластина механически прикреплена к поверхности упругого медицинского устройства или встроена в нее,
при этом расстояние между двумя максимальными амплитудами собственных колебаний опорной пластины пропорционально длине поверхностной акустической волны на поверхности упругого медицинского устройства,
при этом максимальные амплитуды колебаний приводят к процессу распространения поверхностных акустических волн на поверхности упругого медицинского устройства, и длина поверхностных акустических волн составляет не менее 100 мкм, и
каждая точка поверхности упругого медицинского устройства вибрирует с амплитудами, составляющими несколько нм, таким образом, создавая однородное виртуальное нановибрационное покрытие на поверхности упругого медицинского устройства.
38. Устройство по п.37, в котором колебания с частотой второй и высших гармоник находятся в диапазоне от 0,02 до 50 МГц.
39. Устройство по п.37, в котором биморфный пластинчатый пьезорезонатор соединен с источником энергии для возбуждения указанного биморфного пластинчатого пьезорезонатора.
40. Устройство по п.39, в котором источник энергии управляется центральным процессором для генерирования электрических сигналов и получения электрических сигналов от одного или более пластинчатых пьезорезонаторов.
41. Устройство по п.40, в котором память центрального процессора имеет информационный вход, соответствующий типу и размеру медицинского устройства.
42. Устройство по п.40, в котором центральный процессор выполнен с возможностью прикрепления к руке пациента посредством клейкой ленты.
43. Устройство по п.38, в котором тонкий слой пьезоэлектрического материала биморфного пьезорезонатора содержит множество электродов для выборочного изменения мод колебаний, генерируемых опорной пластиной биморфного пьезорезонатора.
| US 4698058, 06.10.1987 | |||
| US 2002069893, 13.06.2002 | |||
| ПУСТОТЕЛЫЙ ВКЛАДЫШ В ОГРАЖДАЮЩЕЙ КОНСТРУКЦИИ ЗДАНИЯ | 1993 |
|
RU2087635C1 |
| Способ получения крахмала из пшеницы | 1957 |
|
SU134212A1 |
| СПОСОБ АКУСТИЧЕСКОЙ ОБРАБОТКИ ОБЪЕТА И УСТРОЙСТВО ДЛЯ ВОЗБУЖДЕНИЯ ЗВУКОВЫХ ВОЛН | 1996 |
|
RU2119801C1 |
| СПОСОБ ОБРАБОТКИ ЗАГРЯЗНЕННЫХ ПОВЕРХНОСТЕЙ | 1993 |
|
RU2118575C1 |
Авторы
Даты
2011-05-27—Публикация
2005-05-18—Подача