Область техники, к которой относится изобретение
Настоящее изобретение относится к жидкой композиции, подходящей для эжекции жидкости, включающей, по меньшей мере, один компонент, выбранный из белка и пептида, и способу эжекции жидкой композиции, и к эжекционному устройству с использованием способа эжекции.
Предшествующий уровень техники
Недавно был предпринят ряд попыток использования белковых растворов в виде капелек. Примеры таких попыток включают применение методик образования мельчайших капелек белковых растворов при трансмукозном введении в качестве способа доставки лекарственных средств и в биочипах и биодатчиках, для которых требуются очень небольшие количества белков. Кроме того, при контроле белковых кристаллов и при скрининге физиологически активных веществ внимание привлекли способы применения микрокапелек белка (см. выложенную заявку на патент Японии № 2002-355025, Allain, L. R. et al., “Fresenius J. Anal. Chem.” 2001, Vol. 371, p. 146-150, и Howard, E. I., Cachau, R. E., “Biotechniques” 2002, Vol. 33, p. 1302-1306).
Кроме того, в последнее время начинается массовое производство белков, в частности ферментов и полезных белков, обладающих физиологическими видами активности, благодаря технологии генной рекомбинации. Поэтому способ переработки белка в капельки жидкости может быть полезной методикой для областей поиска, использования и применения белков в качестве новых лекарственных средств. В частности, приобрела значение методика введения биологических веществ, включая белки, пептиды и другие вещества в виде капелек, в легкие. Легкое имеет площадь альвеолярной поверхности, достигающую от 50 до 140 м2, имеет эпителий в качестве барьера абсорбции в виде очень тонкого слоя с размером, доходящим до 0,1 мкм, и, кроме того, имеет ферментную активность, которая ниже по сравнению с пищеварительным трактом. Соответственно, транспульмональное введение привлекло внимание в качестве пути введения, альтернативного инъекции полимерных пептидных лекарственных средств, типичным примером которых является инсулин.
В целом, было известно, что внутрилегочное осаждение микрокапелек лекарственного средства в значительной степени зависит от пневматического размера частиц микрокапелек. Наряду с другими факторами для доставки в альвеолы как глубокой части легких и введения с высокой воспроизводимостью требуются капельки с размером частиц от 1 до 5 мкм и узким распределением размера частиц.
В качестве способа получения капелек лекарственного средства с узким распределением размера частиц сообщалось о применении принципа эжекции жидкости, используемого в краскоструйной печати (см. выложенную заявку на патент Японии № 2002-248171). При эжекции жидкости с использованием краскоструйного устройства жидкость, подлежащая эжекции, вводится в небольшую камеру, и на жидкость оказывается воздействие физической силы для выталкивания капелек из отверстия. Примеры используемых способов эжекции включают способ, в котором пузырьки генерируются за счет использования электротермических преобразователей, таких как тонкопленочные резисторы, для выталкивания капелек из сопел (термическое краскоструйное устройство), и способ, в котором жидкость выталкивается непосредственно из отверстий, расположенных в верхней части камеры, путем использования электромеханических преобразователей, таких как пьезогенераторы (пьезокраскоструйное устройство).
Генерирование капелек, которые составлены из белка или пептидной жидкости, на основе принципа краскоструйного устройства, связано с проблемой, заключающейся в том, что структура белка дестабилизируется вследствие физической силы (например, давления или силы сдвига), воздействующей во время эжекции, или высокой поверхностной энергии, присущей микрокапелькам. Когда используется термическое краскоструйное устройство, термическая энергия также подается на раствор лекарственного средства. Пространственная структура белка или пептида является уязвимой, и, следовательно, после разрушения структуры вызываются агрегация и разрушение белка или пептида и может осуществляться нормальная эжекция. Описанный выше физический эффект намного больше, чем сила сдвига или термическая энергия, воздействующая при обычном перемешивании или тепловой обработке. (Например, в термическом краскоструйном устройстве предположительно одномоментно оказывается нагрузка 300°С и 90 атм). В то же время прилагаются две или более физических сил. Следовательно, устойчивость белка имеет тенденцию к крайне легкому разрушению по сравнению с условиями, в которых обычно обрабатывается белок. При возникновении этой проблемы белок или пептид агрегируется во время получения капелек, вызывая закупорку сопла и затрудняя выталкивание капелек.
Кроме того, капельки с размером частиц от 1 до 5 мкм, подходящие для легочной ингаляции, меньше по размеру частиц, чем капельки для выпускаемых в настоящее время принтеров, и, следовательно, они подвергаются воздействию большей поверхностной энергии и большей силы сдвига. Следовательно, крайне трудно вытолкнуть белок и пептид в виде микрокапелек, пригодных для легочной ингаляции.
Соответственно, важно разработать эжекционные жидкости, обеспечивающие возможность устойчивой эжекции белков и пептидов.
С другой стороны, в качестве способа для стабилизации белка или пептида известен способ, при котором добавляются поверхностно-активное вещество, глицерин, различные углеводы, растворимый в воде полимер, такой как полиэтиленгликоль и альбумин. Однако этот способ часто трудно осуществим или неэффективен для улучшения стабильности при эжектировании белка и пептида путем использования термического краскоструйного устройства.
Кроме того, даже когда состав получают с включением добавок, подходящих для чернил, используемых при краскоструйной печати, а именно увлажняющих средств, таких как полиолы, включая этиленгликоль и глицерин, и мочевину, такой состав вряд ли будет эффективен для повышения производительности эжекции при эжекции белка или пептида.
В качестве жидких композиций белков, пептидов или им подобных, пригодных для генерирования капелек путем использования термического краскоструйного устройства, описаны жидкие композиции, в которые добавляли соединение, регулирующее поверхностное натяжение, или увлажняющий агент (см. международную публикацию № WO 02/094342). Заявляется, что в этом случае устойчивость белка или пептида в капельках улучшается вследствие воздействия раствора на поверхностное натяжение, вязкость и ввиду увлажнения, и, соответственно, добавляются поверхностно-активное вещество и растворимый в воде полимер, такой как полиэтиленгликоль. Также описаны жидкие композиции с добавлением гуанидина (см. выложенную заявку на патент Японии № 2006-117632).
Однако в международной публикации № WO 02/094342 не раскрыто детальное описание стабильности эжекции. Кроме того, в соответствии с исследованием авторов изобретения было обнаружено, что добавление поверхностно-активного вещества или растворимого в воде полимера оказывает недостаточное действие, при увеличении концентрации белка или пептида. Кроме того, авторы изобретения наблюдали многие случаи, когда невозможно было идентифицировать эффект поверхностно-активного вещества, и обнаружили, что воздействие на поверхностное натяжение, вязкость и увлажняющий эффект не регулируют стабильность эжекции раствора белка или пептида.
Как описано выше, в белковых растворах, известных до настоящего времени, было обнаружено, что стабильность при эжектировании в термических краскоструйных устройствах недостаточна для некоторых типов белков и для некоторых концентраций белков.
Описание изобретения
Настоящее изобретение основано на том обстоятельстве, что была обнаружена композиция с более высокой стабильностью при эжектировании, чем обычные эжекционные жидкости. Другими словами, задача настоящего изобретения состоит в предоставлении эжекционной жидкости (жидкой композиции) для стабильного эжектирования раствора, включающего, по меньшей мере, один компонент, выбранный из белка и пептида, путем использования преимущества термической энергии, и способа эжекции, подходящего для выброса эжекционной жидкости.
Эжекционная жидкость по настоящему изобретению представляет собой эжекционную жидкость для выброса путем передачи термической энергии, включающую белок или пептид; соединение, имеющее группу гуанидина и карбоксильную группу или группу сульфоновой кислоты в одной молекуле и представленное общей формулой (1), или соль соединения; и жидкую среду:
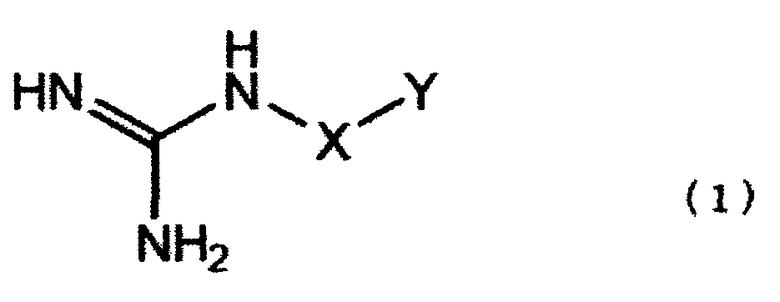
где Х в общей формуле (1) представляет собой необязательно разветвленную алкильную группу, имеющую от одного до восьми атомов углерода, и Y представляет карбоксильную группу или группу сульфоновой кислоты.
Кассета для эжекции жидкости по настоящему изобретению характеризуется включением резервуара, в котором содержится описанная выше эжекционная жидкость, и эжекционной головки, включающей электротермический преобразователь для придания эжекционной жидкости термической энергии.
Жидкостный ингалятор по настоящему изобретению характеризуется включением кассеты и канала всасывания, из которого пользователь вдыхает жидкость, выбрасываемую из эжекционной головки кассеты.
Способ эжекции по настоящему изобретению представляет собой способ эжекции, характеризуемый выбросом жидкой композиции, путем передачи ей термической энергии, включающей белок или пептид; соединение, имеющее группу гуанидина и карбоксильную группу или группу сульфоновой кислоты в одной молекуле и представленное общей формулой (1), или соль соединения; и жидкую среду:
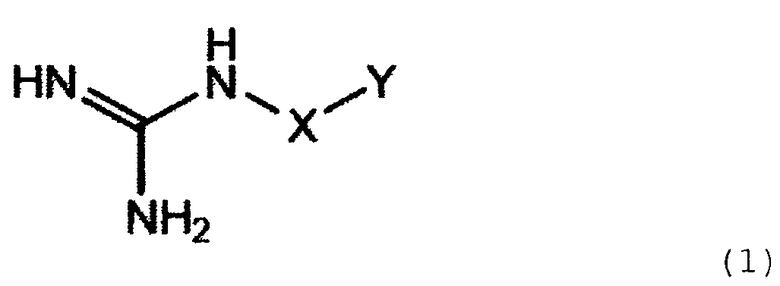
где Х в общей формуле (1) представляет необязательно разветвленную алкильную группу, имеющую от одного до восьми атомов углерода, и Y представляет карбоксильную группу или группу сульфоновой кислоты.
В соответствии с настоящим изобретением путем добавления соединения, имеющего в его одной молекуле группу гуанидина и карбоксильную группу или группу сульфоновой кислоты, к раствору, включающему, по меньшей мере, один из белка и пептида, получается эжекционная жидкость, обеспечивающая возможность стабильного выброса на основе краскоструйного устройства. Капельки жидкости генерируются выбросом из портативного эжекционного устройства, и пользователь вдыхает капельки, так что, по меньшей мере, один вид белка или пептида, который обладает медицинскими свойствами, может переноситься в легкие и может абсорбироваться в организме. С другой стороны, путем выброса эжекционной жидкости на подложку путем использования описанного выше способа эжекционную жидкость можно использовать для получения биочипов и биодатчиков для выявления и для скрининга биологических веществ.
Другие признаки и преимущества настоящего изобретения станут очевидны из следующего описания, взятого в сочетании с сопровождающими чертежами, в которых одинаковые цифры во всех чертежах обозначают те же или одинаковые части.
Краткое описание чертежей
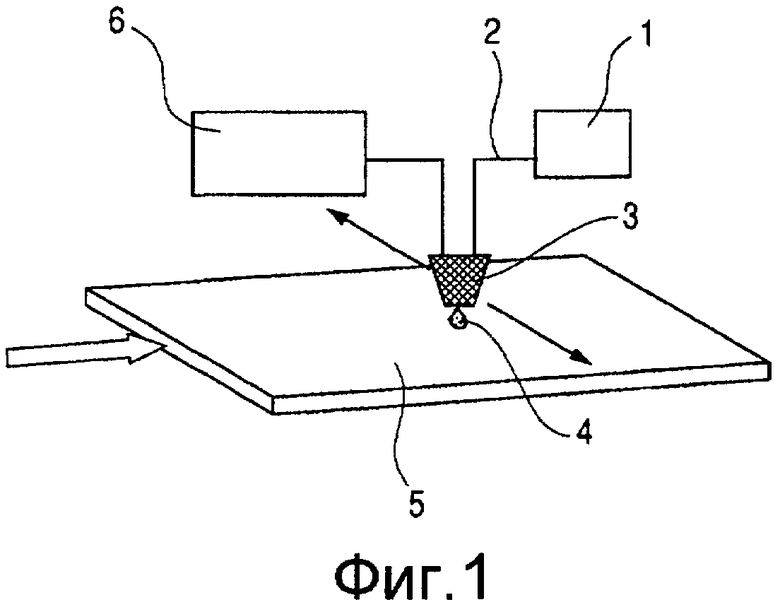
Фиг. 1 схематически иллюстрирует устройство для формирования белкового пятна и пептидного пятна на подложке путем использования эжекционной жидкости в соответствии с настоящим изобретением.
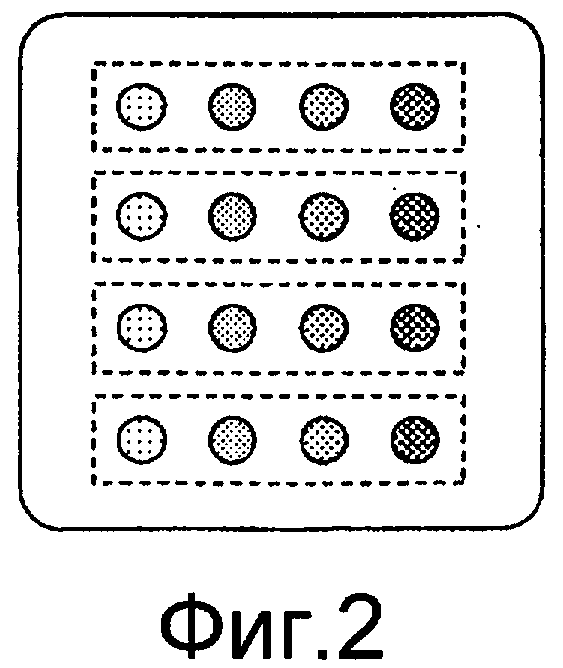
На Фиг. 2 представлен вид сверху, иллюстрирующий пример, в котором пятна белка и пятна пептида расположены на поверхности подложки.
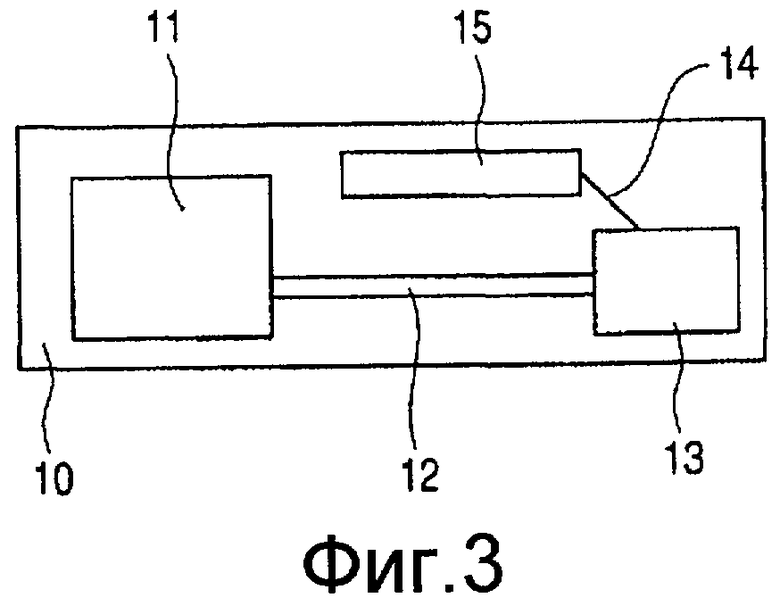
На Фиг. 3 представлен схематический вид, иллюстрирующий узел кассеты эжекции жидкости для использования в ингаляторе.
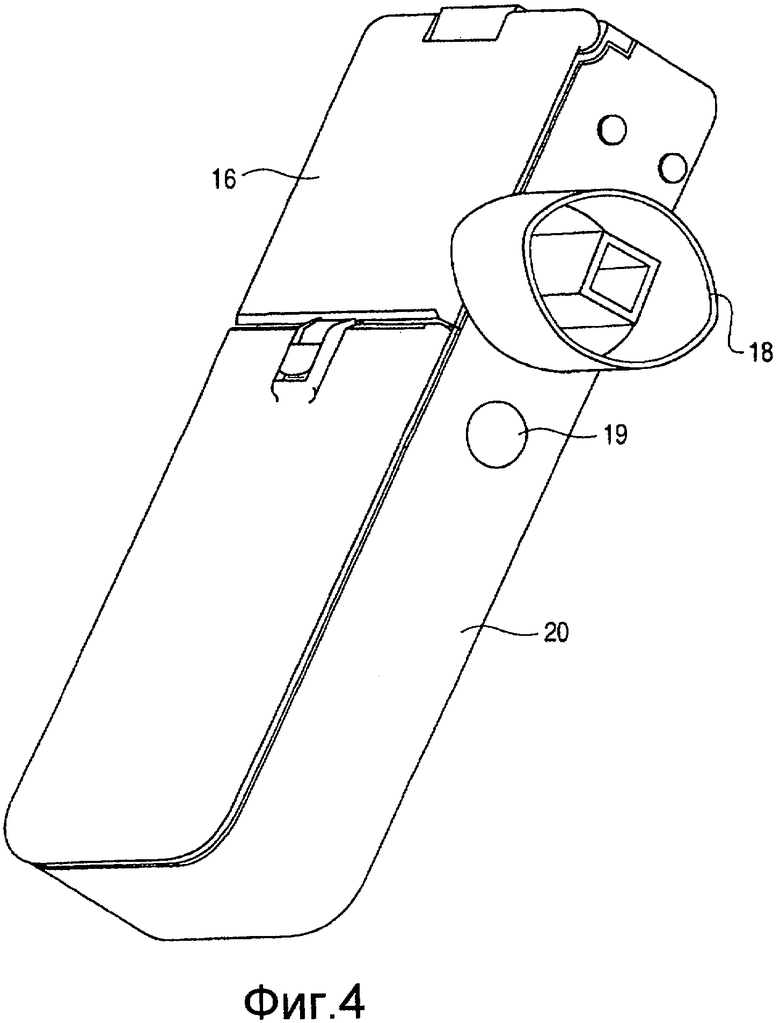
На Фиг. 4 представлен вид в перспективе ингалятора в соответствии с настоящим изобретением.
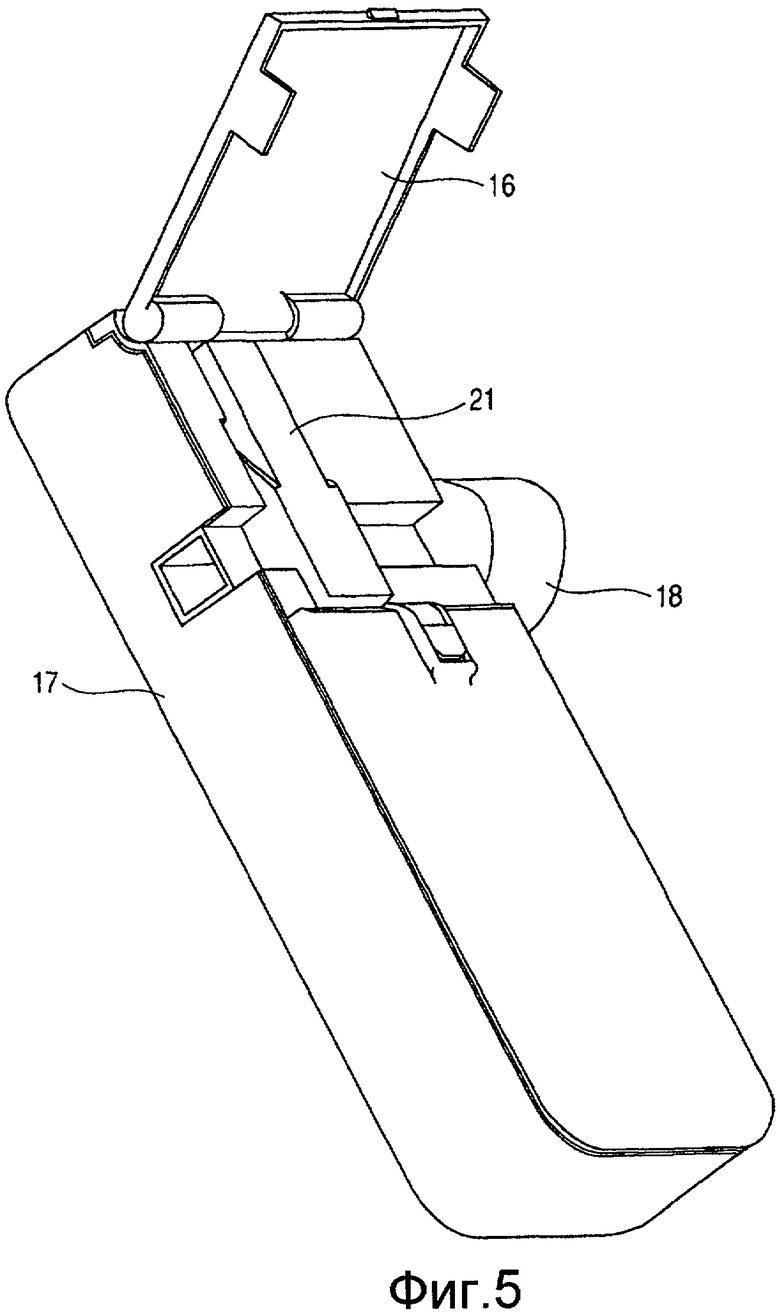
На Фиг. 5 представлен вид в перспективе, иллюстрирующий состояние, в котором открыта крышка доступа в ингалятор, показанный на Фиг. 4.
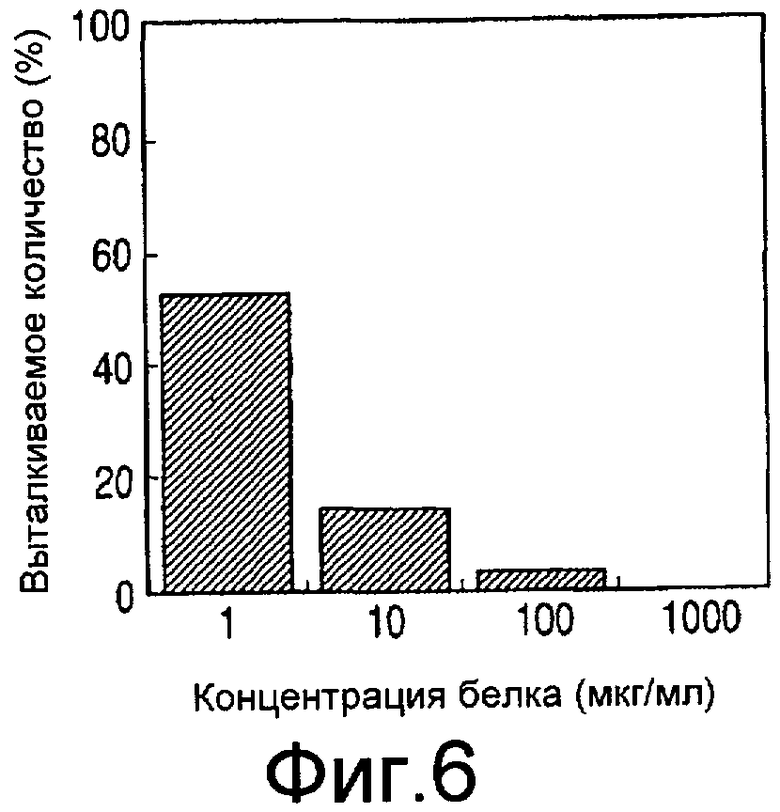
На Фиг. 6 представлен график, иллюстрирующий эжектируемые количества растворов альбумина при эжекции без добавления добавок, используемых в настоящем изобретении, путем использования термического краскоструйного устройства.
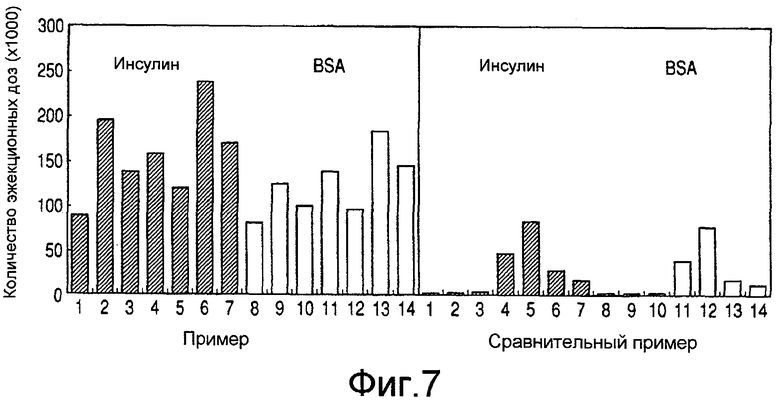
На Фиг. 7 представлен график, иллюстрирующий эжектируемые количества белковых растворов при эжекции с добавлением добавок, используемых в настоящем изобретении, путем использования термического краскоструйного устройства.
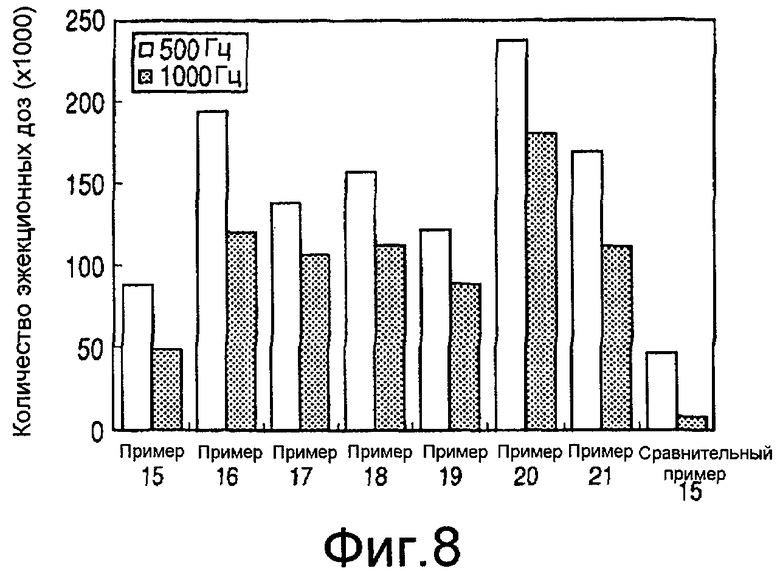
На Фиг. 8 представлен график, иллюстрирующий эжектируемые количества белковых растворов при эжекции путем использования термического краскоструйного устройства с варьирующимися методиками эжекции.
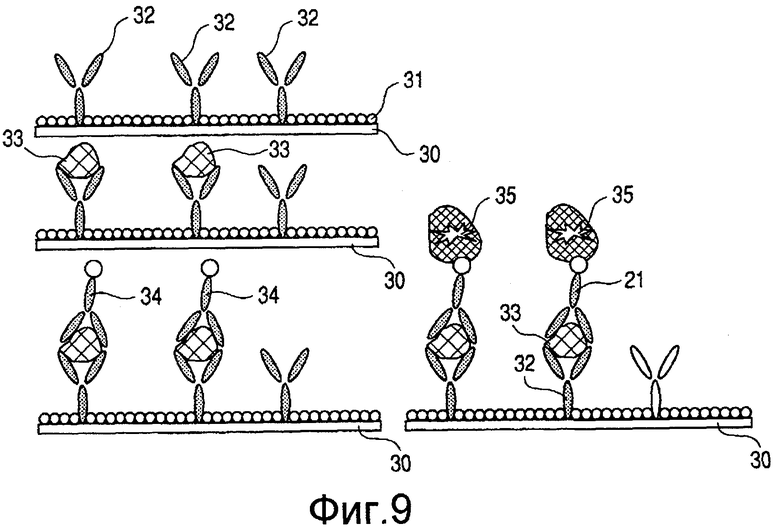
На Фиг. 9 представлена иллюстрация модели экспериментального способа примера 132.
Лучшие способы осуществления изобретения
Теперь предпочтительные варианты осуществления настоящего изобретения будут детально описаны в соответствии с сопровождающими чертежами.
Указанные в настоящем изобретении белки означают любые полипептиды, в которых большое число аминокислот связано друг с другом через пептидные связи, способные к растворению или дисперсии в водных растворах. Кроме того, пептиды, указанные в настоящем изобретении, означают соединения, в которых две или более аминокислоты связаны друг с другом через пептидные связи, и количество аминокислот составляет 50 или менее. Белки и пептиды могут быть химически синтезированы или получены очисткой из натуральных источников; обычно белки и пептиды представляют рекомбинанты натуральных белков и пептидов. Путем химической модификации белков и пептидов посредством ковалентного связывания аминокислотных остатков с белковыми молекулами или пептидными молекулами эффекты белков и пептидов можно также улучшить таким образом, чтобы терапевтические эффекты белков и пептидов длились дольше.
При осуществлении настоящего изобретения могут использоваться различные белки и пептиды с тем, чтобы стать подходящими для применения в виде капелек. Типичнее всего, капельки белков и пептидов в соответствии с настоящим изобретением могут предпочтительно использоваться с целью доставки терапевтически полезных белков и пептидов в легкие.
Примеры белков и пептидов включают кальцитонин; факторы свертывания крови; циклоспорин; различные гематопоэтические факторы, такие как G-CSF (фактор, стимулирующий колонии гранулоцитов), GM-CSF (фактор, стимулирующий колонии гранулоцитов-макрофагов), SCF (фактор стволовых клеток), EPO (эритропоэтин), GM-MSF (фактор, замедляющий движение гранулоцитов-макрофагов) и CSF-1 (колониестимулирующий фактор-1); интерлейкины, такие как с IL-1 по IL-18; IGF (инсулиноподобные факторы роста); M-CSF (фактор, стимулирующий колонии макрофагов); тимосин; и цитокины, включая TNF (фактор опухолевого некроза) и LIF (фактор, ингибирующий миграцию лимфоцитов). Кроме того, примеры других подходящих белков и пептидов, оказывающих терапевтические эффекты, включают вазоактивные пептиды; интерфероны (альфа, бета, гамма или общий интерферон); факторы роста или гормоны, такие как человеческие гормоны роста или другие соматотропные гормоны (такие, как бычьи, свиные или куриные факторы роста); инсулин; окситоцин; ангиотензин; метионин энкефалин; субстанцию Р; ЕТ-1 (эндотелин-1); FGF (фактор роста фибробластов); KGF (фактор роста кератиноцитов); EGF (фактор роста эпидермиса); IGF (инсулиноподобный фактор роста); PDGF (фактор роста, полученный из тромбоцитов); LHRH (люлиберин); GHRH (соматолиберин); FSH (фолликулостимулирующий гормон); DDAVP (десмопрессин); PTH (паратиреоидный гормон); вазопрессин; глюкагоны; и соматостатин. Используются также ингибиторы протеазы, такие как лейпептин, пепстатин, и ингибиторы металлопротеиназы (такие, как TIMP-1 (тканевой ингибитор металлопротеиназы-1), TIMP-2 (тканевой ингибитор металлопротеиназы-2) или другие ингибиторы протеиназы). Используются также факторы роста нервов, такие как BDNF (нейротрофический фактор, полученный из мозга) и NT3 (нейротрофин-3). Используются также активаторы плазминогена, такие как tPA (тканевые активаторы плазминогена), урокиназа и стрептокиназа. Используются также различные гуманизированные антитела и рецепторы. Используются также части пептидов, которые имеют всю или часть основных структур родительских белков и имеют, по меньшей мере, часть биологических свойств родительских белков. Используются также аналоги, такие как замещенные аналоги или дефективные аналоги, или модифицированные аминокислоты, такие как аналоги пептидов, и вещества, содержащие описанные выше вещества, модифицированные растворимыми в воде полимерами, такими как PEG (полиэтиленгликоль) и PVA (поливиниловый спирт). То что описанные выше белки и пептиды способны доставляться в легкие, верифицируется в документе Critical Reviews in Therapeutic Drug Carrier Systems, 12 (2&3) (1995).
Кроме того, когда капельки по настоящему изобретению применяются при изготовлении биочипов и биодатчиков и при скрининге белков и пептидов, то различные ферменты, такие как оксидаза, редуктаза, трансфераза, гидраза, лиаза, изомераза, синтетаза, эпимераза, мутаза и лацеаза, могут использоваться в дополнение к описанным выше белкам и пептидам. Могут также использоваться описанные выше вещества, модифицированные с реагентами для иммобилизации белками и пептидами, подлежащими к использованию в диагностических целях, таких как различные антитела, включая IgG и IgE, и рецепторы, и соответствующие антигены, и аллергены, чаперонин, авидин и биотин.
В качестве белков и пептидов, подлежащих включению в эжекционные жидкости, могут использоваться белки и протеины, каждые из которых имеют молекулярную массу, укладывающуюся в пределы диапазона, например, от 0,5 до 150 кДа. Кроме того, в эжекционной жидкости содержание, по меньшей мере, одного вещества, выбранного из белков и пептидов, выбрано в соответствии с назначением и применением эжекционной жидкости и, предпочтительно, выбрано из диапазона от 1 мкг/мкл до 200 мг/мл или менее, предпочтительнее, из диапазона от 0,1 мг/мкл или более и до 60 мг/мл или менее.
Следует отметить, что, когда в настоящем изобретении применяется термическое краскоструйное устройство, производительность эжекции наиболее эффективна и, следовательно, следующее описание будет сосредоточено на конфигурации, основанной на принципе термического эжекционного устройства. Однако в настоящем изобретении может использоваться пьезоструйное устройство, в котором жидкость в сопле выбрасывается с использованием вибрирующего давления пьезоэлемента. Эжекционное устройство может быть выбрано в соответствии с типом подлежащего эжекции белка или пептида. В настоящем изобретении среди струйных систем способ, которым термическая энергия сообщается жидкости путем использования электротермического преобразователя, выражается как «термическая струйная система», а способ, которым механическая энергия передается жидкости использованием электромеханического преобразователя, выражается как «пьезоструйная система», как это обычно принято в области принтерной техники. Хотя эти термины используются для растворов белков, каждый из этих терминов просто выражает то, что эжекционная энергия сообщается раствору на основе принципа «струйной системы».
В целом известно, что для повышения производительности эжекции типографской краски, эжекционной системой, добавляется поверхностно-активное вещество или растворитель, такое как этиленгликоль. Однако, когда производилась эжекция раствора, содержащего, по меньшей мере, одно вещество из белка и пептида, при простом добавлении этих веществ не было обнаружено повышения производительности эжекции, и была установлена необходимость использования других добавок, отличных от них.
Заявители выполнили тщательное исследование и в последующем обнаружили, что в белковые растворы и пептидные растворы при добавлении соединения, имеющего гуанидиновую группу и карбоксильную группу или группу сульфоновой кислоты в одной молекуле, подходят для стабильной эжекции на основе струйной системы.
Причина, по которой соединение, имеющее гуанидиновую группу и карбоксильную группу или группу сульфоновой кислоты в одной молекуле, в значительной степени способствует стабильности эжекции, неясна, но, возможно, состоит в следующем.
Гуанидиновая группа имеет планарную структуру, а ее аминогруппа работает в качестве донора водорода с тем, чтобы быть способной образовывать водородную связь. Верхняя сторона и нижняя сторона молекулярной плоскости покрываются π-электронами, и, следовательно, гуанидиновая группа также обладает гидрофобностью. Пептидные связи в белке и в пептиде считаются едва различимыми по устойчивости между ситуацией, когда пептидные связи образуют водородные связи с гуанидиновыми группами и когда пептидные связи образуют водородные связи с водой, или пептидные связи взаимно образуют водородные связи. Кроме того, гуанидиновая группа имеет гидрофобные части, и, следовательно, гидрофобные части гуанидиновой группы и гидрофобные части пептида взаимодействуют друг с другом. Ввиду того что часть аминогруппы образует водородную связь с водой, растворимость в воде белка и пептида в денатурированном состоянии увеличивается, и, следовательно, можно подавить взаимодействие белков и взаимодействие пептидов. Возможно, соединение оказывает эффект на основе подавления контакта между белками вследствие отрицательного заряда, который несет одновременно присутствующая карбоксильная группа или одновременно присутствующая группа сульфоновой кислоты. Возможно, благодаря этим эффектам предотвращаются денатурация и агрегация, вызванные энергией, подаваемой во время эжекции на основе краскоструйного устройства, и, следовательно, стабилизируется эжекция.
В соответствии с настоящим изобретением эффект улучшения выполнения эжекции становится выраженным, в частности, в головной части изгоняемых капелек путем использования термической энергии, когда головная часть приводится в действие с высокой частотой.
В качестве соединения, используемого в настоящем изобретении, где соединение имеет гуанидиновую группу и карбоксильную группу или группу сульфоновой кислоты в одной молекуле, предпочтительно соединение, представленное общей формулой (1):
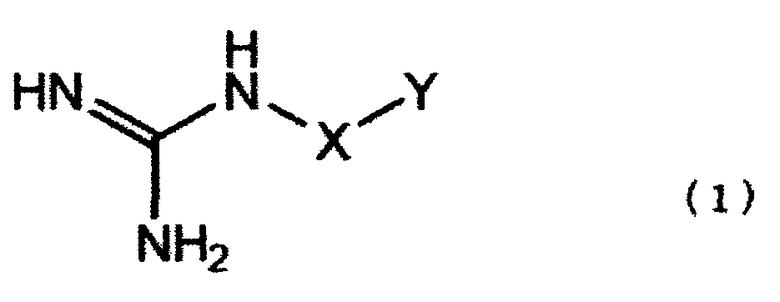
где Х в указанной выше общей формуле (1) представляет необязательно разветвленную алкильную группу, имеющую от одного до восьми атомов углерода. Количество атомов углерода в алкильной группе Х прямо не связано с механизмом, в соответствии с которым происходит устойчивый выброс белка, благодаря соединению; однако количество атомов углерода предпочтительно составляет от одного до восьми, а предпочтительнее, от одного до четырех атомов углерода, с целью поддержания растворимости молекулы. Один или более алкильных атомов водорода в Х могут быть замещены атомами галогена и гидроксигруппами. Когда боковая цепь, ответвленная от Х, имеет функциональную группу или функциональные группы, то боковая цепь предпочтительно имеет одну или более гидроксильных групп, или карбоксильных групп, или групп сульфоновой кислоты. Y представляет карбоксильную группу или группу сульфоновой кислоты. Кроме того, могут также использоваться соли этих соединений. Кроме того, могут также использоваться полимеры, включая любое из этих соединений в виде одной единицы, и могут также использоваться поверхностно-активные вещества, включающие в своей структуре любое из этих соединений.
Примеры более предпочтительных соединений среди соединений, представленных описанной выше формулой (1), включают соединения, характеризуемые тем, что в каждом из этих соединений Х представляет собой необязательно разветвленную алкильную группу, имеющую от одного до восьми атомов углерода и, когда алкильная группа имеет разветвленную боковую цепь, разветвленная боковая цепь имеет карбоксильную группу или группу сульфоновой кислоты на конце боковой цепи. Аналогичным образом, Y представляет карбоксильную группу или группу сульфоновой кислоты. Могут также использоваться соли этих соединений, может также использоваться полимер, включающий любое из этих соединений в виде единицы, и может также использоваться поверхностно-активное вещество, включающее в своей структуре любое из этих соединений.
Молекулярная масса соединения, имеющего группу гуанидина и карбоксильную группу или группу сульфоновой кислоты в одной молекуле, составляет предпочтительно от 117 до 2000, а предпочтительнее, от 117 до 500. Кроме того, с целью получения желательных эффектов, предпочтительно использовать те соединения, которые имеют растворимость в воде 0,1 мас.% или более в нейтральной области (рН от 5,5 до 8,5).
Предпочтительными соединениями являются 2-гуанидинуксусная кислота, 3-гуанидинпропионовая кислота, 4-гуанидинбутановая кислота, α-гуанидинглутаминовая кислота, гуанидинметансульфоновая кислота, 2-гуанидинэтансульфоновая кислота, 3-гуанидинпропансульфоновая кислота и соли этих соединений. Наиболее предпочтительными соединениями являются 3-гуанидинпропионовая кислота и 2-гуанидинэтансульфоновая кислота и соли этих соединений.
Соединение добавляется в количестве от 0,1 части по массе до 50 частей по массе, предпочтительнее, от 0,25 части по массе до 25 частей по массе, а наиболее предпочтительно, от 0,5 части по массе до 10 частей по массе относительно 1 части по массе белка или пептида.
Хотя концентрация добавляемого соединения зависит от типа и концентрации белка или пептида, концентрация добавляемого соединения составляет предпочтительно от 0,001 мас.% до 20 мас.%, предпочтительнее, от 0,05 мас.% до 15 мас.%, а наиболее предпочтительно, от 0,5 мас.% до 10 мас.%.
Кроме того, в соответствии с настоящим изобретением было также обнаружено, что эжекционную стабильность можно поддержать добавлением соединения и поверхностно-активного вещества в комбинации, даже когда концентрация добавки резко снижается. Поверхностно-активное вещество добавляется в количестве от 0,1 части по массе до 1 части по массе относительно 1 части по массе соединения. Соответственно, количество соединения, добавляемого к раствору с такой же концентрацией белка, можно снизить с половины до 1/10. В отличие от соединения, эффект поверхностно-активного вещества, вероятно, включает стабилизацию эжекции путем подавления денатурации белка и вновь растворения агрегированного белка. Вероятно, комбинация этих двух различных эффектов приводит к синергическому эффекту с резким улучшением эжекционной стабильности. Вероятно, что при использовании одного поверхностно-активного вещества эти эффекты невелики, так что агрегацию белка нельзя полностью подавить и, следовательно, нельзя обеспечить эжекционную стабильность.
Указанное в настоящем изобретении «поверхностно-активное вещество» означает соединение, имеющее и полярную часть, и неполярную часть в одной молекуле, или соединение, в котором полярная часть и неполярная часть связаны друг с другом посредством вторичной связи, такой как ионная связь. Другими словами, поверхностно-активное вещество имеет такие характеристики, что поверхностно-активное вещество снижает межповерхностное натяжение посредством его молекулярного совмещения в поверхности раздела между двумя не смешиваемыми растворителями, и способно образовывать мицеллы, где полярная часть и неполярная часть соответственно расположены в локализованных областях, отделенных друг от друга в молекуле поверхностно-активного вещества.
Подходящее для использования поверхностно-активное вещество конкретно не ограничено. Типичные примеры поверхностно-активного вещества включают сложные эфиры жирных кислот сорбитана, такие как сорбитанмонокаприлат, сорбитанмонолаурат и сорбитанмонопальмитат; N-ацильные аминокислоты, каждая из которых представляет поверхностно-активное вещество, имеющее аминокислоту в качестве ее гидрофильной группы, такую как глицин жирной кислоты N-кокосового масла, глутаминовая кислота жирной кислоты N-кокосового масла и N-лауроилглутаминовая кислота; соли жирных кислот аминокислот; сложные эфиры жирных кислот глицерина, такие как глицеринмонокаприлат, глицеринмономиристат и глицеринмоностеарат; сложные эфиры жирных кислот полиглицерина, такие как декаглицерилмоностеарат, декаглицерилдистеарат и декаглицерилмонолинолат; сложные эфиры жирных кислот полиоксиэтиленсорбитана, такие как монолаурат полиоксиэтиленсорбитана, моноолеат полиоксиэтиленсорбитана, моностеарат полиоксиэтиленсорбитана, монопальмитат полиоксиэтиленсорбитана, триолеат полиоксиэтиленсорбитана и тристеарат полиоксиэтиленсорбитана; сложные эфиры жирных кислот полиоксиэтиленсорбитола, такие как тетрастеарат полиоксиэтиленсорбитола и тетраолеат полиоксиэтиленсорбитола; сложные эфиры жирных кислот полиоксиэтиленглицерина, такие как моностеарат полиоксиэтиленглицерила; сложные эфиры жирных кислот полиэтиленгликоля, такие как дистеарат полиэтиленгликоля; простые алкиловые эфиры полиоксиэтилена, такие как простой лауриловый эфир полиоксиэтилена; простые алкиловые эфиры полиоксиэтиленполиоксипропилена, такие как простой гликолевый эфир полиоксиэтиленполиоксипропилена, простой пропиловый эфир полиоксиэтиленполиоксипропилена и простой цетиловый эфир полиоксиэтиленполиоксипропилена; простые алкилфениловые эфиры полиоксиэтилена, такие как простой нонилфениловый эфир полиоксиэтилена; касторовые масла, отвержденные полиоксиэтиленом, такие как полиоксиэтиленкасторовое масло и касторовое масло, отвержденное полиоксиэтиленом (касторовое масло, гидрированное полиоксиэтиленом); полиоксиэтиленовые производные пчелиного воска, такие как пчелиный воск полиоксиэтиленсорбита; полиоксиэтиленовые производные ланолина, такие как полиоксиэтиленланолин; поверхностно-активные вещества, имеющие HLB (гидрофильно-липофильный баланс) от 6 до 18, такие как амиды жирных кислот полиоксиэтилена, включая амид стеариновой кислоты полиоксиэтилена; анионные поверхностно-активные вещества, имеющие алкильную группу, имеющую от 8 до 18 атомов углерода, включая цетилсульфат натрия, лаурилсульфат натрия и олеилсульфат натрия; сульфаты простого алкилового эфира полиоксиэтилена, каждый имеющий среднее количество добавления молей от 2 до 4 этиленоксида и от 8 до 18 атомов углерода в алкильной группе, такие как полиоксиэтиленлаурилсульфат натрия; алкилбензолсульфонаты, каждый имеющий от 8 до 18 атомов углерода в алкильной группе, такие как лаурилбензолсульфонат натрия; алкилсульфосукцинаты, каждый имеющий от 8 до 18 атомов углерода в алкильной группе, такие как лаурилсульфосукцинат натрия; натуральные поверхностно-активные вещества, такие как лецитин и глицерофосфолипид; сфингофосфолипиды, такие как сфингомиелин; и сложные эфиры жирных кислот сахарозы, причем каждая жирная кислота имеет от 8 до 18 атомов углерода. К эжекционной жидкости (жидкой композиции) по настоящему изобретению эти поверхностно-активные вещества могут добавляться каждое по отдельности или в комбинации из двух или более из них.
Предпочтительными поверхностно-активными веществами являются сложные эфиры жирных кислот полиоксиэтиленсорбитана; особенно предпочтительными среди них являются сорбитанмонолаурат полиоксиэтилена 20, сорбитанмоностеарат полиоксиэтилена 20, сорбитантристеарат полиоксиэтилена 20, глицин жирной кислоты N-кокосового масла, глутаминовая кислота жирной кислоты N-кокосового масла, N-лауроилглутаминовая кислота, N-лауроилсаркозин, лаурамидпропилбетаин, соль жирной кислоты аргинина кокосового масла; и наиболее предпочтительными являются сорбитанмонолаурат полиоксиэтилена 20, сорбитанмоноолеат полиоксиэтилена 20, глицин жирной кислоты N-кокосового масла, глутаминовая кислота жирной кислоты N-кокосового масла, N-лауроилсаркозин, лаурамидпропилбетаин и соль жирной кислоты аргинина кокосового масла. Кроме того, особенно предпочтительными для абсорбции в легких являются сорбитанмонолаурат полиоксиэтилена 20 и сорбитанмоноолеат полиоксиэтилена 20.
Хотя концентрация добавляемого поверхностно-активного вещества зависит от типа и содержания одновременно присутствующего белка или пептида, концентрация добавляемого поверхностно-активного вещества предпочтительно находится в диапазоне от 1 мкг/мл до 1,0 г/мл, предпочтительнее, в диапазоне от 1 мг/мл до 100 мг/мл, а наиболее предпочтительно, в диапазоне от 0,2 мг/мл до 50 мг/мл, и выбрана из концентраций критической концентрации мицеллы или более.
Композиция жидкой среды предпочтительно, с точки зрения растворимости белка или ему подобного, такова, что преобладает вода, и пропорция воды в среде составляет 50% или более. Могут использоваться смешанные жидкие среды, содержащие растворимые в воде органические растворители, такие как спирты, в дополнение к основному компоненту среды, а именно воде.
Конкретные примеры водорастворимых органических растворителей включают амиды, такие как диметилформамид и диметилацетамид; кетоны, такие как ацетон; простые эфиры, такие как тетрагидрофуран и диоксан; этанол; полиалкиленгликоли, такие как полиэтиленгликоль и полипропиленгликоль; алкиленгликоли с алкиленовой группой, имеющей от 2 до 6 атомов углерода, такие как этиленгликоль, пропиленгликоль, бутиленгликоль, триэтиленгликоль, 1,2,6-гексантриол, тиодигликоль, гексиленгликоль и диэтиленгликоль; глицерин; простые низшие алкиловые эфиры полиспиртов, такие как простой монометиловый (или этиловый) эфир этиленгликоля, простой монометиловый (или этиловый) эфир диэтиленгликоля и простой монометиловый (или этиловый) эфир триэтиленгликоля, и N-метил-2-пирролидон.
В вариантах осуществления настоящего изобретения с целью устранения микробных воздействий может добавляться противомикробное средство, гермицидное средство или антисептическое средство. Примеры этих средств включают соли четвертичного аммония, такие как бензалконийхлорид и бензатонийхлорид; производные фенола, такие как фенол, крезол и анизол; бензойные кислоты, такие как бензойная кислота и сложный эфир параоксибензойной кислоты; и аскорбиновая кислота.
В вариантах осуществления настоящего изобретения с целью увеличения физической стабильности эжекционной жидкости во время хранения может добавляться масло, глицерин, этанол, мочевина, целлюлоза, полиэтиленгликоль, соли альгиновой кислоты и никотинамид. Кроме того, с целью увеличения химической устойчивости может добавляться аскорбиновая кислота, лимонная кислота, циклодекстрин, токоферол или любые другие антиоксиданты.
С целью регулирования рН эжекционной жидкости к эжекционной жидкости может добавляться буфер. Например, могут использоваться следующие буферы: аскорбиновая кислота, лимонная кислота, разбавленная хлористоводородная кислота и разбавленный гидроксид натрия; и, кроме того, гидрофосфат натрия, дигидрофосфат натрия, гидрофосфат калия, дигидрофосфат калия, PBS (фосфатно-буферный раствор), HEPES (N-2-гидроксиэтилпиперазин-N-2-этансульфоновая кислота) и Tris (тригидроксиметиламинометан) буфер.
В качестве изотонизирующего средства может добавляться аминоэтилсульфоновая кислота, хлорид калия, хлорид натрия, глицерин или гидрокарбонат натрия.
Могут также добавляться добавки, используемые для струйных чернил, такие как этиленгликоли, мочевина, ксилит, EDTA (этилендиаминтетрауксусная кислота) и таурин.
Когда эжекционная жидкость в соответствии с настоящим изобретением используется в качестве аэрозольно распыляемой жидкости, в качестве отдушек и ароматизирующих средств могут добавляться сахариды, такие как глюкоза и сорбит, подслащивающие агенты, такие как аспартам, ментол и различные ароматизирующие агенты. Кроме того, могут также использоваться гидрофобные соединения и маслянистые соединения, а также гидрофильные соединения.
Кроме того, в соответствии с потребностью, могут добавляться в соответствующих количествах различные добавки, подходящие для предполагаемых видов применения эжекционной жидкости, такие как модификатор поверхности, модификатор вязкости, растворитель и увлажняющее средство. Определенные примеры таких смешиваемых добавок включают гидрофильный связывающий агент, гидрофобный связывающий агент, гидрофильный загуститель, гидрофобный загуститель, производные гликоля, спирты и электролиты; они могут добавляться по отдельности или в комбинации двух или более из этих соединений. Следует отметить, что предпочтительнее использовать, в качестве разнообразных веществ, подлежащих использованию в качестве описанных выше добавок, добавки, которые предназначены для лекарственного применения и перечислены в фармакопеях различных стран как дополнительные компоненты, допущенные для добавления, или добавки, допущенные для использования в пищевых продуктах и косметических продуктах, при получении терапевтических жидких составов.
Пропорция добавления каждого из разнообразных веществ, подлежащих введению в качестве описанных выше добавок, варьируется, в зависимости от типов целевых белков и пептидов; однако в целом пропорция добавления каждого из таких соединений выбирается так, чтобы предпочтительно укладываться в диапазон от 0,001% до 40 мас.%, а предпочтительнее, от 0,01% до 20 мас.%. Количество каждой из добавляемых описанных выше добавок варьируется в зависимости от типа, количества и комбинации, но составляет предпочтительно от 0,1 части по массе до 200 частей по массе в отношении 1 части по массе белка и пептида, с точки зрения осуществления эжекции.
Кроме того, когда раствор белка и раствор пептида выбрасывается путем использования термического струйного устройства, частота возбуждения головки которого предпочтительно настолько ниже, насколько возможно. Указанная в настоящем изобретении «частота возбуждения» означает количество импульсов выброса в секунду, подаваемых на электрохимический преобразователь, в случае термического струйного устройства. Причина того, почему стабильность эжекции варьируется, в зависимости от частоты возбуждения, вероятно, состоит в том, что, когда эжекционная жидкость нагревается электротермическим преобразователем термической струйной головки, белок и пептид становятся частично нерастворимыми в воде, и, следовательно, тормозится передача энергии от электротермического преобразователя к раствору. Когда частота разгонки примеси низкая, временно образованные нерастворимые вещества, если они имеются, снова растворяются последующим временем разгонки примеси; с другой стороны, когда частота возбуждения высокая, извлечение растворения становится недостаточным, и, вероятно, стабильность эжекции, посредством этого, снижается. Однако, с целью эффективного изгнания большого количества раствора, необходимо проводить изгнание с частотами определенной величины или выше. В настоящем изобретении частота привода предпочтительно составляет от 0,1 кГц до 100 кГц, а предпочтительнее, от 1 кГц до 30 кГц.
Когда эжекционная жидкость в соответствии с настоящим изобретением используется при получении биочипов и биодатчиков при скрининге белков и пептидов, можно использовать устройство, почти такое же, как устройство в выпускаемых в настоящее время краскоструйных принтерах.
С другой стороны, жидкостный ингалятор в соответствии с настоящим изобретением включает термическую струйную головку, способную выбрасывать микрокапельки эжекционной жидкости, на основании термического краскоструйного устройства. Предпочтительно приспособить механизм, способный независимо приводить в действие отдельные электротермические преобразователи сопел, составляющих головку. В этом случае интегрируются электрические проводники для использования при соединении множества контрольных сигналов, требуемых для независимого привода отдельных электротермических преобразователей, и проводников, соединяющих отдельные электротермические преобразователи. Кроме того, предпочтительно принять форму кассеты эжекции жидкости, в которой объединены резервуар, хранящий эжекционную жидкость, и эжекционная головка, включающая электротермические преобразователи, придающие термическую энергию эжекционной жидкости.
Фиг. 1 схематически иллюстрирует устройство для образования пятен белка и пятен пептида на подложке путем использования эжекционной жидкости в соответствии с настоящим изобретением. Подложка 5 используется в качестве пластины детектирования, на которой образуются иммобилизационные области веществ сравнения, таких как белки, пептиды, ферменты и антитела для использования при выявлении различных веществ, содержащихся в образце. Эжекционная головка 3 включает, по меньшей мере, жидкостный проход (не показан) для передачи жидкости эжекционной энергии и эжекционное сопло (не показано), сообщающееся с жидкостным проходом. Эжекционная энергия передается жидкости, подаваемой через проход подачи жидкости 2 к проходу жидкости из резервуара 1, содержащего жидкость, и, в последующем, жидкость эжектируется в виде капелек 4 из эжекционного сопла на заданное положение на поверхности подложки 5. Эжекционная головка 3 расположена на кассете, способной располагаться вдоль направления плоскости, показанного стрелками, и положение осаждения капелек 4 на подложку 5 регулируется перемещением эжекционной головки 3. Время эжекции капельки 4 регулируется регулятором 6, электрически связанным с эжекционной головкой 3.
Фиг. 2 иллюстрирует вид сверху примера, в котором пятна белка и пятна пептида расположены на поверхности подложки. На чертеже различия плотности цвета пятен представляют различия концентраций белков и пептидов, где каждая из областей, окруженная пунктирными линиями, получается нанесением проб одной эжекционной жидкостью. В показанном примере множество эжекционных узлов, способных соответственно эжектировать различные эжекционные жидкости и способных независимо приводиться, могут располагаться в части эжекционной головки. Путем соединения устройств подачи заданных эжекционных жидкостей соответственно в отдельные узлы могут быть образованы два или более типов пятен на подложке. Кроме того, путем варьирования количеств жидкости, внесенных в соответствующие положения образования пятна, могут образовываться пятна с различными прикрепленными количествами.
Далее описывается случай, где эжекционная жидкость в соответствии с настоящим изобретением используется для орошения, в частности случай, где обсуждаемая эжекционная жидкость вносится в ингалятор. Предпочтительно использовать ингалятор, имеющий структуру, при которой независимо включается часть для превращения эжекционной жидкости в микрокапельки и часть для смешивания распыляемых микрокапелек в переносящий поток газа. Таким образом, путем разделения части для превращения в микрокапельки и части для формирования потока газа, содержащего микрокапельки, можно регулировать выталкиваемое количество, делая его более однородным. Другими словами, когда ингаляция потока газа производится пациенту, которому требуется такое введение, можно более равномерно подобрать количество белка или пептида в качестве эффективного компонента, а именно заданное количество компонента в потоке газа при каждом одиночном введении. Как описано выше, путем обеспечения структуры части эжекционной головки, в которой каждая из множества эжекционных единиц, имеющих большое количество эжекционных сопел, соответственно изгоняет различные эффективные компоненты, можно также регулировать выталкиваемые количества двух или более эффективных компонентов.
Уменьшению размера ингалятора, носимого пользователем, способствует использование в качестве эжекционной головки, служащей в виде механизма распыления, эжекционной головки на основе принципа термического краскоструйного устройства, в котором эжекционные сопла могут быть расположены с высокой плотностью на единицу площади.
В ингаляторе для легочной ингаляции важно, чтобы размер частиц капелек, содержащихся в потоке газа, составлял от 1 до 5 мкм и проявлял узкое распределение размера частиц. Кроме того, когда такой ингалятор используется в виде портативного ингалятора, требуется, чтобы ингалятор имел компактную структуру.
На Фиг. 3 схематически показан пример кассеты для эжекции жидкости в таком ингаляторе. Кассета для эжекции жидкости имеет структуру в виде узла головки кассеты, в котором в корпус 10 интегрированы головка 13, резервуар 11 для помещения эжекционной жидкости, жидкостный канал 12 для подачи жидкости из резервуара 11 в головку 13, электрический разъем 15 для обмена приводных сигналов и регулирующих сигналов с регулятором для регуляции привода отдельных эжекционных узлов головки 13 и внутреннюю монтажную схему 14 между головкой 13 и электрическим разъемом 15. Узел головки кассеты сконструирован в виде структуры, способной отсоединяться от ингалятора, в соответствии с необходимостью. В качестве головки 13 предпочтительно используется головка, имеющая структуру головки для эжекции капелек, описанную в выложенной заявке на патент Японии № 2003-154665.
Описание примера портативного ингалятора, включающего узел головки кассеты, имеющий описанную выше структуру, дано со ссылкой на Фиг. 4 и 5. Ингалятор, иллюстрируемый на Фиг. 4 и 5, имеет структуру примера с уменьшенным размером для ношения пользователем с терапевтической целью.
Фиг. 4 представляет вид в перспективе, показывающий вид ингалятора. В ингаляторе, корпус ингалятора образован из основного корпуса 20 ингалятора и крышки для доступа 16. Корпус, кроме того, содержит регулятор, источник питания (аккумуляторную батарею) и тому подобные элементы (не показаны). Фиг. 5 представляет вид в перспективе, иллюстрирующий состояние, в котором открыта крышка доступа 16 в ингалятор, и, когда крышка доступа 16 открыта, виден узел головки кассеты 21. При вдыхании пользователем, воздух засасывается в ингалятор из отверстия забора воздуха 17 и направляется в мундштук 18 (канал всасывания) с тем, чтобы оставаться в нем; воздух смешивается с капельками, изгоняемыми из эжекционных сопел, образованных в головке 13 узла головки кассеты 21 с тем, чтобы получить смешанный газовый поток. Смешанный газовый поток направляется к выходу из мундштука, имеющего форму, подходящую для вставления в рот. Когда пользователь вставляет в рот наконечник мундштука, удерживает мундштук зубами и делает вдох, капельки, изгоняемые из жидкой эжекционной части, направляются в мундштук 18 и могут эффективно вдыхаться.
Следует отметить, что узел головки кассеты 21 может быть изготовлен в виде структуры, способной отсоединяться от ингалятора, в соответствии с необходимостью.
Путем приспособления структуры, иллюстрируемой на Фиг. 4 и 5, обеспечивается возможность спонтанного достижения подлежащими введению микрокапельками горла и внутренней части трахеи пользователя наряду с вдыхаемым воздухом. Соответственно, количество распыленной жидкости (вводимое количество эффективных компонентов) можно регулировать независимо от величины объема вдыхаемого воздуха.
(Справочный пример 1)
Перед началом описания примеров, с целью дальнейшего понимания сложности при эжекции белковых растворов, показаны эжектируемые количества, полученные в случаях, когда просто эжекция белка производится термическим струйным устройством. Использовались белковые растворы, в которых бычий сывороточный альбумин (BSA) растворялся в растворе фосфатного буфера (PBS). Растворы с различными концентрациями эжектировались с использованием устройства для эжекции жидкости, изготовленного путем модификации принтера Bubblejet (торговая марка) (торговое название: PIXUS950i; выпускаемый Canon Inc.) с тем, чтобы обеспечить возможность извлечения растворов. Эжектируемое количество (количество капельки) чистой воды, полученное выталкиванием таким же образом, как при выталкивании белковых растворов, принималось за 100%, и на основании этого допущения было представлено эжектируемое количество (количество капельки) каждого из отдельных растворов альбумина. Полученные таким образом результаты показаны на Фиг. 6.
Даже при низкой концентрации BSA, достигающей лишь 1 мкг/мл, стабильность эжекции не была совершенной, и при дальнейшем увеличении концентрации белка эжектируемое количество варьировалось с постепенным его уменьшением. Если эжектируемое количество в значительной степени варьируется в зависимости от концентрации белка, например, когда пятна белка и пептида количественно расположены на подложке, то трудно подобрать так, чтобы получить желательные концентрации белка и пептида. Кроме того, также когда эжекционное устройство используется в качестве ингалятора, регулировка концентраций белка и пептида эжекционной жидкости становится трудной при униформализации количеств белка и пептида при каждом одном введении. Кроме того, требуется, чтобы в ингаляторе эжекция проводилась с еще меньшим размером капелек, и, следовательно, эжекция растворов белка и пептида может затрудняться.
Далее, настоящее изобретение более детально описано со ссылкой на примеры, но настоящее изобретение не ограничивается этими примерами. Следует отметить, что «%» означает «мас.%».
Соединения, используемые в примерах, каждое из которых имеет группу гуанидина и карбоксильную группу или группу сульфоновой кислоты в одной молекуле, а именно 3-гуанидинпропионовая кислота и 4-гуанидинбутановая кислота, были закуплены у компании Sigma Aldrich, Inc. Кроме того, 2-гуанидинуксусная кислота, α-гуанидинглутаминовая кислота, гуанидинметансульфоновая кислота, 2-гуанидинэтансульфоновая кислота и 3-гуанидинпропансульфоновая кислота были синтезированы со ссылкой на Vol. 33, p.5933-5936 (1992), Tetrahedron, Vol. 57, p. 7073-7105 (2001) и выложенную заявку на патент Японии № 2002-502378.
(Примеры 1-14 и Сравнительные примеры 1-14)
(Эжекция белковых растворов на основе принципа термического струйного устройства)
Процедура получения эжекционной жидкости показана ниже. В сверхчистой воде был предварительно растворен белок с тем, чтобы иметь соответствующую концентрацию. Соединение, имеющее группу гуанидина и карбоксильную группу или группу сульфоновой кислоты в одной молекуле, добавляют к полученному таким образом раствору при перемешивании. рН раствора доводят до 7,0 0,1 M NaOH или 0,1 М HCl, а затем объем раствора доводят добавлением сверхчистой воды с тем, чтобы он имел заданную концентрацию инсулина.
Эжекционную воду, полученную в соответствии с описанной выше процедурой, заливали в головку принтера Bubblejet (торговая марка) (торговое название: PIXUS950i; выпускаемый Canon Inc.), и путем привода эжекционной головки регулятором эжекции эжекция проводилась с частотой 500 Гц. По времени, используемому для эжекции, количество эжекционных доз было по расчетам сравнимо между жидкостями.
До и после эжекции каждую эжекционную жидкость подвергали анализу ВЭЖХ (условия измерения: аппарат: JASCO Corp., колонка: YMC-Pack Diol-200, 500×8,0 (внутренний диаметр); элюент: 0,1 M KH2PO4-K2HPO4 (рН 7,0), содержащий 0,2 M NaCl; скорость потока: 0,7 мл/мин; температура: 25°С; выявление: УФ при 215 нМ), для идентификации изменения композиции эжекционной жидкости.
В качестве Сравнительных примеров получали растворы инсулина и растворы BSA и эжекционные жидкости получали добавлением к инсулину или BSA соединения, отличного от соединения, имеющего группу гуанидина и карбоксильную группу или группу сульфоновой кислоты в одной молекуле. Эти растворы и эжекционные жидкости подвергали эксперименту эжекции капелек таким же образом, как в примерах. Составы, исследованные в Примерах и в Сравнительных примерах, перечислены ниже в таблице 1, а результаты показаны на Фиг. 7.
На Фиг. 7 показано, что растворы Сравнительных примеров 1-3 и 8-10 почти не эжектировались, независимо от присутствия или отсутствия добавки. С другой стороны, такие добавки, как аргинин и Tween 80, обеспечивали возможность эжекции растворов белка. Увеличение добавляемого количества аргинина увеличивало количество эжекционных доз, но, напротив, увеличение добавляемого количества Tween 80 уменьшало количество эжекционных доз. Напротив, в Примерах 1-14, растворы белка были способны эжектироваться при количестве эжекционных доз, по меньшей мере, вдвое или более большем, чем количество эжекционных доз в случаях Сравнительных примеров 4 и 11, где добавлялся аргинин. Кроме того, ввиду того что количества эжекционных доз в Примерах такие же или больше, чем в Сравнительных примерах 5 и 12, возможно, что соединения по настоящему изобретению дают такие же эффекты, как эффекты, вызванные аргинином, при концентрациях, составляющих половину или меньше, чем концентрация аргинина. В соответствии с результатами анализа ВЭЖХ, в любом из Примеров 1-14, не было обнаружено ни изменение положения пика, ни изменение площади пика и ни изменение композиции жидкости до и после эжекции.
(Примеры 15-21 и Сравнительный пример 15)
(Частота эжекции и количество эжекции)
Для составов Примеров 1-7 и Сравнительного примера 4, эжекцию проводили в тех же условиях, как и в Примере 1, где частота эжекции варьировалась от 500 Гц до 1000 Гц, а количества эжекционных доз были сравнимы. Полученные таким образом результаты показаны на Фиг. 8, где Примеры 15-21 соответствуют Примерам 1-7, а Пример 15 соответствует Сравнительному примеру 4.
Путем увеличения частоты эжекции количество эжекционных доз варьировалось в зависимости от добавляемых соединений. Сравнение Примеров со Сравнительными примерами выявило, что различие количества эжекционных доз при 1000 Гц в 6-25 раз выше, подтверждая, что составы Примеров были более эффективны для эжекции с высокой частотой.
(Примеры 22-61 и Сравнительные примеры 16-30)
(Воздействия на различные белки и концентрации добавок)
Последовательно, в качестве соединения, имеющего группу гуанидина и карбоксильную группу или группу сульфоновой кислоты в одной молекуле, были выбраны 3-гуанидинпропионовая кислота и 2-гуанидинэтансульфоновая кислота и добавлены к различным белкам в определенных концентрациях. Полученные таким образом эжекционные жидкости оценивались экспериментом эжекции. Частота эжекции устанавливалась на 1000 Гц. Каждый эксперимент эжекции проводился в течение 120 секунд, и случаи, когда эжекция была нормальной, отмечены буквой «А», а случай, когда эжекция прекращалась на полпути, обозначен буквой «С». Исследованные составы и полученные результаты в Примерах и Сравнительных примерах перечислены в показанной ниже Таблице 2.
При добавлении 3-гуанидинпропионовой кислоты или 2-гуанидинэтансульфоновой кислоты эжекция белков и пептидов с использованием термического краскоструйного устройства проводилась нормально. Следовательно, было удостоверено, что 3-гуанидинпропионовая кислота и 2-гуанидинэтансульфоновая кислота проявляли эффекты при использовании широких диапазонов белков и пептидов. В результате анализов ВЭЖХ, примененных в Примерах, в которых проводилась нормальная эжекция, до и после эжекции не были обнаружены ни изменения пика на карте, ни изменения композиции жидкости.
(Примеры 62-82)
(Синергические эффекты благодаря соединению, имеющему группу гуанидина и карбоксильную группу или группу сульфоновой кислоты в одной молекуле, и поверхностно-активное вещество)
К растворам белков и растворам пептидов добавляли 3-гуанидинпропионовую кислоту для получения эжекционных жидкостей. Эжекционные жидкости оценивали таким же экспериментом эжекции, как в Примере 22. Составы, исследованные в настоящих Примерах, и полученные таким образом результаты перечислены в показанной ниже Таблице 3.
При одновременном добавлении 3-гуанидинпропионовой кислоты и Tween (торговая марка) 80 полиоксиэтилен 20 сорбитанмоноолеат (выпускаемый компанией Calbiochem Inc.) растворы белков и пептидов были способны эжектироваться при концентрациях 3-гуанидинпропионовой кислоты, сниженных в 5-10 раз, по сравнению со случаями, где добавлялась только 3-гуанидинпропионовая кислота. Общие количества добавок также могут быть резко снижены, и, кроме того, возможность эжекции обеспечивалась даже для тех концентраций белков, которые не давали возможность производить эжекцию при добавлении только 3-гуанидинпропионовой кислоты; такие синергические эффекты также обеспечивали возможность эжекции белковых растворов с более высокими концентрациями. В Примерах проводился анализ ВЭЖХ, и, следовательно, до и после эжекции не были обнаружены изменения пика на карте и изменение композиции жидкости.
(Примеры 83-131 и Сравнительные примеры 31-35)
Изготавливали головку для эжекции жидкости с диаметром сопла 3 мкм на основе термического краскоструйного устройства, и резервуар, соединенный с головкой для эжекции жидкости, заполняли 30% водным раствором этанола. Путем привода эжекционной головки регулятором, электрически соединенным с головкой для эжекции жидкости, жидкость выталкивалась из эжекционного сопла, и размер частиц и распределение размера частиц полученных капелек измеряли лазерным дифракционным анализатором распределения размера частиц (выпускаемым компанией Spraytec, Malvern Instruments, Ltd.) и идентифицировали. В последующем, капельки выявлялись в виде капелек, имеющих отчетливое распределение размера частиц примерно в области 3 мкм.
Каждая из полученных эжекционных жидкостей заливалась в описанную выше кассету головки с диаметром сопла 3 мкм, кассета головки соединялась с регулятором эжекции, и эжекционная жидкость выталкивалась с частотой 20 кГц в течение 1 секунды, и после интервала 60 секунд проводилась следующая эжекция. Это повторялось 50 раз, и то, выталкивалась жидкость или нет, проверялось визуальным осмотром. Случай, когда эжекция наблюдалась 50 раз, оценивался как «А», а случай, где эжекция прекращалась на полпути, оценивался как «С». Исследованные составы и результаты, полученные в Примерах и Сравнительных примерах, перечислены в показанных ниже Таблицах 4-6.
В Сравнительном примере 31 из термического краскоструйного устройства с диаметром сопла 3 мкм эжекции не было, потому что в Сравнительном примере 31 в жидкости не содержалась никакая добавка. В Сравнительных примерах 32-35 было верифицировано, что, когда концентрация добавки была высокой, эжекционная жидкость стабильно выталкивалась. С другой стороны, было верифицировано, что в Примерах эжекционные жидкости стабильно выталкивались при более низких концентрациях добавок по сравнению со Сравнительными примерами, и было верифицировано, что эффект добавления соединений по настоящему изобретению является высоким. В результате анализа ВЭЖХ в каждом из Примеров не было обнаружено ни изменение положения пика, ни изменение площади пика и ни изменение композиции жидкости до и после эжекции.
(Пример 132)
(Получение чипа антитела путем использования струйного принтера и регистрации)
На Фиг. 9 представлена иллюстрация модели настоящего Примера, где показаны подложка 30; маскирующий агент 31; вещество 32, представляющее вещество, специфически реагирующее с подлежащим тестированию веществом, белком, пептидом или им подобным; подлежащее тестированию вещество 33; вещество 34, специфичное для вещества, подлежащего тестированию; и метка 35. Растворы моноклонального антитела против человеческого IL2, против человеческого IL4 и против человеческого IL6 получали использованием PBS, при концентрации каждого раствора от 0,1 до 500 мкг/мл. К этим растворам добавляли 2-гуанидинэтансульфоновую кислоту в количество 0,5% (мас./мас.) и, таким образом, получали эжекционные жидкости. Каждую из этих жидкостей заливали в головку краскоструйного принтера (торговое название: PIXUS950i; выпускаемый компанией Canon Inc.) и проводили эжекцию на покрытое поли-L-лизином предметное стекло.
Стекла после эжекции инкубировали при 4°С и стекла после инкубации подвергали маскировке 1% BSA. После маскировки стекла тщательно промывали и, таким образом, получали подложки чипа антитела.
Затем получали эжекционные жидкости рекомбинантов IL2, IL4 и IL6 в качестве подлежащих тестированию веществ 33, соответствующие чипам, каждое в концентрации 1 мкг/мл с тем, чтобы одновременно содержать 0,5% 2-гуанидинэтансульфоновой кислоты (мас./мас.), 0,5% Tween 20 (мас./мас.) и 0,1% BSA (мас./мас.) путем использования PBS. Каждую из этих жидкостей заливали в головку краскоструйного принтера (торговое название: PIXUS950i; выпускаемый компанией Canon Inc.) и проводили эжекцию таким же образом на описанные выше подложки. После эжекции каждую подложку покрывали покровным стеклом и давали возможность прореагировать при 4°С. После реакции подложки тщательно промывали и сушили.
Затем вещества 34, образующие специфические связи с образцами, подвергали взаимодействию с подложками и после этого на вещества наносили метки 35. В качестве веществ, образующих специфические связи с образцами, с использованием PBS получали растворы антител в концентрации 1 мкг/мл соответствующих меченных биотином антител (биотинизированное моноклональное антитело против человеческого IL2, биотинизированное моноклональное антитело против человеческого IL4 и биотинизированное моноклональное антитело против человеческого IL6) с тем, чтобы каждое вещество имело следующие конечные концентрации: 0,5% 2-гуанидинэтансульфоновой кислоты (мас./мас.), 0,5% Tween 20 (мас./мас.) и 0,1% BSA (мас./мас.). Каждую из этих жидкостей заливали в головку краскоструйного принтера (торговое название: PIXUS950i; выпускаемый компанией Canon Inc.) и проводили эжекцию таким же образом на описанные выше подложки. После эжекции каждую подложку покрывали покровным стеклом и давали возможность прореагировать при 4°С. После реакции подложки тщательно промывали и сушили.
Для мечения, получали раствор 10 мкг/мл меченного Cy3 стрептавидина с использованием PBS с тем, чтобы каждое вещество имело следующие конечные концентрации: 0,5% 2-гуанидинэтансульфоновой кислоты (мас./мас.), 0,5% Tween 20 (мас./мас.) и 0,1% BSA (мас./мас.). Эжекционную жидкость заливали в головку краскоструйного принтера (торговое название: PIXUS950i; выпускаемый компанией Canon Inc.) и проводили эжекцию таким же образом на описанные выше подложки. После эжекции каждую подложку покрывали покровным стеклом и давали возможность прореагировать при 4°С. После реакции подложки тщательно промывали и сушили.
В последующем, каждую из подложек после реакции облучали возбуждающим световым излучением и количество испускаемого светового излучения Су3 измеряли в виде количественной характеристики сигнала флуоресценции путем использования флуоресцентного сканера, оборудованного фильтром, пропускающим волны длиной 532 нм. Следовательно, можно было выявлять сигналы флуоресценции, соответствующие типам и концентрациям образцов.
Настоящее изобретение не ограничено вышеприведенными примерами воплощения, и в него могут быть внесены различные изменения и модификации в пределах сущности и объема настоящего изобретения. Поэтому для оценки объема настоящего изобретения представлена следующая формула изобретения.
Настоящая заявка испрашивает приоритет заявки на патент Японии № 2006-327031, поданной 4 декабря 2006 г., которая включена в настоящее описание путем ссылки.
Изобретение относится к медицине и касается эжекционной жидкости для выброса путем передачи термической энергии, включающей белок или пептид; соединение, имеющее гуанидиновую группу и карбоксильную группу или группу сульфоновой кислоты в одной молекуле и представленное общей формулой (1), или соль этого соединения; и жидкую среду. Изобретение обеспечивает стабильно эффективное эжектирование широкого спектра белков и пептидов при существенно более низких концентрациях стабилизирующей добавки, что в результате повышает безопасность эжектирования лекарственных средств. 5 н. и 9 з.п. ф-лы, 9 ил., 6 табл.
1. Эжекционная жидкость для выброса путем передачи термической энергии, включающая белок или пептид;
соединение, имеющее гуанидиновую группу и карбоксильную группу или группу сульфоновой кислоты в одной молекуле и представленное общей формулой (1), или соль соединения; и жидкую среду:
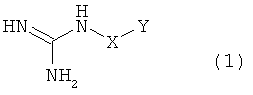
где X в общей формуле (1) представляет необязательно разветвленную алкильную группу, имеющую от одного до восьми атомов углерода, и Y представляет карбоксильную группу или группу сульфоновой кислоты.
2. Эжекционная жидкость по п.1, где соединение, представленное общей формулой (1), содержит одно или два или более соединений, выбранных из группы, состоящей из 2-гуанидинуксусной кислоты, 3-гуанидинпропионовой кислоты, 4-гуанидинбутановой кислоты, α-гуанидинглутаминовой кислоты, гуанидинметансульфоновой кислоты, 2-гуанидинэтансульфоновой кислоты, 3-гуанидинпропансульфоновой кислоты и солей этих соединений.
3. Эжекционная жидкость по п.1, дополнительно содержащая поверхностно-активное вещество.
4. Эжекционная жидкость по п.3, где поверхностно-активное вещество представляет сложный эфир жирной кислоты полиоксиэтиленсорбитана.
5. Кассета для эжекции жидкости, включающая
резервуар, в котором содержится эжекционная жидкость по п.1; и
эжекционную головку, включающую электротермический преобразователь для передачи эжекционной жидкости термической энергии.
6. Ингалятор, включающий
кассету по п.5 и
канал всасывания, из которого пользователь вдыхает жидкость,
изгоняемую из эжекционной головки кассеты.
7. Способ эжекции для выброса жидкой композиции путем передачи ей термической энергии, включающей
белок или пептид;
соединение, имеющее гуанидиновую группу и карбоксильную группу или группу сульфоновой кислоты в одной молекуле и представленное общей формулой (1), или соль соединения; и жидкую среду:
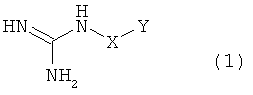
где Х в общей формуле (1) представляет необязательно разветвленную алкильную группу, имеющую от одного до восьми атомов углерода, и Y представляет карбоксильную группу или группу сульфоновой кислоты.
8. Способ эжекции по п.7, где жидкая композиция дополнительно содержит поверхностно-активное вещество.
9. Способ эжекции по п.7, где способ эжекции жидкой композиции путем передачи ей термической энергии основан на термическом струйном устройстве.
10. Применение соединения, имеющего гуанидиновую группу и карбоксильную группу или группу сульфоновой кислоты в одной молекуле и представленного следующей общей формулой (1), или соли соединения в качестве добавки для эжекции жидкой композиции, содержащей белок и пептид, путем передачи термической энергии жидкой композиции:
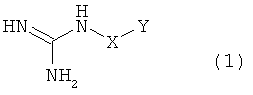
где X в общей формуле (1) представляет необязательно разветвленную алкильную группу, имеющую от одного до восьми атомов углерода, и Y представляет карбоксильную группу или группу сульфоновой кислоты.
11. Эжекционная жидкость по п.1, где соединение, представленное общей формулой (1), добавляют в количестве, составляющем от 0,1 части по массе до 50 частей по массе, в расчете на 1 часть по массе белка или пептида.
12. Кассета для эжекции жидкости по п.5, где соединение, представленное общей формулой (1), добавляют в количестве, составляющем от 0,1 части по массе до 50 частей по массе, в расчете на 1 часть по массе белка или пептида.
13. Ингалятор по п.6, где соединение, представленное общей формулой (1), добавляют в количестве, составляющем от 0,1 части по массе до 50 частей по массе, в расчете на 1 часть по массе белка или пептида.
14. Способ эжекции для выброса жидкой композиции по п.7, где соединение, представленное общей формулой (1), добавляют в количестве, составляющем от 0,1 части по массе до 50 частей по массе, в расчете на 1 часть по массе белка или пептида.
| Пломбировальные щипцы | 1923 |
|
SU2006A1 |
Авторы
Даты
2011-06-10—Публикация
2007-11-09—Подача