Изобретение относится к медицине, а именно к травматологии и ортопедии - для лечения больных, нуждающихся в проведении эндопротезирования тазобедренного сустава. Задачей изобретения является увеличение стабильности имплантата и улучшение результатов операции.
В последние десятилетия наблюдается значительный рост хирургической активности при лечении больных ортопедотравматологического профиля. Ежегодно в мире выполняется около 500 тысяч эндопротезирований тазобедренного сустава и около 300 тысяч - коленного. При статистическом учете хирургических вмешательств было выяснено, что число осложнений стабилизировалось и их снижение не прогнозируется [4; 6]. Количество ревизионных эндопротезирований, большая часть из которых (69±9%) проводится по причине асептической нестабильности компонентов эндопротеза, в США в течение последних шести лет стабильно составляет около 50 тысяч в год [11]. Совершенствование металлоконструкций в последние годы не оказывает значимого влияния на усиление остеоинтеграции и, следовательно, вторичной стабильности компонентов эндопротеза, что косвенно свидетельствует об исчерпанности механистического подхода. Между тем количество ревизионных вмешательств заставляет искать новые пути решения проблемы.
Перспективным направлением является внедрение в практику клеточных технологий тканевой инженерии, в основе которых лежит использование мультипотентных стволовых клеток (СК) и транзиторных клеток (ТК).
Из существующих направлений в настоящее время наиболее изучена и готова к апробации трансплантация выращенных in vitro клеток, которые могут быть получены из различных тканей, но наименее морбидным источником является костный мозг из гребня подвздошной кости, который характеризуется хорошей клеточностью и низким превалированием. В дальнейшем клетки управляемо могут дифференцироваться в различные фенотипы [1; 2].
Для снижения частоты ревизионных операций, обусловленных асептической нестабильностью, целесообразно усиление остеоинтеграции именно на границе металл/кость, где возможности каркасных технологий не столь актуальны. Увеличение образования новой костной ткани и минеральной плотности кости вокруг установленного импланта усиливает остеоинтеграцию и повышает тем самым стабильность вторичной фиксации компонента эндопротеза [7; 12].
Попытки поиска методов усиления формирования новой костной ткани в области ее дефекта при помощи использования аутологичных МСК, подсаженных на остеотрансплантат, в моделях на животных впервые были описаны зарубежными авторами в 1998 г. [5]. Позже были исследованы результаты применения для этих же целей синтетических заменителей кости и костного морфогенного белка-1 (ОР-1, ВМР-7) при установке однополюсных эндопротезов тазобедренного сустава у животных [3; 10]. Впервые получить положительные результаты при использовании аллоостеотрансплантата вместе с выращенными на нем МСК, помещаемого в костномозговой канал бедренной кости перед эндопротезированием у овец, в целях изучения остеоинтеграции удалось только в 2008 г. в Великобритании [9]. Однако в этом случае в качестве носителя МСК должен использоваться аллоостеотрансплантат или же выполняться предшествующий эндопротезированию операции забор аутоостеотрансплантата пациента. Остается также невыясненным эффект от остеоиндукции МСК при их экспандировании в этом случае.
Задачей настоящего исследования является разработка способа использования остеоиндуцированных мезенхимальных стволовых клеток (МСК) на порозном биодеградируемом носителе для усиления остеоинтеграции компонентов эндопротеза тазобедренного сустава и повышения тем самым его вторичной стабильности.
Авторами изобретения предложен способ местного применения остеоиндуцированных мезенхимальных стволовых клеток, экспедированных на биодеградируемом пространственном порозном носителе, включающий проведение двух этапов вмешательства. Забор клеток костного мозга для первого этапа проводят из подвздошной кости. Дальнейшее экспандирование МСК занимает 2-3 недели и, в конечном итоге, заканчивается остеоиндуцированием и пассажем на желатиновую губку.
После экспансии на втором этапе вмешательства мезенхимальные стволовые клетки имплантируются на указанном носителе в область подготовленных вертлужной впадины и костно-мозгового канала бедренной кости непосредственно перед установкой компонентов эндопротеза тазобедренного сустава. В результате аутологичные мезенхимальные стволовые клетки в реципиентном месте дифференцируются в костный фенотип, что альтерирует гистогенез путем усиления репарации и остеогенеза, способствуя повышению остеоинтеграции компонентов.
В качестве имплантируемых конструкций использовались бесцементные эндопротезы тазобедренного сустава Biomet (Франция) со структурированной поверхностью и преимущественно проксимальным типом фиксации.
Заявленный способ осуществляют следующим образом. За 2-3 недели до операции эндопротезирования тазобедренного сустава из гребня подвздошной кости производится забор костного мозга (фиг.1).
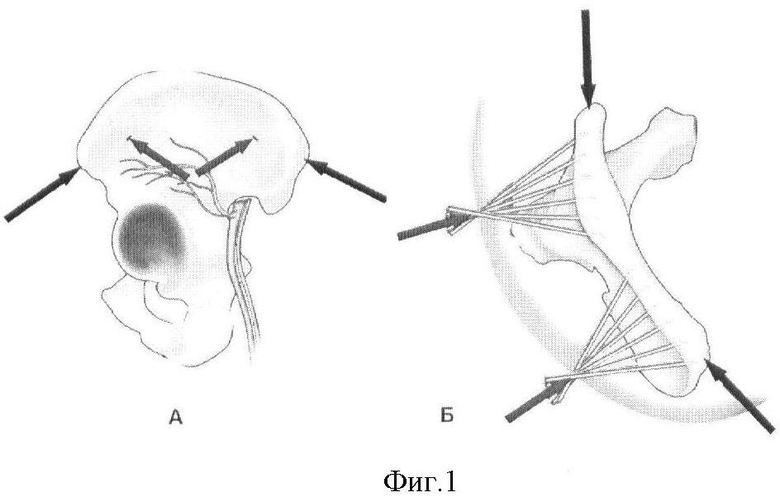
На фиг.1. показана методика забора костного мозга [10].
Костный мозг может быть получен путем аспирации как из передней, так и из задней части гребня подвздошной кости. Используются два стандартных доступа, показанных на фиг.1А. В местах, обозначенных красными стрелками, тупым путем проводят аспирационную иглу по направлению к поверхности подвздошной кости, при этом нужно не повредить ягодичные нервы и сосуды. В большинстве случаев толщина подвздошной кости позволяет выполнить аспирацию сразу после введения иглы в медуллярную полость. Затем иглу подтягивают на себя, отклоняют в сторону на 5 мм и выполняют повторную аспирацию через тот же прокол в подвздошной кости (фиг.1Б). С целью получения большего количества костного мозга можно выполнять серию трепанаций подвздошной кости на расстоянии 8-10 мм друг от друга, при этом используется один и тот же прокол кожи, а движение аспирационной иглы происходит веерообразно. Также возможна аспирация достаточного количества костного мозга через одно трепанационное отверстие. При этой методике иглу вводят в кость, аспирируют содержимое, после этого иглу продвигают глубже по оси кости на 5-10 мм и выполняют повторную аспирацию. Введение иглы по оси может аналогично выполняться как через заднюю, так и через переднюю ости подвздошной кости (черные стрелки).
Выделение и культивирование мезенхимальных стволовых клеток проводили по стандартной методике. Полученный костный мозг в условиях ламинарного шкафа тщательно ресуспендировали, центрифугировали в течение 10 мин при 200g. Надосадочную жидкость сливали, осадок ресуспендировали в среде α-МЕМ и вновь центрифугировали в течение 10 мин при 200g. Клеточный осадок для удаления эритроцитов ресуспендировали в лизирующем буфере, инкубировали в течение 10 мин при комнатной температуре, затем дважды отмывали средой центрифугированием при 200g 10 мин. После последнего центрифугирования клеточный осадок ресуспендировали в полной ростовой среде и высевали клетки в культуральные флаконы в концентрации 4×105 кл/см2. Через 4 часа неприкрепившиеся клетки удаляли 3-кратным промыванием средой α-МЕМ. Клетки культивировали при температуре 37°C, 5% CO2. Смену среды проводили каждые 3-4 дня. При достижении 70% конфлуентного монослоя (10-14 суток) клетки пассировали раствором трипсина-Версена в соотношении 1:4. Далее проводили культивирование МСК на желатиновой губке (Spongostan, Johnson & Johnson). По достижении нужной клеточной массы клетки снимали с культурального пластика раствором трипсина-Версена, фермент ингибировали ростовой средой, суспензию МСК центрифугировали при 200g 10 мин. Осадок клеток ресуспендировали в малом объеме ростовой среды и наслаивали на желатиновые губки. Через 2 часа (после прикрепления клеток) добавляли ростовую среду и культивировали при 37°C, 5% CO2 в течение 10-14 суток до трансплантации.
По готовности к трансплантации аутологичных МСК выполнялось эндопротезирование тазобедренного сустава с установкой компонентов эндопротеза в костное ложе с вышеуказанным носителем и МСК. После обработки вертлужной впадины фрезами до необходимого уровня во внутреннюю поверхность впадины укладывались пленки гемостатической губки Спонгостана (Spongostan, Johnson & Johnson) с МСК, а затем методом press-fit устанавливался бесцементный вертлужный компонент. В костномозговой канал бедренной кости измельченные пленки гемостатической губки Спонгостан с МСК вводили после обработки канала рашпилем и установки костной пробки, а затем забивали бесцементную ножку эндопротеза, добиваясь таким образом равномерного распределения носителя с МСК на границе металл/кость.
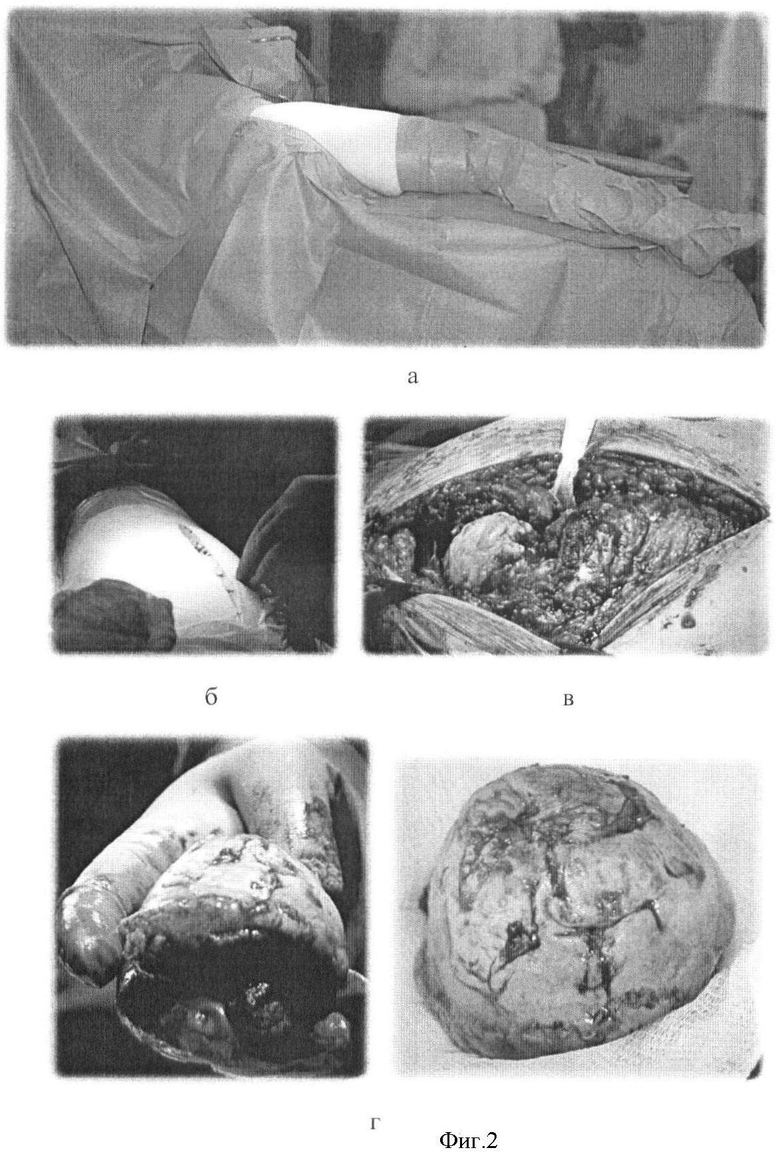
Ход операции иллюстрирован фиг.2.
а - положение больного на операционном столе;
б - выполнение хирургического доступа;
в - в рану вывихнута головка бедренной кости;
г - удаленная головка бедренной кости;
д - обработка фрезами вертлужной впадины;
е - в ацетабулярную впадину уложены губки Спонгостана с культивированными МСК;
ж - процесс заполнения подготовленного рашпилями костномозгового канала бедренной кости Спонгостаном с МСК;
з - ножка эндопротеза установлена.
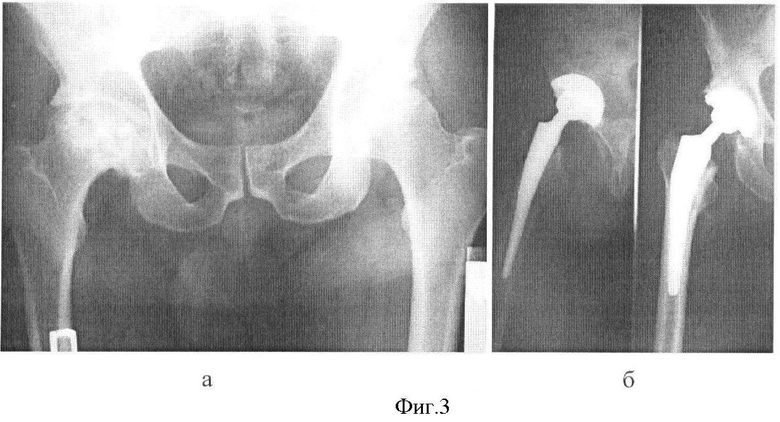
На фиг.3 показаны рентгенограмма до операции (а) и рентгенограммы после операции (б).
На этапе оценки результатов проводились: субъективное обследование, рентгенография, остеоденситометрия, компьютерная томография, гистологические и иммуногистохимические исследования.
В итоге установлено, что использование аутологичных остеоиндуцированных мезенхимальных стволовых клеток, экспандированных на пространственном носителе и помещенных вокруг эндопротеза тазобедренного сустава, позволяет на 25% увеличить в послеоперационном периоде (до 1 года) формирование новой костной ткани и на 12% - показатели костной массы и минеральной плотности костной ткани вокруг установленного металлического импланта.
Заявленный способ использования аутологичных остеоиндуцированных мезенхимальных стволовых клеток может применяться с целью стимуляции сниженных регенераторных возможностей костной ткани пациента, заполнения образовавшихся дефектов кости и повышения тем самым остеоинтеграции и вторичной стабильности компонентов при эндопротезировании тазобедренных суставов.


| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ОДНОЭТАПНОГО ДВУСТОРОННЕГО ЭНДОПРОТЕЗИРОВАНИЯ ТАЗОБЕДРЕННЫХ СУСТАВОВ ПРИ ДВУСТОРОННЕМ ДИСПЛАСТИЧЕСКОМ КОКСАРТРОЗЕ С ПОЛНЫМ ВЫВИХОМ И ВЫСОКИМ СМЕЩЕНИЕМ ГОЛОВОК БЕДРЕННЫХ КОСТЕЙ | 2008 |
|
RU2397720C2 |
| СПОСОБ АУТООСТЕОПЛАСТИКИ ВЕРТЛУЖНОЙ ВПАДИНЫ ПРИ РЕВИЗИОННОМ ЭНДОПРОТЕЗИРОВАНИИ ТАЗОБЕДРЕННОГО СУСТАВА | 2007 |
|
RU2355339C2 |
| СПОСОБ ХИРУРГИЧЕСКОЙ КОРРЕКЦИИ ДЕФОРМАЦИЙ ТАЗОБЕДРЕННОГО СУСТАВА | 2000 |
|
RU2173108C1 |
| ПОВЕРХНОСТНЫЙ ЭНДОПРОТЕЗ ТАЗОБЕДРЕННОГО СУСТАВА С ЯЧЕИСТОЙ СТРУКТУРОЙ И БИОАКТИВНЫМ ПОКРЫТИЕМ | 2023 |
|
RU2810408C1 |
| СПОСОБ ЛЕЧЕНИЯ ПЕРЕЛОМОВ ШЕЙКИ БЕДРЕННОЙ КОСТИ | 2008 |
|
RU2371131C1 |
| СПОСОБ ХИРУРГИЧЕСКОЙ КОРРЕКЦИИ ДЕФЕКТОВ ДИСТАЛЬНЫХ ОТДЕЛОВ БЕДРЕННОЙ КОСТИ | 2007 |
|
RU2356505C1 |
| ПОВЕРХНОСТНЫЙ ЭНДОПРОТЕЗ ТАЗОБЕДРЕННОГО СУСТАВА С ЯЧЕИСТОЙ СТРУКТУРОЙ | 2023 |
|
RU2810409C1 |
| СПОСОБ ЛЕЧЕНИЯ ЛОЖНЫХ СУСТАВОВ ПУТЕМ ТРАНСПЛАНТАЦИИ АУТОЛОГИЧНЫХ МЕЗЕНХИМАЛЬНЫХ СТВОЛОВЫХ КЛЕТОК, БИОТРАНСПЛАНТАТ ДЛЯ ЕГО ПРИМЕНЕНИЯ | 2006 |
|
RU2309756C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ СТЕПЕНИ ПОКРЫТИЯ ВЕРТЛУЖНОГО КОМПОНЕНТА БЕСЦЕМЕНТНОЙ ФИКСАЦИИ В ПРОЦЕНТНОМ СООТНОШЕНИИ ПОСЛЕ ЕГО ИМПЛАНТАЦИИ В ОБРАБОТАННУЮ ВЕРТЛУЖНУЮ ВПАДИНУ ПРИ ПЕРВИЧНЫХ И РЕВИЗИОННЫХ ОПЕРАЦИЯХ ЭНДОПРОТЕЗИРОВАНИЯ ТАЗОБЕДРЕННОГО СУСТАВА | 2009 |
|
RU2412646C2 |
| СПОСОБ ЭНДОПРОТЕЗИРОВАНИЯ ТАЗОБЕДРЕННОГО СУСТАВА ПРИ КОСТНОМ АНКИЛОЗЕ | 2011 |
|
RU2460483C1 |

Изобретение относится к травматологии и ортопедии и может быть применимо для усиления остеоинтеграции компонентов эндопротеза тазобедренного сустава. Забирают у пациента костный мозг. Получают и культивируют мезенхимальные стволовые клетки из костного мозга. Через 2-3 недели выполняют эндопротезирование тазобедренного сустава с бесцементной установкой компонентов эндопротеза в костное ложе. Обрабатывают вертлужную впадину фрезами. Укладывают на внутреннюю поверхность вертлужной впадины пленки гемостатической губки с полученными из костного мозга пациента и культивированными мезенхимальными стволовыми клетками. Устанавливают бесцементный вертлужный компонент эндопротеза. Обрабатывают костно-мозговой канал бедренной кости рашпилем. Устанавливают костную пробку. Вводят измельченные пленки гемостатической губки с полученными из костного мозга пациента и культивированными мезенхимальными стволовыми клетками. Устанавливают в костномозговой канал ножку эндопротеза. Способ позволяет стимулировать регенераторные возможности костной ткани, повысить стабильность эндопротеза. 2 з.п.ф., 3 ил.
1. Способ усиления остеоинтеграции компонентов эндопротеза тазобедренного сустава, отличающийся тем, что на первом этапе забирают у пациента костный мозг, получают и культивируют мезенхимальные стволовые клетки из костного мозга, на втором этапе через 2-3 недели по готовности к трансплантации аутологичных мезенхимальных стволовых клеток выполняют эндопротезирование тазобедренного сустава с бесцементной установкой компонентов эндопротеза в костное ложе следующим образом: обрабатывают вертлужную впадину фрезами, на внутреннюю поверхность вертлужной впадины укладывают пленки гемостатической губки с полученными из костного мозга пациента и культивированными мезенхимальными стволовыми клетками, затем устанавливают бесцементный вертлужный компонент эндопротеза, обрабатывают костномозговой канал бедренной кости рашпилем, устанавливают костную пробку, вводят измельченные пленки гемостатической губки с полученными из костного мозга пациента и культивированными мезенхимальными стволовыми клетками, затем устанавливают в костномозговой канал ножку эндопротеза.
2. Способ по п.1, отличающийся тем, что в качестве гемостатической губки применяют гемостатическую губку Спонгостан.
3. Способ по п.1, отличающийся тем, что вертлужный и бедренный компоненты эндопротеза устанавливают методом пресс-фит.
| KORDA M | |||
| et al | |||
| Use of mesenchymal stem cells to enhance bone formation around revision hip replacements | |||
| J Orthop Res | |||
| Станок для изготовления деревянных ниточных катушек из цилиндрических, снабженных осевым отверстием, заготовок | 1923 |
|
SU2008A1 |
| СПОСОБ УСТАНОВКИ НОЖКИ ЭНДОПРОТЕЗА ТАЗОБЕДРЕННОГО СУСТАВА | 2005 |
|
RU2284788C1 |
| US 7211113, 01.05.2007 | |||
| РУЦКИЙ А.В | |||
| и др | |||
| Остеоинтеграция бесцементного эндопротеза тазобедренного сустава | |||
| Медицина (научно-практический рецензируемый медицинский журнал в Беларуси), 2006, №2, с.24-26. | |||
Авторы
Даты
2011-06-20—Публикация
2009-08-11—Подача