Изобретение относится к медицинской биотехнологии и может быть использовано в производстве биологически активных веществ с антибактериальными, антигрибными, антивирусными и иммуномодулирующими свойствами, а также в создании доставщиков ДНК и лекарственных средств на основе низкомолекулярного хитозана.
Хитозан - природный высокомолекулярный гетерополимер D-глюкозоамина и N-ацетил-D-глюкозоамина, соединенных 1,4-β-гликозидной связью. Хитозан обладает антибактериальными, антигрибными, антивирусными и иммуномодулирующими свойствами, может быть использован как адъювант, радиопротектор, компонент гелевых и мазевых композиций, как доставщик ДНК, лекарственных и других веществ, в качестве элиситора повышает устойчивость растений к бактериальным, грибным и вирусным заболеваниям [1, 2].
Исходный хитозан является биополимером с молекулярной массой 1000 кДа (и выше), что соответствует степени полимеризации, равной 5000, практическое использование которого затруднено из-за высокой вязкости его водных растворов даже при низкой концентрации (менее 0,01%), а также недостаточной растворимости при нейтральных значениях рН и, как следствие, низкой биологической активности. Для снижения вязкости, улучшения растворимости и усиления биологической активности высокомолекулярный хитозан подвергают химической или ферментативной деполимеризации. Полученный в процессе деполимеризации низкомолекулярный хитозан с молекулярной массой от 2 до 20 кДа обладает высокой биологической активностью и способен растворяться в растворах со значениями рН, близкими к нейтральным (рН 6,5-7,0) [3,4]. Ферментативную деполимеризацию высокомолекулярного хитозана обычно проводят в 0,2-0,3 М натрий-ацетатных или натрий-лактатных буферных системах при рН 4,5-6,5 [5, 6]. Наличие солевого буфера объясняется хорошей растворимостью хитозана только в присутствии избытка кислоты, что сопровождается необходимостью после полного растворения хитозана доводить сильнокислый раствор растворенного таким способом полимера (<4,0) до значений рН, оптимальных (4,5-6,5) для ферментов, использующихся для деполимеризации хитозана. Это приводит к наличию в конечном продукте значительных количеств солей, удаление которых в масштабах промышленного производства требует длительного диализа и сопровождается существенными потерями наиболее низкомолекулярных фракций хитозана.
Целью заявленного изобретения является разработка способа, позволяющего получить низкомолекулярный водорастворимый при рН 6,5-7,0 хитозан путем ферментативной деполимеризации в бессолевых условиях.
Поставленная задача достигается путем разработки способа получения низкомолекулярного хитозана, который предусматривает предварительное переосаждение исходного высокомолекулярного хитозана (в результате чего он приобретает способность растворяться при добавлении минимального количесва кислоты), для чего его растворяют в растворе кислоты, а после полного растворения осаждают добавлением раствора щелочи; отмывку переосажденного высокомолекулярного хитозана от образовавшейся соли и избытка щелочи с помощью крупнопористого фильтра (на этой стадии отмывка солей не сопровождается потерей целевого вещества за счет высокой молекулярной массы хитозана); растворение переосажденного хитозана в расчетном количестве кислоты (уксусной, молочной, соляной) до оптимального для ферментативной деполимеризации значения рН (4,5-6,5); добавление ферментного препарата; проведение процесса гидролиза при оптимальной температуре; остановку реакции после определенного промежутка времени.
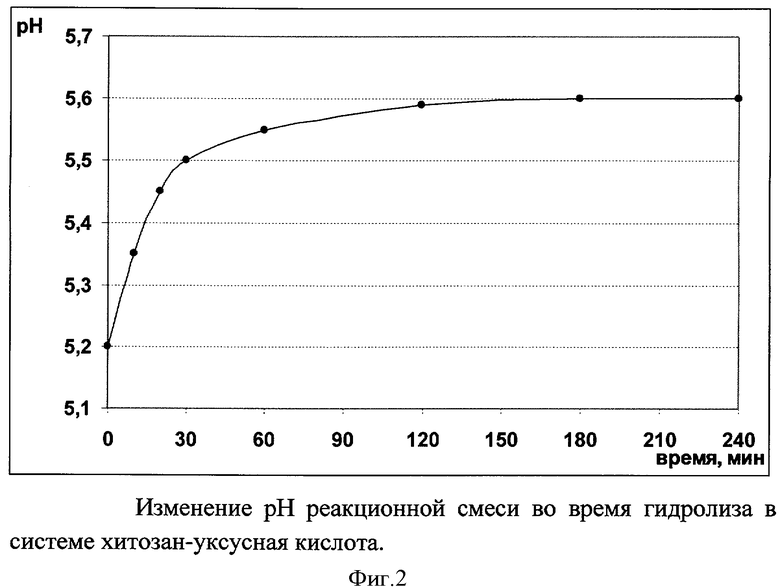
В указанном выше диапазоне значений рН система хитозан-кислота представляет собой буферную систему, что подтверждается образованием плато на графике титрования растворенного в кислоте хитозана раствором щелочи (фиг.1), и, таким образом, не нуждается в использовании солевой буферной системы для поддержания необходимой кислотности среды. В процессе деполимеризации наблюдается небольшое повышение значения рН за счет улучшения доступности аминогрупп низкомолекулярного хитозана, которое происходит в ходе гидролиза (фиг.2). Таким образом, предлагаемая нами схема деполимеризации позволяет не использовать солевую буферную систему во время гидролиза, а следовательно избежать необходимости удалять соли из конечного продукта, и получать хитозан с заданным противоионом: ацетат, лактат, хлорид и другие.
Техническим результатом заявленного изобретения является разработка упрощенного и предотвращающего потери целевого вещества способа получения низкомолекулярного водорастворимого хитозана с молекулярной массой в диапазоне от 2 до 20 кДа с помощью ферментативной деполимеризации в бессолевых условиях, характеризующегося наличием в реакционной среде только целевого вещества (хитозана) и фермента (ферментного препарата), отсутствием в реакционной среде солей (хлорид натрия, ацетат натрия и т.п.), отсутствием необходимости удаления солей по причине отсутствия таковых в ферментной системе и целевом продукте методами, которые сопровождаются потерями целевого продукта.
Пример 1. Получение низкомолекулярного хитозана в бессолевой среде с помощью ферментативного препарата Целловиридин Г20х. Взвешивают 1 г высокомолекулярного крабового хитозана. Растворяют его в 100 мл 0,3%-ного раствора уксусной кислоты. Осаждают растворенный хитозан добавлением 2 мл 10%-ного раствора гидроксида натрия. Отмывают осажденный хитозан с помощью крупнопористого фильтра дистиллированной водой до тех пор, пока значение рН промывных вод не достигнет 5,5. К полученному осадку хитозана добавляют дистиллированную воду, доводя объем смеси до 100 мл. Затем, при постоянном перемешивании, добавляют в смесь 5%-ную уксусную кислоту, доводя рН раствора до 5,5. При таком значении рН переосажденный хитозан полностью растворяется. После установления заданного значения рН к раствору добавляют ферментный препарат Целловиридин Г20х, полученный из гриба Trichoderma viride, в количестве 0,0025 г, достигая фермент-субстратного соотношения 1:400 (фермент:субстрат). Реакцию гидролиза ведут при +55°С в течение 4 часов при перемешивании. Реакцию останавливают нагреванием гидролизата до +100°С в течение 10 минут. Результаты реакции оценивают по падению динамической вязкости раствора гидролизуемого хитозана и средневязкостной молекулярной массы хитозана. Полученные результаты приведены в таблице 1.
Пример 2. Получение низкомолекулярного хитозана в бессолевой среде проводят аналогично примеру 1, но в качестве кислоты для растворения используют не уксусную кислоту, а молочную, соляную или другие. Полученные результаты приведены в таблицах 2 и 3.
Пример 3. Получение низкомолекулярного хитозана в бессолевой среде проводят аналогично примеру 1, но реакцию гидролиза проводят при значениях рН в интервале от 4,5 до 6,5. Полученные результаты приведены в таблице 4.
Пример 4. Получение низкомолекулярного хитозана в бессолевой среде проводят аналогично примеру 1, но реакцию гидролиза проводят при значениях температуры в интервале от +45°С до +65°С. Полученные результаты приведены в таблице 5.
Пример 5. Получение низкомолекулярного хитозана в бессолевой среде проводят аналогично примеру 1, но реакцию гидролиза ведут различные промежутки времени - от 30 до 360 минут. Полученные результаты приведены в таблице 6.
Пример 6. Получение низкомолекулярного хитозана в бессолевой среде проводят аналогично примеру 1, но реакцию гидролиза ведут при различных фермент-субстратных соотношениях - от 1:10 до 1:1000. Полученные результаты приведены в таблице 7.
ЛИТЕРАТУРА
1. Куликов С.Н., Чирков С.Н., Ильина А.В., Лопатин С.А, Варламов В.П. Влияние молекулярной массы хитозана на его противовирусную активность в растениях. Прикладная биохимия и микробиология. 2006. Т.42. №2. С.224-228.
2. Хитин и хитозан: получение, свойства и применение. Под ред. К.Г.Скрябина, Г.А.Вихоревой, В.П. Варламова. Москва: Наука, 2002. 368 с.
3. RU 2188829 С1, 10.09.2002.
4. RU 2073016 С1, 10.02.1997.
5. Il'ina A.V., Tatarinova N.Yu., Varlamov V.P. The preparation of low-molecular-weight chitosan using chitinolytic complex from Streptomyces kurssanovii. Process Biochemistry. 1999. V.34. P.875-878.
6. Ильина A.B., Ткачева Ю.В., Варламов В.П. Деполимеризация высокомолекулярного хитозана ферментным препаратом целловиридин Г20х. Прикладная биохимия и микробиология. 2002. Т.38. №1. С.5-13.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ НАНОКРИСТАЛЛИТОВ НИЗКОМОЛЕКУЛЯРНОГО ХИТОЗАНА | 2016 |
|
RU2627540C1 |
| Способ получения низкомолекулярного хитозана ферментативным гидролизом | 2023 |
|
RU2812997C1 |
| СПОСОБ ПОЛУЧЕНИЯ НИЗКОМОЛЕКУЛЯРНОГО ХИТОЗАНА, РАСТВОРИМОГО В ЩЕЛОЧНЫХ УСЛОВИЯХ | 2008 |
|
RU2384588C2 |
| СПОСОБ ПОЛУЧЕНИЯ ОЛИГОМЕРОВ ХИТОЗАНА | 2011 |
|
RU2445101C1 |
| Способ получения низкомолекулярного хитозана и олигомеров хитозана | 2016 |
|
RU2627870C1 |
| СПОСОБ ПОЛУЧЕНИЯ ВОДОРАСТВОРИМЫХ ОЛИГОМЕРНЫХ ГОМОЛОГОВ ХИТОЗАНА В ГЕТЕРОГЕННОЙ СИСТЕМЕ | 2011 |
|
RU2479590C1 |
| СПОСОБ ПОЛУЧЕНИЯ ГЕПАРИНОВ С НИЗКОЙ МОЛЕКУЛЯРНОЙ МАССОЙ | 2005 |
|
RU2295538C2 |
| СПОСОБ ПОЛУЧЕНИЯ НИЗКОМОЛЕКУЛЯРНОГО ОЛИГОМЕРНОГО ХИТОЗАНА И ЕГО ПРОИЗВОДНЫХ | 2018 |
|
RU2703437C1 |
| СПОСОБ ПОЛУЧЕНИЯ ИММОБИЛИЗОВАННОГО ФЕРМЕНТНОГО ПРЕПАРАТА НА ОСНОВЕ БРОМЕЛАЙНА, ГИАЛУРОНОВОЙ КИСЛОТЫ И ПОЛИСАХАРИДОВ, МОДИФИЦИРОВАННЫХ ВИНИЛОВЫМИ МОНОМЕРАМИ | 2020 |
|
RU2750377C1 |
| БИОСТИМУЛЯТОР РОСТА СЕЛЬСКОХОЗЯЙСТВЕННЫХ РАСТЕНИЙ ИЗ ХИТИНА РАКООБРАЗНЫХ И СПОСОБ ПОЛУЧЕНИЯ БИОСТИМУЛЯТОРА РОСТА СЕЛЬСКОХОЗЯЙСТВЕННЫХ РАСТЕНИЙ ИЗ ХИТИНА РАКООБРАЗНЫХ | 2012 |
|
RU2504953C2 |
Изобретение относится к области биотехнологии. Предложен способ получения низкомолекулярного хитозана с молекулярной массой от 2 до 20 кДа. Растворяют исходный высокомолекулярный хитозан в растворе кислоты. Затем осаждают растворенный в кислоте хитозан добавлением раствора щелочи. Отмывают переосажденный высокомолекулярный хитозан от образовавшейся соли и избытка щелочи с помощью крупнопористого фильтра. Растворяют переосажденный хитозан в растворе кислоты до значения рН 5,5. Добавляют ферментный препарат и проводят процесс гидролиза. Останавливают реакцию после образования низкомолекулярного хитозана. Способ характеризуется отсутствием необходимости удаления солей в ферментативной смеси и целевом продукте, а также низким уровнем потерь вещества. 7 табл.,2 ил.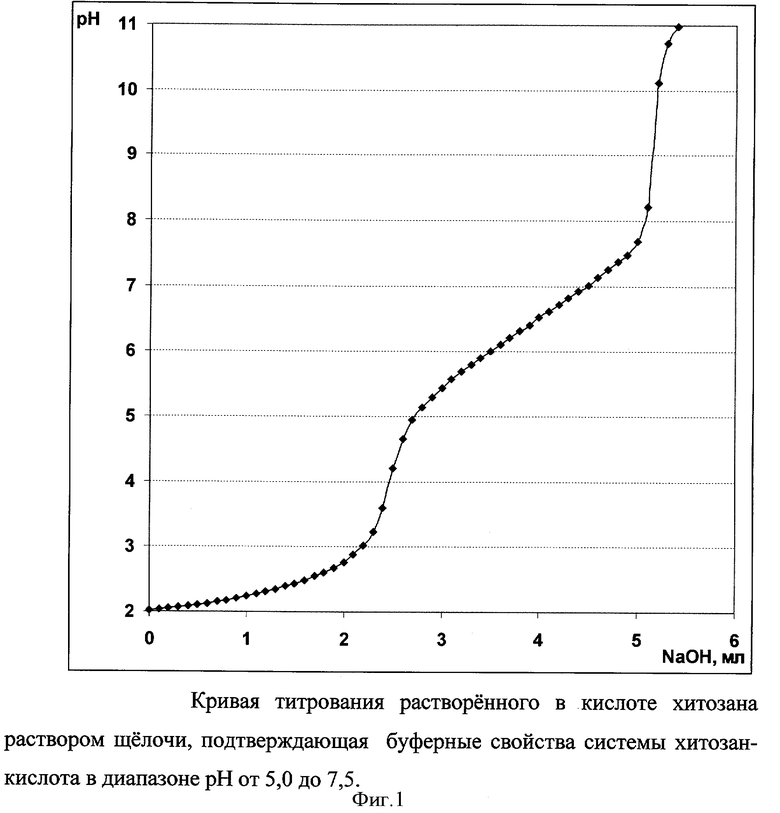
Способ получения низкомолекулярного хитозана с молекулярной массой от 2 до 20 кДа, включающий следующие стадии:
переосаждение исходного высокомолекулярного хитозана;
отмывка переосажденного хитозана с помощью крупнопористого фильтра;
растворение переосажденного хитозана в растворе кислоты до оптимального для ферментативной деполимеризации значения рН 5,5;
ферментативная деполимеризация хитозана с использованием ферментного препарата Целловиридин Г20х.
| СПОСОБ ПОЛУЧЕНИЯ ОЛИГОСАХАРИДОВ ХИТОЗАНА | 2005 |
|
RU2289589C1 |
| НЕМЦЕВ С.В | |||
| и др | |||
| Получение низкомолекулярного водорастворимого хитозана | |||
| Биотехнология, 2001, №6, с.37-42 | |||
| ИЛЬИНА А.В | |||
| и др | |||
| Прибор для промывания газов | 1922 |
|
SU20A1 |
| Прикладная биохимия и микробиология, 2002, т | |||
| Способ сужения чугунных изделий | 1922 |
|
SU38A1 |
| НЕМЦЕВ С.В | |||
| и др. | |||
Авторы
Даты
2011-08-10—Публикация
2009-08-17—Подача