Настоящее изобретение относится к питательной или фармацевтической композиции, содержащей жировой компонент, белковый компонент и углеводный компонент, молочную сыворотку и казеин, а также к применению указанной композиции.
Кормление грудью оптимально для развития младенца и защиты его от инфекций. Однако не все младенцы могут получать грудное молоко. Поэтому продолжают преследовать цель создать детскую смесь, которая имитирует функции женского грудного молока. В дополнение к требуемому сходству составов детского питания и грудного молока также в частности желательно воспроизвести защитное действие грудного молока. Показано, например, что грудное молоко обладает защитным действием от инфекций и аллергических реакций.
В известных детских смесях соотношение казеина и молочной сыворотки приближается к этому соотношению в грудном молоке, насколько это возможно. Считается, что это соотношение определяет оптимальный рост младенца. Однако до сих пор существуют некоторые недостатки, связанные с использованием жвачных животных в качестве источника белка молочной сыворотки. Эти смеси с преобладанием сывороточного белка не предоставляют оптимальной защиты от инфекций. Применение таких детских смесей приводит к задержке развития кишечной флоры младенца по сравнению с младенцами, находящимися на грудном вскармливании, особенно в первые три-четыре недели жизни. Флора младенцев, получающих смеси с преобладанием сывороточного белка, содержит практически такие же бактериальные роды, как и флора младенцев, находящихся на грудном вскармливании, однако, количество полезных бактерий снижено у младенцев, получающих смеси с преобладанием сывороточного белка по сравнению с младенцами, находящимся на грудном вскармливании. Более того, флора младенцев, получающих смеси, содержащие в основном сывороточные белки, происходящие из коровьего молока, содержит повышенное количество патологических бактерий, таких как клостридии и энтеробактерии. Таким образом, вскармливание младенца смесью с преобладанием сывороточного белка приводит к формированию «субоптимальной кишечной флоры».
Поскольку младенцы в первые недели жизни имеют недоразвитую иммунную систему и недоразвитый кишечник, развитие субоптимальной кишечной флоры может привести к инфекции, диарее, аллергической реакции и воспалению. Главным образом младенцы в возрасте от 0 до 30 дней, получающие смесь, содержащую в основном сывороточный белок коровьего молока, подвержены этим рискам, поскольку их фекальная флора наиболее отличается от таковой младенцев, находящихся на грудном вскармливании.
Задача настоящего изобретения состоит в создании питательной или фармацевтической композиции, которая снижает риски, связанные с применением детского питания, в которой преобладает молочная сыворотка.
Эта задача решается композицией по п.1 формулы изобретения.
Композиция по изобретению характеризуется тем, что весовое соотношение казеина к сыворотке составляет от 1:1 до 1:2,4 и что эта композиция содержит:
а) по меньшей мере 3 г аргинина на 100 г белка;
б) по меньшей мере 10 вес.% линолевой кислоты (LA) от общего содержания жирных кислот;
в) по меньшей мере 1 вес.% альфа линолевой кислоты (ALA) от общего содержания жирных кислот;
г) по меньшей мере одну длинноцепочечную полиненасыщенную жирную кислоту (LCPUFA) в количестве, превышающем 0,1 вес.%, от общего содержания жирных кислот, причем указанная длинноцепочечная полиненасыщенная жирная кислота (LCPUFA) выбрана из группы, состоящей из докозагексаеновой кислоты (DHA), арахидоновой кислоты (ARA) и эйкозапентаеновой кислоты (EPA);
д) 5-25 вес.% по меньшей мере одной полиненасыщенной жирной кислоты от общего содержания жирных кислот; и
е) 2-12 г неусвояемых олигосахаридов, имеющих степень полимеризации от 2 до 100, на 100 г сухой массы композиции.
Настоящая композиция стимулирует созревание иммунной системы и развитие кишечника. Композиция по изобретению в частности подходит для профилактики и/или лечения у младенцев воспалительных заболеваний, таких как инфекция, диарея и аллергия. Настоящая композиция:
- стимулирует развитие «оптимальной кишечной флоры» (то есть флоры, подобной флоре, полученной при грудном кормлении);
- стимулирует развитие желудочно-кишечного тракта, таким образом предотвращая поступление таких аллергенов, как болезнетворные бактерии, токсины и пищевые аллергены, в общее кровообращение;
- стимулирует созревание иммунной системы, что приводит к лучшей защите в случае, если аллерген, патоген или токсин проникнет через кишечный барьер и/или попадет в общее кровообращение;
- и в тоже время обеспечивает оптимальное питание младенцу.
Считается, что физиологические процессы, лежащие в основе развития «кишечной флоры низкого риска», развития кишечника и созревания иммунной системы являются тесно взаимосвязанными и взаимозависимыми. Таким образом, детская смесь должна содержать все те ингредиенты в соответствующем соотношении, которые стимулируют развитие кишечника, созревание иммунной системы и развитие кишечной флоры низкого риска. Оптимальной комбинацией ингредиентов младенец лучше защищен от аллергенов. Настоящая композиция обеспечивает такую оптимальную комбинацию ингредиентов. В силу того, что ингредиенты часто действуют на различные механизмы, ингредиенты описываемой композиции действуют синергично, обеспечивая младенцу повышенную сопротивляемость и уменьшение случаев воспалительного заболевания, в частности аллергии.
Описываемая композиция содержит олигосахариды с низкой степенью полимеризации. Эти олигосахариды стимулируют формирование кишечной флоры с низким риском, в частности снижают число (потенциально) патологических кишечных бактерий, таких как клостридия, энтеробактерии и/или энтерококки, и стимулируют колонизацию бифидобактерий и лактобактерий. Бифидобактерии и лактобактерии стимулируют развитие кишечника, например, посредством стимуляции синтеза фукоолигосахаридов эпителиальными клетками кишечника. Наилучшая стимуляция достигается посредством введения смеси различных олигосахаридов, в частности смеси олигосахаридов, включающей в себя и нейтральные, и кислые олигосахариды. Эти олигосахариды также имеют «прямое» действие на иммунную систему посредством снижения Th2 ответа и увеличения Th1 ответа. Было обнаружено, что описываемую композицию, которая включает в себя олигосахариды, можно с успехом применять для восстановления нарушенного баланса ответов Th1/Th2 и для лечения заболеваний, которые связаны с наличием дисбаланса Th1/Th2, таких как аутоиммунная реакция и аллергическая реакция.
Тем не менее, даже при сочетании олигосахаридов с сывороточными белками, происходящих из источников, не являющихся человеком, младенцы, получающие такую композицию, подвержены повышенным рискам инфекционных заболеваний в течение первого месяца жизни. Таким образом, желательно дальнейшее улучшение развития иммунной системы и/или кишечника.
С удивлением было обнаружено, что LCPUFA фактически уменьшают эпителиальную трансклеточную проницаемость. В противоположность тому, что сообщалось Usami et al (Clinical Nutrition 2001, 20(4): 351-359), было обнаружено, что C18 и C20 полиненасыщенные жирные кислоты, в частности эйкозапентаеновая кислота (EPA; C20:5 n3), докозагексаеновая кислота (DHA; C22:56 n3) и арахидоновая кислота (AA; C20:4), способны эффективно снижать проницаемость плотного межклеточного соединения эпителия кишечника, таким образом, стимулируют развитие кишечника. Таким образом, описываемая композиция успешно содержит LCPUFA. Кроме того, незаменимые жирные кислоты линоленовая кислота (C18:2 n6) и альфа-линоленовая кислота (C18:3 n3) необходимы и для развития иммунной системы, и для развития кишечника. В еще одном чрезвычайно предпочтительном варианте, описываемая композиция также содержит гамма-линоленовую кислоту (GLA; C18:3 (n-6)). Вследствие этого, описываемая композиция содержит линоленовую кислоту и альфа-линоленовую кислоту.
Необязательно, но чрезвычайно предпочтительно, описываемая композиция также содержит нуклеотиды и/или нуклеозиды. Нуклеотиды стимулируют развитие кишечника, уменьшают число случаев диареи и стимулируют иммунную систему. Младенцы, получающие смеси, дополненные нуклеотидами, по сравнению с младенцами, получающих смеси без нуклеотидов, имеют возрастающие титры антител после воздействия антигеном и стимуляции антигеном активности клеток-киллеров. (Carver et al Acta Paediatrica, (1999) Vol. 88, No. Sup 430, p. 83-88).
Композиция по изобретению содержит белки молочной сыворотки, происходящие из источника, не являющегося человеком, длинноцепочечные полиненасыщенные жирные кислоты и олигосахариды.
Как было уже сказано выше, настоящее изобретение обеспечивает композицию, содержащую молочную сыворотку и казеин в весовом отношении казеина к сыворотке от 1:1 до 1:2,4 и по меньшей мере 3 г аргинина на 100 г белка.
Диапазон соотношения казеин/сыворотка от 1:1 до 1:2,4 охватывает все значения, лежащие внутри этого диапазона, и, следовательно, следующие значения соотношений казеина к сыворотке: 1:1, 1:1,1, 1:1,2, 1:1,3, 1:1,4, 1:1,5, 1:1,6, 1:1,7, 1:1,7, 1:1,9, 1:1,2, 1:1,3, 1:1,4, 1:1,5, 1:1,6, 1:1,7, 1:1,8, 1:1,9, 1:2,0, 1:2,1, 1:2,2, 1:2,3, и 1:2,4 в предпочтительном варианте осуществления соотношение казеин:сыворотка составляет 1:1,4-1,6, даже более предпочтительно около 1:1,5 (40:60).
Предпочтительно аргинин представлен в количестве от 3 до 8 г аргинина на 100 г белкового компонента. Это диапазон выявляет все значения и в частности все целые значения, лежащие в этом диапазоне, например 3, 4, 5, 6, 7 и 8 г. В данной композиции предпочтительно содержится 4-5 г аргинина на 100 г белка.
Представленные в композиции LCPUFA выбраны из группы, включающей в себя DHA, AA и EPA. Это означает, что в состав могут входить одна или две, или три указанные длинноцепочечные полиненасыщенные жирные кислоты.
Диапазон от 5 до 25 вес.%, установленный для полиненасыщенных жирных кислот, охватывает все значения, попадающие в этот диапазон.
Настоящая композиция не включает в себя композицию, имеющую в своем составе женское грудное молоко. Настоящий способ не включает в себя способ применения композиции, имеющей в своем составе женское грудное молоко. Таким образом, предпочтительно описываемый способ включает в себя применение композиции, имеющей в своем составе вещество, происходящее из источника, не являющегося человеком, предпочтительно волокнистые углеводы, жир и/или белок из источника, не являющегося человеком, предпочтительно растительного, животного, бактериального или синтетического происхождения. Предпочтительно все компоненты и составляющие, входящие в состав композиции по изобретению, получены из источников, не относящихся к человеческому роду.
Макронутриенты
Описываемую композицию можно успешно применять в качестве детского питания. Такая детская смесь предпочтительно содержит жировой компонент, белковый компонент и углеводный компонент и предпочтительно вводится в организм младенца в жидкой форме.
Предпочтительный вариант осуществления настоящего изобретения относится к композиции и в частности к детскому питанию, содержащему 30-60 en% липидов, 5-15 en% белка и 25-75 en% углеводов. Предпочтительно данная композиция содержит 5-15 en% белка, 30-60 en% жира и 25-65 en% углеводов. Более предпочтительно, настоящая композиция содержит 43-53 en% липидов, 7-11 en% белка и 43-53 en% углеводов (en% является сокращением от «энергетический процент» и показывает вклад каждого компонента в общую калорийность композиции).
Белковый компонент описываемого детского питания содержит казеин и сыворотку в указанном весовом отношении. Казеин и/или сыворотка предпочтительно получены из молока млекопитающего, не относящегося к человеческому роду. Для обеспечения оптимального питания младенца в данной композиции содержится аргинин в нормированном количестве. Термин «белок» или белковый компонент в данном контексте означает общий белок, полипептиды, пептиды и аминокислоты. Аргинин является незаменимым в настоящей композиции. Он снижает распространенность воспалительных состояний кишечника (Amin et al Journal of Pediatrics, (2002) Vol. 140, No. 4, p. 425-431). Более того, аргинин стимулирует иммунную систему и требуется для поддержания здоровой иммунной системы (Niever et al, Biomedicine & Pharmacotherapy, (2002) Vol. 56, No. 10, p. 471-482). И казеин, и сыворотка содержат аргинин, но в большинстве молочных источников (например, сыворотка и казеин коровьего молока) казеин и сыворотка обеспечивают недостаточное количество аргинина. Предпочтительно по меньшей мере часть аргинина добавлена в композицию в форме свободной аминокислоты, например, L-аргинина, или в форме ее соли или эфира, при этом свободная аминокислота предпочтительна. В описываемой композиции предпочтительно содержится между 75 и 500 мг аргинина в форме свободной аминокислоты на 100 г сухого детского питания, более предпочтительно между 150 и 400 мг аргинина в форме свободной аминокислоты на 100 г сухого детского питания.
Углеводы в описываемой композиции предпочтительно обеспечены в большей мере лактозой, то есть предпочтительно по меньшей мере 75 вес.% общих перевариваемых углеводов обеспечены лактозой, предпочтительно по меньшей мере 90 вес.%.
Белок с низким содержанием треонина
Детская смесь с преобладанием молочной сыворотки, полученная из источника белка, не относящегося к человеческому роду, по сравнению с грудным молоком обычно имеет высокое содержание биодоступного треонина. Женское молоко содержит относительно небольшие количества биодоступного треонина. Таким образом, в уровне техники обеспечены технологические приемы для уменьшения содержания треонина в смесях с преобладанием молочной сыворотки (например, см. EP 1048226, WO 01/11990 и EP 741522). Применение детского питания с преобладанием молочной сыворотки со сниженным содержанием треонина обеспечивает in vivo содержание треонина, сравнимое с таковым у младенцев, находящихся на грудном вскармливании. Описываемая композиция предпочтительно представляет собой композицию с низким содержанием треонина, то есть композицию, в которой содержится 2-6 г треонина на 100 г белка. Низкое содержание треонина, например, может быть достигнуто посредством использования продуктов из молочной сыворотки, полученных ультрафильтрацией или некоторых кислых сывороточных продуктов.
Содержание незаменимых жирных кислот
Описываемая композиция содержит по меньшей мере 10 вес.% линолевой кислоты (LA) от общего содержания жирных кислот, предпочтительно между 11 и 20 вес.%, более предпочтительно между 12 и 15 вес.%. Описываемая композиция содержит по меньшей мере 1 вес.% альфа линолевой кислоты (ALA) от общего содержания жирных кислот, предпочтительно между 1,5 и 4 вес.% ALA, даже более предпочтительно между 2 и 2,5 вес.%. Для уменьшения нагрузки на кишечник весовое соотношение LA/ALA предпочтительно между 2 и 10, предпочтительно между 5 и 7,5.
Описываемая композиция предпочтительно содержит между 0,05 и 5 вес.% гамма-линоленовой кислоты (GLA) от общего содержания жирных кислот, предпочтительно между 0,1 и 1 вес.%.
Содержание длинноцепочечных полиненасыщенных жирных кислот
Описываемая композиция содержит по меньшей мере одну длинноцепочечную полиненасыщенную жирную кислоту с 20 или 22 атомами углерода (LCPUFA) в количестве, превышающем 0,1 вес.%, от общего содержания жирных кислот, выбранную из группы, состоящей из докозагексаеновой кислоты (DHA), арахидоновой кислоты (AA) и эйкозапентаеновой кислоты (EPA). Предпочтительно данная композиция содержит DHA в количестве, превышающем 0,1 вес.%, от общего содержания жирных кислот, и AA в количестве, превышающем 0,1 вес.%, от общего содержания жирных кислот.
Предпочтительно по меньшей мере одна LCPUFA из этой группы включена в данную композицию в количестве между 0,15 и 1 вес.% от общего содержания жирных кислот. Предпочтительно по меньшей мере две из этих LCPUFA, представленных в количестве между 0,15 и 1 вес.% от общего содержания жирных кислот в данной композиции. Предпочтительно данная композиция содержит AA и DHA, даже более предпочтительно AA, DHA и EPA.
Содержание AA предпочтительно не превышает 5 вес.%, более предпочтительно не превышает 1 вес.%, более предпочтительно между 0,1 и 0,6 вес.% от общего содержания жирных кислот. В описываемую композицию успешно добавлены EPA и/или DHA для сохранения баланса действия АА, например, снижения потенциального провоспалительного действия метаболитов АА. Избыток метаболитов АА может вызвать воспаление. Таким образом, в данной композиции предпочтительно содержатся AA, EPA и/или DHA, где весовое соотношение AA/DHA предпочтительно составляет выше 0,25, предпочтительно выше 0,5, более предпочтительно выше 1. Соотношение AA/DHA предпочтительно ниже 25, предпочтительно ниже 10. Весовое соотношение AA/EPA предпочтительно между 1 и 100, более предпочтительно между 5 и 20. Весовое соотношение EPA/DHA предпочтительно 1 или ниже, более предпочтительно ниже 0,5.
В предпочтительном варианте осуществления, содержание LCPUFA не превышает 3 вес.% от общего содержания жирных кислот, так как это необходимо для имитации грудного молока как можно более близко. По этой же причине, описываемая композиция предпочтительно содержит менее 1 г омега-3 LCPUFA на 100 г жирных кислот, более предпочтительно между 0,1 и 0,75 г на 100 г жирных кислот. Содержание омега-6 LCPUFA предпочтительно не превышает 2 г на 100 г жирных кислот и составляет предпочтительно между 0,1 и 0,75 г на 100 г жирных кислот.
Данные LCPUFA и другие жирные кислоты могут быть обеспечены в виде свободных жирных кислот, в виде триглицеридов, в виде фосфолипидов или как смесь одной или нескольких из вышеперечисленных форм. Описываемая композиция успешно содержит по меньшей мере одну из кислот AA и DHA в фосфолипидной форме, так как это уменьшает распространенность воспалительных заболеваний кишечника. Описываемая композиция предпочтительно содержит между 0,1 и 5 мг AA из фосфолипида на грамм общего жира и между 0,1 и 5 мг DHA из фосфолипида на грамм общего жира. Предпочтительно AA и/или DHA по меньшей мере частично представлены в форме фосфатидилхолина (ФХ) и/или фосфатидилэтаноламина (ФЭ), например AA и/или DHA, содержащие ФЭ и/или ФХ.
Мононенасыщенная жирная кислота
Описываемая питательная смесь для обеспечения адекватного питания предпочтительно также содержит омега-9 (n-9) жирную кислоту (предпочтительно олеиновую кислоту, 18:1). Предпочтительно настоящая композиция обеспечивает по меньшей мере 15 вес.% n-9 жирной кислоты от общего содержания жирных кислот, более предпочтительно по меньшей мере 25 вес.%. Содержание n-9 жирных кислот предпочтительно составляет менее 80 вес.% от общего содержания жирных кислот. Для обеспечения адекватного питания в описываемой композиции предпочтительно весовое соотношение насыщенная жирная кислота/полиненасыщенная жирная кислота между 2 и 5. Предпочтительно весовое соотношение мононенасыщенная жирная кислота/насыщенная жирная кислота между 0,5 и 2.
Описываемая композиция предпочтительно содержит между 5 и 25 вес.% полиненасыщенных жирных кислот от общего содержания жирных кислот, предпочтительно между 10 и 20 вес.%.
Описываемая композиция далее может быть усовершенствована путем включения стеаридоновой кислоты (C18:4n3). Данная композиция предпочтительно содержит между 0,05 и 2 вес.% стеаридоновой кислоты от общего содержания жирных кислот, даже более предпочтительно между 0,1 и 1 вес.%.
Олигосахариды
Описываемая композиция содержит 2-12 г неусвояемых олигосахаридов со степенью полимеризации (DP) 2 и 100 на 100 г сухой массы композиции, предпочтительно между 3 и 8 гми, более предпочтительно между 5 и 7,5 гми. После преобразования порошка в жидкость и введения в организм младенца жидкой смеси эти количества неусвояемых олигосахаридов обеспечивают желательные эффекты, не вызывая кишечный дискомфорт. Подходящие неусвояемые олигосахариды не перевариваются или только частично перевариваются в кишечнике под воздействием кислот или пищеварительных ферментов, представленных в верхних отделах пищеварительного тракта человека (тонкий кишечник и желудок), но не подвергаются ферментации кишечной флорой человека. Эти олигосахариды - предпочтительно водорастворимые (растворимость, превышающая 1 г олигосахарида на 1 литр воды). Среднее значение DP данного олигосахарида предпочтительно меньше 40, даже более предпочтительно 20. Оптимально, описываемая композиция содержит между 2 и 12 г олигосахаридов со значением DP 2-60, более предпочтительно со значением DP 2-10 (то есть сумма масс тех нуклеотидов со значением DP 2, 3, 4, 5, 6, 7, 8, 9 и 10).
В соответствии с еще одним вариантом осуществления по меньшей мере один олигосахарид, входящий в состав описываемой композиции, выбран из группы, состоящей из инулина, фруктоолигосахаридов, неперевариваемых декстринов, галактоолигосахаридов (в том числе трансгалактоолигосахаридов), ксилоолигосахаридов, арабиноолигосахаридов, глюкоолигосахаридов манноолигосахаридов, лакто-N-неотетраозы, фукоолигосахаридов (содержащих по меньшей мере одну фукозную сахаридную единицу), кислых олигосахаридов (см. ниже, например, олигосахариды уроновой кислоты, такие как пектиновый гидролизат) и их смесей.
Предпочтительно описываемая композиция содержит по меньшей мере один компонент, выбранный из группы, состоящей из инулинов и фруктоолигосахаридов, и по меньшей мере один компонент, выбранный из группы, состоящей из галактоолигосахаридов (в том числе трансгалактоолигосахаридов) и пектинового гидролизата. В очень предпочтительном варианте осуществления, настоящая композиция содержит 2-12 г олигосахаридов с DP от 2 до 10 и β-связанных сахаридов галактозы и глюкозы, более предпочтительно трансгалактоолигосахариды (то есть [gal]n-glu, где n равно от 2 до 10). В особенно предпочтительном варианте осуществления, описываемая композиция содержит трансгалактоолигосахариды (то есть [gal]n-glu, где n равно от 2 до 10), пектиновый гидролизат и по меньшей мере один из компонентов, выбранный из группы, состоящей из фруктоолигосахаридов и инулина. Предлагаемым олигосахаридом также может быть олигосахарид, полученный из молока животного, смесь олигосахаридов, полученная из молока животного, или фукозилированный олигосахарид (олигосахарид, содержащий по меньшей мере одну единицу фукозного сахарида).
Для дальнейшего улучшения развития кишки на всем протяжения кишечника, в описываемой композиции предпочтительно 10 вес.% олигосахаридов имеют DP от 2 до 5 (то есть 2, 3, 4 и/или 5), и по меньшей мере 5 вес.% имеют DP от 10 до 100. Предпочтительно по меньшей мере 50 вес.%, более предпочтительно по меньшей мере 75 вес.% олигосахаридов имеют DP от 2 до 10 (то есть 2, 3, 4, 5, 6, 7, 8, 9 и/или 10), потому, что считается, что они работают на всем протяжении подвздошной кишки и проксимальной и средней части толстой кишки, и потому что снижается весовой процент олигосахаридов, необходимых для введения в состав композиции для достижения желаемого эффекта.
Предпочтительные весовые соотношения:
(олигосахариды с DP 2-5):(олигосахариды с DP 6-9); и
(олигосахариды с DP 10- 100):(олигосахариды с DP 6-9).
И то, и другое больше 1.
Предпочтительно оба весовых соотношения больше 2, даже более предпочтительно больше 5.
Описываемая композиция предпочтительно содержит 0,5-10 г галактоолигосахаридов с DP между 2 и 10 на 100 г сухого веса композиции, более предпочтительно от 1 до 5 г. Предпочтительным галактоолигосахаридом является трансгалактоолигосахарид, так как он максимально соответствует олигосахаридам грудного молока. Настоящее изобретение предпочтительно включает в себя 0,5-10 г фруктополисахарида с DP между 10 и 60 на 100 г сухого веса композиции, более предпочтительно между 1 и 5 гми. Термин «фруктополисахарид» относится к углеводному полисахариду, содержащему по меньшей мере 10 β-связанных фруктозных единиц.
Кислые олигосахариды
Для дополнительного улучшения целостности барьера настоящая композиция содержит кислые олигосахариды с DP между 2 и 100, предпочтительно от 2 до 60. Термин кислые или кислотные олигосахариды относится к олигосахаридам, которые содержат по меньшей мере одну кислотную группу, выбранную из группы, состоящей из N-ацетилнейраминовой кислоты, N-гликолоилнейраминовой кислоты, свободной или этерифицированной карбоновой кислоты, сернокислой группы и фосфорнокислой группы. Кислый олигосахарид предпочтительно содержит единицы уроновой кислоты (а именно полимер уроновой кислоты), более предпочтительно единицы галактуроновой кислоты. Настоящая композиция предпочтительно содержит между 0,1 и 10 гми кислых олигосахаридов на 100 г сухого веса настоящей композиции, более предпочтительно между 1 и 6 гми на 100 г сухого веса.
Структура I: Полимерный кислый олигосахарид

где R предпочтительно выбран из группы, состоящей из водорода, гидрокси или кислотной группы, предпочтительно гидрокси; и
по меньшей мере один из радикалов группы, состоящей из R2, R3, R4 и R5, представляет N-ацетилнейраминовую кислоту, N-гликоилнейраминовую кислоту, свободную или этерифицированную карбоновую кислоту, сернокислую группу и фосфорнокислую группу, и оставшиеся R2, R3, R4 и R5 представляют гидрокси и/или водород. Предпочтительно один из радикалов группы, состоящей из R2, R3, R4 и R5, представляет N-ацетилнейраминовую кислоту, N-гликолоилнейраминовую кислоту, свободную или этерифицированную карбоновую кислоту, сернокислую группу или фосфорнокислую группу, и оставшиеся радикалы представляют гидрокси или водород. Еще более предпочтительно один из радикалов группы, состоящей из R2, R3, R4 и R5, представляет свободную или этерифицированную карбоновую группу, а оставшиеся R2, R3, R4 и R5 представляют гидрокси и/или водород; и
n является целым числом и относится к числу гексозных единиц (также см. ниже Степень полимеризации), которые могут быть любой гексозной единицей. Соответственно, n является целым числом между 1-5000. Предпочтительно гексозная единица (единицы) представляет собой единицу уроновой кислоты.
Наиболее предпочтительно R1, R2 и R3 представляют гидрокси, R4 представляет водород, R5 представляет карбоновую кислоту, n является любым числом между 1 и 250, предпочтительно между 1 и 10, и гексозной единицей является галактуроновая кислота.
Обнаружение, измерение и анализ предпочтительных кислых олигосахаридов, используемых в способе по изобретению, описаны у заявителей ранее выданной патентной заявки, относящейся к кислым олигосахаридам, то есть международной патентной публикации WO 00/160378.
Предпочтительно кислый олигосахарид имеет одну, предпочтительно две концевые единицы уроновой кислоты, которые могут быть свободными или этерифицированными. Предпочтительно концевая единица уроновой кислоты выбрана из группы, состоящей из галактуроновой кислоты, глюкуроновой кислоты, гулуроновой кислоты, идуроновой кислоты, маннуроновой кислоты, рибуроновой кислоты и альтруроновой кислоты. Эти единицы могут быть свободными или этерифицированными. В еще более предпочтительном варианте осуществления, концевая гексозная единица имеет двойную связь, которая предпочтительно располагается между позициями C4 и C5 терминальной гексозной единицы. Предпочтительно одна из терминальных гексозных единиц содержит двойную связь. Терминальная гексоза (например, уроновая кислота) предпочтительно имеет структуру, соответствующую следующей структуре II.
Структура II: Предпочтительная терминальная гексозная кислотная группа
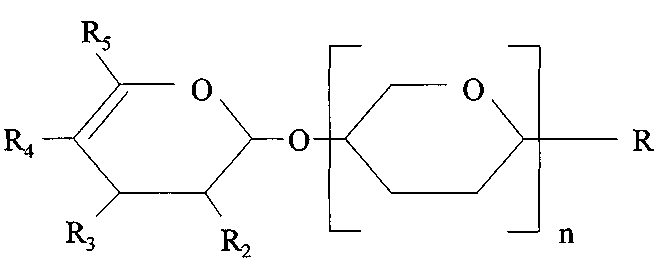
где R предпочтительно выбран из группы, состоящей из водорода, гидрокси или кислотной группы, предпочтительно гидрокси (см. выше); и
по меньшей мере один компонент из группы, состоящей из R2, R3, R4 и R5, представляет N-ацетилнейраминовую кислоту, N-гликолоилнейраминовую кислоту, свободную или этерифицированную карбоновую кислоту, сернокислую группу и фосфорнокислую группу, и оставшиеся R2, R3, R4 и R5 представляют гидрокси и/или водород. Предпочтительно один из радикалов группы, состоящей из R2, R3, R4 и R5, представляет N-ацетилнейраминовую кислоту, N-гликолоилнейраминовую кислоту, свободную или этерифицированную карбоновую кислоту, сернокислую группу и фосфорнокислую группу, и оставшиеся R2, R3, R4 и R5 представляют гидрокси и/или водород. Даже более предпочтительно один из радикалов группы, состоящей из R2, R3, R4 и R5, представляет свободную или этерифицированную карбоновую кислоту, а оставшиеся R2, R3, R4 и R5 представляют гидрокси и/или водород; и n является целым числом и означает число гексозных единиц (также см. ниже Степень полимеризации), которые могут быть любой гексозной единицей. Соответственно n является целым числом между 1-5000, означая число гексозных единиц, причем указанные гексозные единицы предпочтительно являются единицами уроновой кислоты, даже более предпочтительно являются единицами галактуроновой кислоты. Группы карбоновых кислот в этих единицах могут быть свободными или (частично) этерифицированными и предпочтительно, по меньшей мере частично, метилированными.
Наиболее предпочтительно, R2 и R3 представляют гидрокси, R4 представляет водород, и R5 представляет свободную или этерифицированную карбоновую кислоту.
Кислые олигосахариды, используемые в настоящем изобретении, предпочтительно получены из пектина, пектата, альгината, хондроитина, гиалуроновых кислот, гепарина, гепарана, бактериальных углеводов, сиалогликанов, фукоидана, фукоолигосахаридов или каррагенана, более предпочтительно из пектина и/или альгината. Предпочтительно используют пектиновый гидролизат.
Нуклеотиды
Настоящая композиция предпочтительно также содержит между 5 и 100 мг нуклеозидов и/или между 5 и 100 мг нуклеотидов на 100 г сухого веса данной композиции, более предпочтительно между 5 и 50 мг. Нуклеотиды и/или нуклеозиды дополнительно стимулируют иммунную систему, действуя синергично с другими ингредиентами описываемой композиции.
Цинк
Цинк является питательным микроэлементом, необходимым для роста и развития иммунной функции. Дефицит цинка ухудшает в целом иммунную функцию и устойчивость к инфекции. Поэтому описываемая композиция успешно содержит цинк, предпочтительно в количестве 2-100 мг цинка на 100 г сухого веса настоящей композиции, даже более предпочтительно по меньшей мере 4-25 мг цинка на 100 г сухого веса настоящей композиции. Масса цинка рассчитана как элементарный цинк.
Жидкий состав
Описываемая композиция предпочтительно находится в порошковой или жидкой форме, или таблетированной форме, где указанная таблетка имеет массу между 5 и 25 гми. Предпочтительно описываемая композиция обеспечена в порошкообразной форме, поскольку это увеличивает срок годности. Описываемую композицию предпочтительно применяют перорально в жидкой форме. Перед применением описываемой композиции ее предпочтительно смешивают с жидкостью, предпочтительно с водой. В виде жидкости композицию предпочтительно применяют, пока она имеет температуру 35-40°C (предпочтительно около 37°C), жидкий состав предпочтительно готовят следующим образом:
Способ a: смешивают воду с температурой ниже 30°C и композицию, в соответствии с любым из пунктов 1-10, с весовым соотношением вода:композиция 1-10:1; и подогревают смесь, полученную на этапе а), до температуры между 35 и 50°C; или
Способ б: смешивают воду с температурой ниже 60°C и композицию, в соответствии с любым из пунктов 1-10, с весовым соотношением вода:композиция 1-10:1; и охлаждают смесь, полученную на этапе а), до температуры между 35 и 40 °C. Способ a) более подходит для получения жидкой смеси из порошка, в то время как способ б) более подходит для получения жидкой смеси из таблетки.
Нерегулярность стула (например, твердый стул, недостаточный объем стула, диарея) является главной проблемой у многих младенцев и больных людей, которые получают жидкую пищу.
Было обнаружено, что проблемы со стулом можно уменьшить посредством применения описываемой композиции в жидкой форме, имеющей осмолярность между 50 и 500 мОсм/кг, более предпочтительно между 100 и 400 мОсм/кг, наиболее предпочтительно между 220 и 300 мОсм/кг.
В связи с вышеизложенной проблемой диареи, также важно то, что жидкая пища не имеет избыточной плотности калорий, поскольку это является причиной выраженного кишечного стресса. Однако данная смесь необходима для обеспечения достаточного количества калорий для питания младенца. Таким образом, жидкая пища предпочтительно имеет плотность калорий между 0,5 и 0,9 ккал/мл, предпочтительно между 0,6 и 0,8 ккал/мл.
Применение
Описываемая композиция успешно применяется у младенцев в возрасте от 0 до 2 лет. Описываемая композиция также успешно используется в способе обеспечения потребности в питательных веществах у недоношенных младенцев (младенцы, рожденные до 37 недели беременности). В предпочтительном варианте осуществления настоящее изобретение относится к способу вскармливания младенцев в возрасте от 0 до 30 дней.
Описываемую композицию можно успешно использовать для лечения или профилактики заболеваний, при которых причиной развития заболевания является недоразвитие иммунной системы и/или кишечного барьера. Описываемую композицию можно таким образом использовать для лечения или профилактики диареи или аллергической реакции, в частности у младенцев в возрасте от 0 до 2 лет. Описываемая композиция в частности пригодна для лечения и/или профилактики аллергического ринита, аллергического конъюнктивита, аллергического дерматита, атопического дерматита и/или пищевой аллергии.
Описываемая композиция предпочтительно предоставлена в виде расфасованного порошка или расфасованной готовой к употреблению смеси. Для предотвращения порчи продукта, размер упаковки готовой к употреблению смеси предпочтительно не превышает объема однократного применения, например, предпочтительно не превышает 500 мл; и размер упаковки описываемой композиции в форме порошка предпочтительно не превышает 250 приемов. Подходящий размер упаковки для порошковой формы составляет 2000 г или менее, предпочтительно 1000 г или менее.
Расфасованный продукт снабжен этикеткой, на которой потребителю ясно и недвусмысленно разъяснено применение указанного продукта в соответствии одним или несколькими выше или нижеуказанными назначениями, которые охватывает настоящее изобретение. Такие этикетки могут содержать, например, такие слова, как «стимулирует развитие кишечника и/или иммунной системы», «уменьшает аллергическую реакцию», «снижает стресс», «повышает сопротивляемость» или «уменьшает чувствительность» или подобные слова.
Таким образом, сущностью настоящего изобретения является применение композиции, как описано здесь, для производственного получения питательной смеси или лекарственного средства для применения у млекопитающего для лечения и/или профилактики воспалительного заболевания, диареи, экземы и/или атопического дерматита.
Кроме того, сущностью данного изобретения является использование описанной здесь композиции для производственного получения лекарственного средства для использования в способе лечения и/или профилактики воспалительного заболевания, диареи, экземы и/или атопического дерматита, указанный способ включает в себя применение указанной композиции энтерально или перорально у млекопитающих и в частности у младенцев. В предпочтительном варианте осуществления настоящий способ относится к способу лечения и/или профилактике инфекций, причем указанный способ включает в себя применение описываемой композиции.
Изобретение дополнительно иллюстрируется следующими примерами:
Пример 1: Детское питание
Жидкое детское питание, полученное посредством смешивания 13,9 г порошка с водой до получения 100 мл готового продукта, в 100 мл указанного жидкого продукта содержится:
Энергия - 66 ккал.
Белок - 8 en%.
1,3 г (включая 0,6 г казеина; 0,8 г сыворотки; 0,072 г L-аргинина)
Перевариваемые углеводы: 44 en%
7,4 г (включая 7,3 г лактозы)
Жир - 48 en%.
3,5 г (включая 0,41 г линолевой кислоты; 0,08 г α-линолевой кислоты; 0,012 г арахидоновой кислоты; 0,002 г эйкозапентаеновой кислоты; 0,006 г докозагексаеновой кислоты; 1,4 г олеиновой кислоты)
Волокна: 0,8 г (включая 0,05 г фруктополисахарида (Raftiline HP™, Orafti, Tienen, Belgium); 0,55 г трансгалактоолигосахаридов (Vivinal-GOS™ (Borculo Domo Ingredients, Netherlands); 0,20 г пектинового гидролизата, полученного как описано в EP 1373543, пример 1.
Нуклеотиды: 0,89 мг Цитидин-5-монофосфата;
0,55 мг Уридин-5-монофосфата;
0,82 мг Аденозин-5-монофосфата;
0,20 мг Гуанозин-5-монофосфата;
0,34 мг Инозин-5-монофосфата.
Осмолярность: 300 мосмоль/л
В композиции дополнительно содержатся холин (6 мг/100 мл) и таурин (6,3 мг/100 мл); минералы и микроэлементы (в том числе цинк 2мг/100 мл) и витамины в количествах, соответствующих международным стандартам для детской молочной смеси.
Пример 2:
Упакованная детская молочная смесь в соответствии с примером 1, где упаковка снабжена этикеткой с указанием того, что применение данной смеси подходит для предотвращения или лечения аллергической реакции.
Пример 3:
Экспериментальная модель
Действие рациона, включающего в себя кислые олигосахариды, при желании в сочетании с нейтральными олигосахаридами тестировали по реакции гиперчувствительности замедленного типа (ГЧЗТ), что является параметром Th1 иммунологического ответа и определяется посредством измерения увеличения отека уха после локальной антигенной стимуляции.
Используемые кислые олигосахариды (AcOl), со средним значением DP между 2 и 10, получали посредством способа, описанного в международной публикации WO 02/42484 (см. пример 1). Исследовали рационы, содержащие 1 вес.%, 2,5 вес.%, 5 вес.% и 10 вес.% AcOl от общего веса рациона. Использовали смесь нейтральных олигосахаридов (GF), содержащую галактоолигосахариды (GOS) (Vivinal-GOS™ (Borculo Domo Ingredients, Netherlands) и фруктоолигосахариды (FOS) (Raftiline HP™, Orafti, Tienen, Belgium), в весовом отношении GOS:FOS, равном 9:1. Изучали рационы, содержащие 1, 2,5 и 5 вес.% GF от общего веса рациона. Влияния комбинации кислых и нейтральных олигосахаридов (GF и AcOl) изучали с использованием рациона, содержащего 1 вес.% GF и 1 вес.% AcOl от общего веса рациона.
Все параметры представлены в процентах от контрольных значений, то есть относительные значения в группе, получавшей рацион, дополненный олигосахаридами, по сравнению с группой, получавшей контрольный рацион (без олигосахаридов).
Животные и рационы
Самок мышей C57BI/6 в возрасте 6 недель (Harlan Nederland BV, Horst, the Netherlands) размещали группами в условиях обычного 12-часового свето-темнового режима. Размер группы составлял 10 животных в группе и 3 животных в группе отрицательного контроля. Животные получали полусинтетические рационы (Research Diet Services, Wijk bij Duurstede, the Netherlands). Контрольные рационы были изготовлены в соответствии с AIN93G спецификациями (Reeves et al (1993) Development and Testing of the AIN93 purified diets for rodents: results on growth kidney calcification and bone mineralisation in rats and mice. J Nutrition 123(11): 1923-31), рационы с добавлением олигосахаридов основаны на этих спецификациях. Содержание углеводов в дополненных рационах сохраняли постоянным посредством замещения общих углеводов на олигосахариды в весовом отношении. Отдельные углеводные компоненты замещали, соответствуя их нормальному соотношению в рационе. Углеводы в нормальном рационе состоят из крахмала (40% от общего веса), кукурузного крахмала (13,2%), сахарозы (10%) и целлюлозы (5%).
Схема вакцинации
Вакцинации начинали после периода от двух до четырех недель после адаптации к новым жилищам и диетам. В день 0 собирали образцы крови до вакцинации. В день 1 проводили первую вакцинацию, подкожно. Через три недели собирали образцы крови (день 21) и проводили бустер-вакцинацию (день 22). Через девять дней после бустер-инъекции (день 31) измеряли толщину основания уха, используя микрометр для измерения наружных размеров Digimatic (Mitutoyo, Veenendaal, the Netherlands), и реакцию гиперчувствительности замедленного типа (ГЧЗТ) индуцировали посредством инъекции в ушную раковину мыши раствора антигена в/к (внутрикожно). Через 24 часа после этого момента (день 32) определяли реакцию ГЧЗТ, брали образец крови и мышей умерщвляли. Селезенки изолировали и подготавливали для повторной стимуляции ex-vivo.
Вакцины состояли из 100 мкл п/к (подкожно) инъекции смеси 1:1 раствора антигена и адъюванта Stimune (Specol, Cedi-diagnostics BV, Lelystad, the Netherlands). Раствор антигена представлял собой разведение 1:100 вакцины Инфлувак 2002/2003 (Solvay Pharmaceuticals, Weesp, the Netherlands) в PBS. Инфлувак является трехвалентной белковой вакциной, содержащей 3х30 мкг/мл гемагглютинина трех различных штаммов гриппа.
Для определения реакций ГЧЗТ мышам в оба уха подкожно вводили в качестве стимула ГЧЗТ 25 мкл диализированной вакцины Инфлувак.
Клеточные культуры
Спленоциты выделяли из селезенок, используя мелкоячеистые сита (Becton Dickinson, Erembodegem, Belgium). Эритроциты лизировали посредством инкубирования в течение 5 минут на льду. После отмывки культуральной средой, не содержащей фенолового красного, подсчитывали клетки (Coulter Counter, Beckman Coulter, the Netherlands) и хранили замороженными. Для стимуляции культуры обрабатывали 0,1 мкг/мл диализированной вакциной Инфлувак. Клетки высевали в 96-луночные планшеты в разведении 1·106 клеток на лунку. Культуральная среда состояла из RPMI-1640 с буфером HEPES и 2 мМ L-глутамина (Invitrogen, Merelbeke, Belgium) с 10% фетальной телячьей сывороткой (FCS). Культуры инкубировали в течение 5 дней при 37°C и 5% CO2. Затем собирали надосадочные жидкости и замораживали при -80°C до проведения анализа. Клеточную пролиферацию измеряли в параллельных культурах по включению 3H-тимидина, который был добавлен к культурам в последние 18 часов в концентрации 0,4 мкКи/лунку. Через 5 дней, используя харвестер Filtermate (Perkin Elmer, Zaventem, Belgium), клетки собирали и подсчитывали счетчиком клеток Micro-Beta (Perkin Elmer, Zaventem, Belgium). Радиоактивный распад измеряли в течение 1 минуты на лунку, и число импульсов в минуту (cpm) регистрировали как меру скорости пролиферации.
Цитокины исследовали в надосадочных жидкостях культур, стимулированных Инфлуваком. IL-2, IL-5, IL-10 и IFN-гамма исследовали на системе Bio-Plex, используя специальным образом смешанные гранулы для упомянутых цитокинов (Bio-Rad, Veenendaal, the Netherlands). Цитокины исследовали в соответствии с инструкциями фирмы-производителя. IL-4 измеряли посредством ИФА, используя набор Pharmingen OptEIA mouse IL-4 (Becton Dickinson, Erembodegem, Belgium), в соответствии с инструкциями фирмы-производителя.
Результаты
Реакция ГЧЗТ на кислые олигосахариды
Рационы, содержащие AcOl в дозировке 1 вес.%, 2,5 вес.% и 5 вес.%, индуцировали статистически значимое повышение реакции ГЧЗТ, демонстрируя дозозависимое повышение (см. Таблицу 1). Наблюдаемое действие характеризует успешное применение кислых олигосахаридов в способе по изобретению.
Реакция ГЧЗТ на кислые и нейтральные олигосахариды
Сочетание 1 вес.% GF, 2,5 вес.% GF и смесь 1 вес.% GF 1 вес.% AcOl вызывает статистически значимое повышение реакции ГЧЗТ (см. Таблицу 2). Наблюдаемое действие характеризует успешное применение неусвояемых олигосахаридов, в частности комбинации кислых и нейтральных олигосахаридов, в способе по изобретению.
Инфлувак-специфическая пролиферация кислых олигосахаридов
Применение рационов, содержащих 2,5 вес.% и 5 вес.% кислых олигосахаридов (AcOl), индуцирует значительное снижение действия на Инфлувак-специфическую пролиферацию ex vivo (см. Таблицу 3). Наблюдаемое действие характеризует успешное применение кислых олигосахаридов в способе по изобретению.
Инфлувак-специфическая пролиферация смеси кислых и нейтральных олигосахаридов
Применение комбинации 1 вес.% GF и 1 вес.% AcOl индуцирует значительное уменьшение эффектов на антиген-специфическую пролиферацию (см. Таблицу 3). Поскольку эффект на реакции ГЧЗТ значительно улучшается при применении рационов, содержащих только кислые или нейтральные олигосахариды, эти результаты характеризуют синергетическое действие, обеспеченное применением кислых и нейтральных олигосахаридов. Наблюдаемое действие характеризует успешное применение комбинации кислых и нейтральных олигосахаридов в способе по изобретению. Сниженная пролиферация является характерной для уменьшения Th2 ответа, уравновешивания действия Th1/Th2, при использовании настоящего способа.
Th1/Th2 баланс: цитокиновые профили после применения кислых олигосахаридов
Цитокиновые профили измеряли в надосадочных жидкостях культур инфлувак-специфических спленоцитов. Результаты представлены в процентах по сравнению со значениями вакцинированной контрольной группы (а именно не получающей олигосахариды). По сравнению с контрольными, применение рационов, содержащих 2,5 вес.% и 5 вес.% AcOl, приводило к уменьшению Th2-связанных цитокинов IL-4, IL-5 и IL-10, в то время как Th1-связанный цитокин IL-2 был повышен, и IFN-γ не был значительно снижен (см. Таблицу 4). Эти результаты являются характерными для Th1/Th2 уравновешивающего действия кислых олигосахаридов и характерными для успешного применения кислых олигосахаридов в способе по изобретению, например, при лечении и/или профилактике заболеваний, для которых характерен относительно низкий Th1 иммунитет.
Th1/Th2 баланс: цитокиновые профили после применения кислых и нейтральных олигосахаридов
По сравнению с контрольными, применение комбинации 1 вес.% GT и 1 вес.% AcOl приводило к повышению Th2-связанных цитокинов IL-4, IL-5 и IL-10, в то время как Th1-связанные цитокины IL-2 и IFN-γ не были снижены (см. Таблицу 4, где данные представлены в процентах по сравнению со значениями в вакцинированной контрольной группе (то есть не получающей олигосахариды)). Эти результаты являются характерными для Th1/Th2 уравновешивающего действия комбинации кислых и нейтральных олигосахаридов и характеризуют успешное применение кислых олигосахаридов в способе по изобретению, например, при лечении и/или профилактике заболеваний, для которых характерен относительно низкий Th1 иммунитет. В частности соотношение IL-4/IFN отображает баланс Th2/Th1. Другими словами, сниженное соотношение характеризует стимуляцию Th1 и/или ингибирование Th2, и в любом случае характеризует Th1-Th2 уравновешивающее действие описываемых олигосахаридов.
IL4/IFN-γ
| название | год | авторы | номер документа |
|---|---|---|---|
| ИММУНОМОДУЛИРУЮЩИЕ ОЛИГОСАХАРИДЫ | 2004 |
|
RU2388478C2 |
| СВОБОДНОЕ ОТ БЕЛКА ДЕТСКОЕ ПИТАНИЕ | 2007 |
|
RU2441399C2 |
| ПИЩЕВЫЕ КОМПОЗИЦИИ, СОДЕРЖАЩИЕ ПУНИКАЛАГИНЫ | 2009 |
|
RU2542497C2 |
| СПОСОБ ДЛЯ СНИЖЕНИЯ РАСПРОСТРАНЕНИЯ ИНФЕКЦИИ У ДЕТЕЙ МЛАДШЕГО ВОЗРАСТА | 2012 |
|
RU2605198C2 |
| УЛУЧШЕНИЕ ЦЕЛОСТНОСТИ ИНТЕСТИНАЛЬНОГО БАРЬЕРА | 2004 |
|
RU2402240C2 |
| ПРИМЕНЕНИЕ ПИТАТЕЛЬНЫХ КОМПОЗИЦИЙ ДЛЯ ПРЕДУПРЕЖДЕНИЯ ЗАБОЛЕВАНИЙ | 2007 |
|
RU2444912C2 |
| ПИТАТЕЛЬНЫЕ КОМПОЗИЦИИ | 2011 |
|
RU2541396C2 |
| ПИТАТЕЛЬНАЯ КОМПОЗИЦИЯ ДЛЯ СОДЕЙСТВИЯ ЗДОРОВОМУ РАЗВИТИЮ И РОСТУ | 2009 |
|
RU2508121C2 |
| ПИТАТЕЛЬНЫЕ КОМПОЗИЦИИ ДЛЯ МЛАДЕНЦЕВ, ПРЕДНАЗНАЧЕННЫЕ ДЛЯ ПРЕДУПРЕЖДЕНИЯ ОЖИРЕНИЯ | 2006 |
|
RU2444210C2 |
| МОЛОЧНАЯ СМЕСЬ ДЛЯ ГРУДНЫХ ДЕТЕЙ | 2006 |
|
RU2405351C2 |
Питательная и фармацевтическая композиции в виде детского питания содержат жировой, белковый и углеводный компонент и включают в себя молочную сыворотку и казеин при весовом соотношении казеина к сыворотке от 1:1 до 1:2,4. Они содержат по меньшей мере: 3 г аргинина на 100 г белка, от общего содержания жирных кислот: 10 вес.% линолевой кислоты, 1 вес.% альфа-линолевой кислоты, одну длинноцепочечную полиненасыщенную жирную кислоту, выбранную из группы, состоящей из докозагексаеновой, арахидоновой и эйкозапентаеновой кислот, до 25 вес.% по меньшей мере одной полиненасыщенной жирной кислоты и 2-12 г неусвояемых олигосахаридов, имеющих степень полимеризации от 2 до 100 на 100 г сухого веса данной композиции, а также нейтральные и кислые олигосахариды, содержащие единицы уроновой кислоты. Фармацевтическую композицию применяют при лечении и/или профилактике воспалительного заболевания, диареи, экземы и/или атопического дерматита. Предотвращение аллергии или диареи осуществляют введением ребенку композиции энтерально или перорально. Изобретение обеспечивает стимулирование созревания иммунной системы и развитие у младенцев кишечника и кишечной флоры, подобной флоре, полученной при грудном вскармливании, оптимальное питание, предотвращает поступление в общее кровообращение аллергенов и снижает риски, связанные с вскармливанием детской смесью на основе молочной сыворотки. 3 н. и
14 з.п. ф-лы, 4 табл.
1. Питательная композиция в виде детского питания, содержащая жировой компонент, белковый компонент и углеводный компонент и включающая молочную сыворотку и казеин, отличающаяся тем, что весовое соотношение казеина к молочной сыворотке составляет от 1:1 до 1:2,4, при этом композиция содержит:
a) по меньшей мере 3 г аргинина на 100 г белка;
b) полиненасыщенные жирные кислоты, включающие:
по меньшей мере 10 вес.% линолевой кислоты от общего содержания жирных кислот;
по меньшей мере 1 вес.% альфа-линолевой кислоты от общего содержания жирных кислот; и
по меньшей мере одну длинноцепочечную полиненасыщенную жирную кислоту, выбранную из группы, состоящей из докозагексаеновой кислоты, арахидоновой кислоты и эйкозапентаеновой кислоты, в количестве, превышающем 0,1 вес.%, от общего содержания жирных кислот, причем содержание полиненасыщенных жирных кислот составляет до 25 вес.% от общего содержания жирных кислот;
с) 2-12 г неусвояемых олигосахаридов, имеющих степень полимеризации от 2 до 100 на 100 г сухого веса данной композиции и включающих нейтральные и кислые олигосахариды, причем кислые олигосахариды содержат единицы уроновой кислоты.
2. Композиция по п.1, отличающаяся тем, что содержит трансгалактоолигосахариды, пектиновый гидролизат и по меньшей мере один компонент, выбранный из группы, состоящей из фруктоолигосахарида и инулина.
3. Композиция по п.1, отличающаяся тем, что содержит 2-100 мг цинка на 100 г сухого веса данной композиции.
4. Композиция по любому из пп.1-3, отличающаяся тем, что белковый компонент составляет 5-15 эн.% ("энергетических процентов"), жировой компонент составляет 30-60 эн.%, а углеводный компонент составляет 25-75 эн.%.
5. Композиция по любому из пп.1-3, отличающаяся тем, что она дополнительно содержит между 5 и 100 мг нуклеотидов и/или между 5 и 100 мг нуклеозидов на 100 г сухого веса данной композиции.
6. Композиция по любому из пп.1-3, отличающаяся тем, что содержит 2-6 г треонина на 100 г белкового компонента.
7. Композиция по любому из пп.1-3, отличающаяся тем, что содержит докозагексаеновую кислоту в количестве, превышающем 0,1 вес.% от общего содержания жирных кислот, и арахидоновую кислоту в количестве, превышающем 0,1 вес.% от общего содержания жирных кислот, и тем, что весовое соотношение арахидоновая кислота/докозагексаеновая кислота составляет от 0,25 до 25.
8. Фармацевтическая композиция в виде детского питания, применяемого при лечении и/или профилактике воспалительного заболевания, диареи, экземы и/или атопического дерматита, содержащая жировой компонент, белковый компонент и углеводный компонент и включающая молочную сыворотку и казеин, отличающаяся тем, что весовое соотношение казеина к молочной сыворотке составляет от 1:1 до 1:2,4, при этом композиция содержит:
a) по меньшей мере 3 г аргинина на 100 г белка;
b) полиненасыщенные жирные кислоты, включающие:
по меньшей мере 10 вес.% линолевой кислоты от общего содержания жирных кислот;
по меньшей мере 1 вес.% альфа-линолевой кислоты от общего содержания жирных кислот; и
по меньшей мере одну длинноцепочечную полиненасыщенную жирную кислоту, выбранную из группы, состоящей из докозагексаеновой кислоты, арахидоновой кислоты и эйкозапентаеновой кислоты, в количестве, превышающем 0,1 вес.%, от общего содержания жирных кислот, причем содержание полиненасыщенных жирных кислот составляет до 25 вес.% от общего содержания жирных кислот;
c) 2-12 г неусвояемых олигосахаридов, имеющих степень полимеризации от 2 до 100 на 100 г сухого веса данной композиции, и включающих нейтральные и кислые олигосахариды, причем кислые олигосахариды содержат единицы уроновой кислоты.
9. Композиция по п.8, отличающаяся тем, что содержит трансгалактоолигосахариды, пектиновый гидролизат и по меньшей мере один компонент, выбранный из группы, состоящей из фруктоолигосахарида и инулина.
10. Композиция по п.8, отличающаяся тем, что содержит 2-100 мг цинка на 100 г сухого веса данной композиции.
11. Композиция по любому из пп.8-10, отличающаяся тем, что белковый компонент составляет 5-15 эн.% ("энергетических процентов"), жировой компонент составляет 30-60 эн.%, а углеводный компонент составляет 25-75 эн.%.
12. Композиция по любому из пп.8-10, отличающаяся тем, что она дополнительно содержит между 5 и 100 мг нуклеотидов и/или между 5 и 100 мг нуклеозидов на 100 г сухого веса данной композиции.
13. Композиция по любому из пп.8-10, отличающаяся тем, что содержит 2-6 г треонина на 100 г белкового компонента.
14. Композиция по любому из пп.8-10, отличающаяся тем, что содержит докозагексаеновую кислоту в количестве, превышающем 0,1 вес.% от общего содержания жирных кислот, и арахидоновую кислоту в количестве, превышающем 0,1 вес.% от общего содержания жирных кислот, и тем, что весовое соотношение арахидоновая кислота/докозагексаеновая кислота составляет от 0,25 до 25.
15. Способ предотвращения аллергии или диареи у млекопитающего, предусматривающий введение млекопитающему композиции по любому предшествующему пункту.
16. Способ по п.15, в котором указанную композицию вводят энтерально или перорально.
17. Способ по п.15 или 16, в котором указанным млекопитающим является ребенок.
| ЕР 0756828, 05.02.1997 | |||
| RU 93052410 А, 27.10.1997 | |||
| US 6245379 А, 12.06.2001 | |||
| US 5792501 А, 11.08.1998 | |||
| RU 2001109592 A, 27.09.2002. |
Авторы
Даты
2011-08-20—Публикация
2005-08-19—Подача