Изобретение относится к медицине, в частности к методам нейровизуализации, применяемым для изучения зон активации головного мозга, ответственных за ходьбу, как в экспериментальной, так и в восстановительной медицине.
Известен способ нейровизуализации зон активации головного мозга, ответственных за ходьбу, при позитронно-эмиссионной томографии (ПЭТ) у здоровых лиц [Ishii et al., 1995 (1)]. При данной методике испытуемые шагают на беговой дорожке в течение 10 минут с постоянной скоростью (в среднем 1,1 м/с), затем им внутривенно болюсно вводится фтордиоксиглюкоза (18F-FDG) (125±6 МБк), и испытуемые продолжают шагать еще в течение 10 минут. Через 30 минут после введения меченого вещества начинается само сканирование в условиях ПЭТ. Однако к недостаткам этой методики следует отнести необходимость внутривенного введения радионуклидного препарата, длительность сканирования, невозможность использования методики у больных с выраженным нарушением ходьбы, высокую стоимость исследования.
Другим более доступным методом нейровизуализации является функциональная магнитно-резонансная томография (фМРТ), позволяющая косвенно оценить функциональную активность нейронов в ответ на их активацию. При выполнении определенных заданий (активное или пассивное движение, решение задач, чтение и проч.) происходит активация групп нейронов, ответственных за выполнение этих заданий, что приводит к локальному усилению кровотока и изменению соотношения окси- и дезоксигемоглобина крови, что, в свою очередь, ведет к повышению МР-сигнала от этих участков, выявляемому при МРТ-сканировании (фМРТ). В конечном счете это позволяет изучать роль корково-подкорковых зон в контроле различных функций (движение, речь, мышление и др.), однако изучение корковых механизмов контроля ходьбы при фМРТ представляет определенные трудности, связанные с выбором метода стимуляции двигательных зон.
Известен способ нейровизуализации зон активации головного мозга, ответственных за ходьбу, при фМРТ у здоровых лиц с использованием специального устройства, представляющего собой аналог велосипедной рамы с педалями [Mehta JP. et al., 2009 (2)]. При данной методике испытуемые, лежа в МР-томографе, по команде начинают крутить педали со скоростью 30 вращений в минуту в течение 30 с, после чего следует период покоя. Данное чередование повторяется 4 раза. Однако к недостаткам данной методики следует отнести выраженные артефакты от движения ног при сканировании, что приводит к невозможности обработки данных периода активации, и исследователи оценивают зоны деактивации в период покоя. Кроме того, следует отметить, что подобное задание не отражает физиологический акт ходьбы.
Наиболее близким к заявляемому способу является способ нейровизуализации зон активации головного мозга, ответственных за ходьбу, с использованием функциональной МРТ (фМРТ), в которой в качестве метода стимуляции зон активации головного мозга, ответственных за ходьбу (парадигмы), используется «Воображение ходьбы [Jahn et al., 2008 (3)]. Испытуемому после предварительной тренировки, которая проводится до начала исследования, предлагается вообразить различные состояния, такие как лежание, стояние, ходьбу или бег в течение равных промежутков времени в условиях сканирования в МР-томографе по звуковой команде;
данные состояния повторяются по 14 раз для сбора достаточного количества данных. Вместе с тем применение этой парадигмы для оценки корковых механизмов контроля ходьбы у больных имеет ограничения, связанные прежде всего с тем, процесс воображения возможен только при сохранении высших психических функций и прежде всего функции внимания. Поэтому, хотя данная парадигма применима и к больным с тяжелой степенью двигательного дефицита, к ее ограничениям относится необходимость сохранности высших психических функций. Вторым важным недостатком данной парадигмы является то, что процесс воображения невозможно верифицировать.
Задачей изобретения является проведение нейровизуализации зон активации головного мозга, ответственных за ходьбу, с помощью фМРТ при любом состоянии больного.
Данная задача решается путем применения стимуляции зон головного мозга, ответственных за ходьбу (парадигмы), связанной с использованием подошвенного имитатора опорной нагрузки.
Способ осуществляли следующим образом.
Для исследования процесса локомоции авторами, в частности, применялась парадигма, включающая две блоковые парадигмы: имитация опоры на нижние конечности и имитация ходьбы. Стимуляция создавалась при помощи закрепленного на ступнях пациента подошвенного имитатора опорной нагрузки.
До настоящего времени данный аппарат (4, 5, 6) использовался только в терапевтических целях для лечения больных с вынужденной длительной гипокинезией. Применение башмака во время проведения фМРТ заключается в следующем: на каждую ногу пациента, лежащего на столе в МРТ камере, крепятся ортезы (ботинки), содержащие пневмостельки, снабженные пневмокамерами. К каждой пневмостельке подключается пневмопровод, приемный конец которого подключается к блоку управления, вынесенного за пределы камеры МРТ. Имитатор работает по принципу создания пневмомеханического давления на соответствующие опорные зоны стопы с помощью пневмокамер. Во время проведения стимуляции опорных зон стопы голова больного не двигается, что позволяет избежать артефактов во время фМРТ. Кроме того, как нами было установлено в результате исследования, имитатор позволяет моделировать сенсорный образ ходьбы в режиме физиологического потенцирования рефлекторных механизмов шага и активации спинального генератора локомоции и моторных центров более высокого уровня.
Во время имитации опоры на нижние конечности в обе камеры синхронно подавался воздух с постоянным давлением (20 кПа), во время имитации ходьбы подача воздуха с аналогичным давлением осуществлялась попеременно с постоянной частотой. В каждом исследовании блоки покоя чередовались с блоками активации, общим числом 6: 3 блока покоя и 3 блока активации одинаковой продолжительности, по 38 с. Во время периода покоя любая стимуляция испытуемого отсутствовала.
Сканирование проводилось на МР-томографе 1.5 Т Siemens Avanto. Для оценки вещества головного мозга на предмет отсутствия его поражения проводилось исследование в режиме Т2-турбо спин-эхо. Также использовалось приложение BLADE - позволяющее компенсировать непроизвольные движения ногами, в частности у неврологических больных. Исследование проводилось в аксиальной проекции: время повторения (TR) - 4000 мс, время эхо (ТЕ) - 106 мс, поле обзора (FoV) - 230 мм, толщина среза - 5 мм, всего 20 срезов. Также во время каждой сессии был получен трехмерный объем Т 1-структурных срезов высокого разрешения в сагиттальной проекции: время повторения (TR) - 1940 мс, время эхо (ТЕ) - 3.08 мс, поле обзора (FoV) - 250 мм, толщина среза - 1 мм, матрица - 256×256, всего 176 срезов, покрывающих весь объем вещества головного мозга. Функциональные Т2-ВИ изображения для каждой из парадигм были получены при помощи эхопланарной последовательности: время повторения (TR) - 3800 мс, время эхо (ТЕ) - 50 мс, поле обзора (FoV) - 192 мм, угол отклонения - 90 град, матрица - 64×64, толщина среза - 3 мм, всего 36 срезов для каждого из функциональных объемов, общее число последних - 60 в аксиальной проекции.
Во время каждого блока были получены 10 функциональных объемов всего вещества головного мозга. Общая продолжительность каждой парадигмы составила 3 мин 53 сек, за которые было получено всего 60 функциональных срезов головного мозга.
Обработка изображений и статистический анализ осуществлялся на основании стандартных протоколов (см. например 7). Полученные данные были обработаны при помощи пакета статистической обработки SPM5 (Welcome Department of Cognitive Neurology, London, http://www.fil.ion.ucl.ac.uk/spm) в программе MATLAB 6.1 (Mathworks Inc., Natiek, MA, USA). Для каждой парадигмы полученные функциональные данные выравнивались по первому объемному изображению первой серии с последующим созданием среднего изображения и корегистрацией с анатомическими данными. После корегистрации структурные изображения пространственно нормализовывались по соответствующему шаблону головного мозга (Montreal Neurological Institute, MNI) при помощи аффинной нелинейной трансформации. Затем функциональные изображения подвергались повторной выборке с размером воксела 3×3×3 мм и сглаживанию при помощи гауссова кернеля в 10 мм (FWHM). Статистический анализ проводился для каждого пациента в отдельности в рамках общей линейной модели - General Linear Model, а также для всей группы пациентов.
Пример осуществления способа.
Обследована группа здоровых лиц (15 человек), в возрасте от 22 до 65 лет (10 мужчин и 5 женщин) и группа больных (10 человек) с постинсультными гемипарезами, в возрасте от 35 до 67 лет (6 мужчин и 4 женщины). Всем больным проводили фМРТ одновременно с вышеуказанной парадигмой при помощи подошвенного имитатора опорной нагрузки.
Результаты, полученные у здоровых лиц и у больных, приведены в таблицах №1 и 2 и фиг.1 и 2.
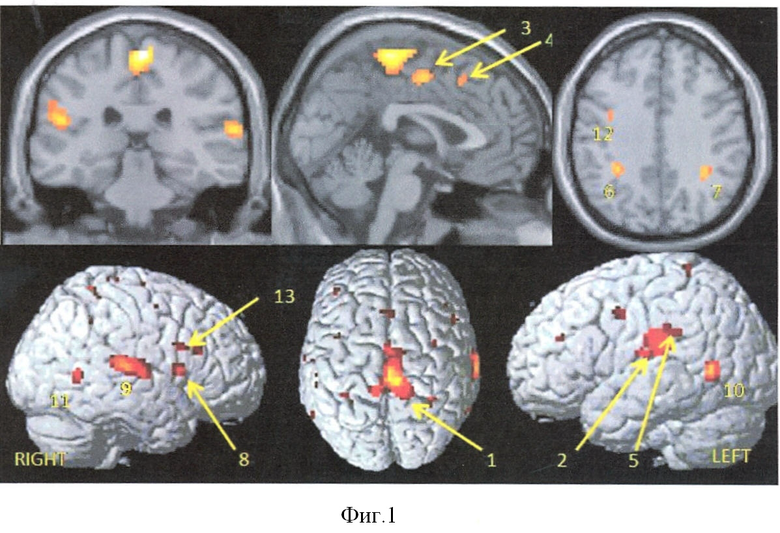
Как видно из фиг.1, зоны активации у здоровых лиц при выполнении фМРТ с предложенной парадигмой при помощи имитатора подошвенной опоры включают (FWE, р<0,05): 1 - парацентральная долька, 2 - постцентральная извилина, L, 3 - медиальная лобная извилина, зона SMA, 4 - поясная извилина, L, 5,6 - нижняя париетальная долька, L, 7 - нижняя париетальная долька, R, 8 - прецентральная извилина, R (front. inf. operc.), 9 - верхняя височная извилина, R, 10 - средняя височная извилина, L, 11 - средняя височная извилина, R, 12 - средняя лобная извилина, L, 13 - нижняя лобная извилина, R.
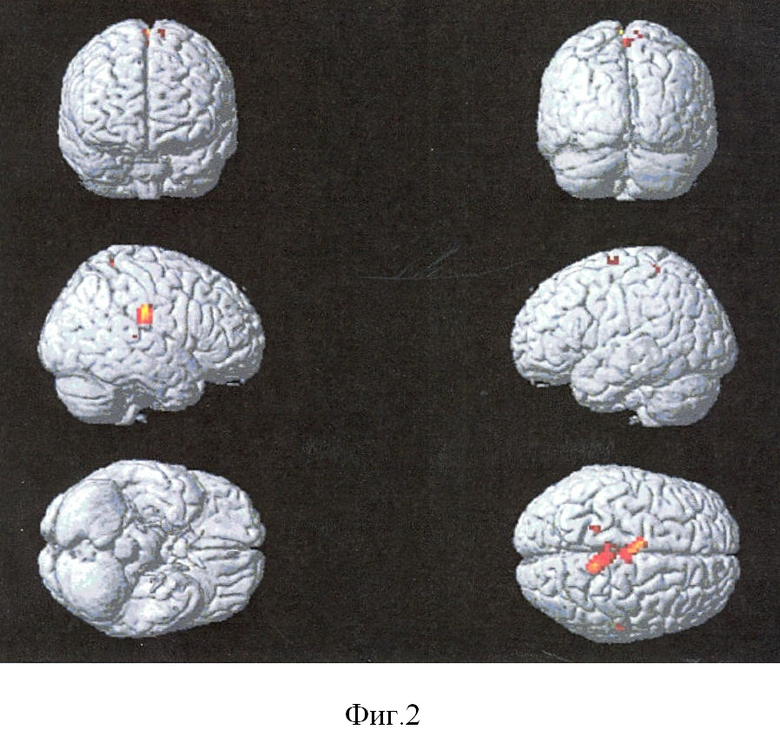
На фиг.2 также видны зоны активации у больных с постинсультными гемипарезами при выполнении фМРТ с предложенной парадигмой при помощи подошвенного имитатора опорной нагрузки. У данных больных активируются парацентральная долька, R, постцентральная извилина, R, медиальная лобная извилина, зона SMA, субкортикальные отделы нижней париетальной дольки, R, верхняя височная извилина (з/3), R, средняя височная извилина (з/3), L, средняя височная извилина, R.
Из анализа таблиц и чертежей очевидно, что у здоровых лиц и у больных активируются схожие зоны, отличающиеся размером, распространенностью. Это доказывает, что использование имитатора позволяет применять его в качестве парадигмы для нейровизуализации зон активации головного мозга, ответственных за ходьбу.
Таким образом, применение стимуляции зон головного мозга, ответственных за ходьбу, связанной с использованием имитатора опорной нагрузки подошвенного позволит повысить точность изучения активации зон головного мозга, ответственных за ходьбу, верифицировать получаемые данные. Она может быть использована как у здоровых лиц, так и у больных с разной степенью двигательных нарушений для определения эффективности тех или иных методов тренировки ходьбы, для выявления процессов активации определенных зон мозга, участвующих в контроле локомоции, в определении процессов реорганизации этих зон в ответ на обучение ходьбе различными методами (кинезотерапии, роботтерапия и т.д.).
Источники информации
1. Ishii K., Senda M., Toyoma H. et al. Brain function in bipedal gait: a PET study. Hum. Brain Mapp., 1995, 3, s.321.
2. Mehta JP. et al., A novel technique for examining human brain activity associated with pedaling using fMRI, J Neurosci Methods, 2009 May 15; 179(2), p.230-29.
3. Jahn K. et al., Imagined locomotion in the blind: an fMRI study, Neuroimage. 2009 Mar 1; 45(1), p.122-128.
4 RU 2330640 C1, 10.08.2008.
5. WO 2006/110058 A1, 19.10.2006.
6. http://www.amc-si.com/index.php?thread=23
7. Бушенева С.Н. Функциональная реорганизация двигательных систем после инсульта, M., дисс. к.м.н., 2007.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ВЫЯВЛЕНИЯ В КОРЕ ГОЛОВНОГО МОЗГА СЕНСОМОТОРНЫХ ЗОН, ОТВЕТСТВЕННЫХ ЗА ЛОКОМОЦИЮ | 2012 |
|
RU2504329C1 |
| СПОСОБ ОЦЕНКИ МЕХАНИЗМОВ ВОССТАНОВЛЕНИЯ НАРУШЕННОГО ДВИГАТЕЛЬНОГО НАВЫКА ХОДЬБЫ У БОЛЬНЫХ С ИШЕМИЧЕСКИМ ИНСУЛЬТОМ РАЗЛИЧНОЙ ЛОКАЛИЗАЦИИ ПОРАЖЕНИЯ ГОЛОВНОГО МОЗГА В РАЗЛИЧНЫЕ ПЕРИОДЫ ЗАБОЛЕВАНИЯ | 2012 |
|
RU2483673C1 |
| СПОСОБ ОЦЕНКИ ЭФФЕКТИВНОСТИ ВОЗДЕЙСТВИЯ, ОТНОСЯЩЕГОСЯ К КОМПЛЕМЕНТАРНОЙ МЕДИЦИНЕ, ПУТЕМ ФУНКЦИОНАЛЬНОЙ МАГНИТНО-РЕЗОНАНСНОЙ ТОМОГРАФИИ ПРИ ЛЕЧЕНИИ БОЛЬНЫХ С АТЕРОСКЛЕРОТИЧЕСКИМИ СТЕНОЗАМИ СОННЫХ АРТЕРИЙ, С ПАНИЧЕСКИМИ РАССТРОЙСТВАМИ | 2019 |
|
RU2723607C1 |
| Способ ранней реабилитации пациентов при остром поражении головного мозга с использованием виртуальной реальности | 2023 |
|
RU2835867C2 |
| СПОСОБ ДИАГНОСТИКИ НЕЙРОДЕГЕНЕРАТИВНОГО ПРОЦЕССА ПРИ БОЛЕЗНИ ПАРКИНСОНА | 2015 |
|
RU2581252C1 |
| Способ прогнозирования развития сепсиса у больных с нетравматическими внутричерепными кровоизлияниями | 2016 |
|
RU2641174C2 |
| Способ оценки состояния центральной нервной системы у пациенток с постмастэктомическим синдромом | 2021 |
|
RU2754059C1 |
| СПОСОБ ОЦЕНКИ ЭФФЕКТИВНОСТИ ДВИГАТЕЛЬНОГО ВОССТАНОВЛЕНИЯ БОЛЬНЫХ, ПЕРЕНЕСШИХ ИНСУЛЬТ | 2005 |
|
RU2303952C2 |
| СПОСОБ ОЦЕНКИ ЭФФЕКТИВНОСТИ ОСТЕОПАТИЧЕСКОЙ МАНИПУЛЯЦИИ ПРИ ЛЕЧЕНИИ БОЛЬНЫХ С ХРОНИЧЕСКОЙ ГОЛОВНОЙ БОЛЬЮ НАПРЯЖЕНИЯ | 2020 |
|
RU2740331C1 |
| Способ интраоперационного нейрофизиологического мониторинга моторных и речевой зон головного мозга | 2019 |
|
RU2716507C1 |
Изобретение относится к экспериментальной и восстановительной медицине, нейровизуализации. Проводят функциональную магнитно-резонансную томографию (фМРТ) одновременно со стимуляцией зон головного мозга, ответственных за ходьбу. Для стимуляции на каждую ногу пациента, лежащего на столе в МРТ-камере, крепят ортезы, содержащие пневмостельки, снабженные пневмокамерами. К каждой пневмостельке подключается пневмопровод, приемный конец которого подключается к блоку управления, вынесенного за пределы камеры МРТ, после чего осуществляют пневмомеханическое давление на соответствующие опорные зоны стопы с помощью пневмокамер. Способ обеспечивает точность изучения активации зон головного мозга, ответственных за ходьбу, при моделировании сенсорного образа ходьбы в режиме физиологического потенцирования рефлекторных механизмов шага и активации спинального генератора локомоции и моторных центров более высокого уровня, в любом состоянии пациента. 2 табл., 2 ил.
Способ нейровизуализации зон активации головного мозга, ответственных за ходьбу, включающий проведение функциональной магнитно-резонансной томографии (фМРТ) одновременно со стимуляцией зон головного мозга, ответственных за ходьбу, отличающийся тем, что стимуляцию проводят следующим образом: на каждую ногу пациента, лежащего на столе в МРТ-камере, крепят ортезы, содержащие пневмостельки, снабженные пневмокамерами, к каждой пневмостельке подключается пневмопровод, приемный конец которого подключается к блоку управления, вынесенного за пределы камеры МРТ, после чего осуществляют пневмомеханическое давление на соответствующие опорные зоны стопы с помощью пневмокамер.
| JAHN K | |||
| et al | |||
| Imagined locomotion in the blind: an fMRI study | |||
| // Neuroimage | |||
| Колосоуборка | 1923 |
|
SU2009A1 |
| Станок для изготовления деревянных ниточных катушек из цилиндрических, снабженных осевым отверстием, заготовок | 1923 |
|
SU2008A1 |
| УСТРОЙСТВО ДЛЯ ПРОФИЛАКТИКИ И ЛЕЧЕНИЯ НАРУШЕНИЙ ЛОКОМОЦИИ (ВАРИАНТЫ) | 2005 |
|
RU2330640C1 |
| УСТРОЙСТВО ДЛЯ НЕЙРО-ОРТОПЕДИЧЕСКОЙ РЕАБИЛИТАЦИИ | 2004 |
|
RU2266082C1 |
| WO 2006110058 A1, 19.10.2006 | |||
| Механический тормоз с ручным и автоматическим торможением | 1932 |
|
SU31042A1 |
| МЕНТА J.P | |||
| et al | |||
| A novel technique for examining human | |||
Авторы
Даты
2011-09-20—Публикация
2010-05-13—Подача