Настоящее изобретение относится к способам конверсии нитратов металлов в соответствующие оксиды металлов.
Нитраты металлов являются практически важными предшественниками оксидов металлов вследствие их относительно низкой стоимости и легкости получения. Их часто подвергают конверсии в соответствующие оксиды металлов при получении катализаторов или сорбентов. Обычно при получении катализаторов или сорбентов подходящий материал-носитель пропитывают одним или несколькими растворимыми нитратами металлов и сушат материал для удаления растворителя. Затем пропитанный носитель обычно нагревают на воздухе при высокой температуре, обычно равной температуре разложения нитрата металла до оксида металла или превышающей указанную температуру; данную стадию часто называют кальцинацией. Однако подобный способ не всегда приводит к получению оксидных материалов удовлетворительного качества. В частности, если оксид металла представляет собой восстанавливаемый оксид металла, дисперсность и распределение кристаллитов оксида металла и, как следствие, восстановленного металла, полученного подобными способами, часто являются неудовлетворительными.
Были предприняты попытки видоизменений подобного способа получения. В ЕР 0421502 описан способ получения катализатора или предшественника катализатора, в котором нитрат кобальта, нанесенный на пористый инертный носитель, подвергают кальцинации в атмосфере, содержащей по меньшей мере 20% об. оксида азота (без учета содержания воды в упомянутой атмосфере). Оксиды азота предпочтительно образуются при разложении нитрата кобальта в условиях отсутствия очистки обжиговой печи или в условиях ее очистки с небольшой скоростью. Утверждается, что подобный способ кальцинации позволяет получить агломераты кристаллитов оксида кобальта размером от 1 до 10 мкм.
В вышеупомянутом документе ЕР 0421502 кальцинация нитрата кобальта проводится на воздухе, причем оксид азота получают из самого нитрата металла. Поскольку вид оксида азота не оговаривается, оксид азота представляет собой диоксид азота (NO2), так как при таком способе кальцинации он является преобладающим среди оксидов азота.
Оксиды металлов, нанесенные на носитель, находят применение в качестве катализаторов, предшественников катализаторов и сорбентов, эффективность которых связана с дисперсностью оксидов металлов на носителе. Поэтому является необходимым повышение дисперсности оксидов металлов, получаемых из нитратов металлов.
Авторами настоящего изобретения найдено, что термообработка в атмосфере смеси газов, которая содержит закись азота (N2O) и не содержит или содержит небольшое количество кислорода, приводит к получению очень высокодисперсных и равномерно распределенных в носителе оксидов металлов. В противоположность способу, описанному в ЕР 0421502, в способе по настоящему изобретению высокие концентрации оксидов азота не являются необходимыми; способ согласно настоящему изобретению обеспечивает получение крайне мелких агломератов оксида металла, обладающих размером кристаллитов <10 нм.
С учетом указанного выше в настоящем изобретении предложен способ конверсии нитратов металлов, нанесенных на носитель, в соответствующие оксиды металлов, нанесенные на носитель, включающий стадию нагрева нитрата металла с целью осуществления его разложения в атмосфере смеси газов, содержащей закись азота, содержание кислорода в которой составляет <5% об.
В настоящем изобретении также предложен оксид металла, нанесенный на носитель, получаемый подобным способом.
Способ согласно настоящему изобретению состоит в помещении нитрата металла, нанесенного на носитель, в атмосферу смеси газов, содержащей закись азота, содержание кислорода в которой составляет менее 5% об., и нагревании нитрата металла, помещенного в подобную газовую смесь, по меньшей мере до температуры его разложения. Таким образом, согласно настоящему изобретению, закись азота не генерируется путем разложения нитрата металла, а входит в состав смеси газов, в которую помещают нитрат металла на время разложения.
Нитрат металла может быть нанесен на носитель многими способами, в том числе смешиванием в сухом или расплавленном состоянии, осаждением и пропиткой. Пропитка является предпочтительной. Например, нитрат металла может быть нанесен на носитель путем пропитки водным или неводным, например раствором этанола, который может содержать другие вещества, и затем высушен для удаления растворителя или растворителей. В растворе могут присутствовать один или несколько нитратов металлов. Для повышения содержания металла или нанесения последовательных слоев различных нитратов металлов перед сушкой могут быть осуществлены одна или несколько стадий пропитки. Пропитка может быть осуществлена любыми способами, известными специалисту в области получения катализаторов или сорбентов, однако предпочтительным является способ так называемой "сухой" пропитки или пропитки "по влагоемкости", поскольку при этом сводится к минимуму количество растворителя, используемое в процессе и подлежащее удалению при сушке. Способ пропитки по влагоемкости является особенно подходящим для пористых материалов носителей и включает стадию смешивания материала носителя с количеством раствора, достаточным только для заполнения пор носителя.
Сушка может быть проведена с применением известных способов при пониженном, атмосферном или повышенном давлении, в том числе с применением сушки распылением или лиофильной сушки. Температура сушки предпочтительно составляет ≤200°С, более предпочтительно ≤160°С, что снижает преждевременное разложение нитрата металла. Сушка может быть проведена либо на воздухе, либо в атмосфере другого кислородсодержащего газа, либо в атмосфере инертного газа, в том числе азота, гелия или аргона.
Таким образом, нитрат металла, нанесенный на носитель, содержит один или несколько нитратов металлов на поверхности и/или в объеме пор носителя.
Нитрат металла подвергают нагреву с целью осуществления его разложения путем нагревания до температуры разложения, при которой он образует оксид металла, или, если необходимо, выше упомянутой температуры. Данная стадия нагрева отличается от сушки (действие которой состоит прежде всего в удалении растворителя) тем, что она вызывает физико-химическую конверсию нитрата металла в соответствующий оксид металла. Из изложенного далее ясно, что согласно способу, соответствующему настоящему изобретению, нитрат металла, нанесенный на носитель, при необходимости может быть в одну стадию как высушен, так и нагрет до разложения. Температура, до которой нагревают нитрат металла с целью проведения его разложения, может лежать в интервале 100-1200°С, однако упомянутая температура предпочтительно лежит в интервале 200-600°С, что обеспечивает конверсию нитрата в оксид при одновременном сведении к минимуму спекания оксида. Тем не менее, поскольку желательным является образование на носителе или внутри него оксидных фаз шпинели или перовскита, может быть желательным использование температур в интервале 500-1200°С. Время, в течение которого нитрат металла, нанесенный на носитель, находится при температуре, лежащей в указанном интервале, предпочтительно составляет <16 ч, более предпочтительно <8 ч.
Предпочтительно по меньшей мере 90% мас., более предпочтительно по меньшей мере 95% мас., наиболее предпочтительно по меньшей мере 99% мас. нитрата металла подвергается конверсии в соответствующий оксид металла.
Признаком настоящего изобретения является то, что атмосфера, в которую помещают нитрат металла, нанесенный на носитель, в течение стадии нагрева содержит очень мало или не содержит свободного кислорода, поскольку найдено, что кислород является источником низкой дисперсности оксида металла в материалах, получаемых из нитратов. Поэтому содержание кислорода (О2) в потоке газа составляет <5% об., предпочтительно <1% об., наиболее предпочтительно <0,1% об.
Поток газа, в который помещают нитрат металла, может представлять собой любой поток газа, содержащий закись азота и <5% об. кислорода. Поток газа предпочтительно содержит один или несколько газов, выбранных из моноксида углерода, диоксида углерода или инертного газа. Инертный газ предпочтительно содержит один или несколько газов, выбранных из азота, гелия или аргона. Поток газа, в который помещают нитрат металла, нанесенный на носитель, предпочтительно состоит из одного или нескольких инертных газов и закиси азота.
Смесь газов может находиться при атмосферном давлении или при давлении выше атмосферного, обычно составляющем примерно до 10 бар абсолютного давления. Для осуществления стадии нагрева могут быть применены различные способы, известные в уровне техники. Например, возможно пропускание потока газа-восстановителя сквозь слой нитрата металла, нанесенного на дисперсный носитель. Если стадия нагрева осуществляется путем пропускания смеси газов сквозь слой нитрата металла, нанесенного на носитель, часовая объемная скорость газовой смеси (GHSV) предпочтительно находится в интервале 100-600000 ч-1, более предпочтительно 600-100000 ч-1, наиболее предпочтительно 1000-60000 ч-1.
С целью сведения к минимуму требований по очистке газа концентрация закиси азота в потоке газа предпочтительно находится в интервале от 0,001 до 15% об., более предпочтительно от 0,01 до 10% об., наиболее предпочтительно от 0,1 до 5% об.
Нитрат металла может представлять собой любой нитрат металла, однако он предпочтительно представляет собой нитрат металла, используемого при получении катализаторов, предшественников катализаторов или растворителей. Нитрат металла может представлять собой нитрат щелочного, щелочноземельного или переходного металла. Предпочтительно нитрат металла представляет собой нитрат переходного металла, т.е. нитрат металла, являющегося выбранным из групп 3-12 включительно периодической таблицы элементов. Легкодоступные нитраты металлов, пригодные для получения катализаторов, предшественников катализаторов или сорбентов, включают нитраты La, Zr, Cr, Mn, Fe, Ru, Co, Rh, Ir, Ni, Pd, Pt, Cu и Zn, более предпочтительно нитраты Cr, Mn, Fe, Ru, Co, Rh, Ir, Ni, Pd, Pt, Cu и Zn.
Под термином "нитрат металла" авторы настоящего изобретения подразумевают соединения нитратов металлов формулы M(NO3)x.(H2O)a, где х - валентность металла М, а может быть равно нулю или целому числу ≥1, а также продукты частичного разложения подобных соединений, образующиеся, например, в ходе предшествующей стадии сушки, в том числе гидроксинитраты металлов.
Авторами настоящего изобретения найдено, что настоящий способ является особенно полезным для получения высокодисперсных оксидов металлов, способных к восстановлению, т.е. оксидов металлов, в которых по меньшей мере часть металла может быть восстановлена до элементарной формы с использованием потока газа-восстановителя, в том числе моноксида углерода и/или водорода. Подобные оксиды металлов, способные к восстановлению, включают оксиды Ni, Co, Cu и Fe, поэтому в предпочтительном варианте осуществления нитрат металла представляет собой нитрат никеля, кобальта, меди или железа, более предпочтительно никеля или кобальта, наиболее предпочтительно никеля.
Носитель, на который может быть нанесен нитрат металла, может представлять собой носитель из металла, углерода, оксида металла, смешанного оксида металла или твердого полимера. Например, носитель может представлять собой простой или смешанный оксид металла, в том числе диоксид кремния или силикаты, или другой тип носителей, пригодный для производства катализаторов или сорбентов, например металлы, сплавы металлов или уголь. В настоящем изобретении могут быть использованы один или несколько носителей.
Согласно настоящему изобретению, предпочтительно, если поток газа содержит <0,1% об. кислорода, в качестве носителей могут быть использованы углеродные носители, в том числе активированный уголь, графит с высокой площадью удельной поверхности, углеродные нановолокна и фуллерены, в виде порошка, окатышей или гранул, обладающие приемлемой пористостью, например, около 0,1 мл/г. Подобные носители не могут быть использованы в способах, известных в уровне техники, по причине проведения кальцинации на воздухе.
Носитель предпочтительно представляет собой оксидный носитель, который может представлять собой материал на основе простого или смешанного оксида металла, в том числе керамику, цеолиты, перовскиты, шпинели и т.п. Оксидный носитель может также иметь форму грунтового покрытия, нанесенного на керамический, металлический, углеродный или полимерный носитель.
Носитель может иметь вид порошка, обладающего среднеповерхностным диаметром D[3, 2] в интервале от 1 до 200 мкм. Термин "среднеповерхностный диаметр", иначе "средний диаметр по Заутеру", определяется по M. Alderliesten, "A Nomenclature for Mean Particle Diameters", Anal. Proc., vol.21, May 1984, pp.167-172 и вычисляется из данных анализа размера частиц, удобным способом проведения которого является дифракция лазерного излучения, например, с применением анализатора Malvern Mastersizer. В качестве носителя также могут быть использованы агломераты подобных порошков, обладающие размером частиц в интервале от 200 мкм до 1 мм. Согласно другому варианту осуществления, носитель может иметь вид формованных частиц, в том числе окатышей, экструдата или гранул, размер частиц при этом обычно лежит в интервале 1-25 мм, а отношение диаметров составляет менее 2 (под размером частиц имеется в виду наименьший линейный размер частицы, например, ширина, длина или диаметр). Согласно другому варианту осуществления, носитель может иметь вид монолитной структуры, например типа пчелиных сот, или представлять собой ячеистый материал, в том числе структуру с открытыми порами.
Носитель предпочтительно является выбранным из оксида алюминия, алюминатов металлов, диоксида кремния, алюмосиликатов, диоксида титана, диоксида циркония или их смесей, в том числе смешанных гелей, в виде порошка, формованных частиц, монолитной или ячеистой структуры.
Носитель может представлять собой диоксид кремния. Диоксид кремния может быть получен из природных источников, например представлять собой кизельгур, может представлять собой пирогенный или коллоидный диоксид кремния, или может быть синтетическим, например, осажденный диоксид кремния, или силикагель. В качестве носителей могут быть использованы упорядоченные мезопористые диоксиды кремния, например SBA-15. Предпочтительными являются осажденные диоксиды кремния. Диоксид кремния может иметь вид порошка или формованного материала, в том числе экструдированных, окомкованных или гранулированных частиц диоксида кремния. Пригодные порошкообразные диоксиды кремния обычно обладают среднеповерхностным диаметром частиц D [3, 2] в интервале от 3 до 100 мкм. Формованные диоксиды кремния могут иметь множество различных форм и размеров частиц в зависимости от пресс-формы или мундштука, использованных при их получении. Например, частицы могут иметь поперечное сечение круглой, дольчатой или другой формы и длину примерно от 1 до более 10 мм. Площадь поверхности по БЭТ для пригодных порошкообразных или гранулированных диоксидов кремния обычно лежит в интервале 10-500 м2.г-1, предпочтительно 100-400 м2.г-1. Объем пор обычно лежит в интервале примерно от 0,1 до 4 мл.г-1, предпочтительно 0,2-2 мл.г-1; средний диаметр пор предпочтительно лежит в интервале от 0,4 до примерно 30 нм. При необходимости диоксид кремния может быть смешан с другим оксидом металла, в том числе диоксидами титана или циркония. В другом варианте осуществления диоксид кремния может представлять собой покрытие на поверхности формованных частиц, предпочтительно состоящих из оксида алюминия; обычно покрытие содержит 0,5-5 монослоев диоксида кремния на лежащем под ним носителе.
Носитель может представлять собой диоксид титана. Носитель на основе диоксида титана предпочтительно представляет собой синтетический, например осажденный, диоксид титана. Диоксид титана может дополнительно содержать, например, до 20% мас. другого жаропрочного оксидного материала, обычно диоксида кремния, оксида алюминия или диоксида циркония. В другом варианте осуществления диоксид титана может представлять собой покрытие на носителе, предпочтительно представляющем собой диоксид кремния или оксид алюминия; покрытие содержит, например, 0,5-5 монослоев диоксида титана на лежащем под ним носителе из диоксида кремния или оксида алюминия. Площадь поверхности по БЭТ для пригодных диоксидов титана обычно лежит в интервале 10-500 м2.г-1, предпочтительно от 100 до 400 м2.г-1. Объем пор диоксида титана обычно лежит в интервале примерно от 0,1 до 4 мл.г-1, предпочтительно от 0,2 до 2 мл.г-1; средний диаметр пор предпочтительно лежит в интервале от 2 до примерно 30 нм.
Сходным образом, носители на основе диоксида циркония могут представлять собой синтетические, например осажденные диоксиды циркония. Диоксид циркония также может дополнительно содержать, например, до 20% мас. другого жаропрочного оксидного материала, обычно диоксида кремния, оксида алюминия или диоксида титана. В другом варианте осуществления диоксид циркония может представлять собой стабилизированный диоксид циркония, например диоксид циркония, стабилизированный оксидом иттрия или оксидом церия. В другом варианте осуществления диоксид циркония может представлять собой покрытие на носителе, предпочтительно представляющем собой диоксид кремния или оксид алюминия; покрытие содержит, например, 0,5-5 монослоев диоксида циркония на лежащем под ним носителе из диоксида кремния или оксида алюминия.
Носитель может представлять собой алюминат металла, например алюминат кальция.
Материал-носитель может представлять собой переходный оксид алюминия. Переходные оксиды алюминия определяются в "Ullman's Encyklopaedie der technischen Chemie", 4, neubearbeitete und erweiterte Auflage, Band 7 (1974), pp.298-299. Пригодные переходные оксиды алюминия могут представлять собой оксиды из группы гамма-оксидов алюминия, например, эта- или хи-оксид алюминия. Подобные материалы могут быть получены кальцинацией гидроксидов алюминия при 400-750°С и обычно обладают площадью поверхности по БЭТ, лежащей в интервале от 150 до 400 м2.г-1. Согласно другому варианту осуществления, переходный оксид алюминия может представлять собой оксид из группы дельта-оксидов алюминия, включающей высокотемпературные формы, в том числе дельта- и тета-оксиды алюминия; последние могут быть получены путем нагрева оксидов алюминия гамма-группы до температуры, превышающей примерно 800°С. Оксиды алюминия дельта-группы обычно обладают площадью поверхности по БЭТ, лежащей в интервале от 50 до 150 м2.г-1. Согласно другому варианту осуществления, переходный оксид алюминия может представлять собой альфа-оксид алюминия. Переходные оксиды алюминия содержат менее 0,5 моль воды на моль Al2O3, причем фактическое количество воды зависит от температуры, до которой проводился нагрев оксида. Пригодные порошки переходных оксидов алюминия обычно обладают среднеповерхностным диаметром D [3, 2], лежащим в интервале от 1 до 200 мкм. Для некоторых областей применения, например, для катализаторов, предназначенных для применения в суспензионных реакциях, предпочтительно использовать очень высокодисперсные частицы, предпочтительно в среднем являющиеся меньшими 20 мкм, например, размером 10 мкм или менее. Для других областей применения, например, для катализаторов реакций, осуществляемых в псевдоожиженном слое, может быть желательным использование частиц большего размера, предпочтительно в интервале от 50 до 150 мкм. Предпочтительно, чтобы порошок оксида алюминия обладал относительно высоким средним диаметром пор, поскольку найдено, что применение подобных оксидов алюминия позволяет получить катализаторы, обладающие особенно высокой селективностью. Предпочтительно использование оксидов алюминия, обладающих средним диаметром пор, равным по меньшей мере 10 нм, предпочтительно в интервале от 15 до 30 нм (термин "средний диаметр пор" в настоящем описании означает отношение учетверенного объема пор, измеренного по кривой десорбции изотермы физической адсорбции при относительном давлении, равном 0,98, к площади поверхности по БЭТ). Материал на основе оксида алюминия предпочтительно представляет собой гамма- или тета-оксид алюминия, более предпочтительно тета-оксид алюминия, обладающий площадью поверхности по БЭТ, равной 90-120 м2.г-1, и объемом пор 0,4-0,8 см3.г-1. Материал-носитель на основе оксида алюминия может иметь вид либо порошка, полученного распылительной сушкой, либо формованных частиц, в том числе сфер, окатышей, цилиндров, колец или окатышей с большим числом отверстий, причем указанные частицы могут быть дольчатыми или содержащими выемки, например могут иметь сечение в виде листа клевера, либо экструдатов, известных специалисту в данной области техники. Выбор носителей на основе оксида алюминия является предпочтительным вследствие их высокой фильтрующей способности и устойчивости к истиранию.
Настоящее изобретение может быть использовано для конверсии нитратов металлов на любом материале-носителе, однако некоторые сочетания нитрата металла с носителем являются более предпочтительными. Например, в зависимости от металла может быть как желательным, так и нежелательным сочетание нитрата металла с носителем, способным при условиях нагрева, используемых для разложения нитрата металла, образовывать смешанные оксиды металлов с полученным оксидом металла, нанесенным на носитель. Для снижения или предупреждения образования смешанного оксида металла по реакции с носителем, в случае, если это является нежелательным, могут быть использованы малоактивные носители, в том числе углерод или альфа-оксид алюминия.
Как указано выше, авторами настоящего изобретения найдено, что способ согласно настоящему изобретению является особенно полезным для получения высокодисперсных способных к восстановлению оксидов металлов, нанесенных на носители. Поэтому, согласно одному из вариантов осуществления, способ также включает стадию нагрева способного к восстановлению оксида металла, нанесенного на носитель, в потоке газа-восстановителя с тем, чтобы вызвать восстановление по меньшей мере части оксида металла. Может быть использован поток любого газа-восстановителя, однако последний предпочтительно содержит моноксид углерода и/или водород.
В соответствии с указанным выше, в настоящем изобретении также предложен восстановленный оксид металла, нанесенный на носитель, получаемый вышеописанным способом. Восстановленный оксид металла, нанесенный на носитель, содержит металл в элементарной форме и, возможно, невосстановленный оксид металла, нанесенные на носитель. Кроме того, на носителе могут присутствовать другие оксиды металлов, способные или не способные к восстановлению.
В данном варианте осуществления оксид металла, нанесенный на носитель, содержит по меньшей мере один оксид металла, способный к восстановлению, предпочтительно один или несколько оксидов, выбранных из оксида никеля, оксида кобальта, оксида меди или оксида железа; восстановление предпочтительно осуществляется водородсодержащим газом.
Поэтому стадия восстановления может быть осуществлена путем пропускания водородсодержащего газа, в том числе водорода, синтез-газа или смеси водорода с азотом, метаном или другим инертным газом, сквозь способный к восстановлению оксид металла, нанесенный на носитель, при повышенной температуре, например, путем пропускания водородсодержащего газа сквозь композицию при температурах в интервале 150-600°С, предпочтительно 300-500°С, в течение 0,1-24 ч при атмосферном или повышенном давлении примерно до 25 бар. Оптимальные условия восстановления оксида никеля, оксида кобальта, оксида меди и оксида железа являются известными специалисту в данной области техники.
В восстановленных оксидах металлов, нанесенных на носитель, полученных способом, соответствующим настоящему изобретению, предпочтительно по меньшей мере 50%, более предпочтительно >80%, наиболее предпочтительно >90% способного к восстановлению оксида металла восстановлено до активной элементарной формы. Способом, соответствующим настоящему изобретению, могут быть получены восстановленные оксиды металлов с очень высокой дисперсностью металла, выражаемой в площади поверхности металла на грамм катализатора или на грамм металла в восстановленном материале. Удобным может быть определение площади поверхности металла по хемосорбции (например, хемосорбции водорода) с использованием способов, известных специалисту в данной области техники.
Оксиды металлов, нанесенные на носитель, и восстановленные оксиды металлов отличаются существенно более высокой дисперсностью оксидов металлов и металлов, чем оксиды металлов и восстановленные оксиды металлов, полученные способами, известными в уровне техники. Причиной этого является то, что присутствие в потоке газа закиси азота при содержании кислорода <5% об. при разложении нитратов металлов предотвращает спекание, которое имеет место в других способах.
Способами сканирующей трансмиссионной электронной микроскопии (STEM) и дифракции рентгеновских лучей (XRD) найдено, что соответствующие настоящему изобретению оксиды металлов, нанесенные на носитель, обладают размером кристаллитов оксида металла, меньшим 10 нм, предпочтительно меньшим 7 нм, при конечном содержании оксида металла на носителе, составляющем до 30% мас. Размеры кристаллитов восстановленных оксидов металла, нанесенных на носитель, также составляют <10 нм, предпочтительно <7 нм.
Оксиды металлов, нанесенные на носитель, и восстановленные оксиды металла, нанесенные на носитель, могут быть использованы во многих областях техники. Указанные области включают катализаторы, предшественники катализаторов, сорбенты, полупроводники, сверхпроводники, магнитные запоминающие устройства, твердотельное запоминающее устройство, пигменты и УФ-абсорбенты. Оксиды металлов, нанесенные на носитель, и восстановленные оксиды металла, нанесенные на носитель, предпочтительно используют в качестве катализаторов, предшественников катализаторов или сорбентов. Термин "сорбенты" в настоящем описании включает адсорбенты и абсорбенты.
Например, восстановленные оксиды меди, нанесенные на носитель, в том числе Cu/ZnO/Al2O3, применяют в качестве катализаторов синтеза метанола и конверсии водяного газа. Восстановленные оксиды никеля, меди и кобальта, нанесенные на носитель, могут быть использованы отдельно или в сочетании с другими оксидами металлов, например оксидом цинка, в качестве катализаторов реакции гидрирования; восстановленные оксиды железа или кобальта могут быть использованы в качестве катализаторов синтеза углеводородов по Фишеру-Тропшу. Восстановленные катализаторы на основе железа также могут быть использованы в реакциях высокотемпературной конверсии и в синтезе аммиака.
Согласно предпочтительным вариантам осуществления, оксиды металлов, нанесенные на носитель, и восстановленные оксиды металлов, нанесенные на носитель, используют в качества катализаторов реакций гидрирования и синтеза углеводородов по Фишеру-Тропшу. В дополнение к Ni, Cu, Co или Fe подобные катализаторы могут также содержать одну или несколько подходящих добавок и/или промоторов, являющихся полезными при реакциях гидрирования и/или при катализе по Фишеру-Тропшу. Например, катализаторы Фишера-Тропша могут содержать одну или более одной добавки, изменяющей физические свойства, и/или один или более одного промотора, влияющего либо на способность катализаторов к восстановлению, либо на их активность, либо на их селективность. Пригодные добавки являются выбранными из соединений калия (К), молибдена (Мо), никеля (Ni), меди (Cu), железа (Fe), марганца (Mn), титана (Ti), циркония (Zr), лантана (La), церия (Се), хрома (Cr), магния (Mg) или цинка (Zn). Пригодные промоторы включают родий (Rh), иридий (Ir), рутений (Ru), рений (Re), платину (Pt) и палладий (Pd). Предпочтительно в состав предшественника катализатора вводят один или несколько промоторов, выбранных из Ru, Re, Pt или Pd. Добавки и/или промоторы могут быть введены в состав катализаторов при помощи подходящих веществ, в том числе кислот, например перрениевой кислоты, солей металлов, например нитратов или ацетатов металлов, или подходящих металлоорганических соединений, в том числе алкоксидов металлов или ацетилацетонатов металлов. Количество металла-промотора может изменяться от 3 до 50% мас., предпочтительно от 5 до 20% мас. от массы восстанавливаемого металла.
Как указано выше, восстановленные оксиды металлов, нанесенные на носитель, могут быть использованы, например в реакциях гидрирования и при синтезе углеводородов по Фишеру-Тропшу. Типичные реакции гидрирования включают гидрирование альдегидов и нитрилов до спиртов и аминов соответственно и гидрирование циклических ароматических соединений или ненасыщенных углеводородов. Катализаторы, соответствующие настоящему изобретению, являются особенно полезными при гидрировании ненасыщенных органических соединений, в особенности масел, жиров, жирных кислот и производных жирных кислот наподобие нитрилов. Подобные реакции гидрирования обычно осуществляют непрерывным или периодическим способом путем обработки гидрируемого соединения водородсодержащим газом под давлением в автоклаве при комнатной или повышенной температуре в присутствии катализатора; например гидрирование может быть проведено с использованием водорода при 80-250°С и давлении в интервале 0,1-5,0×106 Па.
Синтез углеводородов по Фишеру-Тропшу является общеизвестным. Синтез Фишера-Тропша состоит в превращении смеси моноксида углерода и водорода в углеводороды. Смесь моноксида углерода и водорода обычно представляет собой синтез-газ, отношение количества водорода к количеству моноксида углерода в котором лежит в интервале от 1,7:1 до 2,5:1. Реакция может быть проведена в периодическом или непрерывном процессе с применением одного или нескольких суспензионных реакторов с мешалкой, барботажных колонных реакторов, петлевых реакторов или реакторов с псевдоожиженным слоем. Способ может быть осуществлен при давлениях в интервале 0,1-10 МПа и температурах в интервале 150-350°С. Часовая объемная скорость газа (GHSV) в непрерывном режиме лежит в интервале 100-25000 ч-1. Катализаторы согласно настоящему изобретению являются особенно полезными в данном процессе по причине высокой площади поверхности металла на грамм катализатора.
Далее настоящее изобретение иллюстрируется со ссылкой на следующие примеры и чертежи (фиг.1-3), на которых
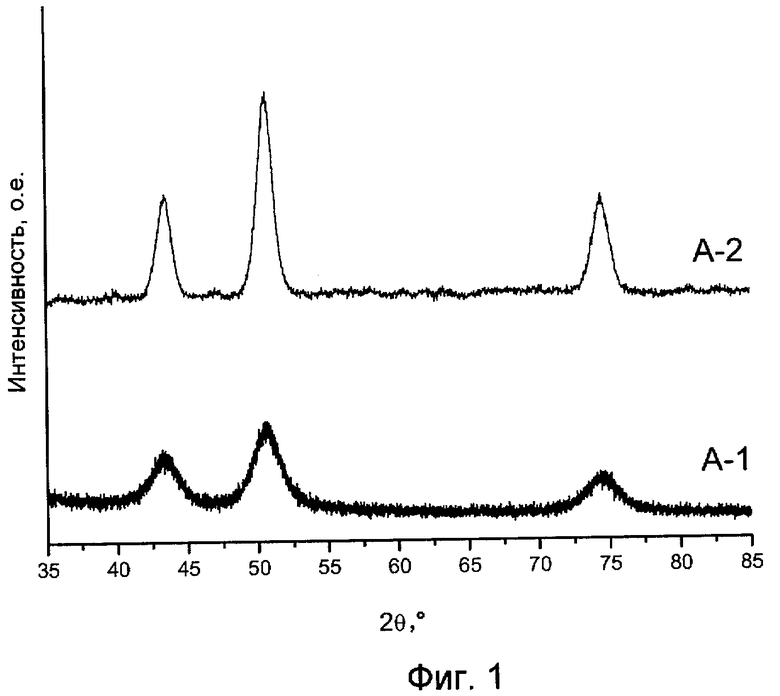
на фиг.1 показаны дифракционные рентгенограммы оксида никеля, нанесенного на диоксид кремния, полученного способом, соответствующим настоящему изобретению (А-1) и не соответствующим настоящему изобретению (А-2),
на фиг.2 показаны микрофотографии оксидов никеля (А-1, А-2), нанесенных на диоксид кремния, полученные способом сканирующей трансмиссионной электронной микроскопии (STEM) в светлом поле;
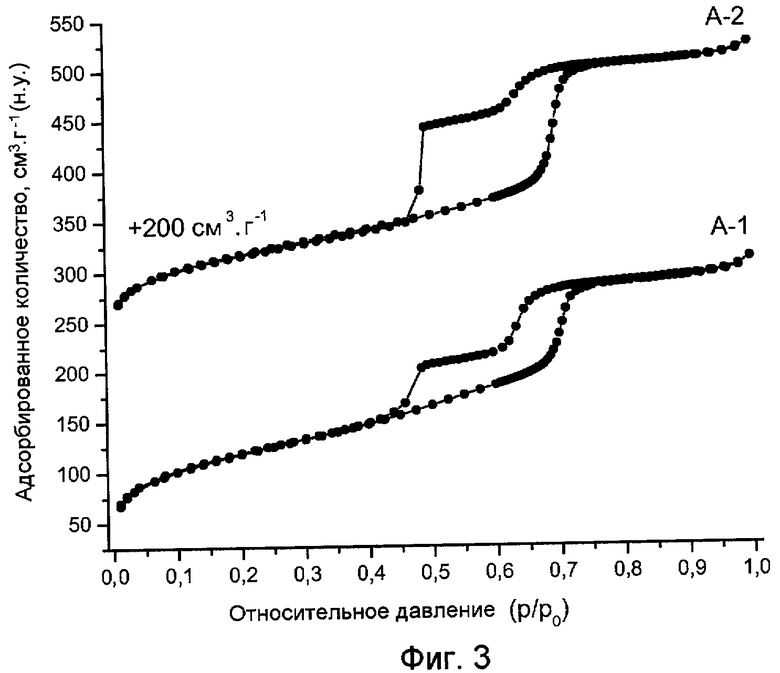
на фиг.3 показаны изотермы физической адсорбции азота на оксидах никеля (А-1, А-2), нанесенных на диоксид кремния.
Пример 1. Оксид никеля, нанесенный на SBA-15
Порошок SBA-15 (площадь поверхности по БЭТ 637 м2.г-1, общий объем пор 0,80 см3.г-1) пропитывали по влагоемкости водным раствором нитрата никеля (II) до содержания никеля, равного 20% мас. Ni/SiO2. После пропитки порошок выдерживали 15 мин для установления равновесия. Затем пропитанную твердую фазу сушили путем нагрева продукта от 25°С до конечной температуры, равной 120°С, со скоростью нагрева 1°С.мин-1. Образец выдерживали при конечной температуре в течение 720 мин. Данный высушенный образец обозначали как образец А. Небольшое количество (40 мг) данного образца подвергали второй стадии термообработки в реакторе идеального вытеснения диаметром 1 см и длиной 17 см. Образец нагревали от 25°С до 450°С со скоростью нагрева 1°С.мин-1 и выдерживали 240 мин при 450°С в потоке гелия, содержащем 1% об. закиси азота (N2O), или на воздухе (т.е. осуществляли кальцинацию). Образец, обработанный термически в соответствии с настоящим изобретением в потоке гелия, содержащем 1% об. закиси азота (N2O), обозначали как А-1, тогда как образец, полученный кальцинацией на воздухе не в соответствии с настоящим изобретением, обозначали как А-2. Условия получения приведены в таблицах 1-3.
Характеристики получали способами дифракции рентгеновских лучей (XRD) на порошке, сканирующей трансмиссионной электронной микроскопии (STEM) и физической адсорбции азота. Дифракционные рентгенограммы регистрировали при комнатной температуре при 2θ, равном от 35 до 85°C, на рентгеновском дифрактометре Bruker-Nonius D8 Advance с использованием излучения Co-Kα12 (λ=1,79026 Å). Средний размер кристаллов оксида никеля вычисляли в соответствии с уравнением Шеррера [см. Scherrer, P. Göttinger Nachrichten 2 (1938) 98] по наиболее интенсивному рефлексу при 2θ=50,8°. Изображения STEM получали с применением микроскопа Tecnai 20 FEG с ускоряющим напряжением 200 кВ. Средний размер частиц оксида никеля вычисляли по диаметру типичных 50 частиц. Изотермы физической адсорбции азота получали при 77 К с применением прибора Micromeritics Tristar 3000. Перед выполнением анализа образцы сушили 14 ч при 120°С в потоке гелия.
Рентгеновские дифрактограммы образца А-2 (фиг.1) показывают, что после термической обработки (т.е. кальцинации) высушенного образца А на воздухе в нем обнаруживаются большие кристаллиты оксида никеля (NiO). Однако, если высушенный образец обрабатывают способом, соответствующим настоящему изобретению, а именно в разбавленном потоке оксида азота (А-1), в нем обнаруживаются очень небольшие кристаллиты NiO. Наблюдаемые средние размеры кристаллитов для образцов А-1 и А-2 приведены в таблице 4.
Два типичных изображения образцов А-1 и А-2, полученных способом STEM в светлом поле, приведены на фиг.2. Изображения показывают, что упорядоченная структура пор SBA-15, образованная открытыми мезопорами цилиндрической формы, сохраняется в обоих образцах. Детали изображений образца А-2, полученного кальцинацией на воздухе, показывают, что частицы оксида никеля неравномерно откладываются по объему носителя и имеют широкое распределение по размеру. Кроме того, видно, что частицы оксида никеля внутри каналов мезопор ограничены стенками мезопор в росте одним направлением, в результате чего образуются анизотропные частицы, закупоривающие поры SBA-15. Более того, имеются частицы оксида никеля размером, превышающим диаметр пор. Видно, что данные частицы сосредоточены на внешней поверхности носителя. Изображения, полученные способом STEM при более высоком увеличении, ясно показывают, что на внешней поверхности частиц SBA-15 присутствует оксид никеля.
Полученные способом STEM изображения образца А-1, приготовленного в соответствии с настоящим изобретением, ясно показывают, что в порах SBA-15 присутствует высокодисперсный и равномерно распределенный оксид никеля. На внешней поверхности носителя частиц оксида никеля не найдено. Сравнение между распределениями частиц NiO по размеру, найденными для образцов А-1 и А-2, может быть проведено по данным таблицы 4.
Изотермы физической адсорбции образца А-2 (Фиг.3) содержат все типичные признаки, отмечаемые для SBA-15. Это указывает на то, что кальцинация на воздухе не причиняет большого ущерба структуре носителя. Однако зарегистрированная ветвь десорбции данного образца показывает резкое замыкание ветви десорбции, происходящее при значении относительного давления, примерно равном 0,48. Указанное резкое замыкание может быть приписано блокированию каналов мезопор SBA-15 кристаллитами оксида никеля. Подобные "пробки" из оксида никеля образуют бутылочные поры, результатом чего является наблюдаемое резкое замыкание изотермы в ходе десорбции. Сравнение данной изотермы с изотермой образца А-1, полученного в соответствии с настоящим изобретением, ясно показывает, что вследствие образования небольших частиц оксида никеля степень блокировки пор значительно уменьшается.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ КОНВЕРСИИ НИТРАТОВ МЕТАЛЛОВ | 2006 |
|
RU2429073C2 |
| СПОСОБ ПОЛУЧЕНИЯ НИТРАТА МЕТАЛЛА НА ПОДЛОЖКЕ | 2010 |
|
RU2516467C2 |
| ПОЛУЧЕНИЕ НИЗКОМОЛЕКУЛЯРНЫХ ОЛЕФИНОВ ИЗ СИНТЕЗ-ГАЗА | 2010 |
|
RU2558954C2 |
| КАТАЛИЗАТОР ДЛЯ ПОЛУЧЕНИЯ ОКИСИ ЭТИЛЕНА | 1992 |
|
RU2014114C1 |
| КАТАЛИЗАТОР ТРОЙНОГО ДЕЙСТВИЯ И ЕГО ИСПОЛЬЗОВАНИЕ В ВЫХЛОПНЫХ СИСТЕМАХ | 2014 |
|
RU2670754C2 |
| СПОСОБ СИНТЕЗА УГЛЕВОДОРОДОВ С5+ В ПРИСУТСТВИИ КАТАЛИЗАТОРА, ПОЛУЧЕННОГО ПРИ ПОМОЩИ ПО МЕНЬШЕЙ МЕРЕ ОДНОГО ЦИКЛИЧЕСКОГО ОЛИГОСАХАРИДА | 2011 |
|
RU2561112C2 |
| СПОСОБ ПЕРЕРАБОТКИ УГЛЕВОДОРОДНЫХ СОЕДИНЕНИЙ, СОДЕРЖАЩИХ НИТРИЛЬНЫЕ ИЛИ АМИННЫЕ ФУНКЦИОНАЛЬНЫЕ ГРУППЫ | 2009 |
|
RU2482104C2 |
| КАТАЛИЗАТОР ДЛЯ ПРОЦЕССА ФИШЕРА-ТРОПША (ВАРИАНТЫ) И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2002 |
|
RU2292238C2 |
| СПОСОБ ПРИГОТОВЛЕНИЯ КАТАЛИЗАТОРА ДЛЯ ОБЕЗВРЕЖИВАНИЯ ГАЗОВЫХ ВЫБРОСОВ (ВАРИАНТЫ) | 2008 |
|
RU2388532C1 |
| КАТАЛИТИЧЕСКАЯ КОМПОЗИЦИЯ И СПОСОБ ПРЕВРАЩЕНИЯ УГЛЕВОДОРОДНОГО СЫРЬЯ | 1996 |
|
RU2169044C2 |

Изобретение относится к способам получения нанесенных оксидов металла. Описан способ конверсии нитрата переходного металла, нанесенного на носитель, в соответствующий оксид переходного металла, нанесенный на носитель, включающий нагрев нитрата переходного металла для осуществления его разложения в атмосфере смеси газов, содержащей закись азота и инертный газ, содержание кислорода в которой составляет менее 5% об., причем концентрация закиси азота в смеси газов лежит в интервале от 0,001 до 15% об. Описан способ восстановления оксида металла, нанесенного на носитель, полученного способом, описанным выше, включающий нагрев оксида металла, нанесенного на носитель, в потоке газа-восстановителя для восстановления по меньшей мере части оксида металла. Технический результат - получены нанесенные оксиды и/или восстановленные нанесенные оксиды металлов, проявляющие высокую активность в качестве катализаторов. 2 н. и 9 з.п. ф-лы, 4 табл., 3 ил.
1. Способ конверсии нитрата переходного металла, нанесенного на носитель, в соответствующий оксид переходного металла, нанесенный на носитель, включающий нагрев нитрата переходного металла для осуществления его разложения в атмосфере смеси газов, содержащей закись азота и инертный газ, содержание кислорода в которой составляет менее 5 об.%, причем концентрация закиси азота в смеси газов лежит в интервале от 0,001 до 15 об.%.
2. Способ по п.1, отличающийся тем, что нитрат металла наносят на материал-носитель путем пропитки из раствора и сушат для удаления растворителя перед стадией нагрева нитрата металла для его конверсии в соответствующий оксид металла.
3. Способ по п.1, отличающийся тем, что смесь газов состоит из одного или нескольких инертных газов и закиси азота.
4. Способ по п.1, отличающийся тем, что инертный газ выбран из азота, гелия или аргона.
5. Способ по п.1, отличающийся тем, что нитрат металла, нанесенный на носитель, нагревают до температуры 100-1200°С.
6. Способ по п.1, отличающийся тем, что нитрат металла представляет собой нитрат никеля, кобальта, меди или железа.
7. Способ по п.1, отличающийся тем, что носитель выбирают из носителей из металла, углерода, оксида металла, смешанного оксида металла или твердого полимера.
8. Способ по п.1, отличающийся тем, что носитель выбирают из оксида алюминия, алюминатов металлов, диоксида кремния, алюмосиликатов, диоксида титана, диоксида циркония или их смесей.
9. Способ восстановления оксида металла, нанесенного на носитель, полученного способом по любому из пп.1-8, включающий нагрев оксида металла, нанесенного на носитель, в потоке газа-восстановителя для восстановления по меньшей мере части оксида металла.
10. Способ по п.9, отличающийся тем, что поток газа-восстановителя содержит моноксид углерода и/или водород.
11. Способ по п.9, отличающийся тем, что оксид металла, нанесенный на носитель, представляет собой оксид никеля, оксид кобальта, оксид меди или оксид железа и восстановление проводят с использованием водородсодержащего газа.
| MARCHETTI S G ет al | |||
| Механический грохот | 1922 |
|
SU41A1 |
| Bengoa et al | |||
| Механический грохот | 1922 |
|
SU41A1 |
Авторы
Даты
2011-12-27—Публикация
2007-08-14—Подача