ССЫЛКА НА СВЯЗАННЫЕ ЗАЯВКИ
По данной заявке испрашивается приоритет предварительной заявки США №60/854060, озаглавленной «Кратковременная затухающая амперометрия», поданной 24 октября 2006 года, которая включена сюда посредством ссылки в полном объеме, приоритет предварительной заявки США №60/869557, озаглавленной «Кратковременная затухающая амперометрия», поданной 11 декабря 2006 года, которая включена посредством ссылки в полном объеме, и приоритет предварительной заявки США №60/869625, озаглавленной «Кратковременная затухающая амперометрия», поданной 12 декабря 2006 года, которая включена посредством ссылки в полном объеме.
ОБЛАСТЬ ИЗОБРЕТЕНИЯ
Биосенсоры обеспечивают анализ биологических жидкостей, таких как цельная кровь, моча или слюна. Обычно биосенсор анализирует образец биологической жидкости для определения концентрации одного или нескольких анализируемых веществ, таких как спирт, глюкоза, мочевая кислота, лактат, холестерол или билирубин в биологической жидкости. Анализ полезен в диагностике и лечении физиологических отклонений. Например, пациент с диабетом может использовать биосенсор для определения уровня глюкозы в цельной крови для корректировки диеты и/или лечения.
Биосенсоры могут быть реализованы с использованием настольных, портативных и подобных им измерительных устройств. Портативные измерительные устройства могут быть ручными. Биосенсоры могут быть созданы для анализа одного или нескольких анализируемых веществ и могут использовать различные объемы биологических жидкостей. Некоторые биосенсоры могут анализировать одну каплю цельной крови, например, от 0,25-15 микролитров (мкл) в объеме. Примеры портативных измерительных устройств включают в себя измерительные приборы Ascensia Breeze® и Elite® корпорации Байер; биосенсоры Precision®, доступные в Abbott в Эбботт Парке, Иллинойс; биосенсоры Accucheck®, доступные в Roche в Индианаполисе, Индиана; и биосенсоры OneTouch Ultra®, доступные в Lifescan в Милпитасе, Калифорния. Примеры настольных измерительных устройств включают в себя BAS 100B Analyzer, доступный в BAS Instruments в Западном Лафайете, Индиана; Электрохимическую рабочую станцию, доступную в CH Instruments в Остине, Техас; другую Электрохимическую рабочую станцию, доступную в Cypress Systems в Лоренсе, Канзас; и Электрохимический прибор EG&G, доступный в Princeton Research Instruments в Принстоне, Нью Джерси.
Биосенсоры обычно измеряют электрический сигнал для определения концентрации анализируемого вещества в образце биологической жидкости. Обычно анализируемое вещество подвергается окислению/восстановлению или окислительно-восстановительной реакции, когда входной сигнал прикладывается к образцу. Фермент или подобная разновидность может быть добавлена к образцу для усиления окислительно-восстановительной реакции. Входной сигнал обычно представляет собой электрический сигнал, такой как электрический ток или электрический потенциал. Окислительно-восстановительная реакция создает выходной сигнал в ответ на входной сигнал. Обычно выходной сигнал представляет собой электрический сигнал, такой как электрический ток или электрический потенциал, который может быть измерен и быть связан с концентрацией анализируемого вещества биологической жидкости.
Многие биосенсоры включают в себя измерительное устройство и сенсорную полоску. Сенсорная полоска может быть предназначена для использования снаружи, внутри или частично внутри живого организма. При использовании снаружи живого организма образец биологической жидкости вводится в емкость для образца в сенсорной полоске. Сенсорная полоска может быть помещена в измерительное устройство до, после или во время введения образца для анализа. Находясь внутри или частично внутри живого организма, сенсорная полоска может быть погруженной в образец все время или образец может вводиться в полоску с перерывами. Сенсорная полоска может включать в себя емкость, которая частично изолирует объем образца или может быть открытой для образца. Подобным образом, подача образца в полоску может идти все время или прерываться для анализа.
Обычно измерительное устройство имеет электрические контакты, которые соединены с электрическими проводниками сенсорной полоски. Электрические проводники обычно соединены с рабочими электродами, противоэлектродами и/или другими электродами, которые проходят в емкость для образца. Измерительное устройство прикладывает входной сигнал через электрические контакты к электрическим проводникам сенсорной полоски. Электрические проводники передают входной сигнал через электроды к образцу, присутствующему в емкости для образца. Окислительно-восстановительная реакция анализируемого вещества образует выходной сигнал в ответ на входной сигнал. Измерительное устройство определяет концентрацию анализируемого вещества в ответ на выходной сигнал.
Сенсорная полоска может включать в себя реактивы, которые взаимодействуют с анализируемым веществом в образце биологической жидкости. Реактивы могут включать в себя ионизатор для облегчения окислительно-восстановительной реакции анализируемого вещества, а также посредники или другие субстанции, которые способствуют переносу электронов между анализируемым веществом и проводником. Ионизатор может представлять собой оксидоредуктазу, например специфичный к анализируемому веществу фермент, который катализирует окисление глюкозы в образце цельной крови. Реактивы могут включать в себя связующее вещество, которое удерживает фермент и посредник вместе.
Многие биосенсоры используют амперометрические способы, когда электрический сигнал с постоянным потенциалом (напряжением) прикладывается к электрическим проводникам сенсорной полоски, тогда как измеренный выходной сигнал представляет собой ток. Таким образом, в амперометрической системе ток может быть измерен в виде постоянного потенциала, приложенного к рабочему электроду и противоэлектроду сенсорной полоски. Затем измеренный ток можно использовать для определения присутствия и/или количества анализируемого вещества в образце. Амперометрия измеряет скорость, с которой подлежащие измерению частицы и, таким образом, анализируемое вещество, будут окислены или восстановлены на рабочем электроде. В дополнение к анализируемым веществам, биологические субстанции и посредники могут служить, например, в качестве подлежащих измерению частиц.
С течением времени, в ходе которого входной сигнал прикладывается к сенсорной полоске, скорость, при которой подлежащие измерению частицы окисляются или восстанавливаются на рабочем электроде, уменьшается. Таким образом, после начального периода с высоким выходным сигналом тока ток, зарегистрированный на сенсорной полоске, уменьшается, в то время как продолжают подавать входной сигнал. Это уменьшение тока в зависимости от времени может быть обозначено как электрохимическое затухание, и скорость этого затухания может быть скореллирована с концентрацией подлежащих измерению частиц и, таким образом, анализируемого вещества в образце. Электрохимическое затухание может представлять собой кратковременное затухание или затухание Коттрелла.
Электрохимическое затухание может быть скореллировано с концентрацией анализируемого вещества в образце через выражение затухания с помощью уравнения, описывающего линию, которая связывает ток и время, например через функцию натурального логарифма (ln). Таким образом, выходной ток может быть выражен как функция времени с экспоненциальным коэффициентом, где отрицательные экспоненциальные коэффициенты указывают на процесс затухания. После начального снижения выходного сигнала тока скорость снижения может оставаться относительно постоянной или продолжать колебаться.
Патент США №5942102 («'102 патент») описывает зависимость между измеренным выходным током и временем в ходе обыкновенного анализа. Электрический сигнал подается на сенсорную полоску примерно 60 секунд после введения в полоску образца цельной крови. В начале наблюдается быстрое снижение тока, за которым следует относительно постоянный или «установившийся» выходной сигнал тока, образованный обратной связью посредника от противоэлектрода к рабочему электроду. Обратная связь посредника, обеспеченная коротким расстоянием между электродами, приводит к току, который становится в основном независимым от времени после начального снижения. В этом обыкновенном анализе концентрация анализируемого вещества в образце может быть определена по концентрации и коэффициенту диффузии посредника следующим образом: (1) измерение тока как функции времени; и затем (2) оценка установившегося тока.
Тогда как способ анализа, описанный в '102 патенте, основывается на установившийся части затухания тока, патенты США №№6153069 («069 патент») и 6413411 («'411 патент») описывают способы, в которых концентрация посредника и, таким образом, анализируемого вещества, лежащего в основе, устанавливается по коэффициенту диффузии посредника. Эти системы выполнены с возможностью обеспечения скорости затухания тока, которая описывается уравнением Коттрелла.
Измерения тока демонстрируют затухание Коттрелла, когда измеренный ток является обратнопропорциональным квадратному корню времени. Измерения тока с затуханием Коттрелла могут быть описаны с помощью уравнения Коттрелла, приведенного ниже как уравнение (1)
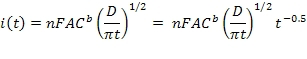 (1)
(1)
где i обозначает измеренный ток; C b обозначает объемную концентрацию электрохимически активных частиц в моль/см3; A обозначает площадь электрода в см2; F обозначает постоянную Фарадея, равную 96500 Кл/эквивалент; n обозначает число перенесенных электронов на эквивалент/моль; D обозначает коэффициент диффузии на см2/с; и t обозначает время электрохимической реакции в секундах. Таким образом, уравнение Коттрелла описывает ток в виде экспоненциальной функции от времени, обладающей постоянной затухания или экспоненциальным коэффициентом -0,5. Дополнительные детали уравнения Коттрелла и пограничные условия, требуемые для коттрелловского поведения, могут быть найдены в главе 5, стр.136-45, Electrochemical Methods: Fundamentals and Applications by Bard and Faulkner (1980).
Система, разработанная для работы с коттрелловским затуханием тока, требует постоянного затухания, равного -0,5. Электрохимическая система, демонстрирующая постоянную затухания -0,5, предполагает, что присутствуют требования, необходимые для коттрелловского постоянного тока, а именно, что анализируемое вещество полностью превращено в подлежащие измерению частицы, и что в основном постоянное распределение концентрации этих подлежащих измерению частиц занимает емкость для образца перед измерением тока. Эти требования дополнительно описаны в '069 и '411 патентах.
Колонка 4, строки 39-40 '411 патента раскрывают то, что начальные инкубационные периоды от 15 до 90 секунд, предпочтительно от 20 до 45 секунд, используются для тестов на глюкозу. После начального инкубационного периода и прикладывания однократного возбуждающего входного сигнала измерения тока, показывающие коттрелловское затухание, могут регистрироваться от 2 до 30 секунд или предпочтительно от 10 до 20 секунд после прикладывания входного сигнала к сенсорной полоске. Потребность в более длинном начальном инкубационном периоде также изображена на фиг.7 '411 патента, где образец вступил в реакцию в сенсорной полоске (инкубация) за 160 секунд перед приложением входного сигнала.
Более длинные инкубационные периоды, требующиеся для полного превращения анализируемого вещества в подлежащие измерению частицы, предоставляют: (1) время для гидратации слоя реактивов, содержащего реактивы; и (2) время для превращения анализируемого вещества с помощью реактивов. Например, колонка 4, строки 36-44 '411 патента описывают инкубационный период достаточной длительности, который позволяет ферментативной реакции пройти до конца. После этого инкубационного периода, когда глюкоза анализируемого вещества полностью превращена в подлежащие измерению частицы, прибор прикладывает известный потенциал к электродам для измерения полученного диффузионно ограниченного (т.е. коттрелловского) тока в определенные моменты времени в ходе полученного коттрелловского затухания тока. Таким образом, превращение анализируемого вещества в подлежащие измерению частицы выполнено до наблюдения коттрелловского затухания. Полная гидратация слоя реактивов также признана в '411 патенте в качестве требования для коттрелловского затухания. '411 патент раскрывает то, что неполное смачивание реактива приводит к неспособности системы придерживаться кривой коттрелловского затухания, что приводит к получению неточного значения концентрации анализируемого вещества.
В дополнение к расширенному инкубационному периоду коттрелловское затухание также требует в основном равномерного распределения концентрации подлежащих измерению частиц в образце, так как увеличивается расстояние до поверхности электродов. В основном постоянное распределение концентрации может быть достигнуто с помощью: (1) относительно больших объемов образцов; и/или (2) относительно больших расстояний между электродами с плоскими гранями или практически плоскими электродами и нижней поверхностью крышки сенсорной полоски. Например, колонка 8, строка 40 '069 патента описывает рабочий электрод, занимающий емкость для образца, обеспечивающую 50 мкл объем образца, где вертикальное расстояние между рабочим электродом и крышкой составляет от 500-2000 мкм. В другом примере, отличном от близко расположенных электродов '102 патента, расстояние между рабочим электродом и противоэлектродом, описанное в колонке 7, строках 62-66 '411 патента, должно быть, по крайней мере, 100 микрон, и предпочтительно больше чем 100 микрон.
Обыкновенные способы анализа обычно удлиняют время, требуемое для анализа образцов за счет требований к инкубационным периодам, расстоянию между электродами и объему емкости для образца, достаточным, чтобы коттрелловское затухание в системе было возможным. Таким образом, в настоящее время сохраняется необходимость в улучшенных биосенсорах; особенно в таких, которые более быстро определяют концентрацию анализируемого вещества в образце и не зависят от оценки величины установившегося тока. Системы, устройства и способы по настоящему изобретению преодолевают, по меньшей мере, один из недостатков, связанных с обыкновенными биосенсорами.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к биосенсорной системе, которая определяет концентрацию анализируемого вещества в биологическом образце по выходному сигналу, обладающему кратковременным затуханием. Выходной сигнал не является обратнопропорциональным квадратному корню времени и, таким образом, обладает постоянной затухания большей или меньшей, чем постоянная затухания коттрелловского затухания.
В одном из аспектов способ для определения концентрации анализируемого вещества в образце включает в себя приложение входного сигнала к образцу после инкубационного периода, образование выходного сигнала, обладающего кратковременным затуханием в ответ на окислительно-восстановительную реакцию подлежащих измерению частиц; и определение концентрации анализируемого вещества на основании выходного сигнала. Анализируемое вещество может содержать глюкозу, и образец может быть введен в сенсорную полоску. Способ может включать перенос, по меньшей мере, одного электрона из или к анализируемому веществу в образце для образования подлежащих измерению частиц, которые могут включать в себя, по меньшей мере, один посредник.
Входной сигнал может включать в себя, по меньшей мере, два возбуждения, разделенных релаксацией, где, по меньшей мере, два возбуждения обладают длительностью от 0,1 до 5 секунд и длительность релаксации составляет, по меньшей мере, 0,1 секунды или, по меньшей мере, 0,5 секунды. Длительность каждого возбуждения и/или релаксации может быть одинаковой или различной. Длительность одной или нескольких релаксаций может быть от 0,1 до 3 секунд. Входной сигнал может включать в себя, по меньшей мере, три возбуждения и, по меньшей мере, две релаксации. Входной сигнал может включать в себя, по меньшей мере, 2 рабочих цикла, длящихся в течение 5 секунд.
Инкубационный период может быть от 0,1 до 8 секунд, от 0,1 до 6 секунд или от 0,5 до 4,75 секунд, например. Инкубационный период и приложение входного сигнала может быть закончено не больше чем за 12, не больше чем за 6, или не больше чем за 4 секунды. Кратковременное затухание может иметь постоянную затухания от -0,52 до -1 или от -0,001 до -0,48. Кратковременное затухание может иметь постоянную затухания не больше чем -0,45 или не больше чем -0,35. Выходной сигнал, на основании которого определяется концентрация анализируемого вещества, может включать в себя значение тока, зарегистрированное в течение 2 секунд приложения входного сигнала к образцу. Концентрация анализируемого вещества в образце может быть определена при приложении входного сигнала в течение не более чем 6, 3 или 1,5 секунд.
Образец может находиться в емкости, определенной основанием сенсорной полоски и нижней поверхностью крышки, основание находится на расстоянии от 20 до 200 микрометров от нижней поверхности крышки. Объем образца в емкости может составлять от 0,25 до 10 микролитров, до от 0,25, до 1,5 микролитра. Емкость может включать в себя, по меньшей мере, один слой реактивов, обладающий начальной средней толщиной не более чем 20 микрометров, менее чем 14 микрометров или не более чем 5 микрометров. Емкость может включать в себя, по меньшей мере, один слой реактивов, обладающий средней начальной толщиной не более 2 микрометров, когда входной сигнал включает в себя, по крайней мере, два возбуждения, по меньшей мере, одно из возбуждений обладает длительностью не более чем 0,5 секунды. Емкость может включать в себя, по меньшей мере, один слой реактивов, содержащий особый диффузионный барьерный слой.
Высота емкости от основания сенсорной полоски до нижней части крышки может составлять не более чем 250 микрометров, объем образца в емкости может составлять не более чем 5 микролитров, емкость может включать в себя, по меньшей мере, один слой реактивов, обладающий средней начальной толщиной не более чем 20 микрометров, и инкубационный период может составлять не более чем 12 секунд. Высота емкости от основания сенсорной полоски до нижней части крышки может составлять не более чем 150 микрометров, объем образца в емкости может составлять не более чем 3,5 микролитра, емкость может включать в себя, по меньшей мере, один слой реактивов, обладающий средней начальной толщиной менее чем 14 микрометров, и инкубационный период может составлять не более чем 6 секунд. Высота емкости от основания сенсорной полоски до нижней части крышки может составлять не более чем 100 микрометров, объем образца в емкости может составлять не более чем 3 микролитра, емкость может включать в себя, по меньшей мере, один слой реактивов, обладающий средней начальной толщиной не более чем 2 микрометра, и инкубационный период может быть не более 2 секунд.
В другом аспекте способ определения концентрации анализируемого вещества в образце включает в себя приложение входного сигнала к образцу после инкубационного периода, равного не более чем 12 секундам, образование выходного сигнала, обладающего кратковременным затуханием в ответ на окислительно-восстановительную реакцию подлежащих измерению частиц; и определение концентрации анализируемого вещества на основании выходного сигнала.
В другом аспекте биосенсор для определения концентрации анализируемого вещества в образце включает в себя измерительное устройство, обладающее процессором, соединенным с интерфейсом сенсора; сенсорную полоску, обладающую интерфейсом образца на основании, интерфейс сенсора электрически соединен с интерфейсом образца, где интерфейс образца расположен рядом с емкостью, образованной с помощью основания; где процессор дает зарядному устройству команду подать входной сигнал на емкость после не более чем 12-секундного инкубационного периода; и где процессор определяет концентрацию анализируемого вещества в образце на основании выходного сигнала, обладающего кратковременным затуханием в ответ на окислительно-восстановительную реакцию анализируемого вещества в образце.
Емкость может включать в себя, по меньшей мере, один рабочий электрод, который электрически соединен с зарядным устройством, слой реактивов на рабочем электроде, обладающий комбинацией ДБС/слой реактивов со средней начальной толщиной приблизительно от 1 микрометра приблизительно до 20 микрометров. Комбинация ДБС/слой реактивов может обладать средней начальной толщиной не более чем 1 микрометр.
В другом аспекте способ определения концентрации анализируемого вещества в образце включает в себя приложение входного сигнала к образцу после не более чем 12-секундного инкубационного периода; образование переменного распределения концентрации подлежащих измерению частиц в емкости для образца; образование выходного сигнала в ответ на окислительно-восстановительную реакцию подлежащих измерению частиц; и определение концентрации анализируемого вещества на основании выходного сигнала.
В другом аспекте способ определения концентрации анализируемого вещества в образце включает в себя введение образца в сенсорную полоску; приложение входного сигнала к образцу после не более чем 8-секундного инкубационного периода; образование выходного сигнала, обладающего кратковременным затуханием в ответ на окислительно-восстановительную реакцию подлежащих измерению частиц; и определение концентрации анализируемого вещества на основании кратковременного затухания выходного сигнала. Кратковременное затухание может представлять собой убывающее затухание тока, полученное в течение от 0,5 до 5 секунд или в течение примерно от 0,5 приблизительно до 3 секунд приложения входного сигнала к образцу.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
Изобретение можно лучше понять с помощью ссылок на следующие чертежи и описание. Детали на чертежах необязательно находятся в масштабе и визуально выделены при иллюстрировании принципов изобретения.
Фиг.1A представляет собой изображение собранной сенсорной полоски в перспективе.
Фиг.1B представляет собой схему с видом сверху сенсорной полоски со снятой крышкой.
Фиг.2A представляет собой схему вида с торца сенсорной полоски с фиг.1B.
Фиг.2B изображает схематическое представление биосенсорной системы, которая определяет концентрацию анализируемого вещества в образце.
Фиг.3 представляет блок-схему электрохимического способа определения присутствия и/или концентрации анализируемого вещества в образце.
Фиг.4A представляет емкость для образца, ограниченную нижней поверхностью электрода и верхней крышкой.
Фиг.4B представляет профили концентраций, образованные сенсорной системой, когда времена инкубации с t 1 до t 5 прошли до приложения входного сигнала.
Фиг.4C представляет зависимость между концентрациями подлежащих измерению частиц в емкости и скоростями затухания тока.
Фиг.5 изображает скорости затухания, полученные от рабочих электродов после варьирования инкубационных периодов для образцов цельной крови, содержащих 50, 100, 200 или 400 мг/дл глюкозы.
Фиг.6A-6C изображает профили тока, полученные от трех сенсорных полосок, каждая из которых обладает отличающейся средней начальной толщиной реакционного слоя при множестве начальных инкубационных периодов.
Фиг.7A-7B изображает кривую натуральных логарифмов тока в зависимости от времени для образцов цельной крови, включающих в себя 100 или 300 мг/дл глюкозы при гематокрите 40%, полученного после 6-секундного начального инкубационного периода.
Фиг.8A-8C представляют собой профили затуханий тока от 0,25-секундного инкубационного периода, после которого стробированный входной сигнал обладает временем возбуждения, равным 0,5 секунды и временем релаксации, равным 0,25 секунды.
Фиг.8D представляет собой калибровочную кривую, полученную нанесением конечных токов ( p1 , p2 , p3 ) первых трех возбуждений, полученных из сенсорных полосок с тонким слоем реактивов, как изображено на фиг.8A-8C.
Фиг.8E представляет собой калибровочную кривую, полученную нанесением конечных токов ( p4 , p5 , p6 ) возбуждений 4, 5 и 6, полученных из сенсорных полосок, обладающих слоем реактивов средней толщины, как изображено на фиг.8A-8C.
ПОДРОБНОЕ ОПИСАНИЕ
Биосенсорная система использует электрохимический процесс с отсутствием постоянной затухания Коттрелла для определения концентрации анализируемого вещества в биологическом образце. Биосенсорная система образует выходной сигнал из биологического образца, обладающий кратковременным затуханием, где выходной сигнал не связан обратной зависимостью с квадратным корнем времени. Кратковременное затухание выходного сигнала биосенсорной системы обладает постоянной затухания, большей или меньшей чем -0,5, и система не зависит от оценки величины установившегося тока для определения концентрации анализируемого вещества. Предпочтительно, кратковременные затухания, на основании которых определяются концентрации анализируемого вещества, непрерывно снижаются.
Коттрелловское затухание зависит от диффузии и может не существовать до тех пор, пока анализируемое вещество не будет полностью превращено в подлежащие измерению частицы и не будет достигнуто, главным образом, постоянное распределение концентрации этих подлежащих измерению частиц, занимающих емкость для образца, перед измерением тока. Относительно большая длительность инкубации и большой объем образцов требуются для получения коттрелловского затухания. Без этих условий выходной ток не будет связан обратной зависимостью с квадратным корнем времени и, таким образом, биосенсоры не будут показывать постоянную затухания, равную -0,5, которая требуется для коттрелловского затухания. Биосенсоры, разработанные для функционирования с коттрелловским затуханием, будут обеспечивать неточные анализы, если выходной ток не связан обратной зависимостью с квадратным корнем времени, или если в выходном сигнале присутствует постоянная затухания, отличная от -0,5.
Данная биосенсорная система функционирует с использованием кратковременных затуханий, когда наблюдаются постоянные затухания меньше или больше -0,5. Кратковременные и, таким образом, некоттрелловские постоянные затухания могут быть следствием относительно короткого инкубационного периода. Кратковременные постоянные затухания также могут быть следствием относительно маленького объема емкости для образца, относительно маленьких расстояний между поверхностями электродов и крышкой сенсорной полоски, и/или относительно коротких возбуждений по отношению к средней начальной толщине слоя реактивов.
Для образования выходного тока с кратковременным затуханием или постоянными кратковременного затухания больше или меньше чем -0,5, биосенсорная система может использовать инкубационные периоды, равные 12 секундам или менее, объемы емкости от 5 мкл или менее, высоты емкостей от 200 мкм или менее, и/или среднюю начальную толщину для слоя реактивов, равную 20 мкм или менее. Предпочтительные инкубационные периоды для использования с объемами емкости 3,5 мкл или менее, высотами емкостей 150 мкм или менее, и/или средней начальной толщиной слоя реактивов, равной 10 мкм или менее, составляют не более чем 8 секунд, не более чем 6 секунд или не более чем 4 секунды. В настоящее время особо предпочтительные инкубационные периоды для использования с объемами образца полосок для образца, равными 3,0 мкл или менее, высотой крышка-зазор полоски для образца, равной 100 мкм или менее, и/или средней начальной толщиной слоя реактивов, равной 2 мкм или менее, составляют не более чем 2 секунды или не более чем 1 секунду. Можно использовать другие инкубационные периоды, объемы емкости, высоты емкости и толщины слоя реактивов.
Фиг.1A и 1B изображают сенсорную полоску 100, которую можно использовать с биосенсорной системой. Фиг.1A представляет собой изображение в перспективе собранной сенсорной полоски 100, включающей в себя основание сенсора 110, по меньшей мере, частично накрытое крышкой 120, которая включает в себя отверстие 130, зону 140 покрытия образца и входное концевое отверстие 150. Частично закрытая емкость 160 для образца (капиллярный зазор или крышка-зазор) образована между основанием 110 и крышкой 120. Так же можно использовать сенсорные полоски других конструкций, такие как те, что описаны в патентах США №№5120420 и 5798031. Несмотря на то, что на фиг.1A-1B показана специфическая конфигурация, сенсорная полоска 100 может иметь другие конфигурации, включая те, которые обладают дополнительными компонентами.
Высота емкости 160 между основанием сенсора 110 и крышкой 120 может быть от 20 до 250 микрометров (мкм), более предпочтительно от 50 до 150 мкм. Объем емкости 160 может составлять от 0,25 до 10 мкл, предпочтительно от 0,8 до 4 мкл и более предпочтительно от 0,5 до 1,5 мкл. Можно использовать другие высоты и объемы.
Жидкий образец для анализа может быть внесен в емкость 160 посредством введения жидкости в отверстие 150. Жидкость заполняет емкость 160, вытесняя предварительно содержавшийся воздух через отверстие 130. Емкость 160 может содержать композицию (не показана), которая помогает удерживать жидкий образец в емкости. Примеры таких композиций включают в себя: водонабухающие полимеры, такие как карбоксиметилцеллюлоза и полиэтиленгликоль; и пористые полимерные матрицы, такие как декстран и полиакриламид.
Фиг.1B изображает вид сенсорной полоски 100 сверху, со снятой крышкой 120. Проводники 170 и 180 могут двигаться под диэлектрическим слоем 190 от отверстия 150 к рабочему электроду 175 и противоэлектроду 185 соответственно. Сенсорная полоска 100 может включать в себя более чем один рабочий электрод. Рабочий электрод и противоэлектрод 175, 185 могут находиться главным образом в одной плоскости. Электроды могут находиться и в другом положении. Диэлектрический слой 190 может частично покрывать электроды 175, 185 и может быть выполнен из любого пригодного диэлектрического материала, такого как изолирующий полимер. Несмотря на то, что показана конфигурация отдельного электрода, электроды могут иметь другие конфигурации, включая конфигурации с дополнительными компонентами.
Противоэлектрод 185 может поддерживать электрохимическую активность на рабочем электроде 175 сенсорной полоски 100. Потенциал для поддержания электрохимической активности на рабочем электроде 175 может быть предоставлен сенсорной системе с помощью образования противоэлектрода 185 из инертного материала, такого как углерод, и включать в себя растворимые окислительно-восстановительные частицы, такие как феррицианид, в емкости 160. Потенциал на противоэлектроде 185 может быть опорным потенциалом, который достигается формированием противоэлектрода 185 из окислительно-восстановительной пары, такой как Ag/AgCl, для предоставления комбинированного опорного противоэлектрода. Окислительно-восстановительная пара включает в себя две спаренных частицы химической субстанции, обладающие различными степенями окисления. Восстановление частиц, обладающих более высокой степенью окисления, образует частицы, обладающие более низкой степенью окисления. Альтернативно, окисление частиц, обладающих более низкой степенью окисления, образует частицы, обладающие более высокой степенью окисления. Сенсорная полоска 100 может быть предоставлена с третьим проводником и электродом для обеспечения опорного потенциала для сенсорной системы.
Рабочий электрод и противоэлектрод 175, 185 могут быть разделены более чем 200 мкм или 250 мкм. Рабочий электрод и противоэлектрод 175, 185 могут быть разделены менее чем 200 мкм. Рабочий электрод и противоэлектрод 175, 185 могут быть разделены другими расстояниями.
Фиг.2A изображает вид с торца сенсорной полоски 100, изображенной на фиг.1B, показывает строение слоя рабочего электрода 175 и противоэлектрода 185, находящихся в емкости 160. Проводники 170 и 180 могут лежать на основании 110. Другие материалы могут находиться между проводниками 170, 180 и основанием 110, таким образом, проводники могут или не могут находиться в физическом контакте с основанием. Часть проводников может пронизывать часть основания. Поверхностные слои 270 и 280 проводников необязательно могут быть размещены на проводниках 170 и 180 соответственно. Другие материалы могут находиться между поверхностными слоями 270, 280 проводников и проводниками 170, 180, таким образом, поверхностные проводники могут или не могут находиться в физическом контакте с проводниками. Часть поверхностных проводников может пронизывать часть проводников. Поверхностные слои 270, 280 проводников могут быть изготовлены из одинаковых или из разных материалов.
Материал или материалы, образующие проводники 170, 180 и поверхностные слои 270, 280 проводников, могут включать в себя любой электрический проводник. Проводники 170, 180 предпочтительно включают в себя тонкий слой металлической пасты или металла, такого как золото, серебро, платина, палладий, медь или вольфрам. Поверхностные слои 270, 280 проводников предпочтительно включают в себя углерод, золото, платину, палладий или их сочетания. Предпочтительные электрические проводники являются неионизирующимися, так что материал не подвергается сетчатому окислению или сетчатому восстановлению в ходе анализа образца. Таким образом, если слой поверхностного проводника не является проводником, проводник предпочтительно изготовлен из неионизирующего материала, такого как углерод, золото, платина, палладий или их сочетаний.
Материал поверхностного проводника может быть нанесен на проводники 170, 180 с помощью любых обыкновенных средств, совместимых с работой сенсорной полоски, включая фольговое нанесение, химическое осаждение из паровой фазы, осаждение суспензии и т.п. В случае осаждения суспензии материал проводника может применяться в качестве чернил для маркировки проводников 170, 180, как описано в патенте США №5798031.
Слои 275 и 285 реактивов могут быть нанесены на проводники 170 и 180 соответственно. Слои образованы, по меньшей мере, из одной композиции реактивов, которая может включать в себя связывающее вещество. Связывающее вещество предпочтительно представляет собой полимерный материал, который, по меньшей мере, частично, является водорастворимым. Связывающее вещество при гидратации может образовывать гель или гелеподобный материал. Связывающее вещество при гидратации может образовывать гель или гелеподобный материал в сочетании с реактивами. Гель или гелеподобный материал может подавлять и/или фильтровать красные клетки крови от прохождения к поверхностному проводнику 270 и/или проводнику 170.
Пригодные частично водорастворимые полимерные материалы для применения в качестве связывающего вещества могут включать в себя поли(этиленоксид) (ПЭО), карбоксиметилцеллюлозу (КМЦ), поливиниловый спирт (ПВС), гидроксиэтиленцеллюлозу (ГЭЦ), гидроксипропилцеллюлозу (ГПЦ), метилцеллюлозу, этилцеллюлозу, этилгидроксиэтилцеллюлозу, карбоксиметилэтилцеллюлозу, поливинилпирролидон (ПВП), полиаминокислоты, такие как полилизин, полистиролсульфонат, желатин, акриловую кислоту, метакриловую кислоту, крахмал, малеиновый ангидрид его соли, его производные и их сочетания. Среди вышеуказанных материалов связывающих веществ ПЭО, ПВС, КМЦ и ГЭЦ являются предпочтительными, причем в настоящее время КМЦ наиболее предпочтительна.
В дополнение к связывающему веществу, слои 275 и 285 реактивов могут включать в себя одинаковые или различные реактивы. Когда содержатся одинаковые реактивы, слои 275 и 285 реактивов могут быть одним и тем же слоем. В одном из аспектов реактивы, которые присутствуют в первом слое 275, могут быть выбраны для использования с рабочим электродом 175, тогда как реактивы, присутствующие во втором слое 285, могут быть выбраны для использования с противоэлектродом 185. Например, реактивы в слое 285 могут облегчать протекание электронов между образцом и проводником 180. Сходным образом, реактивы в слое 275 могут облегчать реакцию анализируемого вещества.
Слой 275 реактивов может включать в себя специфичную к анализируемому веществу ферментативную систему, которая может увеличить специфичность сенсорной системы к анализируемому веществу, особенно в сложных биологических образцах. Ферментативная система может включать в себя один или несколько ферментов, кофакторов и/или других компонентов, которые участвуют в окислительно-восстановительнаой реакции анализируемого вещества. Например, алкогольоксидазу можно использовать для предоставления сенсорной полоски, которая чувствительна к присутствию алкоголя в образце. Такая система может быть полезна в измерении концентраций алкоголя в крови. В другом примере глюкозодегидрогеназу или глюкозоксидазу можно использовать для предоставления сенсорной полоски, которая чувствительна к присутствию глюкозы в образце. Эта система может быть полезна при измерении концентраций глюкозы в крови, например, у пациентов с диабетом или подозрением на диабет.
Ферменты для использования в ферментативной системе включают в себя алкогольдегидрогеназу, лактатдегидрогеназу, β-гидроксибутират дегидрогеназу, глюкоза-6-фосфат-дегидрогеназу, глюкозодегидрогеназу, формальдегид дегидрогеназу, малатдегидрогеназу и 3-гидроксистероиддегидрогеназу. Предпочтительные ферментативные системы могут быть кислородонезависимыми, таким образом, не окисляться кислородом.
Одним таким кислородонезависимым ферментативным семейством для использования в сенсорной полоске для глюкозы являются глюкозодегидрогеназы (ГДГ). Используя различные коферменты или кофакторы, ГДГ могут быть опосредованы различным образом с помощью других посредников. В зависимости от ассоциации с ГДГ, кофактор, такой как флавинадениндинуклеотид (ФАД), может плотно удерживаться главным ферментом, например, как в случае с ФАД-ГДГ; или кофактор, такой как пирролохинолинхинон (ПХХ), может быть ковалентно связан с главным ферментом, например с ПХХ-ГДГ. В каждой из этих ферментативных систем кофактор может удерживаться главным ферментом или коферментом, и апофермент может быть восстановлен до того как ферментативная система будет добавлена в композицию реактивов. Также кофермент может быть независимо добавлен к главному ферменту в композиции реактивов для поддержки каталитической функции главного фермента, например, как в случаях с никотинамидадениндинуклеотидом NAD/NADH+ или никотинамидадениндинуклеотидфосфатом NADP/NADPH+.
Также слой 275 реактивов может включать в себя посредник для более эффективного взаимодействия продуктов окислительно-восстановительной реакции анализируемого вещества с поверхностным проводником 270 и/или проводником 170. Посредники могут быть разделены на две группы на основании их электрохимической активности. Одни посредники, переносящие электроны, способны захватывать один дополнительный электрон в ходе электрохимических реакций. Примеры посредников, переносящих один электрон, включают в себя соединения, такие как 1,1'-диметилферроцен, ферроцианид и феррицианид, и гексамин рутения(III). Посредники, переносящие два электрона, способны захватывать два дополнительных электрона.
Посредники, переносящие два электрона, включают в себя органические хиноны и гидрохиноны, такие как фенатролинхинон; производные фенотиазина и феноксазина; 3-(фениламино)-3H-феноксазины; фенотиазины; и 7-гидрокси-9,9-диметил-9H-акридин-2-он и его производные. Примеры дополнительных посредников, переносящих два электрона, включают в себя электроактивные органические молекулы, описанные в патентах США №№5393615; 5498542; и 5520786, которые включены в настоящий документ в качестве ссылки. Другие электроактивные органические молекулы включают в себя органические молекулы, в которых отсутствует металл, который способен подвергаться окислительно-восстановительной реакции. Электроактивные органические молекулы могут вести себя как окислительно-восстановительные частицы и/или как посредники. Примеры электроактивных органических молекул включают в себя коферменты, пирролохинолинхинон (ПХХ), бензохиноны и нафтохиноны, N-оксиды, нитрозосоединения, гидроксиламины, оксины, флавины, феназины, фенотиазины, индофенолы и индамины.
Предпочтительные посредники, переносящие два электрона, включают в себя 3-фенилимино-3H-фенотиазины (ФИФТ) и 3-фенилимино- 3H-феноксазины (ФИФО). Более предпочтительные посредники, переносящие два электрона, включают в себя карбоновую кислоту или соль, такие как аммонийные соли фенотиазиновых производных. В настоящее время особенно предпочтительные посредники, переносящие два электрона, включают в себя (E)-2-(3H-фенотиазин-3-илиденамино)бензол-1,4-двусульфокислоту, (E)-5-(3H-фенотиазин-3-илиденамино)изофталевую кислоту, аммоний (E)-3-(3H-фенотиазин-3-илиденамино)-5-карбоксибензоат и их сочетания. Предпочтительные посредники, переносящие два электрона, могут обладать окислительно-восстановительным потенциалом, который, по меньшей мере, на 100 мВ ниже, более предпочтительно, по меньшей мере, на 150 мВ ниже, чем у феррицианида.
Слои 275, 285 реактивов могут быть нанесены любыми подходящими средствами, такими как печать, жидкостное нанесение или чернильно-струйное нанесение. В одном из аспектов слои нанесены с помощью печати. При прочих равных условиях угол печатающего лезвия может обратнопропорционально влиять на начальную толщину слоя реактивов. Например, когда лезвие движется под углом приблизительно 82° к основанию 110, слой может иметь начальную толщину, приблизительно равную 10 мкм. Сходным образом, когда используется угол лезвия приблизительно 62° к основанию 110, может быть изготовлен более толстый 30 мкм слой. Таким образом, более низкие углы лезвия могут обеспечивать более толстые слои реактивов. В дополнение к углу лезвия другие факторы, такие как вязкость композиции реактивов, а также размер экрана и состав эмульсии могут оказывать влияние на конечную толщину слоев 275, 285 реактивов.
Когда более тонкие слои реактивов являются предпочтительными, можно использовать способы нанесения, отличные от печати, такие как микропипеттирование, струйная печать или контактное нанесение. Эти способы нанесения, как правило, дают сухие слои реактивов микрометровой или субмикрометровой толщины, например 1-2 мкм. Например, способы контактного нанесения могут обеспечивать среднюю начальную толщину слоя реактивов примерно 1 мкм. Толщина слоя реактивов, получаемая при контактном нанесении, например, может управляться количеством полимера, содержащегося в композиции реактивов, обеспечивая более толстые слои реактивов при более высоком содержании полимера. Более тонкие слои реактивов могут требовать более короткой длительности возбуждений, чем более толстые слои реактивов для поддержания желаемой производительности измерений и/или в основном проводить измерения анализируемого вещества в диффузионном барьерном слое (ДБС).
Рабочий электрод 175 может включать в себя ДБС, который представляет собой неотъемлемую часть слоя 275 реактивов или который представляет собой отдельный слой 290, такой как изображен на фиг.2A. Таким образом, ДБС может быть образован в виде сочетания реактив/ДБС на проводнике, в виде отдельного слоя на проводнике или в виде отдельного слоя на слое реактивов. Когда рабочий электрод 175 включает в себя отдельный ДБС 290, слой 275 реактивов может находиться или может не находиться на ДБС 290. Вместо этого, слой 275 реактивов может находиться на любой части сенсорной полоски 100, что позволяет реактиву растворяться в образце. Например, слой 175 реактивов может находиться на основании 110 или на крышке 120.
ДБС обеспечивает пористое пространство, обладающее внутренним объемом, где могут располагаться подлежащие измерению частицы и также могут фильтроваться красные клетки крови от поверхности проводника. Поры ДБС могут быть выбраны так, что подлежащие измерению частицы могут диффундировать в ДБС, в то время как физически более крупные составные части образца, такие как красные клетки крови, в основном исключаются. Хотя в обыкновенных сенсорных полосках для фильтрации красных клеток крови от поверхности рабочего электрода используются различные материалы, ДБС обеспечивает внутреннее пористое пространство для вмещения и изоляции части подлежащих измерению частиц из образца.
Когда слой 275 реактивов содержит водорастворимое связывающее вещество, любая часть связывающего вещества, которая не растворяется в образце до приложения возбуждения, может функционировать в качестве целого ДБС. Средняя начальная толщина сочетания ДБС/слой реактивов предпочтительно составляет менее чем 20 или 10 мкм и более предпочтительно менее чем 5 мкм. Желательная средняя начальная толщина сочетания ДБС/слой реактивов может быть выбрана для конкретной длительности возбуждения на основании того, когда скорость диффузии подлежащих измерению частиц от ДБС к поверхности проводника, такой как поверхность проводника 170 или поверхность поверхностного проводника 270 с фиг.2A, станет относительно постоянной. Сочетание ДБС/слой реактивов может иметь среднюю начальную толщину 2 мкм, 1 мкм, или меньше в сочетании с длительностью возбуждения, равной 0,25 секунд или менее.
Отдельный ДБС 290 может включать в себя любой материал, который обеспечивает желаемое пористое пространство, будучи частично или плохо растворимым в образце. Отдельный ДБС 290 может включать в себя связывающий реактив материал, в котором отсутствуют реактивы. Отдельный ДБС 290 может иметь среднюю начальную толщину от 1 до 15 мкм, и более предпочтительно от 2 до 5 мкм.
Фиг.2B изображает схематическое изображение биосенсорной системы 200, которая определяет концентрацию анализируемого вещества в образце, таком как биологическая жидкость. Биосенсорная система 200 включает в себя измерительное устройство 202, которое осуществляет способ анализа, и сенсорную полоску 204. Сенсорная полоска 204 может быть электрохимической сенсорной полоской, как изображено на фиг.1A, 1B и 2A, например. Измерительное устройство 202 может быть выполнено в виде настольного устройства, портативного или ручного устройства, или им подобного. Измерительное устройство 202 и сенсорная полоска 204 могут выполнять электрохимический анализ, оптический анализ, их сочетание, или им подобные. Биосенсорная система 200 может определять концентрации анализируемого вещества, включая такие анализируемые вещества как алкоголь, глюкозу, мочевую кислоту, лактат, холестерол, билирубин и т.п. в биологических образцах. Хотя приведена конкретная конфигурация, биосенсорная система 200 может иметь другие конфигурации, включая конфигурации с дополнительными компонентами.
Сенсорная полоска 204 имеет основание 206, которое образует емкость 208 для образца и канал 210 с отверстием 212. Ссылаясь на фиг.1A, канал 210 может быть общим с емкостью 208. Емкость 208 и канал 210 могут быть накрыты крышкой с отверстием. Емкость 208 образует частично закрытый объем (покрышка-зазор). Емкость 208 может содержать композицию, которая способствует удерживанию жидкого образца, такого как водонабухающие полимеры или пористые полимерные матрицы. Реактивы могут быть помещены в емкость 208 и/или канал 210. Композиция реактивов может включать в себя один или несколько ферментов, связывающих веществ, посредников и т.п. Реактивы могут включать в себя химический индикатор для оптической системы. Сенсорная полоска 204 может иметь другие конфигурации.
Сенсорная полоска 204 также может иметь интерфейс 214 образца. В электрохимической системе интерфейс 214 образца имеет проводники, соединенные, по меньшей мере, с двумя электродами, такими как рабочий электрод и противоэлектрод. Электроды могут быть расположены на поверхности основания 206, которое образует емкость 208. Интерфейс 214 образца может иметь другие электроды и/или проводники.
Измерительное устройство 202 включает в себя электросхему 216, соединенную с интерфейсом 218 сенсора и дисплеем 220. Электросхема 216 может включать в себя процессор 222, соединенный с генератором 224 сигнала, дополнительным датчиком 226 температуры и средой 228 для хранения. Электросхема 216 может иметь другие конфигурации, включая конфигурации с дополнительными компонентами.
Генератор 224 сигнала обеспечивает электрический входной сигнал в интерфейс 218 сенсора в ответ процессору 222. В оптических системах электрический входной сигнал можно использовать для операторного управления детектором и источником света в интерфейсе 218 сенсора. В электрохимических системах электрический входной сигнал может быть передан через интерфейс 218 сенсора к интерфейсу 214 образца для приложения электрического входного сигнала к емкости 208 и, таким образом, к образцу.
Электрический входной сигнал может быть потенциалом или током и может быть постоянным, переменным или их сочетанием, таким как, когда сигнал переменного тока прикладывают со сдвигом сигнала постоянного тока. Электрический входной сигнал может быть приложен в виде единичного импульса или множественных импульсов, последовательности или циклов. Также генератор 224 сигнала может записывать выходной сигнал из интерфейса 218 сенсора в качестве генератора-самописца.
Носитель 228 для хранения может быть магнитной, оптической или полупроводниковой памятью, другим считываемым компьютерным устройством хранения данных или им подобным. Носитель 228 для хранения может представлять собой постоянное запоминающее устройство или съемное запоминающее устройство, такое как карта памяти.
Процессор 222 может выполнять анализ анализируемого вещества и обработку данных с использованием считываемого кода компьютерного программного обеспечения и данных, хранящихся в носителе 228 для хранения. Процессор 222 может начинать анализ анализируемого вещества в ответ на присутствие сенсорной полоски 204 в интерфейсе сенсора 218, приложение образца к сенсорной полоске 204, в ответ на входной сигнал пользователя или подобного. Процессор 222 может управлять генератором 224 сигнала с целью обеспечения электрическим входным сигналом в интерфейсе 218 сенсора. Процессор 222 может принимать температуру образца с датчика 226 температуры, если он установлен.
Процессор 222 принимает выходной сигнал из интерфейса 218 сенсора. Выходной сигнал образован в ответ на окислительно-восстановительную реакцию анализируемого вещества в образце. Выходной сигнал может быть образован с использованием оптической системы, электрохимической системы или им подобной. Процессор 222 может определять концентрацию анализируемого вещества в образце по одному или нескольким выходным сигналам с использованием корреляционного уравнения. Результаты анализа анализируемого вещества выводятся на дисплей 220 и могут храниться на носителе 228 для хранения.
Корреляционные уравнения, связывающие концентрации анализируемого вещества и выходные сигналы, могут быть представлены графически, математически, в их сочетании или подобным. Корреляционные уравнения могут быть представлены с помощью таблицы присвоения номера программы (ПНП), другой таблицы соответствия, или подобной, которая хранится в носителе 228 для хранения. Инструкции относительно выполнения анализа могут предоставляться посредством кода считываемого компьютером программного обеспечения, хранящегося на носителе 228 для хранения. Код может быть объектным кодом или любым другим кодом, описывающим или управляющим функциональность, описываемую в настоящем документе. Данные об анализе анализируемого вещества могут быть подвергнуты одной или нескольким обработкам данных в процессоре 222, включая определение скорости затухания, констант K , наклонов, перерывов и/или температуры образца.
В электрохимических системах интерфейс 218 сенсора электрически или оптически соединен с интерфейсом 214 образца. Электрическое соединение включает в себя передачу входного и/или выходного сигналов между постоянными в интерфейсе 218 сенсора и проводниками в интерфейсе 214 образца. Электрическое соединение может осуществляться, например, беспроводным путем или через физический контакт. Интерфейс 218 сенсора передает электрический входной сигнал от генератора 224 сигнала через контакты к коннекторам в интерфейсе 214 образца. Интерфейс 218 сенсора также передает выходной сигнал от образца через контакты в процессор 222 и/или генератор 224 сигнала.
Оптическое соединение включает в себя передачу света между оптическим порталом в интерфейсе 202 образца и детектором в интерфейсе 208 сенсора. Оптическое соединение также включает в себя передачу света между оптическим порталом в интерфейсе 202 образца и источником света в интерфейсе 208 сенсора.
Дисплей 220 может быть аналоговым или цифровым. Дисплей 220 может быть ЖК, светодиодным или вакуумным флуоресцентным дисплеем, выполненным с возможностью отображения числовых показаний прибора.
В употреблении жидкий образец для анализа переносят в емкость 208 посредством введения жидкости в отверстие 212. Жидкий образец протекает через канал 210 и в емкость 208, вытесняя предварительно содержавшийся воздух. Жидкий образец химически взаимодействует с реактивами, расположенными в канале 210 и/или емкости 208. Процессор 222 направляет генератору 224 сигнала указание обеспечить входной сигнал в интерфейс 218 сенсора. В оптической системе интерфейс 218 сенсора управляет детектором и источником света в ответ на входной сигнал. В электрохимических системах интерфейс 218 сенсора обеспечивает входной сигнал к образцу через область контакта с образцом 214. Процессор 222 принимает выходной сигнал, образованный в ответ на окислительно-восстановительную реакцию анализируемого вещества в образце. Процессор 222 определяет концентрацию анализируемого вещества в образце с использованием одного или нескольких корреляционных уравнений. Определившаяся концентрация анализируемого вещества может быть отображена и/или сохранена для дальнейшего использования.
Фиг.3 представляет блок-схему электрохимического анализа 300 для определения присутствия и необязательно концентрации анализируемого вещества 322 в образце 312. На этапе 310 образец 312 вводят в сенсорную полоску 314, такую как сенсорная полоска, изображенная на фиг.1A, 1B и 2A. Слои реактивов, такие как 275 и/или 285, изображенные на фиг.2A, начинают растворяться в образце 312, таким образом, делая возможной реакцию.
На этапе 315 начальный инкубационный период 317 дает реактивам возможность прореагировать с образцом 312 до подачи входного сигнала. Предпочтительно, инкубационный период 317 может составлять от 0,1 до 10 секунд, более предпочтительно от 0,1 до 8 секунд или от 0,5 до 4 секунд. В настоящее время более предпочтительным для инкубационного периода 317 является от 0,1 до 1 секунды. Можно использовать другие инкубационные периоды.
В ходе инкубационного периода 317 часть анализируемого вещества 322, присутствующая в образце 312, химически или биохимически окисляется или восстанавливается на этапе 320 в ходе окислительно-восстановительной реакции для образования подлежащих измерению частиц 332. Подлежащие измерению частицы 332 могут представлять собой окисленное или восстановленное анализируемое вещество 322 или посредник. При окислении или восстановлении электроны могут переноситься к или от анализируемого вещества 322 и к или от подлежащих измерению частиц 332 на этапе 330. Например, посредник может быть восстановлен для образования подлежащих измерению частиц 332 через окисление анализируемого вещества 322. Предпочтительно, чтобы подлежащие измерению частицы 332, образованные в ходе инкубационного периода 317, электрохимически не возбуждались в ходе инкубационного периода 317.
На этапе 340 подлежащие измерению частицы 332 электрохимически возбуждаются (окисленные или восстановленные). Таким образом, электроны избирательно переносятся между анализируемым веществом 322 и рабочим электродом сенсорной полоски 314. Длительность возбуждения 340 может быть от 0,1 до 5 секунд или от 0,1 до 1 секунды. Возбуждение 340 может повторяться.
На этапе 350 ток, образованный в ходе возбуждения на этапе 340, может быть зарегистрирован в виде функции от времени. Если множественные возбуждения от 340 подаются на сенсорную полоску 314, на этапе 350 может быть зарегистрирован один или несколько токов, образующихся в результате возбуждений от 340. Токи могут быть зарегистрированы с помощью измерительного устройства.
На этапе 360 образец подвергается релаксации. Предпочтительно, чтобы ток не регистрировался в ходе релаксации 360. Релаксация 360 может следовать после каждого из возбуждений от 340, когда прикладываются множественные возбуждения. В ходе релаксации 360 ток, присутствующий в ходе возбуждения 340, в значительной мере снижается, по меньшей мере, на половину, предпочтительно порядка амплитуды, и более предпочтительно до нуля. Предпочтительно, состояние с нулевым током обеспечивается с помощью размыкания цепи или другого способа, известного специалистам в данной области для обеспечения практически нулевого протекания тока. Для обеспечения размыкания цепи измерительное устройство может размыкать цепь через сенсорную полоску 314. Если обеспечено состояние с нулевым током, релаксацию 360 можно считать прерывистым инкубационным периодом.
Релаксация 360 может длиться, по меньшей мере, 0,1 или, по меньшей мере, 0,5 секунд. Релаксация 360 может длиться от 0,1 до 3 секунд, от 0,2 до 2 секунд, или от 0,5 до 1 секунды. Можно использовать другие длительности релаксации.
На этапе 370 один или несколько зарегистрированных токов и значений времени из этапа 350 могут быть проанализированы для определения присутствия и/или концентрации анализируемого вещества 322 в образце 312. Предпочтительно, концентрация анализируемого вещества, которую определили по измерению тока, проведенному не позднее 2 секунд или 1 секунды от начала возбуждения, приложенного в начале. Более предпочтительны множественные короткие возбуждения, объединенные с измерением тока, проведенным в первые 2 секунды, 1 секунду или менее от начала приложения начального входного сигнала для определения концентрации анализируемого вещества в образце. Зарегистрированный ток и значения времени могут быть скоррелированы с концентрацией анализируемого вещества 322 в образце 312 с использованием одного или нескольких корреляционных уравнений.
Возбуждение 340 и релаксация 360 составляют единый рабочий цикл. Предпочтительно, входной сигнал, приложенный к сенсорной полоске 314, включает в себя, по меньшей мере, 2, 4 или 6 рабочих циклов, приложенных в течение независимо выбранного 3-, 5-, 7- или 9-секундного временного интервала. Таким образом, начиная с начального приложения входного сигнала, общее время, требуемое для частей возбуждения 340 и релаксации 360 электрохимического анализа 300, может быть не более чем 3, не более чем 5, не более чем 7 или не более чем 9 секунд. Рабочие циклы могут применяться в ходе временных интервалов от 1 до 3 секунд. От 2 до 6 рабочих циклов могут применяться в течение 8 секунд или менее. От 2 до 4 рабочих циклов могут применяться в течение от 3 до 6 секунд. Можно использовать другие интервалы времени.
Для непрерывного наблюдения, которое можно использовать с имплантированными или частично имплантированными сенсорами, рабочие циклы можно повторять непрерывно. Энергия, требуемая для работы системы, может быть уменьшена и срок службы системы может быть увеличен по отношению к способам без релаксаций. Кроме того, применение множественных рабочих циклов может быть разделено более длинными временными интервалами, например 5 минут или более.
Амперометрические сенсорные системы прикладывают потенциал (напряжение) к электродам для возбуждения подлежащих измерению частиц в то время как наблюдают за током (силой тока). Обыкновенные амперометрические сенсорные системы могут поддерживать потенциал возбуждения, в то время как непрерывно измеряется ток, например, от 5 до 10 секунд. В отличие от обыкновенных способов, входные сигналы, используемые в электрохимическом анализе 300, могут замещать непрерывные, продолжительные возбуждения множественными возбуждениями и релаксациями относительно короткой длительности. Более подробное описание множественных возбуждений и релаксаций или «стробированной» импульсной последовательности, приложенной в виде входных сигналов, может быть найдено в WO 2007/013915, поданной 19 июля 2006 года, озаглавленной «Gated Amperometry».
Когда используют кратковременную начальную инкубацию и/или стробированные входные сигналы согласно настоящему изобретению, в результате, могут быть кратковременные или некоттрелловские затухания тока. Не полагаясь на коттрелловскую постоянную затухания, равную -0,5 для определения концентрации анализируемого вещества 322 в образце 312, возможно завершение электрохимического анализа 300 с использованием кратковременных затуханий в течение 8 секунд или менее, в течение 4 секунд или менее, или более предпочтительно, в течение 3 секунд или менее. Электрохимический анализ 300 может быть выполнен за 2 секунды или менее.
Электрохимический анализ 300 может завершаться приблизительно от 0,5 приблизительно до 3 секунд. Электрохимический анализ 300, использующий кратковременные затухания, может быть завершен при использовании других временных интервалов.
Фиг.4A представляет емкость 400 для образца, ограниченную нижней поверхностью 402 электрода и верхней крышкой 403. Также представлена воображаемая верхняя граница 405 слоя реактивов. Таким образом, пространство между поверхностью 402 электрода и воображаемой верхней границей 405 представляет образец, содержащийся в слое реактивов. Сходным образом, пространство между воображаемой верхней границей 405 и верхней крышкой 403 представляет образец над слоем реактивов. Ось X представляет расстояние от поверхности электрода, в то время как ось Y представляет концентрацию подлежащих измерению частиц в образце, образованных в окислительно-восстановительной реакции анализируемого вещества. На чертеже упущен эффект разделения анализируемого вещества между ДБС и жидким образцом в оставшейся части емкости 400.
Профиль 410 концентрации представляет, что будет наблюдаться сразу после введения образца в полоску, тогда как профиль 420 концентрации представляет, что будет наблюдаться после относительно длинного инкубационного периода. Профиль 410 концентрации представляет кратковременное состояние, тогда как профиль 420 концентрации представляет коттрелловское состояние. Множественные кратковременные состояния могут существовать между кратковременным профилем 410 концентрации и коттрелловским профилем 420 концентрации.
Фиг.4B показывает формирование различных профилей концентрации, когда проходят инкубации длительностью от t 1 до t 5 перед подачей входного сигнала на электроды. Профиль концентрации при t 5 представляет инкубационный период от 15 до 30 секунд, изображает практически постоянное распределение концентрации подлежащих измерению частиц на всем протяжении образца, которое будет обеспечивать коттрелловское затухание, обладающее постоянной затухания -0,5. Таким образом, площадь под линией t 5 и связанная концентрация подлежащих измерению частиц практически не меняются вплоть до относительно большого расстояния от поверхности 402 электрода.
В отличие от линии t 5, линия t 4 имеет инкубационный период от 1 до 12 секунд и переменное распределение концентрации подлежащих измерению частиц в образце. Линия t 4 имеет более медленные кратковременные постоянные затухания от -0,30 (1 секунда) до -0,48 (12 секунд). Таким образом, площадь под линией t 4 и лежащая в основе концентрация подлежащих измерению частиц подвергается значительному изменению от поверхности 402 электрода до верхней крышки 403 емкости 400 - таким образом, является переменной.
Так как инкубационный период дополнительно снижен от 0,4 до 1 секунды в t 3 или до от 0,1 до 0,3 секунды в t 2, кратковременные постоянные затухания могут быть в диапазоне от -0,25 до -0,3 для t 3 и от -0,15 до -0,25 для t 2 соответственно. Затухание t 1 представляет второй инкубационный период от 0,01 до 0,1 секунды, который может иметь кратковременную постоянную затухания -0,15 или менее. Так как инкубационный период уменьшен от t 4 до t 1, площадь под линиями и связанная концентрация подлежащих измерению частиц между поверхностью 402 электрода и верхней крышкой 403 емкости 400 становится в большей степени переменной.
Из-за низкой концентрации подлежащих измерению частиц у поверхности 402 электрода, чем в остающейся части емкости 400, например, представленной профилями переменного распределения концентрации от t 1 до t 4 на фиг.4B, скорость затухания тока может быть ниже, чем постоянная затухания -0,5, требуемая для коттрелловского затухания. Это более медленное затухание может быть свойственным большой концентрации подлежащих измерению частиц, отдаленных от поверхности 402 электрода, достигающих поверхности электрода быстрее, чем если бы подлежащие измерению частицы были распределены равномерно на всем протяжении емкости 400 для образца. Сходным образом, более высокие скорости затухания могут быть получены, когда более высокая концентрация подлежащих измерению частиц присутствует у поверхности 402 электрода, чем в оставшейся части в емкости для образца 400.
Фиг.4C представляет зависимость между концентрациями подлежащих измерению частиц в емкости 400 и постоянными затухания тока. Профили 430 и 440 концентрации подлежащих измерению частиц имеют более низкие и более высокие скорости затухания соответственно, чем 420, который соответствует коттрелловской постоянной затухания -0,5. Для профиля 430 концентрации, обладающего постоянной затухания менее чем коттрелловская постоянная затухания -0,5, например -0,3, скорость затухания тока будет ниже, чем наблюдаемая для коттрелловской системы. Сходным образом, для профиля 440 концентрации, обладающего постоянной затухания выше, чем коттрелловская постоянная затухания -0,5, например -0,7, скорость затухания тока будет выше, чем наблюдаемая для коттрелловской системы. Таким образом, в сравнении с коттрелловской постоянной затухания -0,5, представленной с помощью 420, кратковременные постоянные 430, 440 затухания отражают переменные распределения концентрации подлежащих измерению частиц в емкости 400.
Когда для создания коттрелловского затухания используются длинные инкубационные периоды, количество подлежащих измерению частиц, образованных в ходе измерительного возбуждения, мало по сравнению с количеством подлежащих измерению частиц, образованных в ходе предварительного инкубационного периода. Таким образом, в отличие от профиля 420 концентрации, представляющего полное окислительно-восстановительное превращение анализируемого вещества в подлежащие измерению частицы до приложения входного сигнала, профили 430, 440 концентрации представляют неполное превращение. Кроме того, любые изменения в скорости диффузии подлежащих измерению частиц к электроду от конвекции или других путей также малы по отношению к количеству подлежащих измерению частиц, образованных в ходе инкубационного периода. Таким образом, длинные инкубационные периоды, главным образом, негативно действуют, что будет изменять коттрелловскую постоянную затухания -0,5.
Для сравнения, когда используются короткие инкубационные периоды, например 12 секунд, 10 секунд и короче, количество подлежащих измерению частиц, образованных в ходе измерительного возбуждения и любое изменение в скорости диффузии от процессов, отличных от диффузии, может обеспечивать реальную скорость затухания, которая ниже, чем коттрелловское значение -0,5. Этот процесс затухания можно описать с помощью следующего уравнения (2) нормализованного тока:
f(t) = t-a+b+c (2),
где a представляет собой часть постоянной затухания из подлежащих измерению частиц, образованных в ходе инкубационного периода, b представляет собой часть постоянной затухания из подлежащих измерению частиц, образованных в ходе измерительного возбуждения, и c представляет собой часть постоянной затухания, возникающую из изменений в распределении концентрации подлежащих измерению частиц в емкости для образца. Отрицательные значения b и c имеют следствием увеличение измеренной концентрации подлежащих измерению частиц, тогда как положительные значения b и c имеют следствием уменьшение измеренной концентрации подлежащих измерению частиц. Таким образом, если или a, или b не равно нулю, то будет происходить отклонение от величины затухания. Так как коттрелловское затухание обеспечивается значением a -0,5, значительный вклад b или c обеспечивает кратковременную постоянную затухания. В уравнении (2) член a управляет постоянной затухания, полученной из профиля 420 концентрации, тогда как член b делает значительный вклад в постоянную затухания, полученную из профилей 430 и 440 концентрации, где входной сигнал приложен до завершения окислительно-восстановительного превращения анализируемого вещества.
Уравнение (2) устанавливает то, что постоянная затухания системы может изменяться со временем в ответ на то, какой из этих основных факторов влияет на затухание тока во время измерения. Например, более длинные инкубационные периоды увеличивают а , при этом уменьшая b , потому что в ходе инкубационного периода больше анализируемого вещества превращено в подлежащие измерению частицы, в образце остается меньше анализируемого вещества для превращения в подлежащие измерению частицы в ходе возбуждения.
Окислительно-восстановительное превращение анализируемого вещества в подлежащие измерению частицы происходит в гидратированных слоях реактивов. Так как более толстые слои реактивов требуют более длительной гидратации, более толстые слои реактивов будут обеспечивать увеличение в члене b по отношению к члену a , если входной сигнал приложен до того, как слой реактивов будет гидратирован. Коттрелловское затухание не наблюдается прежде, чем слой реактивов будет гидратирован из-за вклада подлежащих измерению частиц, образованных в ходе измерительного возбуждения, в постоянную затухания, член b уравнения (2). Это было определено в колонке 4, строках 58-59 '069 патента, которые раскрывают, что неполное смачивание реактива приводит к неспособности системы придерживаться кривой коттрелловского затухания, что приводит к получению неточного значения концентрации анализируемого вещества. Таким образом, кратковременные постоянные затухания могут быть получены из частично гидратированных слоев реактивов, полученных в результате относительно коротких начальных инкубационных периодов.
Емкости сенсорной полоски, включающие в себя практически постоянное распределение концентрации подлежащих измерению частиц, могут снижать любое влияние на постоянную затухания, свойственное c . Член c также может влиять на постоянную затухания, если длительность возбуждения слишком длинная для объема образца, что приводит к быстрому снижению концентрации подлежащих измерению частиц, так как увеличивается расстояние от поверхности электрода. Использование короткого возбуждения или множественных коротких возбуждений, объединенных с одной или несколькими релаксациями, может способствовать снижению влияния члена c на постоянную затухания.
Например, патент '069 описывает систему, которая обеспечивает коттрелловскую постоянную затухания -0,5, когда 160-секундный начальный инкубационный период объединен с 50 мкл емкостью для образца. Для этой системы, если инкубационный период был значительно укорочен, член b уравнения (2) будет увеличиваться, таким образом, обеспечивая некоттрелловское затухание. Сходным образом, если объем емкости был значительно уменьшен, некоттрелловское затухание будет следствием увеличения члена c уравнения (2).
Фиг.5 изображает постоянные затухания, полученные от сенсорных полосок, обладающих объемом емкости примерно 3,5 мкл и расстоянием от электрода до крышки примерно 250 мкм после изменения инкубационных периодов для образцов цельной крови, содержащих 50, 100, 200 или 400 мг/дл глюкозы. Скорость затухания увеличилась с увеличением времени инкубации; однако коттрелловская постоянная затухания -0,5 не была получена в течение 6-секундного инкубационного периода. Таким образом, система обеспечивает кратковременные затухания при этих обстоятельствах.
Нижеследующая таблица 1 предоставляет постоянные затухания для 1-6-секундных инкубационных периодов с фиг.5 и предоставляет спрогнозированные постоянные для 10- и 15-секундных инкубационных периодов. Спрогнозированная постоянная затухания также предоставлена для 20-секундного инкубационного периода.
В каждом случае входной сигнал включает в себя начальное возбуждение, равное четырем секундам, с последующим прерывистым инкубационным периодом переменной длительности с размыканием цепи, и измерительное возбуждение, равное одной секунде, в ходе которого регистрируется ток. Сенсорная система не достигла условия коттрелловского затухания в ходе любого из инкубационных периодов от одной до шести секунд. Не прогнозируется, что сенсорная система достигнет условия коттрелловского затухания в течение двенадцати секунд даже при низкой концентрации глюкозы 50 мг/дл. Предпочтительные кратковременные постоянные затухания составляют от -0,001 до -0,48 и от -0,52 до -1. Более предпочтительные кратковременные постоянные затухания составляют не более чем -0,45, не более чем -0,35 и не более чем -0,3. Можно использовать другие кратковременные постоянные затухания.
Фиг.6A-6C изображают профили постоянного тока, полученные от трех сенсорных полосок, каждая из которых обладает различной средней начальной толщиной реакционного слоя при начальных инкубационных периодах, равных 0,125, 0,5, 1, 2, 4, и 6 секундам. Емкость для образца каждой полоски составляла примерно 1 мкл. График на фиг.6A был получен от множества сенсорных полосок, обладающих реакционными слоями со средней начальной толщиной приблизительно от 15 мкм приблизительно до 20 мкм («толстая»). Графики на фиг.6B и 6C были получены от множества сенсорных полосок, обладающих реакционными слоями со средней начальной толщиной от 10 мкм до 15 мкм («средняя») и от 1 мкм до 2 мкм («тонкая») соответственно. Можно использовать другие толщины.
Чертежи устанавливают взаимосвязь между временем инкубации, толщиной слоя реактивов и связанной скоростью гидратации слоя. Более толстые слои реактивов требуют более длительного времени для гидратации слоя реактивов, и чем большее время требуется для гидратации слоя реактивов, тем более длительное время нужно, прежде чем затухание тока достигнет точки непрерывного уменьшения. Значения тока, полученные от уменьшающихся кратковременных затуханий, являются предпочтительными для коррелирования с концентрацией анализируемого вещества в образце.
Для полосок с толстым слоем на фиг.6A непрерывно уменьшающиеся затухания тока были получены после инкубационного периода, равного примерно 4 секундам или более. Однако для инкубационных периодов, равных примерно 2 секундам и менее, непрерывно уменьшающиеся затухания постоянного тока не были получены для полосок с толстым слоем до тех пор, пока не был приложен входной сигнал длительностью примерно 2 секунды или более.
На фиг.6B для сенсорных полосок со средней толщиной слоя реактивов непрерывно уменьшающиеся затухания тока были получены после инкубационного периода, равного примерно 2 секундам или более. Для инкубационных периодов, равных примерно 1 секунде и менее, входной сигнал, равный примерно 2 секундам или более, обеспечивает непрерывно уменьшающиеся затухания тока.
На фиг.6C для сенсорных полосок с тонкими слоями реактивов непрерывно уменьшающиеся затухания тока были получены после инкубационного периода, равного примерно 1 секунде или более. Для инкубационных периодов, равных примерно 0,5 секунды и менее, входной сигнал, равный примерно 1 секунде или более, обеспечивает непрерывно уменьшающиеся затухания тока. Таким образом, более тонкие слои реактивов могут быть объединены с более короткими инкубационными периодами для обеспечения более короткого общего времени анализа, тогда как более толстые слои реактивов могут требовать большей длительности инкубационных периодов и/или входных сигналов.
Фиг.7A-7B изображают натуральные логарифмы тока по времени для образцов цельной крови, содержащих 100 или 300 мг/дл глюкозы при 40% гематокрите, полученные после 6-секундного начального инкубационного периода. Объемы емкости для образца и начальная средняя толщина слоя реактивов были как на вышеупомянутых фиг.6A-6C. Графики были построены на основе значений тока, полученных в ходе первых 5 секунд 10-секундного возбуждения, где член a уравнения (2) преобладает над постоянной затухания. Каждая из наблюдаемых постоянных затухания - графики наклонов ln(постоянный ток, нА) к ln(время, с) - отличаются от постоянной коттрелловского затухания -0,5, обладают кратковременными постоянными затухания в диапазоне примерно от -0,35 приблизительно до - 0,45. Таким образом, даже при самом длинном начальном инкубационном периоде, равном 6 секундам, коттрелловское затухание не наблюдалось.
Фиг.8A-8C представляют собой профили затухания тока 0,25-секундного начального инкубационного периода с последующим стробированным входным сигналом, включающим в себя 0,5-секундные возбуждения и 0,25-секундные релаксации для обеспечения длительности рабочего цикла, равной 0,75 секунды. Для анализа образцов цельной крови, содержащих 50, 100 или 400 мг/дл глюкозы при 40% гематокрите, были использованы сенсорные полоски как тонкие, так и со средней толщиной слоя реактивов, обладающие объемом емкости для образца, равным примерно 1 мкл. Непрерывно уменьшающиеся затухания тока, которые могут коррелировать с концентрацией анализируемого вещества в образце 50 мг/дл, были получены для тонкого слоя реактивов в течение 0,75 секунды, таким образом, в ходе первого возбуждения. Для более толстого промежуточного слоя реактивов непрерывно уменьшающиеся затухания тока были получены в течение 3 секунд, таким образом, в ходе третьего возбуждения.
Фиг.8D представляет собой калибровочный график, полученный посредством нанесения конечных точек токов ( p1 , p2 , p3 ) первых трех возбуждений, полученных от сенсорной полоски с тонким слоем реактивов, как изображено на фиг.8A-8C. Чертеж устанавливает то, что значения тока, полученные после очень коротких инкубационных периодов, равных 0,25 секунды, в соответствии с настоящим изобретением, могут быть точно скоррелированы ( R 2 = 0,999) с действительной концентрацией глюкозы в плазме из образцов цельной крови.
Фиг.8E представляет собой калибровочный график, полученный посредством нанесения конечных точек токов ( p4 , p5 , p6 ) возбуждений 4, 5 и 6, полученных от сенсорных полосок, обладающих средней толщиной слоя реактивов, как изображено на фиг.8A-8C. Чертеж устанавливает то, что значения тока, полученные после очень короткого 0,25-секундного начального инкубационного периода и множества рабочих циклов, включающих 0,5-секундные возбуждения и 0,25-секундные релаксации, в соответствии с настоящим изобретением, могут быть точно скоррелированы ( R 2 = 0,99) с действительной концентрацией глюкозы в плазме из образцов цельной крови.
Для обеспечения ясного и непротиворечивого понимания подробного описания и формулы изобретения этой заявки предоставлены следующие определения.
«Образец» представляет собой композицию, которая может содержать неизвестное количество анализируемого вещества. Образец может быть водным, например цельной кровью, мочой, слюной, или производным, например экстрактом, раствором, фильтратом или восстановленным осадком.
«Инкубационный период» представляет собой отрезок времени, за которое образец взаимодействует с реактивами, прежде чем будет приложено возбуждение, например, до приложения первого возбуждения и/или время между возбуждениями, если входной сигнал содержит множественные возбуждения.
«Подлежащие измерению частицы» представляют собой любые электрохимически активные частицы, которые могут быть окислены или восстановлены при соответствующем потенциале на поверхности электрода.
«Оксидоредуктаза» облегчает окисление или восстановление анализируемого вещества или биологического субстрата. См., например, «Oxford Dictionary of Biochemistry» и «Molecular Biology», Revised Edition, A.D. Smith, Ed., New York: Oxford University Press (1997) стр.161, 476, 477 и 560.
Несмотря на то, что были описаны различные варианты осуществления изобретения, специалистам в данной области будет ясно, что другие варианты осуществления и реализации возможны в рамках объема изобретения.
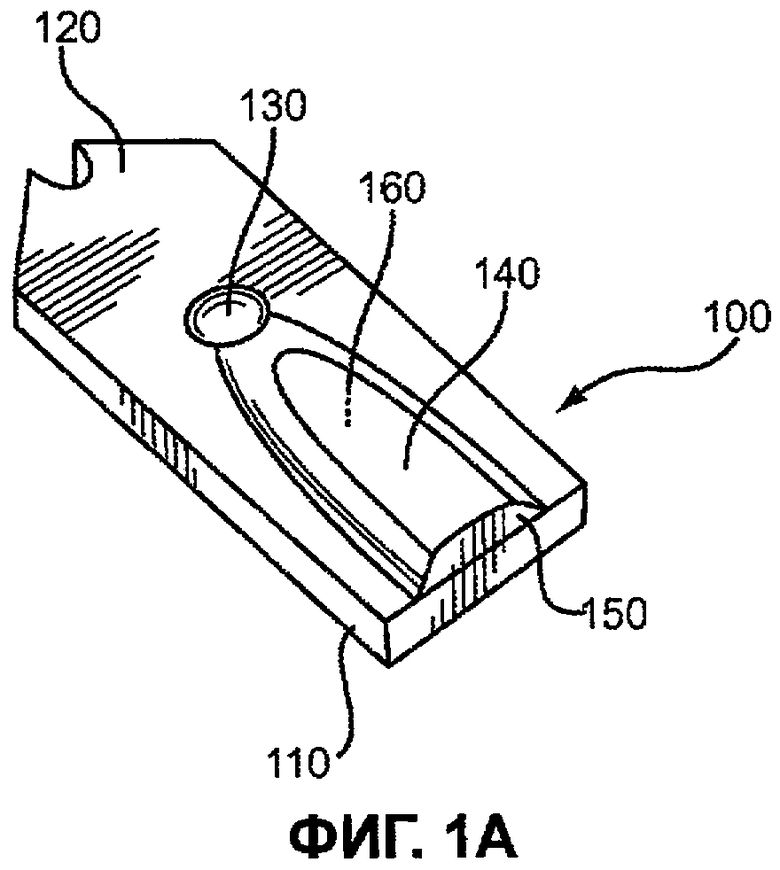
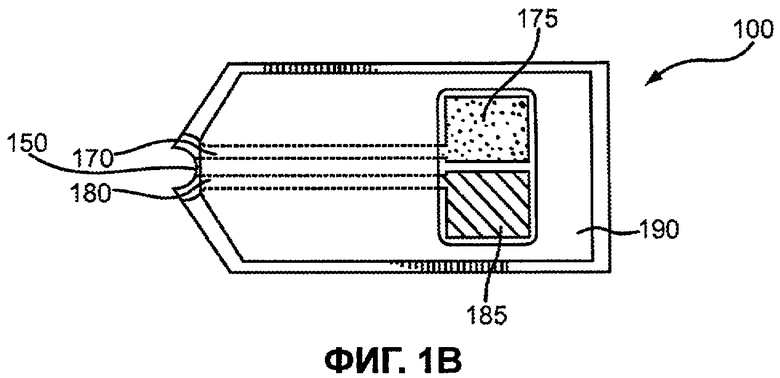
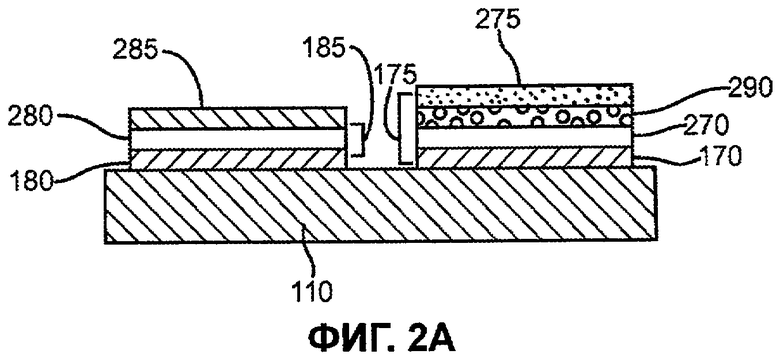
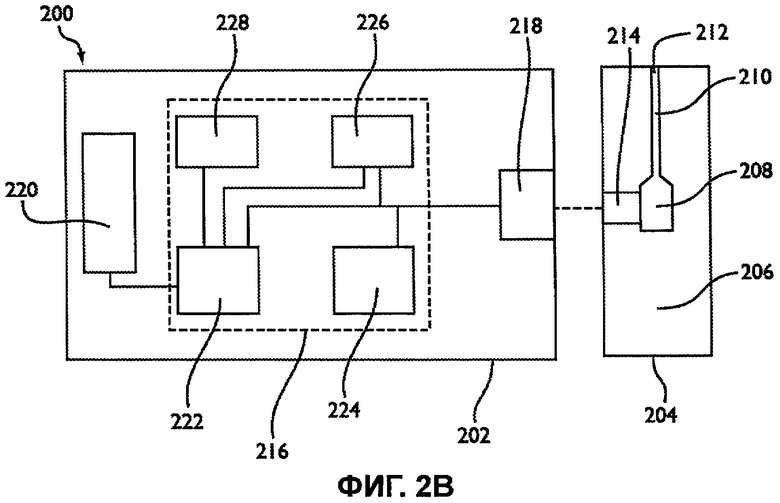
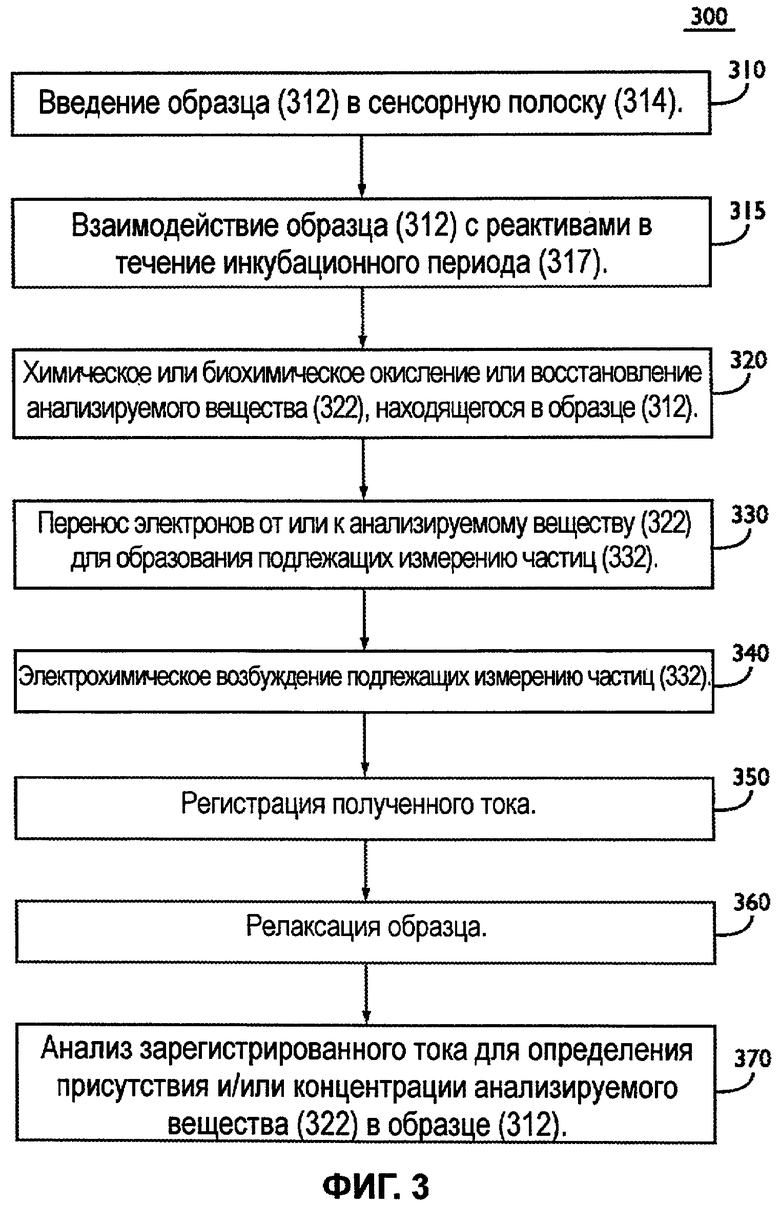
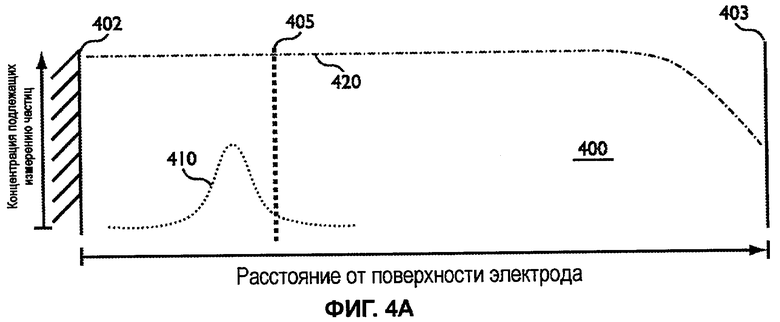
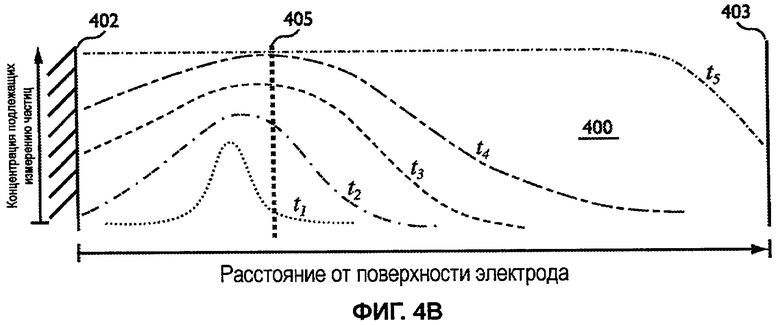
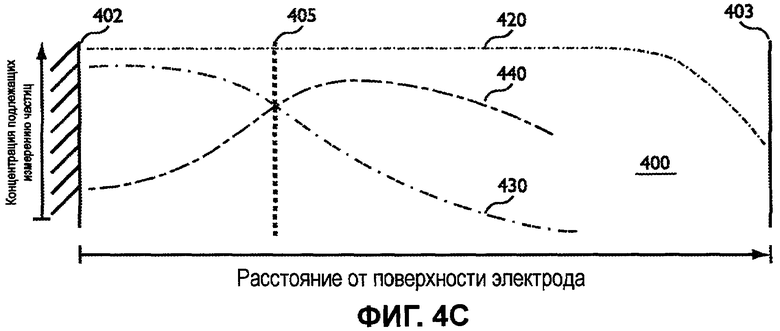
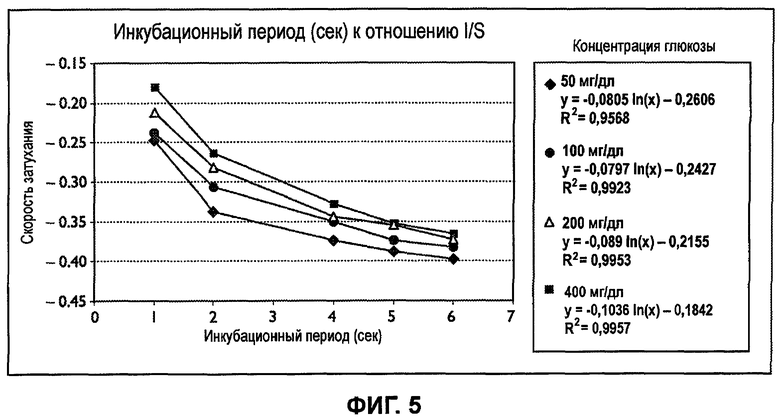
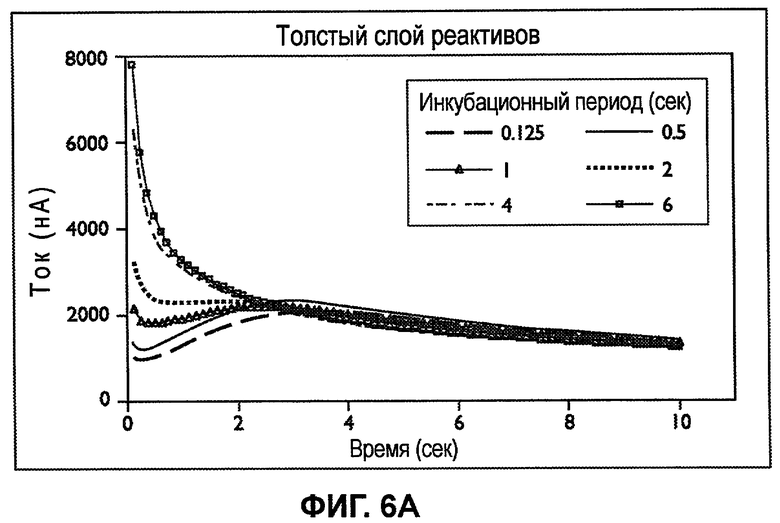
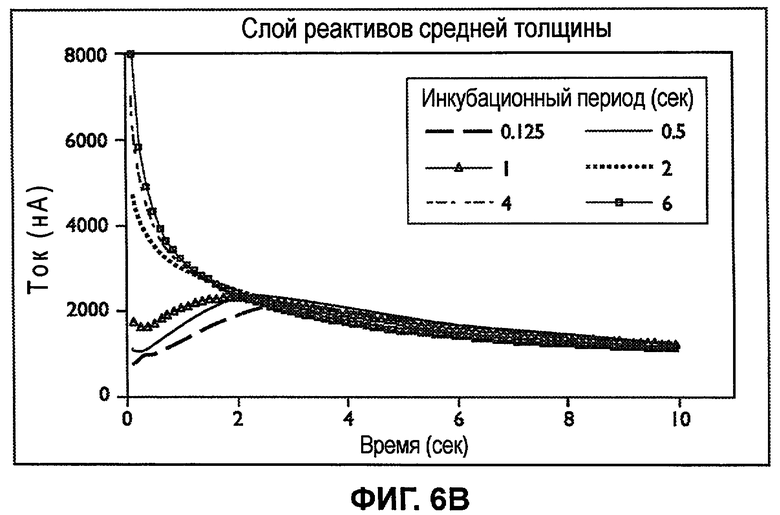
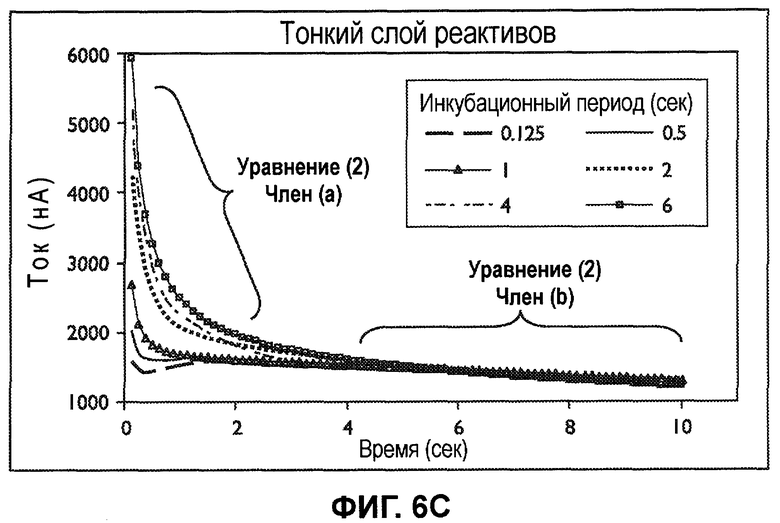
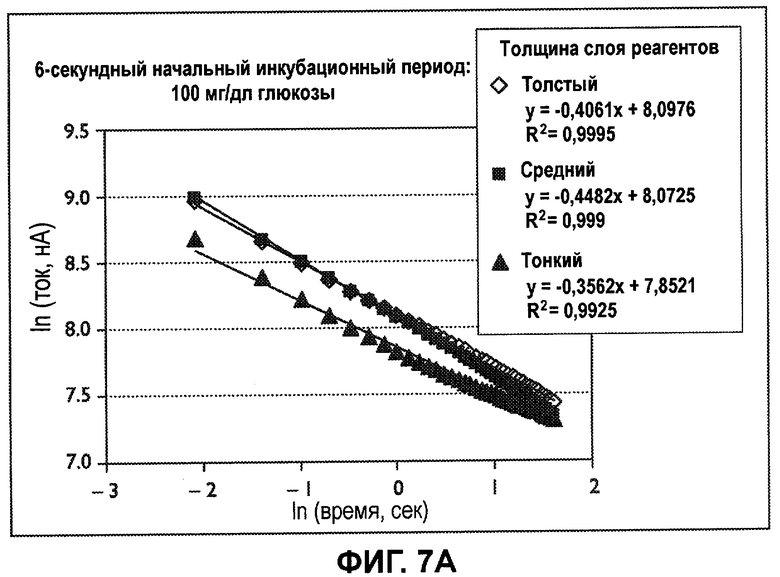
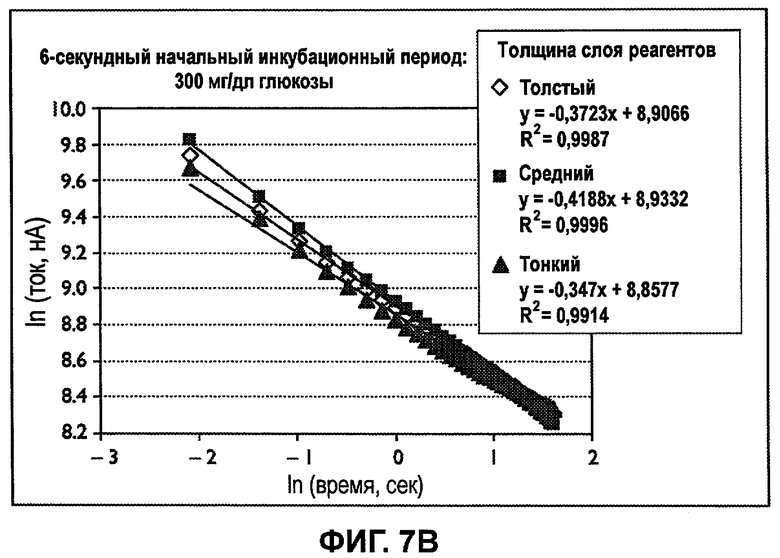
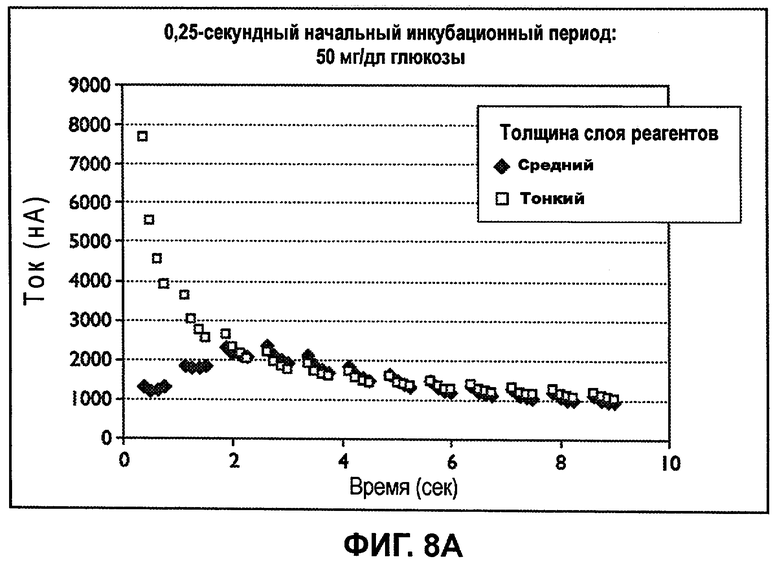
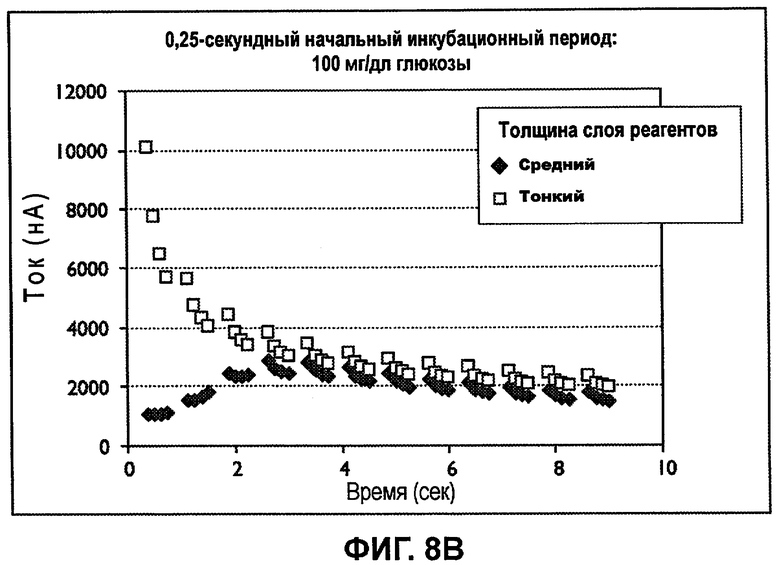
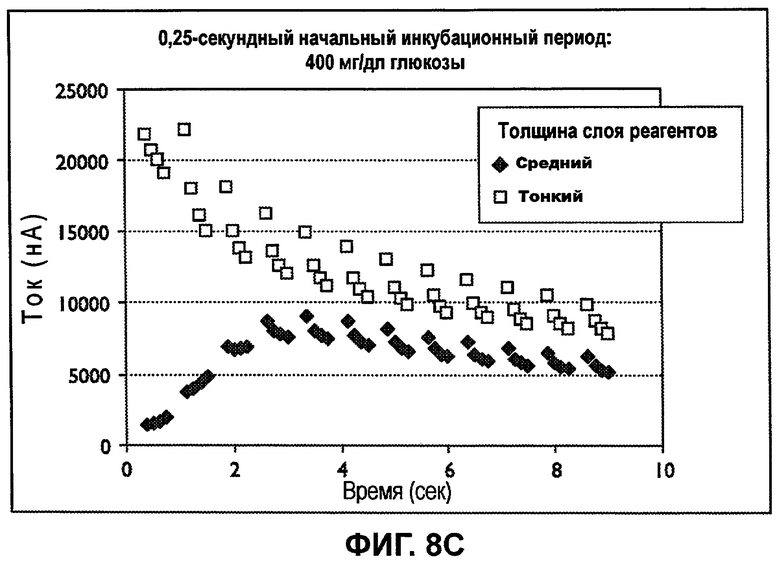
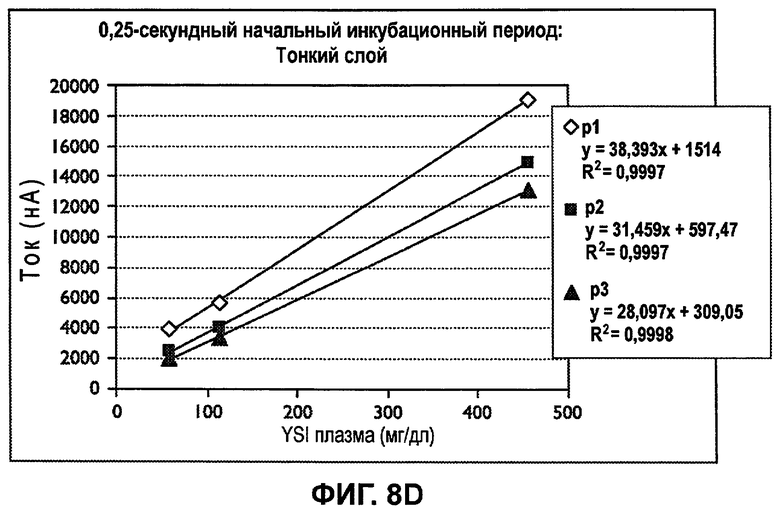
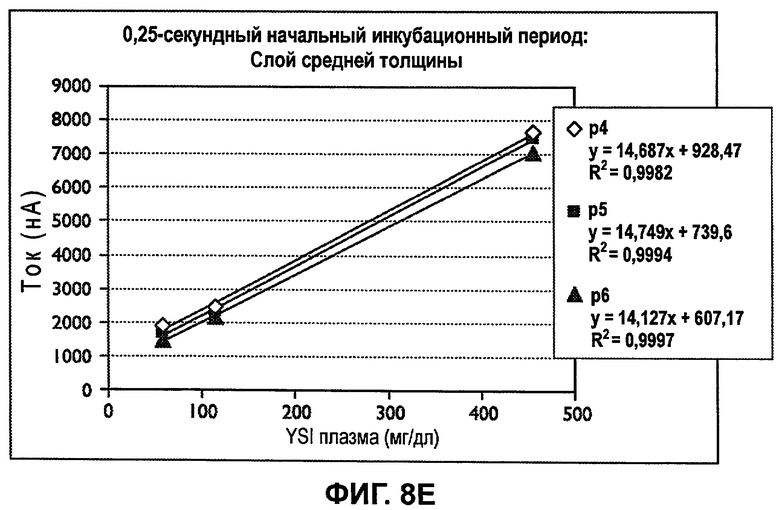
Изобретение относится к области биофизики. Сущность способов определения концентрации анализируемого вещества в образце заключается в том, что определяют концентрацию анализируемого вещества с использованием электрохимического процесса без коттрелловского затухания. Вводят образец в сенсорную полоску, прикладывают сигнал к образцу после инкубационного периода, равного не более чем 8 секундам, генерируют сигнал, обладающий кратковременным затуханием, в ответ на окислительно-восстановительную реакцию подлежащих измерению частиц, причем подлежащие измерению частицы образованы в ходе окислительно-восстановительной реакции части анализируемого вещества в образце. Далее определяют концентрацию анализируемого вещества по кратковременному затуханию сгенерированного сигнала. В другом варианте осуществления способа определения концентрации анализируемого вещества в образце заключается в том, что прикладывают сигнал к образцу после инкубационного периода не более 8 секунд, причем сигнал включает в себя, по меньшей мере, три возбуждения, каждое возбуждение имеет длительность от 0,1 до 5 секунд. Использование заявленного изобретения позволяет более быстро определить концентрацию анализируемого вещества по кратковременному затуханию. 2 н. и 23 з.п. ф-лы, 1 табл., 8 ил.
1. Способ определения концентрации анализируемого вещества в образце, содержащий этапы, на которых:
вводят образец в сенсорную полоску;
прикладывают сигнал к образцу после инкубационного периода, равного не более чем 8 с;
генерируют сигнал, обладающий кратковременным затуханием, в ответ на окислительно-восстановительную реакцию подлежащих измерению частиц, причем подлежащие измерению частицы образованы в ходе окислительно-восстановительной реакции части анализируемого вещества в образце; и
определяют концентрацию анализируемого вещества по кратковременному затуханию сгенерированного сигнала.
2. Способ по п.1, в котором подлежащие измерению частицы содержат, по меньшей мере, один посредник.
3. Способ по п.1, в котором инкубационный период составляет не более чем 6 с.
4. Способ по п.1, в котором инкубационный период составляет не более чем 4,75 с.
5. Способ по п.1, в котором инкубационный период составляет от 0,5 до 4 с.
6. Способ по п.1, в котором кратковременное затухание получено в течение от 0,5 до 5 с приложения сигнала к образцу.
7. Способ по п.1, в котором кратковременное затухание снижается.
8. Способ по п.7, в котором снижающееся затухание тока получают в течение приблизительно от 0,5 приблизительно до 3 с приложения сигнала к образцу.
9. Способ по п.7, в котором концентрацию анализируемого вещества определяют по снижающемуся сгенерированному сигналу однократного возбуждения.
10. Способ по п.1, дополнительно содержащий этап, на котором генерируют переменное распределение концентрации подлежащих измерению частиц в емкости для образца.
11. Способ по п.1, в котором инкубационный период и приложение сигнала заканчиваются не более чем за 6 с.
12. Способ по п.1, в котором инкубационный период и приложение сигнала заканчиваются не более чем за 4 с.
13. Способ по п.1, в котором кратковременное затухание имеет постоянную затухания от -0,52 до -1.
14. Способ по п.1, в котором кратковременное затухание имеет постоянную затухания не более чем -0,35.
15. Способ по п.1, в котором сгенерированный сигнал, по которому определяют концентрацию анализируемого вещества, содержит уровень значения тока, сгенерированного в течение 2 с приложения сигнала к образцу.
16. Способ по п.1, в котором определение концентрации анализируемого вещества по сгенерированному сигналу заканчивают в течение 3 с приложения сигнала.
17. Способ по п.1, где образец вводят в сенсорную полоску из емкости, определенной основанием сенсорной полоски и нижней поверхностью крышки, причем основание находится на расстоянии от 50 до 150 мкм от нижней поверхности крышки,
объем образца внутри емкости составляет не более чем 3,5 мкл, и инкубационный период составляет не более чем 6 с.
18. Способ по п.17, в котором высота емкости от основания сенсорной полоски до нижней части крышки составляет не более чем 100 мкм, объем образца внутри емкости составляет не более чем 3 мкл, емкость включает в себя, по меньшей мере, один слой реактивов, обладающий средней начальной толщиной не более чем 2 мкм, и инкубационный период составляет не более чем 2 с.
19. Способ определения концентрации анализируемого вещества в образце, содержащий этапы, на которых:
прикладывают сигнал к образцу после инкубационного периода не более 8 с, причем сигнал включает в себя, по меньшей мере, три возбуждения, причем каждое возбуждение имеет длительность от 0,1 до 5 с;
генерируют сигнал, обладающий кратковременным затуханием, в ответ на окислительно-восстановительную реакцию подлежащих измерению частиц, причем подлежащие измерению частицы образованы в ходе окислительно-восстановительной реакции части анализируемого вещества в образце; и
определяют концентрацию анализируемого вещества по кратковременному затуханию сгенерированного сигнала.
20. Способ по п.19, в котором возбуждения разделены с помощью, по меньшей мере, двух релаксаций, причем каждая релаксация имеет длительность от 0,1 до 3 с.
21. Способ по п.19, в котором приложенный сигнал включает в себя, по меньшей мере, 2 рабочих цикла, используемых в течение 5 с.
22. Способ по п.19, в котором приложенный сигнал следует за инкубационным периодом от 0,5 до 4 с.
23. Способ по п.19, в котором приложение сигнала заканчивается не более чем за 4 с.
24. Способ по п.19, в котором кратковременное затухание обладает постоянной затухания от -0,52 до -1.
25. Способ по п.19, в котором кратковременное затухание обладает постоянной затухания не более чем -0,35.
| US 20030159944 A1, 28.08.2003 | |||
| US 6153069 A, 28.11.2000 | |||
| ЭЛЕКТРОХИМИЧЕСКИЙ ЭЛЕМЕНТ | 1996 |
|
RU2202781C2 |
| US 2005109637 A1, 26.05.2005 | |||
| Стеблеизмельчитель | 1988 |
|
SU1593958A1 |
Авторы
Даты
2012-01-10—Публикация
2007-10-15—Подача