По заявке испрашивается приоритет согласно предварительной заявке № 60/700787 на выдачу патента США, поданной 20 июля 2005 года, и предварительной заявке № 60/746771 на выдачу патента США, поданной 8 мая 2006 года.
Предшествующий уровень техники
Количественное определение анализируемых веществ в биологических жидкостях полезно при диагностике и лечении физиологических патологий. Например, определение уровня глюкозы в биологических жидкостях, таких как кровь, важно для людей, страдающих диабетом, которые должны часто проверять уровень глюкозы в крови, чтобы регулировать режимы своего питания и/или медикаментозного лечения.
Для этого типа анализа использовались электрохимические системы. Во время анализа анализируемое вещество подвергается окислительно-восстановительной реакции с ферментами или подобными препаратами для генерирования электрического тока, который может измеряться и соотноситься с концентрацией анализируемого вещества. Существенное преимущество может быть предоставлено пользователю при сокращении времени, требуемого для анализа, наряду с обеспечением требуемой точности и воспроизводимости.
Один из примеров системы электрохимического датчика для анализа анализируемых веществ в биологических жидкостях включает в себя измерительное устройство и пластинку датчика. Пластинка датчика содержит реактивы для реакции и переноса электронов из анализируемого вещества во время анализа и электроды для пропускания электронов через проводники, которые соединяют пластинку с устройством. Измерительное устройство включает в себя контакты для приема электронов из пластинки и приложения разности потенциалов между контактами. Устройство может регистрировать ток, проходящий через датчик, и преобразовывать значения тока в измерение содержания анализируемого вещества в образце. Эти системы датчиков могут анализировать одну каплю цельной крови (WB), например, от 1 до 15 микролитров (мкл) по объему.
Примеры настольных измерительных устройств включают в себя BAS 100B Analyzer, поставляемый фирмой BAS Instruments в Уэст-Лафейетте, штат Техас; CH Instrument Analyzer, поставляемый фирмой CH Instruments в Остине, штат Техас; Cypress Electrochemical Workstation, поставляемый фирмой Cypress Systems в Лоренсе, штат Канзас; и EG&G Electrochemical Instrument, поставляемый фирмой Princeton Research Instruments в Принстоне, штат Нью-Джерси. Примеры портативных измерительных устройств включают в себя измерители Ascensia Breeze® и Elite® от корпорации Bayer.
Пластинка датчика может включать в себя рабочий электрод, где анализируемое вещество подвергается электрохимической реакции, и противоэлектрод, где происходит противоположная электрохимическая реакция, обеспечивая протекание тока между электродами. Таким образом, если на рабочем электроде происходит окисление, на противоэлектроде происходит восстановление. Смотрите, например, Fundamentals of Analytical Chemistry (Основы аналитической химии), 4th Edition, D.A. Skoog and D.M. West; Philadelphia: Saunders College Publishing (1982), стр.304-341.
Пластинка датчика может включать в себя электрод точного сравнения для выдачи точного опорного потенциала в измерительное устройство. Несмотря на то, что известны многочисленные материалы электродов сравнения, композиция серебра (Ag) и хлорида серебра (AgCl) является типичной вследствие нерастворимости композиции в водной среде раствора для анализа. Электрод сравнения также может использоваться в качестве противоэлектрода. Пластинка датчика, использующая такую комбинацию противоэлектрода сравнения, описана в патенте США № 5820551.
Пластинка датчика может быть сформирована печатью электродов на изолирующей подложке с использованием многочисленных технологий, раскрытых в патентах США № 6531040, 5798031 и 5120420. Один или более слоев реактива могут формироваться покрытием одного или более из электродов, таких как рабочий и/или противоэлектроды. В одном из аспектов более чем один из электродов может покрываться одинаковыми слоями реактива, как в случае, когда рабочие и противоэлектроды покрываются одинаковым составом. В еще одном аспекте слои реактивов, имеющих разные составы, могут отпечатываться или наноситься микропокрытием на рабочие и противоэлектроды с использованием способа, описанного в предварительной заявке № 60/513817 на выдачу патента США от 24 октября 2003 года. Таким образом, слой реактива на рабочем электроде может содержать фермент, медиатор и связующее вещество, при этом слой реактива на противоэлектроде содержит растворимые окислительно-восстановительные препараты, которые могли бы быть такими же, как медиатор, или другими, и связующее вещество.
Слой реактива может включать в себя ионизирующий агент для ускорения окисления или восстановления анализируемого вещества, а также любые медиаторы или другие вещества, которые способствуют переносу электронов между анализируемым веществом и проводником. Ионизирующий агент может быть специфичным ферментом для анализируемого вещества, таким как глюкозооксидаза или глюкозодегидрогеназа, чтобы ускорить окисление глюкозы в образце цельной крови (WB). Слой реактива также может включать в себя связующее вещество, которое удерживает фермент и медиатор вместе. В Таблице I, приведенной ниже, приведены традиционные комбинации ферментов и медиаторов для использования с определенными анализируемыми веществами.
Связующее вещество может включать в себя различные типы и молекулярные массы полимеров, таких как CMC (карбоксиметилцеллюлоза) и/или PEO (оксид полиэтилена). В дополнение к связыванию реактивов вместе связующее вещество может содействовать в фильтрации красных кровяных телец, предохраняя их от покрытия поверхности электрода.
Примеры традиционных систем электрохимических датчиков для анализа анализируемых веществ в биологических жидкостях включают в себя биодатчики Precision®, поставляемые Abbott в Аббот-Парк, штат Иллинойс; биодатчики Accucheck®, поставляемые Roche в Индианаполисе, штат Индиана; и биодатчики OneTouch Ultra®, поставляемые Lifescan в Милпитасе, штат Калифорния.
Одним из электрохимических способов, которые использовались для определения количества анализируемых веществ в биологических жидкостях, является кулонометрия. Например, Хеллер и другие описывали кулонометрический способ для измерений глюкозы цельной крови (патент US 6120676). В кулонометрии концентрация анализируемого вещества количественно определяется посредством полного окисления анализируемого вещества внутри небольшого объема и интегрирования тока по времени окисления, чтобы воспроизвести электрический заряд, отображающий концентрацию анализируемого вещества. Другими словами, кулонометрия фиксирует суммарное количество глюкозы в пределах пластинки датчика.
Важный аспект кулонометрии состоит в том, что по направлению к концу кривой интегрирования заряда в зависимости от времени скорость изменения тока со временем становится, по существу, постоянной, что приводит к установившемуся режиму. Установившаяся часть кулонометрической кривой образует относительно плоский участок плато, обеспечивая определение соответствующего тока. Однако кулонометрический способ требует полного преобразования всего объема анализируемого вещества для достижения установившегося режима. Как результат - этот способ является времязатратным и не дает быстрых результатов, которых требуют пользователи электрохимических устройств, таких как изделия контроля глюкозы. Еще одна проблема с кулонометрией состоит в том, что небольшой объем элемента датчика должен выдерживаться для того, чтобы обеспечивать точные результаты, что может быть затруднительным при массовом выпуске устройств.
Еще одним электрохимическим способом, который использовался для определения количества анализируемых веществ в биологических жидкостях, является амперометрия. При амперометрии ток измеряется во время импульса считывания, в то время как постоянный потенциал (напряжение) приложен между концами рабочих и противоэлектродов пластинки датчика. Измеренный ток используется для определения количества анализируемого вещества в образце. Амперометрия измеряет скорость, с которой электрохимически активный препарат и соответственно анализируемое вещество окисляется или восстанавливается вблизи рабочего электрода. Многочисленные варианты амперометрического способа для биодатчиков, раскрыты в патентах US 5620579, 5653863, 6153069 и 6413411.
Недостаток известных амперометрических способов заключается в неустановившейся природе тока после приложения потенциала. Скорость изменения тока по времени сначала очень значительна и становится медленнее по мере того, как происходит анализ вследствие природы изменения лежащего в основе диффузионного процесса. Пока скорость потребления восстановленного медиатора на поверхности электрода не равна скорости диффузии, установившийся ток не может быть получен. Таким образом, для амперометрических способов измерение тока в течение длительности переходного процесса до тех пор, пока достигнут установившийся режим, может быть связано с большей неточностью, чем измерение в течение установившегося промежутка времени.
«Гематокритный эффект» обусловливает препятствие точному анализу концентрации глюкозы в образцах WB. Образцы WB содержат красные кровяные (RB) тельца и плазму. Плазма, большей частью, является водой, но содержит некоторое количество протеинов и глюкозу. Гематокрит является объемом составляющей RB-телец относительно суммарного объема образца WB и часто выражается в виде процентного содержания. Образцы цельной крови обычно имеют гематокритные процентные содержания, находящиеся в диапазоне от 20 до 60%, где ~40% является средним значением.
В известных пластинках датчика для определения концентраций глюкозы глюкоза может окисляться ферментом, который, в таком случае, передает электрон медиатору. Этот восстановленный медиатор затем движется к рабочему электроду, где он окисляется электрохимическим образом. Количество окисляемого медиатора может сопоставляться току, протекающему между рабочими и противоэлектродами пластинки датчика. Количественно ток, измеренный на рабочем электроде, прямо пропорционален коэффициенту диффузии медиатора. Гематокритный эффект мешает этому процессу, так как RB-тельца блокируют диффузию медиатора на рабочий электрод. По существу, гематокритный эффект оказывает влияние на величину тока, измеренного на рабочем электроде, без какой-либо привязки к количеству глюкозы в образце.
Образцы WB, имеющие изменяющиеся концентрации RB-телец, могут служить причиной погрешностей в измерении, так как датчик не может проводить различие между более низкой концентрацией медиатора и более высокой концентрацией медиатора в тех случаях, когда RB-тельца блокируют диффузию на рабочий электрод. Например, когда анализируются образцы WB, содержащие идентичные уровни глюкозы, но имеющие гематокриты в 20, 40 и 60%, известные системы датчика будут давать три разных показания глюкозы на основании одного набора калибровочных констант (например, крутизны и перехвата). Даже если концентрации глюкозы одинаковы, система будет сообщать, что образец с гематокритом в 20% содержит глюкозы больше, чем образец с гематокритом в 60%, вследствие RB-телец, мешающих диффузии медиатора на рабочий электрод.
Нормальный диапазон гематокрита (концентрация RBC) для людей составляет от 20 до 60% и центрирован вокруг 40%. Гематокритная систематическая погрешность указывает ссылкой на разницу между эталонной концентрацией глюкозы, полученной эталонным прибором, таким как YSI 2300 STAT PLUS™, поставляемым корпорацией YSI, Елоу-Спринкс, штат Огайо, и экспериментальным показанием глюкозы, полученным из портативной системы датчика для образцов, содержащих отличающиеся уровни гематокрита. Разница между эталонными и экспериментальными показаниями является следствием изменения уровней гематокрита между отдельными образцами цельной крови.
В дополнение к гематокритному эффекту погрешности измерения могут также возникать, когда концентрация измеряемого препарата не коррелирует с концентрацией анализируемого вещества. Например, когда система датчика определяет концентрацию восстановленного медиатора, сформированную в ответ на окисление анализируемого вещества, любой восстановленный медиатор, не сформированный окислением анализируемого вещества, будет приводить к системе датчика, указывающей, что в образце присутствует больше анализируемого вещества, чем на самом деле, вследствие медиаторного фона.
В дополнение к гематокритному и медиаторному фоновому эффектам другие факторы также могут приводить к погрешностям при измерении традиционной системой электрохимического датчика при определении концентрации анализируемого вещества в образце. В одном из аспектов эти погрешности могут привноситься, так как участок пластинки датчика, который удерживает образец, может изменяться по объему от пластинки к пластинке. Погрешности также могут привноситься, когда не предоставлено достаточное количество образца, чтобы полностью заполнить объем цокольного зазора - состояние, указываемое как недозаполнение. В других аспектах, погрешности могут привноситься в измерение случайным «шумом» и когда система датчика испытывает недостаток в способности точно определять изменения температуры в образце.
В попытке преодолеть один или более из этих недостатков традиционные системы датчиков ограничились попыткой многочисленных технологий не только в отношении механической конструкции пластинки датчика и выбора реактива, но также в отношении, каким образом измерительное устройство прикладывает электрический потенциал к пластинке. Например, традиционные способы снижения гематокритного эффекта для амперометричеких датчиков включают в себя использование фильтров, как раскрыто в патентах US 5708247 и 5951836; обращение полярности прикладываемого тока, как раскрыто в WO 01/57510; и посредством способов, которые максимизируют внутреннюю устойчивость образца, как раскрыто в патенте US 5628890.
Многочисленные способы прикладывания электрического потенциала к пластинке, как правило, указываемые как импульсные способы, последовательности или циклы, были использованы для принятия мер для устранения погрешностей при определении концентрации анализируемого вещества. Например, в патенте US 4897162 импульсный способ включает в себя непрерывное прикладывание потенциалов нарастающего и спадающего напряжения, которые соединены, чтобы давать колебание треугольной формы. Более того, в публикации WO 2004/053476, а также в заявках US 2003/0178322 и 2003/0113933 описываются импульсные способы, которые включают в себя непрерывное прикладывание потенциалов нарастающего и спадающего напряжения, которые, кроме того, изменяют полярность.
Другие известные способы комбинируют специальную конфигурацию электродов с последовательностью импульсов, прикладываемой к такой конфигурации. Например, в патенте US 5942102 комбинируют специальную конфигурацию электродов, предусмотренную тонкослойным элементом с непрерывным импульсом, так что продукты реакции с противоэлектрода приходят к рабочему электроду. Эта комбинация используется для проведения реакции до тех пор, пока изменение тока в зависимости от времени не становится постоянным, таким образом, достигая надлежащего установившегося режима для медиатора, движущегося между рабочим и противоэлектродами в течение потенциальной ступени. Несмотря на то, что каждый из этих способов имеет различные преимущества и недостатки, ни один не является безупречным.
Сущность изобретения
Таким образом, имеется насущная потребность в улучшенных системах электрохимических датчиков, особенно таких, которые могут обеспечивать более точное определение концентрации анализируемого вещества за меньшее время. Системы, устройства и способы настоящего изобретения преодолевают, по меньшей мере, один из недостатков, присущих традиционным системам.
Предложен способ определения концентрации анализируемого вещества в образце, который заключается в прикладывании последовательности импульсов к образцу; последовательность импульсов включает в себя, по меньшей мере, 3 рабочих цикла в пределах 180 секунд. Каждый из рабочих циклов может включать в себя возбуждение при постоянном потенциале, в течение которого может записываться ток, и релаксацию. Последовательность импульсов может включать в себя завершающий импульс считывания и может прикладываться к пластинке датчика, включающей в себя слой диффузионного барьера (DBL) на рабочем электроде. Определяемая концентрация анализируемого вещества может иметь меньшую систематическую погрешность, обусловленную медиаторным фоном, чем такой же или другой способ, испытывающий недостаток в последовательности импульсов, включающей в себя, по меньшей мере, 3 рабочих цикла в пределах 180 секунд. Благодаря использованию данных тока при переходном процессе концентрация анализируемого вещества может определяться, когда установившийся режим не достигается в течение участков возбуждения рабочих циклов последовательности импульсов. Обработка данных может применяться к измеренным токам, чтобы определять концентрацию анализируемого вещества в образце.
Предложено ручное измерительное устройство для определения концентрации анализируемого вещества в образце. Устройство содержит стробируемое амперометрическое измерительное устройство, предназначенное для приема пластинки датчика. Стробируемое амперометрическое измерительное устройство содержит, по меньшей мере, два контакта устройства, электрически связанных с устройством отображения через электрическую схему. Пластинка с датчиком имеет, по меньшей мере, первый и второй контакты пластинки датчика. Первый контакт пластинки датчика электрически связан с рабочим электродом, а второй контакт пластинки датчика электрически связан с противоэлектродом через проводники. Первый слой реактива находится на, по меньшей мере, одном из электродов и включает в себя оксидоредуктазу и, по меньшей мере, один препарат из окислительно-восстановительной пары.
Предложено ручное измерительное устройство для приема пластинки датчика для определения концентрации анализируемого вещества в образце. Устройство содержит контакты, по меньшей мере, одно устройство отображения и электронную схему, устанавливающую электрическую связь между контактами и устройством отображения. Схема содержит электрическое зарядное устройство и процессор, причем процессор электрически связан с машиночитаемым запоминающим носителем. Носитель содержит машиночитаемую машинную программу, которая, когда выполняется процессором, побуждает зарядное устройство реализовывать последовательность импульсов, содержащую, по меньшей мере, 3 рабочих цикла в пределах 180 секунд, между контактами.
Предложен способ снижения систематической погрешности, обусловленной медиаторным фоном, при определении концентрации анализируемого вещества в образце, который заключается в прикладывании последовательности импульсов, включающей в себя, по меньшей мере, 3 рабочих цикла в пределах 180 секунд, к образцу.
Предложен способ определения длительности последовательности импульсов, включающей в себя, по меньшей мере, 3 рабочих цикла в пределах 180 секунд, для определения концентрации анализируемого вещества в образце; способ заключается в определении множества наборов калибровочных констант, определенных по токам, записанным в течение, по меньшей мере, 3 рабочих циклов, и определении длительности последовательности импульсов в ответ на определенную концентрацию анализируемого вещества в образце.
Предложен способ подачи сигнала пользователю для добавления дополнительного образца на пластинку датчика, который заключается в определении, является ли пластинка датчика недозаполненной, посредством определения постоянной затухания по токам, записанным в течение последовательности стробированных амперометрических импульсов, и сигнализации пользователю, что следует добавить дополнительный образец на пластинку датчика, если пластинка недозаполнена.
Предложен способ определения температуры образца, удерживаемого пластинкой датчика, который заключается в определении постоянной затухания по токам, записанным в течение последовательности стробированных амперометрических импульсов, и соотнесение постоянной затухания со значением температуры.
Предложен способ определения длительности последовательности импульсов для определения концентрации анализируемого вещества в образце, который заключается в определении температуры образца, удерживаемого пластинкой датчика, по постоянным затухания, определенной по токам, записанным в течение последовательности стробированных амперометрических импульсов.
Следующие определения приводятся ниже для обеспечения четкого и непротиворечивого понимания описания изобретения и формулы изобретения.
Термин «анализируемое вещество» определен в виде одного или более веществ, присутствующих в образце. Анализ определяет наличие и/или концентрацию анализируемого вещества, присутствующего в образце.
Термин «образец» определен для состава, который может содержать неизвестное количество анализируемого вещества. Типично - образец для электрохимического анализа находится в жидком виде и предпочтительно образец является водной смесью. Образец может быть биологическим образцом, таким как кровь, моча или слюна. Образец также может быть производной биологического образца, такой как вытяжка, разбавленный раствор, фильтрат или воссозданный осадок.
Термин «измеряемый препарат» определен для любого электрохимически активного препарата, который может окисляться или восстанавливаться при надлежащем потенциале на рабочем электроде пластинки электрохимического датчика. Примеры измеряемых препаратов включают в себя анализируемые вещества, оксидоредуктазы и медиаторы.
Термин «амперометрия» определен для способа анализа, где концентрация анализируемого вещества в образце определяется электрохимическим измерением скорости окисления или восстановления анализируемого вещества под потенциалом.
Термин «система» или «система датчика» определен для пластинки датчика, электрически связанной посредством проводников с измерительным устройством, которое предусматривает определение количества анализируемого вещества в образце.
Термин «пластинка датчика» определен для устройства, которое удерживает образец во время анализа и предусматривает электрическую связь между образцом и измерительным устройством. Участок пластинки датчика, который удерживает образец, часто указывается ссылкой как «цокольный зазор».
Термин «проводник» определен для электропроводного вещества, которое постоянно остается в течение электрохимического анализа.
Термин «измерительное устройство» определен для одного или более электронных устройств, которые могут прикладывать электрический потенциал к проводникам пластинки датчика и измерять результирующий ток. Измерительное устройство также может включать в себя возможности обработки для определения наличия и/или концентрации одного или более анализируемых веществ в ответ на записанные значения тока.
Термин «точность» определяет, насколько близко количество анализируемого вещества, измеренное пластинкой датчика, соответствует истинному количеству анализируемого вещества в образце. В одном из аспектов точность может выражаться в показателях систематической погрешности.
Термин «воспроизводимость» определяет, насколько близко находятся многочисленные измерения анализируемого вещества для одного и того же образца. В одном из аспектов воспроизводимость может выражаться в показателях распределения или дисперсии среди многочисленных измерений.
Термин «окислительно-восстановительная реакция» определен для химической реакции между двумя препаратами, определяющий перенос, по меньшей мере, одного электрона с первого препарата на второй препарат. Таким образом, окислительно-восстановительная реакция включает в себя окисление и восстановление. Полуэлемент окисления реакции приводит к потере, по меньшей мере, одного электрона первым препаратом наряду с тем, что полуэлемент восстановления приводит к добавлению, по меньшей мере, одного электрона ко второму препарату. Ионный заряд препарата, который окисляется, делается более положительным на величину, равную количеству удаленных электронов. Ионный заряд препарата, который восстанавливается, делается более отрицательным на величину, равную количеству приобретенных электронов.
Термин «медиатор» используется для вещества, которое может окисляться или восстанавливаться, и которое может переносить один или более электронов. Медиатор является реактивом при электрохимическом анализе и не является интересующим анализируемым веществом, но предусматривает косвенное измерение анализируемого вещества. В упрощенной системе медиатор подвергается окислительно-восстановительной реакции в ответ на окисление или восстановление анализируемого вещества. Окисленный или восстановленный медиатор затем подвергается противоположной реакции на рабочем электроде пластинки датчика и регенерируется в свою исходную степень окисления.
Термин «связующее вещество» определяет материал, который обеспечивает физическую поддержку и удержание реактивов наряду с обладанием химической совместимости с реактивами.
Термин «медиаторный фон» определяет систематическую погрешность, привнесенную в измеряемую концентрацию анализируемого вещества, относящуюся к измеряемым препаратам, не чувствительным к лежащей в основе концентрации анализируемого вещества.
Термин «недозаполнение» определяет, когда недостаточное количество образца было помещено на пластинку датчика для получения точного анализа.
Термин «окислительно-восстановительная пара» определяет два связанных препарата химического вещества, имеющих разные степени окисления. Восстановление препарата, имеющего более высокую степень окисления, дает препарат, имеющий более низкую степень окисления. В качестве альтернативы - окисление препарата, имеющего более низкую степень окисления, дает препарат, имеющий более высокую степень окисления.
Термин «степень окисления» определяет формальный ионный заряд химического препарата, такого как мельчайшая частица. Более высокая степень окисления, такая как (III), является более положительной, а более низкая степень окисления, такая как (II), является менее положительной.
Термин «растворимый окислительно-восстановительный препарат» определяет вещество, которое способно подвергаться окислению или восстановлению, и которое растворимо в воде (pH 7, 25°C) при уровне, по меньшей мере, в 1,0 грамм на литр. Растворимый окислительно-восстановительный препарат включает в себя электрически активные органические молекулы, органотранзитные металлические комплексы и переходные металлические координационные комплексы. Термин «растворимый окислительно-восстановительный препарат» исключает элементарные металлы и отдельные ионы металлов, особенно те, которые нерастворимы или трудно растворимы в воде.
Термин «оксидоредуктаза» определяет любой фермент, который способствует окислению или восстановлению анализируемого вещества. Оксидоредуктаза является реактивом. Термин оксидоредуктаза включает в себя «оксидазы», которые способствуют реакциям окисления, где молекулярный кислород является акцептором электронов; «редуктазы», которые способствуют реакциям восстановления, где анализируемое вещество восстанавливается, и молекулярный кислород не является анализируемым веществом; и «дегидрогеназы», которые способствуют реакциям окисления, где молекулярный кислород не является акцептором электронов. Например, Oxford Dictionary of Biochemistry and Molecular Biology, Revised Edition, A.D. Smith, Ed., New York: Oxford University Press (1997), pp.161, 476, 477, and 560 (Оксфордский словарь по биохимии и молекулярной биологии, переработанное издание под редакцией А.Д. Смит, Нью-Йорк: Издательство оксфордского университета (1997), стр.161, 476, 477 и 560).
Термин «электрически активная органическая молекула» определяет органическую молекулу, не имеющую металла, которая способна подвергаться реакции окисления или восстановления. Электрически активные органические молекулы могут служить в качестве медиаторов.
Термин «органотранзитный металлический комплекс», также указываемый ссылкой как «комплекс OTM», определен в качестве комплекса, где переходный металл привязан к, по меньшей мере, одному атому углерода благодаря сигма-связи (формальный заряд -1 на атоме углерода привязан сигма-связью к переходному металлу) или пи-связи (формальный заряд 0 на атомах углерода привязан пи-связью к переходному металлу). Например, ферроцен является комплексом OTM с двумя циклопентадиениловыми (Cp) кольцами, каждое привязано через свои пять атомов углерода к центру железа двумя пи-связями и одной сигма-связью. Другим примером комплекса OTM является феррицианид (III) и его восстановленный аналог ферроцианида (II), где шесть цианолигант (формальный заряд -1 на каждом из 6 лиганд) привязаны сигма-связью к центру железа через атомы углерода.
Термин «координационный комплекс» определяет комплекс, имеющий вполне определенную координационную геометрию, такую как восьмигранная или квадратная плоская. В отличие от комплексов OTM, которые определены своими связями, координационные комплексы определены своей геометрией. Таким образом, координационные комплексы могут быть комплексами OTM (такими как упомянутый ранее феррицианид), или комплексами, где атомы неметаллов, иные чем углерод, такие как гетероатомы, в том числе азот, сера, кислород и фосфор, дативно привязаны к центру переходного металла. Например, гексаамин рутения является координационным комплексом, имеющим вполне определенную восьмигранную геометрию, где шесть лиганд NH3 (формальный заряд 0 на каждой из 6 лиганд) дативно привязаны к центру рутения. Более полное обсуждение органотранзитных металлических комплексов, координационных комплексов и связей переходных металлов приводится в Collman et al., Principles and Applications of Organotransition Metal Chemistry (1987) (Коллман и другие; Принципы и применения химии органотранзитных металлов (1987 год)) и Miessler & Tarr, Inorganic Chemistry (1991) (Мисслер и Тарр; Неорганическая химия (1991 год)).
Термин «установившийся» определяет, когда изменение электрохимического сигнала (тока) по отношению к его независимой входной переменной (напряжению или времени) является, по существу, постоянным, например, в пределах ±10 или ±5%.
Термин «невозвратная точка» определяет значение тока, полученного в качестве функции времени, когда возрастающая скорость диффузии измеряемого препарата к поверхности проводника переходит к относительно постоянной скорости диффузии. До невозвратной точки ток является быстроизменяющимся в зависимости от времени. Подобным образом после невозвратной точки скорость затухания тока становится относительно постоянной, таким образом, отражая относительно постоянную скорость диффузии измеряемого препарата на поверхность проводника.
Термин «относительно постоянный» определяет, когда изменение значения тока или скорость диффузии находится в пределах ±20, ±10 или ±5%.
Термин «средняя начальная толщина» указывает на среднюю высоту слоя до введения жидкого образца. Термин «средний» используется, так как верхняя поверхность слоя является неровной, имеющей пики и впадины.
Термин «интенсивность окисления-восстановления» (RI) определен в качестве суммарного времени возбуждения, деленного на сумму суммарного времени возбуждения и суммарных временных задержек релаксации для последовательности импульсов.
Термин «ручное устройство» определен для устройства, которое может удерживаться в руке человека и является портативным. Примером ручного устройства является измерительное устройство, следующее вместе с элитной системой контроля глюкозы крови Ascensia®, доступной для приобретения у ООО Bayer HealthCare, Тэрритаун, штат Нью-Йорк.
Термин «на» определен как «над» и имеет значение относительно описываемой ориентации. Например, если первый компонент нанесен поверх, по меньшей мере, части второго компонента, первый компонент упоминается «нанесенным на» второй. В другом примере, если первый компонент присутствует выше, по меньшей мере, части второго компонента, первый компонент упоминается находящимся «на» втором. Использование термина «на» не исключает наличия вещества между верхним и нижним компонентами. Например, первый компонент может иметь покрытие поверх его верхней поверхности, тем не менее, второй компонент поверх, по меньшей мере, части первого компонента может быть описан как «на» первом компоненте. Таким образом, использование термина «на» может означать или может не означать, что два компонента, являющиеся связанными, находятся в физическом соприкосновении.
Краткое описание чертежей
Изобретение может быть лучше понято из приведенного со ссылками на чертежи ниже описания, на которых:
Фиг.1A изображает общий вид собранной пластинки датчика, согласно изобретению;
фиг.1B - вид сверху пластинки датчика со снятой крышкой, согласно изобретению;
фиг.2 - схему вида сбоку пластинки датчика по фиг.1B, согласно изобретению;
фиг.3 - блок-схему последовательности операций электрохимического аналитического способа определения наличия и концентрации анализируемого вещества в образце, согласно изобретению;
фиг.4A и 4B - рабочий электрод, имеющий поверхностный проводник и DBL во время прикладывания длинного и короткого импульсов считывания, согласно изобретению;
фиг.5A-5E - пять примеров последовательностей импульсов, где многочисленные рабочие циклы применялись к пластинке датчика после введения образца, согласно изобретению;
фиг.6A - выходные токи при переходном процессе последовательности импульсов, изображенной на фиг.5B, для образцов WB с гематокритом 40%, содержащих 50, 100, 200, 400 и 600 мг/дл глюкозы, согласно изобретению;
фиг.6B - контурный профиль тока, подготовленный вычерчиванием и соединением конечных значений тока по каждому из профилей тока при переходном процессе, показанных на фиг.6A, согласно изобретению;
фиг.6C - контурные профили тока, подготовленные из профилей тока при переходном процессе, сформированных последовательностью импульсов, изображенной на фиг.5E, согласно изобретению;
фиг.6D - диаграммы выходных сигналов относительно входных сигналов для электрохимической системы, использующей последовательности стробированных амперометрических импульсов, согласно изобретению;
фиг.7A и 7B - диаграммы, показывающие улучшение в точности измерения, когда DBL комбинируется с коротким импульсом считывания, согласно изобретению;
фиг.7C и 7D - диаграммы, иллюстрирующие уменьшение в гематокритной систематической погрешности, которое может быть получено, когда последовательность стробированных амперометрических импульсов комбинируется с DBL, согласно изобретению;
фиг.8 - диаграммы токов конечных точек, записанных в многочисленных рабочих циклах, когда последовательность импульсов по фиг.5B прикладывалась к образцам WB, содержащим различные концентрации глюкозы, согласно изобретению;
фиг.9A - профили тока при переходных процессах, полученные из последовательности импульсов, изображенной на фиг.5B, когда образец в 2,0 мкл помещался на 10 разных пластинок датчиков, согласно изобретению;
фиг.9B - профили скорости затухания каждой последовательности импульсов, преобразованной из фиг.9A в качестве функции времени, согласно изобретению;
фиг.10 - диаграммы К констант, определенных из последовательности импульсов для концентраций глюкозы в 50, 100 и 400 мг/дл, в качестве функции температуры, согласно изобретению;
фиг.11 - схему измерительного устройства, согласно изобретению.
Подробное описание предпочтительных вариантов воплощения изобретения
Настоящее изобретение основано на открытии, что последовательность стробированных амперометрических импульсов, включающая в себя многочисленные рабочие циклы, может обеспечивать улучшенную точность и воспроизводимость в отношении анализа наряду с сокращением времени выполнения анализа. Каждый рабочий цикл включает в себя возбуждение, которое может обеспечиваться при постоянном напряжении. Каждый рабочий цикл также включает в себя релаксацию, которая может обеспечиваться разомкнутой цепью. Последовательности импульсов по настоящему изобретению могут сокращать время, требуемое для анализа, поскольку исключена необходимость в дополнительных задержках и импульсах, таких как задержки «инкубации» для обеспечения регидратации реактива, импульсы «выжигания» для обновления электродов и импульсы регенерации медиатора для возобновления состояния окисления медиатора, таким образом, сокращая время анализа.
Даже с более короткими временами анализа последовательности стробированных амперометрических импульсов, по настоящему изобретению, улучшают точность и/или воспроизводимость относительно известных способов. В одном из аспектов точностные погрешности, привнесенные гематокритным эффектом, и погрешности воспроизводимости, привнесенные изменением объема цокольного зазора, могут быть уменьшены благодаря комбинации слоя диффузионного барьера с последовательностями импульсов по настоящему изобретению. В еще одном аспекте могут быть уменьшены погрешности из-за неустановившегося режима датчика и/или медиаторного фона. Последовательности стробированных импульсов по настоящему изобретению также могут предоставлять возможность определения профилей тока при переходном процессе и контурных профилей, которые имитируют установившийся режим. Профили тока при переходном процессе могут использоваться для предоставления множества наборов калибровочных констант, обнаружения недозаполнения и возможности определять температуру образца взамен расчета температуры измерительного устройства.
На фиг.1A и 1B показана пластинка 100 датчика, которая может использоваться в настоящем изобретении. На фиг.1A изображен общий вид собранной пластинки 100 датчика, содержащего основу 110 датчика, по меньшей мере, частично покрытую крышкой 120, которая имеет отверстие 130, вогнутый участок 140 и входной торцевой проем 150. Частично замкнутый объем 160 (цокольный зазор) сформирован между основой 110 и крышкой 120. Также могут использоваться другие конструкции пластинки датчика, совместимые с настоящими изобретением.
Жидкий образец для анализа может переноситься в цокольный зазор 160 введением жидкости в проем 150. Жидкость заполняет цокольный зазор 160 путем выталкивания содержащегося ранее воздуха через отверстие 130. Цокольный зазор 160 может содержать состав (не показан), который способствует удерживанию жидкого образца в цокольном зазоре. Примеры таких составов включают в себя водонаполняемые полимеры, такие как карбоксиметилцеллюлоза и полиэтиленгликоль, и пористые полимерные матрицы, такие как декстран и полиакриламид.
На фиг.1B показан вид сверху пластинки 100 датчика со снятой крышкой 120. Проводники 170 и 180 могут проходить под диэлектрическим слоем от проема 150 к рабочему электроду 175 и противоэлектроду 185 соответственно. В одном из аспектов рабочий и противоэлектрод 175, 185 могут быть, по существу, в одной и той же плоскости, как показано на чертеже. Рабочий и противоэлектрод 175, 185 могут быть разделены на более чем 200 или 250 мкм, и могут быть отделены от верхней части крышки 120, по меньшей мере, на 100 мкм. Диэлектрический слой 190 может частично покрывать электроды 175, 185 и может быть изготовлен из подходящего диэлектрического материала, такого как изолирующий полимер.
Противоэлектрод 185 уравновешивает потенциал на рабочем электроде 175 пластинки 100 датчика. В одном из аспектов этот потенциал может быть опорным потенциалом, достигнутым формированием противоэлектрода 185 из окислительно-восстановительной пары, такой как Ag/AgCl, чтобы предоставить комбинированный противоэлектрод сравнения. В еще одном аспекте потенциал может подаваться в систему датчика формированием противоэлектрода 185 из инертного материала, такого как углерод, и включением растворимого окислительно-восстановительного препарата, такого как феррицианид, в пределы цокольного зазора 160. В качестве альтернативы - пластинка 100 датчика может быть снабжена третьим проводником и электродом (не показаны) для подачи опорного потенциала в систему датчика.
На фиг.2 показан вид с торца пластинки датчика, изображенной на фиг.1B, показывающую структуру слоев рабочего электрода 175 и противоэлектрода 185. Проводники 170 и 180 могут лежать непосредственно под основой 110. Поверхностные слои 270 и 280 проводников, по выбору, могут наноситься на проводники 170 и 180 соответственно. Поверхностные слои 270, 280 проводников могут быть выполнены из одного и того же или из разных материалов.
Материал или материалы, используемые для формирования проводников 170, 180 и поверхностных слоев 270, 280 проводников, могут включать в себя любой электрический проводник. Предпочтительными электрическими проводниками являются неионизирующие из условия, чтобы материал не подвергался наблюдаемому окислению или наблюдаемому восстановлению во время анализа образца. Проводники 170, 180 предпочтительно включают в себя тонкий слой металлической пасты или металла, такого как золото, серебро, платина, палладий, медь или вольфрам. Поверхностные слои 270, 280 проводников предпочтительно включают в себя углерод, золото, платину, палладий или их сочетание. Если поверхностный слой проводника не присутствует на проводнике, проводник предпочтительно сделан из неионизирующего материала.
Поверхностный материал проводника может быть осажден на проводники 170, 180 любым традиционным средством, совместимым с работой пластинки датчика, в том числе нанесением покрытия фольги, химическим осаждением из паровой фазы, суспензионным осаждением и тому подобным. В случае суспензионного осаждения смесь может накладываться в виде пасты на проводники 170, 180.
Слои 275 и 285 реактивов могут осаждаться на проводники 170 и 180 соответственно и включают в себя реактивы и по выбору связующее вещество. Связующий материал предпочтительно является полимерным материалом, который, по меньшей мере, частично является водорастворимым. Подходящие частично водорастворимые полимерные материалы для использования в качестве связующего вещества могут включать в себя оксид полиэтилена (PEO), карбоксиметилцеллюлозу (CMC), поливиниловый спирт (PVA), гидроксиэтиленцеллюлозу (НЕС), гидроксипропилцеллюлозу (HPC), метилцеллюлозу, этилцеллюлозу, этилгидроксилэтилцеллюлозу, карбохиметилэтилцеллюлозу, поливинилпирролидон (PVP), полиаминокислоты, такие как полилизин, полистиролсульфанат, желатин, акриловую кислоту, метакриловую кислоту, крахмал, их малеиновые ангидридные соли, их производные и их сочетания. Среди вышеприведенных связующих материалов предпочтительны PEO, PVA, CMC и PVA, причем в настоящее время CMC и PEO являются более предпочтительными.
В дополнение к связующему веществу слои 275 и 285 реактивов могут включать в себя одинаковые или разные реактивы. В одном из аспектов реактивы, присутствующие в первом слое 275, могут использоваться с рабочим электродом 175, тогда как реактивы, присутствующие во втором слое 285, могут использоваться с противоэлектродом 185. Например, реактивы в слое 285 могут способствовать свободному протеканию электродов между образцом и проводником 180. Подобным образом реактивы в слое 275 могут способствовать реакции анализируемого вещества.
Слой 275 реактива может включать в себя оксиредуктазу, специфичную анализируемому веществу, которая может содействовать реакции анализируемого вещества наряду с улучшением специфичности системы датчика в отношении анализируемого вещества, особенно в сложных биологических образцах. Примеры некоторых специфичных оксидоредуктаз и соответствующих анализируемых веществ даны ниже, в Таблице II.
В настоящее время особенно предпочтительными оксидоредуктазами для анализа глюкозы являются глюкозооксидаза, глюкозодегидрогеназа, их производные или их сочетания.
Слой 275 реактива также может включать в себя медиатор для более эффективной передачи результатов реакции анализируемого вещества на поверхность проводника 270 и/или проводника 170. Примеры медиаторов включают в себя комплексы OTM, координационные комплексы и электрически активные органические молекулы. Отдельные примеры включают в себя ферроценовые компаунды, ферроцианиды, феррицианиды, коферменты замещенных или незамещенных пирролокуинолиновых куинонов (PQQ), замещенных или незамещенных 3-фенилимино-3H-фенотиазинов (PIPT), 3-фенилимино-3H-феноксазина (PIPO), замещенных или незамещенных бензокуинонов, замещенных или незамещенных нафтокуинонов, N-оксидов, нитрозокомпаундов, гидроксиламинов, оксинов, флавинов, феназинов, производных феназинов, фенотиазинов, индофенолов и индаминов.
В настоящее время особенно предпочтительными медиаторами для анализа глюкозы являются феррицианид, гексаамин рутения, PIPT, PIPO или их сочетания. Обзор полезных электрохимических медиаторов для систем биологического окисления-восстановления приведен в Analytica Clinica Acta. 140 (1982) (Аналитические клинические процедуры. 140 (1982 год)), стр.1-18.
Слои 275, 285 реактивов могут быть осаждены любым традиционным способом, таким как печать, жидкостное осаждение или струйное осаждение. В одном из аспектов слои осаждаются печатью. При прочих равных факторах угол печатной лопатки может обратным образом влиять на толщину слоев реактивов. Например, когда лопатка движется под углом около в 82° к основе 110, слой может иметь толщину около в 10 мкм. Подобным образом используется угол лопатки около в 62° по отношению к основе 110, может создаваться более толстый слой в 30 мкм. Таким образом, меньшие углы лопатки могут давать более толстые слои реактивов. В дополнение к углу лопатки другие факторы, такие как вязкость наносимого материала, а также комбинация номера сита и эмульсии, могут воздействовать на результирующую толщину слоев 275, 285 реактивов.
Рабочий электрод 175 также может включать в себя слой диффузионного барьера (DBL), который является неотъемлемым по отношению к слою 275 реактива, или который является отдельным слоем 290, таким как изображенный на фиг.2. Таким образом, DBL может формироваться в качестве комбинированных реактива/DBL на проводнике в качестве отдельного слоя на проводнике или в качестве слоя на слое реактива. Когда рабочий электрод 175 включает в себя отдельный DBL 290, слой 275 реактива может находиться или может не находиться на DBL 290. Вместо нахождения на DBL 290 слой 275 реактива может находиться на любом участке пластинки 100 датчика, который предоставляет реактиву возможность растворяться в образце. Например, слой 175 реактива может находиться на основе 110 или на крышке 120.
DBL предусматривает пористое пространство, имеющее внутренний объем, где может находиться измеряемый препарат. Поры DBL могут быть выбраны так, что измеряемый препарат может диффундировать в DBL наряду с тем, что физически более крупные составляющие образца, такие как RB-тельца, по существу, исключаются. Хотя традиционные пластинки датчика использовали различные материалы для отфильтровывания RB-телец с поверхности рабочего электрода, DBL предусматривает внутреннее пористое пространство для удержания и изоляции порции измеряемого препарата из образца.
Когда слой 275 реактива включает в себя водорастворимое связующее вещество, любая порция связующего вещества, которая не растворяется в образце до применения возбуждения, может функционировать в качестве неотъемлемого DBL. Средняя начальная толщина комбинированного слоя DBL/реактива предпочтительно является меньшей, чем 30 или 23 микрометра (мкм), а более предпочтительно - меньшей, чем 16 мкм. В настоящее время особенно предпочтительными средними начальными толщинами комбинированного слоя DBL/реактива являются от 1 до 30 мкм или от 3 до 12 мкм. Требуемая средняя начальная толщина комбинированного слоя DBL/реактива может выбираться для определенной продолжительности возбуждения на основе того, когда скорость диффузии измеряемого препарата из DBL на поверхность проводника, такую как поверхность проводника 170 или поверхность проводника 270 по фиг.2, становится относительно постоянной.
Более того, использование слишком толстого DBL с короткой продолжительностью возбуждения может вызывать задержку, когда скорость диффузии измеряемого препарата из DBL на поверхность проводника становится относительно постоянной. Например, когда рабочие циклы, включающие в себя последовательные 1-секундные возбуждения, разделенные 0,5-секундными релаксациями, применяются к рабочему электроду, использующему комбинированный слой DBL/реактива, имеющий среднюю начальную толщину в 30 мкм, предпочтительная скорость диффузии может не достигаться до тех пор, пока не были применены, по меньшей мере, 6 рабочих циклов (>~10 секунд). Наоборот, когда одинаковые рабочие циклы применяются к рабочему электроду, использующему комбинированный слой DBL/реактива, имеющий среднюю начальную толщину в 11 мкм, относительно постоянная скорость диффузии может достигаться после второго возбуждения (~2,5 секунды). Таким образом, есть верхний предел для предпочтительной средней начальной толщины DBL для заданного рабочего цикла. Более глубокое рассмотрение взаимозависимости между толщиной DBL, продолжительностью возбуждения и временем для достижения относительно постоянной скорости диффузии, раскрыто в предварительной заявке № 60/655180 на выдачу патента США от 22 февраля 2005 года «Concentration Determination in a Diffusion Barrier Layer» («Определение концентрации в слое диффузионного барьера»).
Отдельный DBL 290 может включать в себя любой материал, который предусматривает требуемое пористое пространство и частично или слабо растворим в образце. В одном из аспектов отдельный DBL 290 может включать в себя связующий материал реактива с отсутствием реактивов. Отдельный DBL 290 может иметь среднюю начальную толщину в, по меньшей мере, 5 мкм, предпочтительно от 8 до 25 мкм, а более предпочтительно - от 8 до 15 мкм.
На фиг.3 показана блок-схема последовательности шагов электрохимического анализа 300 для определения наличия и, по выбору, концентрации анализируемого вещества 322 в образце 312. На шаге 310 образец 312 помещается на пластинку 314 датчика, такую как пластинка датчика, изображенная на фиг.1A-1B и 2. Слои реактива, такие как 275 и/или 285 по фиг.2, начинают растворяться в образце 312, таким образом, предоставляя возможность реакции. На этой стадии при анализе полезно предусмотреть начальную временную задержку или «период инкубации», чтобы реактивы прореагировали с образцом 312. Предпочтительно начальная временная задержка может быть от 1 до 10 секунд. Более глубокое рассмотрение начальных временных задержек раскрыто в патентах США 5620579 и 5653863.
Во время реакции часть анализируемого вещества 322, присутствующего в образце 312, химически или биохимически окисляется или восстанавливается на шаге 320, например, оксидоредуктазой. При окислении или восстановлении электроны, по выбору, могут переноситься между анализируемым веществом 322 и медиатором 332 на шаге 330.
На шаге 340 измеряемый препарат 342, который может быть заряженным анализируемым веществом 322 из 320 или заряженным медиатором 332 с шага 330, электрохимически возбуждается (окисляется или восстанавливается). Например, когда образец 312 является цельной кровью, содержащей глюкозу, которая окислялась оксидазой глюкозы на шаге 320, которая, в таком случае, переносит электрон для восстановления феррицианидного (III) медиатора до ферроцианида (II) на шаге 330, возбуждение на шаге 340 окисляет ферроцианид (II) до феррицианида (III) на рабочем электроде. Таким образом, электрон избирательно переносится с анализируемого вещества глюкозы на рабочий электрод пластинки датчика, где он может детектироваться измерительным устройством.
Ток, являющийся следствием возбуждения на шаге 340, может записываться во время возбуждения в качестве функции времени на шаге 350. На шаге 360 образец подвергается релаксации. Предпочтительно - ток не записывается во время релаксации на шаге 360.
На шаге 370 возбуждение 340, запись 350 и релаксация 360 повторяются, по меньшей мере, дважды для итоговой суммы из, по меньшей мере, трех рабочих циклов в пределах 180-секундного или меньшего заданного интервала времени. Записанные значения тока и времени могут анализироваться для определения наличия и/или концентрации анализируемого вещества 322 в образце 312 на шаге 380.
Система амперометрического датчика прикладывает потенциал (напряжение) к пластинке датчика, чтобы возбудить измеряемый препарат, в то время как отслеживается ток (сила тока в амперах). Традиционные системы амперометрических датчиков могут удерживать потенциал наряду с измерением тока, например, в течение продолжительности непрерывного импульса считывания от 5 до 10 секунд. В противоположность традиционным способам рабочие циклы, используемые при электромеханическом анализе 300, замещают непрерывные импульсы считывания большой длительности многочисленными возбуждениями и релаксациями короткой длительности.
Анализ 300 может повышать точность и/или воспроизводимость определения анализируемого вещества, когда измеряемый препарат, возбужденный на рабочем электроде на шаге 540, по существу, отбирается из внутренней части DBL в противоположность измеряемому препарату, присутствующему в цокольном зазоре пластинки. Фиг.4A и 4B изображают рабочий электрод 400, имеющий поверхностный проводник 430 и отдельный DBL 405, во время прикладывания длинного импульса считывания и короткого возбуждения. Когда образец WB накладывается на рабочий электрод 400, RB-тельца 420 покрывают DBL 405. Анализируемое вещество, присутствующее в образце, формирует внешний анализируемый препарат 410, внешний по отношению к DBL 405. Часть внешнего анализируемого препарата 410 диффундирует в отдельный DBL 405, чтобы предоставить внутренний анализируемый препарат 415.
Как показано на фиг.4A, когда непрерывный 10-секундный импульс считывания прикладывается к рабочему электроду 400, оба, внешний и внутренний анализируемый препараты 410 и 415, возбуждаются на поверхностном проводнике 430 посредством перехода в состояние окисления. Во время длинного импульса считывания внешний анализируемый препарат 410 диффундирует через область образца, где находятся RB-тельца 420, и через DBL 405 на поверхностный проводник 430. Диффузия внешнего анализируемого препарата 410 через RB-тельца 420 во время импульса считывания привносит в анализ гематокритный эффект. Так как существенная часть анализируемого препарата, возбужденного на поверхностном электроде 430 возникает извне DBL 420, длинный импульс считывания, прикладываемый к пластинке датчика, имеющей DBL, может производить действие в отношении гематокритного эффекта подобно короткому импульсу считывания, приложенному к пластинке, не имеющей DBL.
Наоборот, на фиг.4B представлена ситуация, где короткое возбуждение применяется к оснащенной DBL пластинке 400 датчика для возбуждения внутреннего анализируемого препарата 415, по существу, наряду с исключением из возбуждения анализируемого препарата 410, внешнего по отношению к DBL 405. Во время короткого возбуждения анализируемый препарат 410 либо остается внешним по отношению к DBL 405, либо не диффундирует существенно через DBL для достижения поверхностного проводника 430. Таким образом, короткое возбуждение может обеспечить существенное снижение влияния гематокритного эффекта на анализ.
Регулированием продолжительности возбуждения на рабочем электроде может анализироваться анализируемый препарат, внутренний по отношению к DBL, наряду с тем, что анализируемый препарат, внешний по отношению к DBL, по существу, может быть исключен из анализа. Что касается поверхностного проводника 430 рабочего электрода, толщина и внутренний объем DBL 405 предполагаются для изменения скорости диффузии внутреннего анализируемого препарата 415 относительно скорости диффузии внешнего анализируемого препарата 410.
Так как анализируемый препарат, внутренний по отношению к DBL, может диффундировать при иной скорости в проводник рабочего электрода, чем анализируемый препарат, внешний по отношению к DBL, продолжительность возбуждения на рабочем электроде может выбирать, какой анализируемый препарат предпочтительно анализируется. С молекулярной точки зрения разные скорости диффузии анализируемого препарата, внутреннего и внешнего по отношению к DBL, могут предоставить возможность дифференциации.
Поскольку нежелательно ограничиваться любой конкретной теорией, предполагается, что скорость диффузии анализируемого препарата извне DBL в DBL изменяется, тогда как скорость диффузии анализируемого препарата из внутреннего объема DBL на проводник относительно постоянна. Изменяющаяся скорость диффузии анализируемого препарата вне DBL может вызываться RB-тельцами или другими составляющими, присутствующими в образце, и может вызывать гематокритный эффект. Таким образом, погрешности (систематическая погрешность) анализа, привнесенные составляющими образца, в том числе RB-тельцами, могут уменьшаться, по существу, ограничением анализа анализируемым препаратом, имеющим относительно постоянную скорость диффузии.
Другим преимуществом избирательного анализа анализируемого препарата, внутреннего по отношению к DBL, является снижение расхождения результатов измерений из пластинок датчиков, имеющих изменяющиеся объемы цокольного зазора. Если импульс считывания продолжается после момента времени, когда, по существу, весь анализируемый препарат, присутствующий в цокольном зазоре, был проанализирован, анализ больше не представляет концентрацию анализируемого препарата в образце, но взамен определяет количество анализируемого препарата в цокольном зазоре; очень непохожее измерение. Так как продолжительность возбуждения увеличивается относительно объема цокольного зазора, измерение тока будет зависеть от объема цокольного зазора, а не от лежащей в основе концентрации анализируемого вещества. Таким образом, длинные импульсы считывания могут иметь результатом величины, которые чрезвычайно неточны относительно концентрации анализируемого вещества, когда длительность импульса «чрезмерно истребляет» анализируемый препарат, присутствующий в цокольном зазоре.
Как описано в предварительной заявке № 60/617889 на выдачу патента США, может выбираться одиночный короткий импульс считывания или возбуждения, чтобы, по существу, ограничивать возбуждение анализируемого препарата до DBL. Когда используется одиночное возбуждение, продолжительность возбуждения и толщина DBL предпочтительно могут выбираться так, что относительно постоянная скорость диффузии анализируемого препарата из DBL на поверхность проводника достигается во время возбуждения. Если во время возбуждения относительно постоянная скорость диффузии не достигается, концентрация анализируемого препарата в пределах DBL не может точно представлять концентрацию анализируемого препарата в образце, нанося ущерб анализу. Более того, одиночное возбуждение не может эффективно снижать фоновый сигнал от медиатора.
Со ссылкой на фиг.3, возбуждение 340, запись 350 и релаксация 360 составляют одиночный рабочий цикл, который может применяться к пластинке датчика, по меньшей мере, три раза в течение 180-секундного или меньшего промежутка времени. Более предпочтительно - по меньшей мере, 4, 6, 8, 10, 14, 18 или 22 рабочих цикла применяются в течение независимо выбранного 120, 90, 60, 30, 15, 10 или 5-секундного промежутка времени. В одном из аспектов рабочие циклы применяются в течение от 5 до 60-секундного промежутка времени. В другом аспекте от 3 до 18 или от 3 до 10 рабочих циклов могут применяться в пределах 30 секунд или менее. В еще одном аспекте от 4 до 8 рабочих циклов могут применяться в пределах от 3 до 16 секунд.
Потенциал, прикладываемый во время возбуждения 340 рабочего цикла, предпочтительно прикладывается, по существу, при постоянном напряжении и полярности в течение всего времени. Это прямо противоречит традиционным импульсам считывания, где напряжение изменяется или «качается» по многочисленным потенциалам и/или полярностям напряжения во время записи данных. В одном из аспектов длительность шага 340 возбуждения составляет, самое большее, 4 или 5 секунд, а предпочтительно - менее чем 3, 2, 1,5 или 1 секунда. В еще одном аспекте длительность возбуждения 340 составляет от 0,01 до 3 секунд, от 0,01 до 2 секунд или от 0,01 до 1,5 секунд. Более предпочтительно - длительность возбуждения 340 составляет от 0,1 до 1,2 секунд.
После возбуждения 340 на этапе 360 измерительное устройство может размыкать цепь через пластинку 314 датчика, таким образом, предоставляя системе возможность релаксировать. Во время релаксации 360 ток, присутствующий во время возбуждения 340, по существу, снижается, по меньшей мере, наполовину, предпочтительно - на порядок величины, а более предпочтительно - до нуля. Предпочтительно состояние нулевого тока обеспечивается разомкнутой цепью или другим способом, известным специалистам в данной области техники, чтобы обеспечивать, по существу, нулевое протекание тока. По меньшей мере, 3 релаксации может быть предусмотрено в течение рабочих циклов последовательности импульсов.
В одном из аспектов релаксация 360 составляет, по меньшей мере, 10, 5, 3, 2, 1,5, 1 или 0,5 секунд по длительности. В еще одном аспекте релаксация 360 составляет от 0,1 до 3 секунд, от 0,1 до 2 секунд или от 0,1 до 1,5 секунд по длительности. Более предпочтительно - релаксация 360 составляет от 0,2 до 1,5 секунд по длительности и обеспечивается разомкнутой цепью.
Во время этапа релаксации 360 ионизатор может реагировать с анализируемым веществом для формирования дополнительного анализируемого препарата без воздействий электрического потенциала. Таким образом, для системы датчика глюкозы, включающей в себя глюкозооксидазу и феррицианидный медиатор в качестве реактивов, дополнительный ферроцианид (восстановленный медиатор), реагирующий на концентрацию анализируемого вещества образца, может создаваться без влияния от электрического потенциала во время релаксации 360.
Во многих известных способах анализа непрерывно прикладывают напряжение в течение длительности импульса считывания. Приложенное напряжение может иметь постоянный потенциал или может иметь потенциал, который качается от положительного до отрицательного потенциала, либо от положительного или отрицательного потенциала к нулевому потенциалу относительно некоторого потенциала. Даже при нулевом относительном потенциале эти способы непрерывно отводят ток из пластинки датчика в течение импульса считывания, который позволяет электрохимической реакции продолжаться на всем протяжении импульса считывания. Таким образом, реакция, которая создает анализируемый препарат, чувствительный к концентрации анализируемого вещества, и диффузия анилизируемого препарата на рабочий электрод - обе подвергаются воздействию тока во время участка нулевого потенциала традиционного импульса считывания.
Известные способы, в которых непрерывно прикладывают напряжение к и отводят ток из пластинки датчика, даже при нулевом потенциале относительно некоторого потенциала, существенно отличаются от релаксаций по настоящему изобретению. Многочисленные рабочие циклы, применяемые настоящим изобретением, также заметно отличаются от известных способов, которые используют одиночный импульс большой длительности с многочисленными измерениями, например, раскрытыми в патенте США под № 5243516, вследствие многочисленных релаксаций по настоящему изобретению. В противоположность этим способам каждый рабочий цикл последовательностей импульсов по настоящему изобретению предусматривает независимое время диффузии и реакции анализируемого вещества во время релаксации.
На фиг.5A-5E показаны пять примеров последовательностей стробированных амперометрических импульсов, где многочисленные рабочие циклы применялись к пластинке датчика после введения образца. В этих примерах использовались прямоугольные импульсы, однако также могут использоваться другие типы колебательного сигнала, совместимые с системой датчика и опытным образцом. На фиг.5C-5D показаны последовательности импульсов, включающие в себя многочисленные рабочие циклы, имеющие одинаковые времена задержек возбуждения и разомкнутой цепи.
Фиг.5A-5B изображают последовательности импульсов, которые включают в себя 9 рабочих циклов, имеющих одинаковые времена задержек возбуждения и разомкнутой цепи в дополнение к завершающему импульсу 510 считывания большей длительности, который повышается по напряжению. Повышенное напряжение этого завершающего импульса считывания обеспечивает возможность детектировать препарат, имеющий более высокий окислительный потенциал. Более полное обсуждение касательно завершающих импульсов считывания раскрыто в предварительной заявке № 60/669729 на выдачу патента США.
На фиг.5A представлена последовательность импульсов с 9 рабочими циклами, где 0,5-секундные возбуждения повторно отделяются 1-секундными задержками разомкнутой цепи, чтобы дать интенсивность окисления-восстановления (RI) в 0,357 (5/14). Таким образом, на фиг.5A второй рабочий цикл содержит участок 520 возбуждения и участок 530 релаксации. Фиг.5B изображает последовательность импульсов с 9 рабочими циклами, где 1-секундные возбуждения отделяются 0,5-секундными задержками разомкнутой цепи, чтобы дать RI в 0,69 (10/14,5). Фиг.5C изображает последовательность импульсов с 7 рабочими циклами, где 1-секундные возбуждения отделяются 1-секундными задержками разомкнутой цепи, чтобы дать RI в 0,53 (8/15). Применялся завершающий импульс 540 считывания такой же длительности и напряжения, как используемые в течение 7 рабочих циклов. Фиг.5D изображает последовательность импульсов с 6 рабочими циклами, где 1,5-секундные возбуждения отделяются 1-секундными задержками разомкнутой цепи, чтобы дать RI в 0,636 (10,5/16,5). Как на фиг.5C применялся завершающий импульс 540 считывания такой же длительности и напряжения, как предыдущие импульсы рабочих циклов. Фиг.5E изображает последовательность импульсов с 7 рабочими циклами, где относительно короткие 0,25-секундные возбуждения отделяются относительно длинными 1,5-секундными релаксациями. Последовательность импульсов фиг.5E начинается с начального 1-секундного импульса 550 и заканчивается 1,25-секундным завершающим импульсом 540 считывания для обеспечения RI в 0,25 (4/16).
Чем выше RI для последовательности импульсов, тем меньший фоновый сигнал будет привноситься в анализ медиатором. Последовательности импульсов, представленные на фиг.5A-5E, являются окислительными импульсами, предназначенными для возбуждения (то есть, окисления) восстановленного медиатора, который является анализируемым препаратом. Таким образом, чем больше окислительный ток, приложенный к пластинке датчика за заданный промежуток времени, тем меньше риск, что медиатор, восстановленный путями обмена, иными, чем окисление анализируемого вещества, является вносящим вклад в записываемые значения тока.
Таблица III, приведенная ниже, предусматривает крутизну, перехват и отношение перехвата к крутизне для контурных профилей последних четырех рабочих циклов последовательностей (a) и (b) импульсов. Последовательностью (a) импульсов была:
9·(0,5-секундное включение+1,0-секундное выключение)+0,5 секунд=14 секунд, RI=5/14=0,357.
Последовательностью (b) импульсов была:
9·(1,0-секундное включение+0,375-секундное выключение)+1,0 секунд=13,375 секунд, RI=10/13,375=0,748.
Отношения перехвата к крутизне дают показание величины фонового сигнала, относящегося к медиатору, причем большие значения отношения указывают большую долю записанного сигнала, относящуюся к медиаторному фону. Таким образом, частота импульсов (количество возбуждений/суммарное время оценки в секундах) последовательностей (a) и (b) подобны до около 0,7 с-1, повышение RI, обеспеченное последовательностью (b) импульсов, дает на половину меньший фоновый сигнал. В комбинации многочисленные возбуждения последовательности импульсов могут устранять необходимость для начального импульса возобновлять состояние окисления медиатора. В то время как фоновый ток может подвергаться влиянию медиатором, для феррицианида являются предпочтительными последовательности импульсов, имеющие значения RI, по меньшей мере, в 0,01, 0,3, 0,6 или 1, причем значения RI от 0,1 до 0,8, от 0,2 до 0,7 или от 0,4 до 0,6 являются более предпочтительными.
Возвращаясь к фиг.3, на этапе 350 ток, проходящий через проводники пластинки 314 датчика, в течение каждого рабочего цикла последовательности импульсов может записываться в качестве функции времени. Фиг.6A показывает выходные токи, графически изображенные в виде функции времени для последовательности импульсов, представленной на фиг.5B, для образцов WB с гематокритом 40%, содержащих 50, 100, 200, 400 и 600 мг/дл глюкозы. Вместо традиционного импульса считывания с большой длительностью, имеющего результатом обширное окисление анализируемого препарата, каждое возбуждение сопровождается разрывом в профиле тока.
На фиг.6A, когда выходные токи графически изображены в виде функции времени, каждое возбуждение имеет результатом профиль тока при переходном процессе, имеющий высокое начальное значение тока, которое затухает со временем. Предпочтительно рабочие циклы включают в себя короткие независимые возбуждения и релаксации, которые удерживают систему от достижения установившегося режима или режима с медленным затуханием тока во время каждого возбуждения, как требуется в течение импульса считывания традиционных систем. Вместо традиционных установившихся или медленно затухающих токов значения (быстро затухающего) тока при переходном процессе получаются из последовательностей стробированных амперометрических импульсов, так как электрохимическая реакция анализируемого препарата на рабочем электроде является более быстрой, чем скорость, с которой анализируемый препарат подается на рабочий электрод диффузией.
На фиг.6B показана диаграмма контурного профиля, подготовленного соединением конечных значений тока из каждого из профилей тока при переходном процессе (то есть, конечного значения тока из каждого возбуждения), показанных на фиг.6A. Контурный профиль может использоваться для имитации данных, полученных из традиционной системы в устойчивом состоянии, где изменение тока в зависимости от времени является, по существу, постоянным.
Профили тока при переходном процессе, полученные из последовательностей стробированных амперометрических импульсов, и выведенные контурные значения тока существенно отличаются от профилей тока, полученных известным анализом с использованием одиночного импульса считывания. Тогда как токи, записанные по одиночному импульсу считывания, происходят от одиночной релаксации/диффузии, каждый момент времени на контурном профиле токов при переходном процессе возникает из возбуждения после независимого процесса релаксации/диффузии. Более того, по мере того, как продолжительность возбуждения возрастает, взаимозависимость между током и концентрацией анализируемого вещества может уменьшаться, зачастую вследствие гематокритного эффекта. Таким образом, точность анализа, использующего многочисленные короткие возбуждения, может быть повышена по сравнению с анализом, использующим более длинные импульсы считывания, имеющие длительность объединенных многочисленных возбуждений.
Возвращаясь к фиг.6A, невозвратная точка 605 достигается в профиле тока, когда последнее по времени значение тока, полученное для возбуждения, представляет наибольшее последнее по времени значение тока, полученное для любого возбуждения. Таким образом, для фиг.6A невозвратная точка достигается около за 5 секунд. Для каждой из концентраций глюкозы равновесие относительно регидратации DBL может достигаться при наивысшем значении тока в контурном профиле для каждой концентрации глюкозы. Таким образом, токи при переходных процессах по фиг.6A преобразуются в токи контуров по фиг.6B, отсчет 610 (самый высокий) и 620 (самый низкий) утверждают, что равновесие было достигнуто касательно диффузии анализируемого препарата в DBL и регидратации DBL за около пять секунд для концентрации глюкозы 600 мг/дл.
Значения токов, записанные при относительно постоянной скорости диффузии, минимизируют неточности, которые, в ином случае, привносились бы колебаниями скоростей регидратации и диффузии реактивов. Таким образом, как только достигнута относительно постоянная скорость диффузии, записанные значения тока более точно соответствуют концентрации анализируемого препарата и, таким образом, анализируемого вещества. Более того, что касается фиг.6B, полный анализ может завершаться лишь за семь секунд, поскольку, как только известно наивысшее значение 610 тока контурного профиля, его значение может непосредственно сопоставляться концентрации анализируемого вещества. Дополнительные измерительные точки могут быть получены, чтобы снизить фоновую погрешность, относящуюся к медиатору, как обсуждено ранее.
Фиг.6C показывает контурные профили тока, подготовленные из профилей тока при переходном процессе сформированных последовательностью импульсов, изображенных на фиг.5E. Во время каждого 0,25-секундного возбуждения значения тока записывались в середине (~0,125 секунды) и конце (~0,25 секунды), которые могут использоваться для определения постоянной затухания. С использованием более длинного начального импульса с короткими возбуждениями и относительно длительными релаксациями анализ может завершаться около за четыре секунды.
Фиг.6D - диаграмма выходных сигналов относительно входных сигналов для электрохимической системы, использующей последовательности стробированных амперометрических импульсов. Входные сигналы являются потенциалами, приложенными к образцу биологической жидкости. Входные сигналы включают в себя входной сигнал опроса и входной сигнал оценки. Выходные сигналы являются токами, формируемыми из образца. Выходные сигналы включают в себя выходной сигнал опроса и выходной сигнал оценки. Образец формирует выходной сигнал оценки из окислительно-восстановительной реакции глюкозы в цельной крови в ответ на входной сигнал оценки. Входной и выходной сигналы могут быть предназначены для биодатчика, имеющего рабочий и противоэлектроды. Могут использоваться другие биодатчики, в том числе с дополнительными электродами и разными конфигурациями. Могут измеряться концентрации других анализируемых веществ, в том числе таковые в других биологических жидкостях. Могут формироваться другие выходные сигналы, в том числе те, которые спадают в начале, и те, которые спадают во всех импульсах.
Во время исследования образец биологической жидкости помещается в биодатчик. Биодатчик прикладывает сигнал опроса к образцу от около -1,25 секунд до около 0 секунд. Импульсы имеют длительность импульса около 5-10 мс и период повторения импульсов около 125 мс. Биодатчик формирует выходной сигнал опроса в ответ на входной сигнал опроса. Биодатчик измеряет выходной сигнал опроса. Биодатчик может иметь стабилизатор напряжения, который подает выходной сигнал опроса на вход аналогового компаратора.
Когда выходной сигнал опроса является равным или большим, чем пороговое значение опроса, биодатчик прикладывает входной сигнал оценки к электродам от около 0 секунд до около 7 секунд. Пороговым значением опроса может быть около 250 нА. Компаратор может сравнивать выходной сигнала опроса с пороговым значением опроса. Когда выходной сигнал опроса превышает пороговое значение опроса, выходной сигнал компаратора может инициировать запуск входного сигнала оценки.
Во время входного сигнала оценки биодатчик применяет рабочий цикл с первым импульсом, имеющим потенциал около в 400 мВ в течение около 1 секунды к рабочему и противоэлектродам. Первый импульс сопровождается 0,5-секундной релаксацией, которая может быть, по существу, разомкнутой цепью или тому подобным. Выходной сигнал или ток оценки в пределах первого импульса измеряется и сохраняется в устройстве памяти. Биодатчик может прикладывать второй импульс к рабочему и противоэлектродам при около 200 мВ, около в течение 1 секунды. Выходной сигнал или ток оценки в пределах второго импульса измеряется и сохраняется в устройстве памяти. Биодатчик продолжает прикладывание импульсов из входного сигнала оценки к рабочему и противоэлектродам до конца периода оценки или до тех пор, пока требуется биодатчиком. Период оценки может составлять около 7 секунд. Биодатчик может измерять и сохранять выходной сигнал или ток оценки в пределах каждого импульса.
Входной сигнал опроса является электрическим сигналом, таким как ток или потенциал, который пульсирует или включается и выключается при заданной частоте или периоде повторения. Образец формирует выходной сигнал опроса в ответ на входной сигнал опроса. Выходной сигнал опроса является электрическим сигналом, таким как ток или потенциал. Биодатчик может показывать выходной сигнал опроса на устройстве отображения и/или может сохранять выходной сигнал оценки в устройстве памяти. Биодатчик может применять сигнал опроса для выявления, когда образец соединен с электродами. Биодатчик может использовать другие способы и устройства для выявления, когда образец доступен для анализа.
Входной сигнал опроса является рабочим циклом, в котором последовательность импульсов опроса разделена релаксациями опроса. Во время импульса опроса электрический сигнал включен. Во время релаксации опроса электрический сигнал выключен. Включенное состояние может включать в себя промежутки времени, когда электрический сигнал присутствует. Выключенное состояние может включать в себя промежутки времени, когда электрический сигнал не присутствует. Выключенное состояние не может включать в себя промежутки времени, когда электрический сигнал присутствует, но, по существу, не имеет амплитуды. Электрический сигнал может переключаться между включенным состоянием и выключенным состоянием, соответственно посредством замыкания и размыкания электрической цепи. Электрическая цепь может размыкаться и замыкаться механически, электрически или подобным образом.
Входной сигнал опроса может содержать один или более периодов повторения импульсов опроса. Период повторения импульсов опроса является суммой импульса опроса и релаксации опроса. Каждый импульс опроса имеет амплитуду и длительность импульса опроса. Амплитуда указывает интенсивность потенциала, тока или тому подобного для электрического сигнала. Амплитуда может изменяться или быть постоянной в течение импульса опроса. Длительность импульса опроса является временной продолжительностью импульса опроса. Длительности импульсов опроса во входном сигнале опроса могут изменяться или быть, по существу, одинаковыми. Каждая релаксация опроса имеет длительность релаксации опроса, которая является временной продолжительностью релаксации опроса. Длительности релаксаций опроса во входном сигнале опроса могут изменяться или быть, по существу, одинаковыми.
Входной сигнал опроса может иметь длительность импульса опроса менее чем около 300 миллисекунд (мс) и период повторения импульсов опроса менее чем около 1 секунды. Входной сигнал опроса может иметь длительность импульса опроса менее чем около 100 мс и период повторения импульсов опроса менее чем около 500 мс. Входной сигнал опроса может иметь длительность импульса опроса в диапазоне от около 0,5 мс до около 75 мс и период повторения импульсов опроса в диапазоне от около 5 мс до около 300 мс. Входной сигнал опроса может иметь длительность импульса опроса в диапазоне от около 1 мс до около 50 мс и период повторения импульсов опроса в диапазоне от около 10 мс до около 250 мс. Входной сигнал опроса может иметь длительность импульса опроса около в 5 мс и период повторения импульсов опроса около в 125 мс. Входной сигнал опроса может иметь другие длительности импульсов и периоды повторения импульсов.
Биодатчик может прикладывать входной сигнал опроса к образцу в течение периода опроса. Период опроса может быть меньшим, чем около 15 минут, 5 минут, 2 минут или 1 минуты. Период опроса может быть более длительным в зависимости от того, каким образом пользователь использует биодатчик. Период опроса может быть в диапазоне от около 0,5 секунд (с) до около 15 минут. Период опроса может быть в диапазоне от около 5 с до около 5 минут. Период опроса может быть в диапазоне от около 10 с до около 2 минут. Период опроса может быть в диапазоне от около 20 с до около 60 с. Период опроса может быть в диапазоне от около 30 с до около 40 с. Период опроса может содержать менее чем около 200, 100, 50 или 25 периодов повторения импульсов. Период опроса может содержать от около 2 до около 150 периодов повторения импульсов. Период опроса может содержать от около 5 до около 50 периодов повторения импульсов. Период опроса может содержать от около 5 до около 15 периодов повторения импульсов. Период опроса может содержать около 10 периодов повторения импульсов. Могут использоваться другие периоды опроса.
Биодатчик применяет входной сигнал оценки, когда выходной сигнал опроса равен или больше, чем пороговое значение опроса. Пороговое значение опроса может быть большим, чем около 5 процентов (%) ожидаемого входного сигнала оценки в начале первого импульса. Пороговое значение опроса может быть большим, чем около 15% ожидаемого входного сигнала оценки в начале первого импульса. Пороговое значение опроса может быть в диапазоне от около 5 до около 50% ожидаемого входного сигнала оценки в начале первого импульса. Могут использоваться другие пороговые значения оценки. Биодатчик может указывать, что выходной сигнал опроса является равным или большим, чем пороговое значение опроса, на устройстве отображения.
Входной сигнал оценки является электрическим сигналом, таким как ток или потенциал, который пульсирует или включается и выключается при заданной частоте или периоде повторения. Образец формирует выходной сигнал оценки в ответ на входной сигнал оценки. Выходной сигнал оценки является электрическим сигналом, таким как ток или потенциал.
Входной сигнал оценки является последовательностью импульсов оценки, разделенных релаксациями оценки. Во время импульса оценки электрический сигнал включен. Во время релаксации оценки электрический сигнал выключен. Включенное состояние включает в себя промежутки времени, когда электрический сигнал присутствует. Выключенное состояние включает в себя промежутки времени, когда электрический сигнал не присутствует, и не включает в себя промежутки времени, когда электрический сигнал присутствует, но, по существу, не имеет амплитуды. Электрический сигнал переключается между включенным состоянием и выключенным состоянием, соответственно посредством замыкания и размыкания электрической цепи. Электрическая цепь может размыкаться и замыкаться механически, электрически или подобным образом. Входной сигнал оценки может содержать один или более периодов повторения импульсов оценки. Период повторения импульсов оценки является суммой импульса оценки и релаксации оценки. Каждый импульс оценки имеет амплитуду и длительность импульса оценки. Амплитуда указывает интенсивность потенциала, тока или тому подобного у электрического сигнала. Амплитуда может изменяться или быть постоянной в течение импульса оценки. Длительность импульса оценки является временной продолжительностью импульса оценки. Длительности импульсов оценки во входном сигнале оценки могут изменяться или быть, по существу, одинаковыми. Каждая релаксация оценки имеет длительность релаксации оценки, которая является временной продолжительностью релаксации оценки. Длительности релаксации оценки во входном сигнале оценки могут изменяться или быть, по существу, одинаковыми. Входной сигнал оценки может иметь длительность импульса оценки менее чем около 5 с и период повторения импульсов оценки менее чем около 15 с. Входной сигнал оценки может иметь длительность импульса оценки менее чем около 3, 2, 1,5 или 1 с и период повторения импульсов оценки менее чем около 13, 7, 4, 3, 2,5 или 1,5 с. Входной сигнал оценки может иметь длительность импульса оценки в диапазоне от около 0,1 с до около 3 с и период повторения импульсов оценки в диапазоне от около 0,2 с до около 6 с. Входной сигнал оценки может иметь длительность импульса оценки в диапазоне от около 0,1 с до около 2 с и период повторения импульсов оценки в диапазоне от около 0,2 с до около 4 с. Входной сигнал оценки может иметь длительность импульса оценки в диапазоне от около 0,1 с до около 1,5 с и период повторения импульсов оценки в диапазоне от около 0,2 с до около 3,5 с. Входной сигнал оценки может иметь длительность импульса оценки в диапазоне от около 0,4 с до около 1,2 с и период повторения импульсов оценки в диапазоне от около 0,6 с до около 3,7 с. Входной сигнал оценки может иметь длительность импульса оценки в диапазоне от около 0,5 с до около 1,5 с и период повторения импульсов оценки в диапазоне от около 0,75 с до около 2,0 с. Входной сигнал оценки может иметь длительность импульса оценки около в 1 с и период повторения импульсов оценки около в 1,5 с. Входной сигнал оценки может иметь другие длительности импульсов и периоды повторения импульсов.
Биодатчик прикладывает входной сигнал оценки к образцу в течение периода оценки. Период оценки может иметь такую же или иную длительность, чем период опроса. Период оценки входного сигнала оценки может быть меньшим, чем около 180, 120, 90, 60, 30, 15, 10 или 5 с. Период оценки может быть в диапазоне от около 1 с до около 100 с. Период оценки может быть в диапазоне от около 1 с до около 25 с. Период оценки может быть в диапазоне от около 1 с до около 10 с. Период оценки может быть в диапазоне от около 2 с до около 3 с. Период оценки может составлять около 2,5 с. Период оценки может быть меньшим, чем около 50, 25, 20, 15, 10, 8, 6 или 4 периода повторения импульсов оценки. Период оценки может содержать периоды повторения импульсов оценки в диапазоне от около 2 до около 50. Период оценки может содержать периоды повторения импульсов оценки в диапазоне от около 2 до около 25. Период оценки может содержать периоды повторения импульсов оценки в диапазоне от около 2 до около 15. Период оценки может содержать около 10 периодов повторения импульсов оценки. Могут использоваться другие периоды оценки.
Фиг.7A и 7B - графики, иллюстрирующие улучшение в точности измерения, когда DBL комбинируется с коротким импульсом считывания. Образцы цельной крови объединялись с феррицианидом при коэффициенте разбавления 1:5 для представления лежащей в основе концентрации глюкозы и измерялись с помощью 1-секундного импульса считывания. Таким образом, исходные образцы WB с гематокритом 20%, 40% и 60% разбавлялись до гематокрита 16%, 32% и 48% (снижение на 20% всех трех значений гематокрита). Линии 20%, 40% и 60% изображают ток, измеренный для образцов крови, содержащей гематокрит 16%, 32% и 48% соответственно.
Фиг.7A показывает неточности, привнесенные гематокритом и другими эффектами пластинки датчика с неизолированными электродами, не имеющей DBL. Неточность изображена в виде разницы между линиями с гематокритом 20% и 60% (суммарного размаха гематокритной систематической погрешности) и представляет максимальную погрешность измерений, относящуюся к гематокритному эффекту. Меньшие значения систематической погрешности представляют более точный результат. Подобное качество функционирования наблюдалось, когда DBL использовался с более продолжительным импульсом считывания, как обсуждено выше в отношении фиг.4A.
Наоборот, фиг.7B показывает заметное уменьшение расстояния между калибровочными линиями 20% и 60%, когда DBL комбинируется с 1-секундным импульсом считывания. Отдельный DBL из полимера PEO и KC1 (без реактивов) 10% отпечатывалось на проводнике, как используемый для фиг.7A, приведенной выше. Суммарный гематокритный размах систематической погрешности с DBL/коротким импульсом считывания был почти на две трети меньшим, чем суммарный размах систематической погрешности без DBL. Таким образом, последовательности импульсов, включающие в себя многочисленные рабочие циклы, в сочетании с DBL могут значительно повышать точность измерения и обеспечивать требуемое снижение медиаторного фона.
Фиг.7C и 7D иллюстрируют уменьшение гематокритной систематической погрешности, которое может быть получено, когда последовательность стробированных амперометрических импульсов комбинируется с DBL. Фиг.7C демонстрирует, что систематическая погрешность измерения, относящаяся к гематокритному эффекту, находится в пределах ±5%, когда DBL комбинировался с последовательностью импульсов по фиг.5E, и значения тока записывались при 14,875 секундах или 0,125 секундах от последнего импульса. Для сравнения, фиг.7D устанавливает, что систематическая погрешность возрастает до ±15%, когда значение тока при 16 секундах (1,25 секундах от последнего импульса) использовалось для определения концентрации глюкозы в образце. Таким образом, чем больше длительность возбуждения, тем больше наблюдаемая гематокритная систематическая погрешность.
В дополнение к способности настоящего изобретения снижать погрешность от гематокритного эффекта и медиаторного фонового сигнала, комбинация профиля тока при переходном процессе каждого возбуждения и результирующих контурных профилей может использоваться для предоставления многочисленных наборов калибровочных констант для системы датчика, соответственно с повышением точности анализа. Каждый полученный набор калибровочных констант может использоваться для установления отношения определенного показания тока к определенной концентрации анализируемого препарата в образце. Таким образом, в одном из аспектов повышение точности может быть получено усреднением значений глюкозы, полученных с использованием многочисленных наборов калибровочных констант.
Традиционные системы электрохимических датчиков обычно используют один набор калибровочных констант, такой как крутизна и перехват, для преобразования показаний тока в соответствующую концентрацию анализируемого вещества в образце. Однако одиночный набор калибровочных констант может иметь следствием погрешности в концентрации анализируемого вещества, определенной по записанным значениям тока, так как случайные шумы включены в измерение.
Взятием значения тока в фиксированный момент времени в пределах каждого рабочего цикла последовательности импульсов по настоящему изобретению могут создаваться многочисленные наборы калибровочных констант. Фиг.8 графически изображает токи конечных точек, записанные при 8,5, 10, 11,5, 13 и 14,5 секундах (рабочие циклы 6-9 и первый участок завершающего импульса считывания), когда последовательность импульсов, изображенная на фиг.5B прикладывалась к образцам WB, содержащим различные концентрации глюкозы. Каждая из этих пяти калибровочных линий является независимой от других и может использоваться, по меньшей мере, двумя способами.
Во-первых, многочисленные наборы калибровочных констант могут использоваться для определения количества рабочих циклов, которые должны применяться во время последовательности импульсов, чтобы получать требуемую точность, воспроизводимость и время оценки. Например, если значения тока, полученные по первым трем возбуждениям, указывают высокую концентрацию глюкозы, такую как >150 или 200 мг/дл, система датчика может завершать анализ при около 5,5 секундах, таким образом, значительно укорачивая время, требуемое для анализа. Такое укорачивание может быть возможным, так как невоспроизводимость при высоких концентрациях глюкозы типично является меньшей, чем при более низких концентрациях глюкозы. Наоборот, если значения тока, полученные по первым трем возбуждениям, указывают низкую концентрацию глюкозы, такую как <150 или 100 мг/дл, система датчика может растягивать анализ до более чем 7, например, более чем 8 или 10 секунд, чтобы повысить точность и/или воспроизводимость анализа.
Во-вторых, многочисленные наборы калибровочных констант могут использоваться для повышения точности и/или воспроизводимости анализа усреднением. Например, если целевым временем измерения глюкозы является 11,5 секунд, токи при 8,5, 10 и 11,5 секундах могут использоваться для расчета концентраций глюкозы с использованием значений крутизны и перехватов из соответствующих калибровочных линий; поэтому, G8,5=(i8,5-Int8,5)/Slope8,5, G10=(i10-Int10)/Slope10 и G11,5=(i11,5-Int11,5)/Slope11,5. Теоретически, эти три значения глюкозы должны быть эквивалентны, отличаясь только случайными отклонениями. Таким образом, значения G8,5, G10 и G11,5 глюкозы могут усредняться, и может рассчитываться окончательное значение глюкозы (G8,5+G10+G11,5)/3. Усреднение значений из калибровочных линий может обеспечивать снижение шумов в размере 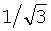 .
.
Непредвиденным преимуществом последовательностей стробированных амперометрических импульсов, включающих в себя относительно короткие возбуждения и относительно длинные релаксации, такие как изображенные на фиг.5E, является способность упрощать калибровку. Наряду с тем, что многочисленные наборы калибровочных констант, которые могут быть получены по профилям переходных процессов и контуров, могут обеспечивать преимущество в отношении точности анализа, последовательность импульсов, такая как изображенная на фиг.5E, может обеспечивать точность, подобную полученной с использованием многочисленных наборов калибровочных констант, по одиночному набору калибровочных констант. Наряду с отсутствием предположения обнаруживаться какой-либо конкретной теорией, этот результат может относиться к относительно длительным временам релаксации в сравнении с короткими релаксациями. Длительные времена релаксации могут обеспечивать состояние, где средняя скорость превращения анализируемого препарата во время возбуждения уравновешивается скоростью диффузии анализируемого препарата в DBL. Этим способом многочисленные наборы калибровочных констант могут сворачиваться в одиночный набор, а преобразование записанных данных в концентрацию анализируемого вещества может упрощаться выполнением последовательности операций усреднения над записанными данными о токе до определения концентрации анализируемого вещества.
Комбинация профилей тока при переходном процессе каждого возбуждения и результирующих контурных профилей также может использоваться для определения, была ли пластинка датчика недозаполнена образцом, таким образом, предоставляя пользователю возможность добавлять дополнительный образец на пластинку датчика. В дополнение к рабочему и противоэлектродам - традиционные системы датчиков могут определять недозаполненное состояние благодаря использованию третьего электрода или пары электродов; однако третий электрод или пара электродов добавляют сложность и себестоимость системе датчика.
Традиционные двухэлектродные системы могут распознавать, что анализ является «плохим», но могут не определять, была ли причина для неудавшегося анализа вызвана недозаполнением или дефектной пластинкой датчика. Способность определять, недозаполнение ли вызывало несостоятельность анализа, является полезной, так как оно может исправляться добавлением дополнительного образца на ту же самую пластинку датчика и повторением анализа, таким образом, предохраняя хорошую пластинку от браковки.
Фиг.9A изображает профили тока при переходном процессе, полученные из последовательности импульсов, изображенной на фиг.5B для 10 анализов, каждый из которых использует разную пластинку датчика, где 2,0 мкл образца помещалось на пластинку. В зависимости от скорости заполнения объема цокольного зазора определенной пластинки датчика 2,0 мкл образца может быть или может не быть достаточным для заполнения пластинки.
На фиг.9B профили тока при переходном процессе по фиг.9A были преобразованы в контурные профили скорости затухания в качестве функции времени. В одном из аспектов скорость затухания может быть представлена в виде константы K, определенной любым из следующих равенств:
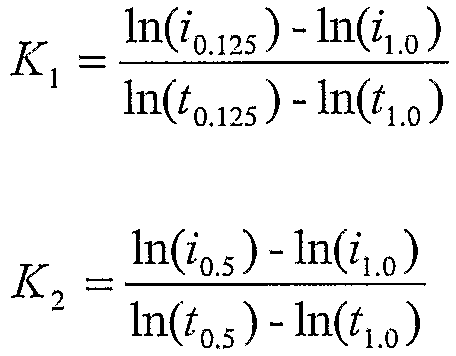
где значения 0,125, 0,5 и 1,0 - в секундах. Таким образом, с использованием константы K процесса затухания профили тока по фиг.9A могут преобразовываться в профили постоянной затухания по фиг.9B.
Фиг.9B устанавливает, что существует существенная разница между профилями затухания недозаполненных датчиков и нормально заполненных датчиков, особенно во временном диапазоне от 3 до 7 секунд. Недозаполнение может определяться из профилей постоянной затухания сравнением разницы между действующей постоянной затухания и заранее выбранным значением. Например, если -0,1 выбрано в качестве верхнего предела для нормально заполненного датчика, что касается фиг.9B, любая постоянная Kl, имеющая значение меньшее, чем -0,1, определенное по возбуждениям в течение от 3 до 5-секундного промежутка времени, может считаться нормально заполненным. Подобным образом любой датчик, имеющий значение K1, большее, чем -0,1, может считаться недозаполненным. Этим способом недозаполнение может определяться в ответ на скорость затухания, полученную из профиля тока при переходном процессе.
Таким образом, на фиг.9B пластинки датчиков, представленные последовательностями 3 и 8, были достаточно заполненными, тогда как восемь пластинок датчиков, представленные последовательностями 1-2, 4-7 и 9-10 были недозаполненными. Этим способом последовательности стробированных амперометрических импульсов по настоящему изобретению предоставляли возможность для выявления недозаполнения в двухэлектродной пластинке датчика, функции, типично требующей третьего электрода для традиционных систем датчиков. Более того, определение недозаполнения производилось за менее чем десять секунд, предоставляя время, чтобы измерительное устройство подавало сигнал пользователю, например, посредством отправки сигнала на светоизлучающее устройство или устройство отображения для добавления большего образца на пластинку.
Так как недозаполнение может определяться по профилям токов при переходном процессе, те же самые значения тока, используемые для определения наличия и/или концентрации анализируемого вещества, могут использоваться для определения, существует ли состояние недозаполнения. Таким образом, недозаполнение может определяться в течение многочисленных рабочих циклов последовательности импульсов без удлинения продолжительности электрохимического анализа сверх требуемой для определения концентрации.
Комбинация профиля тока при переходном процессе каждого возбуждения и результирующего контурного профиля также может использоваться для определения, может ли изменение в температуре образца наносить ущерб анализу. Традиционная система датчика включает в себя термистор в измерительном устройстве или на пластинке для предоставления температуры устройства или пластинки соответственно. Несмотря на то, что эта температура является приближенным значением температуры образца, типично устройство или пластинка находятся при иной температуре, чем образец. Перепад температур между устройством или пластинкой и образцом может привносить систематическую погрешность в анализ.
Посредством определения скорости затухания, например, с помощью постоянной K, как обсуждено ранее, может определяться температура образца. Фиг.10 изображает постоянные K, вычерченные в виде функции температуры, которая была получена по пятому возбуждению последовательности импульсов для концентраций глюкозы в 50, 100 и 400 мг/дл. Графики устанавливают, что скорость затухания повышается по абсолютному значению с повышением температуры. Наряду с нежеланием ограничиваться какой бы то ни было конкретной теорией, это явление может относиться к более низким температурам, замедляющим скорость диффузии различных составляющих, присутствующих в цокольном зазоре. Этим способом температура образца может определяться в ответ на скорость затухания, полученную из профиля тока при переходном процессе.
Так как температура образца может определяться по профилям токов при переходном процессе, те же самые значения тока, используемые для определения наличия и/или концентрации анализируемого вещества, могут использоваться для определения температуры образца. Таким образом, температура образца может определяться в течение многочисленных рабочих циклов последовательности импульсов без удлинения продолжительности электрохимического анализа сверх требуемой для определения концентрации.
В одном из аспектов температура образца может определяться вычислением K по следующему равенству:
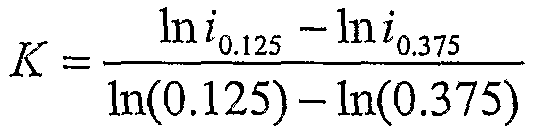
где i0,125 и i0,375 - токи при 0,125 и 0,375 секундах из возбуждения, наиболее чувствительного к изменению температуры, такого как возбуждение, формирующее самое чувствительное затухание тока в отношении изменения температуры ln(0,125) и ln(0,375) - выражения натуральных логарифмов времен при 0,125 и 0,375 секундах соответственно. Из графика этих постоянных K в зависимости от температуры, как показано на фиг.10, температура образца может определяться корреляционной функцией графика. Корреляционная функция может быть подбором многочлена по кривой. Температура, определенная по этому графику, может быть отличной от температуры устройства и может более точно отражать температуру образца.
Преимущество определения температуры образца, в отличие от устройства, состоит в том, что продолжительность анализа может регулироваться, чтобы предусмотреть достаточное время, чтобы регидратация DBL достигла равновесного состояния, таким образом, повышая точность анализа. Например, если температура образца, определенная в течение последовательности импульсов, является, по меньшей мере, на 5 или 10°С ниже температуры окружающей среды, последовательность импульсов может удлиняться, например, дополнительными рабочими циклами.
Фиг.11 изображает схему измерительного устройства 1100, включающего в себя контакт 1120 в электрической связи с электрической схемой 1110 и устройством 1130 отображения. В одном из аспектов, измерительное устройство 1100 является портативным и ручным и чтобы принимать пластинку датчика, такую как пластинка 100 по фиг.1A. В еще одном аспекте измерительное устройство 1100 является ручным измерительным устройством для приема пластинки датчика и реализации последовательностей стробированных амперометрических импульсов.
Контакты 1120 обеспечивают электрическую связь с электрической схемой 1110 и контактами пластинки датчика, такими как контакты 170 и 180 пластинки 100 датчика, изображенной на фиг.1B. Электрическая схема 1110 может включать в себя электрическое зарядное устройство 1150, процессор 1140 и машиночитаемый запоминающий носитель 1145. Электрическое зарядное устройство 1150 может быть стабилизатором напряжения, генератором сигналов или тому подобным. Таким образом, зарядное устройство 150 может прикладывать напряжение к контактам 1120 наряду с записью результирующего тока, чтобы функционировать как зарядно-записывающее устройство.
Процессор 1140 может быть электрически связан с зарядным устройством 1150, машиночитаемым запоминающим носителем 1145 и устройством 1130 отображения. Если зарядное устройство не обеспечивает запись тока, процессор 1140 может быть предназначен для записи тока с контактов 1120.
Машиночитаемый запоминающий носитель 1145 может быть любым запоминающим носителем, таким как магнитная, оптическая, полупроводниковая память и тому подобное. Машиночитаемый запоминающий носитель 1145 может быть стационарным устройством памяти или съемным устройством памяти, таким как съемная карта памяти. Устройство 1130 отображения может быть аналоговым или цифровым, в одном из аспектов - жидкокристаллическим (LCD) дисплеем, приспособленным для отображения цифрового показания.
Когда контакты пластинки датчика, удерживающей образец, находятся в электрической связи с контактами 1120, процессор 1140 может управлять зарядным устройством 1150, чтобы прикладывать последовательность стробированных амперометрических импульсов к образцу, таким образом, начиная анализ. Процессор 1140 может начинать анализ в ответ на вставку пластинки датчика, нанесение образца на предварительно вставленную пластинку датчика или, например, в ответ на пользовательский ввод.
Инструкции по реализации последовательности стробированных амперометрических импульсов могут предусматриваться машиночитаемой машинной программой, сохраненной на машиночитаемом запоминающем носителе 1145. Программа может быть объектной программой или другой программой, описывающей или управляющей функциональными возможностями, описанными в этой заявке. Данные, которые являются следствием последовательности стробированных амперометрических импульсов, могут подвергаться одной или более обработок данных, в том числе определению скоростей затухания, констант K, значений крутизны, перехватов и/или температуры образца в процессоре 1140, и результаты, такие как сопоставленная концентрация анализируемого вещества, выводятся на устройство 1130 отображения. Как с инструкциями касательно последовательности импульсов, обработка данных может приводиться в исполнение процессором 1140 из машиночитаемой машинной программы, сохраненной на машиночитаемом запоминающем носителе 1145.
Без ограничения объема, применения или реализации, способы и системы, описанные ранее, могут быть реализованы с использованием следующего алгоритма:







Алгоритм может содержать другие подпрограммы, в том числе для проверки на погрешности, такие как условия температуры и недозаполнения образца. Константы, которые могут использоваться в алгоритме, даны в Таблице III, приведенной ниже. Могут использоваться другие константы.
Несмотря на то что были описаны различные варианты осуществления изобретения, специалистам в данной области техники будет очевидно, что другие варианты осуществления и реализации возможны в пределах объема изобретения.

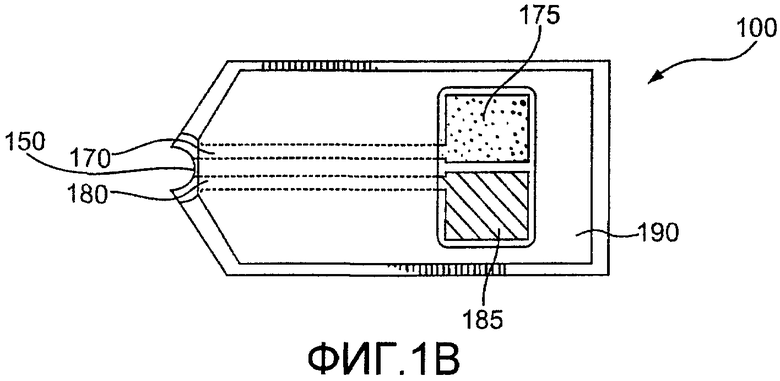
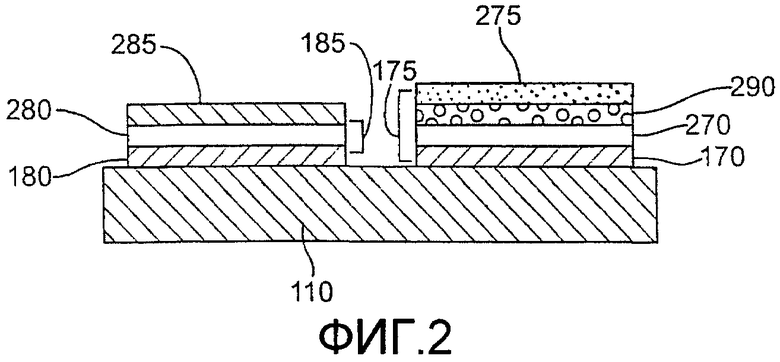
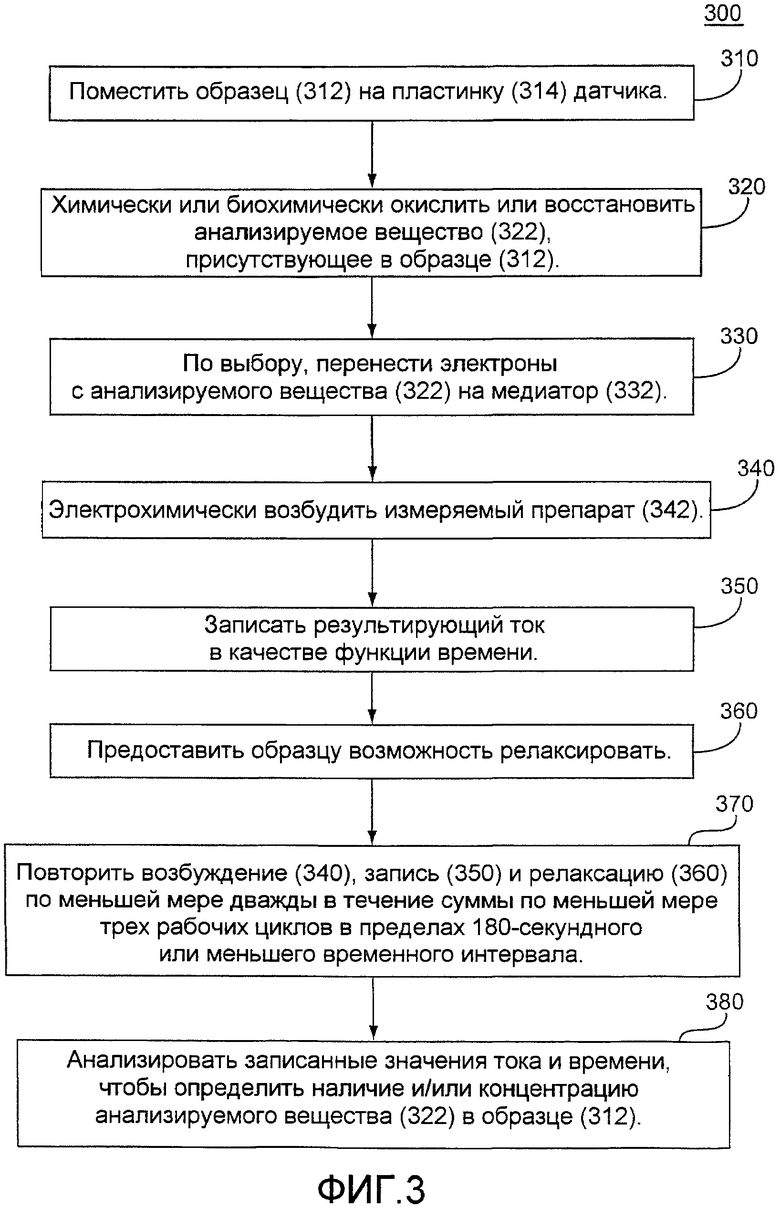

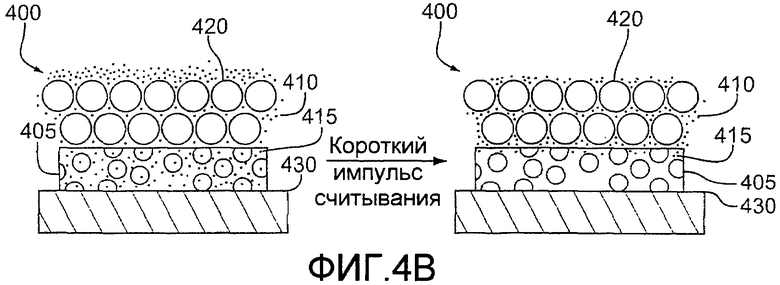

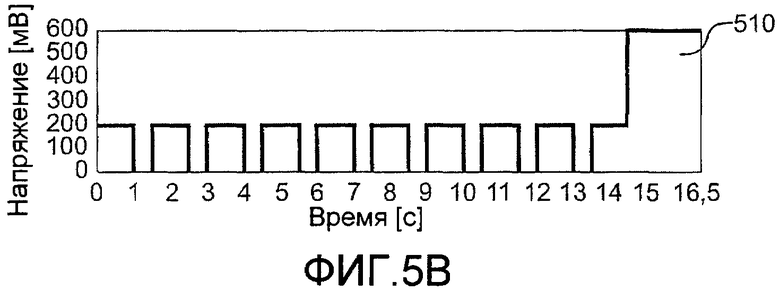
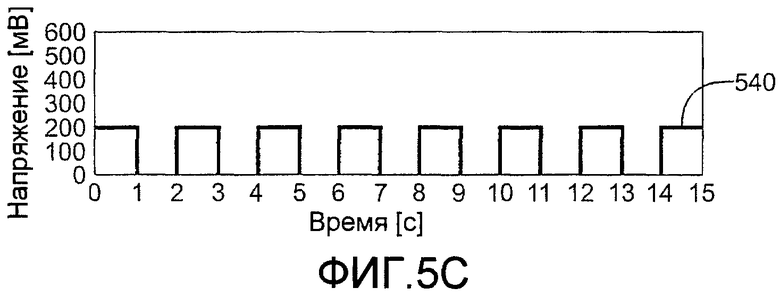
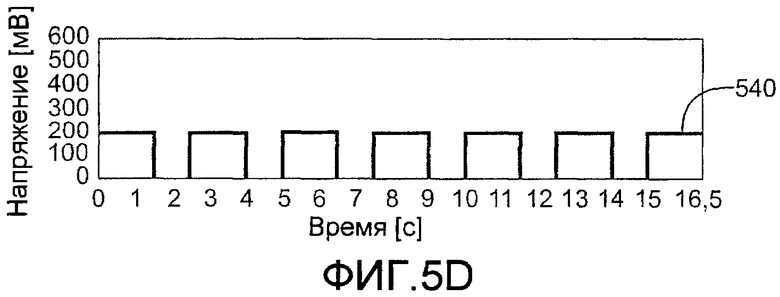
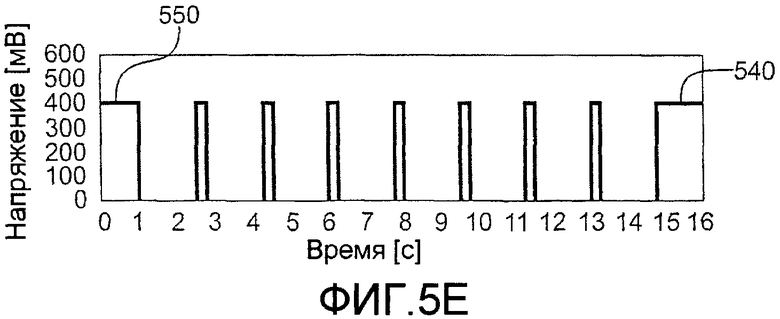
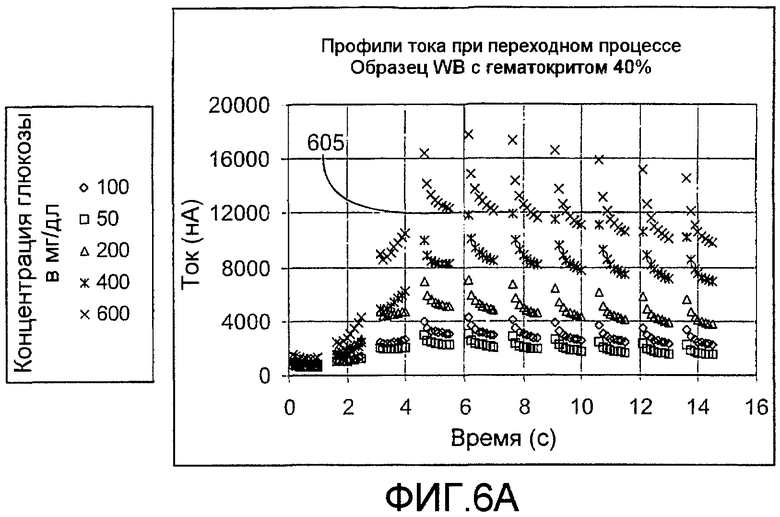
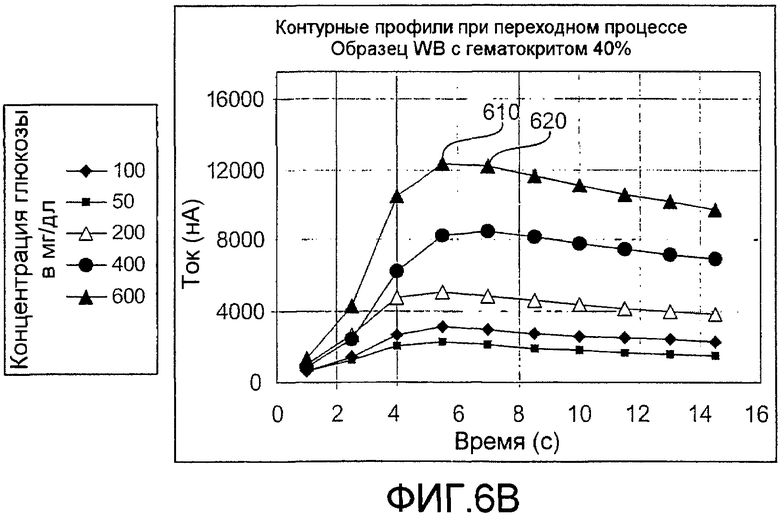
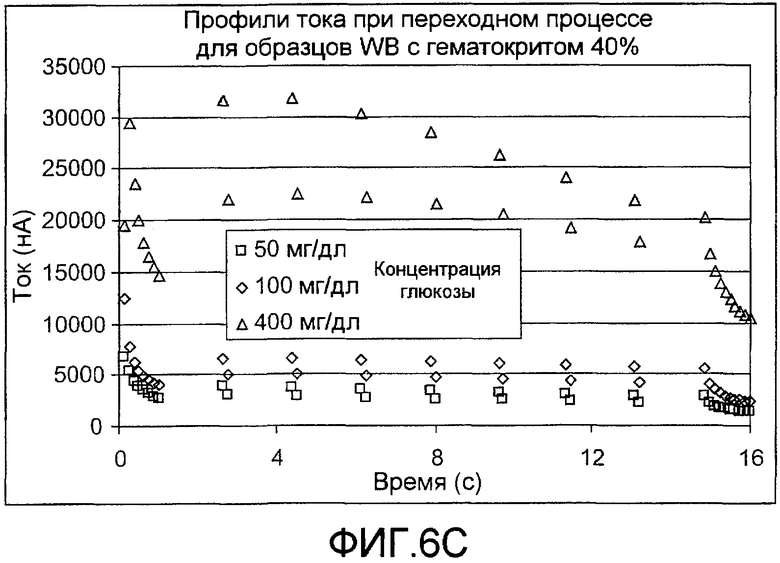
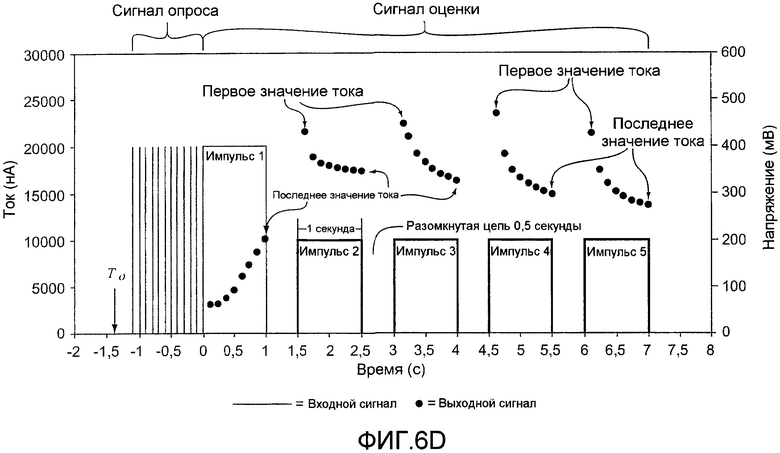
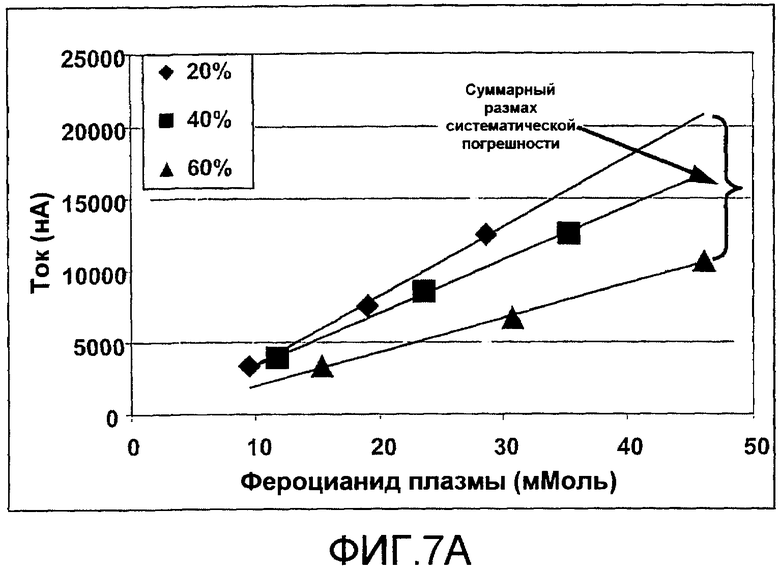
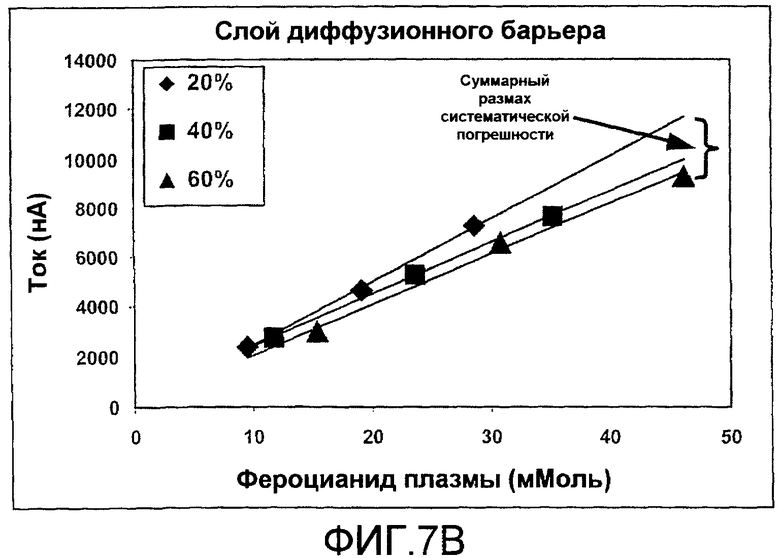
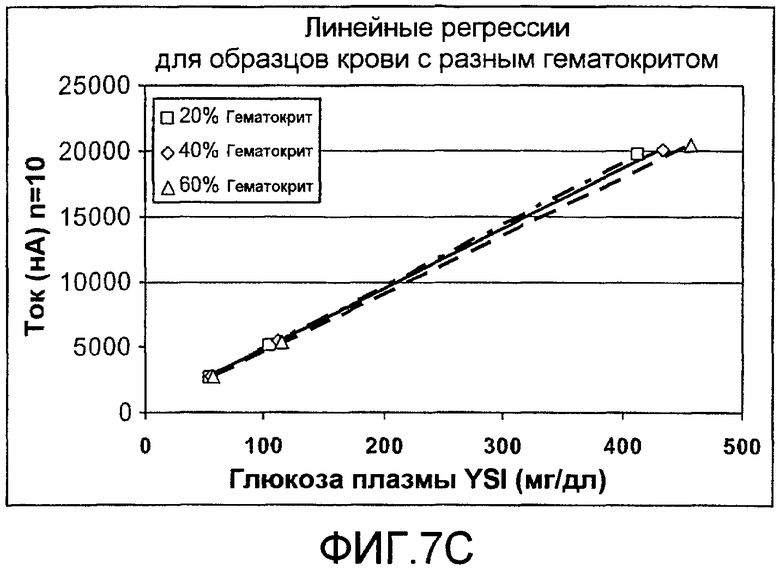
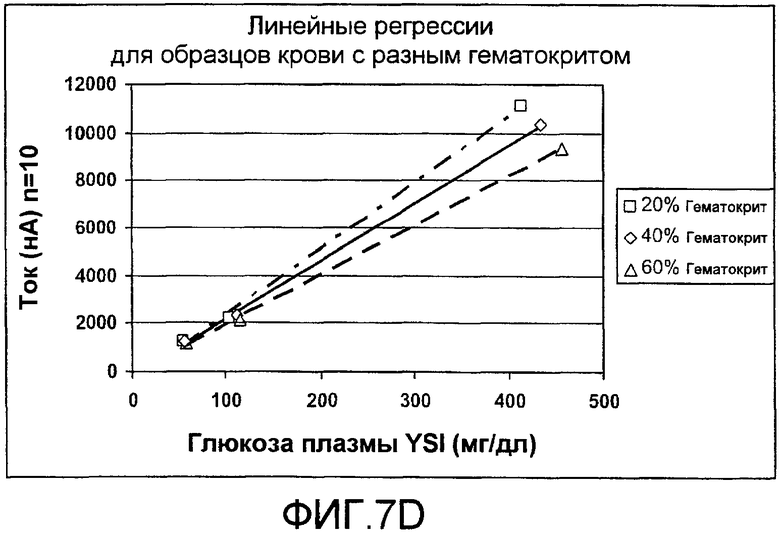
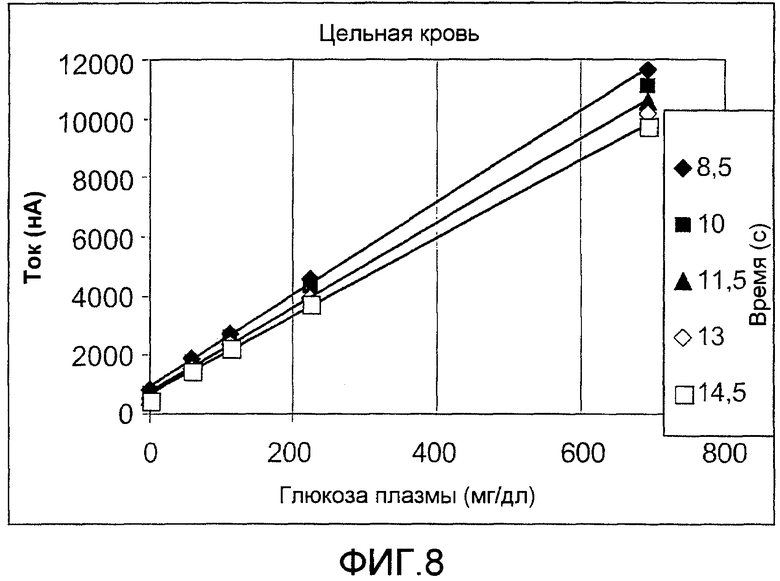
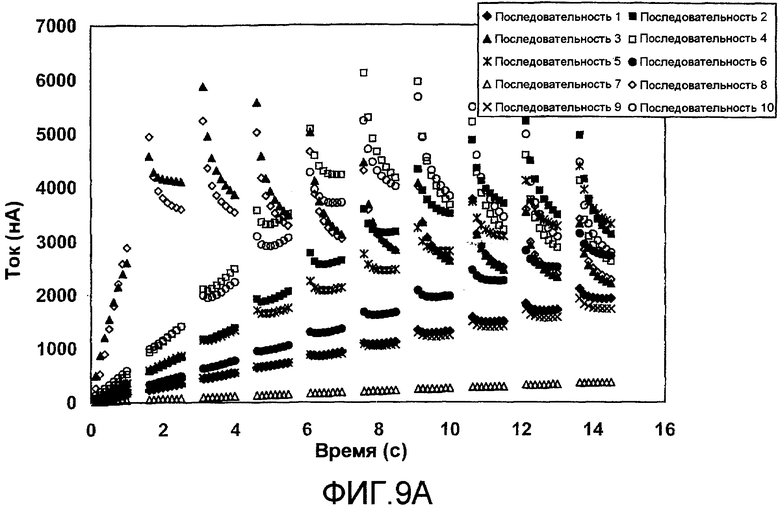
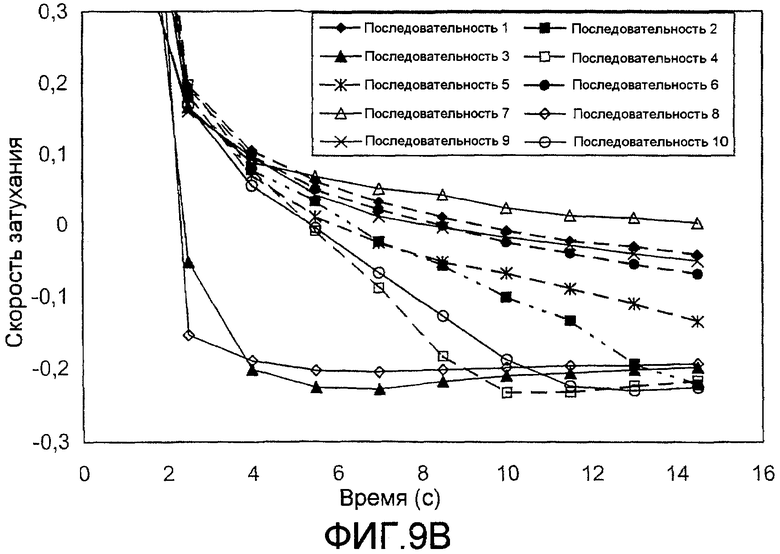
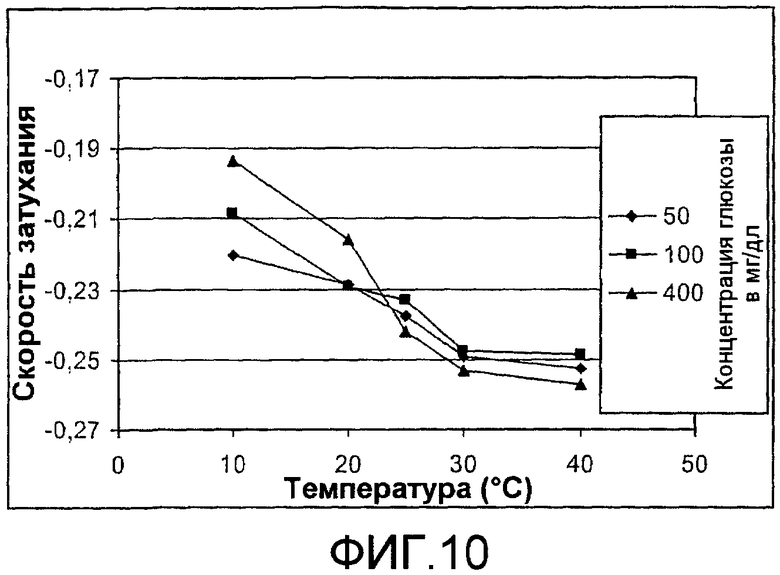
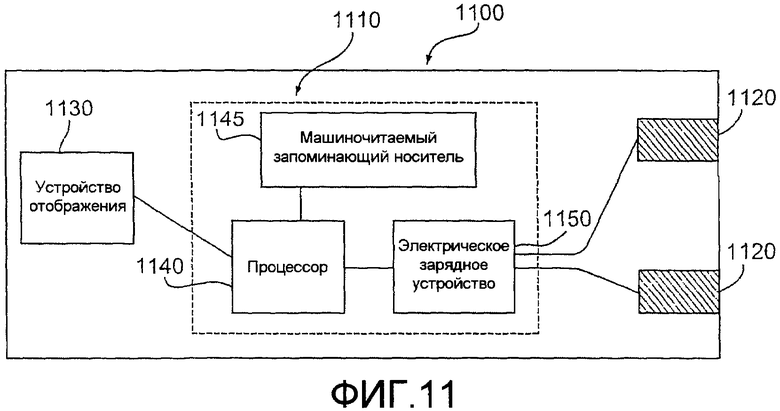
Изобретение относится к области электрохимических методов анализа. Предложена система датчика, устройство и способы для определения концентрации анализируемого вещества в образце. Последовательности стробированных амперометрических импульсов, включающие в себя многочисленные рабочие циклы последовательных возбуждений и релаксаций, обеспечивают более короткое время анализа и/или улучшают точность и/или воспроизводимость анализа. Раскрытые последовательности стробированных амперометрических импульсов могут снижать погрешности анализа, являющиеся результатом гематокритного эффекта, изменения объемов цокольного зазора, неустановившихся режимов, медиаторного фона, недозаполнения, изменений температуры в образце и одиночного набора калибровочных констант. 6 н. и 24 з.п. ф-лы, 3 табл., 11 ил.
1. Амперометрический способ определения концентрации анализируемого вещества в образце, заключающийся в том, что
прикладывают к образцу входной сигнал, содержащий, по меньшей мере, 3 рабочих цикла в пределах 180 с, причем каждый рабочий цикл содержит возбуждение и релаксацию, а входной сигнал имеет интенсивность окисления-восстановления по меньшей мере 0,01 в течение 10 с длительности входного сигнала;
измеряют выходной сигнал от возбуждения, имеющего длительность в пределах от 0,01 до 1,5 с, причем выходной сигнал реагирует на измеряемые препараты;
определяют концентрацию анализируемого вещества в образце в ответ на измеренный выходной сигнал, при этом концентрация определяется скоростью, при которой измеряемые препараты окисляются или восстанавливаются согласно входному сигналу.
2. Способ по п.1, в котором дополнительно помещают образец на пластинку датчика, причем пластинка датчика содержит рабочий электрод и противоэлектрод, электрически связанные с образцом, передают, по меньшей мере, один электрон с анализируемого вещества в образце на медиатор в пластинке датчика и прикладывают входной сигнал к рабочему электроду и противоэлектроду, при этом входной сигнал электрохимически возбуждает измеряемые препараты, выбранные из группы, состоящей из анализируемого вещества, медиатора и их комбинаций.
3. Способ по п.1, в котором образец представляет собой цельную кровь, содержащую красные кровяные тельца (эритроциты).
4. Способ по п.1, в котором измеренный выходной сигнал является наибольшим завершающим во временном значении тока, полученным из рабочих циклов.
5. Способ по п.1, в котором измеряемые препараты представляют собой медиатор, выбранный из группы, состоящей из органопереходных металлических комплексов (ОТМ), координационных комплексов, электрически активных органических молекул и их комбинаций.
6. Способ по п.1, в котором возбуждение, из которого определяют выходной сигнал, имеет длительность от 0,1 до 1,2 с.
7. Способ по п.1, в котором концентрация анализируемого вещества, определяемая заявленным способом, включает в себя меньшую систематическую погрешность, относящуюся к медиаторному фону, чем концентрация анализируемого вещества, определяемая этим или другим способом, но без использования входного сигнала, содержащего, по меньшей мере, 3 рабочих цикла в пределах 180 с.
8. Способ по п.1, в котором входной сигнал содержит от 4 до 8 рабочих циклов, прикладываемых в течение от 3 до 16 с.
9. Способ по п.1, в котором входной сигнал содержит от 3 до 18 рабочих циклов, прикладываемых в течение 30 с.
10. Способ по п.1, в котором дополнительно возбуждают измеряемый препарат, внутренний по отношению к диффузионному барьерному слою, имеющему среднюю первоначальную толщину от 1 до 30 мкм, причем диффузионный барьерный слой содержит полимерный связующий слой, который является частично водорастворимым, и, по существу, исключают из возбуждения измеряемый препарат, внешний по отношению к диффузионному барьерному слою, при этом диффузионный барьерный слой имеет внутреннее пористое пространство, чтобы вмещать и изолировать часть измеряемого препарата от образца.
11. Способ по п.1, в котором дополнительно определяют концентрацию анализируемого вещества в ответ на профиль тока, когда достигается относительно постоянная скорость диффузии измеряемого препарата.
12. Способ по п.1, в котором выходной сигнал содержит, по меньшей мере, один профиль тока, а концентрацию анализируемого вещества в образце определяют в ответ на, по меньшей мере, один профиль тока.
13. Способ по п.12, в котором возбуждения в течение рабочего времени имеют длительность от 0,1 до 1,5 с, а рабочие циклы имеют импульсный интервал от около 0,2 до около 3,5 с.
14. Способ по п.1, в котором релаксация имеет длительность от 0,1 до 3 с.
15. Способ по п.12, в котором возбуждения в течение рабочих циклов имеют длительность от 0,4 до 1,2 с, а рабочие циклы имеют импульсный интервал от около 0,6 до около 3,7 с.
16. Способ по п.12, в котором профиль тока содержит затухание при переходном процессе, при этом концентрацию анализируемого вещества определяют по затуханию при переходном процессе.
17. Способ по п.12, в котором дополнительно формируют многочисленные наборы калибровочных констант в ответ на выходной сигнал.
18. Способ по п.17, в котором дополнительно определяют количество рабочих циклов во входном сигнале в ответ на многочисленные наборы калибровочных констант.
19. Способ по п.17, в котором дополнительно
определяют концентрацию анализируемого вещества в образце в ответ на каждый набор калибровочных констант и
усредняют концентрации анализируемого вещества по наборам калибровочных констант.
20. Способ по п.12, в котором дополнительно определяют температуру образца, удерживаемого пластинкой датчика в ответ на скорость затухания профиля тока.
21. Способ по п.12, в котором дополнительно определяют, когда пластинка датчика недозаполнена, в ответ на профиль тока.
22. Способ по п.21, в котором дополнительно определяют, когда пластинка датчика недозаполнена, если скорость затухания профиля тока меньше выбранного значения.
23. Способ по п.22, в котором выбранным значением является -0,1.
24. Ручное измерительное устройство для определения концентрации анализируемого вещества в образце, предназначенное
для приема пластинки датчика, содержащее
контакты,
по меньшей мере, одно устройство отображения и
электронную схему, устанавливающую электрическую связь между контактами и устройством отображения и содержащую
электрическое зарядное устройство, электрически связанное с процессором, который электрически связан с машиночитаемым запоминающим носителем, содержащим машиночитаемую программу, которая при выполнении процессором побуждает зарядное устройство формировать входной сигнал, содержащий, по меньшей мере, 3 рабочих цикла в пределах 180 с, между контактами, причем каждый рабочий цикл содержит возбуждение и релаксацию, при этом входной сигнал имеет интенсивность окисления-восстановления по меньшей мере 0,01 в течение 10 с длительности входного сигнала;
при этом процессор измеряет выходной сигнал возбуждения, имеющего длительность от 0,01 до 1,5 с и определяет концентрацию анализируемого вещества в образце, когда процессор определяет, что измеренный выходной сигнал является наибольшим завершающим во временном значении тока, полученным из рабочих циклов.
25. Устройство по п.24, в котором образец представляет собой цельную кровь, содержащую красные кровяные тельца (эритроциты).
26. Устройство по п.24, в котором процессор предназначен для измерения, по меньшей мере, одного профиля тока на контактах и для определения концентрации анализируемого вещества в образце в ответ на, по меньшей мере, один профиль тока.
27. Способ снижения систематической погрешности, относящейся к медиаторному фону, при определении концентрации анализируемого вещества в образце, заключающийся в том, что прикладывают к образцу входной сигнал, содержащий, по меньшей мере, 3 рабочих цикла в пределах 180 с и имеющий интенсивность окисления-восстановления по меньшей мере 0,01 в течение 10 с длительности входного сигнала; генерируют измеряемые препараты из медиатора, выбранного из группы, состоящей из органопереходных металлических комплексов (ОТМ), координационных комплексов, электрически активных органических молекул и их комбинаций, определяют концентрацию анализируемого вещества в образце из возбуждения, имеющего длительность от 0,01 до 1,5 с.
28. Способ подачи сигнала пользователю для добавления дополнительного образца на пластинку датчика, заключающийся в том, что определяют, недозаполнена ли пластинка датчика, посредством определения постоянной затухания от токов, записанных в течение, по меньшей мере, двух возбуждений входного сигнала, включающего в себя, по меньшей мере, 3 рабочих цикла в пределах 180 с; и
подают сигнал пользователю для добавления дополнительного образца на пластинку датчика, если пластинка недозаполнена, и определяют концентрацию анализируемого вещества в образце из токов, записанных от входного сигнала.
29. Способ определения температуры образца, удерживаемого пластинкой датчика, заключающийся в том, что
определяют постоянную затухания по токам, записанным в течение, по меньшей мере, двух возбуждений входного сигнала, содержащего, по меньшей мере, 3 рабочих цикла в пределах 180 с; и
соотносят (устанавливают соотношение) постоянную затухания со значением температуры, и определяют концентрацию анализируемого вещества в образце из токов, записанных от входного сигнала.
30. Способ определения длительности входного сигнала, включающего в себя, по меньшей мере, 3 рабочих цикла в пределах 180 с для приложения к образцу, для определения концентрации анализируемого вещества в образце, заключающийся в том, что определяют множество калибровочных точек, определенных по токам, записанным в течение, по меньшей мере, 3 рабочих циклов; и определяют длительность входного сигнала для приложения к образцу в ответ на определенную концентрацию анализируемого вещества в образце, и определяют концентрацию анализируемого вещества в образце из токов, записанных от входного сигнала.
| WO 9858250 А2, 23.12.1998 | |||
| Способ измерения величины пульсаций импульсных высоких напряжений | 1958 |
|
SU121827A1 |
| WO 1999038003, 29.07.1999 | |||
| WO 9614026 A, 17.05.1996 | |||
| US 2004072158 A1, 15.04.2004 | |||
| US 5798031 A, 25.08.1998 | |||
| GUNASINGHAM H et al | |||
| Pulsed amperometric detection of glucose using a mediated enzyme electrode//JOURNAL OF ELECTROANALYTICAL CHEMISTRY AND INTERFACIAL ELECTROCHEMISTRY, vol.287, no.2, 25 July 1990 (1990-07-25), pages 349-362 | |||
| WO 2006042304 A, 20.04.2006. | |||
Авторы
Даты
2012-01-27—Публикация
2006-07-19—Подача