Предлагаемое изобретение относится к области органической химии, в частности к способу получения 1-ацетиладамантана.
1-Ацетиладамантан служит исходным сырьем для синтеза высокоэффективного противовирусного препарата «Ремантадина» и препаратов для ветеринарии (Н.В.Макарова, М.Н.Земцова, И.К.Моиссеев. Вестн. Ун-та им. Наяновой. Самара, 44-47 [1]; И.К.Моисеев, Н.В.Макарова, М.Н.Земцова. ЖОрХ, т.37, в. 4, 489-509 (2001) [2]).
Известные способы получения 1-ацетиладамантана основаны на синтетических трансформациях 1-замещенных адамантанов 1-AdR (R=Br, OH, CN, COOH и т.д.).
1-Бромадамантан при взаимодействии с магнием в диэтиловом эфире образует реактив Гриньяра. Полученный 1-адамантилмагнийбромид может быть превращен в 1-ацетиладамантан двумя путями: либо взаимодействием с ацетилхлоридом (выход 63%), либо с этилацетатом (выход 14%) (А.Г.Юрченко, Т.В.Федоренко. ЖОрХ, т.23, в. 5, 970-976 (1987) [3]).
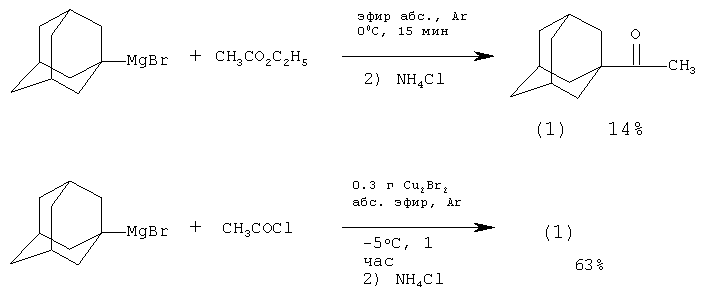
1-Адамантилмагнийбромид получают по следующей методике. В реактор помещают 3.04 г магния, продувают аргоном в течение 15 мин, прибавляют 50 мл диэтилового эфира, свежеперегнанного над дифенилкетилнатрием в токе аргона, и 0.1 мл 1,2-дибромэтана, необходимого для активирования магния. Реакционную смесь кипятят в течение 15 мин, затем при перемешивании прибавляют 2.8 г 1-бромадамантана. Перемешивание и кипячение ведут до исчезновения 1-бромадамантана, после чего смесь охлаждают до 20°С, фильтруют в атмосфере аргона. После этих процедур получено 50 мл раствора реагента Гриньяра с концентрацией 0.126 моль/л (выход 48%).
К эфирному раствору реагента Гриньяра, охлажденному до 0°С, прибавляют по каплям раствор этилацетата в 1-2 мл диэтилового эфира. Через 15 мин реакционную смесь обрабатывают насыщенным водным раствором NH4Cl, отделяют органический слой, а водный экстрагируют диэтиловым эфиром. Объединенный эфирный раствор промывают водой, сушат над сульфатом натрия и отгоняют растворитель. Остаток хроматографируют на силикагеле.
Конденсацию 1-адамантилмагнийбромида с ацетилхлоридом осуществляли по этой же методике в присутствии солей Cu(I).
Недостатки метода:
1. Повышенная склонность реагента Гриньяра к окислению требует тщательной защиты реакционной смеси от кислорода и влаги.
2. Низкий выход 1-адамантилмагнийбромида (48%).
3. Необходимость использования абсолютного диэтилового эфира.
4. Проведение реакции при пониженной температуре (-5-0°С).
5. Низкий выход целевого продукта.
1-Ацетиладамантан с выходом 84% был получен взаимодействием этил-3-(1-адамантил)-3-оксопропаноата AdCOCH2COOEt с 1,4-диазабицикло[2,2,2]-октаном в ксилоле (6 час, 165°С) (B.-S. Huang, E.J.Parish, D.H.Miles. J. Org. Chem. V. 39, N 17, 2647-2648 (1974) [4]).
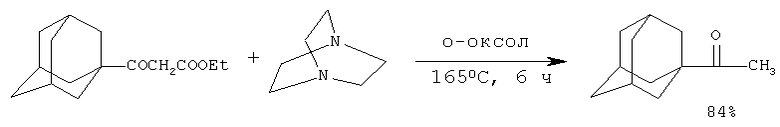
Недостатки метода:
1. Труднодоступность и дороговизна исходных реагентов: этилового эфира 3-адамантилоксопропионовой кислоты и 1,4-диазобицикло[2,2,2]октана.
В работе (Я.Ю.Полис, И.Я.Грава, Д.К.Крузкоп. Способ получения адамантилметилкетона. А.с. 440059 (1977). СССР. // РЖХим. 1977. 22 0 52П [5]) 1-ацетиладамантан получен конденсацией хлорангидрида адамантанкарбоновой кислоты с натриймалоновым эфиром (выход 75%).
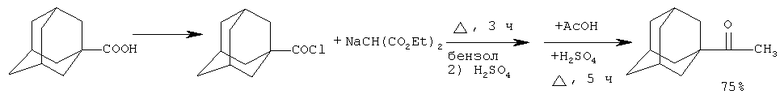
К натриймалонату (получен из 9.3 г Na и 63.5 мл малонового эфира в 100 мл МеОН) прибавляют раствор хлорангидрида адамантанкарбоновой кислоты в абсолютном бензоле, поддерживая температуру кипения во время прибавления и еще кипячение в течение 3 часов. Охлажденную смесь промывают разбавленным раствором H2SO4, бензольный слой промывают водой, бензол отгоняют, вязкую жидкость обрабатывают смесью из 150 мл AcOH и 20 мл концентрированной H2SO4 и 90 мл воды 5 часов при температуре кипения смеси, осадок разбавляют водой, фильтруют и перегонкой с водным паром выделяют 1-ацетиладамантан (выход 75%) [5].
Недостатки метода:
1. Необходимость использования сухих растворителей.
2. Пожароопасность процесса из-за использования металлического натрия.
3. Использование большого избытка концентрированных органических и неорганических кислот.
4. Большое количество неорганических отходов, образующихся при нейтрализации H2SO4.
5. Большие трудо- и энергозатраты.
1-Ацетиладамантан с выходом 95% можно получить фотоацетилированием адамантана диацетилом под действием света Hg-лампы высокого давления (атмосфера N2) (J.Tabushi, S.Kojo. Tetrahedron Lett. N 26, 2329-2332 [6]).
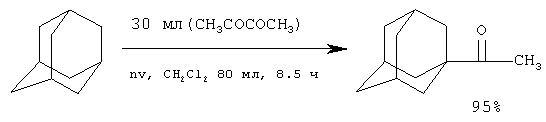
5 г адамантана и 30 мл диацетила в 80 мл CH2Cl2 облучают 8.5 ч, по окончании фотолиза из реакционной смеси выделяют 1-ацетиладамантан с 95% выходом [6].
Недостатки метода:
1. Использование реакторов из кварцевого стекла.
2. Труднодоступность и большой расход диацетила.
3. Невозможность масштабирования процесса.
1-Ацетиладамантан был синтезирован взаимодействием 1-бромадамантана (или 1-гидроксиадамантана) с ацетиленом в присутствии серной кислоты (M.Sasaki, K.Morita. Получение производных 1-ацетиладамантана. Пат.7784 (1972). Япония // РЖХим. 1973. 4Н 339П [7]; M.A.Jmhoff, R.H.Summerville, P. v. R. Schleyer. J. Am. Chem. Soc. V. 92, N 12, 3802-3804 (1970) [8]; K. Bott. Lieb. Ann. Bd. 766, N 1, 51-57 (1972) [9]).
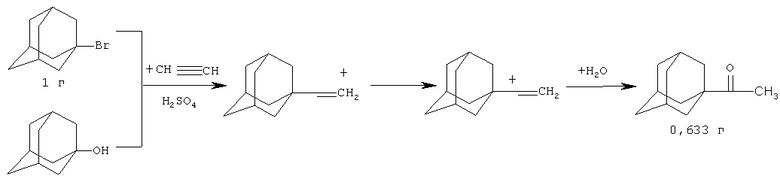
Реакцию проводят по следующей методике:
К 1 г 1-бромадамантана прибавляют смесь H2SO4 и гексана (1:10), охлаждают до 5°С и через полученный раствор в течение 5 часов пропускают ацетилен. В результате реакции образуется осадок, который отделяют, к фильтрату добавляют 300 мл ледяной воды и 100 мл эфира. Эфирный слой отделяют, промывают раствором NaHCO3, упаривают и получают 0.633 г 1-ацетиладамантана [7].
Недостатки методов:
1. Использование взрывоопасного ацетилена.
2. Применение H2SO4.
3. Образование сточных вод, содержащих Na2SO4.
4. Большой расход пожаро-, взрывоопасного эфира для экстракции.
При взаимодействии винилацетата с 1,3-дибромадамантаном под действием комплексов родия (Rh(PPh3)3Cl, [Rh(CO)2Cl]2) при 170°С в течение 8 часов с количественным выходом был получен 1-ацетиладамантан. Реакция сопровождается выделением свободной HBr (Р.И.Хуснутдинов, Н.А.Щаднева, У.М.Джемилев. Изв. АН СССР, Сер.хим. №12, 2897 (1991) [10]).
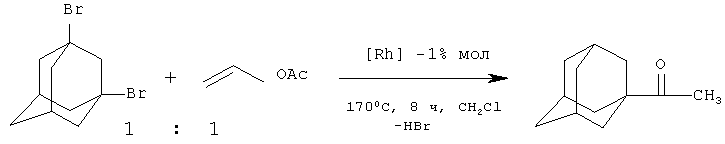
На основании сходства по двум признакам (использование катализатора, образование в результате реакции 1-ацетиладамантана) за прототип взят способ получения 1-ацетиладамантана взаимодействием 1,3-дибромадамантана с винилацетатом под действием комплексов родия [10].
Прототип имеет следующие недостатки:
1. Использование дорогостоящих родийсодержащих катализаторов (Rh(PPh3)3Cl, [Rh(CO)2Cl]2).
2. Труднодоступность 1,3-дибромадамантана.
Задачей настоящего изобретения является упрощение технологии получения 1-ацетиладамантана.
Авторами предлагается способ получения 1-ацетиладамантана, не имеющий недостатков, присущих прототипу.
Сущность способа заключается во взаимодействии 1-хлорадамантана с этилидендиацетатом (ЭДА) в четыреххлористом углероде под действием марганецсодержащих катализаторов (Mn(acac)3, Mn(OAc)2, Mn2(CO)10), активированных ацетонитрилом при 160-180°С в течение 5-7 часов, при мольном соотношении [1-хлорадамантан]: [ЭДА]: [CCl4]: [катализатор]: [CH3CN]=100:100-200:200:3-5:10-15.
В оптимальных условиях при 85-90% конверсии 1-хлорадамантана единственным продуктом реакции является 1-ацетиладамантан.
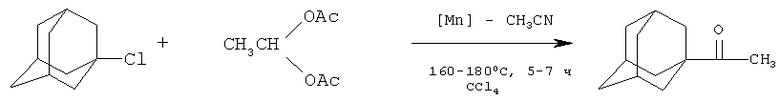
Существенные отличия предлагаемого способа от прототипа:
1. Синтез 1-ацетиладамантана из 1-хлорадамантана и этилидендиацетата.
2. Для получения 1-ацетиладамантана из 1-хлорадамантана и этилидендиацетата используется катализатор, состоящий из соединений марганца, активированных ацетонитрилом.
Преимущества предлагаемого метода:
1. Доступность марганецсодержащих катализаторов.
2. В качестве исходного соединения используется доступный 1-хлорадамантан.
3. Этилидендиацетат, в отличие от винилацетата, в условиях реакции не расходуется на побочные реакции, в частности, не полимеризуется.
4. Высокая селективность процесса.
5. Удешевление себестоимости и упрощение технологии в целом за счет уменьшения энерго- и трудозатрат.
Способ поясняется примерами.
Общая методика. В микроавтоклав из нержавеющей стали (V=17 мл) помещали 0.3-0.5 ммолей Мn2(СО)10 [или Мn(асас)3, Мn(ОАс)2], 1-1.5 ммоля СН3СN, 10 ммолей 1-хлорадамантана, 10-20 ммолей этилидендиацетата (ЭДА), 20 ммолей ССl4, автоклав герметично закрывали и нагревали при 160-180°С в течение 5-7 часов с перемешиванием. После окончания реакции микроавтоклав охлаждали до ~20°С, вскрывали, реакционную массу экстрагировали хлористым метиленом (5 мл × 3 р), растворитель отгоняли, остаток кристаллизовали из гексана. Выход 73-92%.
ПРИМЕР 1. В микроавтоклав помещали 0.3 ммоля Мn2(СО)10, 1 ммоль СН3СN, 10 ммолей 1 хлорадамантана, 20 ммолей этилидендиацетата; 20 ммолей ССl4, автоклав герметично закрывали и нагревали при 180°С в течение 5 часов с перемешиванием. После окончания реакции автоклав охлаждали до комнатной температуры, вскрывали, после обработки реакционной массы, как указано выше, был выделен 1-ацетиладамантан с выходом 90%.
Выделенный 1-ацетиладамантан имел т.пл. 53.2-53.5°С. Ик-спектр (ν, см-1): 1720 (С=O). Спектр ЯМР 13С (СDСl3, ТМС), δ, м.д.: 45.51 (С1), 37.43 (С2, С8, С9), 27.20 (С3, С5, С7), 35.84 (С4, С6, С10), 24.30 (СН3), 212.17 (С=O). Найдено, %: С 80.68; Н 10.03. C12H18O. Вычислено, %: С 80.85; Н 10.18; О 8.98.
Другие примеры, подтверждающие способ, приведены в таблице.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ 1-АЦЕТИЛАДАМАНТАНА | 2008 |
|
RU2408571C2 |
| СПОСОБ ПОЛУЧЕНИЯ N-(1-АДАМАНТИЛ)АЦЕТАМИДА | 2011 |
|
RU2455280C1 |
| СПОСОБ ПОЛУЧЕНИЯ 1-ХЛОР-3-АЦЕТИЛ- И 1,3-ДИХЛОР-5-АЦЕТИЛАДАМАНТАНОВ | 2000 |
|
RU2197467C2 |
| СПОСОБ ПОЛУЧЕНИЯ (1-АДАМАНТИЛ)АЦЕТОНА (2-ОКСОПРОПИЛАДАМАНТАНА) | 2012 |
|
RU2504535C2 |
| СПОСОБ ПОЛУЧЕНИЯ 1-ХЛОРАДАМАНТАНА, 1- И 4-ХЛОРДИАМАНТАНОВ | 2000 |
|
RU2185364C1 |
| СПОСОБ ПОЛУЧЕНИЯ N-(1-АДАМАНТИЛ)АЦЕТАМИДА | 2010 |
|
RU2443680C2 |
| СПОСОБ ПОЛУЧЕНИЯ N-(1-АДАМАНТИЛ)АЦЕТАМИДА | 2008 |
|
RU2401828C2 |
| СПОСОБ ПОЛУЧЕНИЯ N-(1-АДАМАНТИЛ)АЦЕТАМИДА | 2014 |
|
RU2576312C1 |
| СПОСОБ ПОЛУЧЕНИЯ 1-ХЛОРАДАМАНТАНА | 2011 |
|
RU2486169C2 |
| СПОСОБ ПОЛУЧЕНИЯ 1-БРОМАДАМАНТАНА | 2009 |
|
RU2428408C2 |
Настоящее изобретение относится к способу получения 1-ацетиладамантана, который является исходным сырьем для синтеза высокоэффективного препарата «Ремантадин» и препаратов для ветеринарии. Способ заключается во взаимодействии 1-хлорадамантана с этилидендиацетатом (ЭДА), при этом в качестве катализатора используют марганецсодержащие соединения, выбранные из Mn(асас)3, или Мn(ОАс)2, или Mn2(Со)10, активированные ацетонитрилом в среде четыреххлористого углерода при мольном соотношении [1-хлорадамантан]:[ЭДА]:[CCl4]:[катализатор]:[СН3СN]=100:100÷200:200:3÷5:10-15 при температуре 160-180°С в течение 5-7 часов. В оптимальных условиях при конверсии 1-хлорадамантана 85-90% единственным продуктом реакции является 1-ацетиладамантан. 1 табл.
Способ получения 1-ацетиладамантана формулы
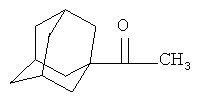
взаимодействием 1-хлорадамантана с этилидендиацетатом (ЭДА), отличающийся тем, что в качестве катализатора используют марганецсодержащие соединения, выбранные из Мn(асас)3, или Мn(ОАс)2, или Мn2(Со)10, активированные ацетонитрилом в среде четыреххлористого углерода при мольном соотношении [1-хлорадамантан]:[ЭДА]:[CCl4]:[катализатор]:[СН3СN]=100:100÷200:200:3÷5:10÷15 при температуре 160-180°С в течение 5-7 ч.
| Хуснутдинов Р.И | |||
| и др | |||
| Винилирование и ацилирование адамантана винилацетатом под действием комплексов родия | |||
| Известия РАН СССР, Серия химическая, 1991, №12, с.2897 | |||
| Способ получения метил(1-адамантил)кетона | 1990 |
|
SU1767836A1 |
| Виброгрейфер | 1981 |
|
SU990634A1 |
Авторы
Даты
2012-01-20—Публикация
2008-12-31—Подача