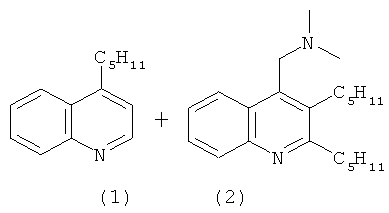
Предлагаемое изобретение относится к органической химии, в частности к способу совместного получения 4-алкилхинолина и (2,3-диалкил-4-хинолинил)- N,N-диметилметанамина формулы (1) и (2):
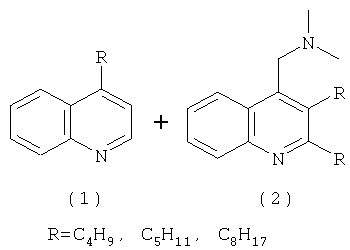
Соединения хинолинового ряда могут найти применение в тонком органическом синтезе, а также производстве продуктов малотоннажной химии - красителей, лекарственных препаратов, средств химической защиты растений, поверхностно-активных веществ, селективных сорбентов и экстрагентов (Ф.А.Селимов, У.М.Джемилев, О.А.Пташко. Металлокомплексный катализ в синтезе пиридиновых оснований. М.: Химия. 2003. 303 с.).
Известен способ (J.Watanabe, J.Tsuji, J.Ohsugi. The ruthenium catalized N-alkylation and N-heterocyclization of aniline using alcohols and aldehydes. Tetrahedron Lett. 1981. v.22. №28. p.2667) получения соединений хинолинового ряда общей формулы (3) взаимодействием анилина с непредельными спиртами под действием катализатора RuCl2(РРh3)3 при температуре 180°С по схеме:
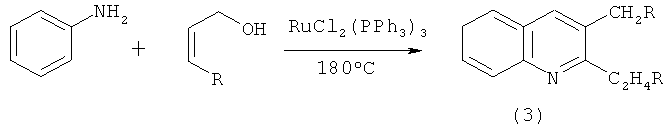
Известным способом не могут быть получены 4-алкилхинолины и (2,3-диалкил-4-хинолинил)-N,N-диметилметанамины формулы (1) и (2).
Известен способ (У.М.Джемилев, Ф.А.Селимов, Р.А.Хуснутдинов, А.А.Фатыхов, Л.М.Халилов, Г.А.Толстиков. Синтез замещенных хинолинов конденсацией анилинов с алифатическими и ароматическими альдегидами под действием катализаторов на основе переходных и редкоземельных элементов. Изв. АН СССР. 1991. №6. С.1407-1413) получения соединения хинолинового ряда общей формулы (4) взаимодействием анилина с масляным альдегидом под действием Pd-содержащего трехкомпонентного катализатора Pd(acac)2-PPh3-AlEt3 при температуре 200°C с выходом 27% по схеме:
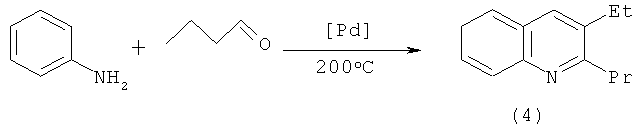
Известный способ не позволяет синтезировать 4-алкилхинолины и (2,3-диалкил-4-хинолинил)-N,N-диметилметанамины формулы (1) и (2).
Предлагается новый способ совместного получения 4-алкилхинолинов и (2,3-диалкил-4-хинолинил)-N,N-диметилметанаминов формулы (1) и (2).
Сущность способа заключается во взаимодействии о-йоданилина с N,N-диметил-2-алкин-1-амином, где (алкин = гептин, октин, ундецин) в присутствии солей хлорида лития (LiCl), карбоната калия (К2СО3), палладиевого катализатора Pd(OAc)2, взятыми в соотношении о-йоданилин: N,N-диметил-2-алкин-1-амин: LiCl:К2СО3:Pd(OAc)2=10:(25-35):10:(25-35):(0.5-1.0), предпочтительно 10:30:10:30:0.8 ммолей, в ДМФА в качестве растворителя при температуре 90-110°С, предпочтительно 100°С, и атмосферном давлении в течение 18-22 ч. Совместный выход 4-алкилхинолинов (1) и (2,3-диалкил-4-хинолинил)-N,N-диметилметанаминов (2) составляет 74-97%, соотношение (1):(2)~1:3. Реакция протекает по схеме:
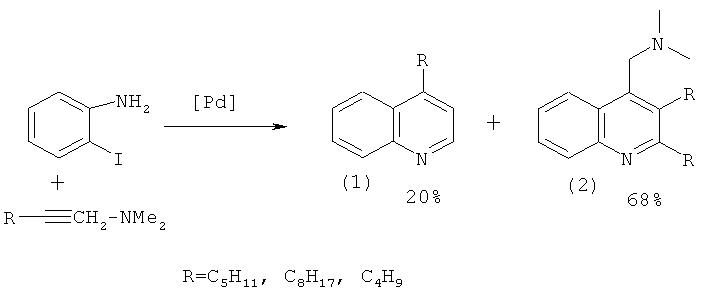
Хинолины (1) и (2) образуются только лишь с участием о-иоданилина и N,N-диметил-2-алкин-1-аминов. В присутствии других дизамещенных ацетиленов (например, диалкил(фенил)ацетилены) или других производных иоданилина (например, м- или n-иоданилины) целевые продукты (1) и (2) не образуются.
Проведение указанной реакции в присутствии катализатора Pd(OAc)2 больше 10 мол % по отношению к о-йоданилину не приводит к существенному увеличению выхода целевых продуктов (1) и (2). Использование катализатора Pd(OAc)2 менее 5 мол % снижает выход (1) и (2), что связано, возможно, со снижением каталитически активных центров в реакционной массе. LiCl следует брать в эквимольном количестве по отношению к о-йоданилину, а N,N-диметил-2-алкин-1-амин и К2СО3 в (2.5-3.5)-кратном избытке. Реакции следует проводить при температуре 90-110°С. При температуре выше 120°С увеличиваются энергозатраты, а при температуре меньше 80°С значительно снижается скорость реакции.
Существенные отличия предлагаемого способа.
В известном способе используются в качестве исходных соединений анилин и масляный альдегид, реакция идет под действием Pd-содержащего трехкомпонентного катализатора Pd(асас)2-PPh3-AlEt3 при температуре 200°С.
В предлагаемом способе в качестве исходных реагентов применяются о-йоданилин, N,N-диметил-2-алкин-1-амины, соли хлорида лития (LiCl) и карбоната калия (К2СО3), реакция идет под действием палладиевого катализатора Pd(OAc)2 при температуре 90-110°С.
Предлагаемый способ обладает следующими преимуществами.
В отличие от известного предлагаемый способ позволяет получать с высокими выходами 4-алкилхинолины (1) и (2,3-диалкил-4-хинолинил)-N,N-диметилметанамины (2).
Способ поясняется следующими примерами.
ПРИМЕР 1. В стеклянный реактор, установленный на магнитной мешалке, помещают 10 мл ДМФА в качестве растворителя, 30 ммолей К2СО3, 10 ммолей LiCl, 0.8 ммолей Pd(OAc)2, 10 ммолей о-йоданилина и 10 ммолей N,N-диметил-2-гептин-1-амина, температуру поднимают до 100°С и выдерживают в течение 20 ч. Из реакционной массы выделяют 4-пентилхинолин (1) и (2,3-дипентил-4-хинолинил)-N,N-диметилметанамин (2) с общим выходом 85% в соотношении (1):(2)~1:3. Соединения 1 и 2 разделяли колоночной хроматографией, элюент гексан: этилацетат, в соотношении 7:3.
Спектральные характеристики 4-пентилхинолина (1) и (2,3-дипентил-4-хинолинил)-N,N-диметилметанамина (2).
Спектр ЯМР 1Н (СDСl3, δ, м.д.) 4-пентилхинолина (1): 0.91 т (3Н, J 7.0 Гц), 1.34-1.47 м (6Н), 3.05 т (2Н, J 7.0 Гц), 7.21 д (J 4.4 Гц, 1Н), 7.54 м (1Н), 7.69 м (1Н), 8.03 д (1Н, J 8.2 Гц), 8.11 д (1Н, J 8.2 Гц), 8.80 д (1Н, J 4.0 Гц). Спектр ЯМР 13С, δ, м.д.: 13.99, 22.49, 29.75, 31.83, 32.10, 118.81, 123.60, 126.20, 127.63, 128.95, 130.13, 148.30, 148.82, 150.12.
Спектр ЯМР 1H (CDCl3, δ, м.д.) (2,3-дипентил-4-хинолинил)-N,N-диметилметанамина (2): 0.95 т (J 6.8 Гц, 6Н), 1.34-1.51 м (8Н), 1.54 м, (2Н), 1.72 м (2Н), 2.32 с (6Н), 2.93 м (2Н), 3.06 м (2Н), 3.84 с (2Н), 7.46 м (1Н), 7.56 м (1Н), 7.99 д (J 8.4 Гц, 1Н), 8.22 д (1Н, J 8.4 Гц). Спектр ЯМР 13С, δ, м.д.: 14.05, 14.08, 22.42, 22.62, 28.83, 29.82, 30.99, 32.25, 32.44, 36.54, 45.49, 55.56, 124.66, 125.44, 127.17, 127.89, 129.39, 133.74, 140.40, δ 146.37, 162.10.
Спектр ЯМР 1Н 4-октилхинолина, δ, м.д.: 0.92 т (3Н, J 7.0 Гц), 1.31-1.51 м (12Н), 3.07 т (2Н, J 7.0 Гц), 7.22 д (J 4.4 Гц, 1Н), 7.54 м (1Н), 7.70 м (1Н), 8.03 д (1Н, J 8.2 Гц), 8.12 д (1Н, J 8.2 Гц), 8.81 д (1Н, J 4.0 Гц). Спектр ЯМР 13С, δ, м.д.: 14.01, 22.48, 28.70, 28.98, 29.45, 30.11, 31.81, 31.98, 118.68, 123.61, 126.21, 127.65, 128.95, 130.15, 148.31, 148.83, 150.15.
Спектр ЯМР 1Н (2,3-диоктил-4-хинолинил)-N,N-диметилметанамин δ, м.д.: 0.89 т (J 6.8 Гц, 6Н), 1.26-1.52 м (20Н), 1.52-1.82 м, (4Н), 2.32 с (6Н), 2.94 т (J 7.8 Гц, 2Н), 2.99 т (J 7.6 Гц, 2Н), 3.85 с (2Н), 7.46 м (1Н), 7.59 м (1Н), 7.99 д (J 8.4 Гц, 1Н), 8.22 д (1Н, J 8.4 Гц). Спектр ЯМР 13С, δ, м.д.: 13.98, 22.19, 28.87, 29.30, 29.30, 29.32, 29.55, 30.04, 30.11, 30.26, 31.27, 31.89, 36.59, 45.50, 55.57, 124.45, 125.42, 127.16, 127.86, 129.16, 133.74, 140.34, 146.41, 162.09.
Спектр ЯМР 1H 4-Бутилхинолин δ, м.д.: 0.90 т (3Н, J 7.0 Гц), 1.32-1.46 м, (4Н), 3.07 т (2Н, J 7.0 Гц), 7.21 д (1Н, J 4.4 Гц), 7.55 м (1Н), 7.68 м (1Н), 8.02 д (1Н, J 8.2 Гц), 8.11 д (1Н, J 8.2 Гц), 8.81 д (1Н, J 4.0 Гц). Спектр ЯМР 13С, δ, м.д.: 13.99, 22.48, 31.85, 32.09, 118.79, 123.58, 126.21, 127.64, 128.95, 130.13, 148.35, 148.84, 150.13.
Спектр ЯМР 1H (2,3-Дибутил-4-хинолинил)-N,N-диметилметанамин, δ, м.д.: 1.02 т (J 7.0 Гц, 3Н), 1.00 т (J 7.0 Гц, 3Н), 1.46-1.53 м (8Н), 2.99 м (2Н), 2.95 м (2Н), 2.32 с (6Н), 3.85 с (2Н), 7.47 м (1Н), 7.59 м (1Н), 7.99 д (J 8.4 Гц, 1Н), 8.21 д (1Н, J 8.4 Гц). Спектр ЯМР 13С, δ, м.д.: 13.86, 14.04, 23.13, 23.30, 28.52, 32.24, 33.39, 36.24, 45.49, 55.53, 124.44, 125.42, 127.167, 127.87, 129.15, 133.68, 140.37, 150.17, 162.05.
Другие примеры, подтверждающие способ, приведены в табл.1.
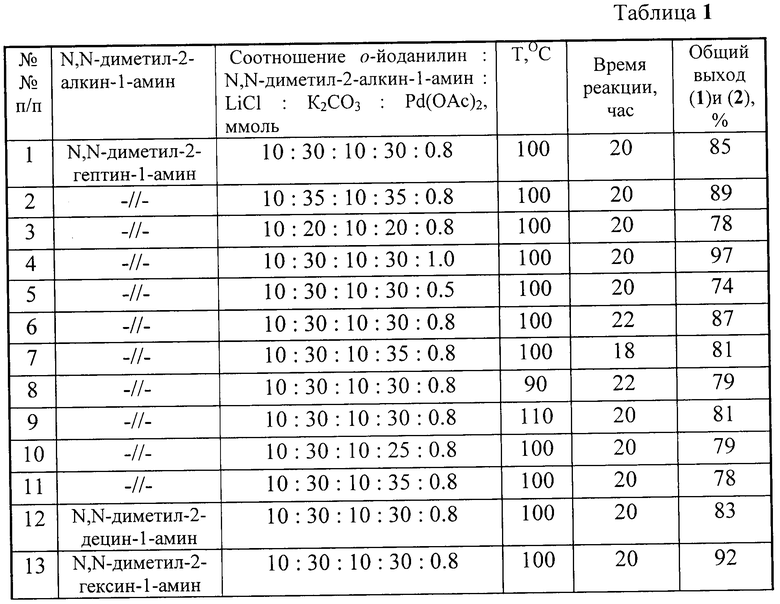
Опыты проводили в ДМФА, взятом в качестве растворителя.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ 2-ФЕНИЛ-3-АЛКИЛХИНОЛИНОВ | 2014 |
|
RU2565787C1 |
| СПОСОБ ПОЛУЧЕНИЯ (2Е,4Е)-N-ИЗОБУТИЛДЕКА-2,4-ДИЕНАМИДА | 2012 |
|
RU2500664C1 |
| СПОСОБ ПОЛУЧЕНИЯ 2,3-ДИАЛКИЛ-1-ФЕНИЛ(АЛКИЛ)ЗАМЕЩЕННЫХ ФОСФОЛ-2-ЕН-1-СУЛЬФИДОВ | 2014 |
|
RU2556008C1 |
| СПОСОБ ПОЛУЧЕНИЯ ЗАМЕЩЕННЫХ ХИНОЛИНОВ ИЗ АНИЛИНА, 1,3-ДИОЛОВ И CCl4 ПОД ДЕЙСТВИЕМ ЖЕЛЕЗОСОДЕРЖАЩИХ КАТАЛИЗАТОРОВ | 2013 |
|
RU2561503C2 |
| СПОСОБ ПОЛУЧЕНИЯ ЗАМЕЩЕННЫХ ХИНОЛИНОВ ИЗ АНИЛИНА, 1,2-ДИОЛОВ И ССl ПОД ДЕЙСТВИЕМ ЖЕЛЕЗОСОДЕРЖАЩИХ КАТАЛИЗАТОРОВ | 2015 |
|
RU2614251C2 |
| 4-ЗАМЕЩЕННЫЕ N-АРИЛ-1,8-НАФТАЛИМИДЫ, ПРОЯВЛЯЮЩИЕ СВОЙСТВА ФЛУОРЕСЦЕНТНЫХ СЕНСОРОВ НА КАТИОНЫ МЕТАЛЛОВ, И СПОСОБЫ ИХ ПОЛУЧЕНИЯ | 2012 |
|
RU2515195C1 |
| СПОСОБ ПОЛУЧЕНИЯ N,N-ДИМЕТИЛ-N-(4-ХИНОЛИНИЛМЕТИЛ)АМИНА | 2008 |
|
RU2404165C2 |
| АЗОСОЕДИНЕНИЯ НА ОСНОВЕ 4-АМИНО-2,3',4'-ТРИЦИАНОДИФЕНИЛА | 2011 |
|
RU2479573C1 |
| СИНТЕЗ НОВОГО КЛАССА ФТОРСОДЕРЖАЩИХ ЖИДКОКРИСТАЛЛИЧЕСКИХ СОЕДИНЕНИЙ С ИСПОЛЬЗОВАНИЕМ ХЛАДОНА 114В2 В КАЧЕСТВЕ ИСХОДНОГО СОЕДИНЕНИЯ | 2012 |
|
RU2505529C1 |
| Способ получения 2,3-диалкил-N-фенил-1,2,3,4-тетрагидрохинолин-4-аминов | 2018 |
|
RU2697876C1 |
Настоящее изобретение относится к органической химии, а именно к способу совместного получения 4-алкилхинолина и (2,3-диалкил-4-хинолинил)-N,N-диметилметанамина формулы (1) и (2), который заключается во взаимодействии о-йоданилина с N,N-диметил-2-алкин-1-амином (где алкин = гептин, октин, ундецин) в присутствии солей хлорида лития (LiCl), карбоната калия (К2СО3), палладиевого катализатора Pd(OAc)2 при мольном соотношении о-йоданилин: N,N-диметил-2-алкин-1-амин: LiCi:К2СО3:Pd(OAc)2=10:(25-35):10:(25-35):(0.5-1.0), при температуре 90-110°С и атмосферном давлении, предпочтительно 100°С в течение 18-22 ч в ДМФА в качестве растворителя. Технический результат: разработан новый способ совместного получения 4-алкилхинолина и (2,3-диалкил-4-хинолинил)-N,N-диметилметанамина, которые могут найти применение в тонком органическом синтезе, а также в производстве красителей, лекарственных препаратов и др. 1 табл.
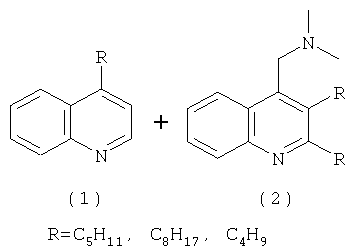
Способ получения 4-алкилхинолина и (2,3-диалкил-4-хинолинил)-N,N-диметилметанамина формулы (1) и (2)
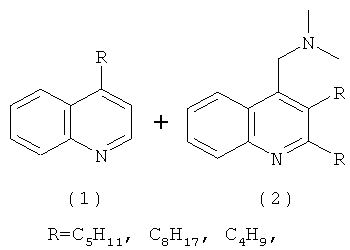
характеризующийся тем, что о-йоданилин подвергают взаимодействию с N,N-диметил-2-алкин-1-амином, (где алкин = гептин, октин, ундецин) в присутствии солей хлорида лития (LiCl), карбоната калия (К2СО3), палладиевого катализатора Pd(OAc)2 при мольном соотношении о-йоданилин: N,N-диметил-2-алкин-1-амин: LiCl:К2СО3:Pd(OAc)2=10:(25-35):10:(25-35):(0,5-1,0), при температуре 90-110°С и атмосферном давлении, предпочтительно 100°С, в течение 18-22 ч в ДМФА в качестве растворителя.
| Способ получения полиэфиров из 9,9-дипропионовой кислоты флуорена | 1960 |
|
SU141487A1 |
| СПОСОБ ПОЛУЧЕНИЯ АЛКИЛПРОИЗВОДНЫХ ХИНОЛИНА | 2005 |
|
RU2283837C1 |
| Rueping, Magnus et al | |||
| "A manganese-catalyzed cross-coupling reaction", Synlett (2), pp.247-250, 2007. | |||
Авторы
Даты
2012-01-20—Публикация
2009-12-07—Подача